Нефтехимия, 2020, T. 60, № 1, стр. 20-25
Структура молекул асфальтенов и нанокластеров на их основе
М. Ю. Доломатов 1, 2, С. А. Шуткова 3, *, Р. З. Бахтизин 1, М. М. Доломатова 1, К. Ф. Латыпов 1, К. А. Гильманшина 2, Б. Р. Бадретдинов 1
1 Башкирский государственный университет. Кафедра физической электроники и нанофизики
450076 Башкортостан, Уфа, Россия
2 Уфимский государственный нефтяной технический университет. Кафедра технологии нефти и газа
450062 Башкортостан, Уфа, Россия
3 Башкирский государственный аграрный университет. Энергетический факультет,
кафедра теплоэнергетики и физики
450001 Башкортостан, Уфа, Россия
* E-mail: Svetlana-Shutkova@yandex.ru
Поступила в редакцию 12.10.2018
После доработки 08.09.2019
Принята к публикации 09.09.2019
Аннотация
Экспериментально и теоретически изучены химическая, электронная и надмолекулярная структуры асфальтенов, выделенных из остатка атмосферно-вакуумной перегонки западно-сибирской нефти (ЗСН). Проведены исследования химической структуры асфальтенов методом ИК-, УФ- и видимой спектроскопии. По спектрам оптического поглощения определена электронная структура молекул асфальтенов с оценкой высшей занятой и низшей свободных молекулярных орбиталей по эффективному потенциалу ионизации и эффективному сродству к электрону. Средняя структура молекул асфальтенов получена по данным химического анализа и спектроскопии. Квантово-химические расчеты, проведенные методом DFT (теория функционала плотности) показали совпадение потенциалов ионизации и сродства к электрону с данными оптической спектроскопии и измерения электропроводности. Проведены расчеты нанокластеров, содержащих до 10 молекулярных фрагментов асфальтенов методом молекулярной механики также показали совпадение с экспериментальными результатами.
Асфальтены составляют наиболее высокомолекулярную часть САВ. По различным данным [1–3] асфальтены содержатся в нефтях до (0.1–45 мас. %), природных асфальтах и битумах (до 73 мас. %), высококипящих фракциях процессов нефтепереработки до (11–30 мас. %). Элементный анализ показал, что асфальтены содержат до 88% углерода, 10% водорода и 14% кислорода, азота, серы и металлов [2–6]. Гетероатомы содержатся во фрагментах макромолекул асфальтенов: атомы N встречаются в гетероароматических фрагментах пиридинного, пиррольного и порфиринового (металло-комплексного) характера [7]; атомы S – в форме сульфидных, тиольных групп и в составе тиофеновых циклов; атомы О – в виде гидроксильных (фенольных, спиртовых), карбоксильных, эфирных, карбонильных групп и фурановых колец.
Согласно данным различных исследований [8–14], асфальтены в растворе толуола при концентрации ниже 100 мг/л образуют наночастицы в виде отдельных нафтено-ароматических плоских конденсированных структур, имеющих боковые алкильные заместители, с молекулярными массами от 400 до 1200 а.е.м., а при более высокой концентрации наночастицы находятся в виде агрегатов, состоящих из 8–10 молекул [8, 9]. В работе [15] методом циклотронной резонансной спектрометрии с Фурье-преобразованием изучены молекулярно-массовые распределения (ММР) фракций асфальтенов, выделенных в н-гептане и других растворителях. Полученные результаты показали, что имеется широкий разброс молекулярных масс. Поэтому также, как и для всех высокомолекулярных соединений целесообразно изучать средние структуры со средними показателями физико-химических свойств, в частности, оперировать со среднечисловыми молекулярными массами, полученными по данным криоскопии в нафталине, и принимать во внимание средние структурно-химические характеристики молекул.
На сегодняшний день приняты две модели строения асфальтенов – “континентальная” и “архипелаг” [16, 17]. Предполагается, что стопкообразные асфальтеновые наноагрегаты формируются из молекул “континентального” типа путем стэкинг-взаимодействия ароматических ядер [14]. Согласно модели “континентального” типа, предложенной Иеном и Маллинсом [18–20], основой молекул асфальтенов является ядро из конденсированных ароматических колец, окруженное алифатической периферией. Мургич [21] предложил модель “архипелаг”, в которой молекулы асфальтенов составлены из нескольких групп конденсированных колец, связанных между собой короткими алифатическими боковыми цепочками. Принципиальное отличие заключается в том, что молекулы “континентального” типа путем стэкинг-взаимодействия ароматических ядер могут образовывать упорядоченные кристалообразные наноструктуры, а структуры, образованные молекулами типа “архипелаг” менее упорядочены.
В работе [22] методом масс-спектрометрической ионизации с применением двухступенчатой лазерной десорбции (L2MS) показано, что доминирующей структурой молекулы нефтяных асфальтенов является модель “континентального” типа. Имеются данные, подтверждающие образование жидкокристаллической фазы лиотропного типа в нефтяных асфальтенах. Так с применением Hot-Stage-электронной микроскопии установлено существование амфолитной, лиотропной жидкокристаллической фазы в растворах нефтяных асфальтенов различного происхождения [23], показано, что в формировании жидкокристаллических структур участвуют области поликонденсированной ароматики и боковые алкильные заместители. Методом атомно-силовой микроскопии определены размерные параметры структур осажденных асфальтенов: нанокластеры – 10–100 нм; агрегаты – 100–350 нм; флокулы – 0.3–1 мкм [24]. Методами ИК-спектроскопии и рентгеновской дифракции показано формирование графитоподобных структур в процессе нагревания пленок гексан-нерастворимых асфальтенов, выделенных из каменноугольного пека. Установлено, что межплоскостные расстояния между ареновыми слоями в межмолекулярных структурах асфальтенов в среднем равны 3.5 Å [23].
Поскольку надмолекулярные структуры, образованные фрагментами асфальтенов, в процессах коксования являются предшественниками нефтяного углерода аморфного или кристаллического типа (игольчатого кокса), особый интерес представляет исследование механизма образования надмолекулярных структур на основе континентальных фрагментов нефтяных асфальтенов. Как известно, эти структуры, в отличие от структур типа “архипелаг”, благоприятны для формирования упорядоченных структур нанокластеров квазикристаллического типа, формирующих мезофазу игольчатого кокса [25]. Поэтому структуры “континентального” типа являются объектами представленной работы.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Объектами исследования являются асфальтены остатков атмосферно-вакуумной перегонки западно-сибирской нефти (ЗСН) с температурой кипения больше 500°С. Для выделения асфальтенов использовали следующую методику [26]. Навеску образца массой 5 г разбавляли н-гептаном в отношении 40 мл на 1 г и оставляли на 14−15 ч. Далее продукт отфильтровывали, а остаток на фильтре промывали н-гептаном до появления бесцветного фильтрата. Затем фильтр высушивали и помещали в аппарат Сокслета. После этого фильтр промывали н-гептаном, затем бензолом. Далее бензол отгоняли из раствора асфальтенов, колбу с асфальтенами высушивали при 150°С до достижения постоянной массы, взвешивали и определяли количество выделенных асфальтенов. Среднечисловая молекулярная масса образца, полученная методом криоскопии в нафталине, составляет 3820 а.е.м. Энергия когезии, определенная по методике [27], составляет 259.23 кДж/моль.
Электронные спектры поглощения в видимой и УФ-области (280–780 нм) для растворов асфальтенов в толуоле исследованы на спектрофотометре СФ-2000. Методом электронной спектроскопии [28] определены эффективные потенциалы ионизации (ЭПИ) и сродства к электрону (ЭСЭ). Рассчитанное значение ЭПИ равно 5.59 эВ, ЭСЭ – 1.85 эВ.
Элементный состав асфальтенов определяли рентгенофлуоресцентным анализом на аппарате Спектроскан Макс G. Согласно проведенным исследованиям содержание углерода составляет 81.04%, водорода – 7.66%, кислорода – 4.94%, азота – 1.56%, серы – 4.80%.
Методом ИК-спектроскопии выполнен структурно-групповой анализ асфальтенов остатков Западно-Сибирской нефти. ИК-спектры регистрировали на ИК-спектрофотометре Shimadzu IRAffinity-1S. Пробы для регистрации ИК-спектра подготавливали растиранием небольшого количества исследуемого вещества в агатовой ступке. Затем порошок, перемешанный с небольшим количеством горячего толуола, наносили на стеклянную пластину и высушивали ИК-лампой для удаления толуола.
На основании ИК-спектра можно сделать заключение о присутствии в структурах асфальтенов конденсированных ароматических структур (1607 см–1). Полосы поглощения при 1365 и 1380 см–1 соответствуют имеющимся в молекулах длинно-цепочным алкильным заместителям. Интенсивное поглощение в ИК-спектре при частотах 1679 см–1 является доказательством наличия в структурах молекул асфальтенов карбонильных групп, соответственно. Изучение ИК-спектра подтвердило присутствие пиррольного кольца (3408 см–1), тиольной группы (2565 см–1) и ОН-группы (3203 см–1) в молекулах асфальтенов.
На основе данных химического анализа и спектроскопии построена усредненная гипотетическая структура молекулы асфальтенов “континентального” типа (рис. 1).
Структура молекулярного фрагмента определяется отношением числа атомов п в состоянии sp2-гибридизации к числу атомов, находящихся в состоянии sp3-гибридизации. Значение отношения $\frac{{{{n}_{{s{{p}^{2}}}}}}}{{{{n}_{{s{{p}^{3}}}}}}}$ равно 0.83 (табл. 1). Структура состоит из пяти ароматических и четырех нафтеновых колец. Молекулярная масса модельной молекулы равна 670 а.е.м. Отношение (С/Н)мол равно 10.38.
Таблица 1.
Структура молекулярного фрагмента асфальтенов
| Молек. масса, а.е.м. |
Число аром. колец |
Число нафтен. колец |
$\frac{{{{n}_{{s{{p}^{2}}}}}}}{{{{n}_{{s{{p}^{3}}}}}}}$ | Количество атомов | (С/Н)мол | ||||
|---|---|---|---|---|---|---|---|---|---|
| C | H | O | N | S | |||||
| 670 | 5 | 4 | 0.83 | 45 | 52 | 2 | 1 | 1 | 10.38 |
Структуры нанокластеров построены из молекулярных фрагментов асфальтенов, количество которых увеличивается от двух до десяти. Молекулярные массы нанокластеров находятся в интервале от 1312 а.е.м. (2 фрагмента) до 6560 а.е.м. (10 фрагментов).
Для уточнения природы взаимодействия молекул асфальтенов проводили электрофизические измерения. Эксперимент осуществляли следующим образом: образец помещали в цилиндрическую термостатированную ячейку, выполненную из фторопласта, с двумя плоскими металлическими электродами в дне и крышке ячейки. Измерения осуществлялись с помощью специально разработанного программно-аппаратного комплекса для определения удельной электропроводности высокоомных материалов на базе платформы NI ELVIS II [29]. Регистрацию температурных зависимостей электропроводности проводили в интервале температур 25–165°С с шагом 5°С. После нагревания до температуры измерения образец выдерживали в течение часа для исключения инерционных эффектов, и только после этого производили измерения.
Получена зависимость натурального логарифма удельной электропроводности образца асфальтенов остатков ЗСН в углеводородной среде от обратной температуры (рис. 2).
Рис. 2.
Зависимость натурального логарифма удельной электропроводности образца асфальтенов остатков Западно-Сибирской нефти от обратной температуры.

По известной зависимости (2) была рассчитана энергия активации электропроводности.
где σ0 – предэкспонента электропроводности (ln σ0 = 0.85); E – энергия активации электропроводности, кДж/моль; T – температура, K; R – универсальная газовая постоянная.Значение энергии активации электропроводности образца равно 129.58 кДж/моль (1.35 эВ).
КВАНТОВО-ХИМИЧЕСКИЕ РАСЧЕТЫ
Исследование электронной и химической структуры наночастиц смолисто-асфальтеновых веществ проведено методом DFT/B3LYP с базисным набором 6-31+G*, используя программный пакет GAUSSIAN. Расчет нанокластеров, образованных молекулами асфальтенов, был проведен методом молекулярной механики ММ+. Все расчеты проведены с полной оптимизацией геометрии.
Известно, что в аморфных материалах, построенных из органических молекул, происходит локализация носителей заряда, обусловленная затуханием волновых функций между молекулами [30]. При этом предполагается, что энергия активация проводимости нанокластера зависит от энергетической щели молекулы в газовой фазе $E_{g}^{0}$ и энергии поляризации Р. Значения энергетической щели в газовой фазе $E_{g}^{0}$ определяются как разность IP потенциала ионизации и EA сродства к электрону молекулы:
Химическое взаимодействие молекул может быть обусловлено образованием водородных связей внутримолекулярного типа и образованием комплексов с переносом заряда. Энергия поляризации возникает при взаимодействии электрона с полярными молекулами и дыркой, поэтому очевидно равенство:
Энергия электростатических электрон-дырочных взаимодействий ${{Е}_{р}}$ определяется по формуле:
где е – элементарный заряд электрона; ε0 – электрическая постоянная; ε – диэлектрическая проницаемость среды (ε = 2); $\bar {r}$ – среднее расстояние между плоскостями молекул в нанокластере ($\bar {r}$ = 3.6 Å).В нашем случае для молекул асфальтенов характерно сильное межмолекулярное взаимодействие за счет образования водородных связей и переноса заряда. Поэтому вносится поправка $\Delta {{E}_{M}},$ которая учитывает межмолекулярное взаимодействие за счет образования водородных связей и дальнодействующих сил Ван-дер-Ваальса [31]. Эти поправки учитываются эмпирическими парными потенциалами в методе молекулярной механики. Энергию межмолекулярного взаимодействия молекул $\Delta {{E}_{M}}$ в структурах нанокластеров определяли по формуле [32]:
где $E$ – потенциальная энергия нанокластера, состоящего из N молекул; ${{E}_{{{{M}_{i}}}}}$ – потенциальная энергия молекулы нанокластера; N – количество молекул в структуре нанокластера.Энергию активации определяли по формуле:
Квантово-химические расчеты свидетельствуют о том, что первый вертикальный потенциал ионизации молекулы асфальтенов (см. структуру) равен 6.56 эВ, сродство к электрону – 0.90 эВ. Аналогичные данные получены термодинамическими методами [25]. Дипольный момент молекулы равен 3.08 D. Учитывая совокупность данных расчета и эксперимента, которые показывают низкие ПИ и высокие СЭ, можно предположить существование химической связи донорно-акцепторного типа между молекулами.
По формуле (5) рассчитаны значения энергии межмолекулярного взаимодействия молекул нанокластеров. Значения энергии межмолекулярного взаимодействия находятся в интервале от 33.85 до 113.42 кДж/моль. Результаты расчета подтверждаются данными эксперимента по определению энергия активации электропроводности образца асфальтенов остатков ЗСН (129.58 кДж/моль). Рассчитаны значения энергии активации проводимости нанокластеров. Расчеты показали, что при увеличении количества молекул в кластере от 2 до 10 значения энергии активации проводимости уменьшаются от 3.31 до 2.48 эВ. Результаты расчета соответствуют данным эксперимента по определению энергии активации электропроводности асфальтенов (1.35 эВ). Учитывая данные УФ- и видимой спектроскопии – низкие значения потенциалов ионизации и высокие значения сродства к электрону, можно предположить существование химической связи донорно-акцепторного типа между молекулами, которые обусловлены образованием комплексов с переносом заряда, качественно соответствующие данным энергии активации электропроводности образца асфальтенов.
Исследования показывают, что, начиная с определенного значения количества молекул в нанокластере (около 6), значения энергии активации принимают определенное значение ($ \approx $2.63 эВ). Следовательно, при определенном количестве молекул наступает стабилизация образованных нанокластеров. Тем самым подтверждается теория, согласно которой наиболее устойчивыми являются наноагрегаты, состоящие из 6–10 нафтеноароматических пластин.
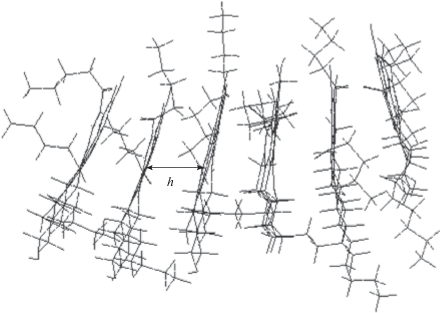
Подтверждена непланарность нафтеноароматических фрагментов в молекулах асфальтенов [33–35]. Исследования показали, что нанокластеры, состоящие от 2 до 10 молекул, представляют с собой непланарную систему, в которой прослеживается небольшой изгиб плоскости нафтеновых колец по отношению к ароматическим кольцам (рис. 3).
Нанокластеры обладают большим значением двугранного угла между нафтеновыми и ароматическими кольцами, а также поворотом плоскостей молекулярных фрагментов по отношению к другим фрагментам в “спиралевидную” форму. При этом группы, замещающие водород в ароматических кольцах по периферии, существенно непланарны плоскости нафтеноароматических пластин. Двугранный угол между виртуальными плоскостями алкильных заместителей и плоскости ароматического кольца находится в интервале от 108° до 158°, что несколько отличается от тетраэдрической структуры, характерной для sp3-гибридизации. Двугранный угол между плоскостью нафтенового кольца и плоскостью ароматических колец в структурах нанокластеров имеет различные значения, находясь в интервале от 161° до 168°. Непланарность структуры свидетельствует о том, что плотная упаковка большого числа нафтеноароматических алкилзамещенных слоев в упорядоченные кристаллические наночастицы нарушается с увеличением числа нафтеноароматических плоскостей, структура разрыхляется и становится более аморфной. Расстояние h между виртуальными плоскостями нафтеноароматических фрагментов нанокластера находится в интервале от 3.5 до 39.2 Å.
Таким образом, показана возможность образования устойчивых нанокластеров асфальтенов со значительной энергией межмолекулярного взаимодействия частиц, что согласуется с экспериментальными данными.
ВЫВОДЫ
1. В процессе изучения спектров поглощения асфальтенов остатков Западно-Сибирской нефти методом оптической спектроскопии подтверждено, что асфальтены являются одновременно сильными донорами и акцептороми электронов. Определены значения эффективного потенциала ионизации (5.59 эВ), эффективного сродства к электрону (1.85 эВ). На основе данных ИК- и УФ-спектроскопии построены гипотетические модели нанокластеров асфальтенов. Квантово-химические расчеты электронной структуры наночастиц показали, что первый вертикальный потенциал ионизации равен 6.56 эВ, сродство к электрону – 0.90 эВ. Результаты расчета энергии активации проводимости (от 3.31 до 2.48 эВ) соответствуют данным эксперимента по определению энергии активации электропроводности образца асфальтенов (1.35 эВ). Полученные результаты соответствуют модели взаимодействия частиц с образованием комплексов с переносом заряда.
2. Подтверждена непланарность структуры нафтеноароматических фрагментов нанокластеров, состоящих из 2–10 молекул. Двугранный угол между плоскостью нафтенового кольца и плоскостью ароматических колец в структурах имеет значения в интервале от 161° до 168°. Расстояние h между виртуальными плоскостями нафтеноароматических фрагментов молекул находится в интервале 3.4–3.7 Å.
3. Рассмотрена экситонная модель переноса заряда между фрагментами наночастиц асфальтенов. Рассчитанная энергия межмолекулярного взаимодействия находится в пределах от 33.85 до 113.42 кДж/моль, что согласуется с данными эксперимента по определению энергии активации электропроводности образца асфальтенов (129.58 кДж/моль). Показано образование устойчивых нанокластеров за счет донорно-акцепторных связей между нафтеноароматическими фрагментами.
Список литературы
Спейт Д. Анализ нефти. Справочник. Пер. с англ. М.: Профессия, 2010. 480 с.
Sharma C., Bhagat S., Erhan S. // Petroleum Science and Technology. 2007. № 25. P. 93.
Rajagopal K., Silva S. // Brazilian J. of Chemical Engineering. 2004. V. 21. № 4. P. 601.
Merino-Garcia D., Shaw J., Carrier H., Yarranton H., Goual L. // Energy Fuels. 2010. 24. № 4. P. 2175.
Spiecker P., Gawrys K., Trail C., Kilpatrick P., Spiecker P. // Colloids and Surfaces A: Physicochem. Eng. Aspects. 2003. 220. № 1. P. 9.
Галимова Г.А., Юсупова Т.Н., Ибрагимова Д.А., Якупов И.Р. // Вестник Казанского технологического университета. 2015. Т. 18. № 20. С. 60.
Mitra-Kirtley S., Mullins O., Van Elp J., George S., Chen J., Cramer S. // J. Am. Chem. Soc. 1993. V. 115. № 1. P. 252.
Hortal A., Martinez-Haya B., Lobato M., Pedrosa J., Lago S. // J. Mass Spectrom. 2006. V. 41. № 7. P. 960.
Lisitza N., Freed D., Sen P., Song Y. // Energy Fuels. 2009. V. 23. № 3. P. 1189.
Betancourt S., Ventura G., Pomerantz A., Viloria O., Dubost F., Zuo J., Monson G., Bustamante D., Purcell J., Nelson R., Rodgers R., Reddy C., Marshall A., Mullins O. // Energy Fuels. 2009. V. 23. № 3. P. 1178.
Gray M., Tykwinski R., Stryker J., Tan X. // Energy Fuels. 2011. V. 25. № 7. P. 3125.
Yen T., Erdman J., Pollack S. // Anal. Chem. 1961. V. 33. № 11. P. 1587.
Bagheri S., Bazyleva A., Gray M., McCaffrey W., Shaw J. // Energy & Fuels. 2010. V. 24. № 8. P. 4327.
Groenzin H., Mullins O. // Energy Fuels. 2000. V. 14. № 3. P. 677.
Logan C. Krajewski, Ryan P. Rodgers, and Alan G. Marshall // Anal. Chem. 2017. V. 89. № 21. P. 11 318.
Sabbah H., Morrow A., Pomerantz A., Zare R. // Energy Fuels. 2011. V. 25. № 4. P. 1597.
Dmitriev D.E., Golovko A.K. // Chemistry for Sustainable Development. 2010. № 18. P. 171.
Мархасин И.Л. Физико-химическая механика нефтяного пласта. М.: Недра, 1974. 100 с.
Mullins O.C. // Energy Fuels. 2010. V. 24. № 4. P. 2179.
Groenzin H., Mullins O.C. // J. Phys. Chem. 1999. V. 103. P. 11 237.
Мургич X. Молекулярное моделирование фракций асфальтенов и смол в нефтях // В книге “Физико-химические свойства дисперсных систем и нефтегазовые технологии”. Ижевск, 2007. С. 580.
Sabbah H., Morrow A.L., Pomerantz A.E., Richard N.Z. // Energy Fuels. 2011. V. 25. P. 1597.
Ганеева Ю.М., Юсупова Т. Н., Романов Г.В. // Доклады Академии наук. 2009. Т. 426. № 5. С. 629.
Коржов Ю.В., Орлов С.А. // Известия Томского политехнического университета. Инжиниринг георесурсов. 2016. Т. 327. № 12. С. 62.
Доломатов М.Ю., Марушкин А.Б., Гимаев Р.Н., Селиверстов Н.М. // Химия и технология топлив и масел. 1986. № 6. С. 83.
Современные методы исследования нефтей. Под ред. Богомолова А.И., Темянко М.Б., Хотынцо-вой Л.И. Л.: Недра, 1984. 431 с.
Хашпер Л.М. Автореф. дис. ... канд. техн. наук. Томск. ИХН СОАН РФ. 1998. 25 с.
Доломатов М.Ю., Мукаева Г.Р. //Журн. прикл. спектроскопии. 1990. Т. 53. № 6. С. 950.
Петров А.М., Доломатов М.Ю., Бахтизин Р.З., Рыжиков О.Л., Хайрудинов И.Р. // Вестник Башкирского государственного университета. 2015. Т. 20. № 3. 2015. С. 826.
Никитенко В.Р. Нестационарные процессы переноса и рекомбинации носителей заряда в тонких слоях органических материалов: Учебное пособие. М.: НИЯУ МИФИ, 2011. 316 с.
Каплан И.Г., Родимова О.Б. // Успехи физических наук. 1978. Т. 126. Вып. 3. С. 403.
Доломатов М.Ю., Бахтизин Р.З., Латыпов К.Ф. // Бутлеровские сообщения. 2018. № 4. С. 64.
Доломатов М.Ю., Шуткова С.А., Дезорцев С.В. // Журн. структур. химии. 2012. Т. 53. № 3. С. 569.
Shutkova S.A., Dolomatov M.Y., Dezortsev S.V. // Petrol. Chemistry. 2012. V. 52. № 4. P. 267. 35. Доломатов М.Ю., Шуткова С.А. // Журн. Структур. химии. 2017. Т. 58. № 7. С. 1311.
Дополнительные материалы отсутствуют.