Нефтехимия, 2020, T. 60, № 1, стр. 148-153
Арилбутилацетали – октаноповышающие оксигенатные добавки к моторным топливам
Л. А. Опарина 1, *, Н. А. Колыванов 1, А. А. Ганина 2, С. Г. Дьячкова 2
1 Иркутский институт химии им. А.Е. Фаворского СО РАН
664033 Иркутск, Россия
2 Иркутский национальный исследовательский технический университет
664074 Иркутск,, Россия
* E-mail: oparina@irioch.irk.ru
Поступила в редакцию 28.05.2019
После доработки 21.08.2019
Принята к публикации 16.09.2019
Аннотация
Исследование посвящено поиску новых оксигенатных добавок, улучшающих качество моторных топлив. Впервые в качестве добавок использованы арилбутилацетали, полученные присоединением фенолов к бутилвиниловым эфирам. Реакция реализуется при комнатной температуре в присутствии каталитических (0.3–0.6 мол. %) количеств CF3CO2H и приводит к образованию целевых продуктов с количественным выходом. Изучены антидетонационные свойства синтезированных соединений. Установлено, что синтезированные арилбутилацетали обладают достаточно высокими октановыми числами по исследовательскому методу (ОЧИ) (до 110 ед.) и могут являться перспективными добавками к автомобильному бензину для повышения детонационной устойчивости: добавки 3 мас. % арилбутилацеталя повышают ОЧИ модельной топливной смеси н-гептан – изооктан на 1.0–1.2 ед., а базового топлива АИ-92-К5 – на 0.1–0.4 ед. Эффективность антидетонационной добавки зависит от строения алкоксильного радикала в молекуле арилбутилацеталя: ОЧ смешения ацеталей с разветвленным изобутоксильным радикалом выше значений линейных бутоксипроизводных на 3.4–6.7 ед. Ацетали, содержащие метильный заместитель в феноксирадикале, имеют более высокие значения ОЧ.
Основной мировой тенденцией улучшения экологических и эксплуатационных свойств автомобильных бензинов является использование многофункциональных добавок, главным образом, оксигенатов. Наличие кислорода в составе топлива позволяет снизить вредные выбросы по оксиду углерода на 30%, а по несгоревшим углеводородам – на 15% [1]. С целью повышения антидетонационных свойств в бензины добавляют компоненты, полученные с применением вторичных методов переработки нефтяных фракций (каталитический крекинг, изомеризация, алкилирование) или вводят в топливо специальные высокооктановые добавки.
Среди оксигенатов, используемых для повышения антидетонационных свойств топлив, наибольшее распространение получают спирты, простые и сложные эфиры, а также ацетали, в том числе циклические (1,3-диоксоцикланы) [2, 3]. Последние относят к категории малоопасных химических веществ, способных улучшать свойства топлив. Техническими результатами их использования в качестве оксигенатных добавок является повышение фазовой стабильности автомобильных топлив при контакте с водой и детонационной стойкости [4–6]. При совместном использовании в топливных композициях спиртов и циклических кеталей отмечено снижение смолообразования [5, 6] и установлен синергетический эффект прироста ОЧ [7].
В последние годы особое внимание уделяется оксигенатным добавкам на основе возобновляемого сырья – целлюлозы, отходов лесной, деревообрабатывающей промышленности и сельского хозяйства, водорослей, лигнина. Использование таких оксигенатов расширяет ресурсы топлив и позволяет повысить их качество за счет снижения токсичности продуктов сгорания [2, 3]. При комплексной переработке растительного сырья получены органические продукты и жидкое топливо (“бионефть”) [8–11]. В частности, быстрый пиролиз растительной биомассы приводит к образованию смеси органических кислородсодержащих соединений (25–45% О), включающей углеводы, фенолы, спирты, сложные эфиры, фураны, альдегиды и т.д. [12]. Многие из этих компонентов, в том числе и соединения фенольного ряда, также могут быть использованы как оксигенатные добавки как к бензину, так и дизельному топливу [13]. Например, добавка анизола (метилфенилового эфира) к бензину (5 мас. %) повышает октановое число топлива на 4 единицы [14].
Ранее нами было изучено применение в качестве оксигенатных добавок к моторным топливам синтетических бутиловых спиртов отечественного производства [15], а также установлена возможность использования арилвиниловых эфиров (модифицированных продуктов каталитической деструкции лигнина) в качестве добавок, повышающих детонационную стойкость бензинов [16]. Цель настоящей работы – поиск новых кислородсодержащих соединений, приемлемых в качестве антидетонационных добавок к моторному топливу. Для достижения поставленной цели синтезированы арилбутилацетали и проведена оценка их влияния на изменение ОЧ топлива.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Ниже представлены методы синтеза арилбутилацеталей различного строения. Формулы исходных веществ и конечных продуктов реакции приведены в табл. 1.
Таблица 1.
Синтез алкиларильных ацеталей
| Виниловый эфир | Фенол | Алкиларилацеталь | Выход 3, % |
|---|---|---|---|
 1а 1а |
 2а 2а |
 3а 3а |
98 |
 1б 1б |
 2а 2а |
 3б 3б |
99 |
 1а 1а |
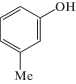 2б 2б |
 3в 3в |
99 |
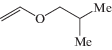 1б 1б |
 2б 2б |
 3г 3г |
97 |
Синтез арилбутилацеталей 3а−г (общая методика). К фенолу 2 (0.25 моль) добавляли 0.10–0.18 г (0.3–0.6 мол. %) СF3CO2H и к полученной смеси в течение 15–20 мин при интенсивном перемешивании по каплям прибавляли свежеперегнанный виниловый эфир 1 (0.25 моль). Реакция сопровождалась экзотермическим эффектом. Максимальную температуру 60–65°С регулировали скоростью добавления винилового эфира. По завершении реакции в ходе самопроизвольного снижения температуры до комнатной (~через 30 мин) кислотный катализатор нейтрализовали 0.1 г K2CO3; после удаления соли получали целевой арилбутилацеталь 3.
1-(н-Бутокси-1-фенокси)этан (3а). Выход 47.55 г (98%), $n_{{\text{D}}}^{{{\text{24}}}}$ 1.4805. ИК-спектр (ν, см–1): 3065, 3036, 2956, 2935, 2873, 1595, 1491, 1464, 1383, 1349, 1292, 1234, 1171, 1130, 1083, 1030, 971, 924, 813, 754, 694, 611, 510. Спектр ЯМР 1H, δ, м. д.: 7.30 м (2H, Ph), 7.02 м (3H, Ph), 5.41 к (1H, J = 5.3 Гц, OCHO), 3.75, 3.50 м (по 1H, OCH2), 1.58 м (2H, CH2Et), 1.52 д (3H, J = 5.3 Гц, MeCH), 1.38 м (2H, CH2Me), 0.92 т (3H, J = 7,3 Гц, Me). Спектр ЯМР 13С, δС, м. д.: 13.7 (МеCH2), 19.2 (СН2Ме), 20.1 (МеСН), 31.7 (СН2Et), 65.5 (ОСН2), 99.5 (ОСНО), 117.3 (С3,5), 121.7 (С4), 129.3 (С2,6), 157.0 (С1). Найдено, %: С 74.02; Н 9.31. C12H18O2. Вычислено, %: С 74.19; Н 9.34.
1-(изо-Бутокси-1-фенокси)этан (3б). Выход 47.98 г (99%), $n_{{\text{D}}}^{{{\text{24}}}}$ 1,4790. ИК-спектр (ν, см–1): 3065, 3036, 2958, 2914, 2875, 1594, 1491, 1385, 1344, 1292, 1235, 1165, 1129, 1084, 1033, 1003, 922, 804, 754, 694, 610, 511. Спектр ЯМР 1H, δ, м. д.: 7.30 м (2H, Ph), 7.03 м (3H, Ph), 5.40 к (1H, J = 5.3 Гц, OCHO), 3.24 дд (2H, J = 9.0, 6.8 Гц, OCH2), 1.85 м (1H, CH), 1.51 д (3H, J = 5.3 Гц, MeCH), 0.89, 0.91 д (по 3H, J = 7.0 Гц, Me2CH). Спектр ЯМР 13С, δС, м. д.: 19.3 (Ме2СН), 20.0 (МеСН), 28.4 (СНМе2), 72.3 (ОСН2), 99.5 (ОСНО), 117.3 (С3,5), 121.7 (С4), 129.3 (С2,6), 157.0 (С1). Найдено, %: С 74.08; Н 9.40. C12H18O2. Вычислено, %: С 74.19; Н 9.34.
1-(н-Бутокси)-1-(3-метилфенокси)этан (3в). Выход 51.50 г (99%), $n_{{\text{D}}}^{{{\text{24}}}}$ 1.4819. ИК-спектр (ν, см–1): 3035, 2986, 2955, 2933, 2872, 2735, 1595, 1488, 1456, 1382, 1348, 1283, 1258, 1160, 1126, 1085, 1029, 954, 912, 875, 854, 778, 743, 693, 618, 445. Спектр ЯМР 1H, δ, м. д.: 7.17 м (1H, C6H4), 6.82 м (3H, C6H4), 5.38 к (1H, J = 5.4 Гц, OCHO), 3.74, 3.49 м (по 1H, OCH2), 2.34 c (3H, MeC6H4), 1.58 м (2H, CH2Et), 1.50 д (3H, J = 5.4 Гц, MeCH), 1.38 м (2H, CH2Me), 0.92 т (3H, J = 7.0 Гц, Me). Спектр ЯМР 13С, δС, м. д.: 13.7 (Ме), 19.2 (СНМе2), 20.1 (МеСН), 21.3 (МеСН), 31.6 (СН2Et), 65.3 (ОСН2), 99.4 (ОСНО), 114.0 (С6), 118.0 (С2), 122.4 (С4), 129.0 (С5), 139.2 (С3), 157.0 (С1). Найдено, %: С 75.00; Н 9.60. C13H20O2. Вычислено, %: С 74.96; Н 9.68.
1-(изо-Бутокси)-1-(3-метилфенокси)этан (3г). Выход 50.43 г (97%), $n_{{\text{D}}}^{{{\text{24}}}}$ 1.4794. ИК спектр (ν, см–1): 3036, 2958, 2925, 2874, 2734, 1595, 1486, 1466, 1383, 1351, 1283, 1256, 1157, 1125, 1086, 1035, 1007, 953, 897, 777, 693, 617, 496, 444. Спектр ЯМР 1H, δ, м. д.: 7.21 м (1H, C6H4), 6.86 м (3H, C6H4), 5.41 к (1H, J = 5.3 Гц, OCHO), 3.27, 3.53 м (по 1H, OCH2), 2.36 c (3H, MeC6H4), 1.89 м (1H, CHMe2), 1.53 д (3H, J = 5.3 Гц, MeCH), 0.94, 0.95 д (6H, J = 7.0 Гц, Me2CH). Спектр ЯМР 13С, δС, м. д.: 19.3 (Ме2СН), 20.0 (МеСН), 21.3 (МеС6Н4), 28.4 (СНМе2), 72.2 (ОСН2), 99.4 (ОСНО), 114.1 (С6), 118.0 (С2), 122.4 (С4), 129.0 (С5), 139.2 (С3), 157.0 (С1). Найдено, %: С 74.80; Н 9.73. C13H20O2. Вычислено, %: С 74.96; Н 9.68.
ОЧИ определяли на стандартной установке с одноцилиндровым двигателем по ГОСТ 8226-2015 “Топливо для двигателей. Исследовательский метод определения октанового числа”. ОЧИ смешения рассчитывали по формуле:
ИК-спектры синтезированных соединений сняты в тонком слое на спектрометре Bruker JFS-25 в области 400–4000 см–1. Спектры ЯМР 1Н и 13С записаны при комнатной температуре на приборе Bruker-DPX-400 с рабочей частотой 400.13 и 100.62 МГц, растворитель – CDCl3. Химические сдвиги ЯМР 1Н и 13С были зарегистрированы относительно CDCl3 в качестве внутреннего стандарта (δ 7.27 и 77.0 м. д., соответственно). Элементный анализ выполняли на анализаторе Flash EA 1112 Series.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Среди известных методов получения ацеталей особого внимания заслуживает атом-экономная реакция электрофильного присоединения ОН-реагентов к виниловым эфирам [17]. Этот метод универсален. Варьируя заместители в виниловом эфире и протогенном реагенте, можно получать разнообразные и часто труднодоступные иными путями симметричные и несимметричные ацетали ацетальдегида.
Необходимые для исследования арилбутилацетали могут быть получены либо из бутиловых спиртов и арилвиниловых эфиров (реакция 1), либо из бутилвиниловых эфиров и фенолов (реакция 2).

Реакция 1 вследствие пониженной электронной плотности двойной связи арилвиниловых эфиров требует жестких условий. Эксперименты показали, что в присутствии катализатора 0.5 мол. % CF3CO2H (60°С, 4 ч) н-BuOH не присоединяется к винил-м-крезиловому эфиру. В спектре ЯМР 1Н не было зафиксировано образование ацеталя 3в даже в следовых количествах. Более жесткие условия реакции (10 мол. % CF3CO2H, 60°С, 8 ч) приводят к побочным процессам, таким как диспропорционирование несимметричного ацеталя 3в и теломеризация арилвинилового эфира, что в итоге снижает выход целевого продукта. Вследствие этого, наработка образцов ацеталей 3 для исследования в качестве добавки к моторным топливам осуществлялась по реакции 2 – из бутилвиниловых эфиров 1а,б и фенолов 2а,б.
Наиболее универсальным методом получения алкилвиниловых (и в частности бутилвиниловых) эфиров является реакция присоединения спиртов к ацетилену в присутствии основных катализаторов, получившая научное и промышленное развитие в 30–70-е гг. прошлого века [18–20]. С открытием академиком Б.А. Трофимовым нового принципа повышения реакционной способности нуклеофильных реагентов за счет использования каталитических сред, состоящих из сильного основания и полярного негидроксильного комплексообразующего растворителя, удалось интенсифицировать классические реакции ацетилена, катализируемые основаниями, и проводить их при умеренных температурах и пониженных (вплоть до атмосферного) давлениях [21, 22].
Бутилвиниловые эфиры реагируют с фенолами значительно легче и селективнее. В стандартных условиях (комнатная температура, эквимольное соотношение реагентов, 0.3–0.6 мол. % CF3CO2H) н-бутил- 1а и изобутилвиниловый 1б эфиры взаимодействуют с фенолом 2а и м-крезолом 2б, образуя соответствующие арилбутилацетали 3а–г с количественным выходом (табл. 1).
Контроль за ходом реакции осуществляли методом ИК-спектроскопии по исчезновению полос поглощения ОН-группы фенолов 2 (в области 3400 см–1) и винилоксигруппы эфиров 1 (3119, 1639, 1612, 1204 см–1) в реакционных смесях. Наличие только одного квартета протонов метиновой (δ ~ 5.4 м. д.) и дублета метильной (δ ~ 1.5 м. д.) групп ацетального фрагмента в спектрах ЯМР 1Н свидетельствует об отсутствии диспропорционирования аддуктов 3 в условиях синтеза.
Синтезированные арилбутилацетали 3а–г – бесцветные подвижные жидкости с приятным запахом, хорошо растворяются в углеводородах и образуют с бензином гомогенные растворы. Плотность этих соединений (0.95–0.97 г/см3) практически не зависит от строения алкильной и арильной части и близка к плотности арилвиниловых эфиров. Температура кипения составляет 250–270°С, что выше, чем для соответствующих арилвиниловых эфиров. Ожидается, что кислород 15.3–16.5% (в бутиловых спиртах 21.6%) будет способствовать уменьшению содержания оксидов и вредных веществ в выхлопных газах.
Оценка влияния синтезированных ацеталей 3а–г на изменение ОЧ проводилась на модельной системе н-гептан–изооктан в соотношении 3 : 7 (ОЧ 70) и базовом топливе, в качестве которого был выбран бензин неэтилированный марки АИ-92-К5 производства АО “АНХК”. Данная марка топлива является наиболее распространенной в России [23].
Испытания на стандартной установке показали, что введение ацеталей 3а–г (3.0 мас. %) в модельную топливную смесь обеспечивает прирост ОЧИ на 1.0–1.2 ед. (табл. 2).
Таблица 2.
ОЧИ смешения ацеталей 3 (3 мас. %) в модельной топливной смеси*
| Добавка | ОЧИ, ед. | Прирост ОЧИ, ед. | ОЧИ смешения, ед. |
|---|---|---|---|
| Без добавки | 70.0 | – | 70.0 |
 3а 3а |
71.0 | 1.0 | 103.3 |
 3б 3б |
71.1 | 1.1 | 106.7 |
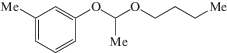 3в 3в |
71.0 | 1.0 | 103.3 |
 3г 3г |
71.2 | 1.2 | 110.0 |
* Представленные в табл. 2 значения ОЧ получены по результатам трех измерений.
Все ацетали обладают достаточно высокими ОЧИ смешения 103.3–110.0, близкими по значению ОЧИ этанола. Последний обладает хорошими эксплуатационными и экологическим показателями, однако его широкое применение ограничивается отсутствием фазовой стабильности и высокими акцизами на спиртосодержащую продукцию [23]. Широко применяемый в России при производстве высокооктановых бензинов метил-трет-бутиловый эфир имеет ОЧИ, равное 118, однако в настоящее время запрещен к использованию во многих странах из-за токсичности и экологической опасности [24].
Антидетонационные свойства исследуемых добавок (по показателю повышения ОЧИ) убывают в ряду: 3г > 3б > 3а = 3в.
Как и для большинства антидетонаторов различных классов, эффективность добавок ацеталей 3а–г к бензину с высоким ОЧИ (90.3) ниже, чем к низкооктановой базовой смеси: при добавке 3 мас. % прирост ОЧИ составил 0.1–0.3 ед. (табл. 3).
Таблица 3.
ОЧИ смешения ацеталей 3 (3 мас. %) в базовом бензине АИ-92-К5*
| Добавка | ОЧИ, ед. | Прирост ОЧИ, ед. | ОЧИ смешения, ед. |
|---|---|---|---|
| Без добавки | 90.3 | – | – |
| 3а | 90.4 | 0.1 | 93.3 |
| 3б | 90.5 | 0.2 | 96.7 |
| 3в | 90.4 | 0.1 | 93.3 |
| 3г | 90.6 | 0.3 | 100.0 |
* Представленные в табл. 3 значения ОЧ получены по результатам трех измерений.
В процессе приготовления автобензинов компаундированием различных компонентов определяющая роль отводится октановым числам смешения, которые отличаются от взвешенной суммы октановых чисел отдельных компонентов [25]. ОЧИ смешения синтезированных ацеталей 3а–г составляет 93.3–100.0 ед.
Наблюдаемые для модельной топливной смеси закономерности прироста ОЧИ в зависти от строения вводимой добавки сохраняются и в бензине. Эффективность антидетонационной добавки зависит от алкоксильного радикала: ОЧ смешения ацеталей 3б,г с разветвленным изобутоксильным радикалом выше значений линейных бутоксипроизводных 3а,в на 3.4–6.7 ед. Как и ожидалось, ацетали, содержащие метильный заместитель в феноксирадикале, имеют более высокие значения ОЧ [26]. Для бутоксипроизводных детонационная стойкость практически не зависит от строения ароматического радикала.
Таким образом, исследованные оксигенаты – аддукты бутилвиниловых эфиров и фенолов – обладают достаточно высокими ОЧИ (до 110 ед.) и могут являться перспективными добавками к автомобильному бензину для повышения антидетонационной устойчивости и улучшения эксплуатационных характеристик.
Список литературы
Брагинский О.Б. // Российский химический журн. 2008. Т. 52. № 6. С. 137.
Максимов А.Л., Нехаев А.И., Рамазанов Д.Н. // Нефтехимия. 2015. Т. 55. № 1. С. 3.
Опарина Л.А., Колыванов Н.А., Гусарова Н.К., Сапрыгина В.Н. // Известия вузов. Прикладная химия и биотехнология. 2018. Т. 8. № 1. С. 19.
Mota C.J.A., da Silv, C.X.A., Rosenbach N., Costa J., da Silva F. // Energy Fuels. 2010. V. 24. P. 2733.
Alptekin E., Canakci M. // Appl. Thermal Eng. 2017. V. 124. P. 504.
Samoilov V.O., Maximov A.L., Stolonogova T.I., Chernysheva E.A., Kapustin V.M., Karpunina A.O. // Fuel. 2019. V. 249. P. 486.
Варфоломеев С.Д., Никифоров Г.А., Вольева В.В., Макаров Г.Г., Трусов Л.И. // Патент РФ № 2365617 / Б.И. 2009. № 24.
Alonso D.M., Bond J.Q., Dumesic J.A. // Green Chemistry. 2010. V. 12. № 9. P. 1493.
Pandey M.P., Kim C.S. // Chemical Engineering & Technology. 2011. V. 34. № 1. P. 29.
Roberts V.M., Stein V., Reiner T., Lemonidou A., Li X., Lercher J.A. // Chemistry. 2011. V. 17. № 21. P. 5939.
Zakzeski J., Bruijnincx P.C.A., Jongerius A.L., Weckhuysen B.M. // Chemical Review. 2010. V. 110. № 6. P. 3552.
Zacher A.H., Loarte M.V., Santosa D.M., Eliott D.C., Jones S.B. // Green Chemistry. 2014. V. 16. P. 491.
McCormick R.L. Ratcliff M.A., Christensen E.D., Fouts L., Luecke J., Chupka G.M., Yanowitz J., Tian M., Boot M.D. // Energy Fuels. 2015. V. 29. № 4. P. 2453.
Хамидуллин Р.Ф., Харлампиди Х.Э., Пучкова Т.Л., Мельник А.Ю., Бадрутдинова А.Р., Галиуллина М.М. // Вестник Казанского технологического университета. 2014. Т. 17. № 21. С. 295.
Кузора И.Е., Дубровский Д.А., Марушенко И.Ю., Артемьева Ж.Н., Забродина С.В., Ганина А.А., Дьячкова С.Г. // Мир нефтепродуктов. 2016. № 10. С. 25.
Опарина Л.А., Высоцкая О.В., Колыванов Н.А., Сапрыгина В.Н., Носова Е.В., Трофимов Б.А. // Известия вузов. Прикладная химия и биотехнология. 2016. Т. 6. № 3. С. 7.
Яновская Л.А., Юфит С.С., Кучеров В.Ф. Химия ацеталей. М.: Наука, 1975. 275 с.
Шостаковский М.Ф. Простые виниловые эфиры. М.: Изд. Академии наук СССР, 1952. 280 с.
Reppe W. // Liebigs Ann. Chem. 1956. Bd 601. S. 81.
Miller S.A. Acetylene, Its Properties, Manufacture and Uses. London: E. Benn, 1966. V. 2. P. 198.
Трофимов Б.А. // Ж. орг. химии. 1986. Т. 22. С. 1991.
Опарина Л.А., Шайхудинова С.И., Паршина Л.Н., Высоцкая О.В., Preiss Th., Henkelmann J., Трофимов Б.А. // Ж. орг. химии. 2005. Т. 41. С. 672.
Емельянов В.Е., Климова Т.А. // Нефтепереработка и нефтехимия. 2013. № 5. С. 7.
Weinberg M., Schulte-Korne E., Peters U., Nierlich F. Methyl-Tert-Butyl Ether. In: Ulmann’s Encyclopedia of Industrial Chemistry. Weinheim: Viley-VCH, 2010. 12 p.
Иванчина Э.Д., Ивашкина Е.Н., Храпов Д.В., Короткова Н.В., Клейменов А.В., Головачев В.А. // Химия и технология топлив и масел. 2017. № 2. С. 24.
Boot M.D., Tian M., Hensen E.J.M., Sarathy M.N. // Progress Energy Combus. Sci. 2017. V. 60. P. 1.
Дополнительные материалы отсутствуют.


