Неорганические материалы, 2019, T. 55, № 1, стр. 39-43
Влияние добавок оксалата железа на фазовый состав продуктов горения смесей кремния и углерода в азотеТ. В. Баринова, В. Ю. Баринов, И. Д. Ковалев
Т. В. Баринова 1, *, В. Ю. Баринов 1, И. Д. Ковалев 1
1 Институт структурной макрокинетики и проблем материаловедения им. А.Г. Мержанова
Российской академии наук
142432 Московская обл., Черноголовка, ул. Академика Осипьяна, 8, Россия
* E-mail: tbarinova@ism.ac.ru
Поступила в редакцию 02.01.2018
Аннотация
Исследовано влияние добавок оксалата железа Fe2(C2O4)3 · 5H2O на фазовый состав продуктов горения смесей кремния и углерода в азоте. Получены зависимости фазового состава продуктов горения от состава шихты и давления азота. Изучена микроструктура полученных порошков. Введение в шихтовые смеси SiО2 приводит к увеличению содержания Si2N2O в продуктах горения.
ВВЕДЕНИЕ
Взаимодействие кремния с азотом в режиме самораспространяющегося высокотемпературного синтеза (СВС) в присутствии добавок органических соединений протекает интенсивно и сопровождается выделением большого количества тепла [1]. В зависимости от условий синтеза, состава шихты и добавок можно получить композиционные порошки с различным соотношением фаз SiC, Si3N4 или Si2N2O [2]. Особенность реакции азотирования кремния в присутствии добавок органических соединений заключается в том, что добавки в процессе синтеза подвергаются пиролизу с образованием газообразных продуктов и углерода в виде сажи, которые препятствуют коагуляции частиц кремния в волне горения, поэтому отпадает необходимость разбавления порошка кремния конечным продуктом. В экспериментах [1] с остановкой фронта горения было показано, что образующиеся в волне горения продукты состоят из наноразмерных кристаллов различной морфологии. После окончания химической реакции происходит увеличение размера частиц в результате процессов вторичного структурообразования, сопровождающихся собирательной рекристаллизацией. Перевод реакции в газовую фазу за счет введения добавок кристаллогидрата хлорного железа в смеси кремния и оксалата аммония способствовал получению нитрида кремния в виде наноразмерных кристаллов, в том числе и поликристаллических волокон, образованных нанокристаллами различной морфологии [3].
Порошки тугоплавких соединений кремния – SiС, Si3N4 и Si2N2O – благодаря своим отличным физико-химическим и термомеханическим свойствам, являются потенциально привлекательными материалами для получения керамики широкого спектра технических применений [4–8]].
Целью данной работы было исследование влияния добавок оксалата железа на фазовый состав продуктов горения смесей кремния и углерода в азоте.
Термическое разложение соли Fe2(С2О4)3 · 5Н2О в азоте происходит в области 130–420°С с образованием газообразных CO, CO2, H2O и твердых Fe3O4 и Fe в виде реакционно-активных наночастиц [9, 10]. Присутствие в реагирующей системе реакционно-активных продуктов распада Fe2(C2O4)3 · 5H2O и сажи должно активизировать физико-химические процессы и массоперенос с участием жидкой и газовой фаз и способствовать получению продуктов горения в виде наноразмерных и ультраразмерных частиц. Использование при синтезе материалов порошков, состоящих из наноразмерных и ультраразмерных частиц, должно обеспечить однородное распределение фаз и создать возможность для моделирования микроструктуры композитных керамик.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
В работе использовали кремний марки КРО со средним размером частиц 12 мкм, сажу марки П804Т с размером частиц от 1 до 2 мкм и Sуд = = 12 м2/г, кристаллогидрат оксалата железа Fe2(C2O4)3 · 5H2O (далее по тексту FOX). Компоненты шихты смешивали в фарфоровой ступке. Навески шихты весом до 30 г насыпной плотности помещали в кварцевый стакан диаметром 40 и высотой до 70 мм и сжигали в сосуде постоянного давления объемом 1.4 л. Стакан располагали горизонтально, образец шихты зажигали с открытого торца раскаленной вольфрамовой проволокой через промежуточный слой порошка титана.
Рентгенофазовый анализ (РФА) проводили на дифрактометре ДРОН-3М с применением СuКα-излучения. Соотношение между фазами продукта рассчитывали по методу корундовых чисел. Морфологию продуктов изучали с помощью электронного микроскопа LEO_1450 c встроенным рентгеновским анализатором INCA ENERGY 350 (EDS).
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
При введении в порошок кремния 0.003 моля FOX на 1 моль Si реакция горения при давлении азота 7 МПа проходит в самоподдерживающемся режиме с образованием плотной спеченной массы, основу которой составляла фаза β-Si3N4. В продукте также присутствовали в небольших количествах α-Si3N4 и Si2N2O. Присутствие в составе продуктов горения до 10% непрореагировавшего кремния свидетельствует о неполном протекании реакции. Дальнейшее повышение содержания FOX в шихте делало невозможным инициирование реакции при давлении азота до 9 МПа.
При введении FOX в смеси кремния и сажи более 0.003 моля удалось инициировать горение смесей и добиться полноты реакции. Во всех проведенных экспериментах доля непрореагировавшего кремния в продуктах горения не превышала 3%. При этом было установлено, что в исследуемых условиях организовать горение смесей кремния и сажи при отсутствии добавок FOX невозможно.
В результате CВC все продукты горения смесей кремния и сажи в присутствии добавок FOX были получены в виде цилиндрических блоков с уплотненной краевой поверхностью (толщиной до 3 мм) и рыхлой основной массой.
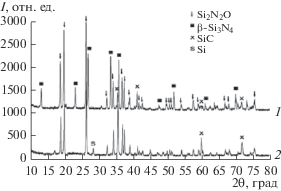
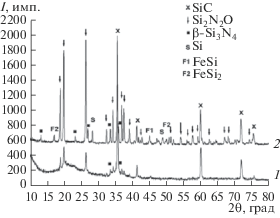
На рис. 1 представлены дифрактограммы продуктов горения составов Si + 0.8C + 0.006FOX и Si + 0.15C + 0.024FOX при 7 МПа. В первом случае (дифрактограмма 1) основным продуктом горения является SiС. При уменьшении содержания в шихте сажи и увеличении количества FOX основным продуктом горения становится Si2N2O (дифрактограмма 2). На дифрактограмме 2 прослеживаются рефлексы силицидов железа – FeSi и FeSi2.
Рис. 1.
Дифрактограммы продуктов горения смесей Si + 0.8C + 0.006Fe2(C2O4)3 ⋅ 5H2O (1) и Si + 0.15C + + 0.024Fe2(C2O4)3 ⋅ 5H2O (2) при ${{p}_{{{{{\text{N}}}_{{\text{2}}}}}}}$ = 7МПа.
На рис. 2 приведены данные микроскопии для смеси Si + 0.8C + 0.006FOX. Видно, что продукт состоит преимущественно из двух типов кристаллов: кристаллов в виде тонких пластин неправильной формы (рис. 2б) и шаровидных образований, состоящих из кристаллов с размерами меньше 55 нм (рис. 2в).
Рис. 2.
Микрофотографии продуктов горения смеси Si + 0.8C + 0.006 Fe2(C2O4)3 · 5H2O: общий вид (а), пластинчатые кристаллы (б) и кристаллы шаровидных образований (в).

Исследование микроструктуры образца, дифрактограмма 1 которого представлена на рис. 1, позволило выявить в составе продуктов частицы на основе FeSi и FeSi2. Микроструктура такой частицы и данные элементного анализа (мас. %) представлены на рис. 3a. Видно, что на поверхности частицы имеется область эвтектического расплава. Согласно диаграмме состояния системы Fе–Si, образование эвтектического расплава возможно при температуре 1220°С. Участки темного (S1) и светлого (S2) цветов близки по составу к FeSi и FeSi2, которые были идентифицированы методом РФА (дифрактограмма 1 на рис. 1). Из анализа микроструктуры можно сделать вывод, что в процессе синтеза формируется железокремниевый расплав. При его охлаждении в первую очередь выделяется FeSi, который имеет температуру плавления 1410°С, при дальнейшем понижении температуры происходит кристаллизация эвтектического состава.
Рис. 3.
Поверхность частицы, образованной силицидами железа (а), и данные элементного анализа (мас. %), структура растущих с ее поверхности кристаллов Si2N2O для смеси Si + 0.15C + 0.024 Fe2(C2O4)3 ⋅ 5H2O (б, в).

По данным элементного анализа, силициды железа содержат углерод, образуя тройную фазу – железокремниевый карбид Fe–Si–C. Согласно [11], железокремниевый карбид Fe–Si–C имеет переменный состав и в условиях синтеза находится в виде жидкой фазы. Образование Fe–Si–C возможно при 1200°С:
(1)
${\text{Fe}} + {\text{SiC}} \to {\text{Fe}}{\kern 1pt} --{\kern 1pt} {\text{Si}}{\kern 1pt} --{\kern 1pt} {\text{C}}.$Участвующий в реакции SiC может образоваться при температуре 1100°С [11]:
Из рис. 3а также видно, что часть поверхности частицы занята кристаллами SiC (S4) и Si2N2О (S3). Рост кристаллов происходит из расплава Fe–Si–C, что хорошо видно из рис. 3б, где показан рост кристаллов Si2N2O. На рис. 3в показана структура Si2N2O при большем увеличении. Видно, что Si2N2O представляет собой сложные кристаллические образования, похожие на ветви деревьев. Образование Si2N2O методом СВС идет в две стадии [8]. Первоначально образуется Si3N4. Очевидно, кристаллы Si3N4 растут по механизму пар–жидкость–кристалл [12], где в качестве жидкой фазы выступает расплав Fe–Si–С.
Как известно [13], при наличии капель жидкого металла адсорбция компонентов растущего кристалла из газовой фазы происходит преимущественно в капле жидкости, которая инициируют направленный рост кристаллов. Так как при получении Si2N2O методом СВС достигаются высокие температуры [8, 14], упругость паров Si при этих температурах также высокая, поэтому возможно образование продуктов горения и в газовой фазе.
На рис. 4–6 представлены зависимости состава продуктов горения (Si2N2O, SiС и Si3N4) от содержания в исходной шихте добавок сажи (рис. 4), FOX (рис. 5) и от давления азота (рис. 6). Анализ полученных данных показывает, что наибольшее влияние на фазовый состав продуктов горения оказывает содержание в шихте сажи и FOX. При малых количествах сажи основным компонентом в продуктах горения является Si2N2O. При увеличении количества сажи в шихте в продуктах горения растет содержание SiС, снижается содержание Si2N2O, на дифрактограммах практически исчезают рефлексы Si3N4. С ростом содержания FOX в шихте (рис. 5) наблюдается увеличение выхода Si2N2O, при этом снижается доля карбида и нитрида кремния. При внесении в шихту менее 0.005 молей FOX продукт горения представляет собой смесь только SiС и Si3N4. Оптимальное давление азота для получения продукта с максимальным содержанием Si2N2O составило 3–4 МПа. При отклонении давления азота от оптимального наблюдается снижение содержания Si2N2O и SiС, при этом увеличивается содержание Si3N4 (рис. 6). Реакция азотирования кремния с образованием Si2N2O протекает в фильтрационном режиме [8, 14], газообразные продукты распада FOX двигаются из области высоких температур навстречу потоку азота и препятствуют его прохождению в зону реакции. При низких давлениях азота (2 МПа) газообразные кислородсодержащие соединения преодолевают сопротивление азота и частично успевают покинуть зону реакции, поэтому в продуктах горения основными фазами являются Si3N4 и SiС. С ростом давления азота повышается температура горения, которая при давлении 9 МПа может превысить температуру существования фазы Si2N2O. Уже при температуре выше 1750°С может происходить разложение Si2N2O с образованием β-Si3N4 по реакции [14]:
(4)
${\text{S}}{{{\text{i}}}_{{\text{2}}}}{{{\text{N}}}_{{\text{2}}}}{\text{O}}\left( {s.} \right) = {\text{S}}{{{\text{i}}}_{{\text{3}}}}{{{\text{N}}}_{4}} + {\text{3SiO}} + {{{\text{N}}}_{2}}.$Рис. 4.
Зависимость состава продуктов горения от количества в шихте сажи при ${{p}_{{{{{\text{N}}}_{{\text{2}}}}}}}$ = 5 МПа и Fe2(C2O4)3 ⋅ ⋅ 5H2O = 0.024 моля.
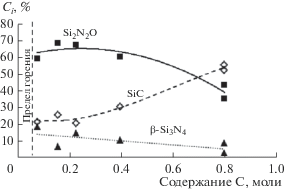
Рис. 5.
Зависимость состава продуктов горения от количества в шихте Fe2(C2O4)3 ⋅ 5H2O при ${{p}_{{{{{\text{N}}}_{{\text{2}}}}}}}$ = 5 МПа и С = 0.8 моля.
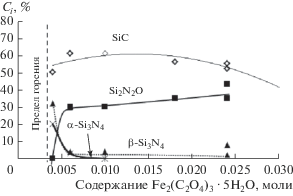
Рис. 6.
Зависимость состава продуктов горения от давления азота ${{p}_{{{{{\text{N}}}_{{\text{2}}}}}}}$ при С = 0.16 моля и Fe2(C2O4)3 ⋅ ⋅ 5H2O = 0.024 моля.
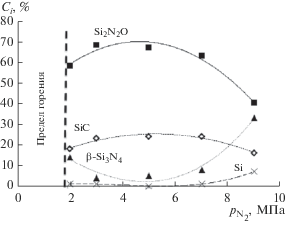
Таким образом, при увеличении давления азота (рис. 6) разложение Si2N2O приводит к повышению содержания β-Si3N4 в продуктах реакции.
Для получения методом СВС порошков с высоким содержанием Si2N2O обычно в состав исходной шихты вводят SiO2 [8]. В проведенных нами экспериментах введение SiO2 в состав исходных смесей привело к увеличению доли Si2N2O в составе продуктов до 75%. На рис. 7 приведены данные РФА для смесей Si + 0.09C + + 0.09SiO2 + 0.006FOX (1) и Si + 0.09C + 0.09SiO2 + + 0.024FOX (2). Из приведенных данных следует, что, меняя количество FОХ в шихте, можно влиять на фазовый состав продуктов горения. При малых количествах FОХ в смеси (рис. 7, дифрактограмма 1) основными фазами в продукте являются Si2N2O (46%) и β-Si3N4(48%), а при увеличении содержания FОХ (дифрактограмма 2) продукты горения представляют собой смесь Si2N2O и SiС с преимущественным содержанием Si2N2O. Исследование микроструктуры показало, что введение SiO2 приводит к огрублению и агломерации частиц продукта.
ЗАКЛЮЧЕНИЕ
При горении кремния в азоте в присутствии сажи и Fe2(C2O4)3 · 5H2O получены порошки, состоящие из Si3N4, SiС, Si2N2O. Фазовый состав продуктов горения зависит от состава шихты и давления азота. Показано, что рост кристаллов Si2N2O может происходить из расплава Fe–Si–С. Введение SiO2 в исходную смесь способствует увеличению доли Si2N2O в составе продуктов, но при этом наблюдается агломерация кристаллов.
Список литературы
Баринова Т.В., Боровинская И.П., Некоторые особенности горения кремния в азоте в присутствии добавок органических соединений // Неорган. материалы. 2014. Т. 50. № 11. С. 1169–1173. doi https://doi.org/10.1134/ S0020168514100045
Barinova T.V., Borovinskaya I.P. Combustion of Silicon Powders Containing Organic Additives in Nitrogen Gas under Pressure: 2. Composition of Combustion Products // Int. J. Self-Propag. High-Temp. Synth. 2009. V. 18. № 1. P. 30–33. doi https://doi.org/10.3103/ S1061386209010063
Barinova T.V., Borovinskaya I.P., Barinov Yu.N., Kovalev I.D., Shchukin A.S. Polycrystalline Silicon Nitride Fibers by SHS: Impact of Ammonium Acetate and Ferric Chloride Additives // Int. J. Self-Prop. High-Temp. Synth. 2018. V. 27. № 2. P. 92–97. doi https://doi.org/10.3103/ S106138621802005X
Agrafiotis Ch.C., Lis J., Puszynski J.A., Hlavacek V. Combustion Synthesis of Silicon Nitride-Silicon Carbide Composites // J. Am. Ceram. Soc. 1990. V. 73. № 11. P. 3214–3517.
Kata D., Pumpuch R. Combustion Synthesis of Multiphase Powders in the Si–C–N System // Solid State Ionics. 1997. V. 101–103. P. 65–70.
Li X., Zhang L., Yin X. Study on in-situ Reaction Synthesis and Mechanical Properties of Si2N2O Ceramic // Ceram. Int. 2013. V. 39. P. 3035–3041. http://dx.doi.org/ https://doi.org/10.1016/j.ceramint.2012.09.082.
Cheng H., Li Y., Kroke E., Herkenhoff S. In situ Synthesis of Si2N2O/Si3N4 Composite Ceramics Using Polysilyloxycarbodiimide Precursors // J. Eur. Ceram. Soc. 2013. V. 33. P. 2181–2189. http://dx.doi.org/https://doi.org/10.1016/ j.jeurceramsoc.2013.02.029.
Studenikin I.A., Grachev V.V. Synthesis of Silicon Oxynitride by Infiltration-Mediated Combustion // Int. J. Self-Prop. High-Temp. Synth. 2008. V. 17. № 4. P. 237–241. doi https://doi.org/10.3103/S106138620804006
Шкарин А.В., Жаброва Г.М., Топор Н.Д., Кушнарев М.Я. Термическая устойчивость и химические превращения оксалатов // Изв. Томского политехн. ин-та. 1969. Т. 199. С. 105–111.
Суздалев И.П., Максимов Ю.В., Имшенник В.К., Новичихин С.В., Матвеев В.В., Третьяков Ю.Д., Лукашин А.В., Елисеев А.А., Малыгин А.А., Соснов Е.А. Иерархия строения и магнитные свойства наноструктуры. оксидов железа // Рос. нанотехнологии. 2006. Т. 1. № 1–2. С. 134–141.
Косолапова Т.Я., Андреева Т.В., Бартницкая Т.Б., Гнесин Г.Г. и др. Неметаллические тугоплавкие соединения. М.: Металлургия, 1985. С. 161.
Kolasinski K.W. Catalytic Growth of Nanowires: Vapor–Liquid–Solid, Vapor–Solid–Solid, Solution–Liquid–Solid and Solid–Liquid–Solid Growth // Curr. Opin. Solid State Mater. Sci. 2006. V. 10. P. 182–191. org/https://doi.org/10.1016/j.cossms.2007.03.002
Гиваргизов Е.И., Чернов А.А. Скорость роста нитевидных кристаллов по механизму пар–жидкость–кристалл и роль поверхностной энергии // Кристаллография. 1973. Т. 18. № 1. С. 147–149.
Чухломина Л.Н., Витушкина О.Г., Верещагин В.И. Самораспространяющийся высокотемпературный синтез керамической композиции на основе нитрида кремния с использованием ферросилиция и ильменита // Стекло и керамика. 2010. № 9. С. 15–18.
Дополнительные материалы отсутствуют.
Инструменты
Неорганические материалы