Неорганические материалы, 2019, T. 55, № 3, стр. 249-256
Взаимосвязь пикнометрической плотности и удельной поверхности нанокристаллических порошков VCy
А. С. Курлов *
Институт химии твердого тела УрО Российской академии наук
620990 Екатеринбург, ул. Первомайская, 91, Россия
* E-mail: kurlov@ihim.uran.ru
Поступила в редакцию 04.04.2018
После доработки 15.10.2018
Принята к публикации 14.09.2018
Аннотация
Методом высокотемпературного твердофазного синтеза с последующим высокоэнергетическим размолом получены нанокристаллические порошки нестехиометрического кубического карбида ванадия VCy с разной нестехиометрией (0.69 ≤ y ≤ 0.76) и средним размером частиц от 20 до 60 нм. Установлено, что размол порошков VCy сопровождается изменением их химического состава, периода кристаллической решетки, удельной поверхности, среднего размера частиц, величины микродеформаций и плотности. Получено выражение, связывающее пикнометрическую плотность и удельную поверхность порошков VCy, с помощью которого определены относительное содержание кислорода и истинная плотность карбидных частиц в порошках. Показано, что основной причиной уменьшения пикнометрической плотности порошков с увеличением их удельной поверхности является адсорбция кислорода на поверхности карбидных частиц.
ВВЕДЕНИЕ
Карбид ванадия VCy с кубической структурой B1 входит в группу сильно нестехиометрических соединений и обладает широкой областью гомогенности – от VC0.65 до VC0.88, верхняя граница которой существенно удалена от стехиометрического состава [1, 2]. Благодаря высокой твердости, химической и термической стабильности карбид ванадия VCy широко используется в металлургической промышленности в качестве легирующей добавки для упрочнения сталей [3, 4], а также как ингибитор роста зерен WC в субмикро- и нанокристаллических твердых сплавах WC–Co [5–9], которые применяются для производства самого высококачественного бурильного и режущего инструмента. Другая перспективная область применения карбида ванадия – использование в качестве катализатора для восстановления кислорода [10–12], окисления спиртов [13], в реакциях гидродесульфуризации [14] и др.
В настоящее время особое внимание ученых приковано к получению, исследованию свойств и применению веществ и материалов в нанокристаллическом состоянии [15]. Карбид ванадия здесь не является исключением. Уменьшение размера частиц и, как следствие, увеличение удельной поверхности порошков карбида ванадия повышает их каталитическую активность, а уменьшение размера карбидных зерен в сталях и твердых сплавах сопровождается увеличением их твердости и прочности. На сегодняшний день известно множество разнообразных методов получения нанокристаллических порошков карбида ванадия, среди которых плазмохимический синтез [16], механосинтез [17], температурно-программируемая карбидизация [18], прекурсорный метод [19] и др. Однако большинство из них не позволяет получать нанопорошки карбида ванадия VCy с заданными нестехиометрией и размером частиц. Простой и универсальный метод получения карбидных нанопорошков с заданным содержанием углерода – высокотемпературное вакуумное спекание металла и углерода [1, 2] с последующим высокоэнергетическим размолом [20]. Этот способ позволяет получать нанокристаллические порошки нестехиометрических карбидов любого заданного состава и размера частиц с узким распределением по размерам.
Ранее уже проводились исследования микрокристаллического нестехиометрического кубического карбида ванадия VCy во всей области его гомогенности [1, 2, 21] и нанокристаллического карбида ванадия с составом VC0.875, соответствующим верхней границе области его гомогенности [16–19, 22]. Однако сведений о нанокристаллических нестехиометрических карбидах ванадия VCy с разными составом и размером частиц найти не удалось.
Чтобы восполнить этот пробел, в настоящей работе впервые обсуждаются микро- и нанокристаллические порошки нестехиометрического кубического карбида ванадия VCy с разным размером частиц и составом в пределах его области гомогенности, а также влияние размола микрокристаллических порошков на изменение их химического состава, периода кристаллической решетки, удельной поверхности, среднего размера частиц, величины микродеформаций и плотности получаемых нанопорошков.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Синтез образцов нестехиометрического кубического (пр. гр. Fm$\bar {3}$m) карбида ванадия VCy с разным составом (y = 0.69, 0.71, 0.73 и 0.76) в пределах его области гомогенности осуществлялся из механоактивированных субмикрокристаллических порошковых смесей ванадия V и углерода C (сажи), компактированных при комнатной температуре в стальной цилиндрической пресс-форме с помощью аксиального прессования при давлении ~350 MПa. Синтез проводился в высокотемпературной вакуумной печи Centorr LF-22-2000 с выдержкой при температуре 1300°C и вакууме ~10–2 Па в течение 5 ч. После синтеза плотные цилиндрические образцы дробились и перетирались в титановой ступке в порошок.
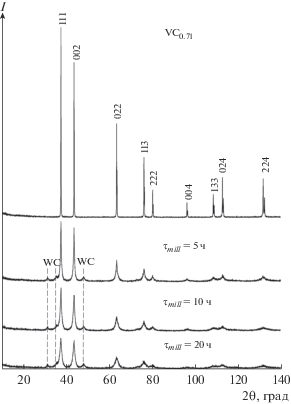
Рис. 1.
Дифрактограммы исходного микрокристаллического порошка VC0.71 и нанокристаллических порошков, полученных размолом исходного порошка в течение 5, 10 и 20 ч (пунктирными линиями отмечены наиболее интенсивные дифракционные отражения примесного карбида вольфрама WC).
Для получения нанокристаллических порошков нестехиометрического кубического карбида ванадия VCy с разным средним размером частиц был использован метод высокоэнергетического размола. Размол микрокристаллических порошков VCy осуществлялся в планетарной шаровой мельнице Retsch PM 200 с использованием мелющих шаров и футеровки размольных стаканов из твердого сплава WC-6 мас. % Co. Средний размер частиц получаемых нанопорошков варьировался путем изменения продолжительности размола от 5 до 20 ч. Остальные параметры размола были фиксированы: скорость вращения опорного диска размольных стаканов 500 об./мин; масса порошка, взятого для размола, 10 г; масса мелющих шаров диаметром 3 мм ~ 100 г; объем размольного стакана 50 мл; объем изопропилового спирта, добавляемого при размоле, 15 мл. После размола порошки сушили в вакуумном шкафу Binder VDL 23 при остаточном давлении ~103 Па и температуре 85°C.
Химический анализ микрокристаллических и размолотых порошков VCy на содержание общего и свободного углерода осуществлялся с помощью анализатора МЕТАВАК CS-30. Содержание кислорода в порошках определялось методом восстановительного плавления в токе аргона на газоанализаторе HORIBA EMGA-620W/С. Содержание примесных элементов в них определялось на масс-спектрометре Perkin Elmer SCIEX-ELAN 9000 и энерго-дисперсионным рентгеновским (EDX) анализом на микроскопе JEOL JSM 6390 LA с анализатором JED 2300.
Кристаллическая структура, фазовый состав и параметры решетки крупнозернистых и размолотых порошков VCy определялись с помощью рентгеновской дифракции на автодифрактометре Shimadzu XRD-7000 с геометрией съемки плоского образца по Бреггу–Брентано в интервале углов 2θ от 10° до 140° с пошаговым сканированием Δ(2θ) = 0.03° и временем экспозиции 2 с в точке в излучении ${\text{Cu}}{{K}_{{{{\alpha }_{{1,2}}}}}}$. Рентгенограммы анализировались методом Ритвельда с помощью программного пакета X’Pert HighScore Plus [23]. По уширению дифракционных отражений методом Вильямсона–Холла для размолотых порошков VCy определялись средний размер DX областей когерентного рассеяния (ОКР), который в первом приближении рассматривался как средний размер частиц порошка, и величина микродеформаций ε без учета их анизотропии [24].
Морфология и размер частиц крупнозернистых и размолотых порошков VCy изучались с помощью сканирующего электронного микроскопа JEOL JSM 6390 LA.
Удельная поверхность SBET крупнозернистых и размолотых порошков VCy измерялась адсорбционным методом Брунауэра–Эммета–Теллера (BET) с помощью анализатора площади поверхности и пористости Micromeritics Gemini VII после дегазации порошков в вакууме ~10 Па при температуре 350°C в течение 1 ч. В приближении одинакового размера и шарообразной формы частиц по измеренной величине SBET определялся средний размер частиц DBET = 6/(ρXSBET), где ρX – рентгеновская плотность.
Рентгеновская плотность ρX карбидов VCy рассчитывалась по формуле
где n = 4 – число формульных единиц VCy, приходящихся на элементарную ячейку с кубической структурой B1; M = 50.942 г/моль + y · · 12.011 г/моль – молярная масса VCy; NA = 6.022 × × 1023 моль−1 – число Авогадро; $V = a_{{B1}}^{3}$ – объем элементарной ячейки карбида VCy с периодом решетки aB1.Пикнометрическая плотность ρHe крупнозернистых и размолотых порошков VCy определялась с помощью гелиевого пикнометра Micromeritics AccuPyc II 1340 с использованием измерительной камеры объемом 1 см3.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Согласно дифракционным данным, все синтезированные карбиды ванадия VC0.69, VC0.71, VC0.73 и VC0.76 являются однофазными и имеют кубическую (пр. гр. Fm$\bar {3}$m) структуру типа B1. По данным химического анализа, весь углерод, содержащийся в синтезированных карбидах ванадия VCy, является связанным и определяет их состав y. В порошках синтезированных карбидов VCy обнаружен кислород, общее содержание которого не превышает ~0.4 мас. % и уменьшается вместе с их удельной поверхностью (табл. 1). Элементный анализ показал, что все порошки синтезированных карбидов ванадия содержат вольфрам в количестве 0.3–0.5 мас. %, наличие которого обусловлено натиранием материала мелющих шаров и футеровки стаканов, изготовленных из твердого сплава WC–6 мас. % Co, при подготовке порошковых смесей для синтеза. Содержание других примесных металлов в синтезированных порошках не превышает 0.05 мас. %.
Таблица 1.
Химический состав, период кристаллической решетки, рентгеновская и пикнометрическая плотности, удельная поверхность и средний размер частиц микрокристаллических порошков синтезированных нестехиометрических карбидов ванадия VCy
| Порошок | ωC ± 0.05, мас. % | ωO ± 0.05, мас. % | aB1 ± 0.0005, Å | ρX ± 0.01, г/см3 | SBET ± 0.01, м2/г | DBET ± 0.1, мкм | ρHe ± 0.01, г/см3 |
|---|---|---|---|---|---|---|---|
| VC0.69 | 13.90 | 0.37 | 4.1299 | 5.59 | 0.64 | 1.7 | 5.60 |
| VC0.71 | 14.34 | 0.19 | 4.1326 | 5.60 | 0.42 | 2.5 | 5.62 |
| VC0.73 | 14.66 | 0.23 | 4.1377 | 5.60 | 0.49 | 2.2 | 5.65 |
| VC0.76 | 15.16 | 0.27 | 4.1414 | 5.62 | 0.60 | 1.8 | 5.65 |
После высокоэнергетического размола микрокристаллических порошков VCy содержание вольфрама в них увеличивается на порядок и составляет 3–5 мас. % в зависимости от продолжительности размола. Вольфрам в порошках карбида ванадия присутствует в виде гексагонального карбида вольфрама WC, являющегося основой материала мелющих шаров и футеровки стаканов. На рентгенограммах всех порошков VCy после размола наблюдаются дифракционные отражения примесной фазы гексагонального (пр. гр. P$\bar {6}$m2) карбида вольфрама WC. Для иллюстрации на рис. 1 приведены дифракционные рентгеновские спектры исходного микрокристаллического порошка карбида ванадия VC0.71 и нанокристаллических порошков, полученных размолом исходного порошка в течение 5, 10 и 20 ч. На рентгенограммах нанопорошков VC0.71 присутствуют слабые отражения примесного WC. Кроме этого, на рис. 1 отчетливо видно, что увеличение продолжительности размола порошка сопровождается уширением его отражений, которое обусловлено малым размером ОКР и наличием микродеформаций в нанопорошках. Средний размер ОКР (DX) во всех изученных нанопорошках VCy приведен в табл. 2. Оценка размера DBET частиц по величине удельной поверхности SBET порошков (табл. 2) в пределах ошибок эксперимента хорошо согласуется с размером DX.
Таблица 2.
Химический состав, период кристаллической решетки, удельная поверхность, средний размер частиц, величина микродеформаций и плотность нанокристаллических порошков карбида ванадия VCy, полученных размолом
| Поро-шок | τmill, ч | ωC ± 0.05, мас. % | ωO ± 0.05, мас. % | aB1 ± 0.0005, Å | ΔaB1/aB1, % | ρX ± 0.01, г/см3 | DX ± 5, нм | ε ± 0.03, % | SBET ± 0.2, м2/г | DBET ± 5, нм | ρHe ± 0.01, г/см3 |
|---|---|---|---|---|---|---|---|---|---|---|---|
| VC0.69 | 5 | 13.96 | 4.54 | 4.1312 | 0.03 | 5.58 | 55 | 0.34 | 18.9 | 57 | 5.11 |
| 10 | 13.14 | 6.31 | 4.1336 | 0.09 | 5.57 | 41 | 0.62 | 27.3 | 39 | 4.97 | |
| 20 | 13.18 | 9.08 | 4.1384 | 0.21 | 5.55 | 24 | 0.90 | 37.9 | 29 | 4.78 | |
| VC0.71 | 5 | 14.10 | 4.31 | 4.1338 | 0.03 | 5.59 | 58 | 0.32 | 16.9 | 64 | 5.19 |
| 10 | 13.41 | 6.09 | 4.1346 | 0.05 | 5.59 | 45 | 0.67 | 21.7 | 49 | 5.06 | |
| 20 | 13.41 | 8.64 | 4.1388 | 0.15 | 5.57 | 27 | 0.86 | 27.9 | 39 | 4.80 | |
| VC0.73 | 5 | 14.38 | 4.18 | 4.1382 | 0.01 | 5.60 | 62 | 0.34 | 20.5 | 52 | 5.17 |
| 10 | 13.60 | 6.39 | 4.1382 | 0.01 | 5.60 | 46 | 0.60 | 27.0 | 40 | 5.03 | |
| 20 | 13.96 | 8.65 | 4.1413 | 0.09 | 5.58 | 24 | 0.87 | 37.8 | 28 | 4.77 | |
| VC0.76 | 5 | 14.61 | 4.24 | 4.1415 | 0.00 | 5.62 | 60 | 0.41 | 19.7 | 54 | 5.16 |
| 10 | 13.82 | 6.10 | 4.1426 | 0.03 | 5.61 | 38 | 0.64 | 27.7 | 39 | 5.02 | |
| 20 | 13.85 | 8.89 | 4.1412 | 0.00 | 5.62 | 25 | 0.84 | 38.9 | 27 | 4.75 |
На рис. 2 в качестве примера показаны СЭМ-изображения исходного микрокристаллического и нанокристаллических порошков VC0.76, полученных размолом в течение 5, 10 и 20 ч. Частицы микрокристаллического порошка имеют размер от 1 до 5 мкм (рис. 2 а), что неплохо согласуется со средним размером частиц DBET. После размола порошок представляет собой совокупность достаточно крупных и в то же время очень рыхлых агрегатов размерами до десятков микрометров, образованных наночастицами, размеры которых уменьшаются с увеличением продолжительности размола, а следовательно, их количество в агрегатах возрастает (рис. 2 б–2г). Похожая картина наблюдается и для остальных порошков VCy, исследуемых в данной работе.
Рис. 2.
СЭМ-изображения порошков VC0.76: а – исходный микрокристаллический порошок; б, в и г – нанокристаллические порошки, полученные размолом исходного порошка в течение 5, 10 и 20 ч соответственно.

Высокоэнергетический размол микрокристаллических порошков VCy сопровождается не только увеличением их удельной поверхности и уменьшением размера частиц, но и увеличением периода решетки aB1, особенно отчетливо это наблюдается для карбидов VC0.69, VC0.71 и VC0.73 (табл. 1 и 2). В работе [25] на крупнозернистых порошках VCy показано, что с увеличением содержания углерода в карбиде увеличивается период решетки aB1. Таким образом, размол VCy должен сопровождаться изменением его состава, а именно, увеличением содержания углерода. Результаты химического анализа (табл. 1 и 2) порошков VCy до и после размола свидетельствуют об обратном: с увеличением продолжительности размола содержание углерода в порошках VCy уменьшается, а содержание кислорода, напротив, растет. В связи с этим увеличение периода решетки при размоле может быть обусловлено внедрением атомов примесного кислорода в вакантные узлы неметаллической подрешетки и образованием оксикарбида ванадия VCyOx [26]. Еще одной причиной изменения периода решетки может быть наличие микродеформаций ε в карбидных частицах, возникающих при высокоэнергетическом размоле, тем более что их величина значительно превышает относительное изменение периода решетки ΔaB1/aB1 в результате размола (табл. 2).
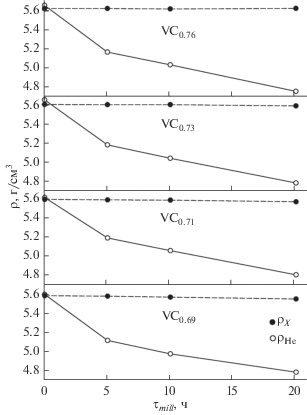
В конечном счете размол порошков VCy сказывается и на их плотности: как на рентгеновской, так и на пикнометрической. Это хорошо иллюстрирует рис. 3 , на котором приведены зависимости плотности порошков VCy от продолжительности размола. Если рентгеновская плотность порошков VCy очень слабо изменяется со временем размола, что обусловлено незначительным изменением периода решетки, согласно выражению (1), то пикнометрическая плотность уменьшается очень значительно, несмотря на то что в порошках вместе с продолжительностью размола увеличивается содержание (3–5 мас. %) примесного WC, плотность которого (15.8 г/см3) почти в три раза превышает плотность VCy (5.6 г/см3). Вероятно, такое изменение пикнометрической плотности нанопорошков, прежде всего, связано с их развитой поверхностью. Удельная поверхность микрокристаллических порошков VCy почти на 2 порядка меньше, чем порошков после размола, а соответственно, микрокристаллические порошки адсорбируют намного меньший объем газа по сравнению с нанопорошками, что подтверждается результатами химического анализа (табл. 1 и 2). Адсорбированные на поверхности наночастиц молекулы газа существенно завышают измеряемый объем нанопорошка, незначительно изменяя его массу, поэтому рассчитанная величина пикнометрической плотности оказывается заниженной, что и наблюдается экспериментально (рис. 3 ).
Проверим эту гипотезу, учитывая только физическую адсорбцию молекул газа на поверхности частиц порошка [27]. Пусть масса порошка, взятого для измерения его пикнометрической плотности ρp равна mp, а объем порошка, который определяется с помощью гелиевого пикнометра, равен Vp, тогда ρp = mp/Vp. Учитывая наличие адсорбированного на поверхности частиц порошка газа, массу и объем порошка можно представить как mp = ms + mg и Vp = Vs + Vg, где ms и Vs – масса и объем частиц порошка; mg и Vg – масса и объем газа, адсорбированного на поверхности частиц порошка. Если истинная плотность частиц порошка (без учета адсорбированного газа) равна ρs = ms/Vs, а массовая доля газа, адсорбированного на поверхности частиц порошка, равна ωg = mg/ms (при ms $ \gg $ mg), тогда пикнометрическую плотность порошка можно записать в следующем виде:
(2)
${{{\rho }}_{p}} = \frac{{1 + {{\omega }_{g}}}}{{\frac{{\text{1}}}{{{{\rho }_{s}}}} + \frac{{{{V}_{g}}}}{{{{m}_{s}}}}}}.$Допустим, что молекулы газа в результате адсорбции образуют на поверхности частиц порошка kg слоев с гексагональной плотнейшей упаковкой (ГПУ), тогда количество молекул адсорбированного газа будет равно
где σg – площадь, занимаемая одной молекулой газа в монослое.С другой стороны, количество молекул адсорбированного газа с молекулярной массой Mg равно ng = mgNA/Mg. Отсюда получаем, что массовая доля газа, адсорбированного на поверхности частиц порошка, равна
(4)
${{\omega }_{g}} = \frac{{{{S}_{{{\text{BET}}}}}{{M}_{g}}{{k}_{g}}}}{{{{\sigma }_{g}}{{N}_{A}}}}.$Объем газа, адсорбированного на поверхности частиц порошка, будет равен Vg = SBETmskghg, где hg – высота монослоя. Подставляя ωg и Vg в выражение (2), получим зависимость пикнометрической плотности порошка от его удельной поверхности
(5)
${{{\rho }}_{p}} = \frac{{1 + {{S}_{{{\text{BET}}}}}\frac{{{{M}_{g}}{{k}_{g}}}}{{{{\sigma }_{g}}{{N}_{A}}}}}}{{\frac{{\text{1}}}{{{{\rho }_{s}}}} + {{S}_{{{\text{BET}}}}}{{k}_{g}}{{h}_{g}}}}.$Поскольку в карбидных нанопорошках содержание кислорода на порядок перекрывает суммарное содержание всех остальных примесей [28], рассмотрим полученную зависимость пикнометрической плотности на примере только молекул кислорода, адсорбированных на поверхности частиц порошка VCy, и сравним ее с экспериментальными данными (табл. 1, 2).
Если предположить, что адсорбированные на поверхности частиц порошка молекулы кислорода образуют ГПУ, то приблизительное значение площади, занимаемой одной молекулой в монослое, можно определить, используя выражение σg = 1.091(Mg/NAρg)2/3 = 0.141 нм2, в котором ρg = 1.41 г/см3 – плотность кислорода в конденсированном состоянии (сжиженном) [29, 30]. Высота монослоя для ГПУ будет равна hg = = dg(2/3)1/2 = 0.247 нм, где dg = 0.302 нм – диаметр молекулы кислорода. С учетом принятых предположений и допущений выражение (5) можно записать в виде
(6)
${{{\rho }}_{p}} = \frac{{1 + A{{S}_{{{\text{BET}}}}}{{k}_{g}}}}{{\frac{1}{{{{\rho }_{s}}}} + B{{S}_{{{\text{BET}}}}}{{k}_{g}}}},$С помощью выражения (6) описаны экспериментальные зависимости пикнометрической плотности порошков VCy от их удельной поверхности (рис. 4 ). В результате аппроксимации определены средние значения истинной плотности ρs частиц порошков VCy и количества монослоев kg кислорода, образованных вследствие адсорбции на поверхности карбидных частиц (табл. 3). Найденные средние значения истинной плотности ρs частиц порошков VCy оказались немного больше их рентгеновской плотности ρX, что объясняется наличием примесного WC в результате размола. Кроме этого, обнаружено, что адсорбированный кислород во всех порошках VCy образует примерно 5–6 монослоев на поверхности частиц, за счет чего и происходит существенное завышение измеряемого объема порошка с большой удельной поверхностью.
Таблица 3.
Результаты аппроксимации экспериментальной зависимости пикнометрической плотности порошков VCy от их удельной поверхности
| Порошок | τmill, ч | ρs, г/см3 | kg | ρp, г/см3 | ωg, мас. % | ωO – ωg, мас. % |
|---|---|---|---|---|---|---|
| VC0.69 | 0 | 5.61 ± 0.02 | 4.9 ± 0.2 | 5.59 ± 0.02 | 0.12 ± 0.01 | 0.25 ± 0.05 |
| 5 | 5.14 ± 0.02 | 3.5 ± 0.2 | 1.0 ± 0.2 | |||
| 10 | 4.97 ± 0.02 | 5.0 ± 0.2 | 1.2 ± 0.2 | |||
| 20 | 4.77 ± 0.02 | 7.0 ± 0.3 | 2.0 ± 0.3 | |||
| VC0.71 | 0 | 5.65 ± 0.07 | 6.0 ± 0.7 | 5.64 ± 0.07 | 0.10 ± 0.01 | 0.09 ± 0.05 |
| 5 | 5.14 ± 0.07 | 3.8 ± 0.5 | 0.5 ± 0.5 | |||
| 10 | 5.02 ± 0.07 | 4.9 ± 0.6 | 1.1 ± 0.6 | |||
| 20 | 4.87 ± 0.07 | 6.3 ± 0.8 | 2.3 ± 0.8 | |||
| VC0.73 | 0 | 5.67 ± 0.03 | 5.0 ± 0.3 | 5.66 ± 0.03 | 0.09 ± 0.01 | 0.14 ± 0.05 |
| 5 | 5.15 ± 0.03 | 3.9 ± 0.3 | 0.3 ± 0.3 | |||
| 10 | 5.01 ± 0.03 | 5.10 ± 0.3 | 1.3 ± 0.3 | |||
| 20 | 4.80 ± 0.03 | 7.14 ± 0.5 | 1.5 ± 0.5 | |||
| VC0.76 | 0 | 5.67 ± 0.03 | 5.1 ± 0.3 | 5.66 ± 0.03 | 0.12 ± 0.01 | 0.15 ± 0.05 |
| 5 | 5.16 ± 0.03 | 3.8 ± 0.3 | 0.5 ± 0.3 | |||
| 10 | 4.99 ± 0.03 | 5.3 ± 0.4 | 0.8 ± 0.4 | |||
| 20 | 4.77 ± 0.03 | 7.5 ± 0.5 | 1.4 ± 0.5 |
Рис. 4.
Пикнометрическая плотность порошков VCy как функция их удельной поверхности SBET (точками на графиках отмечены экспериментальные значения пикнометрической плотности ρHe, а сплошными линиями – их аппроксимация с помощью выражения (6)).
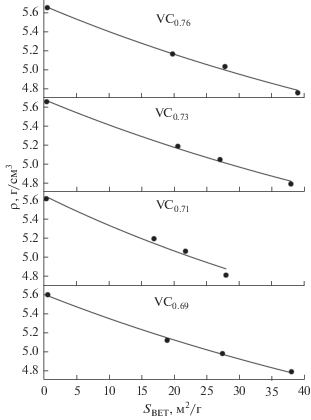
Используя найденные значения ρs и kg, с помощью выражения (6) рассчитаны пикнометрическая плотность порошков ρp и относительное содержание в них кислорода ωg (табл. 3), значения которых хорошо согласуются с экспериментальными данными (табл. 1, 2). Относительное содержание кислорода в порошках VCy, определенное с помощью химического анализа ωO, превышает рассчитанные значения ωg, и разница между ними ωO – ωg возрастает с увеличением удельной поверхности порошка (табл. 3). Во-первых, это может быть связано с тем, что пикнометрическая плотность измерялась на порошках, предварительно участвовавших в измерении их удельной поверхности методом BET, т.е. дегазированных для этих целей, а химический анализ проводился на порошках, не подвергшихся дегазации, следовательно, содержание кислорода в них немного выше, чем в порошках при измерении плотности. Во-вторых, кислород присутствует в порошках карбида ванадия не только в физически адсорбированном виде, как предполагалось в модели, а также может участвовать в хемосорбции, переходя от поверхностного взаимодействия с карбидом ванадия к объемному внедрению, приводя к образованию поверхностных оксидов VOx или оксикарбидов VCyOx, что рассматривалось в качестве одной из причин наблюдаемого увеличения периода решетки в результате размола. Т.е. часть избыточного кислорода ωO – ωg содержится в карбидных частицах в составе оксидных и оксикарбидных фаз, для подтверждения наличия которых необходимы дополнительные исследования.
ЗАКЛЮЧЕНИЕ
Получены микро- и нанокристаллические порошки нестехиометрического кубического карбида ванадия VCy с разным составом в пределах его области гомогенности. Измерения пикнометрической плотности полученных порошков VCy методом гелиевой пикнометрии показали, что пикнометрическая и рентгеновская плотности микрокристаллических порошков практически совпадают, тогда как пикнометрическая плотность нанопорошков заметно уменьшается при увеличении продолжительности размола, сопровождающегося уменьшением среднего размера их частиц и увеличением удельной поверхности. Принимая во внимание только физическую адсорбцию кислорода на поверхности частиц порошков, получили выражение, связывающее их пикнометрическую плотность и удельную поверхность, которое позволяет определять, аппроксимируя экспериментальные данные, относительное содержание кислорода, а также истинную плотность карбидных наночастиц. При сравнении экспериментальных и расчетных значений установлено, что наряду с физической адсорбцией имеет место хемосорбция кислорода, которая может приводить к появлению в порошках оксидных и оксикарбидных фаз.
БЛАГОДАРНОСТЬ
Исследование выполнено в ИХТТ УрО РАН за счет гранта Российского научного фонда (проект РНФ № 14-23-00025).
Автор благодарит О.В. Макарову за помощь в измерении пикнометрической плотности порошков, а также Л.Ю. Булдакову и Д.А. Данилова за помощь в определении содержания углерода и кислорода в исследованных порошках.
Список литературы
Гусев А.И. Нестехиометрия, беспорядок, ближний и дальний порядок в твердом теле. М.: Физматлит, 2007. 856 с.
Gusev A.I., Rempel A.A., Magerl A.J. Disorder and Order in Strongly Nonstoichiometric Compounds: Transition Metal Carbides, Nitrides and Oxides. Berlin–Heidelberg–New York–London: Springer, 2001. 607 p.
Goldschmidt H.J. Interstitial Alloys. New York: Plenum Press, 1967. 820 p.
Baker T.N. Processes, Microstructure and Properties of Vanadium Microalloyed Steels // Mater. Sci. Technol. 2009. V. 25. № 9. P. 1083–1107. doi 10.1179/ 174328409X453253
Fang Z.Z., Wang X., Ryu T., Hwang K.S., Sohn H.Y. Synthesis, Sintering, and Mechanical Properties of Nanocrystalline Cemented Tungsten Carbide – A review // Int. J. Refr. Met. Hard Mater. 2009. V. 27. № 2. P. 288–299 doi 10.1016/j.ijrmhm.2008.07.011
Pötschke J., Gestrich T., Richter V. Grain Growth Inhibition of Hardmetals During Initial Heat-Up // Int. J. Refr. Met. Hard Mater. 2018. V. 72. P. 117–125. doi 10.1016/j.ijrmhm.2017.12.016
Kurlov A.S., Gusev A.I. Tungsten Carbides: Structure, Properties and Application in Hardmetals. Cham–Heidelberg–New York–Dordrecht–London: Springer, 2013. 256 p.
Курлов А.С., Гусев А.И. Физика и химия карбидов вольфрама. М.: Физматлит, 2013. 272 с.
Marshall J.M., Kusoffsky A. Binder Phase Structure in Fine and Coarse WC–Co Hard Metals with Cr and V Carbide Additions // Int. J. Refr. Met. Hard Mater. 2013. V. 40. P. 27–35. doi 10.1016/j.ijrmhm.2013.04.001
Hu Z., Chen C., Meng H., Wang R., Shen P.K., Fu H. Oxygen Reduction Electrocatalysis Enhanced by Nanosized Cubic Vanadium Carbide // Electrochem. Commun. 2011. V. 13. P. 763–765. doi 10.1016/j.elecom.2011.03.004
Huang T., Yu J., Han J., Zhang Z., Xing Y., Wen C., Wu X., Zhang Y. Oxygen Reduction Catalytic Characteristics of Vanadium Carbide and Nitrogen Doped Vanadium Carbide // J. Power Source. 2015. V. 300. P. 483–490. doi 10.1016/j.jpowsour.2015.09.104
Yu J., Gao X., Chen G., Yuan X. Electrocatalytic Performance of Commercial Vanadium Carbide for Oxygen Reduction Reaction // Int. J. Hydrogen Energy. 2016. V. 41. P. 4150–4158. doi 10.1016/j.ijhydene.2016.01.008
Yan Z., Zhang M., Xie J., Shen P.K. Vanadium Carbide and Graphite Promoted Pd Electrocatalyst for Ethanol Oxidation in Alkaline Media // J. Power Source.2013. V. 243. P. 336–342. doi 10.1016/j.jpowsour.2013.06.063
Pinto S., D’Ornelas L., Betancourt P. Synthesis and Characterization of Vanadium Nanoparticles on Activated Carbon and Their Catalytic Activity in Thiophene Hydrodesulphurization // Appl. Surf. Sci. 2008. V. 254. P. 5390–5393. doi 10.1016/j.apsusc.2008.02.100
Коч К., Овидько И.А., Сил С., Вепрек С. Конструкционные нанокристаллические материалы. Научные основы и приложения. М.: Физматлит, 2012. 448 с.
Исаева Н.В., Благовещенский Ю.В., Благовещенская Н.В., Мельник Ю.И., Самохин А.В., Алексеев Н.В., Асташов А.Г. Получение нанопорошков карбидов и твердосплавных смесей с применением низкотемпературной плазмы // Изв. вузов. Порошковая металлургия и функциональные покрытия. 2013. № 3. С. 7–14. doi 10.17073/1997-308X-2013-3-7-14
Hossein-Zadeh M., Razavi M., Safa M., Abdollahi A., Mirzaee O. Synthesis and Structural Evolution of Vanadium Carbide in Nano Scale during Mechanical Alloying // J. King Saud Univ.-Eng. Sci. 2016. V. 28. P. 207–212. doi 10.1016/j.jksues.2014.03.010
Wu Y.D., Zhang G.H., Chou K.C. A Novel Method to Synthesize Submicrometer Vanadium Carbide by Temperature Programmed Reaction from Vanadium Pentoxide and Phenolic Resin // Int. J. Refr. Met. Hard Mater. 2017. V. 62. P. 64–69. doi 10.1016/j.ijrmhm.2016.10.020
Lin H., Tao B.W., Li Q., Li Y.R. In Situ Synthesis of V8C7 Nanopowders from a New Precursor // Int. J. Refr. Met. Hard Mater. 2012. V. 31. P. 138–40. doi 10.1016/ j.ijrmhm.2011.10.003
Kurlov A.S., Gusev A.I. High-Energy Milling of Nonstoichiometric Carbides: Effect of Nonstoichiometry on Particle Size of Nanopowders // J. Alloys Compd. 2014. V. 582. P. 108–118. doi 10.1016/j.jallcom.2013.08.008
Курлов А.С., Гусев А.И. Влияние нестехиометрии на период решетки кубического карбида ванадия VCy // ФТТ. 2017. Т. 59. № 8. С. 1498–1503. doi 10.21883/ FTТ.2017.08.44748.30
Курлов А.С., Белькова Т.Д., Бельков А.М., Ремпель А.А. Нанокристаллические порошки VCy в области гомогенности неупорядоченной кубической фазы // Неорган. материалы. 2015. Т. 51. № 12. С. 1339–1346. doi 10.7868/S0002337X15120040
X’Pert HighScore Plus Version 2.2e. Software for Powder Diffraction Measurements, Phase Identification, Rietveld Refinements and Crystallographic Analyses. PANalytical B. V. 2009.
Гусев А.И., Курлов А.С., Ремпель А.А. Анизотропия деформационных искажений в нанокристаллических порошках VC0.875 // ФТТ. 2015. Т. 57. № 9. С. 1807–1812.
Курлов А.С., Гусев А.И. Эффекты нестехиометрии и упорядочения на периоде базисной решетки карбида ванадия VCy // Письма в ЖЭТФ. 2017. Т. 105. № 6. С. 340–346. doi 10.7868/S0370274X17060030
Щетников Е.Н., Алямовский С.И., Швейкин Г.П., Гельд П.В. Кубические оксикарбиды ванадия // Тр. Ин-та химии. УФАН СССР. 1970. Вып. 17. С. 25–33.
Карнаухов А.П. Адсорбция. Текстура дисперсных и пористых материалов. Новосибирск: Наука, 1999. 470 с.
Красовский П.В., Благовещенский Ю.В., Григорович К.В. Определение содержания кислорода в нанопорошках системы W–C–Co // Неорган. материалы. 2008. Т. 44. № 9. С. 1074–1079.
Emmet P.H., Brunauer S. The Use of Low Temperature Wan der Waals Adsorption Isotherms in Determining in the Surface Area of Iron Synthetic Ammonia Catalysts // J. Am. Chem. Soc. 1937. 59. P. 1553–1564.
McClellan A.L., Harnsberger H.F. Cross-Sectional Areas of Molecules Adsorbed on Solid Surfaces // J. Colloid Interface Sci. 1967. 23. P. 577–599.
Дополнительные материалы отсутствуют.
Инструменты
Неорганические материалы