Неорганические материалы, 2019, T. 55, № 5, стр. 538-543
Исследование особенностей структуры рубидиевых боросиликатных стекол методом ЯМР-спектроскопии
В. Е. Еремяшев 1, 2, *, **, А. С. Мазур 3, П. М. Толстой 3, Л. М. Осипова 2
1 Южно-Уральский государственный университет
454080 Челябинск, пр. Ленина, 76, Россия
2 Институт минералогии УрО Российской академии наук
456317 Челябинская обл., Миасс, Россия
3 Ресурсный центр “Магнитно-резонансные методы исследования” научного парка Санкт-Петербургского государственного университета
198504 Санкт-Петербург, Университетский пр., 26, Россия
* E-mail: eremiashevve@susu.ru
** E-mail: vee-zlat@mail.ru
Поступила в редакцию 27.06.2018
После доработки 30.11.2018
Принята к публикации 10.12.2018
Аннотация
Представлены результаты исследования методом спектроскопии ЯМР на ядрах 11В и 29Si локальной анионной структуры серии боросиликатных стекол системы Rb2O–B2O3–SiO2 с различными мольными соотношениями R = [Rb2O]/[B2O3] и K = [SiO2]/[B2O3]. По относительным интегральным интенсивностям линий в спектрах ЯМР определены доли атомов бора в тройной и четверной координациях, а также концентрации различного типа силикатных Qn-единиц. При сравнении данных об анионной структуре синтезированных стекол системы Rb2O–B2O3–SiO2 и ранее исследованных аналогичных по составу стекол системы Cs2O–B2O3–SiO2 установлено, что различия в степени деполимеризации анионной структуры стекол этих двух серий наиболее выражены при значениях R = 1 и K = 2. При других значениях параметров состава (R = 0.43 и K = 1.43; R = 2.33 и K = 3.33) локальная анионная структура стекол систем Rb2O–B2O3–SiO2 и Cs2O–B2O3–SiO2 изученных составов в значительной степени подобна. Наблюдаемые структурные различия стекол позволяют определить причины отличия значений температуры стеклования, ранее установленного для данных стекол методом дифференциальной сканирующей калориметрии.
ВВЕДЕНИЕ
Важным этапом исследований, посвященных совершенствованию матричных материалов для иммобилизации радиоактивных отходов, является определение термических свойств боросиликатных стекол различных составов [1]. Данные об этих свойствах в зависимости от состава стекла обеспечивают возможность выбора оптимальных параметров синтеза матричных материалов и оценки их термической устойчивости.
Ранее [2] были определены термические свойства аналогичных по составу боросиликатных стекол систем Rb2O–B2O3–SiO2 и Cs2O–B2O3–SiO2 при различных значениях параметров R = = [M2O]/[B2O3] и K = [SiO2]/[B2O3], где M = Rb, Cs и […] – мольная доля компонентов. При сравнении результатов исследования, выполненного методом дифференциальной сканирующей калориметрии (ДСК), было установлено значительное отличие в значении температуры стеклования для стекол состава 0.25Rb2O–0.25B2O3–0.5SiO2 и 0.25Cs2O–0.25B2O3–0.5SiO2 (R =1 и K = 2). Тогда как при других соотношениях компонентов (R = = 0.43 и K = 1.43; R = 2.33 и K = 3.33) для стекол аналогичного состава рубидиевой и цезиевой систем наблюдались близкие значения температуры стеклования. Данный эффект имеет место и по отношению к аналогичным по составу боросиликатным стеклам систем Na2O–B2O3–SiO2 и K2O–B2O3–SiO2 [3].
В соответствии с результатами ранее выполненных исследований основной причиной изменения физико-химических (в т.ч. термических) свойств стекол является изменение в структуре стекол концентрации борсодержащих и кремнийсодержащих структурных единиц различного типа [4–6]. С целью установления структурных факторов, определяющих наблюдаемое для стекол систем Rb2O–B2O3–SiO2 и Cs2O–B2O3–SiO2 отличие в значении температуры стеклования, методом спектроскопии ядерного магнитного резонанса (ЯМР) исследованы особенности локальной анионной структуры стекол системы Rb2O–B2O3–SiO2. Результаты этого исследования были сопоставлены с ранее полученными данными о структуре аналогичных по составу стекол системы Cs2O–B2O3–SiO2 [7].
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Синтез стекол был проведен из реактивов SiO2 калификации “ч. д. а.”, B2O3 квалификации “ос. ч.”в и Rb2CO3 квалификации “х. ч.” (Sigma-Aldrich, США) в соответствии с методикой, описанной в [2, 7, 8], включающей плавление подготовленной смеси в платиновом тигле при температуре 1200–1350°C и охлаждение (закалку) расплава на металлической поверхности. В результате были получены однородные прозрачные стекла.
Отсутствие кристаллических фаз в полученных стеклах было подтверждено методом рентгеновской дифракции (дифрактометр Rigaku Ultima IV, CuKα-излучение, 2θ = 5°–90°). Контроль однородности состава стекол после синтеза осуществлялся с помощью электронного микроскопа (JEOL JSM-7001F, EDS-приставка Oxford). Установлено, что для всех образцов отклонение значений атомных отношений Si/Rb и Si/O на поверхности образцов от расчетных не превышало 2 и 3 отн. % соответственно.
Расчетный состав синтезированных боросиликатных стекол и значения температуры стеклования (tg), ранее определенные методом ДСК [2], представлены в табл. 1.
Таблица 1.
Номинальный состав стекол по синтезу (мольные доли), параметры R = [Rb2O]/[B2O3] и K = = [SiO2]/[B2O3], а также значения температуры стеклования tg
| Обозначение образцов | Химический состав | R | K | tg, °С [2] |
|---|---|---|---|---|
| 15Rb35B | 0.15Rb2O · 0.35B2O3 ∙ 0.5SiO2 | 0.43 | 1.43 | 565 (569*) |
| 25Rb25B | 0.25Rb2O · 0.25B2O3 ∙ 0.5SiO2 | 1 | 2 | 578 (629*) |
| 35Rb15B | 0.35Rb2O · 0.15B2O3 ∙ 0.5SiO2 | 2.33 | 3.33 | 491 (508*) |
Спектры ЯМР были зарегистрированы на оборудовании ресурсного центра “Магнитно-резонансные методы исследования” Научного парка СПбГУ. Для регистрации спектров использовался спектрометр Bruker 400WB Avance III с индукцией внешнего постоянного магнитного поля 9.4 Тл, резонансной частотой 128.4 и 79.5 МГц для ядер 11В и 29Si соответственно. Частота вращения образцов под магическим углом (MAS) составляла 20 кГц. Для размещения примерно одинакового количества предварительно растертого образца использовался ротор из оксида циркония диаметром 3.2 мм. Для возбуждения ядер использовалась последовательность импульсов длительностью 0.2 и 2 мкс и временем задержки 2 и 2.5 с для ядер 11В и 29Si соответственно. Число накоплений составило 32 (11В) и 32 000 (29Si). Химический сдвиг вычислялся как миллионная часть (м. д.) относительно резонансной частоты Н3ВО3 (11В) и (CH3)4Si (29Si), взятых в качестве внешних стандартов. Все спектры измерялись при комнатной температуре.
РЕЗУЛЬТАТЫ ЭКСПЕРИМЕНТА
Во всех полученных 11В-MAS-спектрах ЯМР синтезированных стекол (рис. 1) наблюдается широкая полоса в диапазоне от –10 до 20 м. д. и узкая интенсивная полоса с максимумом вблизи –1 м. д. Основными борсодержащими элементами локальной структуры щелочных боросиликатных стекол являются треугольники ${\text{В O}}_{n}^{'}{\text{О }}_{{3 - n}}^{{\left( {3 - n} \right) - }}$ (O' – мостиковый атом кислорода, O – немостиковый атом кислорода) и тетраэдры [${\text{BO}}_{4}^{'}$]– [9, 10]. Ионы щелочных металлов играют роль компенсатора заряда четырехкоординированного бора в тетраэдрах [${\text{BO}}_{4}^{'}$]– и координируют немостиковые атомы кислорода в треугольниках ${\text{В O}}_{2}^{'}{{{\text{О }}}^{--}}$ и ${\text{В O'О }}_{2}^{{2 - }}.$ В соответствии с данными, полученными в аналогичных исследованиях [7, 8, 11–13], широкая полоса в спектрах указывает на присутствие в стеклах бора в тройной координации (BIII) в составе треугольников ${\text{В O}}_{n}^{'}{\text{О }}_{{3 - n}}^{{\left( {3 - n} \right) - }},$ а узкая соответствует бору в четверной координации (BIV) в тетраэдрах [${\text{BO}}_{4}^{'}$]–. Наблюдаемое при сравнении спектров значительное изменение отношения площади полос, соответствующих трех- и четырехкоординированным атомам бора, указывает на изменение их соотношения в структуре стекол.
Уменьшение интегральной интенсивности сигналов в 11В-MAS-спектрах ЯМР в ряду 15Rb35B → → 25Rb25B → 35Rb15B коррелирует с уменьшением абсолютной концентрации атомов бора в образце.
Для определения относительной концентрации атомов бора в различном координационном окружении (BIII и BIV) в соответствии с подходом, ранее примененным для 11В-спектров ЯМР стекол системы Cs2O–B2O3–SiO2 [7], полученные спектры были представлены в виде суперпозиции двух компонент, имеющих форму линий гауссовой формы (см. рис. 1). Относительные интегральные интенсивности этих компонент отражают долю треугольников ${\text{В O}}_{n}^{'}{\text{О }}_{{3 - n}}^{{\left( {3 - n} \right) - }}$ и тетраэдров [${\text{BO}}_{4}^{'}$]– в структуре синтезированных стекол (N3 и N4 соответственно). Концентрация четырехкоординированных атомов бора была вычислена в соответствии с выражением: N4 = [[B4]/([B4] + [B3])] × × 100%, где [B4] и [B3] – площади резонансных линий, соответствующих атомам бора в трех- и четырехкоординированном состоянии соответственно. Концентрация трехкоординированных атомов бора была вычислена по выражению: N3 = = 100 – N4. Полученные значения N3 и N4 для синтезированных стекол приведены в табл. 2.
Рис. 1.
Спектры ЯМР 11В (а) и 29Si (б) синтезированных боросиликатных стекол системы Rb2O–B2O3–SiO2.
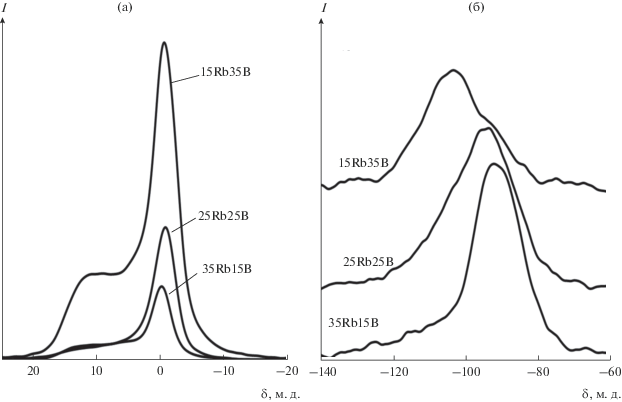
Таблица 2.
Концентрации бора в различном координационном окружении (BIII и BIV) и Qn-единиц в изученных стеклах, рассчитанные по отдельности (Ni) и по отношению к общему количеству структурных единиц ($N_{i}^{'}$)
| Образец | N4 | N3 | ${{N}_{{{{Q}^{4}}}}}$ | ${{N}_{{{{Q}^{3}}}}}$ | ${{N}_{{{{Q}^{2}}}}}$ | $N_{4}^{'}$ | $N_{3}^{'}$ | $N_{{{{Q}^{4}}}}^{'}$ | $N_{{{{Q}^{3}}}}^{'}$ | $N_{{{{Q}^{2}}}}^{'}$ |
|---|---|---|---|---|---|---|---|---|---|---|
| 15Rb35B | 0.41 | 0.59 | 0.84 | 0.14 | 0.02 | 0.24 | 0.36 | 0.35 | 0.06 | 0.01 |
| 25Rb25B | 0.57 | 0.43 | 0.32 | 0.62 | 0.06 | 0.28 | 0.22 | 0.16 | 0.31 | 0.03 |
| 35Rb15B | 0.39 | 0.61 | 0.12 | 0.78 | 0.10 | 0.16 | 0.23 | 0.08 | 0.49 | 0.06 |
29Si-ЯМР-спектры, представленные на рис. 1, имеют достаточно сложную форму, что указывает на сосуществование в структуре стекол кремнийсодержащих единиц различного типа. Сопоставление полученных 29Si-MAS-спектров ЯМР (см. рис. 1) выявило значительное отличие спектра стекла 15Rb35B. Спектры стекол 25Rb25B и 35Rb15B имеют менее значительные различия, связанные с положением главного максимума и низкопольного плеча сигнала.
Основными кремнийсодержащими элементами локальной структуры щелочных боросиликатных стекол являются кремний-кислородные тетраэдры ${\text{SiO}}_{n}^{'}{\text{О }}_{{4 - n}}^{{\left( {4 - n} \right) - }}$ (Qn-единицы), различающиеся по числу мостиковых атомов кислорода (n) [9, 10]. Ионы щелочных металлов координируют немостиковые атомы кислорода в составе кремний-кислородных тетраэдров ${\text{SiO}}_{2}^{'}{\text{О }}_{2}^{{2 - }}$ и ${\text{SiO}}_{3}^{'}{{{\text{О }}}^{ - }}$ (структурные единицы Q2 и Q3). Для количественного определения концентрации Qn-единиц в структуре синтезированных стекол полученные 29Si-MAS-спектры ЯМР, как и спектры ранее изученных аналогичных по составу стекол системы Cs2O–B2O3–SiO2 [7], были представлены в виде суперпозиции трех компонент, имеющих форму линий гауссовой формы с максимумами около –78, –94 и –105 м. д., относительные интегральные интенсивности которых отражают долю единиц Q2, Q3 и Q4 соответственно [7, 8, 14–16]. При анализе полученных значений относительных интегральных интенсивностей этих компонент установлена незначительная концентрация Q2-единицы во всех образцах. В стекле 15Rb35B по сравнению со стеклами 25Rb25B и 35Rb15B значительно выше относительная концентрация Q4-единиц, а концентрация Q3-единиц, наоборот, меньше. Результаты расчетов концентрации единиц Q2, Q3 и Q 4 приведены в табл. 2.
Полученные значения относительных концентраций борсодержащих и кремнийсодержащих структурных единиц (Ni) были пересчитаны в абсолютные значения ($N_{i}^{'}$), отражающие их концентрацию по отношению ко всем типам борсодержащих и кремнийсодержащих единиц в структуре стекла. Результаты расчета приведены в табл. 2. Погрешность определения концентраций структурных единиц составляет ±0.02. Это значение было установлено по колебанию интенсивности линии гауссовой формы при многократном независимом определении их характеристик при работе со спектрами.
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
В соответствии с представленными в табл. 2 данными для синтезированных стекол концентрации BIII и BIV, пропорциональные содержанию боратных треугольников ${\text{В O}}_{n}^{'}{\text{О }}_{{3 - n}}^{{\left( {3 - n} \right) - }}$ и тетраэдров [${\text{В O}}_{4}^{'}$]– в структуре стекла, являются немонотонной функцией отношения [Rb2O]/[B2O3] (рис. 2). При переходе от стекла состава 0.15Rb2O · 0.35B2O3 · · 0.5SiO2 (образец 15Rb35B) к стеклу состава 0.25Rb2O · 0.25B2O3 · 0.5SiO2 (образец 25Rb25B) наблюдаются увеличение концентрации BIII и уменьшение концентрации BIV. Дальнейшее увеличение содержания Rb2O в составе стекла, соответствующее переходу 25Rb25B → 35Rb15B, приводит к уменьшению доли BIII при практически неизменной доле BIV. Аналогичные изменения BIII и BIV были выявлены в ранее изученных аналогичных по составу стеклах системы Cs2O–B2O3–SiO2 (см. рис. 2).
Рис. 2.
Концентрации бора в различном координационном окружении (BIII и BIV) и Qn-единиц в боросиликатных стеклах, рассчитанные по отношению к общему количеству структурных единиц, в зависимости от значения параметра R = [M2O]/[B2O3], где M = Rb, Cs: черные точки и сплошные линии – синтезированные боросиликатные стекла системы Rb2O–B2O3–SiO2, светлые точки и пунктирные линии – ранее изученные боросиликатные стекла системы Cs2O–B2O3–SiO2 [7].
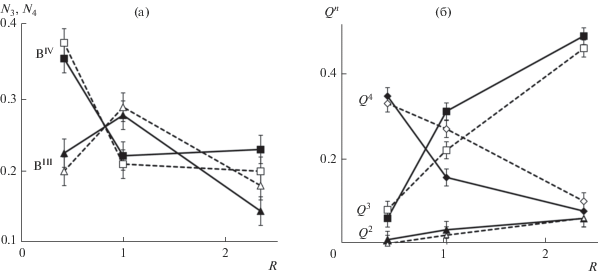
Изменения концентраций Qn-единиц, отражающих долю кремний-кислородных тетраэдров ${\text{SiO}}_{n}^{'}{\text{О }}_{{4 - n}}^{{\left( {4 - n} \right) - }}$ различного типа, также аналогичны наблюдаемым для стекол системы Cs2O–B2O3–SiO2 [7]. По мере увеличения в составе стекла содержания рубидия доля Q4-единиц, содержащих только мостиковые атомы кислорода, уменьшается, а доля Q3- и Q2-единиц увеличивается. Это является закономерным следствием того, что все больше ионов щелочного металла начинает располагаться вблизи немостиковых атомов кислорода, образующихся при разрыве мостиковых связей Si–O–Si(B) в неупорядоченной сетке стекла.
Но в отличие от стекол системы Cs2O–B2O3–SiO2 концентрации Qn-структурных единиц в стеклах системы Rb2O–B2O3–SiO2 изменяются менее линейно. Так, при увеличении R от 0.43 до 1 имеет место более резкое уменьшение доли Q4-единиц, сопровождающееся более значительным увеличением доли Q3-единиц. Однако при R = 2.33 концентрации кремний-кислородных тетраэдров всех типов в структуре стекла состава 0.35Rb2O · · 0.15B2O3 · 0.5SiO2 (образец 35Rb15B) в пределах ошибки расчета (±0.02) совпадает с их концентрациями в структуре стекла состава 0.35Cs2O · · 0.15B2O3 · 0.5SiO2.
Таким образом, при значениях R = 0.43 и K = 1.43 в структуре синтезированных стекол системы Rb2O–B2O3–SiO2 наблюдается преобладание бора в четырехкоординированной форме (BIV), входящего в состав тетраэдров [B${\text{O}}_{4}^{'}$]–. Кремний-кислородные тетраэдры ${\text{SiO}}_{n}^{'}{\text{О }}_{{4 - n}}^{{\left( {4 - n} \right) - }}$ в этом стекле в основном представлены Q4-единицами, а тетраэдры с одним и двумя немостиковым атомом кислорода (Q3- и Q2-единицы) присутствуют в структуре стекла в незначительном количестве. Все это указывает на то, что ионы рубидия в большей степени связаны с борсодержащими структурными единицами [B${\text{O}}_{4}^{'}$]–, и только некоторая часть Rb2O взаимодействует с силикатной составляющей неупорядоченной сетки стекла с образованием немостиковых связей Si–O–.
При R = 1 и K = 2 в структуре синтезированных стекол системы Rb2O–B2O3–SiO2, наоборот, выше доля бора в трехкоординированной форме (BIII) в составе треугольников ${\text{В O}}_{n}^{'}{\text{О }}_{{3 - n}}^{{\left( {3 - n} \right) - }},$ что ранее наблюдалось и для стекол системы Cs2O–B2O3–SiO2. За счет роста содержания Rb2O в составе стекла наблюдается увеличение доли Q3- и Q2-единиц, содержащих одну или две немостиковые связи Si–O–, координируемые ионами Rb+. Более резкое уменьшение концентрации тетраэдров Q4 и рост концентрации Q3-единиц по сравнению с аналогичными по составу стеклами системы Cs2O–B2O3–SiO2 указывает на более значительный рост деполимеризации кремнийсодержащей составляющей сетки стекла. И этот рост закономерно должен сопровождаться снижением доли немостиковых связей B–O– в треугольниках ${\text{В O}}_{n}^{'}{\text{О }}_{{3 - n}}^{{\left( {3 - n} \right) - }},$ которые также координируются ионами щелочного металла.
При R = 2.33 и K = 3.33 в борсодержащей части структуры синтезированных стекол системы Rb2O–B2O3–SiO2 опять преобладает четырехкоординированный бор (BIV) , входящий в состав тетраэдров [B${\text{O}}_{4}^{'}$]–. Наблюдаемое при этом более высоком содержании щелочного металла соотношение Qn-единиц совпадает с этим соотношением для аналогичных по составу стекол системы Cs2O–B2O3–SiO2. Это указывает на менее значительное различие между структурой данных стекол.
ЗАКЛЮЧЕНИЕ
В соответствии с данными проведенного исследования различие локальной анионной структуры аналогичных по составу стекол систем Rb2O–B2O3–SiO2 и Cs2O–B2O3–SiO2 наиболее выражено при значениях параметров R = 1 и K = 2. В стекле состава 0.25Rb2O · 0.25B2O3 ∙ 0.5SiO2, соответствующего данным значениям R и K, по сравнению со стеклом состава 0.25Cs2O · 0.25B2O3 ∙ 0.5SiO2 наблюдается значительно большее участие ионов щелочного металла в формировании кремнийсодержащих Q3-единиц. Таким образом, различие в значении температуры стеклования для аналогичных по составу стекол систем Rb2O–B2O3–SiO2 и Cs2O–B2O3–SiO2 при этих значениях R и K обусловлено разным распределением атомов рубидия и цезия между борсодержащими и кремнийсодержащими структурными единицами стекол. При других содержаниях щелочного металла и бора (R = 0.43 и K = 1.43; R = 2.33 и K = 3.33) различие между локальной анионной структурой стекол систем Rb2O–B2O3–SiO2 и Cs2O–B2O3–SiO2 менее выражено, что проявляется в близких значениях tg.
Список литературы
Nelson A.T., Crum J.V., Tang M. Thermophysical Properties of Multiphase Borosilicate Glass-Ceramic Waste Forms // J. Am. Ceram. Soc. 2014. V. 97. № 4. P. 1177–1186.
Eremyashev V.E., Zherebtsov D.A., Osipova L.M., Danilina E.I. Thermal Study of Melting and Crystallization of Rubidium and Cesium Borosilicate Glasses // Ceram. Int. 2016. V. 42. № 16. P. 18368–18372.
Golubkov V.V., Stolyarova V.L. Glass Transition and Liquidus Temperatures of Low-Alkali Rubidium and Cesium Borosilicate Glasses from the Small-Angle X-ray Scattering Data // Glass Phys. Chem. 2006. V. 32. № 3. P. 287–292.
Inoue H., Masuno A., Watanabe Y., Suzuki K., Iseda T. Direct Calculation of the Physical Properties of Sodium Borosilicate Glass from Its Chemical Composition Using the Concept of Structural Units // J. Am. Ceram. Soc. 2012. V. 95. № 1. P. 211–216.
Grandjean A., Malki M., Montouillout V., Debruycker F., Massiot D. Electrical Conductivity and 11B NMR Studies of Sodium Borosilicate Glasses // J. Non-Cryst. Solids. 2008. V. 354. P. 1664–1670.
Barlet M., Kerrache A., Delaye J.-M., Rountree C.L. SiO2–Na2O–B2O3 Density: A Comparison of Experiments, Simulations and Theory // J. Non-Cryst. Solids. 2013. V. 382. P. 32–44.
Osipov A.A., Eremyashev V.E., Mazur A.S., Tolstoi P.M., Osipova L.M. Structure of Cesium-Borosilicate Glasses According to NMR Spectroscopy // Glass Phys. Chem. 2017. V. 43. № 4. P. 287–293.
Osipov A.A., Eremyashev V.E., Osipova L.M. Structure of Ca–Sr–Ba Sodium–Borosilicate Glasses According to 11B and 29Si NMR Spectroscopy // Glass Phys. Chem. 2018. V. 44. № 2. P. 71–77.
Vedishcheva N.M., Polyakova I.G., Wright A.C. Short and Intermediate Range Order in Sodium Borosilicate Glasses: a Quantitative Thermodynamic Approach // Phys. Chem. Glasses: Eur. J. Glass Sci. Technol. B. 2014. V. 55. № 6. P. 225–236.
Manara D., Grandjean A., Neuville D.R. Advances in Understanding the Structure of Borosilicate Glasses: Raman Spectroscopy Study // Am. Mineral. 2009. V. 94. P. 777–784.
Bray P.J. NMR and NQR Studies of Boron in Vitreous and Crystalline Borates // Inorg. Chem. Acta. 1999. V. 289. № 1–2. P. 158–173.
Dell W.J., Bray P.J., Xiao S.Z. 11B NMR Studies and Structural Modeling of Na2O–B2O3–SiO2 Glasses of High Soda Content // J. Non-Cryst. Solids. 1983. V. 58. P. 1–16.
Angeli F., Charpentier T., de Ligny D., Cailleteau C. Boron Speciation in Soda-Lime Borosilicate Glasses Containing Zirconium // J. Am. Ceram. Soc. 2010. V. 93. № 9. P. 2693–2704.
MacKenzie J.W., Bhatnagar A., Bain D., Bhowmik S., Parameswar C., Budhwani K., Feller S.A., Royle M.L., Martin S.W. 29Si MAS–NMR Study of the Short Range Order in Alkali Borosilicate Glasses // J. Non-Cryst. Solids. 1994. V. 177. P. 269–276.
Schneider J., Mastelaro V.R., Zanotto E.D., Shakhmatkin B.A., Vedishcheva N.M., Wright A.C., Panepucci H. Qn Distribution in Stoichiometric Silicate Glasses: Thermodynamic Calculations and 29Si High Resolution NMR Measurements // J. Non-Cryst. Solids. 2003. V. 325. P. 164–178.
Nanba T., Nishimura M., Miura Y. A Theoretical Interpretation of the Chemical Shift of 29Si NMR Peaks in Alkali Borosilicate Glasses // Geochim. Cosmochim. Acta. 2004. V. 68. № 24. P. 5103–5111.
Дополнительные материалы отсутствуют.
Инструменты
Неорганические материалы


