Неорганические материалы, 2022, T. 58, № 6, стр. 615-624
Вакуумное карбосиликотермическое восстановление оксидов циркония, гафния, ванадия, ниобия, тантала и хрома
Е. И. Истомина 1, *, П. В. Истомин 1, А. В. Надуткин 1, В. Э. Грасс 1, Д. А. Ермакова 1
1 Институт химии ФИЦ Коми НЦ УрО Российской академии наук
167000 Сыктывкар, ул. Первомайская, 48, Россия
* E-mail: istomina-ei@yandex.ru
Поступила в редакцию 22.12.2021
После доработки 16.02.2022
Принята к публикации 17.02.2022
- EDN: DPTAIU
- DOI: 10.31857/S0002337X22050049
Аннотация
Проведено вакуумное карбосиликотермическое восстановление оксидов циркония(IV), гафния(IV), ванадия(V), ниобия(V), тантала(V) и хрома(III) при температуре 1600°С. В качестве восстановителя использовали карбид кремния. Показано, что при восстановлении оксида гафния образуется только карбид гафния; при восстановлении оксидов хрома и ванадия образуются только силицид хрома и силициды ванадия соответственно; при восстановлении оксидов циркония, ниобия и тантала образуются карбиды и силициды соответствующих металлов. Тройные соединения по типу МАХ-фаз не образуются.
ВВЕДЕНИЕ
Актуальным направлением исследований в современном керамическом материаловедении является создание конструкционных материалов для жестких условий эксплуатации. Такие материалы должны длительно противостоять комбинированному действию высоких и экстремально высоких температур, агрессивных сред, динамических и статических нагрузок. Круг веществ-кандидатов, способных обеспечить требуемый уровень эксплуатационных характеристик, весьма ограничен: в основном в него входят некоторые классы бескислородных тугоплавких соединений, в том числе карбиды и силициды переходных металлов IV–VI групп. В настоящее время широкое распространение для синтеза карбидных и силицидных соединений переходных металлов получили методы карботермического и силикотермического восстановления оксидов с использованием в качестве восстановителя соответственно углеродных и кремниевых материалов [1–19]. Вместе с тем сохраняет актуальность поиск новых альтернативных подходов к высокотемпературному восстановительному синтезу, направленному на то, чтобы получать из оксидов тугоплавкие материалы смешанного карбидно-силицидного состава, перспективные для создания на их основе конструкционной керамики для жестких условий эксплуатации.
Одним из таких альтернативных подходов является разрабатываемый нами метод вакуумного карбосиликотермического восстановления оксидов [20–23]. Основная идея метода состоит в том, чтобы использовать в качестве восстановителя карбид кремния (SiC). Поскольку SiC содержит и углерод, и кремний, его использование позволяет одновременно провести процессы карботермического и силикотермического восстановления. В результате открываются принципиально новые возможности для формирования наноструктурированных карбидно-силицидных материалов, в том числе таких, получение которых затруднено либо невозможно при использовании традиционных для высокотемпературной химии методов твердофазного синтеза. В частности, путем вакуумного карбосиликотермического восстановления оксида титана TiO2 были синтезированы с высоким выходом МАХ-фазы Ti3SiC2 и Ti4SiC3 [20, 24, 25]. Следует особо отметить, что МАХ-фаза Ti4SiC3 в виде объемных кристаллов была получена нами впервые. Ранее это соединение удавалось получать только в виде тонких пленок [26, 27], несмотря на то что возможность его существования в виде объемной фазы предсказана теоретически на основании квантово-химических расчетов [28].
Дальнейшее расширение возможностей метода вакуумного карбосиликотермического восстановления для получения тугоплавких карбидов, силицидов, а также гипотетических соединений смешанного карбидно-силицидного состава, образованных по типу МАХ-фаз, может быть достигнуто за счет использования оксидов переходных металлов IV–VI групп. В настоящей работе в качестве исходных оксидов были выбраны ZrO2, HfO2, V2O5, Nb2O5, Та2O5, Cr2O3.
Цель исследования состояла в проведении серии экспериментов по вакуумному карбосиликотермическому восстановлению выбранных оксидов с использованием SiC в качестве восстановителя, а также в изучении фазового состава и микроструктуры полученных продуктов.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
В качестве исходных реагентов в работе использовали порошки оксидов: ZrO2 (чистота 99.5%, ГОСТ 21907-76, Plasmotherm, Россия), HfO2 (99.8%, ТУ 48-4-201-72, PP IGIC NASU, Ukraine), V2O5 (99.9%, ТУ 6-09-02-295-88 Reachim LLC, Россия), Nb2O5 (99.9%, ТУ 6-09-4047-75 Reachim LLC, Россия), Та2O5 (99.9%, ТУ 1764-348-00545484-95, Plasmotherm, Россия), Cr2O3 (99.9%, ТУ 6-09-4272-76, Reachim LLC, Россия). В качестве восстановителя использовали технический карбид кремния (политип 6H-SiC , чистота 99.1%, дисперсность 5 мкм, GOST 26327-84 (64C M5 F1200), Sapphire LLC, Россия). Составы исходных смесей для синтеза приведены в табл. 1. Порошки исходных реагентов смешивали в требуемом соотношении с добавлением воды в качестве временной технологической связки, компактировали и затем гранулировали путем перетирания через сито с размером ячеек 2.5 мм. Полученные гранулы высушивали до полного удаления влаги. Для проведения экспериментов использовали гранулы размером 1.6–2.5 мм.
Таблица 1.
Составы исходных смесей для синтеза, потери массы и фазовый состав продуктов восстановления по данным РФА
| Образец | Состав шихты | Потери массы δm, % | Фазовый состав продуктов по данным РФА, об. % | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ZrC | HfC | NbC | TaC | ZrSi | V5Si3 | NbSi2 | TaSi2 | CrSi | Cr5Si3 | SiC | |||
| 1 | ZrO2 + 2SiC | 47.0 | 30 | ‒ | ‒ | ‒ | 25 | ‒ | ‒ | ‒ | ‒ | ‒ | 45 |
| 2 | HfO2 + 2SiC | 26.8 | ‒ | 50 | ‒ | ‒ | ‒ | ‒ | ‒ | ‒ | ‒ | ‒ | 50 |
| 3 | V2O5 + 4SiC | 53.4 | ‒ | ‒ | ‒ | ‒ | ‒ | 55 | ‒ | ‒ | ‒ | ‒ | 44 |
| 4 | Nb2O5 + 4SiC | 50.6 | ‒ | ‒ | 27 | ‒ | ‒ | ‒ | 60 | ‒ | ‒ | ‒ | 13 |
| 5 | Ta2O5 + 4SiC | 31.8 | ‒ | ‒ | ‒ | 64 | ‒ | ‒ | ‒ | 18 | ‒ | ‒ | 18 |
| 6 | Cr2O3 + 3SiC | 51.2 | ‒ | ‒ | ‒ | ‒ | ‒ | ‒ | ‒ | 20 | 30 | 50 | |
Синтез проводили в лабораторном трехсекционном реакторе, который размещали в рабочей камере вакуумной печи. Детальное описание конструкции и загрузки реактора приведено в работе [24]. Реактор представлял собой систему из трех вложенных друг в друга стеклоуглеродных тиглей марки СУ-2000, внутренние объемы которых были соединены между собой газопроводящими каналами диаметром 5 мм. Гранулированный образец в количестве 10 г загружали в нижнюю секцию реактора. В две верхние секции загружали поглотитель SiO, в качестве которого использовали активированный уголь марки БАУ-А. Такая конструкция реактора обеспечивала защиту печного оборудования от паров SiO. Режим термообработки включал нагрев со скоростью 1500°С/ч; изотермическую выдержку при 1600°С в течение 60 мин; охлаждение со скоростью 4000°С/ч.
Фазовый состав продуктов определяли методом порошковой рентгеновской дифрактометрии на дифрактометре SHIMADZU XRD 6000 (CuKα-излучение, Ni-фильтр). Количественное содержание кристаллических фаз в образцах оценивали по рентгеновским данным методом Ритвельда с помощью программы PowderCell 2.4 [29].
Микроструктуру поверхности продуктов синтеза изучали методом сканирующей электронной микроскопии (СЭМ) на микроскопе TESCAN VEGA 3SBU в режиме отраженных электронов. Локальный элементный состав образцов определяли методом рентгеноспектрального микроанализа (РСМА) с помощью энергодисперсионного микроанализатора X-ACT, совмещенного с электронным микроскопом. Во всех экспериментах оп-ределяли уменьшение массы образцов после термической обработки.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
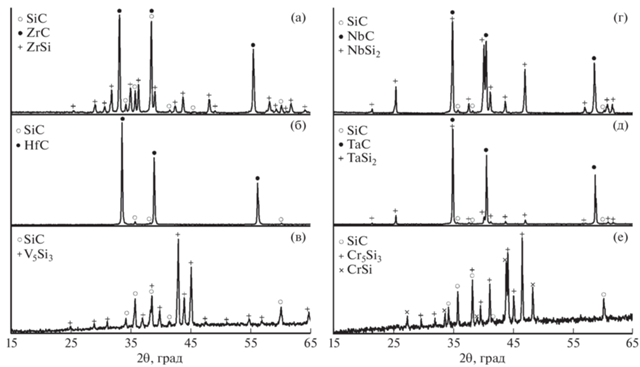
Полученные результаты указывают на протекание процессов карбосиликотермического восстановления соответствующих оксидов металлов. По данным РФА, в продуктах восстановления тройные соединения, образованные по типу МАХ-фазы, не обнаружены. Обнаружены только двойные бескислородные кристаллические фазы, силициды и карбиды соответствующих металлов, качественное и количественное соотношение которых зависит от природы исходного оксида (рис. 1, табл. 1). Следует отметить, что во всех продуктах реакции, по данным РФА, присутствует карбид кремния SiC. Его присутствие вполне закономерно, так как в исходные составы для обеспечения более полного восстановления был заложен избыток восстановителя SiC (табл. 1).
Восстановление ZrO2. Согласно данным РФА, при восстановлении оксида циркония образуются карбид циркония ZrC (кубическая кристаллическая решетка, а = 0.470 нм, пр. гр. Fm3m) в количестве 30 об. % и силицид циркония ZrSi (ромбическая кристаллическая решетка, a = 0.701 нм, b = 0.379 нм, c = 0.531 нм, пр. гр. Pnma) в количестве 25 об. %. (табл. 1, образец 1; рис. 1а).
Обнаруженные методом РФА кристаллические фазы отчетливо различимы при исследовании образцов с помощью СЭМ и идентифицируются методом РСМА. Микроструктура, характерная для образца 1, представлена на рис. 2а. В образце хорошо различимы частицы трех типов: 1) небольшие светлые кристаллы размером 3–5 мкм, по данным РСМА в них присутствуют Zr и С (спектр 1, табл. 2), соответственно, это фаза ZrC; 2) более крупные светлые агломераты неправильной формы, в которых, по данным РСМА, присутствуют Si и Zr (спектр 2, табл. 2), соответственно, это фаза ZrSi; 3) крупные темные кристаллы размером 5–10 мкм, по данным РСМА, определяются Si и С (спектр 3, табл. 2), соответственно, это фаза SiC.
Рис. 2.
СЭМ-изображения и энергетические спектры характеристического рентгеновского излучения представительных участков образцов: 1 (а), 2 (б), 3 (в), 4 (г), 5 (д), 6 (е).
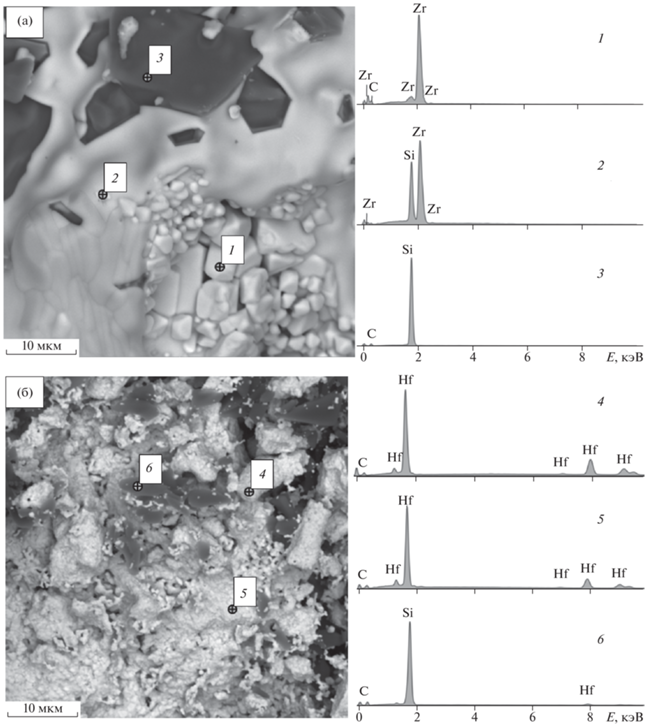
Рис. 2.
Продолжение
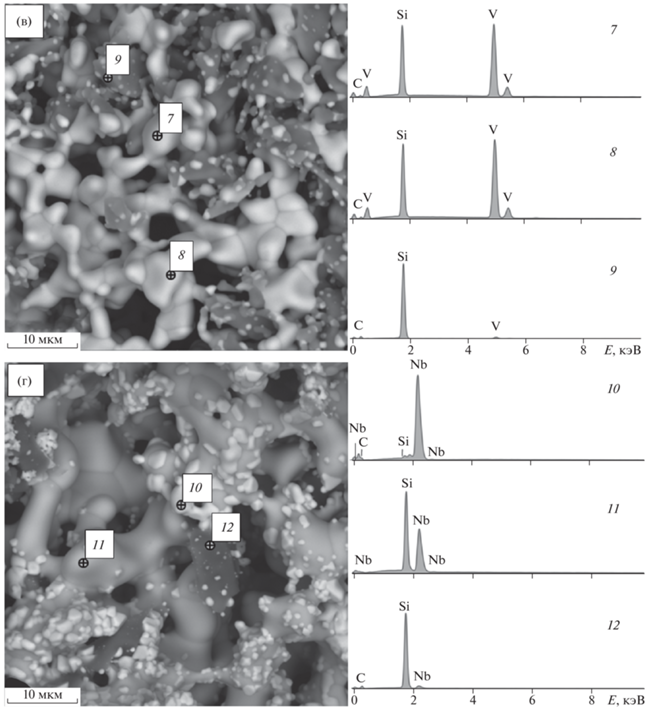
Рис. 2.
Окончание
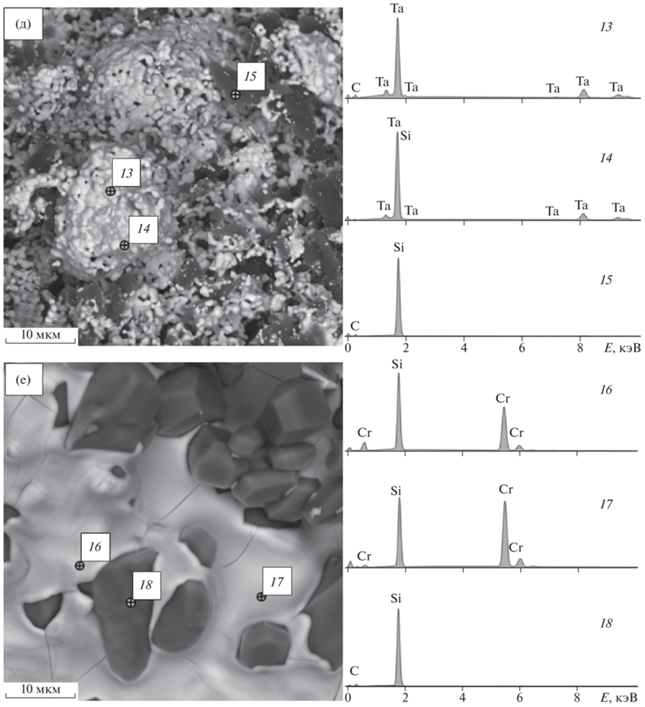
Таблица 2.
Элементный состав представительных участков полученных образцов по данным РСМА
| Рисунок | Спектр | Элементный состав, ат. % | Идентифициро-ванная фаза | |||||||
|---|---|---|---|---|---|---|---|---|---|---|
| C | Si | Zr | Hf | V | Nb | Ta | Cr | |||
| Образец 1 | ||||||||||
| 2а | 1 | 70.0 | − | 30.0 | − | − | − | − | − | ZrC |
| 2 | 22.2 | 35.8 | 42.0 | − | − | − | − | − | ZrSi | |
| 3 | 60.0 | 40.0 | − | − | − | − | − | − | SiC | |
| Образец 2 | ||||||||||
| 2б | 4 | 53.2 | − | − | 43.8 | − | − | − | − | HfC |
| 5 | 62.0 | − | − | 38.0 | − | − | − | − | HfC | |
| 6 | 61.8 | 36.2 | − | 2.0 | − | − | − | − | SiC | |
| Образец 3 | ||||||||||
| 2в | 7 | 16.1 | 31.8 | − | − | 52.1 | − | − | − | V5Si3 |
| 8 | 15.7 | 32.7 | − | − | 51.6 | − | − | − | V5Si3 | |
| 9 | 63.9 | 34.6 | − | − | 1.5 | − | − | − | SiC | |
| Образец 4 | ||||||||||
| 2г | 10 | 53.7 | 1.6 | − | − | − | 44.7 | − | − | NbC |
| 11 | 18.9 | 50.9 | − | − | − | 30.2 | − | − | NbSi2 | |
| 12 | 66.0 | 32.5 | − | − | − | 1.5 | − | − | SiC | |
| Образец 5 | ||||||||||
| 2д | 13 | 64.1 | − | − | − | − | − | 35.9 | − | TaC |
| 14 | 25.1 | 50.8 | − | − | − | − | 24.1 | − | TaSi2 | |
| 15 | 59.8 | 40.2 | − | − | − | − | SiC | |||
| Образец 6 | ||||||||||
| 2е | 16 | 9.9 | 45.9 | − | − | − | − | − | 44.2 | CrSi |
| 17 | 11.6 | 35.4 | − | − | − | − | − | 53.0 | Cr5Si3 | |
| 18 | 64.0 | 36.0 | − | − | − | − | − | − | SiC | |
Восстановление HfO2. При восстановлении оксида гафния, по данным РФА, образуется только карбид гафния HfC (кубическая решетка, а = = 0.464 нм, пространственная группа Fm3m) в количестве 50 об. %. (табл. 1, образец 2; рис. 1б). На рис. 2б представлена микроструктура, характерная для образца 2. В образце различимы частицы двух типов: 1) мелкие светлые частицы размером 1 мкм, в которых, по данным РСМА, присутствуют Hf и С (спектр 4 и 5, табл. 2), соответственно, это фаза HfC; 2) более крупные темные кристаллы, по данным РСМА, в них присутствуют Si и С (спектр 6, табл. 2) , соответственно, это фаза SiC.
Восстановление V2O5. При восстановлении оксида ванадия, по данным РФА, образуется только силицид ванадия V5Si3 (гексагональная кристаллическая решетка, а = 0.717 нм, с = 0.487 нм, пр. гр. P63/mcm) в количестве 55 об. %. (табл. 1, образец 3; рис. 1в). Микроструктура, характерная для образца 3, представлена на рисунке 2 в. В образце различимы частицы двух типов: 1) более светлые, по данным РСМА, в них присутствуют Si и V в соотношении 3 : 5 (спектры 7 и 8, табл. 2), что соответствует фазе V5Si3; 2) темные кристаллы, в которых, по данным РСМА, присутствуют Si и С (спектр 9, табл. 2), что соответствует SiC.
Восстановление Nb2O5. Согласно данным РФА, при восстановлении оксида ниобия образуются карбид ниобия NbC (кубическая кристаллическая решетка, а = 0.446 нм, пр. гр. Fm3m) в количестве 27 об. % и силицид ниобия NbSi2 (гексагональная решетка, а = 0.479 нм, с = 0.658 нм, пр. гр. P6222) в количестве 60 об. %. (табл. 1, образец 4, рис. 1г). Характерная для образца 4 микроструктура представлена на рис. 2г. В образце хорошо различимы частицы трех типов: 1) небольшие светлые кристаллы правильной формы размером 1–3 мкм, по данным РСМА, в них присутствуют Nb и С (спектр 10, табл. 2), что соответствует фазе NbC; 2) более крупные и менее светлые агломераты неправильной формы, в которых, по данным РСМА, присутствуют Si и Nb (спектр 11, табл. 2), что соответствует фазе NbSi2; 3) крупные темные кристаллы размером 5–10 мкм, в которых, по данным РСМА, обнаруживаются Si и С (спектр 12, табл. 2), соответственно, это фаза SiC.
Восстановление Та2O5. При восстановлении оксида тантала, по данным РФА, образуются карбид тантала TaC (кубическая решетка, а = 0.445 нм, пр. гр. Fm3m) в количестве 64 об. % и силицид тантала TaSi2 (гексагональная решетка, а = 0.478 нм, с = 0.657 нм, пр. гр. P6222) в количестве 18 об. % (табл. 1, образец 5; рис. 1д). Микроструктура, характерная для образца 5, представлена на рис. 2 д. В образце различимы частицы трех типов: 1) небольшие светлые кристаллы правильной формы размером 1–2 мкм, по данным РСМА, в них присутствуют Ta и С (спектр 13, табл. 2), что соответствует фазе TaC; 2) небольшие бесформенные более темные частицы, в которых, по данным РСМА, обнаруживаются Si и Ta (спектр 14, табл. 2), что соответствует фазе TaSi2; 3) темные кристаллы, в которых, по данным РСМА, присутствуют Si и С (спектр 15, табл. 2), что соответствует SiC.
Восстановление Cr2O3. По данным РФА, при восстановлении оксида хрома образуются силициды CrSi (кубическая решетка, а = 0.464 нм, пр. гр. P213) в количестве 20 об. % и Cr5Si3 (гексагональная решетка, а = 0.697 нм, с = 0.472 нм, пр. гр. P63/mcm) в количестве 30 об. %. (табл. 1, образец 6; рис. 1е). На рис. 2е представлена микроструктура, характерная для образца 6. В образце хорошо различимы частицы двух типов: 1) светлые неправильной формы, в которых, по данным РСМА, присутствуют Cr и Si в отдельных участках в соотношении 1 : 1, что соответствует фазе CrSi (спектр 16, табл. 2), и в соотношении 5 : 3, что соответствует фазе Cr5Si3 (спектр 17, табл. 2); 2) темные кристаллы, в которых, по данным РСМА, находятся Si и С (спектр 18, табл. 2), что соответствует SiC.
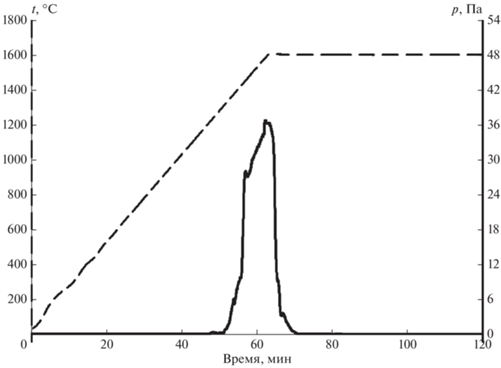
В ходе всех экспериментов по карбосиликотермическому восстановлению наблюдалось активное газообразование. Это приводило к непродолжительному возрастанию давления в вакуумной камере. Типичная кривая изменения давления в вакуумной камере представлена на рис. 3. Газообразование, сопровождающееся ростом давления, начиналось на стадии нагревания и продолжалось до достижения температуры изотермической выдержки 1600°С. После этого давление в вакуумной камере уменьшалось и в течение 10–15 мин изотермической выдержки восстанавливалось до первоначального уровня, что свидетельствовало о завершении газообразования. Согласно данным о потере массы образцов (табл. 1), общее количество газов, выделившихся в ходе термической обработки, составляло около 50% от исходной массы образца. Химический состав газов, образующихся в ходе термической обработки образцов, нами не определялся. Однако можно с уверенностью предположить, что основными компонентами газовой фазы должны быть CO и SiO, которые, как известно, являются основными газообразными продуктами карбосиликотермического восстановления [24, 25]. Подтверждением образования SiO являлось присутствие SiC в углеродном поглотителе, располагавшемся в верхних секциях реактора. Образование SiC происходит в результате взаимодействия SiO с углеродом по реакции
(1)
$~2{\text{C}} + {\text{Si}}{{{\text{O}}}_{{{\text{газ}}}}} = {\text{SiC}} + {\text{C}}{{{\text{O}}}_{{{\text{газ}}}}}.$Таким образом, на основании полученных данных процессы вакуумного карбосиликотермического восстановления оксидов циркония, гафния, ванадия, ниобия, тантала и хрома в условиях избытка карбидкремниевого восстановителя можно описать следующими химическими реакциями:
(2)
$2{\text{Zr}}{{{\text{O}}}_{{\text{2}}}} + 3{\text{SiC}} = 2{\text{ZrC}} + {\text{C}}{{{\text{O}}}_{{{\text{газ}}}}} + 3{\text{Si}}{{{\text{O}}}_{{{\text{газ}}}}},$(3)
$2{\text{Zr}}{{{\text{O}}}_{2}} + {\text{ }}3{\text{SiC}} = {\text{ }}2{\text{ZrSi}} + 3{\text{C}}{{{\text{O}}}_{{{\text{газ}}}}} + {\text{Si}}{{{\text{O}}}_{{{\text{газ}}}}},$(4)
$2{\text{Hf}}{{{\text{O}}}_{2}} + 3{\text{SiC}} = {\text{2HfC}} + {\text{C}}{{{\text{O}}}_{{{\text{газ}}}}} + 3{\text{Si}}{{{\text{O}}}_{{{\text{газ}}}}},$(5)
$10{{{\text{V}}}_{{\text{2}}}}{{{\text{O}}}_{{\text{5}}}} + 31{\text{SiC}} = 4{{{\text{V}}}_{{\text{5}}}}{\text{S}}{{{\text{i}}}_{{\text{3}}}} + 31{\text{C}}{{{\text{O}}}_{{{\text{газ}}}}} + 19{\text{Si}}{{{\text{O}}}_{{{\text{газ}}}}},$(6)
$2{\text{N}}{{{\text{b}}}_{{\text{2}}}}{{{\text{O}}}_{{\text{5}}}} + 7{\text{SiC}} = 4{\text{NbC}} + 3{\text{C}}{{{\text{O}}}_{{{\text{газ}}}}} + 7{\text{Si}}{{{\text{O}}}_{{{\text{газ}}}}},$(7)
$2{\text{N}}{{{\text{b}}}_{{\text{2}}}}{{{\text{O}}}_{{\text{5}}}} + 9{\text{SiC}} = 4{\text{NbS}}{{{\text{i}}}_{{\text{2}}}} + 9{\text{C}}{{{\text{O}}}_{{{\text{газ}}}}} + {\text{Si}}{{{\text{O}}}_{{{\text{газ}}}}},$(8)
$2{\text{T}}{{{\text{a}}}_{{\text{2}}}}{{{\text{O}}}_{{\text{5}}}} + 7{\text{SiC}} = 4{\text{TaC}} + 3{\text{C}}{{{\text{O}}}_{{{\text{газ}}}}} + 7{\text{Si}}{{{\text{O}}}_{{{\text{газ}}}}},$(9)
$2{\text{T}}{{{\text{a}}}_{{\text{2}}}}{{{\text{O}}}_{{\text{5}}}} + 9{\text{SiC}} = 4{\text{TaS}}{{{\text{i}}}_{{\text{2}}}} + 9{\text{C}}{{{\text{O}}}_{{{\text{газ}}}}} + {\text{Si}}{{{\text{O}}}_{{{\text{газ}}}}},$ЗАКЛЮЧЕНИЕ
На основании представленных экспериментальных данных установлено, что при карбосиликотермическом восстановлении оксида гафния образуется только карбид HfC; при карбосиликотермическом восстановлении оксидов ванадия и хрома образуются только силицид ванадия V5Si3 и силициды хрома CrSi, Cr5Si3 соответственно; при восстановлении оксида циркония, оксида ниобия и оксида тантала образуются карбиды ZrC, NbC, TaC и силициды ZrSi, NbSi2, TaSi2 соответствующих металлов. Тройные соединения по типу МАХ-фаз при карбосиликотермическом восстановлении представленных в статье оксидов металлов не образуются.
Список литературы
Sacks M.D., Wang Ch.-A., Yang Z., Jain A. Carbothermal Reduction Synthesis of Nanocrystalline Zirconium Carbide and Hafnium Carbide Powders Using Solution-Derived Precursors // J. Mater. Sci. 2004. V. 39. № 19. P. 6057−6066. https://doi.org/10.1023/B:JMSC.0000041702.76858.a7
Zhanga G., Zhenga Y., Zhanga J., Kea Zh., Zhoua W., Xiong W. Growth of Ceramic Grains during Liquid-Phase Sintering in Ti(C,N)-Based Cermets Prepared by in situ Carbothermal Reduction of TiO2 // Int. J. Refract. Met. Hard Mater. 2019. V. 85. 105060. https://doi.org/10.1016/j.ijrmhm.2019.105060
Liu J.-X., Kan Y.-M., Zhang G.-J. Synthesis of Ultra-Fine Hafnium Carbide Powder and Its Pressureless Sintering // J. Am. Ceram. Soc. 2010. V. 93. № 4. P. 980–986. https://doi.org/10.1111/j.1551-2916.2009.03531.x
Setoudeha N., Saidia A., Welhamb N.J. Carbothermic Reduction of Anatase and Rutile // J. Alloys Compd. 2005. V. 390. № 2. P.138–143. https://doi.org/10.1016/j.jallcom.2004.06.099
Coulibaly M., Arrachart G., Mesbah A., Deschanels X. From Colloidal Precursors to Metal Carbides Nanocomposites MC (M1/4Ti, Zr, Hf and Si): Synthesis, Characterization and Optical Spectral Selectivity Studies // Sol. Energy Mater. Sol. Cells. 2015. V. 143. P. 473–479. https://doi.org/10.1016/j.solmat.2015.07.039
Luo Si-Ch., Guo W.-M., Plucknett K., Lin H.-T. Fine-grained Dual-Phase High-Entropy Ceramics Derived from Boro/Carbothermal Reduction // J. Eur. Ceram. Soc. 2020. V. 41. № 6. P. 3189–3195. https://doi.org/10.1016/j.jeurceramsoc.2020.12.044
Sun G.-D., Wang K.-F., Song Ch.-M., Zhang G.-H. A Low-Cost, Efficient, and Industrially Feasible Pathway for Large Scale Preparation of Tungsten Nanopowders // Int. J. Refract. Met. Hard Mater. 2019. V. 78. P. 100–106. https://doi.org/10.1016/j.ijrmhm.2018.08.013
Sun X., Deng Ch., Ma J., Zhao X., Hao Sh., Li Z., Liu B. The Study of Carbothermic Reduction-Sintering of ZrO2–ZrC–C Composite Microspheres Prepared by Internal Gelation // J. Mater. Sci. 2018. V. 53. № 20. P. 14149–14159. https://doi.org/10.1007/s10853-018-2646-0
Rambo C.R., Bernardes J.C., Sieber H., Muller D. Synthesis of Biomorphic ZrC/C Ceramics from Rattan through Zirconium Oxychloride Infiltration and Carbothermal Reduction // J. Porous Mater. 2021. V. 28. № 1. P. 157–163. https://doi.org/10.1007/s10934-020-00979-w
Симоненко Е.П., Симоненко Н.П., Нагорнов И.А., Мокрушин А.С. и др. Зависимость реакционной способности высокодисперсной системы Ta2O5−HfO2− C от температуры карбонизации ксерогеля // Журн. неорган. химии. 2021. Т. 66. № 5. С. 648–657. https://doi.org/10.31857/S0044457X21050202
Симоненко Е.П., Симоненко Н.П., Нагорнов И.А., Шичалин О.О. и др. Влияние на реакционное искровое плазменное спекание системы Ta2O5−C недостатка углерода и допирования оксидом гафния // Журн. неорган. химии. 2021. Т. 66. № 12. С. 1762–1769. https://doi.org/10.31857/S0044457X21120175
Bhaskar P., Kishor J., Chatterjee A., Majumdar S., Kain V., Dey G.K. A Study on Feasibility of Preparation of W–Cr–Si Alloys by Silicothermic co-Reduction and Characterization of as Cast co-Reduced Alloy // J. Alloys Compd. 2017. V. 701. P. 864–869. https://doi.org/10.1016/j.jallcom.2017.01.163
Peng B., Wu L., Zhu J.-H., Hou Y., Zhang G.-H. A Novel Method for Preparing Ti5Si3 from Ti-Bearing Blast Furnace Slag // Metall. Res. Technol. 2020 V.117. № 6. P. 614. https://doi.org/10.1051/metal/2020073
Istomina E.I., Istomin P.V., Nadutkin A.V., Grass V.E. Desiliconization of Leucoxene Concentrate with Vacuum Silicothermal Reduction // Refract. Ind. Ceram. 2020 V. 61. № 2. P. 129–133. https://doi.org/10.1007/s11148-020-00443-x
Cuskelly D.T., Kisi E.H. Single-Step Carbothermal Synthesis of High-Purity MAX Phase Powders // J. Am. Ceram. Soc. 2016. V. 99. № 4. P. 1137–1140. https://doi.org/10.1111/jace.14170
Cetinkaya S., Eroglu S. Synthesis and Reaction Mechanism of Ti3SiC2 Ternary Compound by Carbothermal Reduction of TiO2 and SiO2 Powder Mixtures // Ceram. Int. 2012. V. 38. P. 6445–6453. https://doi.org/10.1016/j.ceramint.2012.05.020
Cetinkaya S., Eroglu S. Effect of Temperature and Ar Flow Rate on Ti3SiC2 Formation from TiSiO4 Powders Coated with Pyrolytic Carbon // Int. J. Refract. Met. Hard Mater. 2014. V. 43. P. 69–76. https://doi.org/10.1016/j.ijrmhm.2013.11.002
Istomin P., Nadutkin A., Grass V. Fabrication of Ti3SiC2-based Composites from Titania-Silica Raw Material // Mater. Chem. Phys. 2015. V. 162. P. 216–221. https://doi.org/10.1016/j.matchemphys.2015.05.060
Голдин Б.А., Истомин П.В., Рябков Ю.И. Восстановительный твердофазный синтез карбосилицида титана Ti3SiC2 // Неорган. материалы. 1997. Т. 33. № 6. С. 691– 693.
Istomin P., Istomina E., Nadutkin A., Grass V., Presniakov M. Synthesis of a bulk Ti4SiC3 MAX Phase by Reduction of TiO2 with SiC // Inorg. Chem. 2016. V. 55. P. 11050–11056. https://doi.org/10.1021/acs.inorgchem.6b01601
Istomin P., Istomina E., Nadutkin A., Grass V., Leonov A., Kaplan M., Presniakov M. Fabrication of Ti3SiC2 and Ti4SiC3 MAX Phase Ceramics through Reduction of TiO2 with SiC // Ceram. Int. 2017. V. 43. № 18. P. 16128–16135. https://doi.org/10.1016/j.ceramint.2017.08.180
Istomin P., Istomina E., Nadutkin A., Grass V., Kaplan M. Fabrication of Ti3SiC2-Ti4SiC3-SiC Ceramic Composites through Carbosilicothermic Reduction of TiO2 // Int. J. Appl. Ceram. Technol. 2019. V. 16. P. 746–752. https://doi.org/10.1111/ijac.13101
Истомин П.В., Беляев И.М., Истомина Е.И., Надуткин А.В., Грасс В.Э. Карбосиликотермический синтез керамических композитов Ti3SiC2–TiB2–SiC из лейкоксенового концентрата // Неорган. материалы. 2021. Т. 57. № 3. С. 327–334. https://doi.org/10.1134/s0020168521030067
Истомина Е.И., Истомин П.В., Надуткин А.В. Получение Ti3SiC2 восстановлением диоксида титана карбидом кремния // Неорган. материалы. 2016. Т. 52. № 2. С. 166–172. https://doi.org/10.1134/S0020168516020059
Истомина Е.И., Истомин П.В., Надуткин А.В., Грасс В.Э., Богданова А.С. Оптимизация карбосиликотермического синтеза МАХ-фазы Ti4SiC3 // Неорган. материалы. 2018. Т. 54. № 6. С. 554–563. https://doi.org/10.1134/S0020168518060055
Palmquist J.-P., Li S., Persson P.O. A. et al. Mn + 1AXn Phases in the Ti–Si–C System Studied by Thin-Film Synthesis and ab Initio Calculations // Phys. Rev. B. 2004. V. 70. № 16. P. 165401/1-165401/13. https://doi.org/10.1103/PhysRevB.70.165401
Scabarozi T.H., Hettinger J.D., Lofland S.E. et al. Epitaxial Growth and Electrical-Transport Properties of Ti7Si2C5 thin Films Synthesized by Reactive Sputter-Deposition // Scr. Mater. 2011. V. 65. № 9. P. 811–814. https://doi.org/10.1016/j.scriptamat.2011.07.038
Enyashin A.N., Ivanovski A.L. Quantum-Chemical Modelling of Nanotubes of Titanium Silicocarbides Ti2SiC, Ti3SiC2, and Ti4SiC3 // Theor. Exp. Chem. 2009. V. 45. N. 2. P. 98–102. https://doi.org/10.1007/s11237-009-9077-6
Kraus W., Nolze G. Powder Cell – a Program for the Representation and Manipulation of Crystal Structures and Calculation of the X-ray Powder Patterns // J. Appl. Crystallogs. 1996. V. 29. P. 301–303. https://doi.org/10.1107/S0021889895014920
Дополнительные материалы отсутствуют.
Инструменты
Неорганические материалы