Неорганические материалы, 2022, T. 58, № 9, стр. 965-972
Прямой синтез наночастиц меди и ее оксидов из объемного образца методом индукционной потоковой левитации
А. А. Капинос 1, А. Н. Марков 1, А. Н. Петухов 1, К. В. Отвагина 1, О. В. Казарина 1, А. В. Воротынцев 1, *
1 Нижегородский государственный университет им. Н.И. Лобачевского
603022 Нижний Новгород, пр. Гагарина, 23, Россия
* E-mail: an.vorotyntsev@gmail.com
Поступила в редакцию 12.03.2022
После доработки 19.05.2022
Принята к публикации 14.06.2022
- EDN: XDJWCA
- DOI: 10.31857/S0002337X22090068
Аннотация
Наночастицы Cu, Cu@Cu2O и CuO были получены из объемного образца методом индукционной потоковой левитации. Рассматриваемый метод обладает рядом преимуществ, таких как высокая производительность и непрерывность процесса получения наночастиц (НЧ), возможность регулирования их размера в широком диапазоне, бесконтактный нагрев, что обуславливает высокую чистоту получаемого продукта. Для получения наночастиц со структурой core-shell (ядро/оболочка) и оксида меди подпитка кислородом осуществлялась в различные зоны кварцевого реактора. Полученные наночастицы были охарактеризованы различными физико-химическими методами.
ВВЕДЕНИЕ
В материалах на основе наночастиц (НЧ) появляются новые уникальные свойства по сравнению с объемными материалами из-за высокого отношения удельной поверхности к объему [1, 2]. Металлические НЧ нашли применение в качестве катализаторов [3], биосенсорике [4], для хранения информации [5], в оптике [6], медицине для диагностики и лечения заболеваний [7, 8].
К примеру, высокая каталитическая активность НЧ меди вызвала повышенное внимание для применения в органических синтезах [9, 10]. Фотокаталитические свойства НЧ меди используются для очистки сточных вод от органических красителей в промышленных объемах [11]. Благодаря достаточно высокой проводимости НЧ меди используют в токопроводящих чернилах и в электронике [12, 13]. Кроме того, НЧ меди обладают бактерицидными и антимикробными свойствами [14–16].
Основным ограничением в использовании НЧ меди служит их склонность к окислению и, как следствие, высокая агрегация во время хранения [17]. Одним из способом решения данной проблемы является получение НЧ со структурой типа core-shell (ядро/оболочка) [18].
Наночастицы Cu@Cu2O могут применяться в фотокаталитическом преобразовании CO2 в HCOOH [19]. Также было обнаружено, что такие наночастицы являются каталитически активными при получении водорода из борана аммиака путем гидролиза [20, 21].
В последние несколько лет для синтеза НЧ используется множество методов, которые можно разделить на физические и химические. К физическим можно отнести импульсную лазерную абляцию [22], планетарно-шаровое измельчение [23], физическое осаждение из газовой фазы [24] и др. Химические способы синтеза включают золь–гель-метод [25], химическое восстановление [26], сонохимический метод [27], электрохимическое осаждение [28], гидротермический метод [13] и др. Использование опасных химических веществ, высокие температуры, а также сложность подготовки этих методов ограничивают их применение в промышленности.
В настоящее время одним из наиболее перспективных способов получения НЧ является метод индукционной потоковой левитации (ИПЛ). Основными его преимуществами являются высокая производительность (до 100 г/ч), контроль размера НЧ в широком диапазоне (0.5–500 нм), бесконтактный нагрев (до 2500°С) и отсутствие вредных побочных продуктов, что определяет высокую чистоту получаемых НЧ и экологичность. Отличительной чертой данного метода является испарение металла в состоянии левитации в высокочастотном поле индуктора особой конфигурации. И хотя метод ИПЛ (метод Гена–Миллера) был открыт в начале 60-х годов, он не нашел широкого применения в промышленности. В настоящее время все больше научных групп изучают возможности этого метода для получения НЧ металлов и их соединений. В работе [29] описано получение НЧ титана методом ИПЛ в токе аргона, а добавление водорода в качестве реакционного газа позволило получить НЧ гидрида титана [30].
Целью данной работы было получение НЧ Cu, Cu@Cu2O и CuO со средним размером менее 40 нм методом ИПЛ в потоке аргона. Для получения НЧ Cu@Cu2O и CuO подпитка кислородом в поток газа-носителя осуществлялась в различные зоны кварцевого реактора, чем было обусловлено получение разных типов медьсодержащих наночастиц.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Используемые материалы. В качестве исходных материалов были использованы: медная проволока диаметром 0.5 мм (99.999%, Sigma-Aldrich, Германия); гексан “о. с. ч.” (ООО “Компонент-реактив”, Россия); аргон (99.9995%) (ООО “Мониторинг”, Россия) и кислород (99.9995%) (ООО “Мониторинг”, Россия).
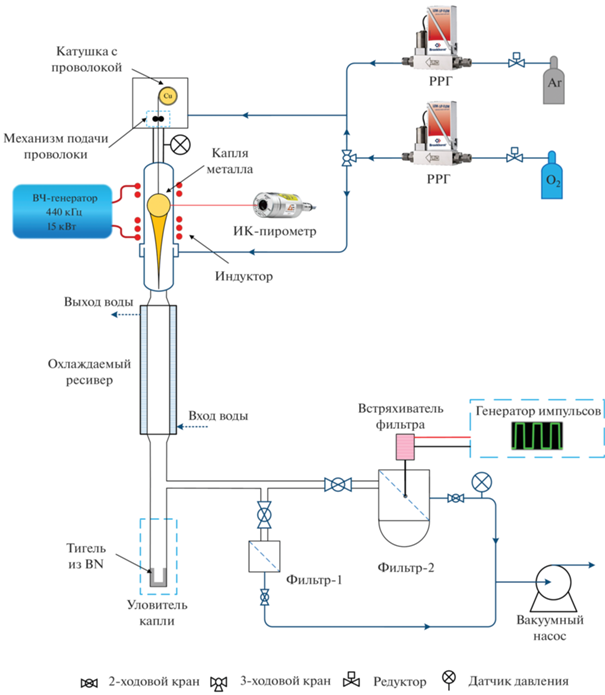
Установка и методика синтеза. Схема установки изображена на рис. 1. Объемный образец подвешивался внутри кварцевого реактора за подпитывающую проволоку и представлял из себя шарик, смотанный из проволоки, массой 0.5 г. На первой стадии вся система откачивалась на вакуум до 10–2–10–3 мбар (давление контролировалось датчиком Pfeiffer Vacuum, США) в течение 3 ч для удаления следовых количеств воды и воздуха. На второй стадии система наполнялась инертным газом до атмосферного давления и подавался газ-хладогент со скоростью потока 10 л/мин (регулировка происходила с помощью массового контроллера расхода газа Bronkhorst, Нидерланды). На индуктор подавалось напряжение и происходил индукционный нагрев образца, который расплавлялся и находился в состоянии левитации. Для того чтобы капля расплавленного металла удерживалась в состоянии левитации, индуктор, изготовленный из медной трубки сечением 3 мм, имел три нижних и два верхних витка, направленных друг другу навстречу (рис. 2а). После разогрева до температуры выше температуры плавления с поверхности расплавленного образца происходило испарение атомов, при этом визуально наблюдался плотный поток образующихся НЧ (рис. 2б).
Для подпитки испаряемого образца, одновременно с началом испарения атомов, осуществлялось восполнение капли путем беспрерывного ввода проволоки диаметром 0.5 мм в расплавленную каплю. Такой малый диаметр проволоки выбран для минимизации влияния температурного градиента на левитирующий образец; кроме того, проволока такого диаметра “не видна” для электромагнитного поля. С этого момента начинался “выход на режим”, который длился 60 мин. Данная стадия необходима для выхода на стационарные условия синтеза. Испарившиеся атомы металла газом-носителем срывались с поверхности капли, образуя НЧ в зоне конденсации, а затем собирались на фильтр-1. По истечении 60 мин кран на фильтр-1 закрывался и открывался кран на фильтр-2, на котором осуществлялся сбор НЧ для дальнейшего изучения (рабочий режим 60–120 мин). Фильтр-2 оборудован электромагнитным встряхивателем, который автоматически срабатывает при повышении давления в системе на 0.01 мбар. Повышение давления в системе связано с забиванием фильтрующего материала НЧ. Для контроля стационарности процесса температура левитирующего образца фиксируется с помощью инфракрасного пирометра IMPAC ISR 6 (Advanced Energy Industries Inc., США). Завершение синтеза НЧ осуществлялось переключением потока газа-носителя с НЧ обратно на фильтр-1, а краны, установленные до и после фильтра-2, закрывались для сохранения полученных НЧ в инертной атмосфере аргона. Затем подача напряжения на индуктор уменьшалась до минимального значения, при котором расплавленный образец удерживался в состоянии левитации для снижения его температуры и прекращения испарения атомов с его поверхности. На заключительном этапе подача напряжения прекращалась и капля под действием силы тяжести падала в нижнюю часть установки, в специальный уловитель в виде стакана, изготовленного из нитрида бора.
Для получения НЧ Cu@Cu2O использовался реактор с дополнительным боковым вводом для подачи кислорода с расходом 3 л/мин в область конденсации через специальный кольцевой зазор. НЧ оксида меди были получены при подаче кислорода вместе с аргоном сверху в прямоточный кварцевый реактор с расходом 3 и 10 л/мин. В первых двух случаях давление в реакторе поддерживалось на уровне атмосферного, а для получения НЧ оксида меди с наименьшим размером давление в системе поддерживалось на уровне 400 мбар.
Дальнейшая работа с полученными НЧ меди проводилась в инертном боксе (Mbraun Labstar, Германия), работающем в атмосфере аргона с концентрацией кислорода меньше 0.5 ppm. При работе с НЧ Cu@Cu2O и CuO такие манипуляции не требовались, так как они инертны к кислороду атмосферного воздуха.
Для индукционного нагрева использовался высокочастотный генератор мощностью 10 кВт с частотой 0.44 МГц, скорость подпитки образца составляла 3 г/ч.
Методы характеризации. Морфологию НЧ Cu и Cu@Cu2O изучали методом просвечивающей электронной микроскопии (ПЭМ). Структурные характеристики нанопорошков оценивали методом низкотемпературной адсорбции азота при 77 K с использованием методов БЭТ, STSA (анализ внешней поверхности по методу статистической толщины). Фазовый состав образцов был определен методом рентгенофазового анализа (РФА). Динамическое рассеяние света (ДРС), ПЭМ, БЭТ, РФА использовались для анализа распределения НЧ по размерам и сравнения в рамках различных методов.
ПЭМ и SAED. ПЭМ, в т.ч. электронная дифракция на выбранной области – SAED, проводилась на приборе LIBRA 200 MC Schottky Carl Zeiss AG (Германия) с автоэмиссионной пушкой, работающей при 200 кВ с пределом разрешения 0.12 нм. Отбор проб проводился на стандартные медные сетки для ПЭМ с формварной поддерживающей сеткой типа Lacey, 200 mesh, пробоподготовка проводилась путем ультразвукового диспергирования наночастиц в н-гексане с последующим нанесением (“фишингом”) на ПЭМ-сетки.
РФА. Фазовый состав синтезированных НЧ был определен с использованием РФА (Shimadzu XRD-7000, Япония). Измерения проводились при 40 кВ и 30 мА. Рассеивающая щель RS передней части детектора имела ширину 0.3 мм. Экспозицию проводили в диапазоне углов (2θ) 10°–80°. Шаг сканирования составлял 0.02°, экспозиция на каждом шаге 0.5 с.
ДРС. Распределение наночастиц по размерам было получено методом ДРС на приборе NANO-flex II (Microtrac Inc., США), позволяющим анализировать частицы в диапазоне от 0.3 нм до 10 мкм. В качестве жидкой фазы для суспензии НЧ был использован н-гексан при значениях ζ-потенциала 40–46 мВ, определенного на приборе NANO-flex Stabino (Microtrac Inc., США). Концентрация приготовленных суспензий составляла 1000 ppm, диспергирование НЧ проводили помещением суспензии в ультразвуковую ванну на 20 мин.
Низкотемпературная адсорбция азота. Удельная площадь поверхности и средний размер частиц определяли по изотермам абсорбции/десорбции азота при 77 K на приборе SorbiMS (ООО МЕТА, Россия). Площадь поверхности рассчитывали методами БЭТ и STSA, по удельной поверхности, полученной методом БЭТ, был рассчитан средний размер частиц.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Как было отмечено ранее, метод ИПЛ применяется для синтеза НЧ металлов. Однако применение газов-окислителей позволяет получать НЧ оксидов металлов, а также НЧ типа соre-shell, обладающие свойствами металлов, но имеющих кристаллический защитный слой до 5 нм, предотвращающий дальнейшее окисление металла.
В работе были экспериментально подобраны конфигурации реакторов, позволившие получить НЧ меди и ее оксида (CuO) в прямоточном реакторе и core-shell в реакторе с боковым вводом. Особенность реактора с боковым вводом позволила получать структуры core-shell благодаря окислению приповерхностного слоя в только что закристаллизованных НЧ. Изменение концентрации кислорода напрямую влияет на толщину оксидной пленки получаемых наноструктур.
Морфологию полученных НЧ исследовали методом ПЭМ. На рис. 3а представлена микрофотография НЧ меди, представляющих собой агломераты со сферическими зернами средним диаметром 36 нм с логнормальным распределением. На SAED-диаграмме на (рис. 3б), наблюдаются дифракционные кольца 111, 200, 220, 400, 311, 420 и 422, характерные для меди.
Рис. 3.
ПЭМ-изображения с распределением по размерам НЧ Cu (а, в, д), SAED-диаграммы (б, г, е) НЧ Cu (а, б), Cu@Cu2O (в, г), CuO (д, е).
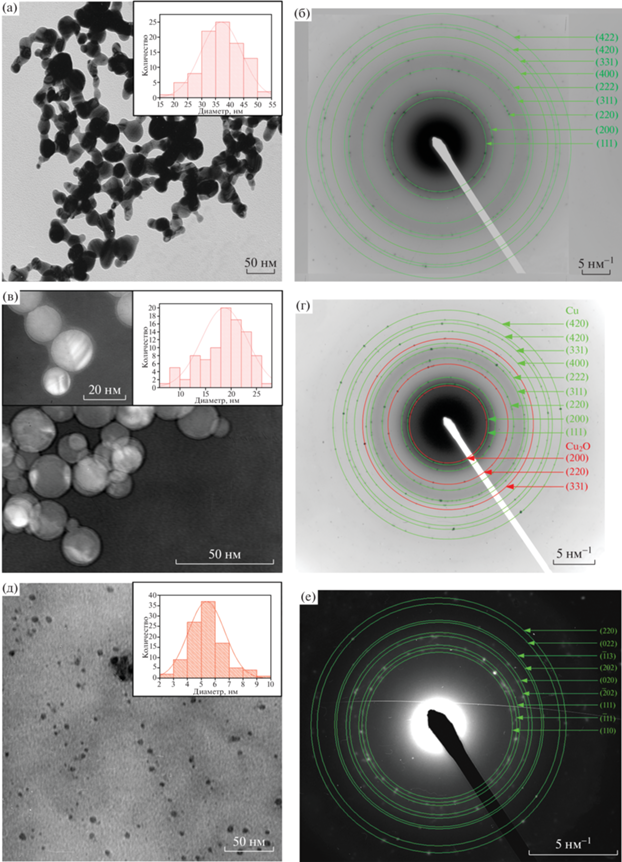
Согласно микрофотографии на рис. 3в, при подаче кислорода через специальный кольцевой зазор в зону конденсации получены наночастицы core-shell, средний размер которых составлял 21 нм со средней толщиной оболочки Cu2O 2 нм. На рис. 3г представлена SAED-диаграмма наночастиц Cu@Cu2O, на которой помимо дифракционных колец от меди обнаружены дифракционные кольца 200, 220 и 311 от Cu2O. Это свидетельствует о том, что оболочка на поверхности НЧ состоит из оксида меди Cu2O.
Состав оболочки обусловлен тем, что кислород подавался через кольцевой зазор в ламинарный поток аргона, поэтому распределение кислорода в зоне реакции (где происходит окисление поверхности образовавшихся НЧ меди) неравномерно (чем ближе к стенкам, тем больше концентрация кислорода). Так как поток НЧ находился в центральной части реактора, где концентрация кислорода наименьшая, окисление поверхности НЧ меди происходило до оксида меди(I).
При подаче смеси аргона и кислорода через верхнюю часть при пониженном давлении (400 мбар) в установке были получены НЧ CuO (рис. 3д), которые представляют собой изолированные сферы со средним размером 5 нм. На SAED-диаграмме (рис. 3е) наблюдаются дифракционные кольца 110, $\bar {1}$11, 111, $\bar {2}$02, 020, 202, $\bar {1}$13, 022 и 220 оксида меди(II).
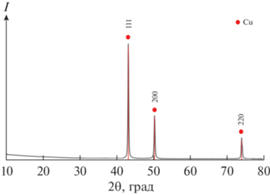
На рис. 4 представлена рентгенограмма наночастиц меди, полученных методом ИПЛ. Наблюдались характерные дифракционные пики меди (PDF № 04-0836), расположенные при 2θ 43.3°, 50.4° и 74.1°. Они соответствуют рефлексам 111, 200 и 220 ГЦК-структуры.
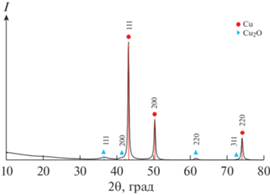
На рентгенограмме НЧ Cu@Cu2O, полученных при добавлении кислорода (рис. 5), присутствуют характерные дифракционные пики меди (рис. 4), а также рефлексы оксида меди(I) 111, 200, 220 и 311 при углах 36.4°, 42.3°, 61.3° и 73.5°. Положения пиков соответствуют стандарту Cu2O (PDF № 05-0667).
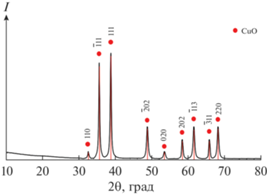
На рентгенограмме НЧ CuO (рис. 6) видны характерные пики оксида меди(II) 110, $\bar {1}$11, 111, $\bar {2}$02, 020, 202, $\bar {1}$113, $\bar {3}$11 и (220) (PDF № 48-1548) при 2θ: 32.52°, 35.55°, 38.73°, 48.75°, 53.4°, 58.31°, 61.57°, 65.8° и 68.13°.
Стоит отметить, что во всех трех образцах не обнаружено рефлексов каких-либо примесных компонентов, что говорит о возможности получения высокочистых НЧ методом ИПЛ. Данный факт обусловлен, во-первых, бесконтактным нагревом металла, предотвращающим взаимодействие капли расплава с частями экспериментальной установки, а во-вторых, одностадийностью данного метода и отсутствием дополнительных загрязнений из используемых реактивов.
На основании полученных рентгенограмм по формуле Шеррера был рассчитан средний размер кристаллитов (табл. 1):
где К – постоянная Шеррера (К = 0.94); λ – длина волны рентгеновского излучения (длина волны CuKα-излучения 0.15418 нм), β – ширина рефлекса на полувысоте, θ – угол дифракции.Таблица 1.
Характеристики полученных НЧ
| Образец | $S_{{{\text{уд}}}}^{{{\text{БЭТ}}}}$, м2/г | $S_{{{\text{уд}}}}^{{{\text{STSA}}}}$, м2/г | DБЭТ, нм | DПЭМ, нм | DРФА, нм | DДРС, нм |
|---|---|---|---|---|---|---|
| Cu | 17.2 | 17.3 | 39 | 36 | 37 | 86 |
| Cu@Cu2O | 21.4 | 21.7 | – | 31 | 34 | 56 |
| CuO | 119.8 | 122.1 | 8 | 5 | 6 | 7 |
На заключительной стадии работы методом динамического рассеяние света были определены размеры полученных НЧ и их распределение по размерам. Суспензии НЧ были приготовлены с концентрацией 1000 ppm в н-гексане. Для каждого образца значения являются средними из трех измерений в течение 90 с.
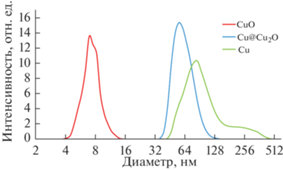
Согласно анализу ДРС (рис. 7), максимум распределения по размерам для НЧ меди приходится на 86 нм, для Cu@Cu2O – 56 нм, для CuO – 7 нм. Столь большое отличие для двух первых образцов связано с высокой склонностью НЧ к агломерации.
Полученные результаты по данным низкотемпературной адсорбции азота (при 77 К) представлены в табл. 1. Сферическая форма полученных НЧ (согласно ПЭМ) позволила оценить их средний размер по БЭТ
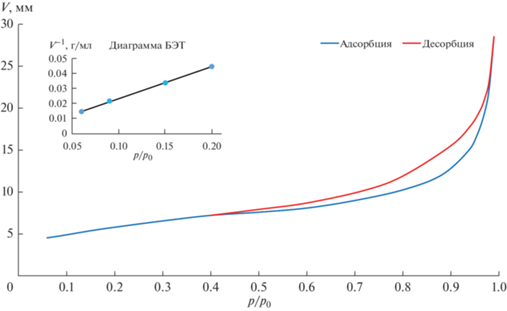
Полученные изотермы адсорбции–десорбции азота имели одинаковую форму для всех трех образцов. На рис. 8 представлена изотерма адсорбции–десорбции азота для НЧ меди. Согласно IUPAC, изотерма относится к типу IV, что характерно для мезопористой структуры. Кроме того, наблюдаемый гистерезис, связанный с капиллярной конденсацией, был отнесен к типу H3. Данный вид гистерезиса присущ твердым телам с щелевидными порами, обусловленными образованием агломератов.
ЗАКЛЮЧЕНИЕ
Методом ИПЛ получены наночастицы Cu, Cu@Cu2O и CuO. Результаты исследований показывают, что НЧ имеют размер меньше 40 нм и обладают кристаллической структурой.
Отсутствие рефлексов каких-либо примесных компонентов на рентгенограммах для всех трех образцов свидетельствует о возможности синтеза методом ИПЛ высокочистых НЧ, что обеспечивается бесконтактным способом нагрева образца, одностадийностью процесса и отсутствием дополнительно используемых реагентов в процессе получения НЧ.
Рассмотрена возможность получения НЧ с различной морфологией при помощи организации различной подачи кислорода в реактор. Снижение давления газа в установке обеспечивает резкое уменьшение среднего размера НЧ, синтезированных методом ИПЛ, вплоть до единиц нанометров. Все образцы были охарактеризованы комплексом физико-химических методов.
Показано, что ИПЛ является экологически чистым способом получения НЧ и может использоваться для синтеза НЧ с контролируемой морфологией в непрерывном режиме с высокой производительностью.
Список литературы
Feynman R. Nanomaterials // Nanomaterials. 2009. P. 1–20.
Taylor R., Coulombe S., Otanicar T., Phelan P., Gunawan A., Lv W., Rosengarten G., Prasher R., Tyagi H. Small Particles, Big Impacts: A Review of the Diverse Applications of Nanofluids // J. Appl. Phys. 2013. V. 113. № 1. P. 011301.
Astruc D. Introduction: Nanoparticles in Catalysis // Chem. Rev. 2020. V. 120. № 2. P. 461–463.
Malekzad H., Sahandi Zangabad P., Mirshekari H., Karimi M., Hamblin M. Noble Metal Nanoparticles in Biosensors: Recent Studies and Applications // Nanotechnol. Rev. 2017. V. 6. № 3. P. 301–329.
Liu S., Fu S., Zhang X., Wang X., Kang L., Han X., Chen X., Wu J., Liu Y. UV-Resistant Holographic Data Storage in Noble-Metal/Semiconductor Nanocomposite Films with Electron-Acceptors // Opt. Mater. Express. 2018. V. 8. № 5. P. 1143–1153.
Taylor R., Phelan P., Otanicar T., Adrian R., Prasher R. Nanofluid Optical Property Characterization: Towards Efficient Direct Absorption Solar Collectors // Nanoscale Res. Lett. 2011. V. 6. № 1. P. 1–11.
Abass S.M., Sunitha S., Ashaq S.M., Khadheer P.S., Choi D. An Overview of Antimicrobial and Anticancer Potential of Silver Nanoparticles // J. King Saud Univ. – Sci. 2022. V. 34. № 2. P. 101791.
Ullah K.A., Chen L., Ge G. Recent Development for Biomedical Applications of Magnetic Nanoparticles // Inorg. Chem. Commun. 2021. V. 134. P. 108995.
Shahbazali E., Hessel V., Noël T., Wang Q. Metallic Nanoparticles Made in Flow and their Catalytic Applications in Organic Synthesis // Nanotechnol. Rev. 2014. V. 3. № 1. P. 65–86.
Ojha N., Zyryanov G., Majee A., Charushin V., Chupakhin O., Santra S. Copper Nanoparticles as Inexpensive and Efficient Catalyst: A Valuable Contribution in Organic Synthesis // Coord. Chem. Rev. 2017. V. 353. P. 1–57.
Fathima J., Pugazhendhi A., Oves M., Venis R. Synthesis of Eco-Friendly Copper Nanoparticles for Augmentation of Catalytic Degradation of Organic Dyes // J. Mol. Liq. 2018. V. 260. P. 1–8.
Kang J., Kim H., Ryu J., Thomas H. H., Jang S., Joung J. Inkjet Printed Electronics Using Copper Nanoparticle Ink // J. Mater. Sci. Mater. Electron. 2010. V. 21. № 11. P. 1213–1220.
Kubota S., Morioka T., Takesue M., Hayashi H., Watanabe M., Smith R. Continuous Supercritical Hydrothermal Synthesis of Dispersible Zero-Valent Copper Nanoparticles for Ink Applications in Printed Electronics // J. Supercrit. Fluids. 2014. V. 86. P. 33–40.
Kruk T., Szczepanowicz K., Stefańska J., Socha R., Warszyński P. Synthesis and Antimicrobial Activity of Monodisperse Copper Nanoparticles // Colloids Surf. B. 2015. V. 128. P. 17–22.
Rajeshkumar S., Menon S., Venkat K.S., Tambuwala M., Bakshi H., Mehta M., Satija S., Gupta G., Chellappan D., Thangavelu L., Dua K. Antibacterial and Antioxidant Potential of Biosynthesized Copper Nanoparticles Mediated Through Cissus Arnotiana Plant Extract // J. Photochem. Photobiol., B. 2019. V. 197. P. 111531.
Calabrese C., La P.V., Testa M., Liotta L. Antifouling and Antimicrobial Activity of Ag, Cu and Fe Nanoparticles Supported on Silica and Titania // Inorg. Chim. Acta. 2022. V. 529. P. 120636.
Yabuki A., Tanaka S. Oxidation Behavior of Copper Nanoparticles at Low Temperature // Mater. Res. Bull. 2011. V. 46. № 12. P. 2323–2327.
Kim I., Kim Y., Woo K., Ryu E., Yon K., Cao G., Moon J. Synthesis of Oxidation-Resistant Core–Shell Copper Nanoparticles // RSC Adv. 2013. V. 3. № 35. P. 15169–15177.
Wang H., Cheng S., Cai X., Cheng L., Zhou R., Hou T., Li Y. Photocatalytic CO2 Reduction to HCOOH over Core-shell Cu@Cu2O Catalysts // Catal. Commun. 2022. V. 162. P. 106372.
Kalidindi S.B., Sanyal U., Jagirdar B.R. Nanostructured Cu and Cu@Cu2O Core Shell Catalysts for Hydrogen Generation from Ammonia–borane // Phys. Chem. Chem. Phys. 2008. V. 10. № 38. P. 5870–5874.
Mayyas A., Wei M., Levis G. Hydrogen as a Long-Term, Large-Scale Energy Storage Solution when Coupled with Renewable Energy Sources or Grids with Dynamic Electricity Pricing Schemes // Int. J. Hydrogen Energy. 2020. V. 45. № 33. P. 16311–16325.
Sadrolhosseini A., Noor A., Shameli K., Mamdoohi G., Moksin M., Adzir M.M. Laser Ablation Synthesis and Optical Properties of Copper Nanoparticles // J. Mater. Res. 2013. V. 28. № 18. P. 2629–2636.
Khayati G., Nourafkan E., Karimi G., Moradgholi J. Synthesis of Cuprous Oxide Nanoparticles by Mechanochemical Oxidation of Copper in High Planetary Energy Ball Mill // Adv. Powder Technol. 2013. V. 24. № 1. P. 301–305.
Richter K., Birkner A., Mudring A. Stabilizer-Free Metal Nanoparticles and Metal–Metal Oxide Nanocomposites with Long-Term Stability Prepared by Physical Vapor Deposition into Ionic Liquids // Angew. Chem. Int. Ed. 2010. V. 49. № 13. P. 2431–2435.
Jia F., Zhang L., Shang X., Yang Y. Non-Aqueous Sol–Gel Approach towards the Controllable Synthesis of Nickel Nanospheres, Nanowires, and Nanoflowers // Adv. Mater. 2008. V. 20. № 5. P. 1050–1054.
Zhang Q., Yang Z., Ding B., Lan X., Guo Y. Preparation of Copper Nanoparticles by Chemical Reduction Method Using Potassium Borohydride // Trans. Nonferrous Met. Soc. China. 2010. V. 20. suppl. 1. P. s240–s244.
Vijay K.R., Elgamiel R., Diamant Y., Gedanken A., Norwig J. Sonochemical Preparation and Characterization of Nanocrystalline Copper Oxide Embedded in Poly(Vinyl Alcohol) and Its Effect on Crystal Growth of Copper Oxide // Langmuir. 2001. V. 17. № 5. P. 1406–1410.
Huang L., Jiang H., Zhang J., Zhang Z., Zhang P. Synthesis of Copper Nanoparticles Containing Diamond-Like Carbon Films by Electrochemical Method // Electrochem. Commun. 2006. V. 8. № 2. P. 262–266.
Markov A.N., Vorotyntsev A.V., Andronova A.A. Direct Synthesis of Titanium Nanoparticles by Induction Flow Levitation Technique // Key Eng. Mater. 2021. V. 887. P. 178–183.
Kuskov M., Zhigach A., Leipunsky I., Afanasenkova E., Safronova O., Berezkina N., Vorobjeva G. Synthesis of Nanopowders of Titanium Compounds via Flow-Levitation Method and Study their Properties // IOP Conf. Ser. Mater. Sci. Eng. 2019. V. 558. № 1. P. 012023.
Дополнительные материалы отсутствуют.
Инструменты
Неорганические материалы