Журнал неорганической химии, 2019, T. 64, № 9, стр. 901-908
Синтез, структура и термические свойства сложных оксидов LnGa0.5Sb1.5O6 СО структурой типа розиаита
А. В. Егорышева 1, *, С. В. Голодухина 1, А. В. Тюрин 1, А. В. Хорошилов 1, В. О. Веселова 1, Р. Д. Светогоров 2
1 Институт общей и неорганической химии им. Н.С. Курнакова РАН
119991 Москва, Ленинский пр-т, 31, Россия
2 Национальный исследовательский центр “Курчатовский институт”
123182 Москва, пл. Академика Курчатова, 1, Россия
* E-mail: anna_egorysheva@rambler.ru
Поступила в редакцию 17.03.2019
После доработки 20.03.2019
Принята к публикации 15.04.2019
Аннотация
Методом соосаждения с последующим отжигом синтезирован ряд сложных оксидов LnIII${\text{Ga}}_{{0.{\text{5}}}}^{{{\text{III}}}}$${\text{Sb}}_{{{\text{1}}.{\text{5}}}}^{{\text{V}}}$O6 (Ln = La–Tb). Фазы с Ln = Ce, Pr, Eu и Tb получены впервые. Построено изотермическое сечение фазовой диаграммы системы Ce2Ox–Ga2O3–Sb2Oy при 900°С. Методом Ритвельда рассчитаны структуры и показано, что все соединения LnGa0.5Sb1.5O6 (Ln = La–Tb) относятся к структурному типу розиаита PbSb2O6. На примере LaGa0.5Sb1.5O6 определена изобарная теплоемкость и рассчитаны термодинамические функции (энтропия, инкремент энтальпии и приведенная энергия Гиббса) в интервале температур от 15 до 1300 K.
ВВЕДЕНИЕ
Сложные оксиды редкоземельных элементов (РЗЭ) относятся к крайне востребованным материалам, широко используемым в различных областях науки и техники. Прежде всего интерес представляют их люминесцентные и генерационные свойства [1, 2], а также магнитные [3, 4] и каталитические [5, 6]. Цирконаты и гафнаты лантаноидов со структурой пирохлора благодаря низкой теплопроводности и высокой химической и фазовой стабильности при высоких температурах, зарекомендовали себя как перспективные термобарьерные покрытия [7, 8]. На основе танталатов и ниобатов РЗЭ создаются протонные проводники для керамических топливных ячеек PCFC [9]. Легированные РЗЭ диоксид циркония и ортофосфаты используются в качестве инертной матрицы для смешанного оксидного ядерного топлива [10]. Систематическое изучение свойств новых сложных оксидов РЗЭ позволит создать более совершенные материалы на их основе.
В конце 60-х гг. при изучении гетеровалентного замещения в структурном типе PbSb2O6 (розиаита) было установлено, что в данном структурном типе кристаллизуются сложные оксиды РЗЭ, состав которых варьируется в достаточно широких пределах [11–14]. Были синтезированы теллураты и антимонаты РЗЭ с общими формулами: LnMIIITeO6 (Ln – лантаноиды, включая Y, MIII = = Al, Ga, Cr, Fe, Rh), LaMIIITeO6 (MIII = Fe, Rh), ${\text{LaM}}_{{{1 \mathord{\left/ {\vphantom {1 3}} \right. \kern-0em} 3}}}^{{{\text{II}}}}$Sb5/3O6 (MII = Mg, Co, Ni, Cu), ${\text{LaM}}_{{0.{\text{5}}}}^{{{\text{III}}}}$Sbl.5O6 (MIII = Al, Cr, Ga, Fe, Rh, In) и LnMIVSbO6 (Ln – лантаноиды, MIV = Ge, Sn, Ti). Однако изучение этих соединений ограничилось расчетом параметров кристаллической решетки и регистрацией оптических спектров поглощения.
К настоящему времени наиболее полно исследованы соединения LnCrTeO6 и LaFeTeO6 [15–20]. Изучены их структура и магнитные свойства, определена энергия образования, рассчитаны коэффициенты термического расширения. Первые попытки использования соединений этого класса показали их полифункциональность. На основе LnCrTeO6 (Ln = La, Nd, Gd, Dy, Er, Tm, Yb) получена новая серия “зеленых” пигментов с высокими рабочими параметрами [20]. Соединения L-nFe0.5${\text{Sb}}_{{{\text{1}}.{\text{5}}}}^{{\text{V}}}$O6, где Ln = La–Sm, показали себя как эффективные катализаторы в реакции окисления СО [21]. Кроме того, на примере модельной реакции разложения кристаллического фиолетового установлено [22], что LaFe0.5Sb1.5O6 обладает фотокаталитической активностью.
Ранее [23] нами было показано, что соединения La1 – xPrxGa0.5Sb1.5O6 являются перспективными люминофорами видимого света. Однако для успешного использования материала недостаточно знаний об их функциональных свойствах. Немаловажное значение имеет наличие сведений о стабильности этих соединений, возможных фазовых превращениях и температурных зависимостях термодинамических функций. В настоящей работе приведены результаты исследования по установлению границ существования ряда изоструктурных оксидов LnIII${\text{Ga}}_{{0.{\text{5}}}}^{{{\text{III}}}}$${\text{Sb}}_{{{\text{1}}.{\text{5}}}}^{{\text{V}}}$O6, разработке методики синтеза новых соединений, а также изучению их структуры и термодинамических характеристик.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
В качестве исходных реагентов использовали Ln(NO3)3 · xH2O (Ln = La, Ce, Pr, Nd, Sm, Eu, Gd, x = 5, 6 в зависимости от РЗЭ), TbCl3 · 6H2O, GaCl3 и Sb2O3. С учетом летучести сурьмы навеску Sb2O3 брали с 20%-ным избытком. Синтез LnGa0.5Sb1.5O6 проводили методом соосаждения с последующим отжигом, что позволило снизить температуру синтеза по сравнению с твердофазным методом. Смесь твердых компонентов растворяли в концентрированной соляной кислоте (37% HCl), затем добавляли раствор GaCl3 и H2O. В результате обратного соосаждения в NH4OH выпадал осадок, содержащий нерастворимые формы лантана, сурьмы и галлия. После отделения осадка, его промывали и высушивали при 50°С. Отжиг осуществляли в платиновых тиглях в печах резистивного нагрева на воздухе. Для снижения потери оксида сурьмы синтез проводили ступенчатым отжигом при температурах 650 (24 ч), 900 (24 ч) и 1180°C (в течение 5 сут). Степень прохождения реакции определяли методом рентгенофазового анализа (РФА) и с помощью весового контроля из расчета полного удаления избытка оксида сурьмы. Равновесие считали установившимся, если рентгенограммы после двух последующих отжигов не различались. Элементный состав образцов был подтвержден методом EDX.
РФА проводили на дифрактометре Bruker D8 Advance (CuKα-излучение, Ni-фильтр, детектор LYNXEYE) при комнатной температуре. Данные дифракции были собраны в диапазоне углов 2θ от 10° до 55° с шагом 0.01°, время накопления 0.3 с/шаг. Идентификацию известных фаз проводили с помощью базы данных JCPDS Research Associateship. Структура LnGa0.5Sb1.5O6 уточнена методом Ритвельда на основе данных рентгеновской дифракции синхротронного излучения с использованием программного обеспечения Jana2006 в предположении пр. гр. P$\overline 3 $1m [24]. Измерения выполнены на экспериментальной станции РСА УНУ “Курчатовский источник синхротронного излучения”, оснащенной 2D‑детектором Rayonix SX165, при длине волны λ = 0.78465 Å в диапазоне углов 2θ 2°–56°. В качестве углового стандарта использовали поликристаллический LaB6 (NIST SRM 660a).
Теплоемкость LaGa0.5Sb1.5O6 в интервале температур 13.88–351.24 K измеряли с помощью калориметрической низкотемпературной адиабатической установки БКТ-3, сконструированной и изготовленной в АОЗТ “Термис” (г. Менделеево Московской обл.). Образец массой 0.66497 г загружали в тонкостенный титановый цилиндрический контейнер с внутренним объемом 1 см3. Герметизацию контейнера осуществляли в атмосфере гелия при давлении ∼0.3 бар. Температуру калориметра измеряли железо-родиевым термометром сопротивления. Конструкция установки и методика измерений подробно описаны в [25, 26].
Измерения теплоемкости LaGa0.5Sb1.5O6 в интервале температур 305–1305 K проводили на установке синхронного термического анализа Netzsch STA 449 F1 Jupiter для образца массой 18.85 мг в атмосфере газообразного аргона 5.5 (99.9995 об. %) в платиновых тиглях с крышкой, имеющей небольшое отверстие. Общий расход газа в процессе эксперимента составлял 50 мл/мин, образец нагревали со скоростью 20 град/мин. В качестве файла коррекции использовали данные для пустого тигля, полученные в идентичных условиях. Обработку значений проводили с помощью программного обеспечения Netzsch Ploteus.
Для расчета стандартных термодинамических функций в широком интервале температур проводили анализ и обработку экспериментальных данных по низкотемпературной теплоемкости путем экстраполяции теплоемкости к 0 K, а также сглаживание экспериментальных данных с учетом особенностей зависимости Сp(Т). Задача выполнена с использованием сплайн-аппроксимации по программе, являющейся частью математического обеспечения банка данных ИВТАНТЕРМО [27]. Молекулярная масса, использованная для расчетов, определена с помощью атомных масс [28] и составила 452.40337 г/моль.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
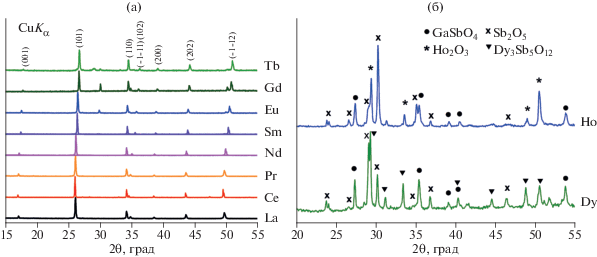
Изучено влияние условий соосаждения на фазовый состав продукта реакции. Установлено, что рН раствора является основным фактором, определяющим однофазность образцов. Образцы L-аGa0.5Sb1.5O6 без примеси были получены при значениях рН над осадком (после добавления аммиака) ≥9.57 (рис. 1). Уменьшение рН на 0.3–0.4 единицы, обусловленное добавлением меньшего количества раствора аммиака, приводит к появлению примесей в получаемом продукте. Данные условия синтеза были распространены на весь ряд синтезированных нами составов LnGa0.5Sb1.5O6, где Ln = Ce–Ho.
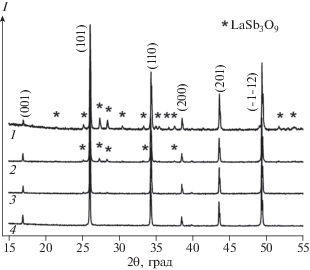
Рис. 1.
Дифрактограммы образцов состава L-aGa0.5Sb1.5O6, полученных методом соосаждения при различных значениях рН раствора над осадком после добавления аммиака: 8.24 (1), 9.28 (2), 9.57 (3), 9.94 (4).
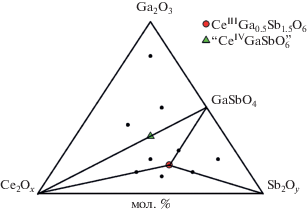
Известно, что в большинстве оксидных соединений церий присутствует в степени окисления +4, Ce3+ встречается значительно реже. Поэтому для определения состава (CeIVFeSbO6 или CeIIIFe0.5Sb1.5O6), реализующегося в структурном типе PbSb2O6, нами было построено изотермическое сечение фазовой диаграммы системы Ce2Ox–Ga2O3–Sb2Oy при 900°С. Составы исследованных образцов, необходимых для построения сечения фазовой диаграммы, были выбраны в соответствии с методом перекрещивающихся разрезов.
Установлено, что в данной системе при синтезе на воздухе реализуется только одно соединение – двойной оксид GaSbO4 в граничной системе Ga2O3–Sb2Oy. Других бинарных соединений в граничных системах Ce2Ox–Ga2O3 и Ce2Ox–Sb2Oy не обнаружено, что согласуется с данными [29, 30]. Единственный тройной оксид CeGa0.5Sb1.5O6, образующийся в этой системе, соответствует трехвалентному церию (рис. 2). Изотермическое сечение системы может быть представлено в виде четырех треугольников сосуществующих фаз: CeO2–Ga2O3–GaSbO4, CeGa0.5Sb1.5O6–GaSbO4–Sb2O5, CeGa0.5Sb1.5O6–CeO2–GaSbO4 и CeGa0.5Sb1.5O6–CeO2–Sb2O5. Изображенное на рис. 2 изотермическое сечение представляет проекцию более сложной системы Ce2O3–Ce2O4–Ga2O3–Sb2O3–Sb2O5. Действительно, в двух треугольниках сосуществующих фаз – CeGa0.5Sb1.5O6–CeO2–GaSbO4 и CeGa0.5Sb1.5O6–CeO2–Sb2O5 – в термодинамическом равновесии находятся фазы, в которых церий существует в различных степенях окисления, а в треугольнике CeGa0.5Sb1.5O6–GaSbO4–Sb2O5 в равновесии существуют фазы с Sb3+ и Sb5+. Температуры плавления и составы тройных эвтектик в системе мы не определяли.
Дальнейшее исследование показало, что в структурном типе розиаита реализуются соединения LnGa0.5Sb1.5O6 в ряду с La по Tb (рис. 3а). Получить аналогичные соединения с диспрозием и гольмием не удалось (рис. 3а). Необходимо отметить, что ранее [14] для ряда LnGa0.5Sb1.5O6 было установлено существование фаз со структурой антимоната свинца для Ln = La, Nd, Sm и Gd. Мы существенно расширили этот ряд. Впервые были получены тройные оксиды с Ln = Ce, Pr, Eu и Tb.
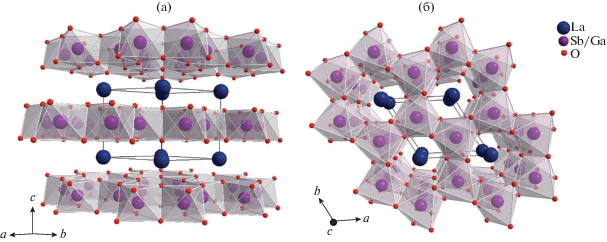
Методом Ритвельда для модели пр. гр. P$\overline 3 $1m были решены структуры всех впервые синтезированных соединений (табл. 1, рис. 4). L-nGa0.5Sb1.5O6 имеет слоистую структуру. Двумерные слои расположены в плоскости ab. Они образованы из шестичленных колец сшитых по ребру октаэдров (Ga/Sb)O6. В направлении оси c представляют собой гексагонально-призматические туннели (рис. 5). Катионы Ln3+ находятся между слоями, заполняя пространство туннелей. В [21] нами было выдвинуто предположение, что подобное расположение ионов приводит к электростатической стабилизации соединений в ряду LnFe0.5Sb1.5O6. Кислород, находящийся в позиции с низкой локальной симметрией, координирован, с одной стороны, ионами лантаноида, находящимися в межслоевом пространстве, а с другой – ионами сурьмы и железа, лежащими в плоскости слоя. Катион Sb5+ имеет большую поверхностную плотность заряда, и в соответствии с правилами Фаянса его поляризующая способность выше, поэтому внешняя электронная оболочка кислорода сдвинута к катионам сурьмы. Вследствие этого в структуре возникает анионная поляризация, в позициях аниона образуются индуцированные диполи, ориентированные перпендикулярно к плоскости слоя. При увеличении порядкового номера РЗЭ радиус иона Ln3+ уменьшается, а значит, увеличивается поверхностная плотность заряда Ln3+. Это, в свою очередь, приводит к уменьшению поляризации аниона кислорода. Количественно поляризующая способность катиона описывается ионным потенциалом Ф = = Z +/R, где Z+ – заряд катиона, R – его ионный радиус [31]. Следовательно, при увеличении порядкового номера РЗЭ разность ионных потенциалов Ф между катионами в октаэдрах и в межслоевом пространстве уменьшается и слоистая структура становится неустойчивой из-за снижения электростатической стабилизации.
Таблица 1.
Результаты уточнения структур соединений LnGa0.5Sb1.5O6 по методу Ритвельда для модели пр. гр. P$\overline 3 $1m
| Параметр | LaGaSbO | CeGaSbO | PrGaSbO | NdGaSbO | SmGaSbO | EuGaSbO | GdGaSbO | TbGaSbO | |
|---|---|---|---|---|---|---|---|---|---|
| a, Å | 5.22754(2) | 5.21872(6) | 5.21411(3) | 5.20986(3) | 5.20029(4) | 5.19539(3) | 5.19167(5) | 5.18372(9) | |
| c, Å | 5.21666(4) | 5.16491(8) | 5.12538(4) | 5.08930(3) | 5.02751(5) | 4.99464(5) | 4.96763(7) | 4.93828(11) | |
| V, Å3 | 123.4577(11) | 121.821(3) | 120.6749(15) | 119.6303(11) | 117.7443(18) | 116.7539(15) | 115.956(2) | 114.918(4) | |
| Заселенность Ga | 0.233(4) | 0.249(10) | 0.225(7) | 0.233(5) | 0.208(8) | 0.223(6) | 0.232(9) | 0.205(15) | |
| Заселенность Sb | 0.767(4) | 0.751(10) | 0.775(7) | 0.767(5) | 0.792(8) | 0.777(6) | 0.768(9) | 0.795(15) | |
| ОКР, нм | 601 | 618 | 362 | 298 | 147 | 224 | 214 | 88 | |
| Микродеформация, % | 0.19 | 0.10 | 0.12 | 0.14 | 0.16 | 0.21 | 0.22 | 0.15 | |
| Ln, U | U11 | 0.0151(2) | 0.0149(4) | 0.0160(3) | 0.0145(2) | 0.0115(4) | 0.0115(3) | 0.0088(4) | 0.0100(7) |
| U22 | 0.0151(2) | 0.0149(4) | 0.0160(3) | 0.0145(2) | 0.0115(4) | 0.0115(3) | 0.0088(4) | 0.0100(7) | |
| U33 | 0.0055(4) | 0.0048(7) | 0.0063(5) | 0.0076(4) | 0.0073(6) | 0.0065(4) | 0.0038(6) | 0.0094(11) | |
| U12 | 0.00755(11) | 0.0074(2) | 0.00802(15) | 0.00724(12) | 0.0058(2) | 0.00575(13) | 0.0044(2) | 0.0050(4) | |
| U13 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | |
| U23 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | |
| Sb, U | U11 | 0.0050(2) | 0.0053(4) | 0.0065(3) | 0.0049(2) | 0.0033(4) | 0.0037(3) | 0.0020(4) | 0.0089(8) |
| U22 | 0.0050(2) | 0.0053(4) | 0.0065(3) | 0.0049(2) | 0.0033(4) | 0.0037(3) | 0.0020(4) | 0.0089(8) | |
| U33 | 0.0069(4) | 0.0083(7) | 0.0054(5) | 0.0071(4) | 0.0050(7) | 0.0044(5) | 0.0016(7) | 0.0086(13) | |
| U12 | 0.00251(10) | 0.0026(2) | 0.00323(14) | 0.00244(11) | 0.0016(2) | 0.00187(14) | 0.0010(2) | 0.0044(4) | |
| U13 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | |
| U23 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | |
| O, Uизо | 0.0049(6) | 0.0047(12) | 0.0083(9) | 0.0054(6) | 0.0084(10) | 0.0046(7) | 0.0036(11) | 0.0007(18) | |
| O, x | 0.3734(5) | 0.3713(11) | 0.3679(9) | 0.3682(6) | 0.3648(10) | 0.3642(7) | 0.3654(11) | 0.3696(18) | |
| O, z | 0.2850(4) | 0.2865(9) | 0.2823(7) | 0.2826(5) | 0.2777(9) | 0.2776(6) | 0.2758(10) | 0.2638(17) | |
| Rp | 1.96 | 4.32 | 3.13 | 2.70 | 3.41 | 2.90 | 3.96 | 5.76 | |
| wRp | 2.74 | 6.69 | 4.86 | 3.60 | 5.15 | 3.93 | 6.00 | 8.17 | |
| R(obs) | 1.48 | 1.65 | 2.66 | 1.18 | 1.74 | 1.33 | 1.74 | 3.04 | |
| wR(obs) | 2.69 | 2.33 | 5.61 | 3.30 | 2.57 | 2.44 | 2.59 | 4.49 | |
| R(all) | 1.55 | 2.18 | 2.87 | 1.24 | 1.74 | 1.33 | 2.74 | 3.04 | |
| wR(all) | 2.72 | 2.35 | 5.68 | 3.37 | 2.57 | 2.44 | 2.59 | 4.49 | |
| GOOF | 0.94 | 2.28 | 1.55 | 1.19 | 2.00 | 1.45 | 2.20 | 2.81 | |
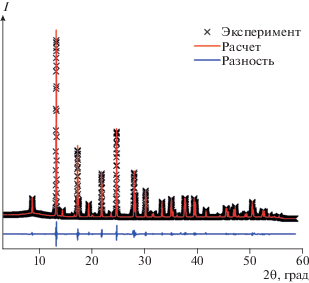
Рис. 5.
Экспериментальная и расчетная дифрактограммы синтезированного CeGa0.5Sb1.5O6. Внизу приведена разностная кривая.
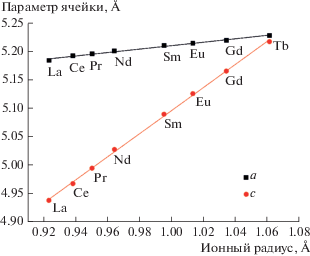
В ряду соединений LnGa0.5Sb1.5O6, где Ln = = La–Tb, параметры кристаллической решетки монотонно уменьшаются с уменьшением ионного радиуса иона РЗЭ (рис. 6). Параметр а определяется геометрией шестичленных колец, образованных октаэдрами (Ga/Sb)O6. Поэтому его изменение незначительно (лишь 0.04 Å). В то же время параметр с, определяющий расстояние между слоями, напрямую зависит от размеров иона лантаноида, и уменьшение параметра с существенно больше (0.28 Å). При этом радиус катиона РЗЭ изменяется от лантана к тербию на 0.14 Å. Таким образом, с уменьшением радиуса иона лантаноида слои октаэдров сближаются, что может быть следствием уменьшения анионной поляризации. Можно предположить, что именно уменьшение вклада электростатических взаимодействий в энергию кристаллической решетки является причиной того, что соединения лантаноидов с меньшими радиусами – DyGa0.5Sb1.5O6 и HoGa0.5Sb1.5O6 – не реализуются в структурном типе розиаита. В силу низкой устойчивости розиаитов конца ряда (Ln = Eu, Gd и Tb) нам, по-видимому, не удалось получить однофазные образцы. Следует отметить, что, в отличие от железосодержащих аналогов LnFe0.5Sb1.5O6 (Ln = La–Sm) [21], в ряду LnGa0.5Sb1.5O6 присутствуют соединения с европием, гадолинием и тербием. Причиной этого может быть меньшая величина радиуса Ga3+ и, соответственно, большее значение ионного потенциала по сравнению с Fe3+.
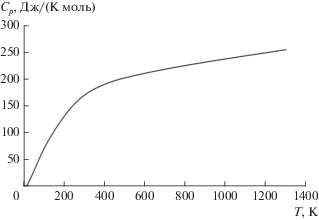
Измерение температурной зависимости теплоемкости и расчет термодинамических функций в диапазоне 15–1300 K проводили на примере LaGa0.5Sb1.5O6. Как видно на рис. 7, аномалий теплоемкости не зафиксировано. Для экстраполяции величины теплоемкости к T = 0 K использовали аддитивную схему на основании моделей Дебая и Эйнштейна. Сглаживание экспериментальных данных по низкотемпературной теплоемкости проводили методом аппроксимирующего сплайна. В табл. 2 приведены значения термодинамических функций LaGa0.5Sb1.5O6. Погрешность термодинамических функций рассчитывали из среднеквадратичного отклонения экспериментальных точек от сглаженной кривой и погрешности экстраполяции к 0 K [27]. Она составляла не более ±10% до 20 K, ±2% от 20 до 50 K, 0.5% в интервале 50−350 K и увеличивалась до 3% при T > 350 K.
Таблица 2.
Температурные зависимости термодинамических функций для LaGa0.5Sb1.5O6
| T, K | $C_{p}^{0},$ Дж/(K моль) | S0, Дж/(K моль) | Ф0(T), Дж/(K моль) | H0(T) – H0(0), Дж/моль |
|---|---|---|---|---|
| 15 | 3.344 | 1.101 | 0.2746 | 12.39 |
| 20 | 6.752 | 2.524 | 0.6472 | 37.54 |
| 25 | 10.35 | 4.415 | 1.205 | 80.23 |
| 30 | 14.13 | 6.634 | 1.921 | 141.4 |
| 35 | 18.05 | 9.104 | 2.768 | 221.8 |
| 40 | 22.09 | 11.78 | 3.725 | 322.1 |
| 45 | 26.24 | 14.62 | 4.776 | 442.9 |
| 50 | 30.45 | 17.60 | 5.909 | 584.6 |
| 60 | 39.02 | 23.91 | 8.377 | 931.8 |
| 70 | 47.60 | 30.57 | 11.07 | 1365 |
| 80 | 56.01 | 37.48 | 13.94 | 1883 |
| 90 | 64.05 | 44.54 | 16.94 | 2484 |
| 100 | 71.62 | 51.69 | 20.06 | 3163 |
| 110 | 78.78 | 58.85 | 23.26 | 3915 |
| 120 | 85.56 | 66.00 | 26.52 | 4737 |
| 130 | 92.02 | 73.10 | 29.83 | 5625 |
| 140 | 98.20 | 80.15 | 33.18 | 6576 |
| 150 | 104.1 | 87.13 | 36.54 | 7588 |
| 160 | 109.9 | 94.04 | 39.92 | 8659 |
| 170 | 115.5 | 100.9 | 43.30 | 9786 |
| 180 | 121.0 | 107.6 | 46.69 | 10 970 |
| 190 | 126.3 | 114.3 | 50.07 | 12 210 |
| 200 | 131.5 | 120.9 | 53.45 | 13 500 |
| 210 | 136.4 | 127.5 | 56.82 | 14 840 |
| 220 | 141.2 | 133.9 | 60.18 | 16 220 |
| 230 | 145.7 | 140.3 | 63.52 | 17 660 |
| 240 | 150.0 | 146.6 | 66.85 | 19 140 |
| 250 | 154.0 | 152.8 | 70.17 | 20 660 |
| 260 | 157.8 | 158.9 | 73.46 | 22 220 |
| 270 | 161.3 | 164.9 | 76.74 | 23 810 |
| 280 | 164.6 | 170.9 | 80.00 | 25 440 |
| 290 | 167.7 | 176.7 | 83.23 | 27 100 |
| 298.15 | 170.0 | 181.4 | 85.85 | 28 480 |
| 300 | 170.5 | 182.4 | 86.44 | 28 790 |
| 310 | 173.2 | 188.1 | 89.63 | 30 510 |
| 320 | 175.6 | 193.6 | 92.79 | 32 260 |
| 330 | 178.0 | 199.0 | 95.93 | 34 030 |
| 340 | 180.1 | 204.4 | 99.04 | 35 820 |
| 350 | 182.2 | 209.6 | 102.1 | 37 630 |
| 400 | 190.8 | 234.5 | 117.1 | 46 960 |
| 450 | 197.4 | 257.4 | 131.5 | 56 670 |
| 500 | 202.7 | 278.5 | 145.1 | 66 680 |
| 550 | 207.1 | 298.0 | 158.2 | 76 930 |
| 600 | 211.2 | 316.2 | 170.6 | 87 390 |
| 650 | 215.1 | 333.3 | 182.5 | 98 050 |
| 700 | 218.8 | 349.4 | 193.8 | 108 900 |
| 750 | 222.2 | 364.6 | 204.7 | 119 900 |
| 800 | 225.6 | 379.0 | 215.1 | 131 100 |
| 850 | 228.8 | 392.8 | 225.2 | 142 500 |
| 900 | 231.9 | 406.0 | 234.9 | 154 000 |
| 950 | 234.9 | 418.6 | 244.2 | 165 700 |
| 1000 | 237.8 | 430.7 | 253.2 | 177 500 |
| 1050 | 240.7 | 442.4 | 262.0 | 189 400 |
| 1100 | 243.5 | 453.6 | 270.4 | 201 500 |
| 1150 | 246.4 | 464.5 | 278.6 | 213 800 |
| 1200 | 249.2 | 475.1 | 286.6 | 226 200 |
| 1250 | 252.1 | 485.3 | 294.3 | 238 700 |
| 1300 | 255.0 | 495.3 | 301.9 | 251 400 |
ЗАКЛЮЧЕНИЕ
В результате проведенных исследований установлено, что существование соединений ряда L-nGa0.5Sb1.5O6 зависит от поляризующей способности катионов, которая определяет возможность электростатической стабилизации кристаллической решетки соединения. В ряду LnGa0.5Sb1.5O6 реализуются фазы с Ln = La–Tb. РЗЭ с меньшими радиусами соединения со структурой розиаита не образуют. Ранее [20] на примере твердых растворов La1– xPrxGa0.5Sb1.5O6 было показано, что они являются перспективными люминофорами видимого света. Существование широкого ряда изоструктурных LaGa0.5Sb1.5O6 соединений указывает на возможность синтеза на его основе твердых растворов с другими РЗЭ для получения новых люминесцентных материалов. Отсутствие переходов на температурной зависимости говорит о стабильности LaGa0.5Sb1.5O6 вплоть до 1300 K и способности работать в условиях высокой плотности лазерного возбуждения.
Список литературы
Handbook of solid-state lasers: materials, systems and applications. Oxford: Woodhead, 2013.
Mill B.V., Kazei Z.A., Tsymbarenko D.M. // Russ. J. Inorg. Chem. 2018. V. 63. № 10. P. 1283. https://doi.org/10.1134/S0036023618100133
Gardner J.S., Gingras M.J.P., Greedan J.E. // Rev. Mod. Phys. 2010. V. 82. № 1. P. 53. https://doi.org/10.1103/RevModPhys.82.53
Raju N.P., Dion M., Gingras M.J.P. et al. // Phys. Rev. B: Condens. Matter. 1999. V. 59. № 22. P. 14489. https://doi.org/10.1103/PhysRevB.59.14489
Royer S., Duprez D. // ChemCatChem. 2011. V. 3. № 1. P. 24. https://doi.org/10.1002/cctc.201000378
Krasnobaeva O.N., Belomestnykh I.P., Nosova T.A. et al. // Russ. J. Inorg. Chem. 2018. V. 63. № 11. P. 1419. https://doi.org/10.1134/S0036023618110098
Joulia A., Vardelle M., Rossignol S. // J. Eur. Ceram. Soc. 2013. V. 33 № 13–14. P. 2633. https://doi.org/10.1016/j.jeurceramsoc.2013.03.030
Simonenko N.P., Sakharov K.A., Simonenko E.P. et al. // Russ. J. Inorg. Chem. 2015. V. 60. № 12. P. 1452. https://doi.org/10.1134/S0036023615120232
Chesnaud A., Estradé S., Morata A. et al. // J. Eur. Ceram. Soc. 2015. V. 35. № 11. P. 3051. https://doi.org/10.1016/j.jeurceramsoc.2015.04.014
Ciacchi F.T., Crane K.M., Badwal S.P.S. // Solid State Ionics. 1994. V. 73. № 1–2. P. 49. https://doi.org/10.1016/0167-2738(94)90263-1
Blasse G. // J. Inorg. Nucl. Chem. 1966. V. 28. № 4. P. 1124. https://doi.org/10.1016/0022-1902(66)80216-6
Kasper H.M. // Mater. Res. Bull. 1969. V. 4. № 1. P. 33. https://doi.org/10.1016/0025-5408(69)90013-0
Kasper H.M. // Solid State Res. 1969. V. 3. № 23. P. 27.
Blasse G., De Pauw A.D.M. // J. Inorg. Nucl. Chem. 1970. V. 32. № 8. P. 2533. https://doi.org/10.1016/0022-1902(70)80298-6
Gupta N.K., Roy S.P., Joshi P.V. et al. // J. Alloys Compd. 2006. V. 417. № 1–2. P. 300. https://doi.org/10.1016/j.jallcom.2005.09.044
Phatak R., Krishnan K., Kulkarni N.K. et al. // Mater. Res. Bull. 2010. V. 45. № 12. P. 1978. https://doi.org/10.1016/j.materresbull.2010.08.002
Vats B.G., Phatak R., Krishnan K., Kannan S. // Mater. Res. Bull. 2013. V. 48. № 9. P. 3117. https://doi.org/10.1016/j.materresbull.2013.04.076
Lavat A.E., Mercader R.C., Baran E.J. // J. Alloys Compd. 2010. V. 508. № 1. P. 24. https://doi.org/10.1016/j.jallcom.2010.08.054
Narsinga Rao G., Sankar R., Panneer Muthuselvam I. et al. // J. Magn. Magn. Mater. 2014. V. 370. P. 13. https://doi.org/10.1016/j.jmmm.2014.06.057
Gayo G.X., Troncoso F., Lavat A.E. // Ceram. Int. 2016. V. 40. № 1. P. 611. https://doi.org/10.1016/j.ceramint.2013.06.042
Egorysheva A.V., Ellert O.G., Liberman E.Y. et al. // J. Alloys Compd. 2019. V. 777. P. 655. https://doi.org/10.1016/j.jallcom.2018.11.008
Egorysheva A.V., Ellert O.G., Gajtko O.M. et al. // Ceram. Int. 2016. V. 42. № 12. P. 13976. https://doi.org/10.1016/j.ceramint.2016.05.211
Egorysheva A.V., Gajtko O.M., Golodukhina S.V. et al. // Ceram. Int. 2019. https://doi.org/10.1016/j.ceramint.2019.05.233.
Petrícek V. // Z. Kristallogr. 2014. V. 229. № 5. P. 345. https://doi.org/10.1515/zkri-2014-1737
Varushchenko R.M., Druzhinina A.I., Sorkin E.L. // J. Chem. Thermodyn. 1997. V. 29. № 6. P. 623. https://doi.org/10.1006/jcht.1996.0173
Malyshev V.V., Mil’ner G.A., Sorkin E.L. et al. // Prib. Tekh. Eksp. 1985. № 6. P. 195.
Иориш В.С., Толмач П.И. // Журн. физ. химии. 1986. Т. 60. № 10. С. 2583.
Coursey J.S. // NIST Physical Measurement Laboratory [Электронный ресурс]. URL: https://www.nist. gov/pml/atomic-weights-and-isotopic-compositions-relative-atomic-masses.
Hewston T.A. // Inorg. Chem. 1983. V. 22. № 14. P. 1967. https://doi.org/10.1021/ic00156a006
Портной К.И., Тимофеева Н.И. Кислородные соединения редкоземельных элементов M.: Металлургия, 1986.
Fajans K. // Struct. Bond. Berlin, Heidelberg: Springer, 1967. P. 88. https://doi.org/10.1007/BFb0118879
Дополнительные материалы отсутствуют.
Инструменты
Журнал неорганической химии