Журнал неорганической химии, 2020, T. 65, № 10, стр. 1365-1370
In situ и ex situ исследование термолиза хромата тетраамминплатины(II)
В. И. Лагунова a, b, *, Е. Ю. Филатов a, П. Е. Плюснин a, С. В. Коренев a
a Институт неорганической химии им. А.В. Николаева СО РАН
630090 Новосибирск, пр-т Академика Лаврентьева, 3, Россия
b Новосибирский государственный университет
630090 Новосибирск, ул. Пирогова, 1, Россия
* E-mail: lagunovavarvara@gmail.com
Поступила в редакцию 18.03.2020
После доработки 04.05.2020
Принята к публикации 27.05.2020
Аннотация
Сравнительный анализ показал, что термолиз комплексной соли [Pt(NH3)4]CrO4 в атмосфере синтетического воздуха в условиях in situ и ex situ протекает по разным путям. При разложении в условиях эксперимента ex situ, в отличие от in situ, происходит формирование промежуточной фазы PtCrO2 со структурой делафоссита. Конечным продуктом разложения является гомогенная смесь металлической платины и оксида хрома(III). Показано, что комплексное соединение [Pt(NH3)4]CrO4 обладает отрицательным объемным коэффициентом теплового расширения в температурном диапазоне 30–200°С (–1.9 × 10–5 1/K). Эксперименты еx situ показали устойчивость комплексного соединения при последовательном циклическом нагревании до 200°С и охлаждении до комнатной температуры.
ВВЕДЕНИЕ
Комплексные соли, содержащие два металла, представляют интерес как предшественники для получения разнообразных наноразмерных металлических и металлоксидных материалов [1–3]. Процесс термического разложения комплексных соединений во многом зависит от атмосферы термолиза и скорости нагрева образца. Состав конечных продуктов разложения варьирует в зависимости от условий термодеструкции, а также от состава исходной комплексной соли [4–6]. Получаемые в результате разложения таких соединений металлические и металлоксидные наночастицы могут обладать уникальными физико-химическими свойствами, среди которых можно выделить электропроводящие свойства. Например, нестехиометрический делафоссит Cu0.66Cr1.33O2 имеет самые высокие значения электропроводности среди оксидов с полупроводниковой проводимостью p-типа [7], что позволяет применять его в солнечных батареях, сенсорных экранах и светодиодах [8].
Металлические наночастицы также могут обладать магнитными свойствами. Например, сплав Fe–Ni обладает высокой намагниченностью и магнитной проницаемостью [9], поэтому данное соединение применяется в качестве магнитного материала для создания различных объектов методом трафаретной печати. Получаемые этим методом объекты обладают высокой магнитной проницаемостью и могут использоваться в различных индукторах и трансформаторах.
Наноразмерные биметаллические соединения широко используются в качестве катализаторов в органической и неорганической химии для научных и промышленных приложений [10–12]. Одним из примеров применения в промышленности катализаторов на основе наносплавов является использование нанесенного на никелевую пену сплава Pd–Ni для удаления кислорода из метана в угольных пластах [13].
Катализаторы, получаемые термолизом комплексных солей, содержащих платину в качестве металлического центра, могут также использоваться в промышленно значимых реакциях. Так, в работе [14] подробно изучен процесс термического разложения комплексных солей [Pt(NH3)4]C2O4 и [Pt(NH3)4](OOCCH2COO) в атмосфере азота и в окислительной атмосфере для разработки метода альтернативного получения катализаторов на основе платины. В работе [15] при термическом разложении растворов [Pt(NH3)4]CrO4 и [Cr(NH3)5Cl][PtCl4] с металлическими подложками в автоклаве при температуре 190°С получены катализаторы для реакций окисления пропана и н-гексана, проявляющие более высокую активность по сравнению с чистым платиновым катализатором, приготовленным в тех же условиях. В работе [16] получены комплексные соли [M(NH3)4]A (M = Pd, Pt; A = = ${\text{C}}{{{\text{r}}}_{{\text{2}}}}{\text{O}}_{{\text{7}}}^{{{\text{2}}--}},$ CrO42–) и методом рентгеноструктурного анализа установлена структура [Pt(NH3)4]CrO4 (I41/amd, a = 7.3302(2), b = 7.3302(2), c = = 15.2399(5) Å). Исследовано термическое поведение солей в окислительной, восстановительной и инертной атмосфере. Гомогенная смесь металлической платины и оксида хрома(III), полученная в процессе термического разложения [Pt(NH3)4]CrO4 в атмосфере синтетического воздуха, показала высокую каталитическую активность в процессе полного окисления угарного газа (CO TOX).
В настоящей работе подробно изучен процесс термического разложения [Pt(NH3)4]CrO4 в синтетическом воздухе методом синхронного термического анализа с одновременной регистрацией выделяющихся газов методом рентгеновской дифракции in situ на станции синхротронных исследований и проведено сравнение с данными, полученными при помощи дифрактометрии ex situ, с целью установления механизма термодеструкции комплексной соли и условий формирования промежуточных фаз.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
РФА. Рентгенодифрактометрическое исследование образцов синтезированных соединений проводили на дифрактометре ДРОН-RM4 (CuKα-излучение, графитовый монохроматор, комнатная температура). Образцы готовили растиранием в агатовой ступке с добавлением гептана. Полученную суспензию наносили на полированную сторону стандартной кварцевой кюветы. После высыхания образец представлял собой тонкий ровный слой толщиной ~100 мкм. В качестве внешнего эталона использовали образец поликристаллического кремния (a = 5.4309 Å), приготовленный аналогичным образом. Регистрацию дифрактограмм проводили в пошаговом режиме (∆2θ = 0.1°) в диапазоне углов 2θ от 5° до 60° для комплексных солей и от 5° до 95° для продуктов термолиза.
Термическое разложение комплексной соли исследовали методом РФА в условиях in situ с использованием высокотемпературной камеры XRK-900 (Anton Paar, Austria), установленной на порошковом дифрактометре на линии прецизионной дифрактометрии в Сибирском центре синхротронного и терагерцевого излучения (СЦСТИ), и однокоординатного детектора OD-3M-350 [17]. Детектор имеет 3328 каналов, охватывающих диапазон углов 2θ, равный 30°. Длина волны синхротронного излучения λ = 1.740 Å. Рентгенограммы регистрировали в течение 60 с. Образцы комплексного соединения загружали в открытый держатель, пропускающий газ (воздух), а затем помещали его в камеру реактора.
Фазовый состав продуктов термолиза устанавливали путем анализа положений отдельных рефлексов в области углов 2θ от 60° до 95°, где ошибка измерения межплоскостного расстояния минимальна. Индицирование кристаллических фаз проводили по аналогии с рентгенограммами чистых веществ согласно картотеке PDF [18].
Уточнение параметров решетки осуществляли полнопрофильным методом по всему массиву отражений с использованием прикладных программ PowderCell 2.4 [19] и TOPAS-Academic V6 [20]. Размер областей когерентного рассеяния (ОКР) кристаллических фаз определяли посредством Фурье-анализа профилей одиночных дифракционных пиков и по формуле Шеррера (программа Winfit 1.2.1) [21].
Термический анализ. ТГА проводили на приборе TG 209 F1 Iris (Netzsch, Germany). Синхронный термический анализ TG-DSC/EGA-MS (термогравиметрия, дифференциальная сканирующая калориметрия и масс-спектрометрия с анализом выделяющихся газов) осуществляли на приборе, состоящем из термического анализатора STA 449 F1 Jupiter и квадрупольного масс-спектрометра QMS 403D Aeolos (Netzsch, Germany). Измерения проводили в тиглях из Al2O3 в интервале температур 30–1000°С при скорости нагрева 10 град/мин и скорости потока газа 60 мл/мин в атмосфере синтетического воздуха (80 об. % Ar, 20 об. % O2), масса образца 10–50 мг. Обработку экспериментальных результатов проводили при помощи стандартного программного обеспечения Proteus. Точность измерения массы составляла ±0.1 мг, температуры – ±1°С.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Дифракционное исследование в условиях in situ. Нагрев проводили в атмосфере синтетического воздуха со скоростью 10 град/мин. При повышении температуры от 30 до 200°С на дифрактограммах наблюдается разнонаправленное смещение рефлексов комплексной соли как в сторону бóльших, так и в сторону меньших углов без изменения интенсивности, что свидетельствует об анизотропном изменении параметров элементарной ячейки без разрушения кристаллической структуры (рис. 1).
Рис. 1.
Дифракционные картины [Pt(NH3)4]CrO4 при нагревании в атмосфере синтетического воздуха в условиях in situ.
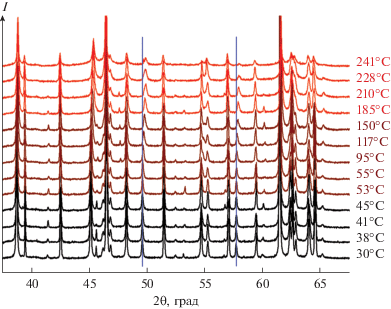
Расчет параметров и объема кристаллической ячейки в каждой температурной точке в интервале 30–200°С показал, что при нагревании параметр c уменьшается от 15.194(4) до 15.118(4) Å, а параметр a увеличивается от 7.312(2) до 7.320(2) Å. В целом наблюдается уменьшение объема элементарной ячейки, что свидетельствует об отрицательном коэффициенте теплового расширения. Проведенные нами расчеты дают для объемного коэффициента термического расширения значение –1.9 × 10–5 1/K. Следует отметить, что к настоящему времени известно не так много объектов, параметры элементарной ячейки которых уменьшаются при нагреве, причем для некоторых веществ данная особенность проявляется лишь при определенных температурах. Например, для ZrW2O8 коэффициент линейного теплового расширения составляет –8.8 × 10–6 1/K в температурном интервале 0.3–430 K [22], а для упорядоченного ZrMo1.8W0.2O8 это значение составляет –9.6 × 10–6 1/K (300–400 K) [23]. Для сплавов на основе титана (ALLVAR) коэффициент теплового расширения составляет –16 × 10–6 1/K при комнатной температуре [24].
Также были проведены исследования ex situ термической устойчивости комплексного соединения при проведении 10 циклов нагрева до температуры 200°С и охлаждения. Показана устойчивость соли [Pt(NH3)4]CrO4. На дифрактограммах всех образцов после каждого цикла нагрева и охлаждения не наблюдается каких-либо различий: интенсивность, ширина и положения рефлексов сохраняются.
Начиная с температуры 241°С в условиях in situ происходит постепенное уменьшение интенсивности рефлексов комплексной соли, что говорит о начале процесса термодеструкции (рис. 2). При температуре 241°С на дифрактограмме присутствуют малоинтенсивные уширенные пики исходного соединения, а уже при 254°С на дифрактограмме полностью исчезают рефлексы комплексной соли и наблюдается поднятие фона в области углов, соответствующих ГЦК-фазе металла.
Рис. 2.
Дифракционные картины продуктов термолиза [Pt(NH3)4]CrO4 в атмосфере синтетического воздуха при различных температурах в условиях in situ.
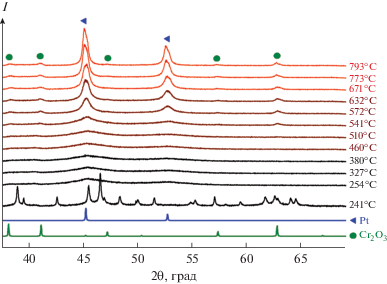
Дальнейший нагрев приводит к укрупнению частиц и увеличению интенсивности пиков. При температуре 541°С на дифрактограмме появляются дополнительные рефлексы, соответствующие фазе оксида хрома(III). Параметр ГЦК-фазы при этом составляет 3.934(8) Å, что с учетом термического расширения соответствует металлической платине [25]. Размер ОКР металлической фазы составляет 3 нм. При дальнейшем повышении температуры наблюдается смещение рефлексов от ГЦК-фазы в сторону меньших углов, это связано с эффектом термического расширения. Разложение заканчивается при температуре 790°С, конечный продукт представляет собой смесь оксида хрома(III) и металлической платины. Параметр ГЦК-фазы составляет 3.950(3) Å, ОКР – 11–15 нм.
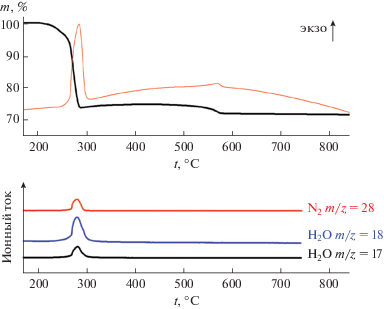
Дифракционное и термическое исследование в условиях ex situ. Основная ступень термического разложения [Pt(NH3)4]CrO4 в атмосфере синтетического воздуха является экзотермической, протекает в интервале температур 200–300°С, приводит к потере 26.5% массы и сопровождается выделением газообразного азота и воды (рис. 3). Выделение аммиака не зафиксировано. Это свидетельствует о протекании окислительно-восстановительной реакции, связанной с окислением аммиака до азота и восстановлением платины до металлического состояния, а хрома до степени окисления +3. При температуре 290°С остаточная масса составляет 73.7%, что соответствует брутто-составу PtCrO2 или 1/2Cr2O3 + 1/2(PtO + Pt). После основного газовыделения в температурном диапазоне 300–415°С происходит небольшой набор массы (~1%), связанный с постепенным окислением металлической платины до оксида, затем следует ступень потери массы до 71.9%. Такое поведение связано с низкой устойчивостью оксида платины PtO, который образуется при окислении металлической платины с развитой поверхностью кислородом при 415°С. При температуре 450°С начинается медленная потеря массы, а процесс разложения основной массы оксида платины до металлической платины с выделением кислорода происходит в интервале 550–580°С, и он также является экзотермическим. Дальнейший нагрев до 1000°С сопровождается монотонным падением массы, связанным с постепенным разложением оксида платины, находящегося в аморфном состоянии.
Рис. 3.
Кривые термического анализа [Pt(NH3)4]СrO4 в атмосфере синтетического воздуха (скорость нагревания 10 град/мин).
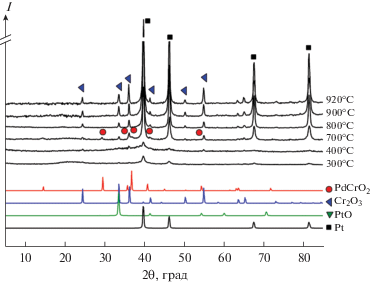
Дифракционные картины разложения комплексной соли [Pt(NH3)4]CrO4 в условиях ex situ (рис. 4) подробно описаны в работе [16]. Дифрактограммы в условиях ex situ отличаются от разложения в условиях in situ. При температуре 300°С и в ex situ, и в in situ экспериментах на дифрактограммах присутствуют только рефлексы металлической платины, а при 400°С в закалочных экспериментах дополнительно появляются пики оксида хрома(III). В то же время в эксперименте in situ оксид хрома(III) находится в аморфном состоянии и кристаллизуется только при 540°С. При температуре 700°С в эксперименте ex situ, в отличие от in situ, на дифрактограмме появляются рефлексы фазы со структурой делафоссита на основе платины, что подтверждается сравнением с положением рефлексов от делафосситоподобного PdCrO2 [26].
Рис. 4.
РФА продуктов термолиза [Pt(NH3)4]СrO4 в атмосфере синтетического воздуха при различных температурах.
Таким образом, в режиме непрерывного нагрева (in situ) комплексная соль [Pt(NH3)4]CrO4 претерпевает аморфизацию с последующим выделением и укрупнением металлической платины. Позднее кристаллизуется оксид хрома(III). Образование других промежуточных кристаллических фаз не зафиксировано.
ЗАКЛЮЧЕНИЕ
Показано, что процессы разложения [Pt(NH3)4]CrO4 в атмосфере синтетического воздуха отличаются при проведении термолиза в условиях in situ и ex situ. В закалочных экспериментах, в отличие от in situ, зарегистрированы рефлексы фазы PtCrO2 со структурой делафоссита, которая существует в очень узком температурном интервале. Конечным продуктом термолиза синтезированного соединения является однородная смесь металлической платины и оксида хрома(III).
Комплексная соль [Pt(NH3)4]CrO4 обладает отрицательным линейным коэффициентом теплового расширения (–1.9 × 10–5 1/K) в температурном диапазоне 30–200°С без разрушения кристаллической структуры. Эксперименты по циклированию показали устойчивость данной комплексной соли при последовательном нагреве до 200°С и охлаждении.
Список литературы
Potemkin D.I., Maslov D.K., Loponov K. et al. // Front. Chem. 2018. V. 6. https://doi.org/10.3389/fchem.2018.00085
Zadesenets A.V., Filatov E.Y., Plyusnin P.E. et al. // New J. Chem. 2018. V. 42. № 11. P. 8843. https://doi.org/10.1039/c8nj00956b
Korol’kov I.V., Martynova S.A., Yusenko K.V. et al. // Russ. J. Inorg. Chem. 2010. V. 55. № 9. P. 1347. [Корольков И.В., Мартынова С.А., Юсенко К.В. и др. // Журн. неорган. химии. 2010. Т. 55. № 9. С. 1429.]https://doi.org/10.1134/S0036023610090032
Kirilovich A.K., Plyusnin P.E., Piryazev D.A. et al. // Russ. J. Inorg. Chem. 2017. V. 62. № 7. P. 886. [Кирилович А.К., Плюснин П.Е., Пирязев Д.А. и др. // Журн. неорган. химии. 2017. Т. 62. № 7. С. 905.]https://doi.org/10.1134/S0036023617070099
Yusenko K.V., Pechenyuk S.I., Vikulova E.S. et al. // J. Struct. Chem. 2019. V. 60. № 7. P. 1062. [Юсенко К.В., Печенюк С.И., Викулова Е.С. и др. // Журн. структур. химии. 2019. V. 60. № 7. P. 1110.]https://doi.org/10.1134/S0022476619070060
Makotchenko E.V., Plyusnin P.E., Shubin Y.V. et al. // Russ. J. Inorg. Chem. 2017. V. 62. № 1. P. 12. [Макотченко Е.В., Плюснин П.Е., Шубин Ю.В. и др. // Журн. неорган. химии. 2017. Т. 62. № 1. С. 15.]https://doi.org/10.1134/S0036023617010119
Lunca-Popa P., Botsoa J., Bahri M. et al. // Sci. Rep. 2020. V. 10. № 1. P. 1. https://doi.org/10.1038/s41598-020-58312-z
Zhang K.H.L., Xi K., Blamire M.G. et al. // J. Phys. Condens. Matter. 2016. V. 28. № 38. https://doi.org/10.1088/0953-8984/28/38/383002
Yatsugi K., Ishizaki T., Akedo K. et al. // J. Nanoparticle Res. 2019. V. 21. № 3. https://doi.org/10.1007/s11051-019-4497-2
Kaewsai D., Yeamdee S., Supajaroon S. et al. // Int. J. Hydrogen Energy. 2018. V. 43. № 10. P. 5133. https://doi.org/10.1016/j.ijhydene.2018.01.101
Potemkin D.I., Saparbaev E.S., Zadesenets A.V. et al. // Catal. Ind. 2018. V. 10. № 1. P. 62. https://doi.org/10.1134/S2070050418010099
Fang H., Yang J., Wen M. et al. // Adv. Mater. 2018. V. 30. № 17. https://doi.org/10.1002/adma.201705698
Zhang Q., Wu X.-P., Li Y. et al. // ACS Catal. 2016. V. 6. № 9. P. 6236. https://doi.org/10.1021/acscatal.6b01226
Yu J., Lei J., Yan C. et al. // Asian J. Chem. 2014. V. 26. № 15. P. 4755.
Tupikova E.N., Platonov I.A., Khabarova D.S. // Kinet. Catal. 2019. V. 60. № 3. P. 366. [Тупикова Е.Н., Платонов И.А., Хабарова Д.С. // Кинетика и катализ. 2019. Т. 60. № 3. С. 388.]https://doi.org/10.1134/S0023158419030145
Filatov E., Lagunova V., Potemkin D. et al. // Chem. Eur. J. 2020. V. 26. № 19. P. 4341. https://doi.org/10.1002/chem.201905391
Aulchenko V.M., Evdokov O.V., Kutovenko V.D. et al. // Nucl. Instruments Methods Phys. Res. Sect. A. Accel. Spectrometers, Detect. Assoc. Equip. 2009. V. 603. № 1–2. P. 76. https://doi.org/10.1016/j.nima.2008.12.164
Powder Diffraction File. PDF-2. International Centre for Diffraction Data. Pennsylvania. USA. 2014.
Kraus W., Nolze G. // PowderCell 2.4, Program for the representation and manipulation of crystal structures and calculation of the resulting X-ray powder patterns. Federal Institute for Materials Research and Testing. Berlin, 2000.
Coelho A.A. TOPAS-Academic. Vers. 6.0 (Computer Software). Coelho Software, Brisbane. 2019.
Krumm S. // An interactive Windows program for profile fitting and size/strain analysis. Materials Science Forum. 1996. V. 228–231. P. 183. https://doi.org/10.4028/www.scientific.net/MSF.228-231.183
Mary T.A., Evans J.S., Vogt T. et al. // Science. 1996. V. 272. P. 90. https://doi.org/10.1126/science.272.5258.90
Petrushina M.Y., Dedova E.S., Filatov E.Y. et al. // Sci. Rep. 2018. V. 8. № 1. P. 1. https://doi.org/10.1038/s41598-018-23529-6
Monroe J.A., McAllister J.S., Content D.S. et al. Advances in Optical and Mechanical Technologies for Telescopes and Instrumentation III. 2018. V. 10706. https://doi.org/10.1117/12.2314657
Arblaster J.W. // Platin. Met. Rev. 2013. V. 57. № 2. P. 127. https://doi.org/10.1595/147106713X665030
Mackenzie A.P. // Reports Prog. Phys. 2017. V. 80. № 3. https://doi.org/10.1088/1361-6633/aa50e5
Дополнительные материалы отсутствуют.
Инструменты
Журнал неорганической химии


