Журнал неорганической химии, 2020, T. 65, № 8, стр. 1027-1034
Люминесцентные свойства шпинелей, активированных ионами марганца
Н. М. Хайдуков a, М. Н. Бреховских a, *, Н. Ю. Кирикова b, В. А. Кондратюк b, В. Н. Махов b
a Институт общей и неорганической химии им. Н.С. Курнакова РАН
119991 Москва, Ленинский пр-т, 31, Россия
b Физический институт им. П.Н. Лебедева РАН
119991 Москва, Ленинский пр-т, 53, Россия
* E-mail: mbrekh@igic.ras.ru
Поступила в редакцию 12.03.2020
После доработки 30.03.2020
Принята к публикации 31.03.2020
Аннотация
Разработан метод синтеза соединений на основе шпинели MgAl2O4, активированных ионами марганца, который дает возможность создавать люминофоры красного (пик полосы при 651 нм) или зеленого цвета свечения (пик полосы при 525 нм) вследствие люминесценции ионов Mn4+ или Mn2+ соответственно, а также люминофоров, обладающих одновременно красной и зеленой полосами люминесценции. Оба типа люминесценции демонстрируют достаточно высокую температурную стабильность, особенно зеленая люминесценция, а именно: температура, при которой интенсивность люминесценции уменьшается в два раза по сравнению с максимальной интенсивностью, составляет T0.5 = 448 и 737 K для красной Mn4+ и зеленой Mn2+ люминесценции соответственно. С другой стороны, у люминофоров, обладающих обеими полосами люминесценции, температурные зависимости интенсивности красной и зеленой люминесценции становятся более похожими друг на друга из-за наличия передачи энергии от ионов Mn4+ к ионам Mn2+. Обе полосы люминесценции эффективно возбуждаются в синей спектральной области, что позволяет применять канонический трехцветный RGB (red green blue) способ для создания светодиодных источников белого света на основе комбинации из синего светодиода и люминофора, содержащего ионы марганца, с оптимально подобранным отношением интенсивностей зеленой и красной полос люминесценции.
ВВЕДЕНИЕ
В последнее время источники белого света, основанные на использовании светодиодов, получили невероятно широкое распространение и продолжают заменять другие, менее эффективные, типы ламп, в частности, в бытовом освещении. В этом контексте продолжается поиск и разработка новых люминофоров для таких светодиодных источников с целью дальнейшего повышения их эффективности. Большое внимание уделяется разработке новых узкополосных красных люминофоров со свечением в области 620–650 нм для светодиодных источников теплого белого света [1]. Общеизвестно, что ионы Mn4+ в октаэдрическом окружении испускают узкополосную люминесценцию в красной области спектра [2–13], т.е. красные люминофоры, активированные ионами Mn4+, считаются одними из наиболее перспективных для применения в таких источниках.
Проблемой в светодиодной технике является тот факт, что зеленые светодиоды, занимающие критическую область спектра для цветового восприятия света, имеют существенно более низкую эффективность по сравнению с красными и синими светодиодами. Это обстоятельство, известное как “зеленый зазор”, существенно ограничивает разработку светодиодных источников света для широкого применения. Одним из вариантов разработки зеленых светодиодов может быть использование люминофоров, эффективно преобразующих излучение синего светодиода в зеленую люминесценцию. Люминофоры на основе люминесценции ионов Mn2+ являются хорошо известными примерами зеленых люминофоров [14].
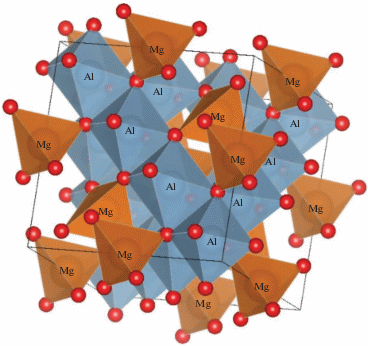
Одними из часто используемых матриц для создания люминофоров являются соединения структурной группы шпинели. Однако свойства таких материалов могут сильно зависеть от метода синтеза [15, 16]. Кристаллическая структура нормальной шпинели MgAl2O4 имеет следующий вид (рис. 1): каждый двухвалентный катион (Mg2+) в структуре шпинели располагается в центре тетраэдра, а каждый трехвалентный катион (Al3+) расположен в октаэдре [17, 18]. Таким образом, структура характеризуется сочетанием тетраэдров и октаэдров, причем каждая вершина является общей для одного тетраэдра и трех октаэдров. Эти особенности структуры обусловливают такие свойства шпинели, как оптическая изотропия, отсутствие спайности, химическая и термическая стойкость, довольно высокая твердость и др. С другой стороны, в структуре возможна инверсия, и часть двухвалентных катионов может находиться на октаэдрической позиции, а трехвалентные катионы – на тетраэдрической позиции. В результате, в кристаллической структуре шпинели создается разупорядоченность, аналогичная той, которая наблюдается в твердых растворах. Указанные особенности предоставляют широкие возможности для легирования матрицы шпинели на тетраэдрических и октаэдрических позициях оптически активными ионами различного зарядового состояния. Тем не менее до настоящего времени указанные свойства шпинели не были в полной мере реализованы для разработки люминофоров, в частности, содержащих ионы марганца.
Целью работы являются разработка методов синтеза люминофоров красного или зеленого цвета свечения, а также люминофоров, обладающих одновременно красной и зеленой полосами люминесценции, на основе матрицы шпинели MgAl2O4, активированной ионами марганца, и исследование спектральных и температурных свойств люминесценции синтезированных люминофоров.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Керамики со структурой шпинели, содержащие 0.2 ат. % ионов марганца, были синтезированы методом высокотемпературных твердофазных реакций с использованием MgCO3 (ос. ч.), Al2O3 (99.99), MnO2 (99.99) и LiF (ос. ч.) [19, 20]. Эти исходные материалы взвешивали в соответствии с теоретическим составом 0.996MgAl2O4 ⋅ ⋅ 0.002MnO2 ⋅ 0.002LiF и растирали в агатовой ступке для гомогенизации. Порошковые смеси одноосно прессовали в матрице из нержавеющей стали при давлении ~150 МПа в таблетки диаметром 10 мм и толщиной ~2 мм. Спрессованные таблетки прокаливали при различных температурах.
Принимая во внимание, что MnO2 разлагается с потерей кислорода при температуре выше 530°С, спрессованные смеси подвергали последовательному отжигу в корундовых тиглях при температурах 500, 600, 700, 1000 и 1200°С в течение 6 ч в воздушной атмосфере для каждого температурного режима. После каждого отжига таблетки растирали для гомогенизации и прессовали заново. В результате синтеза были получены таблетки, имеющие слабо-желтую окраску – образец I. Образец I дробили и растирали, в полученный порошок добавляли 3 мас. % H3BO3 в качестве плавня. Смесь прессовали в таблетки, которые отжигали при температуре 1300°С в течение 4 ч в воздушной атмосфере образец II.
Кроме того, таблетки смеси исходных реактивов подвергали отжигу при температуре 1000°С в течение 6 ч без предварительных отжигов при более низких температурах. Керамику дробили, растирали в порошок, в него добавляли 3 мас. % H3BO3, затем смесь прессовали в таблетки, которые отжигали при температуре 1300°С в течение 4 ч на воздухе – образец III. Затем таблетки образца III помещали в графитовый тигель и отжигали при температуре 1300°С в атмосфере CO – образец IV.
Были синтезированы также образцы, содержащие фтор, а именно соединение Mg1.25Al1.75O3.75F0.25, активированное ионами марганца. Для синтеза использовали MgAl2O4, содержащий ионы марганца (образец II), MgO и MgF2. Смесь исходных реактивов в соответствующей пропорции была спрессована в таблетки, которые отжигали при температурах 1100 (образец V) и 1150°С (образец VI) в течение 4 ч в атмосфере аргона. Состав и условия синтеза шпинелей приведены в табл. 1. Фазовый состав и структуру синтезированных керамик контролировали с помощью рентгеновского дифракционного анализа на дифрактометре D8 Advance (Bruker) в монохроматическом CuKα-излучении. Для идентификации синтезированных соединений использовали пакет программ EVA (Bruker) и базу кристаллографических данных ICDD PDF-2.
Таблица 1.
Состав и условия синтеза образцов шпинели
| № образца | Состав | Отжиг | Атмосфера синтеза | |
|---|---|---|---|---|
| t, °С | время, ч | |||
| I | MgAl2O4:Mn | 500, 600, 700, 1000, 1200 | 6* | Воздух |
| II | MgAl2O4:Mn + 3 мас. % H3BO3 | 1000–1300 | 4 | Воздух |
| III | MgAl2O4:Mn + 3 мас. % H3BO3 | 1000 | 4 | Воздух |
| IV | MgAl2O4:Mn2+ | 1300 | 4 | CO |
| V | Mg1.25Al1.75O3.75F0.25:Mn | 1100 | 4 | Аргон |
| VI | Mg1.25Al1.75O3.75F0.25:Mn | 1150 | 4 | Аргон |
Спектры люминесценции синтезированных образцов исследовали на установке, в состав которой в качестве возбуждающих источников излучения входили УФ (385 нм) и синий (455 нм) светодиоды фирмы Mightex, управляемые контроллером SLA-1000-2, которые являются аналогами светодиодов, используемых в коммерческих светодиодных источниках белого света. Спектры люминесценции анализировали с помощью светосильного монохроматора МДР-12, управляемого с персонального компьютера через контроллер КСП-3.3.001.0 (ОКБ “Спектр”). Люминесценцию регистрировали фотоумножителем ФЭУ-100.
Спектры возбуждения люминесценции синтезированных образцов исследовали, используя в качестве возбуждающего источника излучения стандартную галогеновую лампу накаливания (рабочая спектральная область 330–550 нм) и решеточный монохроматор МДР-12, установленный в канал возбуждения люминесценции. Люминесценцию от образца регистрировали фотоумножителем ФЭУ-100, перед которым устанавливали светофильтры для выделения регистрируемой полосы люминесценции. Чтобы учесть спектральную зависимость интенсивности возбуждающего излучения, измеренные спектры возбуждения люминесценции нормировали на спектр возбуждения люминесценции желтого люмогена, который имеет постоянный квантовый выход в указанном спектральном диапазоне. Типичное спектральное разрешение при измерении спектров люминесценции и возбуждения люминесценции составляло 1 нм.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
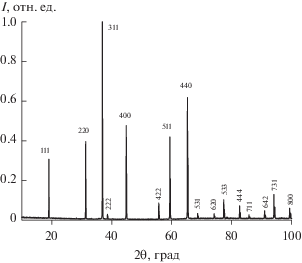
Результаты рентгенофазового анализа подтверждают, что все синтезированные образцы керамик принадлежат к кубической сингонии и имеют структурный тип шпинели (рис. 2). Параметр кубической решетки a, определенный из анализа рентгенограмм, изменяется в пределах 8.07–8.09 Å для керамик, синтезированных при различных условиях. Какая-либо закономерность в изменении параметра a не прослеживается.
Рис. 2.
Рентгенограмма шпинели MgAl2O4:Mn (образец II). Рядом с пиками указаны индексы Миллера соответствующих плоскостей кристаллической решетки (hkl).
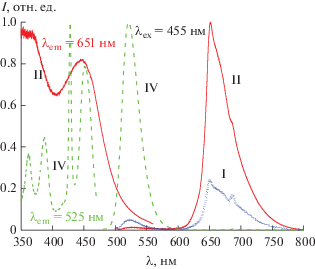
Спектры люминесценции и возбуждения люминесценции люминофоров MgAl2O4:Mn, синтезированных при различных условиях, показаны на рис. 3. Максимум интенсивной полосы красной люминесценции расположен при ~651 нм (образцы I и II), а спектр ее возбуждения содержит две основные полосы с максимумами при ~446 и ~364 нм. В соответствии с общепринятой моделью и имеющимися литературными данными [2], полоса красной люминесценции обусловлена запрещенным по спину переходом в ионах Mn4+: 2E → 4A2, а полосы возбуждения (поглощения) обусловлены разрешенными по спину переходами в Mn4+: 4A2 → 4T2 и 4A2 → 4T1 соответственно [21]. Полученные спектры хорошо соответствуют имеющимся в литературе данным [22–24]. Принимая во внимание тот факт, что ионные радиусы ионов Mn4+ (0.53 Å) и Al3+ (0.535 Å) в октаэдре практически одинаковы [25], а также общепринятое положение, что ионы Mn4+ могут стабилизироваться в кристаллической решетке только в октаэдрическом окружении, естественно предположить, что ионы Mn4+ замещают ионы Al3+ в октаэдрических узлах решетки матрицы. Зарядовая компенсация при этом достигается в результате гетеровалентного замещения: Al3+ + Mg2+ → Li+ + Mn4+.
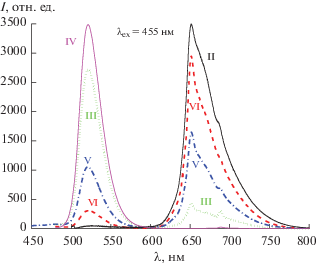
Рис. 3.
Спектры люминесценции (справа) образцов шпинели MgAl2O4:Mn (0.2 ат. %), синтезированных при температуре 1200 и 1300°С на воздухе (образцы I и II соответственно), а также шпинели MgAl2O4:Mn, отожженной в атмосфере CO (образец IV) при возбуждении синим светодиодом, и спектры возбуждения люминесценции (слева): красной люминесценции (651 нм) от образца II и зеленой люминесценции (525 нм) от образца IV.
Интенсивность люминесценции Mn4+ существенно ниже у образца, отожженного при более низкой (1200°С) температуре. Видимо, температуры 1200°С недостаточно, чтобы большая часть ионов марганца стабилизировалась в октаэдрических узлах решетки в зарядовом состоянии +4. Можно предположить, что ионы марганца в этом случае входят в матрицу шпинели в основном в виде Mn3+, замещая ионы Al3+, на что не требуется зарядовой компенсации. Данных по люминесцентным свойствам ионов Mn3+ почти нет, что может быть связано с тем, что в спектральной области, представляющей интерес для рассматриваемых применений, ионы Mn3+ не имеют заметной оптической активности [26]. В спектрах большинства образцов наблюдается также узкий пик при ~687 нм, который обусловлен люминесценцией примесных ионов Cr3+, имеющихся в синтезированных люминофорах из-за недостаточно высокой чистоты исходных реактивов, использованных при синтезе, и замещающих ионы Al3+.
Как видно из рис. 3 и 4, в эмиссионном спектре синтезированных образцов (образцы III и IV) имеется широкая полоса в зеленой области спектра с максимумом при ~525 нм, которая обусловлена люминесценцией ионов Mn2+, возникающей благодаря запрещенному по спину переходу 4T1 → 6A1 [4]. Считается общепризнанным, что ионы Mn2+ замещают ионы Mg2+ в тетраэдрических узлах решетки шпинели [27], поскольку это не требует зарядовой компенсации, а ионные радиусы Mn2+ и Mg2+ в тетраэдрическом окружении близки (0.66 и 0.57 Å соответственно [25]). В спектре возбуждения зеленой люминесценции выделяется характерная узкая полоса около 430 нм, обусловленная переходом 6A1 → [4E, 4A1] в ионе Mn2+, энергия которого не зависит от силы кристаллического поля, а также более широкая полоса с пиком при 452 нм, соответствующая переходу 6A1 → 4T2 в ионе Mn2+. Последняя полоса по своим характеристикам практически совпадает с полосой излучения стандартного синего светодиода.
Рис. 4.
Изменение отношения интенсивностей красной и зеленой люминесценции ионов марганца в образцах I–VI, синтезированных при различных условиях (см. табл. 1).
Таким образом, в зависимости от процедуры отжига спектральные свойства люминофора MgAl2O4:Mn могут быть существенно видоизменены, а именно: в шпинели, подвергнутой длительному отжигу при низких температурах, доминирует красная люминесценция ионов Mn4+, а в шпинели, синтезированной без низкотемпературного отжига, доминирует зеленая люминесценция ионов Mn2+. Критическим моментом для получения красной люминесценции ионов Mn4+ является необходимость стабилизировать в матрице шпинели ионы марганца в четырехвалентном состоянии при отжиге при достаточно низкой температуре.
Отношение интенсивностей красной и зеленой люминесценции можно варьировать, изменяя условия синтеза (рис. 4). Предполагается, что частичное замещение ионов Al3+ ионами Mg2+ усиливает интенсивность красной люминесценции ионов Mn4+ в люминофорах, в структуре которых Mn4+ замещает Al3+ в октаэдрических позициях, в результате гетеровалентного замещения: Al3+ + Al3+ → Mg2+ + Mn4+ с зарядовой компенсацией ионов Mn4+ избыточными ионами Mg2+ [2]. В соответствии с данными [5, 7], в шпинели замещение ионов Al3+ ионами Mg2+ может также обусловливать трансформацию Mn2+ в Mn4+. Однако в нашем случае наблюдается обратная тенденция. Люминофор Mg1.25Al1.75O3.75F0.25:Mn, в котором часть ионов Al3+ замещена ионами Mg2+ (образец V), в дополнение к красной люминесценции MgAl2O4:Mn (образец II, использованный для синтеза) демонстрирует также зеленую люминесценцию ионов Mn2+. Отношение интенсивностей зеленой и красной полос люминесценции в Mg1.25Al1.75O3.75F0.25:Mn можно изменять температурой синтеза (образцы V и VI). Вероятно, при введении MgF2 в MgAl2O4:Mn происходит замещение Al3+ в тетраэдрической позиции в частично инверсионной шпинели с преимущественным распределением ионов фтора в тетраэдрическом окружении, что обусловливает трансформацию ионов Mn3+ в Mn2+ для компенсации заряда в тетраэдрах. Повышение температуры ведет к статистическому распределению ионов фтора в структуре шпинели и соответственно к обратной трансформации ионов Mn2+ в Mn3+ в тетраэдрической позиции в структуре шпинели.
Зеленая и красная люминесценция ионов Mn2+ и Mn4+ в шпинели обладает достаточно высокой температурной стабильностью (рис. 5). В частности, интенсивность зеленой люминесценции люминофора MgAl2O4:Mn2+, отожженного в атмосфере CO (образец IV), составляет 60% при температуре 400°С от интенсивности при комнатной температуре. Наблюдаемая температурная зависимость интенсивности люминесценции может быть описана хорошо известной формулой для температурного тушения через энергетический барьер (энергию активации):
(1)
$I\left( T \right) = \frac{{{{I}_{0}}}}{{1 + A\exp \left( { - \frac{{{{E}_{a}}}}{{{{k}_{{\text{B}}}}T}}} \right)}},$Рис. 5.
Температурные зависимости интегральной интенсивности зеленой люминесценции люминофора MgAl2O4:Mn (0.2%), синтезированного в атмосфере CO (образец IV, 1), а также зеленой (Mn2+, 2) и красной (Mn4+, 3) люминесценции люминофора Mg1.25Al1.75O3.75F0.25:Mn (образец V). Линиями показаны кривые моделирования данных зависимостей по формуле (1).
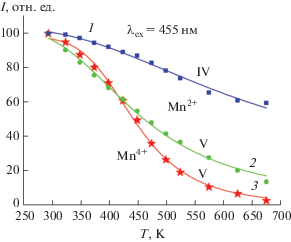
При измерениях температурных зависимостей интенсивности красной и зеленой люминесценции для люминофора, обладающего обоими типами люминесценции, форма кривой температурной зависимости для зеленой люминесценции становится более похожей на кривую для красной люминесценции с T0.5 ≈ 462 K, т.е. во всей области температур, где происходит температурное тушение красной люминесценции, интенсивность зеленой люминесценции также сильно падает. Этот факт демонстрирует, что возбуждающее излучение синего светодиода поглощается преимущественно ионами Mn4+ (на сильном разрешенном по спину переходе 4A2 → 4T2) с последующей частичной передачей энергии ионам Mn2+. С другой стороны, похожие температурные зависимости для полос красной и зеленой люминесценции означают, что цветовые свойства люминофора почти не изменяются с температурой, что очень важно для практического применения.
Максимум интенсивности полосы люминесценции Mn4+ в MgAl2O4 при ~651 нм очень близок к оптимальному значению для красного люминофора для светодиодных ламп теплого белого света, т.е. люминофор на основе шпинели MgAl2O4, в которой доминирует красная полоса люминесценции Mn4+, имеет перспективу использования в качестве красной компоненты свечения для светодиодных источников теплого белого света. С другой стороны, спектр зеленой люминесценции Mn2+ в MgAl2O4 также близок к оптимальному для зеленого люминофора, и эта зеленая люминесценция эффективно возбуждается в спектральной области, хорошо соответствующей спектру излучения стандартного синего светодиода.
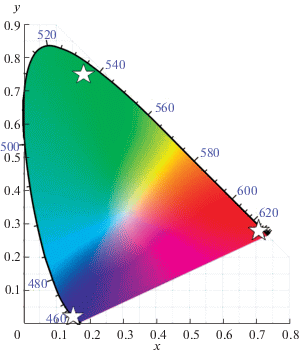
Люминофор на основе MgAl2O4:Mn, обладающий красной и зеленой полосами люминесценции, эффективно возбуждающейся в синей области спектра, может рассматриваться как альтернатива однополосному желтому люминофору YAG:Ce, применяемому в стандартных светодиодных лампах белого света. Такой однофазный двухцветный люминофор может быть использован для создания белых светодиодов по канонической схеме RGB источника белого света. Рассчитанные цветовые координаты (CIE1931) для спектров люминесценции MgAl2O4:Mn изменяются от x = 0.18; y = 0.75 для люминофора, обладающего только зеленой люминесценцией Mn2+, до x = 0.72; y = 0.28 для люминофора с чисто красной люминесценцией Mn4+ (рис. 6). Использование люминофоров с разным отношением интенсивностей красной и зеленой полос люминесценции в сочетании с синим светодиодом потенциально дает возможность варьировать в широком диапазоне цветовые характеристики результирующего источника белого света. Важно отметить, что отношение интенсивностей красной и зеленой люминесценции в спектре излучения люминофора MgAl2O4:Mn может подбираться с помощью контролируемого изменения условий синтеза, что обеспечивает гибкость настройки цветовых характеристик люминофора, требуемых для конкретного применения.
ЗАКЛЮЧЕНИЕ
Исследованы спектральные свойства и температурная стабильность люминесценции люминофоров на основе соединений со структурой шпинели, активированных ионами марганца. Разработанный метод синтеза реализует возможность создавать люминофоры красного (x = 0.72; y = 0.28) или зеленого (x = 0.18; y = 0.75) цвета свечения на основе люминесценции ионов Mn4+ или Mn2+ соответственно, а также люминофоров, обладающих одновременно красной и зеленой полосами люминесценции, с помощью контролируемого изменения условий синтеза. Обе полосы люминесценции эффективно возбуждаются в синей области спектра, что позволяет использовать данные люминофоры в сочетании с синим светодиодом для создания светодиодных источников белого света по канонической трехцветной (RGB) схеме. Красная и зеленая люминесценция ионов марганца в шпинели обладает достаточно высокой температурной стабильностью, хотя она несколько выше для зеленой люминесценции ионов Mn2+, чем для красной люминесценции ионов Mn4+.
Список литературы
Lin Y.-C., Karlsson M., Bettinelli M. // Top. Curr. Chem. (Z). 2016. V. 374. P. 21. https://doi.org/10.1007/s41061-016-0023-5
Brik M.G., Srivastava A.M. // J. Lumin. 2013. V. 133. P. 692. https://doi.org/10.1016/j.jlumin.2011.08.047
Zhou Z., Zhou N., Xia M. et al. // J. Mater. Chem. 2016. V. 4. P. 9143. https://doi.org/10.1039/C6TC02496C
Adachi S. // J. Lumin. 2018. V. 197. P. 119. https://doi.org/10.1016/j.jlumin.2018.01.016
Adachi S. // J. Lumin. 2018. V. 202. P. 263. https://doi.org/10.1016/j.jlumin.2018.05.053
Zhou Q., Dolgov L., Srivastava A.M. et al. // J. Mater. Chem. 2018. V. 6. P. 2652. https://doi.org/10.1039/C8TC00251G
Senden T., van Dijk-Moes R. J. A., Meijerink A. // Light Sci. Appl. 2018. V. 7. P. 1. https://doi.org/10.1038/s41377-018-0013-1
Jansen T., Gorobez J., Kirm M. et al. // ECS J. Solid State Sci. Technol. 2018. V. 7. P. 3086. https://doi.org/10.1149/2.0121801jss
Jansen T., Jüstel T., Kirm M. et al. // J. Lumin. 2018. V. 198. P. 314. https://doi.org/10.1016/j.jlumin.2018.02.054
Jansen T., Jüstel T., Kirm M. et al. // Opt. Mater. 2018. V. 84. P. 600. https://doi.org/10.1016/j.optmat.2018.07.061
Kirm M., Oja M., Kozlova J. et al. // Phys. Solid State. 2019. V. 61. № 5. P. 853–859. https://doi.org/10.1134/S1063783419050147
Khaidukov N., Brekhovskikh M., Toci G. et al. // J. Lumin. V. 216. P. 1. https://doi.org/10.1016/j.jlumin.2019.116754
Adachi S. // ECS J. Solid State Sci. Technol. 2020. V. 9. P. 016001.https://doi.org/10.1149/2.0022001JSS
Blasse G., Grambier B.C. Luminescent Materials. Berlin: Springer-Verlag, 1994. 233 p.
Соколовский А.Е., Бобкова Н.М., Родион Е.В. // Журн. прикл. химии. 2003. Т. 76. № 3. С. 360.
Иванова А.С., Дзисько В.А., Кетчик С.В. // Журн. неорган. химии. 1980. Т. 25. № 9. С. 2330.
Momma K., Izumi F. // J. Appl. Crystallogr. 2011. V. 44. P. 1272. https://doi.org/10.1107/S0021889811038970
Jain A., Ong S.P., Hautier G. et al. // APL Materials. 2013. V. 1. № 1. P. 011002. https://doi.org/10.1063/1.4812323
Simentsova I.I., Plyasova L.M., Shtertser N.V. et al. // Russ. J. Inorg. Chem. 2017. V. 62. P. 39. https://doi.org/10.1134/S003602361701020X
Ketsko V.A., Beresnev E.N., Kop’eva M.A. et al. // Russ. J. Inorg. Chem. 2010. V. 55. P. 427. https://doi.org/10.1134/S0036023610030216
Tanabe Y., Sugano S. // J. Phys. Soc. Jpn. 1954. V. 9. P. 776. https://doi.org/10.1143/JPSJ.9.766
Wakui Y., Shan Y.J., Tezuka K. et al. // Mater. Res. Bull. 2017. V. 90. P. 51.https://doi.org/10.1016/j.materresbull.2017.02.001
Lia S., Zhaoa S.-Y., Yec T.-N. et al. // J. Compos. Biodegradable Polym. 2017. V. 5. P. 17.https://doi.org/10.12974/2311-8717.2017.05.01.3
Zhang Y., Liu Y., Yang L. et al. // J. Lumin. 2020. V. 220. P. 117016. https://doi.org/10.1016/j.jlumin.2019.117016
Shannon R.D. // Acta Crystallogr., Sect. A. 1976. V. 32. P. 751. https://doi.org/10.1107/S0567739476001551
Kück S., Hartung S., Hurling S. et al. // Phys. Rev. B. 1998. V. 57. P. 2203. https://doi.org/10.1103/PhysRevB.57.2203
Song E.H., Zhou Y.Y., Wei Y. et al. // J. Mater. Chem. 2019. V. 7. P. 8192. https://doi.org/10.1039/c9tc02107h
Дополнительные материалы отсутствуют.
Инструменты
Журнал неорганической химии