Журнал неорганической химии, 2021, T. 66, № 4, стр. 456-463
Синтез и структура гибридных галовисмутатов – производных N-ацетонилпиридиния
П. А. Буйкин a, b, c, *, А. Ю. Руденко c, d, А. Б. Илюхин a, В. Ю. Котов a, b
a Институт общей и неорганической химии им. Н.С. Курнакова РАН
119991 Москва, Ленинский пр-т, 31, Россия
b Научно-исследовательский университет “Высшая школа экономики”
101000 Москва, ул. Мясницкая, 20, Россия
c Высший химический колледж РАН, Российский химико-технологический университет им. Д.И. Менделеева
125047 Москва, Миусская пл., 9, Россия
d Институт органической химии им. Н.Д. Зеленского РАН
119991 Москва, Ленинский пр-т, 47, Россия
* E-mail: peterzzz@mail.ru
Поступила в редакцию 30.09.2020
После доработки 28.10.2020
Принята к публикации 30.10.2020
Аннотация
Получены и структурно охарактеризованы новые гибридные галовисмутаты N-ацетонилпиридиния N-(ω-иодоацетонил)пиридиния и N-ацетонил-2,6-диметилпиридиния I–VII. Препаративный метод синтеза предложен для соединений I, III и VII, для соединений II, IV–VI удалось выделить и охарактеризовать отдельные кристаллы. В структуре [C8H10NO]2K[BiBr6] (II) обнаружен новый тип 1D-цепей {K[BiBr6]$\} _{n}^{{2n - }}$ с участием катионов K+. Бромовисмутаты N-ацетонил-2,6-диметилпиридиния [C10H14NO]3[Bi2Br9] V и VI (пр. гр. P21/n) являются полиморфами cо сходным строением. Иодовисмутаты [C8H10NO]4[Bi4I16] (III) и [C10H14NO]4[Bi4I16] ⋅ 0.69I2 (VII) образованы анионами [Bi4I16]4–, при этом в структуре VII молекулы I2 связывают фрагменты [Bi4I16] в 1D-анионную цепь.
ВВЕДЕНИЕ
Гибридные галовисмутаты вызывают широкий интерес благодаря их высокой гидролитической стабильности [1] и низкой токсичности. Низкие значения ширины запрещенной зоны (Eg) для некоторых гибридных галовисмутатов [2–6] позволяют рассматривать их как перспективные светопоглощающие материалы [7–9]. Привлекают внимание фотохромные [3, 10, 11] и ферроэлектрические свойства гибридных галовисмутатов [12–15]. Известно значительное число галовисмутатов, являющихся катионными производными пиридина, замещенными по разным положениям ароматического кольца [16, 17]. Наиболее изучены галовисмутаты катионов на основе N-замещенных пиридинов с неполярными алкильными заместителями. Соединения с полярными алкильными заместителями встречаются реже. Известно всего одно соединение в Кембриджском банке структурных данных (CSD [18], версия 09.2020), содержащее полярный ацетонильный заместитель в N-положении пиридинового кольца, – двойной иодовисмутат N-ацетонилпиридиния-пиридиния [1-(CH2C(O)CH3)Py]2(HPy)[BiI6] [19]. Свидетельства, подтверждающие однофазность этого соединения, в [19] не приведены.
Цель настоящей работы – синтез и структурное исследование бромо- и иодовисмутатов N-ацетонилпиридиния, а также N-ацетонил-2,6-диметилпиридиния. Мы полагали, что наличие полярных групп в составе катионов приведет к образованию прочных ассоциатов с участием водородных связей в кристаллической структуре галовисмутата, что, в свою очередь, скажется на физических свойствах конечных соединений.
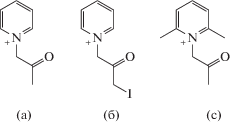
Схема 1 . Катионы N-ацетонилпиридиния [1-(CH2C(O)CH3)Py]+ (а), ω-иодацетонилпиридиния [1-(CH2C(O)CH2I)Py]+ (б) и N-ацетонил-2,6-диметилпиридиния [1-(CH2C(O)CH3)-2,6-CH3Py]+ (в).
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Синтез хлорида N-ацетонилпиридиния. В круглодонную колбу, содержащую 10 мл ацетона и 3.0 мл пиридина (0.038 моль), по каплям добавляли 3.1 мл хлорацетона (0.038 моль). Смесь кипятили в течение 2 ч с обратным холодильником. Раствор охлаждали до комнатной температуры. Выпавший осадок отфильтровывали под вакуумом, промывали этиловым спиртом, диэтиловым эфиром и высушивали на воздухе. Выход 5.67 г (87%).
ЯМР 1Н (300 MГц, ДМСО-d6), δ: 9.02 (d, J = = 5.8 Гц, 2H), 8.70 (t, J = 7.9 Гц, 1H), 8.25 (t, J = = 7.3 Гц, 2H), 6.01 (s, 2H), 2.32 (s, 3H).
Синтез бромида N-ацетонилпиридиния. В круглодонную колбу, содержащую 10 мл ацетона и 3.0 мл пиридина (0.038 моль), по каплям добавляли 3.2 мл бромацетона (0.038 моль). Смесь кипятили в течение 2 ч с обратным холодильником. Раствор охлаждали до комнатной температуры. Выпавший осадок отфильтровывали под вакуумом, промывали этиловым спиртом, диэтиловым эфиром и высушивали на воздухе. Выход 7.55 г (92%).
ЯМР 1Н (300 MГц, ДМСО-d6), δ: 9.18 (d, J = = 6.0 Гц, 2H), 8.69 (t, J = 7.8 Гц, 1H), 8.23 (t, J = = 7.0 Гц, 2H), 6.18 (s, 2H), 2.32 (s, 3H). Согласно данным ЯМР, вещество содержит небольшое количество неидентифицированных примесей.
Синтез бромида N-ацетонил-2,6-диметилпиридиния. В круглодонную колбу, содержащую 10 мл ацетона и 4.4 мл 2,6-диметилпиридина (0.038 моль), по каплям добавляли 3.2 мл бромацетона (0.038 моль). Смесь кипятили в течение 2 ч с обратным холодильником. Раствор охлаждали до комнатной температуры. Выпавший осадок отфильтровывали под вакуумом, промывали этиловым спиртом, диэтиловым эфиром и высушивали на воздухе. Выход 3.62 г.
ЯМР 1Н (300 МГц, ДМСО-d6), δ: 8.43 (t, J = = 7.8 Гц, 1H), 7.97 (d, J = 7.8 Гц, 2H), 5.92 (s, 2H), 2.68 (s, 6H), 2.47 (s, 3H). Согласно данным ЯМР, вещество содержит неидентифицированные примеси.
Синтез [1-(CH2C(O)CH3)Py]4[Bi2Br10] (I). К раствору хлорида N-ацетонилпиридиния (0.500 г, 2.92 ммоль) и KBr (2.10 г, 17.6 ммоль) в 20 мл H2O приливали раствор Bi(NO3)3 · 5H2O (1.42 г, 2.92 ммоль) и KBr (2.20 г, 20.0 ммоль) в 10 мл H2O. Выпавший бледно-желтый осадок оставляли кристаллизоваться в маточном растворе в течение недели. Образовавшиеся кристаллы [1-(CH2C(O)CH3)Py]4[Bi2Br10] (I) отфильтровывали под вакуумом, промывали этиловым спиртом и высушивали на воздухе. По данным РФА (рис. S9a ), полученный продукт является однофазным. Выход 1.18 г (92%). Детали уточнения по Ритвельду: пр. гр. Pnma, a = 19.0698(10), b = 21.1122(11), c = = 12.2862(6) Å, Rexp = 2.62%, Rwp = 8.11%, Rp = = 5.92%, GOF = 3.09. При синтезе соединения I с использованием бромида N-ацетонилпиридиния вместо хлорида N-ацетонилпиридиния по приведенной выше схеме наряду с основной фазой I в продукте реакции обнаружено несколько кристаллов фазы [1-(CH2C(O)CH3)Py]2K[BiBr6] (II).
Синтез [1-(CH2C(O)CH3)Py]4[Bi4I16] (III). К раствору хлорида N-ацетонилпиридиния (0.500 г, 2.92 ммоль) и KI (1.50 г, 8.98 ммоль) в 20 мл H2O приливали раствор Bi(NO3)3 · 5H2O (1.42 г, 2.92 ммоль) и KI (3.00 г, 18.0 ммоль) в 10 мл H2O. Выпавший оранжевый осадок оставляли кристаллизоваться в маточном растворе в течение недели. Образовавшиеся красные кристаллы [1-(CH2C(O)CH3)Py]4[Bi4I16] (III) отфильтровывали под вакуумом, промывали этиловым спиртом и высушивали на воздухе. По данным РФА (рис. S9b ), полученное вещество соответствует структуре III и содержит незначительную примесь неидентифицированного компонента (наиболее интенсивные пики примеси находятся при 2θ = 23.7°, 29.3°, 29.9° и 35.6°). Выход 2.15 г (86%). Детали уточнения по Ритвельду: пр. гр. $P\bar {1}$, a = = 11.4230(6), b = 12.3501(7), c = 14.0611(6) Å, α = = 67.769(4)°, β = 79.589(4)°, γ = 69.130(3)°, Rexp = = 1.96%, Rwp = 8.19%, Rp = 5.53%, GOF = 4.18. При синтезе соединения III с использованием бромида N-ацетонилпиридиния вместо хлорида N-ацетонилпиридиния среди кристаллов основной фазы III были обнаружены кристаллы соединения [1-(CH2C(O)CH3)Py]3[1-(CH2C(O)CH2I)Py][Bi2I9]I3 (IV). Выделение последнего свидетельствует о загрязнении используемого для синтеза бромида N-ацетонилпиридиния бромидом ω-бром-N-ацетонилпиридиния.
Получение кристаллов полиморфов α-[1-(CH2C(O)CH3)-2,6-CH3Py]3[Bi2Br9] (V) и β-[1-(CH2C(O)CH3)-2,6-CH3Py]3[Bi2Br9] (VI). К раствору бромида N-ацетонил-2,6-диметилпиридиния (0.500 г, 2.05 ммоль) и KBr (1.00 г, 8.40 ммоль) в 20 мл H2O приливали раствор Bi(NO3)3 · 5H2O (1.00 г, 2.05 ммоль) и KBr (2.00 г, 16.8 ммоль) в 10 мл H2O. Выпавший бледно-желтый осадок оставляли кристаллизоваться в маточном растворе в течение недели. Образовавшиеся кристаллы α-[1-(CH2C(O)CH3)-2,6-CH3Py]3[Bi2Br9] (V) и β-[1-(CH2C(O)CH3)-2,6-CH3Py]3[Bi2Br9] (VI) отфильтровывали под вакуумом, промывали этиловым спиртом и высушивали на воздухе. По данным РФА (рис. S10 ), продукт наряду с фазами V и VI содержит как минимум еще одну неидентифицированную фазу. Выход 0.92 г.
Синтез [1-(CH2C(O)CH3)-2,6-CH3Py]4[Bi4I16] · · 0.69I2 (VII). К раствору бромида N-ацетонил-2,6-диметилпиридиния (0.500 г, 2.05 ммоль) и KI (1.40 г, 8.38 ммоль) в 20 мл H2O приливали раствор Bi(NO3)3 · 5H2O (1.12 г, 2.31 ммоль) и KI (2.80 г, 16.8 ммоль) в 10 мл H2O. Выпавший оранжевый осадок оставляли кристаллизоваться в маточном растворе в течение недели. Образовавшиеся красные кристаллы [1-(CH2C(O)CH3)-2,6-CH3Py]4[Bi4I16] · · 0.69I2 (VII) отфильтровывали под вакуумом, промывали этиловым спиртом и высушивали на воздухе. По данным РФА (рис. S9c ), выделенный порошок является однофазным. Выход 0.54 г (28%). Детали уточнения по Ритвельду: пр. гр. ${{P{{2}_{1}}} \mathord{\left/ {\vphantom {{P{{2}_{1}}} с}} \right. \kern-0em} с}$, a = 13.2539(7), b = 23.2230(13), c = = 12.8722(7) Å, β = 94.644(4)°, Rexp = 1.51%, Rwp = = 4.09%, Rp = 3.12%, GOF = 2.71.
Рентгеноструктурный анализ. Экспериментальные данные для соединений I–VII получены на дифрактометре Bruker SMART APEX3 (λ(MoKα), графитовый монохроматор) [20] (табл. S1 ). Поглощение учтено полуэмпирическим методом по эквивалентам (программа SADABS) [21]. Структуры определены комбинацией прямого метода и синтезов Фурье. Величины заселенностей разупорядоченных фрагментов получены при изотропном уточнении структур с фиксированными тепловыми параметрами разупорядоченных атомов и в последующих расчетах не уточняли. Структуры уточнены полноматричным анизотропно-изотропным (часть разупорядоченных атомов) МНК. Атомы водорода рассчитаны из геометрических соображений. Все расчеты выполнены по программам SHELXS и SHELXL [22].
Экспериментальные данные для структур I–VII депонированы в Кембриджском банке структурных данных (CCDC № 1998965–1998971); deposit@ccdc.cam.ac.uk или http://www.ccdc.cam.ac.uk).
Рентгенофазовый анализ выполняли на дифрактометре Bruker D8 Advance (CuKα, позиционно-чувствительный 1D-детектор LynxEye, геометрия на отражение). Диапазон измерений 2θ = = 5°–50° для всех образцов. Полнопрофильный анализ порошков проведен с помощью программы TOPAS 4.2 [23]. Уточнение по методу Ритвельда проводили с использованием структурных моделей I, III и VII.
Спектры диффузного отражения регистрировали на спектрофотометре Ocean Optics (модель QE65000) в диапазоне частот 11 000–50 000 см–1 при комнатной температуре. Спектры были перестроены в координатах зависимости функции Кубелка–Мунка [24] от энергии света. Для получения функции Кубелка–Мунка использовали уравнение:
где F(Rd) – абсолютное отражение слоя образца. Оптическую ширину запрещенной зоны (Eg) оценивали экстраполяцией линейной части соответствующей кривой на F(Rd) = 0.Спектры 1Н ЯМР регистрировали на спектрометре Bruker AM300 (300 МГц) в ДМСО-d6 при 303 K.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Взаимодействие хлорида N-ацетонилпиридиния с водным раствором Bi(NO3)3/KBr приводит к образованию продукта [1-(CH2C(O)CH3)Py]4[Bi2Br10] (I). Структура I образована тремя кристаллографически независимыми катионами [1-(CH2C(O)CH3)Py]+ и анионом [Bi2Br10]4– (рис. 1). Два из трех катионов расположены на плоскости m, анион – в центре инверсии. Катионы, расположенные в частной позиции, участвуют друг с другом в стекинг-взаимодействии (рис. S1 ) – кратчайшие контакты 3.43 Å, расстояние между плоскостями пиридиновых колец 3.26 Å (плоскости параллельны из соображений симметрии).
Кратчайшие контакты Br…Br (3.94 Å) объединяют анионы [Bi2Br10]4– в 1D-цепочки (рис. S2 ). В I можно выделить слои, образованные катионами, расположенными в частных позициях (рис. S3 ). Значение оптической ширины запрещенной зоны полученного продукта составляет 2.91 эВ (рис. S8a ).
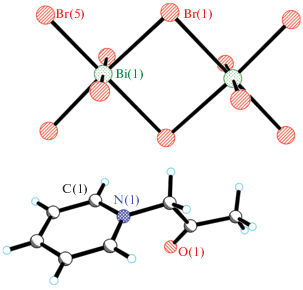
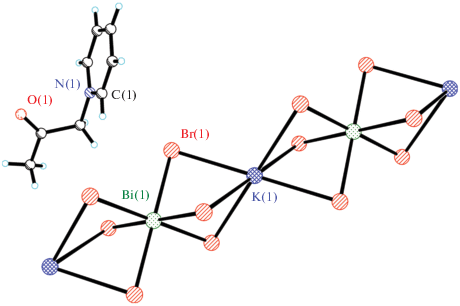
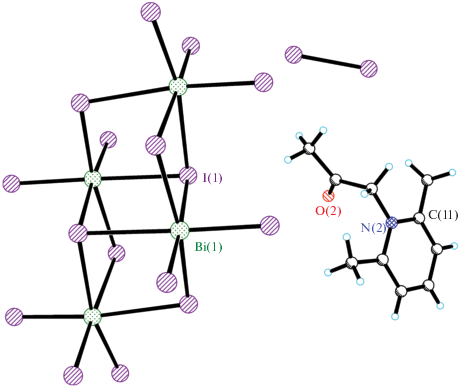
При взаимодействии бромида N-ацетонилпиридиния с водным раствором Bi(NO3)3/KBr наряду с продуктом I образуется также фаза [1 -(CH2C(O)CH3)Py]2K[BiBr6] (II). В структуре II катионы K+ объединяют анионы [BiBr6]3– в 1D-цепочки (рис. 2).
Все структурные единицы в II расположены в частных позициях – катион и один из атомов Br на плоскости m, атомы K и Bi в позиции 2/m. Органические катионы и 1D-цепочки по отдельности образуют два типа слоев (рис. S4 ).
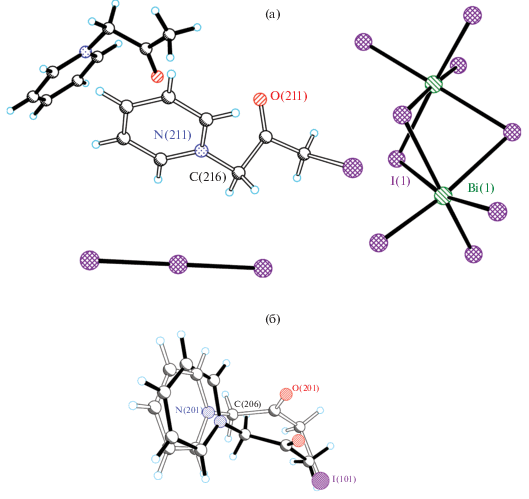
При взаимодействии хлорида N-ацетонилпиридиния с водным раствором Bi(NO3)3/KI получено соединение [1-(CH2C(O)CH3)Py]4[Bi4I16] (III). Соединение III содержит катионы [1-(CH2C(O)CH3)Py]+ и центросимметричные анионы [Bi4I16]4– (рис. 3). Контакт I…I (3.79 Å) объединяет анионы в 1D-цепь (рис. S5 ).
Использование вместо хлорида бромида N-ацетонилпиридиния приводит к образованию темно-красных кристаллов фазы [1-(CH2C(O)CH3)Py]3[1-(CH2C(O)CH2I)Py][Bi2I9]I3 (IV) наряду с продуктом III. Присутствие катиона [1-(CH2C(O)CH2I)Py]+ в структуре IV обусловлено наличием примеси бромида ω-бромоацетонилпиридиния в исходном бромиде N-ацетонилпиридиния, использованном для синтеза. Среди семи структурных единиц в IV (четыре кристаллографически независимых катиона [1-(CH2C(O)CH3)Py]+ и [1-(CH2C(O)CH2I)Py]+, два аниона ${\text{I}}_{3}^{ - }$ и анион [Bi2I9]3–) упорядочены лишь один [1-(CH2C(O)CH3)Py]+ и [Bi2I9], в центросимметричных анионах I3 концевые атомы I разупорядочены по двум позициям (заселенность позиций 0.18 и 0.82), в двух из трех смешанных позиций [1-(CH2C(O)CH3)Py] + [1-(CH2C(O)CH2I)Py] атомы I разупорядочены по двум позициям (рис. 4).
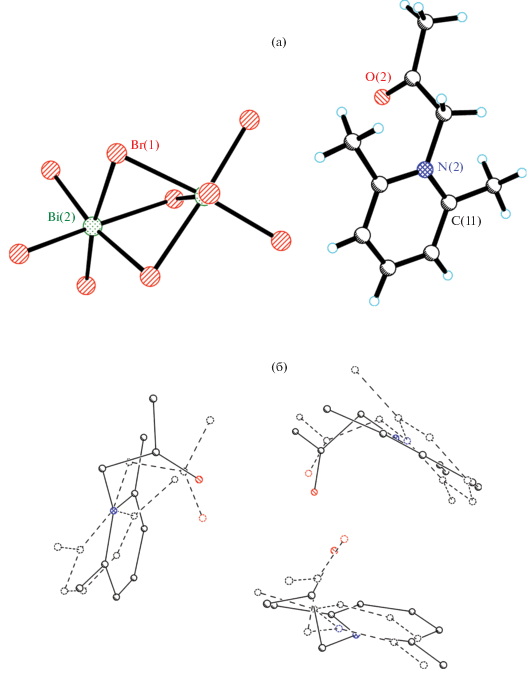
Взаимодействием бромида N-ацетонил-2,6-диметилпиридиния с водным раствором Bi(NO3)3/KBr получена кристаллическая смесь, содержащая две полиморфные структуры бромовисмутата [1-(CH2C(O)CH3)-2,6-CH3Py]3[Bi2Br9] (V, темно-желтые блоки) и (VI, светло-желтые иголки). Структуры соединений V и VI образованы катионами [1-(CH2C(O)CH3)-2,6-CH3Py] и анионами [Bi2Br9]3– (рис. 5а). В обеих структурах можно выделить близко расположенные друг к другу три катиона (рис. 5б). Взаимное расположение анионов в полиморфах различно: в V атомы I(7), связанные между собой центром инверсии, образуют короткий контакт 3.52 Å (рис. S6 ), кратчайшее расстояние I…I между атомами I соседних анионов в VI составляет 4.84 Å. Объем элементарных ячеек полиморфов V и VI отличается примерно на 2% (4615.8 и 4726.4 Å3, пр. гр. для обоих полиморфов P21/n, Z = 4).
Рис. 5.
Фрагмент структуры V (а) и иллюстрация наложения фрагментов [1-(CH2C(O)CH3)-2,6-CH3Py]3 из структур V и VI (б).
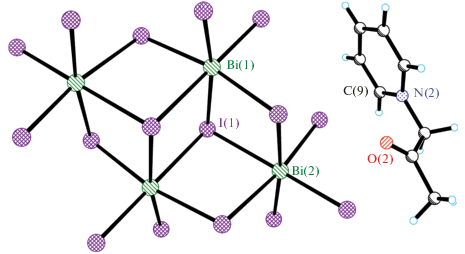
Иодовисмутат N-ацетонил-2,6-диметилпиридиния [1-(CH2C(O)CH3)-2,6-CH3Py]4[Bi4I16] ⋅ 0.69I2 (VII) получен взаимодействием водных растворов N-ацетонил-2,6-диметилпиридиния и Bi(NO3)3/KI на воздухе. Значение оптической ширины запрещенной зоны VII составляет 2.08 эВ (рис. S8 с). В структуре VII один из двух кристаллографически независимых катионов [1-(CH2C(O)CH3)-2,6-CH3Py] разупорядочен по двум позициям, анион [Bi4I16]4– и молекула I2 расположены в центрах инверсии (рис. 6), заселенность позиции I2 составляет 0.69. Короткие контакты I…I (3.68 Å) между молекулой I2 (длина связи 2.782(4) Å) и анионом образуют цепь [Bi4I16]…I2…[Bi4I16] (рис. S7 ). В табл. S2 приведены расстояния I…I в 10 структурах с фрагментом M–I…I2…I–M. Широкий интервал расстояний I…I (3.24–3.62 Å) с учетом того, что расстояние I–I в центральном фрагменте варьируется гораздо в меньших пределах (2.73–2.81 Å), указывает на то, что не существует четкой границы между ассоциатом (I…I2…I)2– и анионом ${\text{I}}_{4}^{{2 - }}$. Для сравнения в некоординированном анионе ${\text{I}}_{4}^{{2 - }}$ кратчайшее расстояние (CCDC версия 5.41, ноябрь 2019 [25]) с участием терминальных атомов I составляет 3.12 Å, а в центральном фрагменте – 2.75 Å [26]. Подробно строение некоординированного аниона ${\text{I}}_{4}^{{2 - }}$ рассмотрено в [27].
ЗАКЛЮЧЕНИЕ
Рассмотрено семь новых гибридных галовисмутатов N-ацетонилпиридиния, N-(ω-иодоацетонил)пиридиния и N-ацетонил-2,6-диметилпиридиния. В структуре II обнаружен новый тип 1D-цепей {K[BiBr6]$\} _{n}^{{2n - }}$, образованных анионами [BiBr6]3– и катионами K+. По строению эти цепи близки к ранее описанным цепям {K[Bi2Br11]$\} _{n}^{{4n - }}$ [16] и островным ассоциатам {K[BiI6]2}5– [28]. Во всех случаях катион калия координирован шестью атомами галогенов. В структуре VII молекулы I2 и анионы [Bi4I16]4– также образуют 1D-цепи. Подобные соединения стали объектом подробного изучения после публикации работы [29]. Формально могут быть выделены цепи анионов и в структурах I и III. Значения оптической ширины запрещенной зоны полученных соединений (как 0D, так и 1D) имеют высокие значения, характерные для островных галовисмутатов. Отсутствие уникального сочетания свойств, присущих гибридным галоплюмбатам со структурой перовскита [30–32] (кубическая сингония кристалла, низкие значения Eg, образование непрерывной серии твердых растворов), делает их малоперспективными для использования в солнечной энергетике. Несмотря на наличие полярных карбонильных групп, ни в одном из выделенных соединений I–VII образование прочных водородных связей (<2.15 Å) не наблюдалось, что, по-видимому, и обусловило близость свойств полученных соединений с ранее охарактеризованными островными галовисмутатами.
Список литературы
Hoefler S.F., Trimmel G., Rath T. // Monatsh. Chem. 2017. V. 148. № 5. P. 795. https://doi.org/10.1007/s00706-017-1933-9
Bi W.H., Leblanc N., Mercier N. et al. // Chem. Mater. 2009. V. 21. № 18. P. 4099. https://doi.org/10.1021/cm9016003
Leblanc N., Allain M., Mercier N. et al. // Cryst. Growth Des. 2011. V. 11. № 6. P. 2064. https://doi.org/10.1021/cg2003244
Chen Y., Yang Z., Guo C.X. et al. // Eur. J. Inorg. Chem. 2010. № 33. P. 5326. https://doi.org/10.1002/ejic.201000755
Adonin S.A., Gorokh I.D., Novikov A.S. et al. // Chem. Eur. J. 2017. V. 23. № 62. P. 15612. https://doi.org/10.1002/chem.201703747
Kotov V.Y., Ilyukhin A.B., Korlyukov A.A. et al. // New J. Chem. 2018. V. 42. № 8. P. 6354. https://doi.org/10.1039/c7nj04948j
Usoltsev A.N., Elshobaki M., Adonin S.A. et al. // J. Mater. Chem. A. 2019. V. 7. № 11. P. 5957. https://doi.org/10.1039/C8TA09204D
Zhang Z., Li X.W., Xia X.H. et al. // J. Phys. Chem. Lett. 2017. V. 8. № 17. P. 4300. https://doi.org/10.1021/acs.jpclett.7b01952
Park B.-W., Philippe B., Zhang X. et al. // Adv. Mater. 2015. V. 27. № 43. P. 6806. https://doi.org/10.1002/adma.201501978
Wang Y.-L., Chen X.-H., Shu W. et al. // J. Coord. Chem. 2019. V. 72. № 4. P. 573. https://doi.org/10.1080/00958972.2019.1570167
Wang P., Sheng W.-W., Chen Z.-R. et al. // J. Cluster Sci. 2020. https://doi.org/10.1007/s10876-020-01829-0
Leblanc N., Mercier N., Zorina L. et al. // J. Am. Chem. Soc. 2011. V. 133. № 38. P. 14924. https://doi.org/10.1021/ja206171s
Mencel K., Starynowicz P., Siczek M. et al. // Dalton Trans. 2019. V. 48. № 39. P. 14829. https://doi.org/10.1039/C9DT02916H
Jakubas R., Gągor A., Winiarski M.J. et al. // Inorg. Chem. 2020. V. 59. № 6. P. 3417. https://doi.org/10.1021/acs.inorgchem.9b03193
Jakubas R., Rok M., Mencel K. et al. // Inorg. Chem. Front. 2020. V. 7. № 10. P. 2107. https://doi.org/10.1039/D0QI00265
Buikin P.A., Rudenko A.Y., Baranchikov A.E. et al. // Russ. J. Coord. Chem. 2018. V. 44. № 6. P. 373. https://doi.org/10.1134/s1070328418060015
Buikin P., Rudenko A.Y., Ilyukhin A. et al. // Russ. J. Coord. Chem. 2020. V. 46. № 2. P. 111. https://doi.org/10.1134/S1070328420020049
Groom C.R., Bruno I.J., Lightfoot M.P. et al. // Acta Crystallogr., Sect. B. 2016. V. 72. № 2. P. 171. https://doi.org/10.1107/S2052520616003954
Peng Y., Lu S.-F., Wu D.-X. et al. // Acta Crystallogr., Sect. C: Cryst. Struct. Commun. 2000. V. 56. № 5. P. 183. https://doi.org/10.1107/S0108270100005230
Bruker // APEX3 and SAINT, Bruker AXS Inc., Madison, Wisconsin, USA, 2016.
Sheldrick G.M. // SADABS, Göttingen (Germany): Univ. of Göttingen, 1997.
Sheldrick G.M. // Acta Crystallogr., Sect. C. 2015. V. 71. P. 3. https://doi.org/10.1107/s2053229614024218
Caelho A. // TOPAS 4.2, Bruker AXS GmbH, Karlsruhe, Germany, 2009.
Kubelka P., Munk F. // Z. Tech. Phys. 1931. V. 12. P. 593.
Groom C.R., Allen F.H. // Angew. Chem. Int. Ed. 2014. V. 53. № 3. P. 662. https://doi.org/10.1002/anie.201306438
Megen M., Jablonka A., Reiss G.J. // Z. Naturforsch. B. 2014. V. 69. № 7. P. 753. https://doi.org/10.5560/znb.2014-4088
Grześkiewicz A.M., Kubicki M. // New J. Chem. 2018. V. 42. № 13. P. 10661. https://doi.org/10.1039/C8NJ00737C
Kotov V.Y., Ilyukhin A.B., Buikin P.A. et al. // Mendeleev Commun. 2019. V. 29. № 5. P. 537. https://doi.org/10.1016/j.mencom.2019.09.020
Shestimerova T.A., Golubev N.A., Yelavik N.A. et al. // Cryst. Growth Des. 2018. V. 18. № 4. P. 2572. https://doi.org/10.1021/acs.cgd.8b00179
Nakamura Y., Shibayama N., Hori A. et al. // Inorg. Chem. 2020. V. 59. № 10. P. 6709. https://doi.org/10.1021/acs.inorgchem.9b03421
Franz A., Tobbens D.M., Steckhan J. et al. // Acta Crystallogr., Sect. B. 2018. V. 74. № 5. P. 445. https://doi.org/10.1107/S2052520618010764
Askar A.M.M.S. Study of Methylammonium Lead Triiodide Intrinsic Stability and Solid-Solution behaviour in Mixed Halide Perovskite Systems, 2018. https://doi.org/10.7939/R3FT8F13G
Дополнительные материалы
- скачать ESM.docx
- Table S1. Crystal data and structure refinement for I-VII. 2
Table S2. Interatomic distances I…I in fragment M-I…I2…I-M. 4
Fig. S1. Stacking interactions in the structure I 5
Fig. S2. 1D anionic chain [Bi2Br10]4- in structure I 5
Fig. S3-S4. Projections of I and II along c axis 6
Fig. S5-S7. Anionic fragments in structures III, V and VII 8
Fig. S8. Diffuse reflectance spectra of I and VII. 9
Fig. S9. X-ray Rietveld refinement profiles for I, III and VII 10
Fig. S10. XRD patterns of V and VI mixture 11
Инструменты
Журнал неорганической химии