Журнал неорганической химии, 2023, T. 68, № 8, стр. 1011-1020
Применение анионообменного осаждения для получения нанопорошка феррита никеля, модифицированного плазмонными частицами
С. В. Сайкова a, b, *, Д. И. Немкова b, Е. В. Пикурова a, b, А. С. Самойло b
a Институт химии и химической технологии СО РАН – обособленное подразделение
ФИЦ КНЦ СО РАН
660036 Академгородок, 50/24, Красноярск, Россия
b Сибирский федеральный университет
660041 Красноярск, Свободный пр-т, 79, Россия
* E-mail: ssai@mail.ru
Поступила в редакцию 08.02.2023
После доработки 13.03.2023
Принята к публикации 23.03.2023
- EDN: MKWNNB
- DOI: 10.31857/S0044457X23600160
Аннотация
Магнитные гибридные наночастицы на основе феррита никеля и золота являются перспективными материалами для использования в медицине, микроэлектронике и плазмонно-усиленном фотокатализе. Каталитическая активность применяемых гибридных материалов зависит от состава, морфологии, поверхностного заряда и размера магнитного ядра. В настоящей работе для синтеза наноструктурированного порошка NiFe2O4 используется анионообменное соосаждение железа и никеля с последующей термической обработкой полученных гидроксидов. Методом дробного факторного эксперимента (ДФЭ 27-4) исследовано влияние реакционных параметров на процесс формирования NiFe2O4. В найденных оптимальных условиях синтезированы порошки со средним размером кристаллитов 22.7 ± 1.0 нм. Прямым восстановлением золота аминокислотой – метионином – получены гибридные частицы NiFe2O4/Au, формирование которых доказано методами оптической спектроскопии, просвечивающей электронной микроскопии, рентгенофотоэлектронной спектроскопии.
ВВЕДЕНИЕ
В последнее десятилетие стремительно развиваются исследования в области получения гибридных наночастиц, являющихся комбинацией различных по составу и типу наноструктур. Интерес к таким веществам определяется свойствами и функциями, которые приобретает гибридный материал в результате объединения исходных компонентов. Подобные наночастицы незаменимы в биологии и медицине, сенсорных технологиях, “зеленой химии”, микроэлектронике и особенно в катализе. Золотосодержащие катализаторы широко применяются в органическом синтезе, для очистки воздуха и водорода в топливных элементах, а также для деградации органических веществ до безвредных продуктов (СO2 и Н2O) в мягких условиях [1–3].
Получение магнитных гибридных наночастиц, содержащих золото, открывает обширные возможности их использования благодаря комбинации биосовместимости и магнитных свойств. Такие частицы могут контролироваться внешним магнитным полем, что обеспечивает легкое отделение материала от реакционной смеси. Кроме того, магнитные наночастицы, покрытые золотой оболочкой, являются перспективными материалами для разработки селективных МРТ-контрастирующих агентов, направленной доставки лекарств, магнитной гипертермии, биосенсоров и др. [4, 5]. Каталитическую активность магнитных гибридных наночастиц исследовали в работах [6–9], в частности, в реакциях восстановления нитроароматических соединений до аминов. Особый интерес представляют гибридные катализаторы на основе ферритов и золота, поскольку они удовлетворяют таким требованиям, как высокий коэффициент поглощения солнечного и УФ-спектров, высокая стабильность в водной среде и к солнечному излучению, низкая стоимость и безвредность. Кроме того, шпинельная структура ферритов обеспечивает “дополнительные места” для проведения каталитической реакции [10], а функционализация поверхности наночастицами золота вследствие эффекта поверхностного плазмонного резонанса смещает край поглощения в длинноволновой диапазон спектра. Все это обеспечивает повышение фотокаталитической активности материалов и эффективность разложения органических загрязнителей.
Каталитическая активность получаемых гибридных материалов зависит от состава, морфологии, поверхностного заряда и размера магнитного ядра – наночастиц феррита никеля, поэтому в ходе синтеза магнитного ядра необходимо выдерживать определенные реакционные параметры процесса и понимать, как влияют различные факторы на состав и морфологию образованных частиц.
Основными способами синтеза наночастиц феррита никеля являются твердофазный метод [11, 12], золь-гель метод [13–17], а также метод щелочного соосаждения [18–22]. Эти методы хотя и обладают вполне определенными достоинствами, имеют ряд недостатков, таких как трудоемкость и дороговизна, длительность процесса, загрязнение продуктов примесями осадителя, а также сложность контроля размера получаемых частиц.
В настоящей работе для синтеза наноразмерных ядер NiFe2O4 использовали анионообменное соосаждение железа и никеля [23] с последующей термической обработкой полученных гидроксидов. Этот метод заключается в обмене анионами между раствором и ионитом в ОН-форме и осаждении гидроксидов из раствора. Осаждение проводят при комнатной температуре и давлении окружающей среды в стабильных условиях при постоянном уровне pH. Данный способ позволяет получать однородные по составу, размерам и морфологии частицы, также не содержащие примесей и поэтому не требующие повторных операций промывки и очистки [24–26]. Анионообменное соосаждение устраняет необходимость в дорогостоящем оборудовании, обеспечивает высокий выход продуктов и низкие затраты, экономию времени и энергии.
Цель данной работы – подбор оптимальных условий анионообменного осаждения для получения феррита никеля, модифицированного плазмонными частицами (NiFe2O4/Au).
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
В работе использовали следующие реактивы: декстран-40 (молярная масса 40 000 Да, PanReac AppliChem), соли металлов (х. ч., Химреактивснаб) Ni(NO3)2 ⋅ 6H2O, Fe(NO3)3 ⋅ 9H2O, FeCl3 ⋅ 6H2O, NiCl2 ⋅ 6H2O. Применяли также гелевый анионит АВ-17-8 (ГОСТ 20301-74, ПАО “АЗОТ”), содержащий в качестве ионогенных групп четвертичные триметиламмониевые группы, и полифункциональный анионит конденсационного типа АВ-16ГС (ГОСТ 20301-74, Химреактивснаб), содержащий вторичные и третичные аминогруппы алифатического ряда и пиридиниевые группы. Все аниониты были переведены в ОН-форму, для чего исходный сорбент в хлоридной форме отмывали от мономеров 1 М раствором NaCl (т : ж = 1 : 3), обрабатывали 5–6 раз 2 М NаОН (т : ж = 1 : 3) по 1 ч, промывали водой до рН 6–7 и высушивали при температуре 60°С. Полная обменная емкость анионитов в OH-форме, установленная по 0.1 М раствору HCl [21], составила 1.5 ммоль экв/г для АВ-17-8 и 1.3 ммоль экв/мл для АВ-16ГС.
Для получения наночастиц феррита никеля рассчитанное количество анионита (с учетом отношения числа эквивалентов ОН-ионов в навеске ионита к общему числу эквивалентов металлов – k) приводили в контакт со смесью 0.16 M растворов хлоридов или нитратов никеля и железа(III), взятых в стехиометрическом соотношении (в некоторых опытах к растворам добавляли 3 г декстрана-40), и перемешивали на шейкере 1.5–3 ч со скоростью 120 мин–1 при температуре 25–60°С. Условия опытов приведены в табл. 1, 2. Знак “+” в матрице планирования эксперимента (табл. 2) соответствует верхнему уровню варьирования данного фактора, указанному в табл. 1, знак “–” – нижнему уровню варьирования. Анионит отделяли, пропуская смесь через сито с диаметром отверстий 0.16 мм, и трижды элюировали 0.1 М HCl (каждая порция – 20 мл). Осадок после центрифугирования (6000 об/мин) высушивали в течение 2 ч при температуре 80°С и прокаливали 3 ч при 650°С. В некоторых опытах для повышения скорости отслаивания поверхностного осадка, фиксированного на зерне анионита [25], и увеличения выхода продукта перед отделением анионита проводили дополнительную стадию охлаждения реакционной смеси на ледяной бане до 10°С.
Таблица 1.
Значения независимых переменных
| Параметр | Х1, анионит | X2, T, °C | X3, декстран-40 | X4, отношение k* | X5, состав раствора | X6, стадия охлаждения | X7, время, ч |
|---|---|---|---|---|---|---|---|
| Верхний уровень варьирования | АВ-16ГС | 25 | Есть | 1.2 | FeСl3 + NiCl2 | Есть | 1.5 |
| Нижний уровень варьирования | АВ-16-8 | 60 | Нет | 0.8 | Fe(NO3)3 + Ni(NO3)2 | Нет | 3.0 |
* $k = \frac{{\bar {n}({\text{O}}{{{\text{H}}}^{ - }})}}{{n({\text{F}}{{{\text{e}}}^{{3 + }}} + {\text{N}}{{{\text{i}}}^{{2 + }}})}}{\text{, где }}\bar {n}({\text{O}}{{{\text{H}}}^{ - }})$ – количество эквивалентов ОН-ионов в навеске ионита, $n({\text{F}}{{{\text{e}}}^{{3 + }}} + {\text{N}}{{{\text{i}}}^{{2 + }}})$ – общее число эквивалентов металлов.
Таблица 2.
Матрица планирования эксперимента ДФЭ 27-4
| № опыта | X0 | X1 | X2 | X3 | X4 | X5 | X6 | X7 |
|---|---|---|---|---|---|---|---|---|
| 1 | + | – | – | – | + | + | + | – |
| 2 | + | + | – | – | – | – | + | + |
| 3 | + | – | + | – | – | + | – | + |
| 4 | + | + | + | – | + | – | – | – |
| 5 | + | – | – | + | + | – | – | + |
| 6 | + | + | – | + | – | + | – | – |
| 7 | + | – | + | + | – | – | + | – |
| 8 | + | + | + | + | + | + | + | + |
Для получения гибридных наночастиц NiFe2O4/Au использовали модифицированную методику [27]: к 25 мг добавляли 20 мл 0.03 М раствора аминокислоты (α-амино-γ-метилтиомасляной кислоты (метионин)) и 1 мл 0.1 М HAuCl4, доводили pH до 10 и оставляли перемешиваться 4 ч при температуре 37°С [27, 28]. Покрытые частицы отделяли методом магнитной сепарации при действии постоянного магнитного поля, промывали, высушивали при 60°С и исследовали физическими методами.
Термический анализ проводили на синхронном термическом анализаторе SDT Q600, совмещенном с ИК-Фурье-спектрометром Nicolet 380 с интерфейсом TGA/FT-IR (приставка для анализа газовой фазы). Съемку термограмм осуществляли при нагревании со скоростью 20 град/мин в атмосфере воздуха, скорость продувки воздуха составляла 50 мл/мин.
Фазовый состав образцов определяли методом рентгенофазового анализа на дифрактометре Shimadzu XDR-600 в СuKα-излучении, идентификацию фаз осуществляли с помощью картотеки базы данных Объединенного комитета по стандартам в порошковой дифракции Joint Committee on Powder Diffraction Standards (JCPDS).
Химический состав продуктов анионообменного осаждения устанавливали методом атомно-абсорбционной спектрометрии (AAS Perkin Elmer AAnalyst 400).
Гидродинамический диаметр и ζ-потенциал частиц определяли методом динамического рассеяния света с использованием прибора Zetasizer NanoZS (Malvern Instruments) на длине волны лазерного излучения 632.8 нм и угле рассеяния 173°. Навески порошков феррита никеля (0.01 г) диспергировали в 5 мл дистиллированной воды при обработке ультразвуком (ультразвуковая ванна “Сапфир”, мощность – 50 Вт, рабочая частота – 35 кГц) в течение 10 мин. Образец полученного гидрозоля (1 мл) переносили в пластиковую кювету (l = 1 см) для измерения.
Микрофотографии и рентгеновские карты распределения элементов в образце получали на электронном микроскопе Hitachi 7700М при ускоряющем напряжении 100–110 кВ.
РФЭ-спектры регистрировали на спектрометре SPECS (SPECS Gmbh), оснащенном полусферическим электронным анализатором PHOIBOS 150-МКД-9, при возбуждении монохроматическим излучением AlKα (E = 1486.6 эВ). Энергия прохождения анализатора составляла 10 эВ для сканирования с высоким разрешением и 20 эВ для обзорных спектров. Для устранения неоднородного электростатического заряда образцов применяли электронную пушку, в качестве эталона использовали пик C1s при 284.45 эВ.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Оптимизация условий получения наночастиц феррита никеля
Анионообменное соосаждение ионов железа(III) и никеля(II) анионитом в ОН-форме [29, 30] может быть представлено реакцией:
(1)
$\begin{gathered} 8{\text{RОН + Ni}}{{{\text{A}}}_{{\text{2}}}}{\text{ + 2Fe}}{{{\text{A}}}_{3}} \to 8{\text{RA + }} \\ {\text{ + Ni}}{{\left( {{\text{ОН}}} \right)}_{2}}{\kern 1pt} \downarrow + {\text{ }}2{\text{Fe}}{{\left( {{\text{ОН}}} \right)}_{3}}{\kern 1pt} \downarrow , \\ \end{gathered} $В ходе анионообменного соосаждения анионит поглощает анионы используемых солей, что способствует как смещению равновесия процесса и, соответственно, повышению степени осаждения, так и упрощению процедуры синтеза за счет исключения стадии промывки осадка. Получаемый продукт не содержит примесей исходных веществ и является однородным по морфологии, размеру и свойствам [31, 32].
Исследование влияния условий процесса анионообменного соосаждения на формирование фазы феррита никеля проводили с использованием метода дробного факторного эксперимента (ДФЭ) 27-4 [33]. На основании анализа литературных данных и предварительных опытов были выбраны факторы, влияющие на формирование наночастиц феррита никеля (табл. 1). С целью стабилизации коллоидной системы и снижения доли поверхностного осадка на зерне анионита процесс проводили в присутствии полисахарида декстрана-40 (фактор X3), а также использовали дополнительную стадию охлаждения системы до 10°С (фактор X6). Эффективность такого подхода была показана нами ранее [25, 34].
В работе использовали матрицу планирования ДФЭ 27-4 (табл. 2). Обработку результатов проводили в соответствии с работой [33]. В качестве целевой функции модели была выбрана мольная доля фазы феррита никеля, определенная методом рентгенофазового анализа (p, %).
При реализации ДФЭ проведены две серии из восьми опытов и определено количество никеля и железа в реагирующих фазах: контактных растворах, осадках, элюатах. На основании полученных данных рассчитана молярная доля металлов в фазе ионита (χ, %), установлено мольное соотношение ионов никеля и железа в продукте осаждения (стехиометрическое отношение Ni/Fe = 0.5), выход продукта (отношение числа молей металлов в осадке к их начальному количеству – η, %) и доля фазы NiFe2O4 в полученном после прокаливания образце (p, %). Кроме того, из данных рентгенофазового анализа по формуле Шеррера рассчитан размер области когерентного рассеяния (d, нм). Все полученные результаты представлены в табл. 3.
Таблица 3.
Результаты реализации ДФЭ 27-4
| № | Контактный раствор | Элюаты | n(Ni)/n(Fe) | p, % | χ, % | η, % | d, нм | ||
|---|---|---|---|---|---|---|---|---|---|
| Ni, ммоль | Fe, ммоль | Ni, ммоль | Fe, ммоль | ||||||
| 1 | 0.03 | 0.00 | 0.12 | 0.25 | 0.49 | 100.0 | 7.7 | 91.7 | 17.8 |
| 2 | 0.40 | 0.10 | 0.19 | 0.10 | 0.34 | 41.5 | 6.0 | 83.6 | 30.0 |
| 3 | 0.30 | 0.04 | 0.06 | 0.13 | 0.41 | 52.4 | 3.5 | 89.0 | 29.2 |
| 4 | 0.03 | 0.00 | 0.23 | 0.11 | 0.43 | 31.3 | 7.6 | 92.3 | 18.6 |
| 5 | 0.02 | 0.00 | 0.08 | 0.18 | 0.50 | 90.5 | 5.4 | 94.2 | 18.8 |
| 6 | 0.20 | 0.04 | 0.24 | 0.12 | 0.38 | 40.6 | 7.5 | 87.5 | 32.9 |
| 7 | 0.15 | 0.01 | 0.08 | 0.15 | 0.45 | 61.0 | 5.0 | 92.0 | 27.9 |
| 8 | 0.04 | 0.03 | 0.23 | 0.12 | 0.44 | 61.0 | 7.6 | 90.9 | 33.8 |
| Δ | ±0.03 | ±0.02 | ±0.03 | ±0.02 | ±0.03 | ±1.0 | ±1.5 | ±1.8 | ±0.2 |
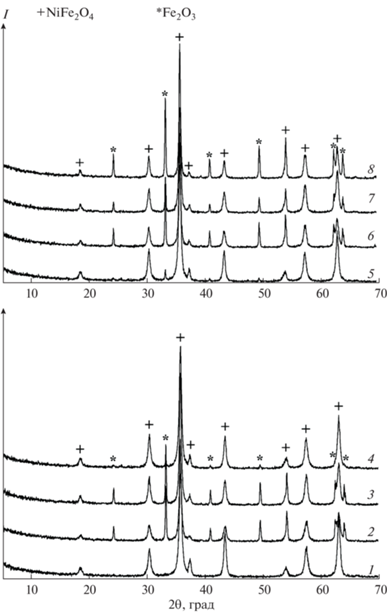
На рис. 1 приведены дифрактограммы полученных образцов для всех восьми опытов, из которых видно, что чистая фаза феррита никеля образуется только в опыте 1, в остальных образцах помимо целевого продукта присутствует гематит, что, вероятно, связано с отклонением состава прекурсоров в опытах 2–4 и 6–7 от стехиометрии, а также с преимущественным формированием менее растворимого гидроксида железа в начале процесса диффузии ОН-ионов из гранул анионита в раствор. Другой причиной такого отклонения является неполное осаждение ионов никеля, что связано с нехваткой количества анионита (фактор X4), а также с комплексообразованием (при использовании слабоосновного анионита АВ16-ГС образуются комплексные соединения никеля с его функциональными группами).
Статистический анализ результатов эксперимента проводили в программе STATISTICA DOE. Среднюю квадратичную ошибку и доверительный интервал (Δ, табл. 3) определяли при вероятности, равной 0.95. В ходе анализа подтверждена однородность выборочных дисперсий, определены коэффициенты регрессии и порог значимости коэффициентов регрессии (табл. 4).
Таблица 4.
Значения коэффициентов уравнения регрессии (значимые факторы подчеркнуты)
| Δb | b0 | b1 | b2 | b3 | b4 | b5 | b6 | b7 |
|---|---|---|---|---|---|---|---|---|
| 1.5 | 59.8 | –16.7 | –8.5 | 3.1 | 11.1 | 1.4 | 6.4 | 0.9 |
На основании полученных данных выведена математическая модель, описывающая зависимость доли фазы феррита никеля в продукте от условий проведения процесса:
(2)
$\begin{gathered} p = 59.8--16.7{{Х}_{1}}--8.5{{Х}_{2}} + \\ + \,\,3.1{{Х}_{3}} + 11.1{{Х}_{4}} + 6.4{{Х}_{6}}. \\ \end{gathered} $Видно, что на выход целевой фазы сильно влияют тип анионита (X1) и его количество (X4), менее значимыми являются температура процесса (X2), наличие декстрана-40 (X3) и проведение стадии охлаждения до 10°C (X6). Сильноосновный анионит и более высокая температура синтеза приводят к повышению степени осаждения ионов никеля, что способствует формированию осадка стехиометрического состава. В присутствии декстрана-40 происходит снижение доли поверхностного осадка, фиксированного на зерне ионита, что повышает выход продукта.
Не влияет на анионообменное осаждение природа аниона исходной соли и длительность процесса в интервале 1.5–3 ч, что говорит о его высокой скорости. В результате анализа полученной математической модели были определены оптимальные условия синтеза наночастиц феррита никеля методом анионообменного соосаждения: сильноосновный анионит АВ-17-8; декстран-40; время осаждения 1.5 ч; отношение эквивалентов ОН-групп и металлов (k), равное 1.2; температура синтеза 60°C, использование дополнительной стадии охлаждения до температуры 10°C для более полного отделения фазы осадка от зерен ионита.
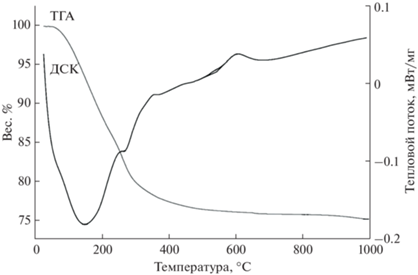
На рис. 2 приведена термограмма прекурсора образца, полученного в оптимальных условиях. На кривой ДСК наблюдается несколько тепловых эффектов, связанных с разложением исходных гидроксидов, особый интерес представляет экзоэффект с максимумом при 604.4°С, вероятно, соответствующий процессам ферритообразования и кристаллизации феррита никеля. По данным термического анализа, для термообработки выбрана температура выше точки предполагаемой кристаллизации (650°С) и время термообработки 3 ч.
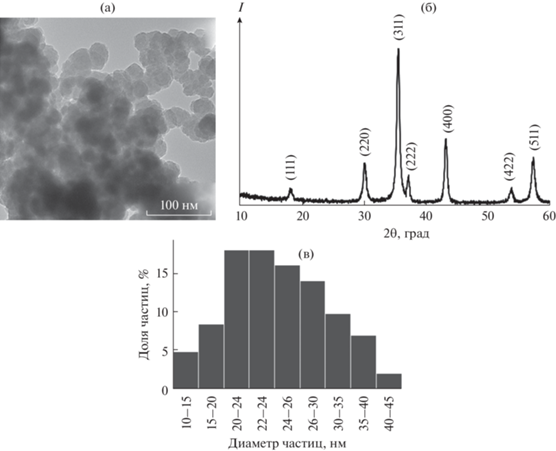
Образец, синтезированный в оптимальных условиях, представляет собой чистую фазу феррита никеля (рис. 3б) c медианным размером частиц 22.7 ± 1.0 нм (рис. 3а, 3в), что совпадает с величиной, рассчитанной по формуле Дебая–Шеррера и равной 16.4 ± 0.2 нм. Значение ζ-потенциала для полученных частиц составляет всего –0.6 мВ, поэтому они склонны к формированию агломератов: гидродинамический диаметр равен 215 ± 3 нм.
Получение гибридных частиц NiFe2O4/Au
Для осаждения золота на поверхности оксидных частиц, как правило, используют два основных метода: адсорбцию готовых зародышей золота на ядрах и прямое восстановление металла из золотохлористоводородной кислоты на поверхности частицы. Первый метод, являющийся многоступенчатым процессом, более сложен и трудоемок [35–38]. В настоящей работе для покрытия магнитных ядер золотой оболочкой выбран более простой (one-pot) метод прямого восстановления [27, 28]. В качестве восстановителя использовали α-амино-γ-метилтиомасляную кислоту (метионин), которая одновременно может выступать в качестве стабилизатора. Выбор кислоты обусловлен ее биологической совместимостью и разнообразием функциональных групп (S, NH2), которые позволяют использовать метионин в качестве так называемого “якоря”. При введении аминокислоты в золь наночастиц феррита никеля возможно ее прикрепление к поверхности магнитных ядер через NH2-группу. Дальнейшее введение в реакционную среду золотохлористоводородной кислоты приводит к восстановлению золота и его прикреплению к метионину за счет сульфидной группы последнего.
На рис. 4 приведены микрофотографии (ПЭМ) полученных частиц, поверхность некоторых из них инкрустирована золотыми зародышами (рис. 4а), размер которых варьируются от 0.5 до 7 нм. Вокруг частиц феррита заметен тонкий слой органического вещества (область более низкого контраста), вероятно, являющийся продуктом окисления метионина. Видно, что именно органический слой позволяет прикрепить частицы Au к поверхности нанокристалла. Плотность покрытия частиц феррита золотыми кластерами, определенная нами на основании анализа микрофотографий ~200 частиц, составляет 80 ± 10 нч на частицу.
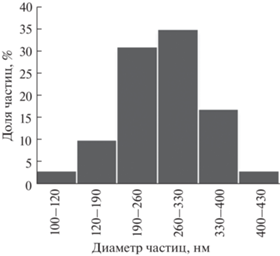
Кроме того, данные ПЭМ свидетельствуют о формировании в тех же условиях и довольно крупных (260 ± 70 нм) частиц типа ядро-оболочка NiFe2O4@Au (рис. 4б, диаграмма распределения этих частиц по размерам приведена на рис. 5), которые образовались вследствие покрытия золотом агломератов из нескольких десятков исходных наночастиц феррита никеля. Подобные агломераты мы наблюдали ранее при покрытии золотой оболочкой феррита никеля, полученного в других условиях методом щелочного соосаждения [25], но после нескольких стадий осаждения золота.
Рис. 5.
Диаграмма распределения частиц NiFe2O4@Au по размерам: а – микрофотография, б–г – рентгеновские карты распределения Ni, Au, Fe.
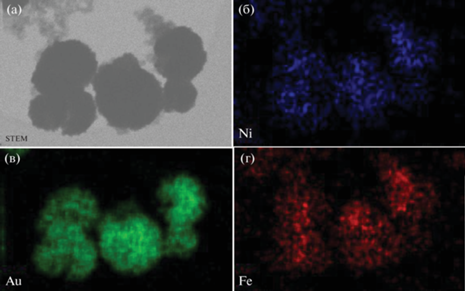
Наличие золота на поверхности феррита никеля доказано данными EDX-анализа, а также результатами РФЭС. На рис. 6 приведена рентгеновская карта распределения элементов, полученная при помощи сканирующей просвечивающей электронной микроскопии. Видно, что в одном месте пространства локализованы как ионы железа и никеля, так и атомы золота. Кроме того, высокая интенсивность сигналов золота свидетельствует о присутствии золота на поверхности полученных частиц типа ядро-оболочка.
Рис. 6.
Изображения частиц NiFe2O4@Au, полученные методом сканирующей просвечивающей электронной микроскопии: а – обзорный спектр, б – Au4f.
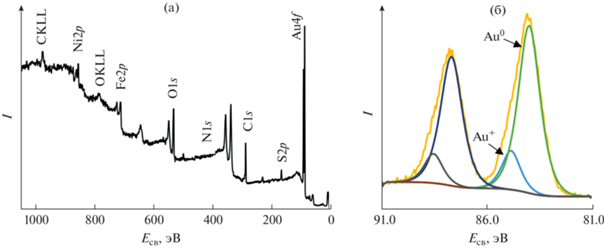
Методом РФЭС с разрешением по глубине изучено химическое состояние поверхности образцов NiFe2O4@Au. На основании анализа обзорного спектра (рис. 7а) установлено, что в нем присутствуют интенсивные линии, соответствующие Au4f, S2p, O1s и C1s, при этом линии, характерные для никеля и железа Fe2p, имеют крайне низкую интенсивность, что говорит об образовании довольно толстой золотой оболочки (>2 нм) на поверхности феррита.
Спектр золота Au4f7/2,5/2 (рис. 7б) может быть описан двумя компонентами. Основной дуплет с энергией связи пика Au4f7/2 84.1 эВ соответствует металлическому Au, компонента при 85.0 эВ обусловлена частицами Au+.
Согласно данным [39, 40], восстановление золота метионином является довольно сложным процессом, включающим образование промежуточного комплекса золота с аминокислотой и внутримолекулярный окислительно-восстановительный процесс, в результате чего образуются ионы [AuCl2]–, которые адсорбируются на поверхности феррита никеля и затем диспропорционируют на [AuCl4]– и металлическое золото. Таким образом, формирование золотой оболочки определяется адсорбцией отрицательно заряженных комплексов [AuCl4]– и [AuCl2]– на частицах феррита. ζ-Потенциал поверхности NiFe2O4, полученного анионообменным осаждением, протекающим при pH 6, в отличие от щелочного осаждения, используемого в большинстве работ [16–20, 28, 35], близок к нулю (–0.6 мВ), поэтому адсорбция комплексов золота эффективна, и уже на первой стадии синтеза образуются частицы типа ядро-оболочка.
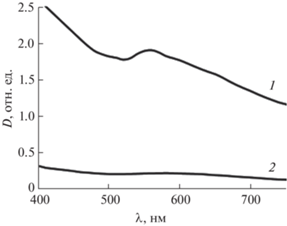
На рис. 8 приведены электронные спектры поглощения гидрозолей полученных частиц феррита никеля, записанные в интервале длин волн 400–750 нм. Кривая 1 соответствует гибридным частицам с золотом на поверхности, кривая 2 – чистому NiFe2O4. Видно, что образец с золотом на поверхности имеет максимум поглощения при 560 нм, что обусловлено поверхностным плазмонным резонансом (ППР) наночастиц золота. Согласно теории Ми–Друде [41], для изолированных НЧ Au0 размером 4–10 нм характерно положение плазмонного пика около 520 нм, однако их адсорбция на поверхности феррита приводит к “красному сдвигу” и уширению ППР [42], что обусловлено смещением поверхностной электронной плотности металла. Золото хорошо закреплено и не отделяется от магнитного ядра под действием магнитного поля, а также в ходе постсинтетической обработки. Таким образом, полученные гибридные частицы демонстрируют поглощение за пределами запрещенной зоны феррита никеля, что делает их потенциальными кандидатами для использования в плазмонно-усиленном фотокатализе. Кроме того, проведенные нами исследования магнитных свойств полученных материалов показали [28], что они сохраняются и для гибридных частиц, следовательно, их перемещением и отделением легко управлять посредством внешнего магнитного поля.
ЗАКЛЮЧЕНИЕ
В работе для получения наноструктурированных порошков феррита никеля применен метод анионообменного соосаждения железа и никеля с использованием анионита в ОН-форме. Методом математического планирования и обработки результатов ДФЭ 27-4 изучено влияние реакционных параметров и подобраны оптимальные условия синтеза наноразмерного феррита никеля. В оптимальных условиях получены частицы, представляющие собой чистую фазу феррита никеля и имеющие размер 22.7 ± 1.0 нм.
На основе полученных магнитных ядер в результате одностадийного восстановления золота метионином синтезирован гибридный материал NiFe2O4/Au, представляющий собой как наночастицы феррита, инкрустированные зародышами золота размером 0.5–7 нм, так и структуры типа ферритное ядро-золотая оболочка размером 260 ± ± 60 нм. Их состав и строение подтверждены методами рентгенофазового анализа, оптической спектроскопии, просвечивающей электронной микроскопии и рентгенофотоэлектронной спектроскопии.
Список литературы
Alyabyev S.B., Beletskaya I.P. // Russ. Chem. Rev. 2017. V. 86. P. 689. https://doi.org/10.1070/RCR4727
Redina E.A., Greish A.A., Mishin I.V. et al. // Catal. Today. 2015. V. 241. P. 246. https://doi.org/10.1016/j.cattod.2013.11.065
Кривенцов В.В., Володин А.М., Новгородов Б.Н. и др. // Химическая физика и мезоскопия. 2019. Т. 21. № 1. С. 29. https://doi.org/10.15350/17270529.2019.1.5
Ямен А., Попков В.И. // Медицина: теория и практика. 2019. Т. 4. С. 35.
Мелешко А.А., Афиногенова А.Г., Афиногенов Г.Е. и др. // Инфекция и иммунитет. 2020. Т. 10. № 4. С. 639. https://doi.org/10.15789/2220-7619-AIA-1512
Silvestri A., Mondini S., Marelli M. et al. // Langmuir. 2016. V. 32. № 28. P. 7117. https://doi.org/10.1021/acs.langmuir.6b01266
Saire-Saire S., Barbosa E.C.M., Garcia D. et al. // RSC Adv. 2019. V. 9. № 38. P. 22116. https://doi.org/10.1039/C9RA04222A
Wang X., Wang L., Lim I.-I.S. et al. // J. Nanosci. Nanotechnol. 2009. V. 9. № 5. P. 3005. https://doi.org/10.1166/jnn.2009.206
Lin F., Doong R. // Appl. Catal., A: General. 2014. V. 486. P. 32. https://doi.org/10.1016/j.apcata.2014.08.013
Dom R., Subasri R., Radha K., Borse P.H. // Solid State Commun. 2011. V. 151. P. 470. https://doi.org/10.1080/17458080.2012.690893
Peymanfar R., Ramezanalizadeh H. // Optik. 2018. V. 169. P. 424. https://doi.org/10.1016/j.ijleo.2018.05.072
Yang H., Zhang X., Weiqin A., Guanzhou Q. // Mater. Res. Bull. 2004. V. 39. № 6. P. 833.
Azizi A., Sadrnezhaad S.K. // Ceram. Int. 2010. V. 36. P. 2241. https://doi.org/10.1016/j.ceramint.2010.06.004
Lisnevskaya I.V., Bobrova I.A., Lupeiko T.G. // J. Magn. Magn. Mater. 2016. V. 37. P. 86. https://doi.org/10.1016/j.jmmm.2015.08.084
Лисневская И.В., Боброва И.А., Петрова А.В., Лупейко Т.Г. // Журн. неорган. химии. 2012. Т. 57. С. 535.
Sivakumar P., Ramesh R., Ramanand A. et al. // Mater. Res. Bull. 2011. V. 46. P. 2208.
Mana R., Raguram T., Rajni K.S. // Mater. Today: Proc. 2019. V. 18. P. 1753.
Chen D.H., He X.R. // Mater. Res. Bull. 2001. V. 36. P. 1369. https://doi.org/10.1016/S0025-5408(01)00620-1
Hassan A., Khan M.A., Shahid M. et al. // J. Magn. Magn. Mater. 2015. V. 393. P. 56. https://doi.org/10.1016/j.jmmm.2015.05.033
Velmurugan K., Venkatachalapathy V.S.K., Sendhilnathan S. // Mater. Res. 2010. V. 13 P. 299. https://doi.org/10.1590/S1516-14392010000300005
Gadkari A.B., Shinde T.J., Vasambekar P.N. // J. Mater. Sci.: Mater. Electron. 2010. V. 21. P. 96. https://doi.org/10.1007/s10854-009-9875-6
Maaz K., Karim S., Mumtaz A. et al. // J. Magn. Magn. Mater. 2009. V. 321. P. 1838. https://doi.org/10.1016/j.jmmm.2008.11.098
Пат. РФ RU 2771498. Опубл. 05.05.2022.
Pashkov G.L., Saikova S.V., Panteleeva M.V. // Theor. Found. Chem. Eng. 2016. V. 50. № 4. P. 575. https://doi.org/10.1134/S0040579516040254
Сайкова С.В., Киршнева Е.А., Пантелеева М.В. и др. // Журн. неорган. химии. 2019. Т. 64. № 10. С. 1013.
Сайкова С.В., Киршнева Е.А., Фадеева Н.П. и др. // Журн. неорган. химии. 2022. Т. 67. № 2. С. 158.
Mikalauskaite A., Kondrotas R., Niaura G., Jagminas A. // J. Phys. Chem. 2015. V. 119. P. 17398. https://doi.org/10.1021/acs.jpcc.5b03528
Saykova D., Saikova S., Mikhlin Yu. et al. // Metals. 2020. V. 10. P. 1075. https://doi.org/10.3390/met10081075
Saikova S., Pavlikov A., Trofimova T. et al. // Metals. 2020. V. 11. № 5. https://doi.org/10.3390/met11050705
Сайкова С.В., Пашков Г.Л., Пантелеева М.В. Реакционно-ионообменные процессы извлечения цветных металлов и синтеза дисперсных материалов. Красноярск: Сиб. Федер. ун-т, 2018. 198 с.
Вулих А.И. Ионообменный синтез. М.: Химия, 1973. 232 с.
Сайкова С.В., Пантелеева М.В., Николаева Р.Б. // Журн. прикл. химии. 2002. Т. 75. № 11. С. 1823.
Адлер Ю.П., Маркова Е.В., Грановский Ю.В. Планирование эксперимента при поиске оптимальных условий. М.: Наука, 1976 г. 280 с.
Сайкова С.В., Трофимова Т.В., Павликов А.Ю., Самойло А.С. // Журн. неорган. химии. 2020. Т. 65. № 3. С. 287.
Rio I.S.R., Rodrigues A.R.O., Rodrigues C.P. et al. // Materials. 2020. V. 13. № 4. P. 815. https://doi.org/10.3390/ma13040815
Meledandri C. J., Stolarczyk J. K., Brougham D.F. // ACS Nano. 2011. V. 5. № 3. P. 1747. https://doi.org/10.1021/nn102331c
An P., Zuo F., Li X. et al. // Nano. 2013. V. 8. № 6. P. 1350061. https://doi.org/10.1142/S1793292013500616
Stoeva S.I., Huo F., Lee J.-S., Mirkin C.A. // J. Am. Chem. Soc. 2005. V. 127. № 44. P.15362. https://doi.org/10.1021/ja055056d
Kim G., Weiss S.J., Levine R.L. // Biochim. Biophys. Acta. 2014. V. 1840. № 2. P. 901. https://doi.org/10.1016/j.bbagen.2013.04.038
Glisic B.D., Djuran M.I., Stanic Z.D., Rajkovic S. // Gold Bull. 2014. V. 47. № 2. P. 33. https://doi.org/10.1007/s13404-013-0108-7
Mie G. // Ann. Phys. 1908. V. 25. № 2. P. 377. https://doi.org/10.1002/andp.19083300302
Henglein A. // J. Phys. Chem. 1993. V. 97. № 21. P. 5451.
Дополнительные материалы отсутствуют.
Инструменты
Журнал неорганической химии