Океанология, 2020, T. 60, № 6, стр. 851-857
О трансформации химического состава морской воды при взаимодействии с терригенными аэрозолями
А. В. Савенко 1, *, В. С. Савенко 2
1 Московский государственный университет им. М.В. Ломоносова,
геологический факультет
Москва, Россия
2 Московский государственный университет им. М.В. Ломоносова,
географический факультет
Москва, Россия
* E-mail: Alla_Savenko@rambler.ru
Поступила в редакцию 02.03.2020
После доработки 10.05.2020
Принята к публикации 22.06.2020
Аннотация
Экспериментально изучена трансформация химического состава морской воды при взаимодействии с лессами – аналогом природных терригенных аэрозолей плейстоцена. Показано, что в результате этого процесса происходит изменение концентраций главных ионов (K, Ca, SO4, HCO3), биогенных элементов (Si, P) и фтора, тогда как изменение содержания хлоридов, натрия и магния не обнаружено в силу их высоких концентраций в морской воде. С увеличением массовой доли твердой фазы концентрации сульфатов и гидрокарбонатов возрастают, а калия – уменьшаются. Концентрации кальция и фтора либо увеличиваются, либо снижаются в зависимости от содержания подвижных форм этих элементов в образцах. Выделение в морскую воду кремния и фосфора имеет асимптотический предел: 2.5–3.3 мг Si/л и 0.012–0.040 мг P/л. Зависимость изменения концентраций изученных компонентов в морской воде от массовой доли твердой фазы соответствует гиперболической функции, но в области относительно небольших значений массовой доли описывается линейным уравнением, в котором величина углового коэффициента прямо пропорциональна концентрации компонента в водной вытяжке из данного образца лесса. Изменение состава морской воды при взаимодействии с лессами можно предсказывать по составу их водных вытяжек.
Терригенный осадочный материал поступает в Мировой океан из двух основных источников: с речным стоком твердых веществ и в форме аэрозолей, переносимых воздушным путем из областей с аридным и семиаридным климатом. Несмотря на то, что в настоящее время поток эолового материала по абсолютной массе примерно на порядок меньше речного стока твердых веществ, в ближайшем геологическом прошлом – в периоды похолодания и усиления оледенения – соотношение флювиального и эолового потоков вещества могло существенно смещаться в пользу последнего [8].
Экспериментально установлено, что при взаимодействии с аэрозолями происходит изменение химического состава морской воды [9–13]. Поскольку состав терригенных аэрозолей в прошлом мог существенно отличаться от наблюдаемого в современный период, трансформация состава контактирующей с ними морской воды также могла быть иной. При этом очень сложно хотя бы приближенно оценить предполагаемые различия химической трансформации морской воды. Единственный способ преодоления указанного затруднения состоит, пожалуй, в экспериментальном моделировании эоловой трансформации химического состава морской воды с использованием в качестве аналога природных аэрозолей пород доисторического возраста, которые служили источниками терригенного эолового материала. К таким породам можно отнести лессы – плейстоценовые осадочные породы покровного залегания, занимающие на суше площадь свыше 10 млн км2. Вне зависимости от принимаемого генезиса лессов (эолового, криогенного или какого-либо еще) можно считать установленным фактом их генетическую связь с областями прохладного засушливого климата (степи и полупустыни) [3, 4]. Такие климатические условия благоприятствуют ветровой эрозии, максимальное развитие которой отмечается в периоды глобального похолодания при усилении атмосферной циркуляции [8].
Цель настоящей работы состояла в экспериментальном определении количественных характеристик трансформации химического состава морской воды при ее взаимодействии с лессами, рассматриваемыми в качестве аналога природных терригенных аэрозолей плейстоцена.
МАТЕРИАЛ И МЕТОДИКА ИССЛЕДОВАНИЙ
В экспериментах использовали растертые до однородного состояния образцы лессовидного суглинка, отобранного под Ростовом-на-Дону, и лессов, взятых на Приобском плато, правобережье р. Лугост в пригороде Душанбе, а также около г. Алмалык и пос. Марджонбулак в Узбекистане.
Опыты состояли из двух серий. В первой серии определяли содержание водорастворимых солей по их переходу из образцов в дистиллированную воду при постоянной массовой доле твердой фазы m = 0.100 (или 100 г/л). Во второй серии изучали изменение состава 35‰ морской воды при ее взаимодействии с образцами лессов при разных массовых долях твердой фазы: от 0.0125 до 0.100 (12.5–100 г/л) в соответствии с методом переменных массовых отношений твердая фаза : раствор [7]. Герметично закрытые полипропиленовые емкости с суспензиями в течение 10 мес. перемешивали на шейкере по 6–8 ч в сутки до установления постоянных значений pH, после чего отфильтровывали растворы через мембранный фильтр с размером пор 0.22 мкм. В фильтрате измеряли величину pH и концентрацию фторидов методом прямой потенциометрии [6], а также содержание главных ионов (Na, K, Mg, Ca, Cl, SO4) методом капиллярного электрофореза [2], щелочности (≈HCO3) объемным титрованием и биогенных элементов (Si, P) стандартными колориметрическими методами [5]. Погрешность измерений составила ±0.005 ед. pH и ±3% для остальных компонентов.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Результаты экспериментов представлены в табл. 1. По направленности изменения концентраций растворенных форм с возрастанием массовой доли (содержания) твердой фазы в суспензии (m, г/л) изученные компоненты разделяются на 4 группы. В первую группу входят компоненты, содержащиеся в морской воде в наибольших количествах: хлориды, натрий и магний, для которых возможные изменения концентраций при контакте с лессами находятся в пределах точности измерений, не показывая зависимости от количества твердой фазы. Вторая группа объединяет компоненты, концентрации которых в морской воде возрастают при увеличении массовой доли взаимодействующих с ней лессов: сульфаты, гидрокарбонаты, кремний и фосфор, причем поступление кремния и фосфора асимптотически приближается к некоторым постоянным значениям, различным для каждого из образцов (рис. 1). К третьей группе, характеризующейся снижением концентрации в морской воде по мере увеличения массовой доли лессов, принадлежит лишь один элемент – калий (рис. 1). Наконец, четвертую группу составляют элементы, концентрации которых с возрастанием массовой доли твердой фазы для одних образцов лессов увеличиваются, а для других – уменьшаются: кальций и фтор (рис. 1).
Таблица 1.
Концентрации растворенных компонентов ([i], мг/л) и их изменение (Δ[i], мг/л) при взаимодействии лессов с дистиллированной и морской водой
| Образец | m* | pH | Na | K | Mg | Ca | Cl | SO4 | HCO3 | Si | P | F | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| [i] | Δ[i] | [i] | Δ[i] | [i] | Δ[i] | [i] | Δ[i] | [i] | Δ[i] | [i] | Δ[i] | [i] | Δ[i] | [i] | Δ[i] | [i] | Δ[i] | [i] | Δ[i] | |||
| Взаимодействие с дистиллированной водой | ||||||||||||||||||||||
| Дистиллированная вода | 0 | – | 0.1 | – | 0.2 | – | 0.1 | – | 0.5 | – | 0.2 | – | 0.1 | – | 1.8 | – | 0.01 | – | 0.0013 | – | 0.04 | – |
| Лессовидный суглинок, Ростов-на-Дону | 100 | 7.89 | 78.3 | 78.2 | 0.9 | 0.7 | 7.5 | 7.4 | 209 | 208 | 5.2 | 5.0 | 591 | 591 | 171 | 169 | 21.9 | 21.9 | 0.0360 | 0.0347 | 1.47 | 1.43 |
| Лесс, Приобское плато | 100 | 8.15 | 110 | 110 | 1.0 | 0.8 | 46.8 | 46.7 | 144 | 144 | 78.2 | 78.0 | 506 | 506 | 183 | 181 | 4.07 | 4.06 | 0.0281 | 0.0268 | 1.15 | 1.11 |
| То же, Душанбе | 100 | 8.32 | 58.7 | 58.6 | 2.3 | 2.1 | 9.7 | 9.6 | 23.1 | 22.6 | 9.8 | 9.6 | 40.6 | 40.5 | 233 | 231 | 4.63 | 4.62 | 0.0104 | 0.0091 | 3.93 | 3.89 |
| То же, Алмалык | 100 | 8.11 | 98.4 | 98.3 | 3.1 | 2.9 | 10.7 | 10.6 | 46.7 | 46.2 | 50.3 | 50.1 | 181 | 181 | 168 | 166 | 4.96 | 4.95 | 0.0116 | 0.0103 | 0.76 | 0.72 |
| То же, Марджонбулак | 100 | 8.13 | 2.7 | 2.6 | 3.0 | 2.8 | 4.1 | 4.0 | 48.6 | 48.1 | 1.2 | 1.0 | 3.9 | 3.8 | 159 | 157 | 5.59 | 5.58 | 0.0110 | 0.0097 | 0.36 | 0.32 |
| Взаимодействие с морской водой | ||||||||||||||||||||||
| Морская вода | 0 | – | 10 990 | – | 415 | – | 1324 | – | 428 | – | 19 740 | – | 2770 | – | 145 | – | 0.03 | – | 0.0017 | – | 1.29 | – |
| Лессовидный суглинок, Ростов-на-Дону | 12.5 | 7.76 | 11 020 | 30 | 386 | –29 | 1356 | 32 | 507 | 79 | 19 770 | 30 | 2834 | 64 | 153 | 8 | 9.75 | 9.72 | 0.0445 | 0.0428 | 1.39 | 0.10 |
| 25 | 7.71 | 10 960 | –30 | 362 | –53 | 1358 | 34 | 575 | 147 | 19 690 | –50 | 2895 | 125 | 160 | 15 | 11.1 | 11.1 | 0.0549 | 0.0532 | 1.48 | 0.19 | |
| 50 | 7.60 | 11 050 | 60 | 326 | –89 | 1298 | –26 | 701 | 273 | 19 730 | –10 | 3014 | 244 | 170 | 25 | 12.9 | 12.9 | 0.0616 | 0.0599 | 1.64 | 0.35 | |
| 100 | 7.42 | 10 930 | –60 | 283 | –132 | 1300 | –24 | 921 | 493 | 19 830 | 90 | 3198 | 428 | 183 | 38 | 14.6 | 14.6 | 0.0665 | 0.0648 | 1.89 | 0.60 | |
| Лесс, Приобское плато | 12.5 | 7.88 | 11 000 | 10 | 397 | –18 | 1314 | –10 | 467 | 39 | 19 690 | –50 | 2818 | 48 | 158 | 13 | 1.79 | 1.76 | 0.0269 | 0.0252 | 1.36 | 0.07 |
| 25 | 7.84 | 10 980 | –10 | 381 | –34 | 1340 | 16 | 502 | 74 | 19 770 | 30 | 2876 | 106 | 171 | 26 | 1.96 | 1.93 | 0.0330 | 0.0313 | 1.41 | 0.12 | |
| 50 | 7.78 | 10 980 | –10 | 349 | –66 | 1338 | 14 | 566 | 138 | 19 730 | –10 | 2968 | 198 | 191 | 46 | 2.17 | 2.14 | 0.0372 | 0.0355 | 1.50 | 0.21 | |
| 100 | 7.71 | 11 030 | 40 | 296 | –119 | 1307 | –17 | 662 | 234 | 19 790 | 50 | 3150 | 380 | 220 | 75 | 2.55 | 2.52 | 0.0378 | 0.0361 | 1.65 | 0.36 | |
| То же, Душанбе | 12.5 | 7.82 | 11 010 | 20 | 405 | –10 | 1343 | 19 | 415 | –13 | 19 710 | –30 | 2792 | 22 | 159 | 14 | 1.70 | 1.67 | 0.0098 | 0.0081 | 1.73 | 0.44 |
| 25 | 7.79 | 11 020 | 30 | 393 | –22 | 1300 | –24 | 408 | –20 | 19 780 | 40 | 2806 | 36 | 172 | 27 | 2.05 | 2.02 | 0.0110 | 0.0093 | 2.19 | 0.90 | |
| 50 | 7.75 | 10 950 | –40 | 376 | –39 | 1340 | 16 | 391 | –37 | 19 700 | –40 | 2844 | 74 | 195 | 50 | 2.51 | 2.48 | 0.0122 | 0.0105 | 3.03 | 1.74 | |
| 100 | 7.71 | 10 980 | –10 | 346 | –69 | 1288 | –36 | 369 | –59 | 19 770 | 30 | 2919 | 149 | 232 | 87 | 2.93 | 2.90 | 0.0134 | 0.0117 | 4.53 | 3.24 | |
| То же, Алмалык | 12.5 | 7.92 | 11 010 | 20 | 406 | –9 | 1298 | –26 | 436 | 8 | 19 750 | 10 | 2795 | 25 | 153 | 8 | 1.80 | 1.77 | 0.0101 | 0.0084 | 1.27 | –0.02 |
| 25 | 7.81 | 10 950 | –40 | 395 | –20 | 1327 | 3 | 448 | 20 | 19 760 | 20 | 2818 | 48 | 160 | 15 | 2.17 | 2.14 | 0.0113 | 0.0096 | 1.24 | –0.05 | |
| 50 | 7.72 | 10 980 | –10 | 379 | –36 | 1311 | –13 | 463 | 35 | 19 700 | –40 | 2876 | 106 | 172 | 27 | 2.48 | 2.45 | 0.0128 | 0.0111 | 1.19 | –0.10 | |
| 100 | 7.62 | 11 010 | 20 | 351 | –64 | 1340 | 16 | 491 | 63 | 19 760 | 20 | 2968 | 198 | 187 | 42 | 3.04 | 3.01 | 0.0140 | 0.0123 | 1.12 | –0.17 | |
| То же, Марджонбулак | 12.5 | 7.85 | 10 970 | –20 | 404 | –11 | 1338 | 14 | 444 | 16 | 19 750 | 10 | 2770 | 0 | 151 | 6 | 1.98 | 1.95 | 0.0098 | 0.0081 | 1.08 | –0.21 |
| 25 | 7.84 | 11 020 | 30 | 393 | –22 | 1325 | 1 | 456 | 28 | 19 700 | –40 | 2778 | 8 | 156 | 11 | 2.37 | 2.34 | 0.0110 | 0.0093 | 1.00 | –0.29 | |
| 50 | 7.80 | 10 980 | –10 | 378 | –37 | 1299 | –25 | 483 | 55 | 19 780 | 40 | 2784 | 14 | 164 | 19 | 2.72 | 2.69 | 0.0125 | 0.0108 | 0.90 | –0.39 | |
| 100 | 7.64 | 10 990 | 0 | 348 | –67 | 1320 | –4 | 519 | 91 | 19 790 | 50 | 2795 | 25 | 177 | 32 | 3.39 | 3.36 | 0.0137 | 0.0120 | 0.77 | –0.52 | |
Рис. 1.
Зависимости изменения концентраций растворенных компонентов в морской воде Δ[i]SW от массовой доли (содержания) лессов m: 1 – лессовидный суглинок, Ростов-на-Дону; 2 – лесс, Приобское плато; 3 – то же, Душанбе; 4 – то же, Алмалык; 5 – то же, Марджонбулак. Числа справа от кривых – концентрации компонентов i в водных вытяжках из соответствующих образцов лессов (${{[i]}_{{{{{\text{H}}}_{{\text{2}}}}{\text{O}}}}}$, мг/л, для Р – мкг/л).
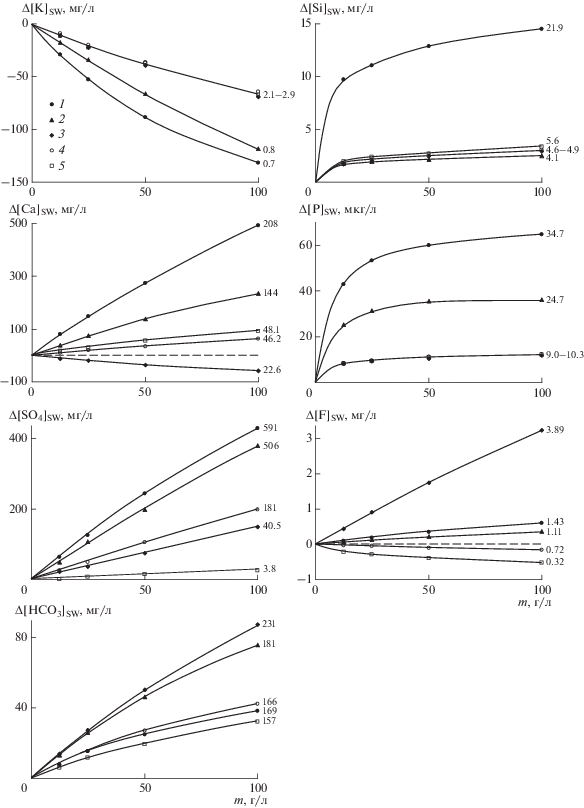
В экспериментах по взаимодействию морской воды с лессами общей чертой поведения всех подвергающихся трансформации компонентов служит близкое соответствие зависимостей изменения концентраций их растворенных форм ($\Delta {{[i]}_{{{\text{SW}}}}}$, мг/л) от содержания твердой фазы (m, г/л) гиперболической функции:
(1)
$\Delta {{[i]}_{{{\text{SW}}}}} = \frac{{{{A}_{{i({\text{SW}})}}}m}}{{1 + {{B}_{{i({\text{SW}})}}}m}},$Уравнение (1) может быть преобразовано к линейному виду
(3)
${1 \mathord{\left/ {\vphantom {1 {\Delta {\kern 1pt} {{{[i]}}_{{{\text{SW}}}}}}}} \right. \kern-0em} {\Delta {\kern 1pt} {{{[i]}}_{{{\text{SW}}}}}}} = {{a}_{i}} + {{b}_{i}}({1 \mathord{\left/ {\vphantom {1 m}} \right. \kern-0em} m}),$Таблица 2.
Численные значения параметров ai, bi и коэффициента корреляции r в уравнении (3) и параметров ${{A}_{{i({\text{SW}})}}}$ и ${{B}_{{i({\text{SW}})}}}$ в уравнении (1)
| Образец | ai | bi | r* | ${{A}_{{i({\text{SW}})}}}$ | ${{B}_{{i({\text{SW}})}}}$ |
|---|---|---|---|---|---|
| K | |||||
| Лессовидный суглинок, Ростов-на-Дону | –0.0036 | –0.387 | 0.999 | –2.58 | 0.0093 |
| Лесс, Приобское плато | –0.0014 | –0.694 | 0.999 | –1.44 | 0.0020 |
| То же, Душанбе | –0.0023 | –1.12 | 0.998 | –0.89 | 0.0021 |
| То же, Алмалык | 0.0011 | –1.40 | 0.997 | –0.71 | –0.00079 |
| То же, Марджонбулак | –0.0052 | –1.01 | 0.999 | –0.99 | 0.0051 |
| Ca | |||||
| Лессовидный суглинок, Ростов-на-Дону | 0.00062 | 0.151 | 0.999 | 6.62 | 0.0041 |
| Лесс, Приобское плато | 0.0012 | 0.306 | 0.999 | 3.27 | 0.0039 |
| То же, Душанбе | –0.011 | –0.860 | 0.990 | –1.16 | 0.013 |
| То же, Алмалык | –0.0018 | 1.48 | 0.995 | 0.68 | –0.0012 |
| То же, Марджонбулак | 0.0038 | 0.746 | 0.999 | 1.34 | 0.0051 |
| SO4 | |||||
| Лессовидный суглинок, Ростов-на-Дону | 0.00034 | 0.192 | 0.999 | 5.21 | 0.0018 |
| Лесс, Приобское плато | –0.00022 | 0.257 | 0.998 | 3.89 | –0.00086 |
| То же, Душанбе | 0.0028 | 0.546 | 0.993 | 1.83 | 0.0051 |
| То же, Алмалык | –0.00015 | 0.506 | 0.999 | 1.98 | –0.00030 |
| То же, Марджонбулак | 0.013 | 2.81 | 0.999 | 0.36 | 0.0046 |
| HCO3 | |||||
| Лессовидный суглинок, Ростов-на-Дону | 0.0096 | 1.50 | 0.998 | 0.67 | 0.0064 |
| Лесс, Приобское плато | 0.0038 | 0.894 | 0.999 | 1.12 | 0.0043 |
| То же, Душанбе | 0.0024 | 0.877 | 0.999 | 1.14 | 0.0027 |
| То же, Алмалык | 0.0067 | 1.54 | 0.999 | 0.65 | 0.0044 |
| То же, Марджонбулак | 0.0099 | 2.04 | 0.999 | 0.49 | 0.0049 |
| Si | |||||
| Лессовидный суглинок, Ростов-на-Дону | 0.067 | 0.468 | 0.974 | 2.14 | 0.14 |
| Лесс, Приобское плато | 0.40 | 2.20 | 0.936 | 0.45 | 0.18 |
| То же, Душанбе | 0.33 | 3.53 | 0.985 | 0.28 | 0.093 |
| То же, Алмалык | 0.33 | 3.09 | 0.976 | 0.32 | 0.11 |
| То же, Марджонбулак | 0.30 | 2.85 | 0.970 | 0.35 | 0.11 |
| P | |||||
| Лессовидный суглинок, Ростов-на-Дону | 14.4 | 112 | 0.999 | 0.0089 | 0.13 |
| Лесс, Приобское плато | 25.2 | 180 | 0.994 | 0.0056 | 0.14 |
| То же, Душанбе | 83.2 | 533 | 0.985 | 0.0019 | 0.16 |
| То же, Алмалык | 78.7 | 535 | 0.982 | 0.0019 | 0.15 |
| То же, Марджонбулак | 80.6 | 570 | 0.982 | 0.0018 | 0.14 |
| F | |||||
| Лессовидный суглинок, Ростов-на-Дону | 0.33 | 129 | 0.999 | 0.0078 | 0.0026 |
| Лесс, Приобское плато | 1.33 | 169 | 0.999 | 0.0059 | 0.0079 |
| То же, Душанбе | 0.011 | 28.2 | 0.999 | 0.035 | 0.00039 |
| То же, Алмалык | –1.62 | –400 | 0.999 | –0.0025 | 0.0041 |
| То же, Марджонбулак | –1.68 | –37.8 | 0.991 | –0.026 | 0.044 |
Отношение ${{{{A}_{{i({\text{SW}})}}}} \mathord{\left/ {\vphantom {{{{A}_{{i({\text{SW}})}}}} {{{B}_{{i({\text{SW}})}}}}}} \right. \kern-0em} {{{B}_{{i({\text{SW}})}}}}}$ характеризует предельное (максимально возможное) изменение концентрации компонента i в морской воде при контакте с веществом лессов:
(4)
$\Delta [i]_{{{\text{SW}}}}^{{\max }} = \frac{{{{A}_{{i({\text{SW}})}}}}}{{{{B}_{{i({\text{SW}})}}}}}.$Для зависимостей $\Delta {{[i]}_{{{\text{SW}}}}}{\kern 1pt} - {\kern 1pt} m$ на рис. 1 дополнительно приведены численные значения концентраций компонентов i в водных вытяжках из соответствующих образцов лессов (${{[i]}_{{{{{\text{H}}}_{{\text{2}}}}{\text{O}}}}}$, мг/л), которые показывают наличие связи последних с ${{A}_{{i({\text{SW}})}}}$:
(5)
${{A}_{{i({\text{SW}})}}} = {{\alpha }_{i}} + {{\beta }_{i}}{{[i]}_{{{{{\text{H}}}_{{\text{2}}}}{\text{O}}}}},$ВЫВОДЫ
1. Взаимодействие лессов с морской водой приводит к изменению концентраций компонентов основного солевого состава (калия, кальция, сульфатов, гидрокарбонатов), биогенных элементов (кремния, фосфора) и фтора. Изменение содержания хлоридов, натрия и магния не установлено в силу высоких концентраций этих элементов в морской воде. Концентрации сульфатов, гидрокарбонатов, кремния и фосфора возрастают с увеличением массовой доли твердой фазы, причем выделение в морскую воду кремния и фосфора имеет асимптотический предел: 2.5–3.3 мг Si/л и 0.012–0.040 мг P/л. Содержание калия при увеличении массовой доли твердой фазы для всех образцов лессов снижается, тогда как концентрации кальция и фтора либо увеличиваются, либо снижаются в зависимости от содержания подвижных форм этих элементов в образцах.
2. Зависимость изменения концентраций изученных компонентов в морской воде $\Delta {{[i]}_{{{\text{SW}}}}}$ от массовой доли твердой фазы m соответствует гиперболической функции, но в области относительно небольших значений m описывается линейным уравнением $\Delta {{[i]}_{{{\text{SW}}}}} = {{A}_{{i({\text{SW}})}}}m$, в котором величина углового коэффициента ${{A}_{{i({\text{SW}})}}}$ прямо пропорциональна концентрации компонента i в водной вытяжке из данного образца лесса. По результатам анализа водных вытяжек можно предсказывать изменение состава морской воды, происходящее при ее взаимодействии с лессами.
Источник финансирования. Работа выполнена при финансовой поддержке РФФИ (проект № 18-05-01133).
Список литературы
Виноградов А.П. Введение в геохимию океана. М.: Наука, 1967. 215 с.
Комарова Н.В., Каменцев Я.С. Практическое руководство по использованию систем капиллярного электрофореза “КАПЕЛЬ”. СПб.: Изд-во “Веда”, 2006. 212 с.
Конищев В.Н. Лессовые породы: новые возможности изучения их генезиса // Инженерная геология. 2015. № 5. С. 22–36.
Кригер Н.И. Лесс, его свойства и связь с географической средой. М.: Наука, 1965. 296 с.
Лурье Ю.Ю. Унифицированные методы анализа вод. М.: Химия, 1971. 375 с.
Савенко В.С. Введение в ионометрию природных вод. Л.: Гидрометеоиздат, 1986. 77 с.
Савенко В.С., Савенко А.В. Экспериментальные методы изучения низкотемпературных геохимических процессов. М.: ГЕОС, 2009. 303 с.
Broecker W.S. Abrupt climate change: Causal constraints provided by the paleoclimate record // Earth Sci. Rev. 2000. V. 51. № 1–4. P. 137–154.
Herut B., Collier R., Krom M.D. The role of dust in supplying nitrogen and phosphorus to the Southeast Mediterranean // Limnol. Oceanogr. 2002. V. 47. № 3. P. 870–878.
Maring H.B., Duce R.A. The impact of atmospheric aerosols on trace metal chemistry in open ocean surface seawater, 1. Aluminum // Earth Planet. Sci. Lett. 1987. V. 84. № 4. P. 381–392.
Nenes A., Krom M.D., Mihalopoulos N. et al. Atmospheric acidification on mineral aerosols: A source of bioavailable phosphorus for the oceans // Atmos. Chem. Phys. 2011. V. 11. № 13. P. 6265–6272.
Solmon F., Chuang P.Y., Meskhidze N., Chen Y. Acidic processing of mineral dust iron by anthropogenic compounds over the north Pacific Ocean // J. Geophys. Res. Atmos. 2009. V. 114. № D2. D02305. P. 1–20.
Thuróczy C.-E., Boye M., Losno R. Dissolution of cobalt and zinc from natural and anthropogenic dusts in seawater // Biogeosciences. 2010. V. 7. № 6. P. 1927–1936.
Дополнительные материалы отсутствуют.


