Океанология, 2022, T. 62, № 6, стр. 878-886
Растворенное органическое вещество поверхностного слоя воды Геленджикской бухты в сентябре 2021 года по данным флуориметрии и лидарных измерений
А. Н. Дроздова 1, *, В. В. Пелевин 1, И. Н. Крылов 1, 2, Е. А. Стрельцова 1, Б. В. Коновалов 1
1 Институт океанологии им. П.П. Ширшова РАН
Москва, Россия
2 Химический факультет МГУ им. М.В. Ломоносова
Москва, Россия
* E-mail: adrozdova@ocean.ru
Поступила в редакцию 23.11.21
После доработки 12.01.22
Принята к публикации 28.04.22
- EDN: QHAXHJ
- DOI: 10.31857/S003015742206003X
Аннотация
Представлены результаты исследования органического вещества поверхностного слоя воды Геленджикской бухты Черного моря и прилегающих районов оптическими методами. Показана эффективность дистанционного лазерного зондирования для определения релевантной сетки станций для пробоотбора. Установлен незначительный вклад терригенного растворенного органического вещества (РОВ). Небольшое увеличение концентрации гуминовых веществ наблюдалось в районе выноса реки Су-Аран. Максимальное содержание биолабильного РОВ характерно для прибрежных станций в Геленджикской бухте. В восточной части бухты, в районе главного городского причала, зафиксированы высокие содержания РОВ, взвешенного органического вещества, а также максимальное содержание растворенного и взвешенного органического вещества в совокупности по данным флуоресцентного лидара.
ВВЕДЕНИЕ
Растворенное органическое вещество (РОВ) является неотъемлемой частью морских экосистем и важным компонентом цикла углерода [5, 6]. Так, например, оно имеет особое значение для повышения эффективности морской пищевой сети, возвращаясь на более высокие трофические уровни за счет включения в бактериальную биомассу (микробная петля), участвует в процессах переноса ряда элементов в составе металлоорганических комплексов [13], уменьшает негативное влияние ультрафиолетового излучения на популяции фитопланктона [7]. Состав и содержание РОВ во многом определяют процессы, протекающие в экосистемах, и являются поэтому перспективными индикаторами биогеохимических изменений, связанных с антропогенной нагрузкой, изменением климата или другими факторами [13].
Одним из перспективных методов оценки содержания органического вещества (ОВ), обеспечивающих высокое пространственное разрешение, является лидарная съемка [19]. Метод дистанционного лазерного зондирования верхнего квазиоднородного слоя (ВКС) получил относительно широкое мировое применение в практике экологического мониторинга. Традиционно подобная дорогостоящая, и обычно громоздкая аппаратура используется в задачах обнаружения и оценки степени загрязненности акватории нефтепродуктами (см, например, [8]). Однако судовые флуоресцентные лидары успешно используются и для исследований мелкомасштабного пространственного распределения органического вещества во взвешенном и растворенном виде [15, 21]. Основными преимуществами дистанционных лидарных измерений является высокая производительность (частота) измерений, неинвазивность и высокая чувствительность метода, а также скорость проведения большого количества зондирований значительной по площади акватории при установке лидара на быстроходное судно. Иными словами, появляется возможность квазиодномоментной съемки водного объекта с высоким пространственным разрешением [17]. При этом в случае проведения калибровки лидара на пробах воды для конкретной акватории “здесь и сейчас”, лидарные измерения концентраций имеют высокую точность: средняя относительная погрешность лидарных измерений концентраций в весовых единицах для общего органического углерода и взвеси составляет 10% [17].
Важным направлением в использовании лидаров, в том числе в программах экологического мониторинга, является понимание факторов, формирующих сигнал флуоресценции. Так, в работе [4] показано, что в условиях доминирования терригенного стока вклад взвешенной составляющей в сигнал окрашенного органического вещества (ООВ) существенен и должен быть учтен, а следовательно, для верификации лидара на подобных акваториях требуется использовать данные об общем органическом углероде. Для вод открытого моря обычно характерна обратная ситуация, при которой взвешенным органическим веществом (ВОВ) можно пренебречь на фоне растворенного.
Не менее востребованным при изучении флуоресцирующей фракции РОВ в настоящее время является параллельный факторный анализ (PARAFAC) трехмерных зависимостей интенсивности флуоресценции от длин волн возбуждения и испускания [9]. Этот подход позволяет получить данные о классе близких по оптическим свойствам веществ [23].
Наконец, нецелесообразно пренебрегать классической спектрофотометрической методикой (и ее вариациями) определения концентраций ООВ, основанной на измерении спектрального показателя поглощения фильтрата, а также осадка на фильтре. Подобная методика использовалась в настоящей работе для анализа проб воды на содержание взвешенного органического вещества.
В данной работе описанные выше методы были использованы для оценки качества поверхностного слоя воды Геленджикской бухты. При этом лидарные измерения и отображения результатов в онлайн-режиме на экране оператора позволили выбрать оптимальные точки отбора проб воды с точки зрения поиска локальных экстремумов и максимизации диапазона концентраций органического вещества для лабораторного анализа. Город Геленджик является одним из самых крупных курортов на черноморском побережье, и мониторинг экологического состояния Геленджикской бухты с позиции рассмотрения загрязнения сточными городскими водами представляется важным мероприятием не только для научной, но и для природоохранной и санитарно-эпидемиологической служб [3].
МАТЕРИАЛЫ И МЕТОДЫ
Натурные исследования проводились с борта катера “Ашамба” 27 и 28 сентября 2021 в ходе экспедиции “Черное море – 2021”. Основной задачей являлось выявление фоновых значений концентраций и состава органического вещества естественного и антропогенного происхождения, отличных от взвешенного в поверхностном слое или плавающего на поверхности моря пластикового мусора. Для флуоресцентного и спектрофотометрического анализа компонентов ОВ выполнен отбор 27 проб морской воды. Пробы отбирались с поверхности ведром на ходу судна и на станциях, особое внимание при этом уделялось синхронизации с лидарными измерениями. В день измерений пробы морской воды (объемом 5 л) были профильтрованы через фильтры марки GF/F “Whatman” (с условным диаметром пор ~0.7 мкм), после чего высушены и заморожены при температуре –18°С для анализа в лаборатории. Фильтрат был отобран в стеклянные виалы емкостью 40 мл и хранился не более одной недели при температуре 2–3°С до последующего анализа в стационарной лаборатории.
Лидарное зондирование. В ходе работ использовался ультрафиолетовый флуоресцентный лидар УФЛ-9, установленный в носовой части судна и зондирующий водную толщу под углом 30 градусов к вертикали. Основная длина волны возбуждающего излучения составляла 355 нм (третья гармоника Nd:YAG лазера). Лидарная съемка осуществлялась в квазинепрерывном режиме с частотой 2 Гц на ходу судна, регистрировалась суммарная флуоресценция РОВ и ВОВ в диапазоне 430–450 нм. Толщина слоя зондирования оценочно составляла 5 м [21] и не превышала толщину верхнего квазиоднородного слоя, определяемого вертикальной стратификацией плотности вследствие термического прогрева и интенсивностью ветрового перемешивания. Регистрация эхо-сигнала производилась в четырех спектральных каналах с автоматизированной регулировкой фотоприемников, в одном из которых регистрировалась флуоресценция РОВ. Все сигналы нормировались на рамановское рассеяние для учета переменной геометрии зондирования и других непостоянных условий локации с борта судна. На станциях лидар переводился в соответствующий режим работы и последовательно записывал эхо-сигнал в 11 спектральных каналах, которые служили в том числе для контроля корректности вычисления рамановского реперного сигнала, играющего ключевую роль в измерениях. По уровню сигнала в канале обратного рассеяния отбраковывались шумы от попадания лазером в пену, возникающую на поверхности моря при обрушении волн.
Регистрация спектров флуоресценции РОВ выполнена на спектрофлуориметре “Флюорат-02-Панорама” фирмы “Люмэкс” при комнатной температуре в диапазоне от 240 до 600 нм с шагом 2 нм, при варьировании длины волны возбуждения от 230 до 550 нм с шагом 5 нм. Длина кюветы – 1 см, погрешность установки монохроматоров возбуждения и регистрации составляла ±1 нм, спектральное разрешение монохроматоров – 5 нм. На основании полученных спектров флуоресценции рассчитаны индексы гумификации (HIX) [27] и вклада автохтонного РОВ (BIX) [12] с использованием пакета Albatross [14].
Факторный анализ спектров флуоресценции РОВ. Для выполнения расчетов использовали пакет Albatross [14], написанный на языке программирования R. В отличие от описанного в работе подхода, области шириной +/– 25 нм, соответствующие сигналу упругого и комбинационного рассеяния в первом и втором порядке дифракции интерполировали по Уиттэкеру [11] с параметрами λ1 = 10–2, λ2 = 1. Модель PARAFAC валидировали при помощи метода разделения на половины с 20 случайными перемешиваниями.
Вычисление концентрации ВОВ в осадке на фильтрах производилось по данным оптических измерений – спектральным показателям поглощения света ВОВ при 440 нм и минеральной взвесью при 750 нм, с использованием эмпирических уравнений, которые получены в результате сопоставления концентраций компонентов взвеси, измеренных прямым (весовым) методом, и спектральных значений оптической плотности взвеси, осажденной на мембранные фильтры [1].
Определение содержания растворенного органического углерода (РОУ) выполнялось методом высокотемпературного сжигания на анализаторе TOC-VCPH/CPN (Shimadzu). Перед началом серии анализов проводилась калибровка прибора по стандартным растворам гидрофталата калия известной концентрации. Калибровочный диапазон составлял 0.1–250 мг С/л. Погрешность прибора – 1%, воспроизводимость результатов анализов ± 5%.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
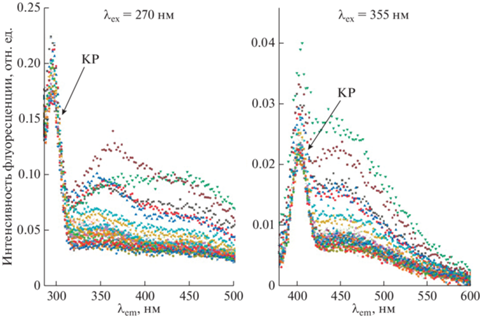
Максимальная интенсивность флуоресценции наблюдалась при длинах волн 300–500 нм при возбуждении 240–350 нм. В этом диапазоне флуоресцируют большинство флуорофоров как автохтонного, так и аллохтонного происхождения [24]. Наличие нескольких флуорофоров обычно наглядно удается продемонстрировать на спектрах флуоресценции при возбуждении на 270–280 нм, так как в этом диапазоне поглощают как гуминовые вещества, так и биолабильное РОВ, а также некоторые органические загрязнители, например, нефтепродукты. Так, в спектрах флуоресценции 27 исследованных образцов, представленных на рис. 1, при длине волны возбуждения λex = 270 нм хорошо видны 2 максимума флуоресценции λem на ~ 370 и 450 нм. Для сравнения на рис. 1 приведены спектры флуоресценции образцов при λex = 355 нм, соответствующей 3-й гармонике Nd:YAG лазера. В этом случае наблюдается один максимум на ~450 нм, обусловленный флуоресценцией только гуминовых веществ.
Рис. 1.
Спектры флуоресценции РОВ всех исследуемых образцов морской воды при возбуждении на длинах волн 270 (слева) и 355 нм (справа). КР – комбинационное рассеяние на молекулах воды.
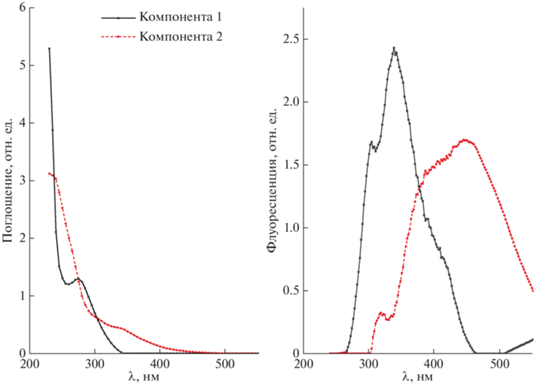
Критерий определения оптимального числа компонент PARAFAC-разложения, предложенный в работе [14], дает основание предположить наличие 5 компонент – флуорофоров. Однако 27 образцов оказалось недостаточно для полной валидации такой модели, поэтому было выполнено простейшее разложение на 2 компоненты. Спектры поглощения и флуоресценции отдельных компонент приведены на рис. 2.
Рис 2.
Спектры поглощения и флуоресценции групп флуорофоров, выявленных при PARAFAC разложении трехмерных спектров флуоресценции РОВ.
Максимумы поглощения и флуоресценции индивидуальных компонент представлены в табл. 1. Сравнение спектров полученных компонент с базой данных OpenFluor (https://openfluor.lablicate.com/) показало совпадение с более чем 30 моделями, описывающими флуоресценцию РОВ различных акваторий. Компоненту 2 идентифицируют как гуминовое вещество терригенного происхождения [10, 18], а компоненту 1 – как автохтонное РОВ, являющееся результатом микробиологической активности [25, 26]. Также, компонента 1 часто встречается в акваториях вблизи урбанизированных территорий [22]. Это может быть связано как с присутствием загрязнителей, имеющих схожие спектральные характеристики, так и с увеличением концентрации автохтонного РОВ. Так, при изучении водотоков штата Мэн было показано, что флуоресцентный и стехиометрический состав РОВ значительно изменился по градиенту от сельской местности к городской [20]. В частности, доля гуминоподобного аллохтонного РОВ снизилась, в то время как доля более биодоступного автохтонного РОВ увеличилась в более урбанизированных районах. Увеличение доли автохтонного РОВ было связано с увеличением скорости распада растворенного органического вещества.
Таблица 1.
Максимумы поглощения и флуоресценции компонент PARAFAC
| Компонента | λex, нм | λем, нм |
|---|---|---|
| 1 | <245, 275 | 340 |
| 2 | <400 нм | 445 |
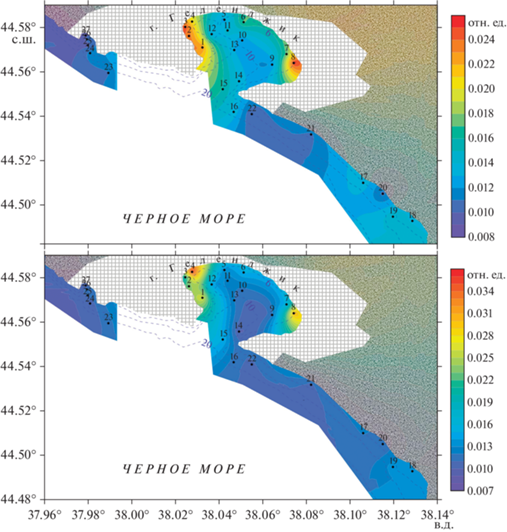
На рис. 3 представлены распределения относительного содержания компонент 1 и 2 в Геленджикской бухте и на станциях вблизи черноморского побережья. Отчетливо выделяются 2 области, для которых характерна наибольшая концентрация флуоресцирующего РОВ: 1) у западного берега Геленджикской бухты в районе Геленджикского порта (на станциях 1–4); 2) в восточной части Геленджикской бухты вблизи главного городского причала на станции 8. Интенсивность флуоресценции РОВ в указанных районах примерно в 3 раза превышала интенсивность флуоресценции за пределами бухты, например, на станциях 24–27, а интенсивность флуоресценции ООВ, по данным лидара, почти на порядок. Наибольшее содержание растворенных гуминовых веществ зафиксировано на станции 4 в районе стока реки Су-Аран (заключена в коллектор), в то время как на станциях 1–3 флуоресцирующее РОВ представлено преимущественно биолабильными низкомолекулярными соединениями. Станция 8 вблизи городского главного причала, неподалеку от которой также расположены 3 городские канализационно-насосные станции, характеризуется высоким содержанием как 1й, так и 2й компонент РОВ, а также максимальными концентрациями ВОВ. За пределеми Геленджикской бухты увеличение концентрации предположительно автохтонного РОВ наблюдалось на станциях 18 и 19. В целом же для всех исследуемых образцов характерна низкая величина индекса гумификации HIX (0.9 < HIX < 2.2, среднее значение составило 1.3) и, наоборот, высокое значение BIX (1.0 < BIX < 1.5, среднее значение – 1.2), что указывает на незначительный вклад терригенного РОВ [12].
Рис. 3.
Концентрация 1й (сверху) и 2й (снизу) компонент/групп флуорофоров PARAFAC. Над точками пробоотбора указаны номера станций. Пунктирными линиями отмечены изобаты.
Полученные данные согласуются с результатами исследования состава углеводородов в прибрежных водах северо-восточной части Черного моря в июне 2012 года [2]. В частности, изучение взвеси поверхностных вод Геленджикской бухты показало, что основу углеводородов составляли автохтонные биогенные соединения, основным источником которых является фитопланктон. Также, были сделаны предположения о присутствии терригенного органического вещества.
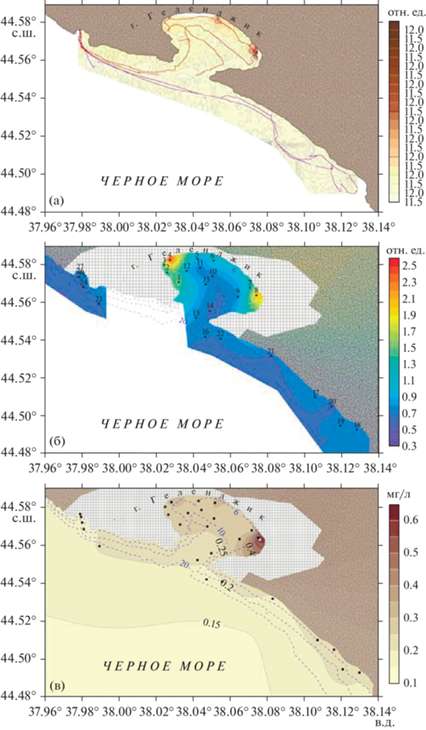
Для сопоставления результатов флуориметрического анализа с данными лидарного зондирования были рассмотрены распределения интенсивности флуоресценции ООВ in situ при зондировании лазером с λex = 355 нм (рис. 4а) и интенсивности флуоресценции РОВ в фильтрате при той же длине волны возбуждения (рис. 4б). Полученное по лидару распределение во многом повторяет распределение содержания компоненты 2 (флуоресценция гуминовых веществ), что объясняется особенностями вероятности молекулярных переходов флуорофоров при возбуждении на 355 нм (см. спектры поглощения компонент на рис. 2). Полученный результат хорошо согласуется с выводами, представленными в работе [16], где обсуждаются хорошие перспективы использования коэффициента поглощения aCDOM (350) для оценки вклада терригенного РОВ. Максимальные концентрации ООВ по лидару за все время экспедиции были зафиксированы в Геленджикской бухте вблизи ст. 8, при этом основной вклад в флуоресценцию внесло ВОВ, что подтверждается данными анализа осадка на фильтрах (см. рис. 4в). Также для проверки этого вывода было выполнено определение содержания РОУ, его концентрации составили на станции 4 – 3.25 мг/л, а на станции 8 – 3.54 мг/л. Это подтверждает сделанный выше вывод о доминирующем вкладе ВОВ в максимальный сигнал флуоресценции ОВ за всю экспедицию, полученный на ст. 8.
Рис. 4.
(а) Интенсивность флуоресценции ООВ по данным лидара при длине волны возбуждения 355 нм, линии на рисунке сформированы точками лидарных измерений; (б) интенсивность флуоресценции РОВ фильтрата при длине волны возбуждения 355 нм; (в) концентрация ВОВ; – в ВКС Геленджикской бухты и прилегающих районах, 27 и 28 сентября 2021 г.
Данные лидарного зондирования содержат более 50 000 отдельных измерений флуоресценции ООВ, характеризующих изменчивость концентраций флуоресцирующих примесей в пространственных масштабах от 10 м и более. В данной статье мы работаем с масштабами неоднородностей от 100 и более метров. Карта на рис. 4а наглядно демонстрирует, насколько пространственно неоднороден ВКС, несмотря на ветровой форсинг и различные гидрологические факторы. Дополнительно хочется отметить, что увеличить информативность карты распределения флуоресцирующего РОВ в бухте, особенно вдоль береговой линии, можно было бы, подходя ближе к берегу, однако для этого требуется судно с меньшей осадкой. Также заслуживает отдельного упоминания чистота вод вблизи берега в Голубой бухте (станции 24–27), однако надо принять во внимание, что работы проводились уже после окончания активного курортного сезона.
ЗАКЛЮЧЕНИЕ
Показана эффективность использования флуоресцентного лидара в комплексных исследованиях для оперативного отслеживания изменчивости концентрации органического вещества и определения максимально релевантной сетки станций для пробоотбора. Так, 27 проб оказалось достаточно для построения карт распределения флуоресцирующей фракции РОВ и ВОВ в поверхностном слое Геленджикской бухты и прилегающих районов Черного моря, отражающих, в том числе, локальные увеличения концентрации компонент ОВ в районах выноса реки Су-Аран, Геленджикского порта и главного городского причала Геленджика.
Соотношение интенсивности флуоресценции гуминовых веществ и РОВ автохтонного и/или антропогенного происхождения указывает на незначительный вклад терригенного материала. Увеличение доли гуминовых веществ (максимум флуоресценции 455 нм) зафиксировано в районах выноса реки Су-Аран, которая берет начало на склонах Маркотхского хребта, протекает через весь город и впадает в бухту, а также вблизи главного городского причала. Максимальное содержание биолабильного РОВ (максимум флуоресценции 340 нм) характерно для прибрежных станций в Геленджикской бухте, и в частности, в районе Геленджикского порта. Содержание флуоресцирующего РОВ там было примерно в 3 раза выше, чем за пределами бухты.
Сопоставление данных лидарной съемки, спектрофлуориметрического анализа РОВ, содержания ВОВ и РОУ позволили сделать вывод о доминирующем вкладе ВОВ в максимальный сигнал флуоресценции на востоке бухты. Там наблюдались высокие содержания обоих флуорофоров РОВ, максимальное содержание ВОВ по данным анализов проб воды на фильтрах, а также максимальное содержание растворенного и взвешенного органического вещества в совокупности, по данным флуоресцентного лидара.
Благодарности. Авторы благодарят Андрея Зацепина и Петра Завьялова за всестороннюю помощь в организации работ по проекту, Александра Грабовского и Льва Якушкина за помощь в проведении экспедиционных работ.
Источники финансирования. Работа выполнена в рамках государственного задания Министерства науки и образования России (тема FMWE-2021-0001), а также при поддержке грантов РФФИ (№ 19-55-80 004 БРИКС_т, организация морских экспедиционных исследований и лидарная съемка) и РНФ (№ 21-77-10 064, PARAFAC анализ спектров флуоресценции РОВ).
Список литературы
Коновалов Б.В., Кравчишина М.Д., Беляев Н.А. и др. Определение концентрации минеральной взвеси и взвешенного органического вещества по их спектральному поглощению // Океанология. 2014. Т. 54. № 5. С. 704–704.
Немировская И.А., Полякова А.В., Юхимук В.Д. Распределение и состав углеводородов в прибрежных водах северо-восточной части Черного моря // Вестник Московского университета. Серия 5. География. 2013. № 6. С. 16–22.
Никифоров Д.А. Загрязнение Геленджикской бухты сточными водами // Всероссийский журнал научных публикаций. 2011. Т. 3. № 4. С. 88–90.
Пелевин В.В., Завьялов П.О., Беляев Н.А. и др. Пространственная изменчивость концентраций хлорофилла “а”, растворенного органического вещества и взвеси в поверхностном слое Карского моря в сентябре 2011 г. по лидарным данным // Океанология. 2017. Т. 57. № 1. С. 183–193.
Романкевич Е.А., Ветров А.А., Пересыпкин В.И. Цикл углерода в современном океане и актуальные проблемы биогеохимии // Океанология на старте ХХI века. М.: Наука, 2008. С. 78–107.
Amon R.M.W. The role of dissolved organic matter for the organic carbon cycle in the Arctic Ocean // In: Stein R.S., Macdonald R.W. (Eds.) The Organic Carbon Cycle in the Arctic Ocean. Berlin: Springer, 2004. P. 83–99.
Arrigo K.R., Brown C.W. Impact of chromophoric dissolved organic matter on UV inhibition of primary productivity in the sea // Marine Ecology Progress Series. 1996. V. 140. P. 207–216.
Babichenko S., Poryvkina L., Rebane O. et al. Compact HLIF LiDAR for marine applications // International Journal of Remote Sensing. 2016. V. 37. № 16. P. 3924– 3937.
Bro R. PARAFAC. Tutorial and applications // Chemometrics and intelligent laboratory systems. 1997. V. 38. № 2. P. 149–171.
DeFrancesco C., Guéguen C. Long-term Trends in Dissolved Organic Matter Composition and Its Relation to Sea Ice in the Canada Basin, Arctic Ocean (2007–2017) // Journal of Geophysical Research: Oceans. 2021. V. 126. № 2. e2020JC016578.
Eilers P.H. A perfect smoother // Analytical chemistry. 2003. № 75. № 14. P. 3631–3636.
Huguet A., Vacher L., Relexans S. et al. Properties of fluorescent dissolved organic matter in the Gironde Estuary // Organic Geochemistry. 2009. V. 40. № 6. P. 706–719.
Jaffé R., McKnight D., Maie N. et al. Spatial and temporal variations in DOM composition in ecosystems: The importance of long-term monitoring of optical properties // Journal of Geophysical Research: Biogeosciences. 2008. V. 113. G04032.
Krylov I.N., Drozdova A.N., Labutin T.A. Albatross R package to study PARAFAC components of DOM fluorescence from mixing zones of arctic shelf seas // Chemometrics and Intelligent Laboratory Systems. 2020. V. 207. 104176.
Kutser T., Hedley J., Giardino C. et al. Remote sensing of shallow waters–A 50 year retrospective and future directions // Remote Sensing of Environment. 2020. V. 240. 111619.
Mann P.J., Spencer R.G.M., Hernes P.J. et al. Pan-Arctic trends in terrestrial dissolved organic matter from optical measurements // Frontiers in Earth Science. 2016. V. 4. 25. P. 1–18.
Molkov A.A., Fedorov S.V., Pelevin V.V. et al. Regional models for high-resolution retrieval of chlorophyll a and TSM concentrations in the Gorky Reservoir by Sentinel-2 imagery // Remote Sensing. 2019. V. 11. № 10. 1215.
Osburn C.L., Anderson N.J., Stedmon C.A. et al. Shifts in the source and composition of dissolved organic matter in Southwest Greenland lakes along a regional hydro-climatic gradient // Journal of Geophysical Research: Biogeosciences. 2017. V. 122. № 12. P. 3431–3445.
Palmer S.C.J., Pelevin V.V., Goncharenko I. et al. Ultraviolet fluorescence LiDAR (UFL) as a measurement tool for water quality parameters in turbid lake conditions // Remote Sensing. 2013. V. 5. № 9. P. 4405–4422.
Parr T.B., Cronan C.S., Ohno T. et al. Urbanization changes the composition and bioavailability of dissolved organic matter in headwater streams // Limnology and Oceanography. 2015. V. 60. № 3. P. 885–900.
Pelevin V., Zlinszky A., Khimchenko E. et al. Ground truth data on chlorophyll-a, chromophoric dissolved organic matter and suspended sediment concentrations in the upper water layer as obtained by LIF lidar at high spatial resolution // International journal of remote sensing. 2017. V. 38. № 7. P. 1967–1982.
Smith M.A., Kominoski J.S., Gaiser E.E. et al. Stormwater runoff and tidal flooding transform dissolved organic matter composition and increase bioavailability in urban coastal ecosystems // Journal of Geophysical Research: Biogeosciences. 2021. V. 126. № 7. e2020JG006146.
Stedmon C.A., Markager S., Bro R. Tracing dissolved organic matter in aquatic environments using a new approach to fluorescence spectroscopy // Marine chemistry. 2003. V. 82. № 3–4. P. 239–254.
Stedmon C.A., Nelson N.B. The optical properties of DOM in the ocean // In: Hansell D.A., Carlson C.A. (Eds.) Biogeochemistry of marine dissolved organic matter. Elsevier, 2015. P. 481–508.
Walker S.A., Amon R.M.W., Stedmon C.A. Variations in high-latitude riverine fluorescent dissolved organic matter: A comparison of large Arctic rivers // Journal of Geophysical Research: Biogeosciences. 2013. V. 118. № 4. P. 1689–1702.
Yamashita Y., Maie N., Briceño H. et al. Optical characterization of dissolved organic matter in tropical rivers of the Guayana Shield, Venezuela // Journal of Geophysical Research: Biogeosciences. 2010. V. 115. G00F10. P. 1–15.
Zsolnay A., Baigar E., Jimenez M. et al. Differentiating with fluorescence spectroscopy the sources of dissolved organic matter in soils subjected to drying // Chemosphere. 1999. V. 38. № 1. P. 45–50.
Дополнительные материалы отсутствуют.


