Петрология, 2023, T. 31, № 6, стр. 677-684
Влияние содержания щелочей на растворимость циркона в силикатных расплавах
А. А. Борисов a, *, А. Н. Кошлякова a, b
a Институт геологии рудных месторождений, петрографии, минералогии и геохимии РАН
Москва, Россия
b Институт геохимии и аналитической химии им. В.И. Вернадского РАН
Москва, Россия
* E-mail: aborisov@igem.ru
Поступила в редакцию 26.11.2022
После доработки 30.01.2023
Принята к публикации 25.04.2023
- EDN: EFWFIU
- DOI: 10.31857/S0869590323060055
Аннотация
В температурном интервале 1300–1400°С при 1 атм. общего давления экспериментально исследовано влияние щелочей на растворимость циркона в модельных многокомпонентных силикатных расплавах. Показано, что повышение растворимости циркона в расплаве при добавлении Na2O или K2O сопоставимо. Коротко рассмотрены достоинства и недостатки предложенных в литературе параметров, описывающих влияние состава расплава на растворимость циркона.
ВВЕДЕНИЕ
В классических статьях (Watson, 1979; Watson, Harrison, 1983) авторы впервые предложили использовать насыщение кислых силикатных расплавов Zr в равновесии с цирконом (Zrn) в качестве геотермометра. Позднее было предложено несколько обновленных моделей по растворимости Zrn в расплаве (Boehnke et al., 2013; Gervasoni et al., 2016; Borisov, Aranovich, 2019; Crisp, Berry, 2022). При этом модель (Borisov, Aranovich, 2019) была откалибрована для широкого спектра составов – от кислых до основных.
Все модели, помимо температурного фактора, содержат член, описывающий влияние состава расплава на растворимость Zrn. В работах (Watson, Harrison, 1983; Boehnke et al., 2013) для этих целей использован эмпирический параметр M = = (Na + K + 2Ca)/(AlSi), ат. доли, безгласно предполагающий одинаковое влияние щелочей на растворимость Zrn. Параметр G = (3Al2O3 + SiO2)/ (Na2O + K2O + CaO + MgO + FeO), мол. доли, в работе (Gervasoni et al., 2016) предполагает одинаковое влияние сильных (Na2O и K2O) и слабых (CaO, MgO, FeO) оксидов-модификаторов на растворимость Zrn. Наконец, в модели (Crisp, Berry, 2022) авторы описали влияние состава расплава на растворимость циркона от параметра λ, оптической основности расплава. Параметр λ рассчитывается из основности (λi) индивидуальных оксидов (см. схему расчета, например, в Mills, 1993). Поскольку ${{\lambda }_{{{\text{N}}{{{\text{a}}}_{{\text{2}}}}{\text{O}}}}}$ = 1.15 и ${{\lambda }_{{{{{\text{K}}}_{{\text{2}}}}{\text{О}}}}}$ = 1.4, эквимолярная замена Na2O на K2O должна приводить к незначительному повышению растворимости Zrn в расплаве.
Особо остановимся на модели (Borisov, Aranovich, 2019), описывающей влияние состава расплава на параметр:
(1)
$\begin{gathered} ~B = 0.14({{{{X}_{{{\text{Ti}}{{{\text{O}}}_{2}}}}}} \mathord{\left/ {\vphantom {{{{X}_{{{\text{Ti}}{{{\text{O}}}_{2}}}}}} {{{X}_{{{\text{Si}}{{{\text{O}}}_{2}}}}}}}} \right. \kern-0em} {{{X}_{{{\text{Si}}{{{\text{O}}}_{2}}}}}}}) + 1.3({{{{X}_{{{\text{CaO}}}}}} \mathord{\left/ {\vphantom {{{{X}_{{{\text{CaO}}}}}} {{{X}_{{{\text{Si}}{{{\text{O}}}_{{\text{2}}}}}}}}}} \right. \kern-0em} {{{X}_{{{\text{Si}}{{{\text{O}}}_{{\text{2}}}}}}}}}) + 1.5({{{{X}_{{{\text{N}}{{{\text{a}}}_{2}}{\text{O}}}}}} \mathord{\left/ {\vphantom {{{{X}_{{{\text{N}}{{{\text{a}}}_{2}}{\text{O}}}}}} {{{X}_{{{\text{Si}}{{{\text{O}}}_{{\text{2}}}}}}}}}} \right. \kern-0em} {{{X}_{{{\text{Si}}{{{\text{O}}}_{{\text{2}}}}}}}}}) - 4.5({{{{X}_{{{{{\text{K}}}_{{\text{2}}}}{\text{O}}}}}} \mathord{\left/ {\vphantom {{{{X}_{{{{{\text{K}}}_{{\text{2}}}}{\text{O}}}}}} {{{X}_{{{\text{Si}}{{{\text{O}}}_{{\text{2}}}}}}}}}} \right. \kern-0em} {{{X}_{{{\text{Si}}{{{\text{O}}}_{{\text{2}}}}}}}}})-- \\ - \,\,2.7{{({{{{X}_{{{\text{A}}{{{\text{l}}}_{{\text{2}}}}{{{\text{O}}}_{{\text{3}}}}}}}} \mathord{\left/ {\vphantom {{{{X}_{{{\text{A}}{{{\text{l}}}_{{\text{2}}}}{{{\text{O}}}_{{\text{3}}}}}}}} {{{X}_{{{\text{Si}}{{{\text{O}}}_{{\text{2}}}}}}}}}} \right. \kern-0em} {{{X}_{{{\text{Si}}{{{\text{O}}}_{{\text{2}}}}}}}}})}^{2}} + {{({{{{X}_{{{\text{MgO}}}}}} \mathord{\left/ {\vphantom {{{{X}_{{{\text{MgO}}}}}} {{{X}_{{{\text{Si}}{{{\text{O}}}_{{\text{2}}}}}}}}}} \right. \kern-0em} {{{X}_{{{\text{Si}}{{{\text{O}}}_{{\text{2}}}}}}}}})}^{2}} - 3.7{{({{{{X}_{{{\text{CaO}}}}}} \mathord{\left/ {\vphantom {{{{X}_{{{\text{CaO}}}}}} {{{X}_{{{\text{Si}}{{{\text{O}}}_{{\text{2}}}}}}}}}} \right. \kern-0em} {{{X}_{{{\text{Si}}{{{\text{O}}}_{{\text{2}}}}}}}}})}^{2}} + 75{{({{{{X}_{{{{{\text{K}}}_{{\text{2}}}}{\text{O}}}}}} \mathord{\left/ {\vphantom {{{{X}_{{{{{\text{K}}}_{{\text{2}}}}{\text{O}}}}}} {{{X}_{{{\text{Si}}{{{\text{O}}}_{{\text{2}}}}}}}}}} \right. \kern-0em} {{{X}_{{{\text{Si}}{{{\text{O}}}_{{\text{2}}}}}}}}})}^{2}}, \\ \end{gathered} $предложенный авторами, он, пожалуй, слишком громоздок для того, чтобы напрямую сравнить влияние Na и K на растворимость Zrn. Заметим, что авторы в поисках адекватной модели также пытались описать растворимость циркона более простой зависимостью вида: lgZr (ppm) = 1/T(K) + + ∑di(${{{{X}_{i}}} \mathord{\left/ {\vphantom {{{{X}_{i}}} {{{X}_{{{\text{Si}}{{{\text{O}}}_{{\text{2}}}}}}}}}} \right. \kern-0em} {{{X}_{{{\text{Si}}{{{\text{O}}}_{{\text{2}}}}}}}}}$) + c, где Xi – мольные доли петрогенных оксидов, а di и с – эмпирические коэффициенты. В этом случае для щелочей были получены следующие значения эмпирических коэффициентов: dNa = 3.64 ± 0.92 и dK = 0.07 ± 1.48 (1σ). Исключительно низкое значение dK предполагает практически полное отсутствие влияния К на растворимость Zrn. При этом высокое значение dNa резко контрастирует с dK, хотя здравый смысл подсказывает, что эффект щелочей на растворимость циркона должен быть сопоставим. Все это авторам (Borisov, Aranovich, 2019) представлялось маловероятным, поэтому они предпочли более сложное выражение для параметра В.
Отметим, что все модели основаны на статистической обработке существующих на то время экспериментов, которая не всегда позволяет корректно разделить влияние петрогенных оксидов, в частности щелочей, на растворимость циркона. Например, в базе данных (Borisov, Aranovich, 2019) из 119 экспериментов 67 расплавов были бесщелочные, а остальные составы содержали оксиды Na и K в сопоставимых количествах. Специальных опытов для сравнения влияния Na и К на растворимость циркона в расплавах не проводилось, за исключением ранней работы (Watson, 1979). Автор в простой системе SiO2–A12O3–Na2O–K2O варьировал мольным соотношением Na2O/K2O, зафиксировав долю оксидов кремния и алюминия, и показал, что растворимость циркона в расплаве практически не меняется. Подобные опыты в более сложных по составу системах весьма желательны.
Таким образом, для дальнейшего улучшения моделей растворимости циркона в силикатных расплавах нам представляется важным проведение экспериментов, специально направленных на: (1) уточнение влияния калия и (2) сравнение влияния щелочей Na и K на растворимость циркона в многокомпонентных силикатных расплавах.
МЕТОДИКА ЭКСПЕРИМЕНТОВ
Эксперименты выполнены методом петли в вертикальной трубчатой печи либо на воздухе, либо в смеси Н2–CO2. Температура в рабочей зоне печи определялась с помощью термопары типа ТПР, калиброванной по точке плавления чистого Au (1064°C) и Ni (1453°C). Погрешности в определении температуры не превышают ±2°C.
Известно, что потери щелочей из экспериментальных расплавов при работе методом петли могут быть значительными (например, Corrigan, Gibb, 1979). В настоящей работе мы использовали два разных подхода для решения этой проблемы.
1. Серия опытов по определению влияния К на растворимость циркона. Вместо того, чтобы бороться с неизбежной потерей калия из расплава, мы использовали этот процесс для получения образцов со значительными вариациями K2O в образцах. Ранее, в (Borisov et al., 2017) успешно использовали подобный подход для исследования влияния Na и K на соотношение Fe3+/Fe2+ в силикатных расплавах.
Состав эвтектики в системе SiO2–анортит (SA) был приготовлен из оксидов SiO2, Al2O3, MgO и карбоната CaCO3, тщательно смешанных в ступке, расплавлен, выдержан два часа при температуре 1600°C и закален в стекло. Истолченное стекло было обогащено (+20%) смесью ZrO2–SiO2, по стехиометрии соответствующей циркону (состав SAZ). Аликвоты SAZ были обогащены карбонатом K2CO3 (состав SAZK). Оба состава (SAZ и SAZK) были одновременно выдержаны в вертикальной трубчатой печи на воздухе при фиксированной температуре 1400°С в течение 24, 46 и 69 ч (Институт минералогии Ганноверского университета, Ганновер, Германия). В ходе опытов состав SAZK теряет часть исходного К (чем больше выдержка, тем больше потери). Изначально безкалиевый состав SAZ при этом может получить некоторое количество К от соседнего образца SAZK через паровую фазу. В случае, если уравновешивание циркон/ расплав происходит быстрее, чем потери/поступления К, все образцы, полученные при фиксированной температуре, но при разных выдержках, должны показать единую систематическую зависимость растворимости циркона от содержания К2О в образцах. После закалки образцы были залиты в шашки и отполированы для анализа на микрозонде.
Анализ выполнен на микрозонде Cameca SX100 (Институт минералогии Ганноверского университета, Ганновер, Германия) при следующих условиях: ускоряющее напряжение 15 кВ, ток зонда 15 нА, время счета 10–20 с, диаметр зонда 20 мкм. А.А. Борисов (2009) показал, что использование зонда диаметром 20 мкм гарантирует пренебрежимо малые потери щелочей из стекол в ходе микрозондового анализа. От 7 до 10 точек было проанализировано в каждом образце. Усредненные данные по экспериментальным стеклам SAZ и SAZK приведены в табл. 1 наряду с условиями экспериментов.
Таблица 1.
Условия экспериментов, выполненных методом “классической петли” и микрозондовый анализ экспериментальных стекол
| Образе | T, °C | Выдержка, ч | Состав стекол, мас. % | |||||||
|---|---|---|---|---|---|---|---|---|---|---|
| SiO2 | Al2O3 | CaO | K2O | er. | ZrO2 | er. | Сумма | |||
| SAZ-7* | 1400 | 24 | 68.49 | 18.06 | 9.92 | 0.64 | 0.02 | 1.95 | 0.22 | 99.05 |
| SAZK-7 | » | » | 64.92 | 14.56 | 8.24 | 7.84 | 0.08 | 3.41 | 0.13 | 98.97 |
| SAZ-8 | 1399 | 46 | 70.44 | 16.67 | 9.17 | 1.15 | 0.03 | 1.61 | 0.07 | 99.04 |
| SAZK-8 | » | » | 64.99 | 15.03 | 9.02 | 6.68 | 0.09 | 3.24 | 0.18 | 98.96 |
| SAZ-6 | 1400 | 69 | 70.69 | 16.88 | 9.25 | 0.79 | 0.02 | 1.46 | 0.07 | 99.07 |
| SAZK-6 | » | » | 65.73 | 15.00 | 8.82 | 6.42 | 0.05 | 3.04 | 0.09 | 99.00 |
| SAZK'-6 | » | » | 65.94 | 15.25 | 8.92 | 5.99 | 0.06 | 2.97 | 0.10 | 99.08 |
2. Серия опытов по сравнению влияния K и Na на растворимость циркона. Здесь мы использовали метод “петля в тигле” (“crucible supported loop technique”, Borisov et al., 2006), ранее успешно использованный для изучения растворимости металлов в силикатных расплавах (Borisov et al., 2006), распределения щелочей между смешивающимися расплавами (Борисов, 2008, 2009), а также распределения Na (Borisov et al., 2008) и Ni (Koshlyakova et al., 2022) между оливином и расплавом. Суть метода состоит в помещении образцов на Pt-петлях в кварцевый тигель с источником щелочей – смесью SiO2 и K2O (и/или Na2O) определенного состава. Смесь плавится при температуре эксперимента и ее состав остается постоянным в течение опыта, создавая постоянное давление паров щелочей в атмосфере контейнера, которому подвержены образцы. Подробное описание метода, в том числе при работе с комплексными (Na-K, Ca-Na) источниками щелочей см. в работе (Koshlyakova et al., 2022).
В качестве основы выбраны два состава: эвтектический в системе SiO2–Al2O3–MgO, к которому было подмешано 10 мас. % Fe2O3 (HAF), и эвтектический в системе энстатит–анортит–кремнезем, также с 10 мас. % Fe2O3 (HRF). Аликвоты HAF были модифицированы некоторым количеством SiO2 (HAFS) и CaO + SiO2 (HAFCS). Эти исходные смеси (HRF, HAF, HAFS и HAFCS) ранее использовались для исследования влияния состава расплава на соотношение в нем Fe3+/Fe2+ (Borisov et al., 2017, 2018). Аликвоты составов HRF, HAFS и HAFCS были обогащены (+20%) смесью ZrO2–SiO2, по стехиометрии соответствующей циркону (составы HRFZ, HAFSZ и HAFCSZ). Опыты проведены с этими конечными составами как методом “классической петли”, так и методом “петля в тигле” с использованием либо Na-, либо K-источника.
Эксперименты проведены в высокотемпературной вертикальной трубчатой печи Nabertherm RHTV 1700 (ГЕОХИ РАН) при температурах 1300, 1350 и 1400°С и фугитивности кислорода, соответствующей буферу QFM + 1 (QFM – буфер кварц-фаялит-магнетит). Фугитивность кислорода задавалась смесью газов H2–CO2 и измерялась с помощью ZrO2 сенсора (Carboprobe DS, Econox®) непосредственно до и сразу после эксперимента. Погрешность в определении lgfO2 не превышала ±0.2. Все эксперименты завершались закалкой в воду. После закалки образцы были залиты в шашки и отполированы для анализа.
Химический состав стекол и минеральных фаз, полученных в ходе экспериментов, изучался в Лаборатории локальных методов исследования вещества на кафедре петрологии Геологического факультета МГУ. Исследования проведены на сканирующем электронном микроскопе JEOL JSM-IT500, оснащенном энерго-дисперсионным спектрометром INCA X-Maxn, количественный анализ и изображения получены при ускоряющем напряжении 20 кВ и силе тока 0.7 нА, время накопления спектра 100 с. Для предотвращения повреждения образцов исследования проводились при расфокусированном до 20 мкм электронном пучке. Использование низких токов и расфокусированного пучка позволило избежать потери щелочей из стекол во время анализа. Для наиболее щелочных стекол были сделаны дополнительные анализы со временем накопления спектра 50 с. Сравнение этих анализов показало отсутствие занижения (с учетом ошибки измерения) содержаний K и Na при большем времени накопления спектра. Ко всем анализам была применена процедура матричных ZAF-поправок. В каждом образце проанализировано семь точек, усредненные данные по экспериментальным стеклам HRFZ, HAFSZ и HAFC9SZ приведены в табл. 2, наряду с условиями экспериментов.
Таблица 2.
Экспериментальные условия опытов по сравнению влияния Na и K на растворимость циркона и состав экспериментальных стекол
| Образец | Т, °С | $\lg f{{{\text{O}}}_{2}}$* | Выдержка, ч | Источник щелочей | Кристаллические фазы** | Состав стекол, мас. % | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| SiO2 | Al2O3 | FeO | MgO | CaO | Na2O | er. | K2O | er. | ZrO2 | er. | Сумма | ||||||
| HRFZ-1 | 1300 | –6.30 | 40.7 | Нет | Zrn (Bdy) | 58.85 | 11.24 | 3.43 | 10.43 | 11.14 | 0.18 | 0.01 | 0.33 | 0.01 | 2.69 | 0.01 | 98.28 |
| HAFSZ-1 | » | » | 40.7 | » | Zrn (Bdy), Sil, En | 57.98 | 15.63 | 7.60 | 14.71 | 0.05 | 0.27 | 0.01 | 0.33 | 0.01 | 2.00 | 0.02 | 98.56 |
| HAFCSZ-1 | » | » | 40.7 | » | Zrn (Bdy), Sil, En | 59.17 | 8.86 | 6.29 | 9.96 | 10.75 | 0.21 | 0.01 | 0.26 | 0.00 | 2.84 | 0.01 | 98.34 |
| HRFZ-6 | 1299 | –6.20 | 39.0 | Na-Si | Zrn (Bdy) | 55.75 | 10.42 | 2.52 | 9.60 | 10.34 | 5.20 | 0.01 | 0.17 | 0.01 | 4.68 | 0.02 | 98.66 |
| HAFSZ-6 | » | » | 39.0 | » | Zrn (Bdy), En, Ol | 61.33 | 13.96 | 5.67 | 8.14 | 0.00 | 6.42 | 0.02 | 0.24 | 0.00 | 2.22 | 0.03 | 97.98 |
| HAFCSZ-6 | » | » | 39.0 | » | Zrn, Bdy | 56.65 | 8.11 | 5.15 | 9.09 | 9.85 | 4.86 | 0.02 | 0.16 | 0.01 | 4.57 | 0.04 | 98.44 |
| HRFZ-4 | 1300 | –6.19 | 40.0 | K-Si | Zrn (Bdy) | 55.38 | 10.26 | 2.80 | 9.59 | 10.34 | 0.25 | 0.01 | 5.95 | 0.04 | 4.15 | 0.02 | 98.72 |
| HAFSZ-4 | » | » | 40.0 | » | Zrn (Bdy), En, Ol | 61.50 | 13.98 | 5.82 | 4.88 | 0.00 | 0.38 | 0.01 | 10.51 | 0.15 | 1.64 | 0.06 | 98.71 |
| HAFCSZ-4 | » | » | 40.0 | » | Zrn (Bdy) | 55.38 | 7.96 | 5.67 | 9.30 | 10.04 | 0.23 | 0.01 | 5.59 | 0.02 | 4.36 | 0.04 | 98.54 |
| HRFZ-3 | 1350 | –5.72 | 29.0 | Нет | Zrn (Bdy) | 58.75 | 11.15 | 3.23 | 10.29 | 11.03 | 0.25 | 0.00 | 0.32 | 0.01 | 3.54 | 0.04 | 98.56 |
| HAFSZ-3 | » | » | 29.0 | » | Zrn, Qz | 59.38 | 13.33 | 7.08 | 15.31 | 0.01 | 0.31 | 0.01 | 0.38 | 0.01 | 2.77 | 0.06 | 98.58 |
| HAFCSZ-3 | » | » | 29.0 | » | Zrn (Bdy) | 59.67 | 8.62 | 6.06 | 9.67 | 10.41 | 0.24 | 0.01 | 0.27 | 0.01 | 3.69 | 0.03 | 98.63 |
| HRFZ-7 | 1349 | –5.73 | 30.0 | Na-Si | Zrn (Bdy) | 55.53 | 10.37 | 3.12 | 9.56 | 10.26 | 4.23 | 0.02 | 0.10 | 0.00 | 5.38 | 0.03 | 98.56 |
| HAFSZ-7 | » | » | 30.0 | » | Zrn (Bdy), En | 59.35 | 11.53 | 5.89 | 12.66 | 0.00 | 5.26 | 0.01 | 0.14 | 0.00 | 3.39 | 0.02 | 98.23 |
| HAFCSZ-7 | » | » | 30.0 | » | Zrn (Bdy) | 56.22 | 7.94 | 5.13 | 8.81 | 9.61 | 4.77 | 0.01 | 0.12 | 0.01 | 5.85 | 0.03 | 98.45 |
| HRFZ-5 | 1349 | –5.72 | 29.0 | K-Si | Bdy | 54.49 | 9.72 | 2.42 | 9.10 | 9.76 | 0.25 | 0.01 | 7.78 | 0.07 | 4.98 | 0.03 | 98.49 |
| HAFSZ-5 | » | » | 29.0 | » | Bdy, Ol, Zrn, En | 59.96 | 12.29 | 5.27 | 7.97 | 0.00 | 0.40 | 0.00 | 9.81 | 0.10 | 2.77 | 0.06 | 98.45 |
| HAFCSZ-5 | » | » | 29.0 | » | Zrn, Bdy | 56.19 | 7.57 | 4.77 | 8.52 | 9.21 | 0.25 | 0.00 | 6.66 | 0.03 | 5.52 | 0.02 | 98.69 |
| HRFZ-15 | 1400 | –5.26 | 20.0 | Нет | Zrn (Bdy) | 58.43 | 11.03 | 2.57 | 10.13 | 10.92 | 0.19 | 0.01 | 0.34 | 0.01 | 4.68 | 0.02 | 98.29 |
| HAFSZ-15 | » | » | 20.0 | » | Zrn (Bdy) | 64.20 | 12.14 | 4.15 | 13.68 | 0.00 | 0.48 | 0.01 | 0.74 | 0.01 | 3.05 | 0.04 | 98.44 |
| HAFCSZ-15 | » | » | 20.0 | » | Zrn (Bdy) | 59.64 | 8.57 | 5.28 | 9.63 | 10.37 | 0.19 | 0.01 | 0.36 | 0.01 | 4.81 | 0.03 | 98.85 |
| HRFZ-17 | 1400 | –5.28 | 20.0 | Na-Si | Bdy | 55.59 | 9.74 | 2.50 | 9.07 | 9.79 | 5.59 | 0.02 | 0.00 | 0.00 | 6.69 | 0.02 | 98.96 |
| HAFSZ-17 | » | » | 20.0 | » | Bdy | 60.01 | 10.41 | 3.69 | 11.41 | 0.00 | 7.85 | 0.06 | 0.06 | 0.00 | 5.09 | 0.04 | 98.52 |
| HAFCSZ-17 | » | » | 20.0 | » | Zrn (Bdy), Bdy | 56.23 | 7.57 | 5.32 | 8.43 | 9.09 | 4.83 | 0.02 | 0.00 | 0.00 | 7.30 | 0.03 | 98.76 |
| HRFZ-16 | 1400 | –5.27 | 21.0 | K-Si | Zrn (Bdy) | 57.51 | 10.80 | 2.35 | 10.00 | 10.69 | 0.09 | 0.01 | 2.02 | 0.02 | 5.09 | 0.05 | 98.56 |
| HAFSZ-16 | » | » | 21.0 | » | Zrn (Bdy) | 60.49 | 11.56 | 4.60 | 13.29 | 0.07 | 0.18 | 0.01 | 4.79 | 0.01 | 3.62 | 0.01 | 98.60 |
| HAFCSZ-16 | » | » | 21.0 | » | Zrn (Bdy) | 58.92 | 8.36 | 4.72 | 9.26 | 10.05 | 0.10 | 0.01 | 2.33 | 0.02 | 5.27 | 0.04 | 99.00 |
Примечание. Одинаковые номера образцов означают, что все они получены в одной и той же плавке; * среднее между измерениями ячейкой до и после эксперимента; **фазы: Zrn – циркон, (Bdy) – бадделеит в ядре циркона, Bdy – бадделеит как отдельная фаза, Sil – кристаллический SiO2, En – энстатит, Ol – оливин.
РЕЗУЛЬТАТЫ ЭКСПЕРИМЕНТОВ И ИХ ОБСУЖДЕНИЕ
Серия опытов по определению влияния К на растворимость циркона. Все экспериментальные стекла этой серии насыщены цирконом, который является единственной кристаллической фазой. На рис. 1 показана зависимость содержания ZrO2 в стеклах от содержания K2O. Все точки за исключением самого короткого опыта с безкалиевым составом (SAZ-7) лежат на одной прямой, характеризующей влияние калия на растворимость циркона при фиксированной температуре 1400°С. Заметим, что богатый K состав с этой же выдержкой (SAZK-7) лежит на единой прямой со всеми остальными составами. Таким образом, для этого расплава, в отличие от безкалиевого, 24 ч выдержи оказалось достаточным для достижения равновесия. Это не удивительно: добавление К2О, сильного оксида-модификатора, существенно понижает степень полимеризации расплава, понижает его вязкость и делает достижение равновесия с кристаллическими фазами более быстрым.
Рис. 1.
Влияние содержания K2О на растворимость циркона в расплавах SAZ (низкокалиевые) и SAZK (высококалиевые). Очевидно, что состав SAZ с самой короткой выдержкой (24 ч) не является равновесным (см. детали в тексте).
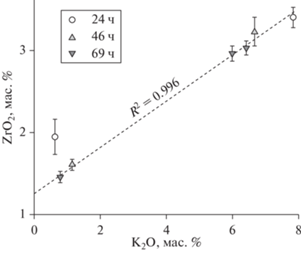
Все равновесные точки на рис. 1 идеально (R2 = = 0.996) описываются зависимостью:
(2)
$~{{C}_{{{\text{Zr}}{{{\text{O}}}_{{\text{2}}}}}}} = 0.281{{C}_{{{{{\text{K}}}_{{\text{2}}}}{\text{O}}}}} + 1.265,$где Сi – содержание соответствующего оксида в мас. %. Из уравнения (2) следует, что повышение содержания К2О в расплаве от нуля до 8 мас. % увеличивает растворимость циркона в расплаве почти в 3 раза, от 1.3 до 3.5 мас. % ZrO2.
Серия опытов по сравнению влияния К и Na на растворимость циркона. Практически все экспериментальные образцы содержат циркон (Zrn) и бадделеит (Bdy). Бадделеит чаще всего наблюдается в ядрах кристаллов Zrn в качестве захороненной фазы. Подобное соотношение наблюдали в своих опытах (Borisov, Aranovich, 2019). Однако в некоторых образцах Bdy наблюдается в виде самостоятельной фазы. Кроме этих двух фаз в некоторых опытах также присутствуют кристаллический SiO2, оливин (в среднем Mg1.8Fe0.2SiO4) и энстатит (в среднем Mg0.9Fe0.1SiO3). Отметим, что в трех образцах, HRFZ-5, HRFZ-17 и HAFSZ-17, мы не нашли циркон. Строго говоря, эти опыты не должны использоваться для выяснения влияния состава на растворимость циркона. Мы предполагаем, однако, что кристаллы Zrn в этих образцах могли быть крайне немногочисленны либо были сполированы в ходе приготовления шашек, либо не вскрыты. Наше решение было использовать эти образцы в обсуждении, но в дальнейшем понять, отличаются ли данные по содержанию Zr в этих опытах от основной массы экспериментов.
Сравнение опытов без источника (метод “классической петли”) или с источником щелочей (метод “петля в тигле”) позволяет понять влияние натрия и калия на растворимость циркона в трех разных составах при трех разных температурах (рис. 2). Рисунки 2а и 2б демонстрируют, что в целом эффект щелочей сопоставим. Добавление как Na, так и K приводит к значительному увеличению растворимости циркона в расплаве.
Рис. 2.
Влияние содержания щелочей на растворимость циркона в расплавах HRFZ (а), HAFCSZ (б) и HAFSZ (в). Na – опыты с источником Na2O–SiO2, K – c источником K2O–SiO2 (см. детали в тексте).
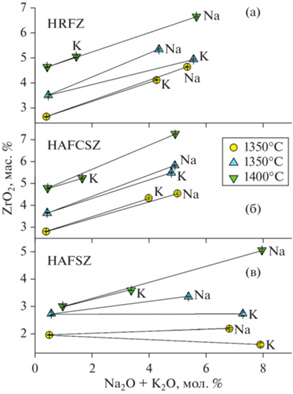
Неожиданно противоположный тренд демонстрируют образцы HAFSZ-1 (бесщелочной) и HAFSZ-4 (К-источник), см. рис. 2в. Дело в том, что при 1300°С в обр. HAFSZ-4 дополнительно кристаллизуется оливин, что приводит к резкому изменению валового состава стекла. В частности, содержание SiO2 в этом стекле возрастает, а содержание MgO резко уменьшается, по сравнению с таковым в стекле, обр. HAFSZ-4, что и приводит к уменьшению растворимости циркона, несмотря на увеличение содержания калия. Мы можем прояснить ситуацию следующим образом. Все стекла, обр. HAFSZ (=HAF + SiO2 + Zrn ± Na2O ± K2O) и обр. HAFCSZ (=HAF + CaO + SiO2 + Zrn ± Na2O ± K2O), – это модификации исходного состава HAF. Кроме температуры (от 1300 до 1400°С) мы имеем переменными ${{X}_{{{\text{Si}}{{{\text{O}}}_{{\text{2}}}}}}}$, XCaO, ${{X}_{{{\text{N}}{{{\text{a}}}_{{\text{2}}}}{\text{O}}}}}$ и ${{X}_{{{{{\text{K}}}_{{\text{2}}}}{\text{O}}}}}$. Поскольку во многих опытах кристаллизация дополнительных фаз пироксена и оливина привела к серьезным вариациям оксида магния, его также следует добавить в качестве переменной. Мы нашли, что все 18 стекол данного состава отлично (R2 = 0.991) описываются единым уравнением:
(3)
$\begin{gathered} \lg {{C}_{{{\text{Zr}}{{{\text{O}}}_{{\text{2}}}}}}}\left( {{\text{мас}}.\,\% } \right) = {{ - 6102} \mathord{\left/ {\vphantom {{ - 6102} {T({\text{K}})}}} \right. \kern-0em} {T({\text{K}})}} + 1.29({{{{X}_{{{\text{MgO}}}}}} \mathord{\left/ {\vphantom {{{{X}_{{{\text{MgO}}}}}} {{{X}_{{{\text{Si}}{{{\text{O}}}_{{\text{2}}}}}}}}}} \right. \kern-0em} {{{X}_{{{\text{Si}}{{{\text{O}}}_{{\text{2}}}}}}}}}) + \\ + \,\,1.82({{{{X}_{{{\text{CaO}}}}}} \mathord{\left/ {\vphantom {{{{X}_{{{\text{CaO}}}}}} {{{X}_{{{\text{Si}}{{{\text{O}}}_{{\text{2}}}}}}}}}} \right. \kern-0em} {{{X}_{{{\text{Si}}{{{\text{O}}}_{{\text{2}}}}}}}}}) + 2.70({{{{X}_{{{\text{N}}{{{\text{a}}}_{{\text{2}}}}{\text{O}}}}}} \mathord{\left/ {\vphantom {{{{X}_{{{\text{N}}{{{\text{a}}}_{{\text{2}}}}{\text{O}}}}}} {{{X}_{{{\text{Si}}{{{\text{O}}}_{{\text{2}}}}}}}}}} \right. \kern-0em} {{{X}_{{{\text{Si}}{{{\text{O}}}_{{\text{2}}}}}}}}}) + 2.51({{{{X}_{{{{{\text{K}}}_{{\text{2}}}}{\text{O}}}}}} \mathord{\left/ {\vphantom {{{{X}_{{{{{\text{K}}}_{{\text{2}}}}{\text{O}}}}}} {{{X}_{{{\text{Si}}{{{\text{O}}}_{{\text{2}}}}}}}}}} \right. \kern-0em} {{{X}_{{{\text{Si}}{{{\text{O}}}_{{\text{2}}}}}}}}}) + 3.67. \\ \end{gathered} $Сравнение экспериментальных данных по растворимости циркона с рассчитанными по уравнению (3) показано на рис. 3. Мы видим, что образцы HAFSZ-1 и HAFSZ-4, демонстрирующие аномальный тренд на рис. 2в, описываются уравнением (3) ничуть не хуже остальных образцов (ошибка <2σ). Таким образом, “аномальное” понижение растворимости Zrn в расплаве при повышении содержания К действительно связано с влиянием на растворимость циркона других компонентов расплава. На рис. 3. также отмечен обр. HAFSZ-17, имеющий только Bdy в равновесии с расплавом. Как и остальные образцы на рисунке, он также показывают расчетную ошибку менее 2σ.
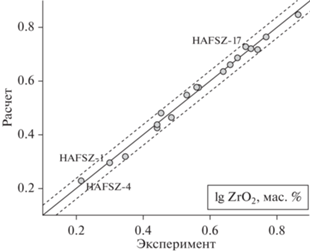
Рис. 3.
Сравнение экспериментальных данных по растворимости циркона в расплавах HAFCSZ и HAFSZ с рассчитанными по уравнению (3). Заметим, что образцы HAFSZ-1 и HAFSZ-4 (демонстрирующие аномальный тренд на рис. 2в), а также обр. HAFSZ-17 (имеющий только Bdy в равновесии с расплавом) показывают расчетную ошибку менее 2σ (см. детали в тексте).
Уравнение (3) позволяет напрямую сравнить влияние Na и K на растворимость циркона. Мы видим, что эмпирические коэффициенты для щелочей (dNa = 2.70 ± 0.15, dK = 2.51 ± 0.22, 1σ) совпадают в пределах ошибки, что предполагает очень похожий эффект добавления щелочей на растворимость Zrn.
Наконец, найдем уравнение регрессии в форме (3) для всех составов, рассматриваемых в работе. Поскольку в общей базе данных суммарное FeO варьирует от 0 до 7.6 мас. %, параметр ${{{{X}_{{{\text{FeO}}}}}} \mathord{\left/ {\vphantom {{{{X}_{{{\text{FeO}}}}}} {{{X}_{{{\text{Si}}{{{\text{O}}}_{{\text{2}}}}}}}}}} \right. \kern-0em} {{{X}_{{{\text{Si}}{{{\text{O}}}_{{\text{2}}}}}}}}}$ следует добавить в качестве переменной. Итак, 33 наших стекла неплохо (R2 = 0.946) описываются уравнением:
(4)
$\begin{gathered} \lg {{C}_{{{\text{Zr}}{{{\text{O}}}_{{\text{2}}}}}}}\left( {{\text{мас}}.{\text{ }}\% } \right) = \\ = {{ - 6926} \mathord{\left/ {\vphantom {{ - 6926} {T({\text{K}})}}} \right. \kern-0em} {T({\text{K}})}} + 1.26({{{{X}_{{{\text{FeO}}}}}} \mathord{\left/ {\vphantom {{{{X}_{{{\text{FeO}}}}}} {{{X}_{{{\text{Si}}{{{\text{O}}}_{{\text{2}}}}}}}}}} \right. \kern-0em} {{{X}_{{{\text{Si}}{{{\text{O}}}_{{\text{2}}}}}}}}}) + \\ + \,\,0.99({{{{X}_{{{\text{MgO}}}}}} \mathord{\left/ {\vphantom {{{{X}_{{{\text{MgO}}}}}} {{{X}_{{{\text{Si}}{{{\text{O}}}_{{\text{2}}}}}}}}}} \right. \kern-0em} {{{X}_{{{\text{Si}}{{{\text{O}}}_{{\text{2}}}}}}}}}) + 1.71({{{{X}_{{{\text{CaO}}}}}} \mathord{\left/ {\vphantom {{{{X}_{{{\text{CaO}}}}}} {{{X}_{{{\text{Si}}{{{\text{O}}}_{{\text{2}}}}}}}}}} \right. \kern-0em} {{{X}_{{{\text{Si}}{{{\text{O}}}_{{\text{2}}}}}}}}}) + \\ + \,\,2.77({{{{X}_{{{\text{N}}{{{\text{a}}}_{{\text{2}}}}{\text{O}}}}}} \mathord{\left/ {\vphantom {{{{X}_{{{\text{N}}{{{\text{a}}}_{{\text{2}}}}{\text{O}}}}}} {{{X}_{{{\text{Si}}{{{\text{O}}}_{{\text{2}}}}}}}}}} \right. \kern-0em} {{{X}_{{{\text{Si}}{{{\text{O}}}_{{\text{2}}}}}}}}}) + 2.81({{{{X}_{{{{{\text{K}}}_{{\text{2}}}}{\text{O}}}}}} \mathord{\left/ {\vphantom {{{{X}_{{{{{\text{K}}}_{{\text{2}}}}{\text{O}}}}}} {{{X}_{{{\text{Si}}{{{\text{O}}}_{{\text{2}}}}}}}}}} \right. \kern-0em} {{{X}_{{{\text{Si}}{{{\text{O}}}_{{\text{2}}}}}}}}}) + 4.15. \\ \end{gathered} $Отметим, что все три образца, имеющие только Bdy в равновесии с расплавом, показывают расчетную ошибку менее 2σ. Это подтверждает правильность нашего решения включить образцы, где видимый циркон отсутствует, в общий анализ.
На рис. 4 мы показали зависимость величины эмпирических параметров di из уравнения (4) от основности индивидуальных оксидов λi (значения взяты из работы Mills, 1993). Теперь, пользуясь уравнением (4) и рис. 4, коротко обсудим корректность параметров M, G и λ, используемых различными авторами для описания влияния состава расплава на растворимость циркона.
Рис. 4.
Корреляция оптической основности оксидов (λi) и эмпирических коэффициентов di для соотношений ${{{{X}_{{{\text{оксид}}}}}} \mathord{\left/ {\vphantom {{{{X}_{{{\text{оксид}}}}}} {{{X}_{{{\text{Si}}{{{\text{O}}}_{{\text{2}}}}}}}}}} \right. \kern-0em} {{{X}_{{{\text{Si}}{{{\text{O}}}_{{\text{2}}}}}}}}}$ в уравнении (4).
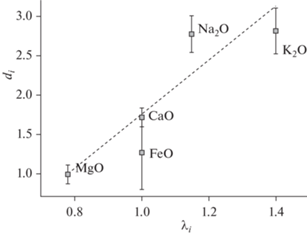
Итак, эмпирические коэффициенты для щелочей (dNa = 2.77 ± 0.23, dK = 2.81 ± 0.29, 1σ) совпадают в пределах ошибки, т.е. (Watson, Harrison, 1983) справедливо предположили в своем параметре M = (Na + K + 2Ca)/(AlSi) одинаковое влияние щелочей на растворимость Zrn. Однако соотношение dNa/dCa ≈ 1.6, т.е. влияние Са на параметр М может быть несколько завышено.
Соотношения dNa/dFe ≈ 2.2 и dNa/dMg ≈ 2.8. Таким образом, (Gervasoni et al., 2016), предложивший параметр G = (3Al2O3 + SiO2)/(Na2O + K2O + CaO + + MgO + FeO), слишком упрощает ситуацию, полагая одинаковым влияние сильных (Na2O и K2O) и слабых (CaO, MgO, FeO) оксидов-модификаторов на растворимость Zrn.
Наконец, на рис. 4 мы видим неплохую линейную зависимость эмпирических параметров di из уравнения (4) от основности индивидуальных оксидов λi. Таким образом, модель (Crisp, Berry, 2022), описывающая растворимость циркона от оптической основности расплава λ, в целом должна работать. Тем не менее наши эксперименты ясно показали одинаковое (в пределах ошибки) влияние Na2O и K2O на растворимость циркона, что не учитывает модель (Crisp, Berry, 2022).
ЗАКЛЮЧЕНИЕ
В температурном интервале 1300–1400°С при 1 атм. общего давления экспериментально исследовано влияние щелочей на растворимость циркона в модельных многокомпонентных силикатных расплавах. Использованы как метод “классической петли”, так и метод “петля в тигле”.
Единое уравнение (4), описывающее растворимость циркона в наших экспериментах (33 состава расплава), дает одинаковые в пределах ошибки эмпирические коэффициенты для щелочей (dNa = = 2.77 ± 0.23, dK = 2.81 ± 0.29, 1σ). Таким образом, Na2O и K2O повышают растворимость циркона в расплавах и их влияние сопоставимо.
Коротко рассмотрены достоинства и недостатки предложенных в литературе параметров, описывающих влияние состава расплава на растворимость циркона.
Уравнение (4) получено для узкого круга составов и не призвано заменить собою более сложные модели, предложенные в литературе. Однако проведенные эксперименты могут быть в дальнейшем использованы для новой калибровки растворимости циркона в природных силикатных расплавах.
Благодарности. Авторы выражают благодарность Ренату Альмееву (Ганновер) и Наталии Кошляковой (Москва) за помощь в микрозондовом анализе. Авторы признательны Олегу Луканину (ГЕОХИ РАН) за конструктивное обсуждение результатов работы.
Источники финансирования. Работа поддержана Российским Национальным фондом (грант № 22-17-00052).
Список литературы
Борисов А.А. Экспериментальное исследование распределения K и Na между смешивающимися жидкостями // Петрология. 2008. Т. 16. № 6. С. 593–605.
Борисов А.А. Зависимость коэффициентов активности щелочей от кремнекислотности и глиноземистости расплавов: экспериментальное исследование // Петрология. 2009. Т. 17. № 6. С. 623–635.
Boehnke P., Watson E.B., Trail D. et al. Zircon saturation re-revisited // Chem. Geol. 2013. V. 351. P. 324–334.
Borisov A., Aranovich L. Zircon solubility in silicate melts: new experiments and probability of zircon crystallization in deeply evolved basic melts // Chem. Geol. 2019. V. 510. P. 103–112.
Borisov A., Lahaye Y., Palme H. The effect of sodium on the solubilities of metals in silicate melts // Amer. Mineral. 2006. V. 91. P. 762–771.
Borisov A., Pack A., Kropf A., Palme H. Partitioning of Na between olivine and melt: an experimental study with application to the formation of meteoritic Na2O-rich chondrule glass and refractory forsterite grains // Geochim. Cosmochim. Acta. 2008. V. 72. P. 5558–5573.
Borisov A., Behrens H., Holtz F. Effects of strong network modifiers on Fe3+/Fe2+ in silicate melts: an experimental study // Contrib. Mineral. Petrol. 2017. V. 172. Article 34.
Borisov A., Behrens H., Holtz F. Ferric/ferrous ratio in silicate melts: a new model for 1 atm data with special emphasis on the effects of melt composition // Contrib. Mineral. Petrol. 2018. V. 173. Article 98.
Crisp L.J., Berry A.J. A new model for zircon saturation in silicate melts // Contrib. Mineral. Petrol. 2022. V. 177. Article 71.
Corrigan G., Gibb F.G.F. The loss of Fe and Na from a basaltic melt during experiments using the wire-loop method // Mineral. Mag. 1979. V. 43. P. 121–126.
Gervasoni F., Klemme S., Rocha-Júnior E.R.V., Berndt J. Zircon saturation in silicate melts: a new and improved model for aluminous and alkaline melts // Contrib. Mineral. Petrol. 2016. V. 171. Article 21.
Koshlyakova A., Sobolev A., Krasheninnikov S. et al. Ni partitioning between olivine and highly alkaline melts: an experimental study // Chem. Geol. 2022. V. 587. Article 120615.
Mills K.C. The influence of structure on the physico-chemical properties of slags // ISIJ International. 1993. V. 33. P. 148–155.
Watson E.B., Harrison T.M. Zircon saturation revisited: temperature and composition effects in a variety of crustal magma types // Earth Planet. Sci. Lett. 1983. V. 64. P. 295–304.
Watson E.B. Zircon saturation in felsic liquids: experimental results and applications to trace element geochemistry // Contrib. Mineral. Petrol. 1979. V. 70. P. 407–419.
Дополнительные материалы отсутствуют.


