Почвоведение, 2020, № 7, стр. 816-827
Влияние водорастворимых компонентов почв на размер и электрокинетический потенциал наноалмазов
a МГУ им. М.В. Ломоносова
119991 Москва, Ленинские горы, 1, Россия
b Институт биохимии РАН им. А.Н. Баха, Федеральный исследовательский центр
“Фундаментальные основы биотехнологии” Российской академии наук
119071 Москва, Ленинский пр., 33, Россия
* E-mail: knat@darvodgeo.ru
Поступила в редакцию 13.11.2019
После доработки 13.11.2019
Принята к публикации 30.01.2020
Аннотация
Возрастающие темпы применения наночастиц привели к необходимости рассматривать их как токсиканты нового класса. Наноалмазы занимают особое положение, так как используются в товарах широкого потребления, например, в горюче-смазочных материалах, что увеличивает риск загрязнения почв этими наночастицами. Цель работы: оценка влияния водорастворимых компонентов почв на электрокинетический потенциал (ζ-потенциал) и размер наноалмазов детонационного синтеза. Объектами исследования служили водные экстракты из 15-ти образцов почв зонального ряда. При внесении наноалмазов в водные экстракты почв наблюдали рост средневзвешенного гидродинамического диаметра наноалмазов с 24 до 69–683 нм и падение ζ-потенциала по абсолютной величине с –22 до –(11.2–19.5) мВ; в одном случае был отмечен рост этого показателя по абсолютной величине до –34.5 мВ. Наибольшее увеличение размеров наноалмазов наблюдали в водных экстрактах с высокими рН и отношением Ca/(Fe + Al). На основании установленных обратных корреляционных связей ζ-потенциала наноалмазов с коэффициентом экстинкции ${\text{E}}_{{465}}^{{{\text{OC}},0.01\% }}$ почвенного растворенного органического вещества и содержанием железа в водных экстрактах было высказано предположение о возможности повышения стабильности наноалмазов в почвенных растворах в присутствии низкомолекулярных компонентов растворенного органического вещества и при высоких концентрациях железа. Полученные результаты позволяют предполагать коагуляцию и уменьшение подвижности наноалмазов в почвах вследствие их взаимодействия с водорастворимыми компонентами почв; исключение могут составлять солонцы (Solonetz), где возможно увеличение подвижности наноалмазов.
ВВЕДЕНИЕ
Использование нанотехнологий в последние десятилетия привело к интенсивному развитию многих сфер человеческой деятельности, прежде всего медицины и аналитической химии, так как позволило разработать принципиально новые способы доставки лекарств и методы диагностики [27]. Возрастающие темпы производства и применения используемых в этих технологиях наночастиц привели к необходимости рассматривать их как токсиканты нового класса, которые могут прямо или косвенно наносить ущерб здоровью человека и окружающей среде [2, 4, 12]. Среди получающих все большее распространение наноматериалов алмазные наночастицы, или наноалмазы (НА), занимают особое положение [20]. Наряду с традиционными для наноматериалов областями применения, связанными с получением достаточно дорогостоящих продуктов, занимающих узкие ниши на рынке (лекарства, катализаторы, сенсоры и т.п.), НА могут быть использованы также в производстве товаров широкого потребления, таких как горюче-смазочные материалы (ГСМ). НА стали основой для создания нового класса присадок, разработанных для защиты и восстановления узлов трения в различных механизмах и машинах за счет улучшения антифрикционных свойств и трибологических характеристик смазочных материалов [14]. Возможности российских производителей по выпуску НА сейчас оцениваются как 5 т/год, а среди потребляемых в России углеродных наноматериалов доля НА максимальна и составляет 91% [3]. Аналогичные тенденции наблюдаются и в остальном мире: НА рассматриваются как один из наиболее привлекательных углеродных материалов для нанотехнологий [8]. Основной причиной этого, скорее всего, является возможность получения НА с использованием относительно дешевой технологии, основанной на детонации взрывчатых веществ и разработанной российскими учеными еще в 60-х гг. прошлого века [1]. Таким образом, НА относятся к наночастицам с высоким риском попадания в окружающую среду.
Исследования, направленные на оценку взаимодействия НА с объектами окружающей среды, показывают, что НА вызывают окислительный стресс у бактерий [15], не токсичны для нематод Caenorhabditis elegans [18], но могут быть токсичны для растений [6], рыб [19] и млекопитающих [31]. Однако нами не было найдено работ, связанных с изучением другого важного аспекта этого взаимодействия – оценкой поведения НА в различных объектах окружающей среде, в том числе в почве.
Известно, что поведение наночастиц в окружающей среде определяется, прежде всего, их коллоидной стабильностью [30]: подвижность наночастиц в почвенном растворе контролируется скоростью их осаждения и агрегации, которая зависит от pH, общей минерализованности, катионного состава и характеристик растворенного органического вещества (РОВ) [24, 26, 30]. Поэтому целью работы явилась оценка влияния водорастворимых компонентов почв на электрокинетический потенциал и размер НА.
ОБЪЕКТЫ И МЕТОДЫ
Выделение водорастворимых веществ из почв и их характеристика. Для исследования использовали образцы из слоя 0–5 см почв различных почвенно-географических зон. Всего было использовано 15 образцов (табл. 1): 3 образца дерново-подзолистых почв (ДП, Albic Retisol), 2 – серых лесных (СЛ, Haplic Phaeozem), 1 – чернозема типичного (ЧТ, Chernozems Chernic), 3 – черноземов обыкновенных (ЧО, Endocalcic Chernozem), 2 – черноземов выщелоченных (ЧВ, Luvic Chernic Phaeozem), 1 – лугово-черноземной солонцеватой почвы (ЛЧ, Gleyic Chernozem (Protosodic), 2 – каштановых почв (К, Haplic Kastanozem) и 1 солонца (СОЛ, Solonetz (Humic)). Места пробоотбора, краткое описание почв, их агрохимическая характеристика и гранулометрический состав приведены в литературе [5]. Выделение водорастворимых веществ проводили согласно методике получения почвенных растворов, используемой для изучения их компонентов с наночастицами [10]. Для этого навески воздушно-сухой почвы, пропущенной через сито с диаметром ячеек 2 мм, массой 2 г помещали в стерильные полипропиленовые пробирки и приливали 10 мл дистиллированной воды. Пробирки интенсивно встряхивали и оставляли для экстракции на 24 ч, после чего проводили центрифугирование (15 мин, 1000 g) и фильтрование через мембранные фильтры с диаметром пор 0.45 мкм (Millex-HP, Millipore, Ирландия) для отделения коллоидных частиц. Несмотря на то, что анализ водной вытяжки 1 : 5 (в/о), использованный в данной работе, не дает адекватного представления об истинном составе почвенной жидкой фазы, именно анализ экстрактов, получаемых с фиксированным отношением почвы и воды 1 : 5, наиболее часто используется при исследовании почвенного РОВ [11], а также минерализованности, насыщенности натрием и щелочности почвы, поскольку он требует меньше времени и лучше воспроизводим, чем анализ насыщенных экстрактов [29].
Таблица 1.
Свойства водных экстрактов почв, использованных в работе (среднее ± стандартное отклонение, n = 3)
| Ин-декс | pH | ОС, мг/л | ${\text{E}}_{{465}}^{{{\text{OC}},0.01\% }}$ | SUVA254, л/(мг OC × м) |
σ, мкСм/см | НС, мг/л | Al | Ca | Fe | K | Mg | Na | Si |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| мМ | |||||||||||||
| ДП1* | 5.3 ± 0.1 | 53 ± 1 | 0.018 | 0.71 | 55 ± 4 | 1.1 ± 0.1 | 0.10 ± 0.02 | 0.27 ± 0.04 | 0.05 ± 0.01 | 0.07 ± 0.01 | 0.08 ± 0.08 | 9.5 ± 1.4 | 0.05 ± 0.01 |
| ДП2 | 4.8 ± 0.1 | 154 ± 2 | 0.010 | 0.29 | 167 ± 7 | 0.2 ± 0.1 | 0.14 ± 0.03 | 0.42 ± 0.05 | 0.03 ± 0.01 | 0.10 ± 0.02 | 0.14 ± 0.03 | 9.7 ± 1.5 | 0.06 ± 0.01 |
| ДП3 | 5.2 ± 0.1 | 117 ± 2 | 0.017 | 0.62 | 111 ± 2 | 0.5 ± 0.1 | 0.25 ± 0.05 | 0.36 ± 0.06 | 0.10 ± 0.02 | 0.19 ± 0.04 | 0.14 ± 0.03 | 10.3 ± 1.6 | 0.08 ± 0.02 |
| СЛ1 | 5.8 ± 0.1 | 139 ± 2 | 0.004 | 0.49 | 321 ± 4 | 0.9 ± 0.1 | 0.13 ± 0.03 | 1.08 ± 0.16 | 0.05 ± 0.01 | 0.28 ± 0.04 | 0.36 ± 0.07 | 9.8 ± 1.5 | 0.07 ± 0.01 |
| СЛ2* | 6.5 ± 0.1 | 45 ± 1 | 0.012 | 1.04 | 110 ± 1 | 5.8 ± 0.1 | 0.58 ± 0.09 | 0.55 ± 0.08 | 0.19 ± 0.03 | 0.27 ± 0.04 | 0.14 ± 0.03 | 9.6 ± 1.4 | 0.04 ± 0.01 |
| ЧТ | 6.2 ± 0.1 | 57 ± 1 | 0.010 | 0.77 | 102 ± 1 | 1.1 ± 0.1 | 0.32 ± 0.06 | 0.53 ± 0.08 | 0.15 ± 0.03 | 0.10 ± 0.02 | 0.15 ± 0.03 | 9.5 ± 1.4 | 0.08 ± 0.02 |
| ЧО1 | 6.7 ± 0.1 | 148 ± 2 | 0.018 | 0.60 | 262 ± 2 | 3.1 ± 0.1 | 0.13 ± 0.03 | 1.03 ± 0.15 | 0.05 ± 0.01 | 0.48 ± 0.07 | 0.38 ± 0.08 | 8.6 ± 1.3 | 0.05 ± 0.01 |
| ЧО2* | 7.5 ± 0.1 | 44 ± 1 | 0.002 | 0.92 | 177 ± 1 | 10.7 ± 0.2 | 0.07 ± 0.01 | 0.82 ± 0.12 | 0.03 ± 0.01 | 0.12 ± 0.02 | 0.16 ± 0.03 | 9.6 ± 1.4 | 0.06 ± 0.01 |
| ЧО3 | 6.7 ± 0.1 | 100 ± 1 | 0.015 | 0.48 | 203 ± 3 | 1.5 ± 0.2 | 0.09 ± 0.02 | 0.88 ± 0.13 | 0.04 ± 0.01 | 0.09 ± 0.02 | 0.27 ± 0.05 | 9.3 ± 1.4 | 0.06 ± 0.01 |
| ЛЧ | 6.7 ± 0.1 | 75 ± 1 | 0.010 | 0.58 | 185 ± 3 | 10.8 ± 0.2 | 0.10 ± 0.02 | 0.78 ± 0.12 | 0.04 ± 0.01 | 0.06 ± 0.01 | 0.23 ± 0.04 | 10.4 ± 1.6 | 0.07 ± 0.02 |
| ЧВ1* | 7.5 ± 0.1 | 44 ± 1 | 0.016 | 1.00 | 231 ± 4 | 17.9 ± 0.3 | 0.05 ± 0.01 | 0.96 ± 0.14 | 0.02 ± 0.01 | 0.09 ± 0.02 | 0.37 ± 0.07 | 9.7 ± 1.5 | 0.06 ± 0.01 |
| ЧВ2 | 6.2 ± 0.1 | 59 ± 9 | 0.044 | 0.52 | 637 ± 11 | 10.2 ± 0.2 | 0.24 ± 0.05 | 2.11 ± 0.31 | 0.10 ± 0.02 | 0.30 ± 0.06 | 0.51 ± 0.10 | 11.5 ± 1.7 | 0.06 ± 0.01 |
| К1* | 8.2 ± 0.2 | 34 ± 1 | 0.013 | 0.86 | 349 ± 7 | 32.5 ± 0.5 | 0.01 ± 0.01 | 1.54 ± 0.23 | 0.01 ± 0.01 | 0.27 ± 0.04 | 0.34 ± 0.07 | 9.7 ± 1.5 | 0.06 ± 0.01 |
| К2 | 7.6 ± 0.1 | 23 ± 1 | 0.010 | 1.17 | 137 ± 6 | 12.7 ± 0.2 | 0.04 ± 0.01 | 0.64 ± 0.09 | 0.02 ± 0.01 | 0.06 ± 0.01 | 0.17 ± 0.03 | 9.5 ± 1.4 | 0.06 ± 0.01 |
| СОЛ | 7.4 ± 0.1 | 73 ± 1 | 0.039 | 3.76 | 107 ± 2 | 2.0 ± 0.1 | 3.67 ± 0.55 | 0.38 ± 0.06 | 1.59 ± 0.24 | 0.63 ± 0.09 | 0.82 ± 0.12 | 11.7 ± 1.8 | 0.11 ± 0.02 |
Для обозначения водных экстрактов к сокращенному названию почвы, из которой они были получены, добавляли порядковый номер, например, водные экстракты ДП1, ДП2, ДП3. Часть водных вытяжек была получена из почв, вовлеченных в сельскохозяйственное использование (ДП1, СЛ2, ЧО2, ЧВ1 и К1).
Определение содержания органического и неорганического углерода (ОС и НС) в полученных экстрактах проводили с использованием анализатора TOC-LCPN (Shimadzu, Япония); в качестве стандарта использовали гидрофталат калия. Спектры поглощения в ультрафиолетовой и видимой области спектра регистрировали на спектрофотометре 512 UV/Vis Spectrophotometer PortLab (Portlab, Великобритания) в кварцевой кювете с длиной оптического пути 1 см. Для характеристики растворенного органического вещества на основании полученных спектров рассчитывали коэффициент экстинкции ${\text{E}}_{{465}}^{{{\text{OC}},0.01\% }}$ – поглощение при концентрации органического углерода 0.01% при длине волны 465 нм, отражающий молекулярную массу РОВ, и характеризующий гидрофобность параметр SUVA254 – отношение поглощения при 254 нм к концентрации ОС [11]. Водородный показатель pH определяли на рН-метре Hanna pH211 (HannaInstruments, США). Минеральный состав (Al, As, B, Ca, Cd, Co, Cr, Cu, Fe, Hg, I, K, Li, Mg, Mn, Na, Ni, Pb, Se, Si, Sn, Sr, V, Zn) экстрактов определяли методом масс-спектрометрии с индуктивно связанной плазмой (МС-ИСП) на квадрупольном масс-спектрометре Nexion 300D (Perkin Elmer, США). Удельную электропроводность экстрактов σ измеряли на двуугловом анализаторе размеров частиц и молекул методом динамического рассеяния света с оптикой неинвазивного обратного рассеяния Zetasizer Nano ZS (Malvern, Великобритания).
Проведение экспериментов по взаимодействию НА с водорастворимыми веществами из почв. Для проведения экспериментов использовали НА марки RUDDM (Synthetic diamond powder RUDDM 0–150, Реал-Дзержинск, РФ), получаемые при взрыве литого заряда из смеси тринитротолуола и гексогена, характеризующиеся высокой дисперсионной устойчивостью и используемые в качестве добавки к смазкам и маслам, таким как “Карат-М” и “ССМР”. Суспензию НА с концентрацией 2.1 г/л готовили путем смешивания навески НА с дистиллированной водой с последующим озвучиванием (мощность 30 Вт, частота 37 кГц, продолжительность 1 ч) в ультразвуковой ванне S10H Elmasonic (Elmi, Латвия). 0.1 мл суспензии НА вносили к 1.5 мл водного экстракта из почв, получая таким образом суспензию с концентрацией 0.13 г/л. В качестве контроля использовали суспензию НА в дистиллированной воде. Повторность трехкратная. Суспензии НА в воде и водных экстрактах из почв оставляли при 25°C на 24 ч в режиме орбитального встряхивания со скоростью 5 об./мин на встряхивателе Intelli Mixer (Elmi, Латвия). Далее в суспензиях регистрировали спектры поглощения в ультрафиолетовой и видимой области спектра на спектрофотометре 512 UV/Vis Spectrophotometer Port Lab (Portlab, Великобритания) в кварцевой кювете с длиной оптического пути 1 см и измеряли параметры, отвечающие за коллоидную стабильность НА: размер и электрокинетический потенциал (ζ-потенциал) наночастиц (Zetasizer Nano ZS, Malvern, Великобритания). В качестве размера наночастиц использовали их среднечисловой гидродинамический диаметр (СЧГД), соответствующий диаметру частиц с максимальным содержанием, и средневзвешенный гидродинамический диаметр (СВГД), рассчитываемый на основании распределения частиц по размеру.
Обработка результатов включала в себя расчет средних значений и стандартных отклонений. Значимость влияния компонентов водной вытяжки на размер и ζ-потенциал НА оценивали с помощью однофакторного дисперсионного анализа с последующим расчетом наименьшей существенной разницы (НСР). Для оценки взаимосвязей между изучаемыми параметрами использовали корреляционный анализ. Коэффициент корреляции считали отличным от 0, если он превышал 0.53 или 0.55, что соответствует уровню значимости α = 0.05 при объеме корреляционного ряда 15 или 14 соответственно.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Характеристика водорастворимых веществ почв. Водные экстракты исследованных почв характеризовались широким разбросом значений по всем выбранным для их описания показателям (табл. 1), которые в целом, однако, соответствовали обычно приводимым в литературе данным [10, 11, 29]. Водородный показатель изменялся от кислого (4.8) до щелочного (8.2) и закономерно возрастал в зональном ряду почв от дерново-подзолистых через серые лесные и черноземы обыкновенные к каштановым. Концентрация ОС в водных экстрактах исследованных почв сельскохозяйственного использования лежала в диапазоне 34–53 мг/л и была ниже, чем в целинных и залежных почвах, для которых аналогичное варьирование составило 57–154 мг/л. В случае каштановых почв, напротив, содержание РОВ было выше в освоенном варианте. При пересчете концентрации ОС в водном экстракте на содержание РОВ в почве полученный интервал значений для всего ряда исследованных почв был 115–770 мг ОС/кг, что хорошо согласуется с приводимыми в литературе величинами, составляющими десятки–сотни мг ОС/кг [9]. Удельная электропроводность σ изменялась от 55 (ДП1) до 637 мкСм/см (ЧВ2), что также соответствует опубликованному диапазону от 32 [23] до 3280 мкСм/см [29].
Значения SUVA254 для РОВ исследованных почв лежали в диапазоне 0.10–3.76 л/(мг OC × м), типичном для органического вещества почв и природных вод, для которых эти величины обычно составляют от 1 до 6 л/(мг OC × м) [13]. В целом можно сказать, что более высокие показатели SUVA254 были характерны для РОВ почв, вовлеченных в сельскохозяйственное использование. Например, для РОВ СЛ1, полученного из серой лесной целинной почвы, SUVA254 составил 0.49 л/(мг OC × м), а для СЛ2, выделенной из серой лесной освоенной – 1.04 л/(мг OC × м). Для аналогичной пары РОВ черноземов выщелоченных – 0.52 и 1.00 л/(мг OC × м) соответственно, для черноземов обыкновенных – 0.60 и 0.92 л/(мг OC × м). Исключение составила каштановая почва, где для РОВ при переходе от целинной к освоенной почве наблюдали уменьшение SUVA254 с 1.17 до 0.96 л/(мг OC × м). Так как увеличение SUVA254 обычно объясняют возрастанием содержания ароматических структур, то полученные результаты могут указывать на уменьшение в РОВ почв сельскохозяйственного использования относительного содержания алифатических фрагментов, связанное, по-видимому, с их большей доступностью к биодеградации [13].
Из исследованных минеральных элементов концентрация большинства не превышала 1 мкМ (As, B, Cd, Co, Cr, Cu, Hg, I, Li, Mn, Ni, Pb, Se, Sn, Sr, V, Zn), а их доля от общего содержания определяемых минеральных элементов – 1%. Поэтому далее рассматривали только основные элементы: Al, Ca, Fe, K, Mg, Na, и Si. Основным катионом в водных вытяжках был Na (8.59–11.72 мМ), далее следовал Ca (0.27–2.11 мМ). Ранее преобладание этих ионов в почвенном растворе было продемонстрировано на примере пойменных карбонатных (Calcic Fluvisols) и бурых (Endosalic Calcisols) почв [28]. Авторы объясняли этот факт высокими кларками Na и Ca в земной коре при одновременной высокой подвижности в почвенных условиях.
Было установлено, что водная вытяжка солонца отличается от всех остальных почв по минеральному составу, так характеризовалась содержанием Al, Fe и Si на 1–2 порядка больше, чем остальные почвы. Скорее всего, наблюдаемое отличие вызвано пептизацией почвенных коллоидов в присутствии натрия, концентрация которого была максимальной в водном экстракте из этой почвы. Полученные результаты хорошо согласуются с высокими значениями SUVA254, обнаруженными для РОВ солонца и указывают на то, что в случае солонца в водной вытяжке присутствуют коллоидные частицы с размером частиц меньше 0.45 мкм. Известно, что рост SUVA254 может быть обусловлен поглощением присутствующих в образце коллоидов при 254 нм [13].
Интересно отметить, что концентрации Ca, K, Mg и Si в водной вытяжке 1 : 5 были сопоставимы с таковыми, опубликованным для почвенных растворов, полученных методом прямого отжима из буроземов (Dystric Cambisols). Согласно представленным в работе [25] данным, средняя концентрация Ca, K, Mg и Si по 24 образцам составляла 0.525, 0.180, 0.125 и 0.036 мМ. Для исследованной выборки из 14 почв (исключая солонец) аналогичные величины были 1.188, 0.272, 0.297 и 0.043 мМ. Для Al и Na, однако, концентрации, определяемые в вытяжке, получаемой прямым отжимом, были на один порядок ниже, чем в водной вытяжке 1 : 5. Сравнение полученных результатов с анализом лизиметрических вод, проведенным для 42 различных европейских почв [16], показало, что концентрация Al, Ca, K, Mg и Na в водной вытяжке 1 : 5 была на один–два порядка больше.
Сопоставление характеристик водных вытяжек исследованных почв показало наличие прямой взаимосвязи SUVA254 и pH (r = 0.67). Обнаруженная корреляция хорошо согласуется с концептуальной моделью поведения РОВ, в которой при низких значениях pH органические соединения РОВ конденсируются, что приводит к ограничению доступности хромофоров свету; при высоком pH, напротив, РОВ находится преимущественно в развернутом состоянии и действию света подвержено большее количество хромофоров, что приводит к увеличению поглощения света [21].
Интересно отметить, что нами не было обнаружено корреляционной связи между удельной электропроводностью σ и концентрацией Na (r = 0.32), но была показана связь этого показателя с концентрацией Ca (r = 0.97). Ранее аналогичные наблюдения были сделаны для водных вытяжек 1 : 5 в работе [29], причем авторы отмечали, что в насыщенных пастах между концентрацией Na и удельной электропроводностью корреляция существует. По-видимому, концентрация натрия в разбавленных водных экстрактах 1 : 5 обусловлена, главным образом, его содержанием в земной коре, тогда как для кальция важную роль играют также процессы растворения его карбоната и сульфата [28]. Поэтому на фоне приблизительно равной концентрации Na в растворах в определении удельной электропроводности ведущую роль начинает играть Ca – второй по концентрации элемент. Действительно, для исследованного ряда почв отношение максимальной установленной концентрации Na в водной вытяжке к минимальной составило 1.3, тогда как для Ca этот показатель достигал 7.9.
Влияние водорастворимых веществ почв на размер и ζ-потенциал наноалмазов. НА в дистиллированной воде (контроль) характеризовались узким мономодальным распределением гидродинамического диаметра d с максимумом при 21 нм и рассчитанным СВГД 24 нм (рис. 1). Сходство значений СЧГД и СВГД наночастиц (отношение СВГД/СЧГД составило 1.1) в этом случае указывает на низкую полидисперсность системы и близость распределения НА по размерам к нормальному типу. В течение времени эксперимента суспензия была устойчива и изменений в распределении d не наблюдали. ζ-потенциал НА в дистиллированной воде был –22 мВ (табл. 2), что позволяет характеризовать их как наночастицы с низким ζ-потенциалом, склонные к коагуляции или флокуляции. Тем не менее, за время эксперимента ζ-потенциал, как и размер НА, в дистиллированной воде не менялся. Принимая во внимание, что ζ-потенциал отражает величину общего заряда в межфазной области на поверхности частицы [22], можно предположить возможность частичной миграции исследуемых НА в почвенных условиях, которые характеризуются присутствием отрицательно заряженных коллоидов и частиц.
Рис. 1.
Распределение НА в дистиллированной воде (сплошная линия) и в водных экстрактах почв (пунктирная линия) по данным динамического светорассеяния.
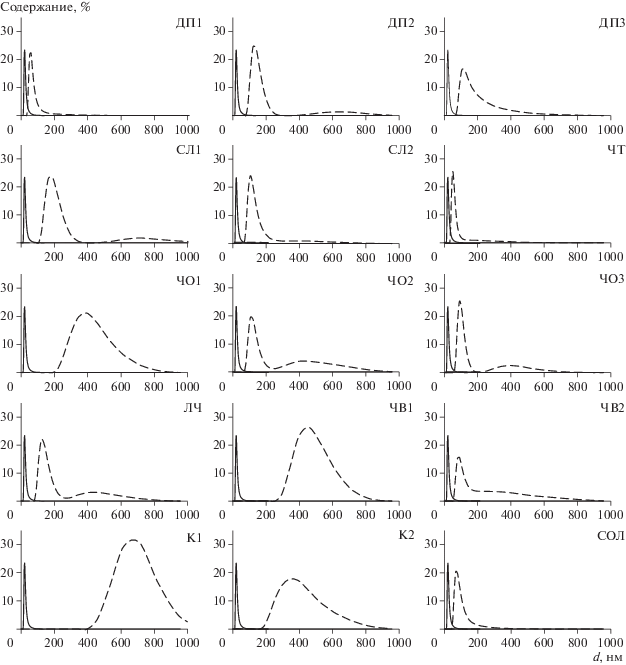
Таблица 2.
Гидродинамический диаметр d и ζ-потенциал НА в дистиллированной воде (контроль) и водных экстрактах использованных в работе почв
| Индекс | Гидродинамический диаметр d, нм | СВГД/СЧГД | ζ-потенциал, мВ | |
|---|---|---|---|---|
| СЧГД | СВГД | |||
| Контроль | 21 ± 0.4 | 24 ± 0.5 | 1.1 | –(22.0 ± 4.2) |
| ДП1* | 58 ± 1 | 69 ± 1 | 1.2 | –(19.5 ± 1.1) |
| ДП2 | 122 ± 2 | 164 ± 3 | 1.3 | –(11.9 ± 0.3) |
| ДП3 | 106 ± 2 | 169 ± 3 | 1.6 | –(16.9 ± 0.6) |
| СЛ1 | 190 ± 4 | 223 ± 4 | 1.2 | –(11.2 ± 0.8) |
| СЛ2* | 106 ± 2 | 139 ± 3 | 1.3 | –(18.2 ± 2.2) |
| ЧТ | 51 ± 1 | 69 ± 1 | 1.4 | –(15.4 ± 0.2) |
| ЧО1 | 396 ± 8 | 413 ± 8 | 1.0 | –(13.8 ± 0.4) |
| ЧО2* | 106 ± 2 | 200 ± 4 | 1.9 | –(13.2 ± 0.4) |
| ЧО3 | 91 ± 2 | 137 ± 3 | 1.5 | –(11.7 ± 0.5) |
| ЛЧ | 122 ± 2 | 188 ± 4 | 1.5 | –(12.3 ± 0.8) |
| ЧВ1* | 459 ± 9 | 472 ± 9 | 1.0 | –(11.9 ± 0.2) |
| ЧВ2 | 91 ± 2 | 172 ± 3 | 1.9 | –(12.7 ± 0.3) |
| К1* | 712 ± 14 | 683 ± 14 | 1.0 | –(11.7 ± 1.2) |
| К2 | 342 ± 7 | 391 ± 8 | 1.1 | –(12.4 ± 1.2) |
| СОЛ | 68 ± 1 | 93 ± 2 | 1.4 | –(34.5 ± 0.9) |
| НСР | 9 | 9 | – | 2.3 |
При внесении НА в водные экстракты почв во всех случаях происходило смещение пика распределения в сторону более высоких значений гидродинамического диаметра; наиболее ярко этот сдвиг был выражен для каштановой почвы К1. Соответственно, в этих условиях НА приобретали бóльшие размеры частиц (табл. 2). В ряде случаев было отмечено также возрастание отношения СВГД/СЧГД до величин, приближающихся к двум (ЧО2 и ЧВ2), что указывает на рост полидисперсности суспензии НА и отражает возможность образования агломератов наночастиц в присутствии водорастворимых компонентов почв. Этот процесс хорошо иллюстрируется появлением “плеча” на распределениях d: для водного экстракта ЧО2 такое плечо обнаруживалось в диапазоне 300–800 нм, для ЧВ2 – в диапазоне 200–700 нм.
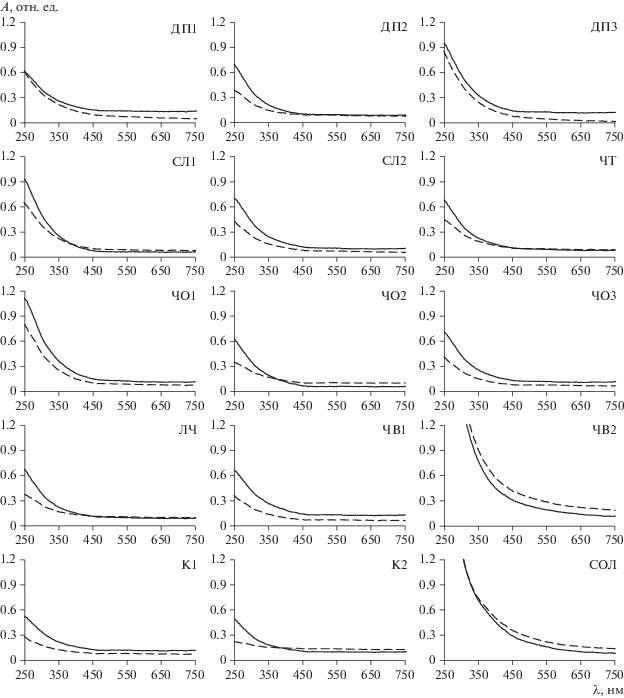
Наблюдаемое увеличение гидродинамического радиуса НА в водных экстрактах почв объясняется высокой сорбционной способностью наночастиц. Хорошо известно, что углеродные наночастицы активно сорбируют РОВ [7, 17] и присутствующие в растворе катионы металлов [32]. На процесс сорбции РОВ наночастицами указывает также тот факт, что практически во всех случаях поглощение суспензий НА в водных экстрактах почв при длине волны λ меньше 450 нм было меньше, чем можно было бы ожидать из суперпозиции электронных спектров поглощения НА и водных экстрактов, снятых индивидуально (рис. 2). Исключение составили образцы ЧВ2 и СОЛ. Для ЧВ2 ранее было показано образование агломератов наночастиц, вызывающее появление “плеча” на распределении НА по размерам (рис. 1) и приводящее к росту отношения СВГД/СЧГД, отражающего увеличение полидисперсности системы (табл. 2). Для ЧО2, также характеризующегося высоким отношением СВГД/СЧГД, был зафиксировано превышение оптических плотностей суспензии НА в водном экстракте над расчетными величинами при длинах волн более 400 нм, что также указывает на образование коллоидных частиц. В случае солонца высокие значения поглощения в этом диапазоне можно объяснить, по-видимому, значительным содержанием коллоидов небольшого размера (меньше 0.45 мкм) в исходном водном экстракте. Их взаимодействие с НА привело к образованию коллоидов большего размера и, как следствие, к более выраженной способности поглощать свет.
Рис. 2.
Электронные спектры поглощения НА в присутствии водорастворимых веществ почв (пунктирная линия) и расчетные спектры, полученные путем суперпозиции индивидуальных спектров НА и водорастворимых веществ почв (сплошная линия).
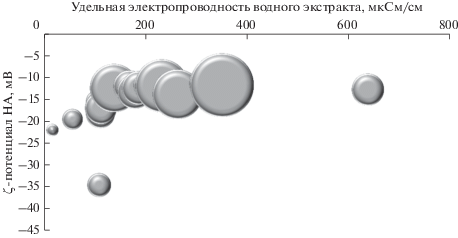
Таким образом, данные, полученные методами динамического светорассеяния и спектрофотометрии, свидетельствуют об активном взаимодействии НА с водорастворимыми компонентами, приводящем к модификации поверхности НА. Очевидно, что в этих условиях следует ожидать изменения электрокинетического потенциала образующихся наночастиц. Действительно, измерения ζ-потенциала показали, что внесение НА в водные экстракты приводило к значимому изменению этого показателя. В большинстве случаев было зафиксировано уменьшение ζ-потенциала от –11.2 до –19.5 мВ, что указывает на уменьшение коллоидной стабильности НА и их вероятную коагуляцию в почвенных условиях. Исключением был солонец, в присутствии водорастворимых веществ которого ζ-потенциал вырос до –34.5 мВ, то есть наночастицы перешли в разряд устойчивых. Ранее для наночастиц Fe0 со сходным электрокинетическим потенциалом (–39 мВ) была продемонстрирована их мобильность в условиях водоносных горизонтов с низкой минерализованностью (<40 мМ Na+ и <0.5 мМ Ca2+) [22]. Поэтому в солонце можно предположить возможность увеличения миграционной способности НА, модифицированных водорастворимыми компонентами этой почвы. Таким образом, в целом в почвах следует ожидать коагуляцию и уменьшение подвижности НА вследствие их взаимодействия с компонентами водных экстрактов почв, хотя в некоторых случаях мобильность НА может возрастать. Зависимость гидродинамического диаметра и ζ-потенциала НА от удельной электропроводности водных экстрактов, отражающей общее содержание водорастворимых компонентов, приведена на рис. 3. Полученные результаты демонстрируют общую тенденцию увеличения СВГД и падения ζ-потенциала НА при возрастании удельной электропроводности водных экстрактов почв с некоторыми исключениями. Например, для НА в водном экстракте солонца при удельной электропроводности 107 мкСм/см был отмечен нехарактерный для других случаев высокий ζ-потенциал наночастиц –34.5 мВ (нижняя точка на рис. 3); в водном экстракте одного из исследованных выщелоченных черноземов (ЧВ2) при максимальной удельной электропроводности 637 мкСм/см – относительно низкое значение СВГД 172 нм (правая точка на рис. 3). Это свидетельствует, что поведение НА в почвах будет зависеть не только от общей минерализованности почвенного раствора, но и от его других характеристических особенностей.
Рис. 3.
Зависимость СЧГД (размеры точек) и ζ-потенциала НА от удельной проводимости почвенных водных экстрактов.
Проведенный корреляционный анализ показал наличие прямой взаимосвязи между СВГД и рН (r = 0.63, рис. 4). Принимая во внимание обсужденную ранее концептуальную модель поведения РОВ, подразумевающую конденсированное состояние компонентов РОВ при низких значениях pH и развернутое при высоких [21], можно предположить возрастание сорбции РОВ на НА при увеличении рН. Это предположение хорошо объясняет аномальное поведение ЧВ2: при рН его водного экстракта 6.2 (табл. 2) СВГД НА составил 172 нм и был близок к почвам с близкими значениями рН: ЧТ (рН 6.2, СВГД 69 нм) и СЛ2 (рН 6.5, СВГД 139 нм).
Рис. 4.
Зависимость гидродинамического диаметра и ζ-потенциала НА от свойств почвенных водных экстрактов.
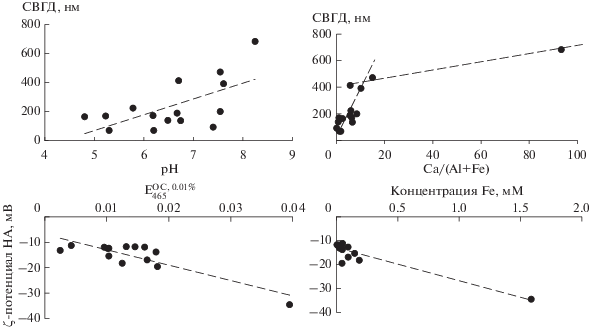
Среди исследованных минеральных компонентов корреляционный анализ не показал ни одной статистической значимой взаимосвязи их концентрации с размерами НА. Однако прямая корреляция была установлена между СВГД и отношением концентрации кальция к сумме концентраций железа и алюминия Ca/(Fe + Al) (r = 0.79). Рассмотрение корреляционного поля (рис. 4) показало, что линейный рост СВГД при увеличении Ca/(Fe + Al) в водной вытяжке становится менее выраженным при значениях этого отношения более 15. Если коэффициент линейного уравнения, описывающего зависимость СВГД от Ca/(Fe + Al) в диапазоне 0–15, равен 24, то для всего диапазона отношений Ca/(Fe + Al) он уменьшается до 5. При этом значимая корреляционная связь (r = = 0.80) между СВГД и Ca/(Fe + Al) сохраняется и при исключении из выборки точки, соответствующей максимальному отношению Ca/(Fe + Al) (крайняя правая точка на графике, почва К1). Установленная зависимость, по-видимому, отражает процессы перехода алюминия и железа из истинно растворенного в коллоидное состояние с последующей сорбцией на НА при росте концентрации кальция в растворе. Однако доказательство высказанного предположения требует проведения дополнительных исследований.
Для электрокинетического потенциала было показано наличие обратной линейной взаимосвязи с коэффициентом экстинкции ${\text{E}}_{{465}}^{{{\text{OC}},0.01\% }}$ (r = –0.86) и содержанием железа в водных экстрактах (r = = –0.93) (рис. 4). Так как с ростом молекулярной массы коэффициенты экстинкции РОВ уменьшаются, то полученные результаты указывают на то, что повышение стабильности НА в водных экстрактах почв возможно только в присутствии низкомолекулярных органических веществ. Взаимодействие НА с высокомолекулярными компонентами РОВ, напротив, будет приводить к снижению их ζ-потенциала до величин, характерных для нестабильных наночастиц. Рассмотрение корреляционного поля “ζ-потенциал НА – содержание Fe” показало неравномерное распределение точек на графике: солонец, в водном экстракте которого отмечали максимальное содержание железа и самое высокое значение ζ-потенциала, располагался отдельно от остальных почв. Поэтому дополнительно был рассчитан коэффициент корреляции для этих параметров для выборки, не содержащей солонец. Расчеты показали, что обратная линейная связь между этими показателями сохраняется (r = –0.62), что указывает на возможные рост стабильности НА при высоких концентрациях железа в почвенном растворе.
ЗАКЛЮЧЕНИЕ
Исследованные НА детонационного синтеза активно взаимодействуют с водорастворимыми компонентами почв, что приводит к увеличению гидродинамического диаметра и изменению ζ-потенциала наночастиц. Наибольшее увеличение размеров НА и, как следствие, низкую стабильность наночастиц, можно ожидать в почвенных растворах с высокими рН и отношением Ca/(Fe + Al). Наличие обратных корреляционных связей ζ-потенциала НА с коэффициентом экстинкции ${\text{E}}_{{465}}^{{{\text{OC}},0.01\% }}$ почвенного РОВ и содержанием железа в водных экстрактах позволило высказать предположение о возможности повышения стабильности НА в почвенных растворах в присутствии низкомолекулярных компонентов РОВ и при высоких концентрациях железа. В целом полученные результаты позволяют сделать вывод, что в почвах следует ожидать коагуляцию и уменьшение подвижности НА вследствие их взаимодействия с водорастворимыми компонентами почв; исключение могут составлять солонцы, где можно предположить возможность увеличения миграционной способности НА, модифицированных водорастворимыми компонентами этой почвы.
Список литературы
Долматов В.Ю. Ультрадисперсные алмазы детонационного синтеза. Получение, свойства, применение. СПб.: Изд-во СПбГПУ, 2003. 344 с.
Колесников С.И., Тимошенко А.Н., Казеев К.Ш., Акименко Ю.В., Мясникова М.А. Оценка экотоксичности наночастиц меди, никеля и цинка по биологическим показателям чернозема // Почвоведение. 2019. № 8. С. 986–992.
Перед прыжком // В мире нано. 2010. № 5. С. 25–28.
Терехова В.А., Гладкова М.М. Инженерные наноматериалы в почве: проблемы оценки их воздействия на живые организмы // Почвоведение. 2014. № 1. С. 82.
Филиппова О.И., Холодов В.А., Сафронова Н.А., Юдина А.В., Куликова Н.А. Микроагрегатный, гранулометрический и агрегатный состав гумусовых горизонтов зонального ряда почв европейской России // Почвоведение. 2019. № 3. С. 335–347. https://doi.org/10.1134/S0032180X19030031
Basiuk V.A., Terrazas T., Luna-Martínez N., Basiuk E.V. Phytotoxicity of carbon nanotubes and nanodiamond in long-term assays with Cactaceae plant seedlings // Fullerenes, Nanotubes and Carbon Nanostructures. 2019. V. 27(2). P. 141–149. https://doi.org/10.1080/1536383X.2018.1531393
Bo Zh., Avzar S.Y., Corliss M.K., Chung M., Cho N.-J. Influence of natural organic matter (NOM) coatings on nanoparticle adsorption onto supported lipid bilayers // J. Hazard. Mater. 2017. V. 339. P. 264–273. https://doi.org/10.1016/j.jhazmat.2017.06.031
Borodina T., Trushina D., Artemov V., Bukreeva T., Shchukin D. Modification of the polyelectrolyte capsule shell by nanodiamonds for remote microwave opening // Mater. Lett. 2019. V. 251. P. 81–84. https://doi.org/10.1016/j.matlet.2019.05.037
Cai Y., Chang S.X., Ma B., Bork E.W. Watering increased DOC concentration but decreased N2O emission from a mixed grassland soil under different defoliation regimes // Biol. Fert. Soils. 2016. V. 52. P. 987–996. https://doi.org/10.1007/s00374-016-1135-3
Degenkolb L., Kaupenjohann M., Klitzke S. The variable fate of Ag and TiO2 nanoparticles in natural soil solutions – sorption of organic matter and nanoparticle stability // Water, Air Soil Pollut. 2019. V. 230. P. 62. https://doi.org/10.1007/s11270-019-4123-z
Gao S.-J., Zhao C., Shi Z.-H., Zhong J., Liu J.-G., Li J.-Q. Spectroscopic characteristics of dissolved organic matter in afforestation forest soil of Miyun district, Beijing // J. Analyt. Meth. Chem. 2016. ArticleID 1480857. https://doi.org/10.1155/2016/1480857
Gao Y., Yang T.T., Jin J. Nanoparticle pollution and associated increasing potential risks on environment and human health: a case study of China // Environ. Sci. Pollut. Res. 2015. V. 22(23). P. 19297–19306. https://doi.org/10.1007/s11356-015-5497-0
Hansen A.M., Kraus T.E.C., Pellerin B.A., Fleck J.A., Downing B.D., Bergamaschi B.A. Optical properties of dissolved organic matter (DOM): Effects of biological and photolytic degradation // Limnol. Oceanogr. 2016. V. 61(3). P. 1015–1032. https://doi.org/10.1002/lno.10270
Ivanov M., Shenderova O. Nanodiamond-based nanolubricants for motor oils // Curr. Opin. Solid State Mater. Sci. 2017. V. 21. P. 17–24. https://doi.org/10.1016/j.cossms.2016.07.003
Jira J., Rezek B., Kriha V., Artemenko A., Matolínová I., Skakalova V., Stenclova P., Kromka A. Inhibition of E. coli growth by nanodiamond and graphene oxide enhanced by Luria-Bertani medium // Nanomater. 2018. V. 8(140). https://doi.org/10.3390/nano8030140
Johnson J., Pannatier E.G., Carnicelli S., Cecchini G., Clarke N., Cools N., Hansen K., Meesenburg H., Nieminen T.M., Pihl-Karlsson G., Titeux H., Vanguelova E., Verstraeten A., Vesterdal1 L., Waldner P., Jonard M. The response of soil solution chemistry in European forests to decreasing acid deposition // Global Change Biol. 2018. V. 24. P. 3603–3619. https://doi.org/10.1111/gcb.14156
Lee S., Kim K., Shon H.K., Kim S.D., Cho J. Biotoxicity of nanoparticles: effect of natural organic matter // J. Nanoparticle Res. 2011. V. 13(7). P. 3051–3061. https://doi.org/10.1007/s11051-010-0204-z
Mochalin V.N., Shenderova O., Ho D., Gogotsi Y. The properties and applications of nanodiamonds // Nature Nanotechnol. 2012. V. 7. P. 11–23. https://doi.org/10.1038/nnano.2011.209
Nunn N., D’Amora M., Prabhakar N., Panich A.M., Froumin N., Torelli M.D., Vlasov I., Reineck P., Gibson B., Rosenholm J.M., Giordani S., Shenderova O. Fluorescent single-digit detonation nanodiamond for biomedical applications // Meth. Applic. Fluoresc. 2018. V. 6(3). 035010. https://doi.org/10.1088/2050-6120/aac0c8
Nunn N., Torelli M., McGuire G., Shenderova O. Nanodiamond: a high impact nanomaterial // Curr. Opin. Solid State Mater. Sci. 2017. V. 21. P. 1–9. https://doi.org/10.1016/j.cossms.2016.06.008
Pace M.L., Reche I., Cole J.J., Antonio Fernandez-Barbero A., Mazuecos I.P., Prairie Y.T. pH change induces shifts in the size and light absorption of dissolved organic matter // Biogeochem. 2012. V. 108. P. 109–118. https://doi.org/10.1007/s10533-011-9576-0
Saleh N., Kim H.-J., Phenrat T., Matyjaszewski K., Tilton R.D., Lowry G.V. Ionic strength and composition affect the mobility of surface-modified Fe0 nanoparticles in water-saturated sand columns // Environ. Sci. Technol. 2008. V. 42(9). P. 3349–3355. https://doi.org/10.1021/es071936b
Sanderson T.M., Barton Ch., Cotton C., Karathanasis T. Long-term evaluation of acidic atmospheric deposition on soils and soil solution chemistry in the Daniel Boone National Forest, USA // Water, Air Soil Pollut. 2017. V. 228. Article 403. https://doi.org/10.1007/s11270-017-3583-2
Schaumann G.E., Philippe A., Bundschuh M., Metreveli G., Klitzke S., Rakcheev D., Grün A., Kumahor S.K., Kühn M., Baumann T., Lang F., Manz W., Schulz R., Vogel H.-J. Understanding the fate and biological effects of Ag- and TiO2-nanoparticles in the environment: the quest for advanced analytics and interdisciplinary concepts. Sci. Total Environ. 2015. V. 535 P. 3–19. https://doi.org/10.1016/j.scitotenv.2014.10.035
Schön W., Mittermayr F., Leis A., Mischak I., Dietzel M. Temporal and spatial variability of chemical and isotopic composition of soil solutions from cambisols – field study and experiments // Sci. Total Environ. 2016. V. 572. P. 1066–1079. https://doi.org/10.1016/j.scitotenv.2016.08.015
Thio B.J.R., Zhou D., Keller A.A. Influence of natural organic matter on the aggregation and deposition of titanium dioxide nanoparticles // J. Hazard. Mater. 2011. V. 189. P. 556–563. https://doi.org/10.1016/j.jhazmat.2011.02.072
Tinwala H., Wairkar S. Production, surface modification and biomedical applications of nanodiamonds: A sparkling tool for theranostics // Mater. Sci. Engineer.: C. 2019. V. 97. P. 913–931. https://doi.org/10.1016/j.msec.2018.12.073
Visconti F., de Paz J.M., Rubio J.L. Principal component analysis of chemical properties of soil saturation extracts from an irrigated Mediterranean area: implications for calcite equilibrium in soil solutions // Geoderma. 2009. V. 151(3–4). P. 407–416.
Visconti F., de Paz J.M., Rubio J.L. What information does the electrical conductivity of soil water extracts of 1 to 5 ratio (w/v) provide for soil salinity assessment of agricultural irrigated lands? // Geoderma. 2010. V. 154. P. 387–397. https://doi.org/10.1016/j.geoderma.2009.11.012
Zehlike L., Peters A., Ellerbrock R.H., Degenkolb L., Klitzke S. Aggregation of TiO2 and Ag nanoparticles in soil solution – effects of primary nanoparticle size and dissolved organic matter characteristics // Sci. Total Environ. 2019. V. 688. P. 288–298. https://doi.org/10.1016/j.scitotenv.2019.06.020
Zhang Y.X., Zhang W.J., Fedutik Y., Mao Z.W., Gao C.Y. Nanodiamonds of different surface chemistry influence the toxicity and differentiation of rat bone mesenchymal stem cells in vitro // J. Nanosci. Nanotechnol. 2019. V. 19(9). P. 5426–5434. https://doi.org/10.1166/jnn.2019.16545
Zhu Y., Zhang Yu., Shi G., Yang J., Zhang J., Li W., Li A., Tai R., Fang H., Fan Ch., Huang Q. Nanodiamonds act as Trojan horse for intracellular delivery of metal ions to trigger cytotoxicity // Particle and Fibre Toxicology. 2015. V. 12:2. https://doi.org/10.1186/s12989-014-0075-z
Дополнительные материалы отсутствуют.


