Почвоведение, 2021, № 11, стр. 1332-1345
Сравнение методов определения соединений углерода пирогенно измененных органических соединений
А. А. Дымов a, *, В. В. Старцев a, Н. М. Горбач a, И. В. Паюсова a, Д. Н. Габов a, О. Доннерхак b
a Институт биологии ФИЦ Коми научного центра УрО РАН
167982 Сыктывкар, ул. Коммунистическая, 28, Россия
b Институт почвоведения, Университет Лейбница
30419 Ганновер, Herrenhäuser Str., 2, Германия
* E-mail: aadymov@gmail.com
Поступила в редакцию 26.02.2021
После доработки 25.04.2021
Принята к публикации 27.04.2021
Аннотация
На примере торфяной почвы (Rheic Hemic Histosol (Lignic)), расположенной на юге средней тайги Республики Коми, проведено исследование почвенного органического вещества (ПОВ) с целью поиска биомаркеров и особенностей органического вещества, связанных с воздействием пожаров. Показано, что пожары оказывают существенное влияние на органическое вещество торфов. Пирогенную активность определяли по содержанию макроуглей. Органическое вещество исследовали методом твердотельной 13С-ЯМР-спектроскопии, определяли концентрации полициклических ароматических углеводородов (ПАУ) и бензолполикарбоновых кислот (БПКК). Показано, что данные методы позволяют диагностировать влияние пожаров на состав ПОВ. В составе горизонтов с признаками пирогенеза возрастает доля углерода, представленного ароматическими фрагментами, существенно увеличивается концентрация ПАУ, преимущественно за счет нафталина, фенантрена и хризена. По результатам оценки содержания БПКК впервые для территории европейского севера оценены запасы углерода пирогенно-измененных соединений (PyC), которые составляют 4.4 кг/м2. Показатели, характеризующие соединения и молекулярные фрагменты пирогенно измененных органических соединений, полученные различными методами, хорошо коррелируют между собой. Коэффициенты корреляции Пирсона между содержанием углерода, входящего в состав ароматических соединений (Сaryl) и СБПКК, составляют R = 0.84 (р < 0.05), с индивидуальными БПКК R = = 0.81–0.90 (р < 0.05).
ВВЕДЕНИЕ
Пожары – один из ведущих факторов изменения большинства наземных экосистем планеты [28, 32, 34, 57]. Экосистемы северных широт содержат существенные запасы материалов, которые потенциально могут быть подвержены пирогенному воздействию [11, 23, 53]. В первую очередь пожарами могут уничтожаться лесная подстилка, торф, растения напочвенного покрова и древесного яруса. В ходе голоцена пирогенная активность в бореальных лесах была различной. В зависимости от среднегодовой температуры воздуха и количества осадков интенсивность и частота пожаров в отдельные этапы голоцена отличалась [4, 12, 14, 30, 35].
В настоящее время углерод пирогенно измененных органических соединений (PyC) рассматривается как один из наиболее стабильных и устойчивых к микробиологическому разложению пулов почвенного углерода [10, 54, 55]. Считается, что PyC может сохраняться в почвах до нескольких тысяч лет [49]. Благодаря этому во многих современных работах он рассматривается как важный пул по секвестрированию углерода из атмосферы [38, 39]. Во многих работах именно с ним связаны перспективы по сглаживанию влияния растущей концентрации углекислого газа в атмосфере. Несмотря на общепризнанную важность PyC в экосистемах, в настоящее время нет единого подхода к его определению в почвах [45]. Проведенные ранее работы позволили выявить, что при пожарах наблюдается многократное увеличение содержания полициклических ароматических углеводородов (ПАУ) [24, 26, 37]. Часть исследователей связывает содержание пирогенного углерода с ароматическими фрагментами в области 110–165 миллионных долей (м. д.) спектров ядерного магнитного резонанса [50].
В настоящее время возрастает интерес к болотным экосистемам и различным аспектам их функционирования [9]. Выявлено, что торфа содержат значительные количества углерода, в том числе пирогенного происхождения [50]. Торфяные пожары приводят к катастрофическим последствиям [7, 8, 58]. На территории Республики Коми торфяные почвы занимают около 10% территории [22]. К настоящему времени достаточно подробно изучен геоботанический состав [5], морфологические и некоторые химические свойства торфяных почв равнинной части республики [18]. Подробно изучен состав органического вещества торфов северных регионов [21, 51, 56]. Но при этом данные, касающиеся влияния пожаров на химические свойства торфяных почв на территории европейского севера, отсутствуют.
Цель работы – оценка возможностей применения различных современных методов для определения содержания соединений углерода пирогенно модифицированных органических соединений на примере торфяной почвы.
ОБЪЕКТЫ И МЕТОДЫ
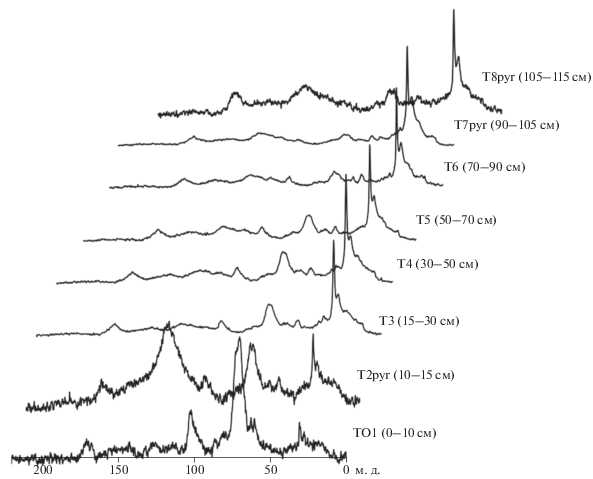
Полевые исследования проводили в августе 2019 г. В качестве объекта взят торфяник, развивающийся под сосняком багульниково-сфагновым в окрестностях национального парка “Койгородский”. Объект расположен на отрогах Северных Увалов, являющихся водоразделом бассейнов Волги и Северной Двины [2]. Согласно почвенно-географическому районированию [19], данная территория находится на границе средне-таежного Луза-Сысольского округа подзолистых и болотно-подзолистых почв, и южно-таежного Летского округа дерново-подзолистых почв. Среднегодовая температура составляет 1–2°С, количество осадков – 800 мм, из них на лето приходится 400–500 мм [1]. Общий вид ландшафта и строения почвы представлены на рис. 1. Почвенный профиль представляет собой торфяную толщу, подстилаемую суглинистым минеральным горизонтом G. Согласно [20], почва отнесена к торфяно-олиготрофной, по IUSS [47] к Rheic Hemic Histosol (Lignic). Строение почвенного профиля: ТO1 (0–10 см)–Т2pyr (10–15 см)–Т3 (15–30 см)–Т4 (30–50 см)–Т5 (50–70 см)–Т6 (70–90 см)–Т7pyr (90–105 см)–Т8pyr (105–115 см)–G (115–130 см). Органическая часть профиля состоит из растительных остатков, находящихся на разной стадии разложения: от свежего очеса мхов (степень разложения 5–10%), до средне и хорошо разложившихся в нижних горизонтах мхов (25–30% степени разложения до глубины 70 см). Цвет торфа меняется от желто-бурого до бурого и темно-бурого соответственно. В горизонте T2pyr на глубине 10–15 см выявлены углистые включения различного размера, что может свидетельствовать о прохождении пожара. С глубины 70 см торфяная толща представляет собой органо-минеральные отложения, которые сильно гумусированы. Вероятно, торфонакопление началось после заболачивания территории в результате прохождения участка пожаром. Плотность сложения определяли в трехкратной повторности в горизонте TO1 буром с диаметром 12.6 см, в нижележащих торфяных горизонтах буром с объемом 50 см3.
Количественные химические анализы почв проводили в аккредитованной экоаналитической лаборатории и отделе почвоведения Института биологии Коми научного центра Уральского отделения Российской академии наук (сертификат РОСС RU.0001.511257 от сентября 2019 г.). Общее содержание органических углерода и азота определяли на анализаторе EA-1100 (Carlo Erba). рН определяли с помощью Edge HI2002-02 pH-метра (Hanna Instruments, Румыния) с цифровым электродом (±0.01 pH) при соотношении почва : раствор для подстилок – 1 : 25, для минеральных горизонтов – 1 : 2.5. Обменные катионы экстрагировали согласно [60] с использованием механического программируемого вакуумного экстрактора с последующим определением содержания катионов в растворе (Ca2+, Mg2+, Na+, K+) методом атомно-эмиссионной спектроскопии с индуктивно-связанной плазмой. Для определения возраста отложений выполнено радиоуглеродное датирование образцов торфа в аналитическом центре изотопных исследований ИМКЭС СО РАН жидкостно-сцинтилляционным методом с помощь cпектрометра-радиометра Quantulus (Том ЦКП СО РАН). Калибровку радиоуглеродного возраста в календарный возраст произвели с помощью программы CALIB REV-7.10 [25]. Содержание стабильных изотопов 13С и 15N определяли в Институте почвоведения университета Лейбница (Ганновер, Германия).
Подсчет макроскопических частиц угля в торфе осуществляли по классической методике [12, 52]. Образцы торфа объемом 1 см3 отбирали через каждые 2 см. Далее образец заливали 5%-ным водным раствором NaOCl, и ждали не менее 24 ч при комнатной температуре. После образец промывали дистиллированной водой на сите с диаметром ячеи 125 мкм и помещали в чашку Петри. Затем макрочастицы угля подсчитывали под стереоскопическим микроскопом при 40-кратном увеличении. Данные по количеству частиц угля переносили в таблицу Excel для дальнейшего анализа данных в программах Clam и Char Analysis в среде программирования R [46].
В программе Clam интерполировали значения глубин отобранных образцов с возрастом и рассчитывали модель скорости вертикального прироста торфяной толщи для получения медианных значений. Далее полученную информацию сопоставляли с концентрацией макроскопических частиц угля и вносили в Char Analysis для получения данных о скорости накопления угля и достоверных пожарных событиях локального уровня. Для выделения пожаров локального уровня программа рассчитывает данные и выделяет фоновые и пороговые значения скорости накопления угля. Фоновые значения – низкочастотные колебания скорости аккумуляции угля, отражающие в большей степени региональный сигнал пожарной динамики, а также ряд параметров: возможные погрешности пробоподготовки и анализа, фактор разложения обгоревших остатков внутри торфяной колонки и переотложения ранее выпавшего угля. Пороговое значение, предполагающее, что “шумы” (Signal-to-NoiseIndex, SNI) распределены согласно гауссовой модели рассеивания примесей внутри установленного пользователем временного окна. Для унификации статистических функций использовали разрешение окна, равное 1000 годам. В качестве порога установлен 95-й процентиль распределения шумов. Если определяемые значения скорости накопления угля оказывались выше, чем этот порог, то это классифицировали как достоверное пожарное событие локального уровня.
Определение содержания ПАУ. Для полного извлечения ПАУ из почв использовали систему ускоренной экстракции растворителями ASE-350 (Dionex Corporation, США). Образец торфа массой 1 г помещали в экстракционную ячейку и трижды экстрагировали смесью хлористый метилен : ацетон (1 : 1) при температуре 100°С. Затем экстракты концентрировали с применением аппарата Кудерна–Даниша при температуре в термостате 70°С и заменяли растворитель на гексан. Полученный концентрат пробы объемом 3 см3 очищали от органических примесей методом колоночной хроматографии, с использованием оксида алюминия II степени активности по Брокману. В качестве элюента использовали 30 см3 смеси гексан : хлористый метилен (4 : 1). Элюат концентрировали с применением аппарата Кудерна–Даниша при температуре в термостате 85°С, до объема 5 см3, затем добавляли 3 см3 ацетонитрила и упаривали при температуре 90°С до полного удаления гексана. Было определено содержание 15 индивидуальных ПАУ. Степень канцерогенности ПАУ оценена при помощи приведения всех изучаемых полиаренов к уровню канцерогенности бенз[а]пирена (бензпиреновый эквивалент Kпау). Kпау рассчитывали по индексу токсичности (It) и содержанию полиаренов в почвах согласно [15].
Водорастворимое органическое вещество (ВОВ). Содержание углерода (CВОВ) и азота (NВОВ) водорастворимых органических соединений определяли на анализаторе TOC-VCPN (Япония, Shimadzu) c модулем TNM-1. Экстракцию водорастворимых веществ проводили деионизированной водой (ELGA Lab Water, Англия) при комнатной температуре (20–23°С) при соотношении 1 : 50 (почва : вода) для минеральных горизонтов и 1 : 100 для органогенных горизонтов в пробирках BIOFIL. Фильтрование осуществляли непосредственно после встряхивания на установках Millipore с использованием кварцевых фильтров (MN, Германия, с размером пор 0.4 мкм).
Хроматографическое фракционирование лабильного (щелочерастворимого вещества) делали по методике Милановского [13] на колонке 1 × 10 см с гидрофобизированным гелем агарозы (Octyl Sepharose CL-4В, Pharmacia) на хроматографической системе Biologic LP (Bio RAD, США). Анализировали щелочные экстракты (0.1 М NaOH) в соотношении почва : раствор (1 : 10). Подробно методика описана ранее [13]. Содержание углерода в щелочной вытяжке определяли методом мокрого сжигания хромовой смесью. Коэффициенты экстинкции рассчитывали при двух длинах волн 465 и 650 нм на КФК3 согласно Орлову с соавт. [16].
ЯМР спектроскопия. Состав органического вещества определяли методом твердотельной 13С-ЯМР спектроскопии. 13С-ЯМР спектры регистрировали на спектрометре Bruker Avance III 400WB (Bruker, Германия) с рабочей частотой 100.53 МГц с использованием твердофазной методики CP-MAS (“кросс-поляризация с вращением под магическим” углом) в ресурсном центре научного парка “Магнитно-резонансные методы исследований” Санкт-Петербургского государственного университета. Частота вращения образца – 12.5 кГц, время контакта – 2 мс, время релаксации – 2 с. Химические сдвиги представлены относительно тетраметилсилана со сдвигом 0 м. д., в качестве стандарта использовали пик адамантана. Предварительно образцы обрабатывали 10% плавиковой кислотой для удаления парамагнитных примесей изотопов железа согласно [43, 59]. Для полуколичественной обработки применяли численное интегрирование по областям, соответствующим расположению функциональных групп и молекулярных фрагментов, с использованием программы TopSpin 3.2 (Bruker, Германия).
Содержание ароматических структур (AR) определяли по сумме площадей сигналов при 110–145 и 145–165 м. д., а алифатических составляющих (AL) – по сумме 0–110, 165–185 м. д. Степень разложения органического вещества оценивали согласно [27] по соотношению алкил (0–45 м. д.) к О,N-алкил (45–110 м. д.).
Определение содержания БПКК. Концентрации БПКК в образцах почвы определяли согласно [31] в Институте почвоведения университета Лейбница (Ганновер, Германия). Для удаления поливалентных металлов около 1 г почвы обрабатывали в 10 мл 4 М трифторуксусной кислоты при 105°С в течение 4 ч. После охлаждения остаток несколько раз промывали деионизированной водой путем фильтрации через стекловолоконный фильтр (Whatman GF/F) и сушили при 40°С в течение 3 ч. Затем остаток переносили в реакторы, к которым добавляли 4 мл 65% HNO3 и сжигали при 170°С в течение 8 ч в реакторе высокого давления. Смесь количественно переносили и фильтровали с помощью целлюлозного фильтра (Whatman 1450–055) в мерные колбы объемом 25 см3. Затем 4 см3 аликвоты разбавляли деионизированной водой и добавляли 100 мкл лимонной кислоты в качестве первого внутреннего стандарта. Раствор пропускали через катионообменную смолу (Dowex 50 WX8, 200–400). Водные образцы подвергали сублимационной сушке и повторному растворению в метаноле. В качестве второго внутреннего стандарта добавляли 100 мкл 2.2'-дифенилдикарбоновой кислоты в метаноле. После сушки в азотной атмосфере образцы были дериватизированы. Дериватизацию проводили в течение 2 ч при 90°С с использованием N, O-бис(триметилсилил)-трифторацетамида (BSTFA) и N-триметилсилил иодида (TMSI) в соотношении 49/1 [29]. Определение Б-ПКК осуществляли на газовом хроматографе HP 6890 (Agilent Technologies, USA) с пламенным ионизирующим детектором. Шесть БПКК были использованы в качестве стандартов [42]. Всего определено содержание восьми БПКК. Для расчета содержания PyC рекомендуется использовать содержание кислот с числом карбоксильных групп более 4, поскольку кислоты с меньшим количеством карбоксильных групп могут иметь биотическое происхождение [41, 44]. Бк4 рассчитывали как сумму (пиромелитовая, меллофаниковая и пренитовая) кислот. Использовали соотношения Бк4/Бк6 и Бк5/Бк6, где Бк5 это содержание углерода бензолпентакарбоновой кислоты, Бк6 содержание углерода в меллитовой кислоте.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Формирование исследуемого торфяника началось около 9 тыс. лет назад. Необходимо отметить, что исследуемая торфяная залежь неоднократно подвергалась пожарам, как на протяжении раннего голоцена, так и в современный период. По содержанию углей можно предположить, что данный торфяник неоднократно горел, наиболее активно в атлантический и суббореальный периоды (рис. 2). Вероятно, большие пики свидетельствуют о горении верхнего органогенного горизонта. Хорошо выраженный пирогенный горизонт на глубине 10–15 см, свидетельствует о мощном пожаре, прошедшем около 140 лет назад на данной территории. Время, прошедшее с момента последнего пожара, определяли по возрасту древостоя. Выположенные участки графика вероятно свидетельствуют о горении прилегающих к данному участку лесов.
Физико-химические свойства почвы представлены в табл. 1. Торфяно-олиготрофная почва сильнокислая – показатели рНKCl (3.0–3.9). Максимальной кислотностью исследованных почв характеризуется верхний олиготрофно-торфяный горизонт, в нижних торфяных горизонтах кислотность несколько снижается. Распределение кислотности по профилю почв носит равномерно-элювиальный характер. Зольность торфяных горизонтов почвы составляет 2.6–9.5%. Выявлено увеличение зольных остатков в пирогенном горизонте T2pyr до 4.5%.
Таблица 1.
Физико-химические и химические свойства исследуемых почв
| Гори-зонт | Глубина, см |
рН | C | N | C/N | Ca2+ | Mg2+ | K+ | Na+ | ∑ | CEC | BS | Зола | CВОВ | NВОВ | ρ | δ13С, ‰ PDB | δ15N, ‰ Air | |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| KCl | H2O | г/кг | смоль(экв)/кг | % | г/кг | г/cм3 | |||||||||||||
| ТO1 | 0–10 | 3.0 | 4.4 | 485 ± 17 | 13.9 ± 1.5 | 41 | 4.5 | 2.8 | 2.97 | 0.18 | 10.4 | 90 | 12 | 2.6 | 3.51 | 0.29 | 0.08 ± 0.03 | –30.16 | –0.71 |
| T2pyr | 10–15 | 3.1 | 4.1 | 568 ± 20 | 9.5 ± 1.0 | 70 | 4.1 | 1.3 | 0.40 | 0.09 | 5.9 | 111 | 5 | 4.5 | 1.32 | 0.08 | 0.19 ± 0.02 | –26.88 | 1.68 |
| T3 | 15–30 | 3.2 | 4.5 | 541 ± 19 | 15.0 ± 1.6 | 42 | 2.2 | 0.7 | 0.08 | 0.07 | 3.0 | 42 | 7 | 2.6 | 1.35 | 0.09 | 0.19 ± 0.02 | –28.06 | 0.74 |
| T4 | 30–50 | 3.8 | 4.5 | 491 ± 17 | 11.3 ± 1.2 | 51 | 2.0 | 0.6 | 0.05 | 0.07 | 2.7 | 89 | 3 | 2.7 | 1.07 | 0.08 | 0.21 ± 0.01 | –28.46 | 1.97 |
| T5 | 50–70 | 3.3 | 4.5 | 541 ± 19 | 14.1 ± 1.6 | 45 | 2.9 | 0.9 | 0.04 | 0.07 | 3.9 | 103 | 4 | 2.8 | 1.40 | 0.09 | 0.23 ± 0.01 | –29.11 | 1.35 |
| T6 | 70–90 | 3.5 | 4.8 | 555 ± 19 | 13.0 ± 1.4 | 50 | 2.9 | 1.0 | 0.04 | 0.09 | 4.0 | 99 | 4 | 3.6 | 1.20 | 0.09 | 0.26 ± 0.01 | –29.31 | 1.42 |
| T7pyr | 90–105 | 3.7 | 4.6 | 529 ± 19 | 12.0 ± 1.3 | 51 | 3.2 | 1.1 | 0.06 | 0.08 | 4.5 | 97 | 5 | 9.5 | 0.80 | 0.07 | 0.94 ± 0.08 | –29.65 | 0.67 |
| T8pyr | 105–115 | 3.9 | 4.7 | 102 ± 10 | 5.5 ± 1.1 | 22 | 2.1 | 0.8 | 0.20 | 0.07 | 3.2 | 36 | 9 | 75.4 | 0.70 | 0.04 | 0.94 ± 0.08 | –29.22 | –0.62 |
| G | 115–130 | 3.8 | 4.9 | 11.5 ± 2.7 | 0.71 ± 0.14 | 19 | 1.5 | 1.0 | 0.18 | 0.04 | 2.6 | 13 | 20 | 95.4 | 0.21 | 0.01 | Не опр. | ||
Содержание обменных оснований неравномерно распределено по профилю почв. Максимальное содержание выявлено для катионов кальция. Катионов магния, калия и натрия несколько меньше. Содержание Ca2+ в торфяных горизонтах варьировало от 2.1–4.5 смоль(экв.)/кг, в минеральном – 1.5 смоль(экв)/кг. Наибольшее содержание выявлено для верхнего подгоризонта TO1.
Распределение содержания углерода и азота по профилю почвы равномерное с резким уменьшением в минеральных горизонтах. Содержание углерода в исследуемой почве варьирует от 568 г/кг в органических и органо-минеральных горизонтах до 11.5 г/кг в минеральном горизонте G. Концентрация азота в торфяных горизонтах составляет 5.5–15.0 г/кг, в минеральном – 0.71 г/кг. Отношение углерода к азоту почвы изменяется от 22–70 в органических горизонтах, до 19 – в минеральном. В целом распределение отношения C/N вниз по профилю почв закономерно уменьшается.
При анализе содержания углерода (СВОВ) и азота (NВОВ) водорастворимых органических соединений выявлено, что максимальное содержание приходится на верхние органогенные горизонты, представленные свежим очесом мхов. Распределение ВОВ по профилю почвы равномерно убывающее. Содержание СВОВ варьирует вниз по профилю от 3.51 в верхнем органогенном горизонте до 0.21 г/кг в минеральном.
Результаты хроматографии гидрофобного взаимодействия позволяют разделить смесь щелочерастворимых веществ на пять фракций, различающихся амфифильными свойствами. Гидрофильные фракции представлены фрагментами алифатической природы. Первая фракция значимо коррелирует с алифатическими соединениями группы О-алкил замещенными алифатическими (R = 0.76, p < 0.05) и ди-О,N–алифатическими фрагментами дважды замещенными гетероатомами (R = 0.82, p < 0.05). Вероятно, именно продукты экстракции целлюлозы и гемицеллюлозы доминируют в составе данной фракции. Сумма гидрофильных фракций (первая и вторая фракции) составляла 17–54%. Содержание первой гидрофильной фракции варьировало в профиле почвы 8.6–45.6%, второй фракции – 5.9–11.8%. Максимальное содержание выявлено для горизонта ТO1, представленного очесом свежих мхов. Распределение щелочерастворимых гидрофильных соединений в целом повторяет распределение ВОВ в профиле почвы. Коэффициент корреляции между первой фракцией с СВОВ составляет R = 0.72 (p < 0.05), с NВОВ – R = 0.73 (p < < 0.05). С глубиной наблюдается уменьшение доли гидрофильных соединений. Хроматографическое фракционирование позволило выявить высокое содержание фракций щелочерастворимого органического вещества, связанного с лигнино- и целлюлозоподобными соединениями [13], относящимися к гидрофобным фракциям (фракции 3 и 4) в профиле исследуемого торфяного разреза (табл. 2). Третья фракция варьировала в профиле от 16.1 до 51.3%, четвертая – от 28.0 до 40.3%. Содержание фракции 5 незначительно 0.9–3.0%. Необходимо отметить, что для изучения влияния пожаров прошлых эпох содержание углерода водорастворимых соединений и отдельных амфифильных фракций играет меньшую индикационную роль по сравнению с современными пожарами в лесных экосистемах на минеральных почвах [6].
Таблица 2.
Относительное содержание амфифильных фракций в составе ПОВ (%), содержание щелочерастворимого органического вещества, отношение коэффициентов экстинкции
| Горизонт | Глубина, см | ω(С) 0.1 M NaOH, % | Сщел, % от Собщ | E465/E650 | Номер хроматографической фракции | Dh* | ||||
|---|---|---|---|---|---|---|---|---|---|---|
| 1 | 2 | 3 | 4 | 5 | ||||||
| ТO1 | 0–10 | 5.51 ± 0.04 | 11.4 | 8.1 | 45.6 | 8.6 | 16.1 | 28.0 | 1.7 | 1.18 |
| Т2pyr | 10–15 | 8.69 ± 0.05 | 17.9 | 4.3 | 17.6 | 8.1 | 34.0 | 38.7 | 1.5 | 0.35 |
| Т3 | 15–30 | 14.2 ± 0.3 | 29.3 | 5.5 | 12.2 | 11.8 | 51.3 | 23.7 | 1.1 | 0.32 |
| Т4 | 30–50 | 13.85 ± 0.07 | 28.6 | 5.5 | 12.6 | 9.2 | 44.4 | 32.5 | 1.3 | 0.28 |
| Т5 | 50–70 | 16.7 ± 0.05 | 34.4 | 5.2 | 9.8 | 6.5 | 44.4 | 36.3 | 3.0 | 0.20 |
| Т6 | 70–90 | 18.43 ± 0.23 | 35.8 | 4.9 | 8.6 | 8.3 | 45.9 | 36.0 | 1.3 | 0.20 |
| Т7pyr | 90–105 | 4.01 ± 0.06 | 38.0 | 6.3 | 12.1 | 5.9 | 40.8 | 40.3 | 0.90 | 0.22 |
| Т8pyr | 105–115 | 0.235 ± 0.001 | 8.3 | 5.9 | 29.7 | 8.0 | 33.6 | 28.7 | Не обн. | 0.61 |
Гидрофильные органические соединения в основном относятся к миграционно-способным компонентам ОВ, которые хорошо растворяются и легко перемещаются в профиле почв. В условиях застойного увлажнения болотных экосистем накопление гидрофильных фракций происходит лишь в верхних горизонтах торфяных почв. Срединные и нижние торфяные горизонты богаты гидрофобными фракциями (46–83%), представленными биополимерами из растительных остатков различной степени разложения. Видимо, увеличение содержания гидрофобных фракций, представленных высокомолекулярными структурными компонентами, в том числе ароматической природы может косвенно указывать на пирогенное воздействие. Отношение E465/E650 минимально в горизонте Tpyr, максимально в горизонте свежего мохового очеса на глубине 0–10 см. В остальных торфяных горизонтах значения изменяются от 4.9 до 6.3. Однако значимого влияния пирогенеза на состав щелочерастворимого органического вещества и содержание амфифильных фракций не выявлено.
Необходимо отметить, что в исследуемой почве сосредоточены достаточно высокие запасы общего углерода (184 кг С/м2) и азота (4.6 кг N/м2). Эти значения существенно больше данных оценок для почв региона, основанных на данных опубликованных для необлесенных болот с расчетными, а не определяемыми в полевых условиях значениях плотности [17]. Вероятно, высокие значения связаны с периодически повторяющимися пожарами, приводящими не только к поступлению частично обуглившихся частиц с высоким содержанием углерода, но и возрастанию плотности сложения торфов. Увеличение плотности торфов пирогенных горизонтов описано ранее для почв Средней Сибири [7]. В данной почве возрастание плотности связано с поступлением золы (R = 0.98, р < 0.05).
Спектры ядерного магнитного резонанса органического вещества горизонтов разреза представлены на рис. 3. Результаты интегрирования приведены в табл. 3. Содержание фрагментов в составе почвенного органического вещества зависит в первую очередь от состава растений, которые аккумулируются в торфяной залежи. Так, верхние горизонты торфяника, представленные преимущественно мхами и слаборазложившимися остатками, характеризуются преобладанием полисахаридов при низкой доле ароматических составляющих. Состав органического вещества на глубинах 15–105 см остается достаточно стабильным с долей алифатических фрагментов от 39 до 44%. Содержание целлюлозоподобных веществ составляет 12 до 21%. Доля метоксильных фрагментов не высока и составляет около 6–7%. Доля гемицеллюлозы (CO-Alk-O) не превышает 7%. Содержание ароматических компонентов – показатель, который часто связывают с влиянием пирогенеза, существенно увеличивается в горизонтах T2pyr (10–15 см) и T8pyr (105–115 см), где содержится значительное количество углей. В данных горизонтах доля арильных фрагментов, представленных соединениями в интервалах 110–145 и 145–165 м. д., увеличивается до 32.3–44.4%.
Таблица 3.
Относительное содержание (%) молекулярных фрагментов в составе ПОВ по результатам 13CPMAS ЯМР спектроскопии
| Гори-зонт | Глубина, см | Alkyl C | O-Alkyl C | Aryl C | Carboxyl C/Amide/Easter | Alkyl/ О,N-alkyl | AR/AL | Caryl, %* | ||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| CAlk-H | ${{{\text{C}}}_{{{\text{C}}{{{\text{H}}}_{{\text{3}}}}{\text{ - O}}}}}$ | CAlk-O | СО-Alk-O | CAr-H(C) | СAr-O,N | CCOOH(R) | СC=0 | |||||
| 0–45 | 45–60 | 60–95 | 95–110 | 110–145 | 145–165 | 165–185 | 185–220 | |||||
| ТO1 | 0–10 | 16.0 | 7.0 | 45.4 | 11.6 | 11.3 | 4.6 | 3.9 | 0.1 | 0.2 | 0.2 | 7.7 |
| T2pyr | 10–15 | 19.1 | 5.9 | 18.0 | 6.8 | 36.4 | 8.0 | 5.0 | 0.9 | 0.6 | 0.9 | 25.2 |
| T3 | 15–30 | 39.2 | 7.4 | 21.4 | 6.3 | 14.5 | 5.3 | 4.7 | 1.1 | 1.1 | 0.3 | 10.7 |
| T4 | 30–50 | 38.3 | 7.2 | 20.4 | 6.3 | 15.9 | 5.7 | 4.7 | 1.4 | 1.1 | 0.3 | 10.6 |
| T5 | 50–70 | 36.3 | 7.2 | 18.7 | 6.4 | 17.9 | 6.8 | 5.2 | 1.5 | 1.1 | 0.4 | 13.4 |
| T6 | 70–90 | 42.5 | 7.1 | 14.7 | 5.6 | 18.5 | 6.6 | 4.6 | 0.4 | 1.5 | 0.4 | 13.9 |
| T7pyr | 90–105 | 44.2 | 6.4 | 12.0 | 4.2 | 18.7 | 6.8 | 5.6 | 2.2 | 2.0 | 0.4 | 13.5 |
| T8pyr | 105–115 | 34.0 | 6.9 | 13.9 | 6.0 | 24.4 | 7.9 | 7.0 | – | 1.3 | 0.5 | 3.3 |
Анализ содержания стабильных изотопов в составе органического вещества позволил выявить некоторое утяжеление (увеличение доли изотопов 13С и 15N) состава органического вещества пирогенного горизонта на глубине 10–15 см по сравнению с верхними и нижележащими торфяными горизонтами. Выявлены значимые корреляции с содержанием бензолполикарбоновых кислот С4–6БК (R = 0.87, p < 0.05).
Содержание ПАУ часто используют для диагностики и оценки влияния пожаров на состав ПОВ [6, 61, 62]. Концентрация ПАУ существенно различается в горизонтах исследуемой почвы (табл. 4). В горизонтах с выраженными пирогенными признаками выявлено значительное увеличение как суммарного содержания ПАУ, так и индивидуальных соединений. Можно предположить, что пирогенное происхождение характерно для нафталина, фенантрена, флуарентена и хризена. При исследовании постпирогенных автоморфных бореальных почв увеличение содержания ПАУ преимущественно было связано с данными соединениями [6, 36]. В нижних горизонтах на глубине 90–105 см выявлено значительное возрастание доли тяжелых пятиядерных ПАУ. Высокие концентрации выявлены для бенз[k]флуорантен и дибенз[a,h]антрацен, что, вероятно, определяется биогенным фактором [40]. Суммарные запасы ПАУ в рассматриваемой почве составляют 4.7 г/м2.
Таблица 4.
Содержание ПАУ, нг/г
| Гори-зонт | Глуби-на, см | 2-ядерные | 3-ядерные | 4-ядерные | 5-ядерные | 6-ядерные | ∑ ПАУ | I | II | III | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| НАФТ | АЦЕ | ФЛУ | ФЕН | АНТ | ФЛА | ПИР | БаАНТ | ХРИ | БbФЛА ФЛА |
БkФЛА | БaПИР | ДБahАНТ | БghiПЕР | ИПИР | ||||||
| ТO1 | 0–10 | 90 ± ± 40 | – | – | 180 ± ± 40 | 2.9 ± ± 1.5 | – | – | – | – | – | 1.8 ± ± 0.9 | 1.3 ± ± 0.7 | 7 ± 3 | 8 ± 4 | 16 ± 7 | 335 | 0.01 | 0.02 | 10 |
| T2pyr | 10–15 | 650 ± ± 230 | – | 20 ± 8 | 260 ± ± 60 | 5.0 ± ± 2.5 | 26 ± 12 | – | – | 46 ± ± 24 | – | 15 ± ± 7 | 8 ± 4 | 60 ± ± 30 | – | – | 1102 | 0.03 | 0.02 | 71 |
| T3 | 15–30 | 130 ± ± 70 | – | 10 ± 4 | 85 ± ± 19 | 1.9 ± ± 1.0 | – | – | – | 6 ± ± 3 | – | 2.4 ± ± 1.2 | 5.4 ± ± 2.7 | 11 ± ± 5 | – | – | 265 | 0.06 | 0.02 | 17 |
| T4 | 30–50 | 209 ± ± 104 | – | 18 ± 7 | 111 ± ± 24 | 7 ± 4 | – | – | – | 10 ± ± 5 | – | – | – | 28 ± ± 13 | – | – | 400 | 0.00 | 0.06 | 29 |
| T5 | 50–70 | 160 ± ± 80 | – | 16 ± 6 | 97 ± ± 21 | 4.9 ± ± 2.5 | – | – | – | – | – | – | – | – | – | – | 295 | 0.00 | 0.05 | 0 |
| T6 | 70–90 | 110 ± ± 60 | – | 11 ± 4 | 70 ± ± 40 | 4.4 ± ± 2.2 | – | – | – | – | – | – | – | – | 10 ± 4 | – | 227 | 0.00 | 0.06 | 0 |
| T7pyr | 90–105 | 100 ± ± 50 | – | – | 70 ± ± 40 | 2.2 ± ± 1.1 | – | – | – | 55 ± ± 28 | 67 ± ± 28 | 19 ± ± 9 | 860 ± ± 210 | 260 ± ± 80 | 42 000 ± ± 9000 | – | 43 642 | 6.88 | 0.03 | 1549 |
| T8pyr | 105–115 | 44 ± ± 22 | – | – | 26 ± ± 13 | 1.3 ± ± 0.7 | – | – | – | 4.0 ± ± 2.1 | – | – | 2± 1.9 ± 1.5 | 15 ± ± 7 | 8200 ± ± 1800 | – | 8356 | 0.10 | 0.05 | 100 |
| G | 115–130 | 28 ± ± 14 | – | 11 ± 4 | 80 ± ± 40 | 3.9 ± ± 2.0 | – | – | – | – | – | – | – | – | – | – | 138 | 0.00 | 0.05 | 0 |
* Прочерк – ниже предела определения (для АЦЕ < 6, ФЛУ < 6, ФЛА < 20, ПИР < 20, БаАНТ < 6, ХРИ < 3, БbФЛА < 6, БkФЛА < 1, БаПИР < 1, ДБahАНТ < 6, БghiПЕР < 6, ИПИР < 6). НАФТ – нафталин, АЦЕ – аценафтен, ФЛУ – флуорен, ФЕН – фенантрен, АНТ – антрацен, ФЛА – флуорантен, ПИР – пирен, БаАНТ – бенз[a]антрацен, ХРИ – хризен, БbФЛА – бенз[b]флуорантен, БkФЛА – бенз[k]флуорантен, БаПИР – бенз[a]пирен, ДБahАНТ – дибенз[a,h]антрацен, БghiПЕР – бенз[ghi]перилен, ИПИР – индено[1,2,3-cd]пирен. Отношения ПАУ: I – (ПИР + БаПИР)/(ФЕН + ХРИ); II – AНТ/(AНТ + ФЕН); III – КПАУ, нг/г.
Канцерогенная опасность ПАУ в исследуемых почвах наиболее выражена в пирогенных горизонтах T2pyr, T7pyr, T8pyr (табл. 4). Для выявления антропогенной эмиссии использовали отношение количеств “техногенных” ПАУ к “природным” (ПИР + БаПИР)/(ФЕН + ХРИ), где ПИР, БаПИР, ФЕН, ХРИ – модули поступления пирена, бенз[а]пирена, фенантрена, хризена соответственно. Значение данного отношения >1 свидетельствует о наличии полиаренов, поступивших из “пирогенных” источников. Согласно данным, пирогенная составляющая наиболее выделяется в горизонте T7pyr (6.9), то есть преобладают полиарены, образовавшиеся в результате сгорания органических веществ.
Для ПАУ с относительной молекулярной массой 178 отношение антрацена к сумме антрацена и фенантрена (AНТ/(AНТ+ФЕН) или AНТ/178) <0.10 является индикатором “нефтяного” или природного происхождения этих соединений, в то время как отношение AНТ/178 > 0.10 указывает на образование ПАУ в результате пирогенеза [63]. Во всех исследованных горизонтах это соотношение <0.10, что указывает на преимущественно природный характер образования ПАУ. Вычисление индикаторных соотношений ПАУ, которые показывают степень пирогенности или “природности” исследуемой ассоциации, в почвах не совсем корректно, поскольку численные значения границ природные/техногенные, могут быть совершенно отличными от тех, что представлены в литературе для других географических регионов.
Одним из наиболее широко используемых способов определения PyC является метод БПКК. Именно на основании данного метода произведены современные мировые оценки содержания PyC [48]. Содержание бензолполикарбоновых кислот (табл. 5) позволяет количественно оценить долю углерода пирогенного происхождения в составе почвенного органического вещества. В исследуемой почве суммарное содержание БПКК изменяется от 0.7 до 18.4% от массы, или в пересчете на углерод, содержащийся в молекулах кислот, – от 0.3 до 8.2%, что составляет 0.6 до 14.4% от общего содержания углерода в горизонтах почвы. Наибольшее содержание PyC выявлено в пирогенном горизонте на глубине 10–15 см, что вероятно, связанно с пожаром 140-летней давности. Влияние пожаров, приведших к формированию данного торфяника, и относящихся к периоду около 9 тыс. лет до настоящего времени способствовали аккумуляции PyC в нижних горизонтах в количествах 2.4–6.9% от общего углерода. Пересчитав запасы PyC с учетом плотности сложения отдельных горизонтов, мы оценили содержание PyC в данной почве в 4.78 кг/м2 (если рассчитывать по всем восьми БПКК) или 4.36 кг/м2, если рассчитывать по 4–6 замещенным кислотам. Необходимо отметить, что в целом публикации по содержанию БПКК на территории России редки и в основном приурочены к автоморфным почвам Сибири. Данные по содержанию PyC в торфах единичны. Нами были получены несколько большие значения по запасам и содержанию PyC по сравнению с торфяными почвами лесотундры на территории Красноярского края [44]. Это может быть связано с более южным расположением нашего участка, и как следствие, большей подверженностью пожарам как в настоящее время, так и в отдельные периоды голоцена. Результаты по концентрациям PyC для исследуемой почвы существенно больше таковых для подзолов [33].
Таблица 5.
Содержание бензолполикарбоновых кислот (БПКК) в исследуемой почве
| Гори-зонт | Глуби-на, см |
Бк3* | Бк4 | Бк5 | Бк6 | Сум-ма, % | С1–6Бк | С4–6Бк | С4Бк/С6Бк | С5Бк/С6Бк | СБПКК/Собщ, % |
PyC запасы | |||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| I | II | III | IV | V | VI | VII | VIII | С1–С6 | С4–С6 | ||||||||
| % | кг/м2 | ||||||||||||||||
| TO1 | 0–10 | 0.01 | 0.06 | 0.00 | 0.06 | 0.06 | 0.07 | 0.23 | 0.21 | 0.70 | 0.32 | 0.28 | 1.00 | 1.17 | 0.65 | 0.026 | 0.022 |
| T2pyr | 10–15 | 0.45 | 0.67 | 0.00 | 0.96 | 1.82 | 1.41 | 6.58 | 6.46 | 18.36 | 8.19 | 7.61 | 0.73 | 1.07 | 14.42 | 0.78 | 0.72 |
| T3 | 15–30 | 0.01 | 0.10 | 0.00 | 0.09 | 0.10 | 0.11 | 0.67 | 0.57 | 1.65 | 0.74 | 0.68 | 0.60 | 1.22 | 1.36 | 0.21 | 0.19 |
| T4 | 30–50 | 0.02 | 0.17 | 0.01 | 0.18 | 0.20 | 0.20 | 1.40 | 1.19 | 3.37 | 1.50 | 1.40 | 0.56 | 1.24 | 3.05 | 0.63 | 0.59 |
| T5 | 50–70 | 0.02 | 0.08 | 0.01 | 0.11 | 0.16 | 0.13 | 0.53 | 0.63 | 1.67 | 0.74 | 0.69 | 0.70 | 0.89 | 1.37 | 0.34 | 0.32 |
| T6 | 70–90 | 0.01 | 0.06 | 0.00 | 0.09 | 0.14 | 0.10 | 0.46 | 0.57 | 1.44 | 0.64 | 0.60 | 0.65 | 0.85 | 1.16 | 0.33 | 0.31 |
| T7pyr | 90–105 | 0.05 | 0.15 | 0.00 | 0.27 | 0.41 | 0.38 | 0.82 | 0.71 | 2.79 | 1.27 | 1.16 | 1.67 | 1.21 | 2.39 | 1.79 | 1.64 |
| T8pyr | 105–115 | 0.08 | 0.12 | 0.00 | 0.04 | 0.04 | 0.03 | 0.71 | 0.57 | 1.58 | 0.71 | 0.61 | 0.22 | 1.32 | 6.92 | 0.67 | 0.57 |
| Сумма | 4.78 | 4.36 | |||||||||||||||
Примечание. СБПКК – содержание углерода бензолполикарбоновых кислот в горизонте, с учетом содержания углерода в отдельных молекулах. Запасы рассчитаны с учетом плотности и мощности горизонтов. * Цифрой указано число карбоксильных групп в составе БПКК. Даны тривиальные названия (химическое название): I – гемимеллитовая (бензол-1,2,3-трикарбоновая кислота); II – тримеллитовая (бензол-1,2,4-трикарбоновая кислота); III – тримезиновая (1,3,5-бензолтрикарбоновая кислота); IV – пиромеллитовая (1,2,4,5-бензолтетракарбоновая кислота); V – меллофаниковая (1,2,3,5-бензолтетракарбоновая кислота); VI – пренитовая (1,2,3,4-бензолтетракарбоновая кислота); VII – 1,2,3,4,5-бензолпентакарбоновая кислота; VIII – меллитовая (бензол-1,2,3,4,5,6-гексакарбоновая кислота) кислоты.
Полученные данные позволяют сделать вывод, что большинство используемых подходов позволяет диагностировать пирогенные признаки в составе ПОВ. При этом многие показатели имеют хорошую корреляцию между собой. Наиболее значимые коэффициенты корреляций представлены в табл. 6. Суммарное содержание БПКК кислот имеет значимые коэффициенты корреляций с концентрацией нафталина (R = 0.98, p < 0.05), фенантрена (R = 0.78, p < 0.05), флуореантена (R = 0.86, p < 0.05), ароматических фрагментов (CAr-H(C)), определяемых методом ЯМР спектроскопии (R = 0.88, p < 0.05). При этом суммарное содержание ПАУ коррелирует лишь с общим содержанием углерода в образце. Значимые корреляции с высоким коэффициентом выявлены для индивидуальных БПКК и ряда ПАУ. Для всех индивидуальных БПКК, за исключением тримезиновой кислоты, коэффициенты корреляции с нафталином составляют (от 0.96 до 0.98, p < 0.05), с фенантреном (от 0.75 до 0.78, p < 0.05), флуорантеном (0.82–0.86, p < 0.05), хризеном (0.73–0.74, p < 0.05).
Таблица 6.
Коэффициенты корреляции Пирсона некоторых исследуемых параметров
| Параметр | CAr-H(C) | AR | Caryl, % | НАФТ | ФЕН | ФЛА | ХРИ |
|---|---|---|---|---|---|---|---|
| Гемимеллитовая | 0.93* | 0.90* | 0.76* | 0.93* | 0.73* | 0.81* | 0.61 |
| Тримеллитовая | 0.88* | 0.85* | 0.80* | 0.96* | 0.75* | 0.83* | 0.65 |
| Тримезиновая | –0.22 | –0.21 | –0.03 | –0.01 | –0.07 | 0.04 | –0.29 |
| Пиромеллитовая | 0.84* | 0.81* | 0.88* | 0.96* | 0.78* | 0.83* | 0.73* |
| Меллофаниковая | 0.86* | 0.83* | 0.88* | 0.96* | 0.78* | 0.83* | 0.70 |
| Пренитовая | 0.85* | 0.81* | 0.88* | 0.96* | 0.78* | 0.82* | 0.73* |
| Бензолпентакарбоновая | 0.88* | 0.84* | 0.82* | 0.98* | 0.77* | 0.86* | 0.60 |
| Меллитовая | 0.88* | 0.85* | 0.84* | 0.98* | 0.78* | 0.87* | 0.59 |
| Сумма, % | 0.88* | 0.84* | 0.84* | 0.98* | 0.78* | 0.86* | 0.63 |
| СБПКК | 0.88* | 0.84* | 0.84* | 0.98* | 0.78* | 0.86* | 0.63 |
ЗАКЛЮЧЕНИЕ
Сравнение данных, полученных с помощью ЯМР спектроскопии, и содержания ПАУ показало, что эти методы позволяют диагностировать поступление пирогенно модифицированных органических соединений. В составе молекулярных фрагментов ПОВ с пирогенными признаками существенно увеличивается доля углерода, связанного с бензольными ядрами. В составе ПАУ горизонтов увеличивается концентрация нафталина, флуорантена, фенантрена и хризена, которые, вероятно, имеют пирогенную природу. Но при этом увеличение содержания молекулярных ароматических фрагментов и ряда индивидуальных ПАУ можно использовать в качестве маркеров пирогенеза. Данные параметры могут свидетельствовать лишь об общем тренде возрастания ароматичности почвенного органического вещества. Общие запасы ПАУ крайне малы, их концентрации лишь частично характеризуют общие содержания и запасы PyC в почвах.
Более реалистичную картину по концентрациям и запасам PyC в почвах позволяет выявить метод определения БПКК. Благодаря жесткому кислотному гидролизу из почвы извлекается большее количество ароматического углерода, которое более полно отражает его концентрации. Для количественных оценок по определению углерода пирогенного происхождения он более применим.
Список литературы
Атлас Республики Коми по климату и гидрологии / Под ред. А.И. Таскаева. М.: Наука, 1997. 116 с.
Варсанофьева В.А. Геоморфология. Производительные силы Коми АССР. Т. 1. Геологическое строение и полезные ископаемые. М.: Изд-во АН СССР, 1953. С. 257–270
Габбасова И.М., Сулейманов Р.Р., Ситдиков Р.Н., Гарипов Т.Т. Пирогенная деградация осушенных торфяных почв // Почвоведение. 2005. № 6. С. 724–730.
Голубева Ю.В. Климат и растительность голоцена на территории Республики Коми // Литосфера. 2008. № 2. С. 124–128.
Дегтева С.В., Гончарова Н.Н. Проблемы охраны болот Республики Коми // Известия Коми научного центра УрО РАН. 2012. № 10. С. 29–35.
Дымов А.А. Сукцессии почв в бореальных лесах Республики Коми. М.: ГЕОС, 2020. 336 c. https://doi.org/10.34756/GEOS.2020.10.37828
Ефремова Т.Т., Ефремов С.П. Пирогенная трансформация органического вещества почв лесных болот // Почвоведение. 2006. № 12. С. 1441–1450.
Зайдельман Ф.Р. Минеральные и торфяные почвы Полесских ландшафтов. М.: Красанд, 2013. 440 с.
Инишева Л.И. Торфяные почвы: их генезис и классификация // Почвоведение. 2006. № 7. С. 781–786.
Красильников П.В. Устойчивые соединения углерода в почвах: происхождение и функции // Почвоведение. 2015. № 9. С. 1131–1144. https://doi.org/10.7868/S0032180X15090075
Краснощеков Ю.Н. Почвы горных лесов Прибайкалья и их трансформация под влиянием пожаров // Почвоведение. 2018. № 4. С. 387–401. https://doi.org/10.7868/S0032180X18040019
Куприянов Д.А., Новенко Е.Ю. Реконструкция динамики лесных пожаров Центральной Мещеры в голоцене (по данным палеоантракологического анализа) // Сибирский экологический журн. 2019. № 3. С. 253–263. https://doi.org/10.15372/SEJ20190302
Милановский Е.Ю. Гумусовые вещества почв как природные гидрофобно-гидрофильные соединения. М.: ГЕОС, 2009. 186 с.
Новенко Е.Ю., Мазей Н.Г., Куприянов Д.А., Волкова Е.М., Цыганов А.Н. Динамика растительности и экологических условий в центре Восточно-Европейской равнины в Голоцене // Экология. 2018. № 3. С. 184–193. https://doi.org/10.7868/S0367059718030034
Опекунов А.Ю., Митрофанова Е.С., Опекунова М.Г. Техногенная транформация состава донных отложений рек и каналов Санкт-Петербурга // Геоэкология. Инженерная геология. Гидрогеология. Геокриология. 2017. № 4. С. 48–61.
Орлов Д.С., Садовникова Л.К., Суханова Н.И. Химия почв. Изд-во: Высшая школа, 2005. 561 с.
Пастухов А.В., Каверин Д.А. Запасы почвенного углерода в тундровых и таежных экосистемах Северо-восточной Европы // Почвоведение. 2013. № 9. С. 1084–1094. https://doi.org/10.7868/S0032180X13070083
Пастухов А.В., Каверин Д.А. Экологическое состояние мерзлотных бугристых торфяников на северо-востоке Европейской России // Экология. 2016. № 2. С. 94–102. https://doi.org/10.7868/S0367059716010108
Подзолистые почвы центральной и восточной частей европейской территории СССР. Л.: Наука, 1981. С. 118–152.
Полевой определитель почв России. М., 2008. 182 с.
Сартаков М.П. Спектроскопия ЯМР 13 гуминовых кислот торфов Среднего Приобъя // Химия растительного сырья. 2008. № 3. С. 135–139.
Торфяные ресурсы Республики Коми. Сыктывкар, 2000. 613 с.
Фуряев В.В. Роль пожаров в процессе лесообразования. Новосибирск: Наука, Сибирская издательская фирма РАН, 1996. 253 с.
Цыбарт А.С., Геннадиев А.Н. Влияние пожаров на свойства лесных почв Приамурья (Норский заповедник) // Почвоведение. 2008. № 7. С. 783–792.
Чичагова О.А. Радиоуглеродное датирование гумуса почв. М.: Наука, 1985. 158 с.
Abakumov E., Pechkin A., Chebykina (Maksimova) E., Shamilishvili G. Effect of the Wildfires on Sandy Podzol Soils of Nadym Region, Yamalo-Nenets Autonomous District, Russia // Appl. Environ. Soil Sci. 2020. Art. 8846005. https://doi.org/10.1155/2020/8846005
Baldock J.A., Preston C.M. Chemistry of carbon decomposition processes in forests as revealed by solid-state carbon-13 nuclear magnetic resonance // Carbon Forms and Functions in Forest Soils. Madison, Wisconsin, 1995. P. 89–117.
Bento-Goncalves A., Vieira A., Ubeda X., Martin D. Fire and soils: Key concepts and recent advances // Geoderma. 2012. V. 191. P. 3–13. https://doi.org/10.1016/j.geoderma.2012.01.004
Birk J.J., Dippold M., Wiesenberg G.L.B., Glaser B. Combined quantification of faecal sterols, stanols, stanones and bile acids in soils and terrestrial sediments by gas chromatography–mass spectrometry // J. Chromatography A. 2012. V. 1242. P. 1–10. https://doi.org/10.1016/j.chroma.2012.04.027
Bobrovsky M.V., Kupriaynov D.A., Khanina L.G. Anthracological and morphological analysis of soils for the reconstruction of the forest ecosystem history (Meshchera Lowlands, Russia) // Quat. Int. 2019. P. 70–82. https://doi.org/10.1016/j.quaint.2018.06.033
Brodowski S., Rodionov A., Haumaier L., Glaser B., Amelung W. Revised black carbon assessment using benzene polycarboxylic acids // Org. Geochem. 2005. V. 36. P. 1299–1310. https://doi.org/10.1016/j.orggeochem.2005.03.011
Certini G. Fire as a soil-forming factor // Ambio. 2014. V. 43. P. 191–195.
Czimczik C.I., Schmidt M.W.I., Schulze E.D. Effects of increasing fire frequency on black carbon and organic matter in Podzols of Siberian Scots pine forests // Eur. J. Soil Sci. 2005. V. 56. P. 417–428.
Doerr S.H., Santın C. Global trends in wildfire and its impacts: perceptions versus realities in a changing world // Philosophical Transactions of the Royal Society B. Biological Sciences. 2016. V. 371. P. 1–10. https://doi.org/10.1098/rstb.2015.0345
Dyakonov K.N., Novenko E.Y., Mironenko I.V., Kuprijanov D.A., Bobrovsky M.V. The role of fires in the Holocene landscape dynamics of the southeastern part of Meshchera lowlands // Doklady Earth Sciences. 2017. V. 477. P. 1336–1342. https://doi.org/10.1134/S1028334X17110125
Dymov A.A., Gabov D.N., Milanovskii E.Yu. 13C-NMR, PAHs, WSOC and repellence of fire affected soils (Albic Podzols, Russia) // Environ. Earth Sci. 2017. V. 76. P. 1–10. https://doi.org/10.1007/s12665-017-6600-2
Dymov A.A., Gabov D.N. Pyrogenic alterations of Podzols at the North-East European part of Russia: morphology, carbon pools, PAH content // Geoderma. 2015. V. 241–242. P. 230–237. https://doi.org/10.1016/j.geoderma.2014.11.021
Egli M., Mastrolonardo G., Seiler R., Raimondi S., Favilli F., Crimi V., Krebs R., Cherubini P., Certini G. Charcoal and stable soil organic matter as indicators of fire frequency, climate and past vegetation in volcanic soils of Mt. Etna, Sicily // Catena. 2012. V. 88. P. 14–26. https://doi.org/10.1016/j.catena.2011.08.006
Forbes M.S., Raison R.J., Skjemstad J.O. Formation, transformation and transport of black carbon (charcoal) in terrestrial and aquatic ecosystems // Sci. Total Environ. 2006. V. 370. P. 190–206. https://doi.org/10.1016/j.scitotenv.2006.06.007
Gabov D.N., Yakovleva Ye.V., Vasilevich R.S. Vertical distribution of PAHs during the evolution of permafrost peatlands of the European arctic zone // Appl. Geochem. 2020. V. 123. P. 104790. https://doi.org/10.1016/j.apgeochem.2020.104790
Glaser B. Eigenschaften und Stabilität des Humuskörpers der ‘Indianerschwarzerde’ Amazoniens. Dissertation thesis, University of Bayreuth. Germany. Bayreuther Bodenkundliche Berichte, 1999. V. 68.
Glaser B., Haumaier L., Guggenberger G., Zech W. Black carbon in soils: The use of benzenecarboxylic acids as specific markers // Org. Geochem. 1998. V. 29. P. 811–819.
Goncalves C.N., Dalmolin S.D., Dick D.P., Knicker H., Klamt E., Kögel-Knabner I. The effect of 10% HF treatment on resolution of CPMAS 13C NMR spectra and on the quality of organic matter in Ferralsols // Geoderma. 2003. V. 116. P. 373–392.
Guggenberger G., Rodionov A., Shibistova O., Grabe M., Kasansky O.A., Fuchs H., Mikheyeva N., Zrazhevskaya G., Flessa H. Storage and mobility of black carbon in permafrost soils of the forest tundra ecotone in Northern Siberia // Global Change Biol. 2008. V. 14. P. 1367–1381.
Hammes K., Schmidt M.W.I., Smernik R.J. et al. Comparison of quantification methods to measure fire-derived (black/elemental) carbon in soils and sediments using reference materials from soil, water, sediment and the atmosphere // Global Biogeochem. Cycles. 2007. V. 21. Art. GB3016. https://doi.org/10.1029/2006GB002914
Higuera P. CharAnalysis 0.9: diagnostic and analytical tools for sediment charcoal analysis. User’s Guide, Montana State University, Bozeman, MT. 2009.
IUSS Working Group WRB, 2015. World Reference Base for Soil Resources 2014, update 2015. International soil classification system for naming soils and creating legends for soil maps. World Soil Resources Reports No. 106. FAO, Rome.
Jones M.W., Coppola A.I., Santín C., Dittmar T., Jaffé R., Doerr S.H., Quine T.A. Fires prime terrestrial organic carbon for riverine export to the global oceans // Nat. Commun. 2020. V. 11. P. 2791.
Kuzyakov Y., Bogomolova I., Glaser B. Biochar stability in soil: Decomposition during eight years and transformation as assessed by compound specific 14C analysis // Soil Biol. Biochem. 2014. V. 70. P. 229–236. https://doi.org/10.1016/j.soilbio.2013.12.021
Leifeld J., Alewell C., Bader C., Krüger J.P., Mueller C.W., Sommer M., Steffens M., and Szidat S. Pyrogenic Carbon Contributes Substantially to Carbon Storage in Intact and Degraded Northern Peatlands // Land Degrad. Develop. 2018. V. 29. P. 2082–2091. https://doi.org/10.1002/ldr.2812
Lodygin E.D., Alekseev I.I., Vasilevich R.S., Abakumov E.V. Complexation of lead and cadmium ions with humic acids from arctic peat soils // Environ. Res. 2020. V. 191. https://doi.org/10.1016/j.envres.2020.110058
Mooney S., Tinner W. The analysis of charcoal in peat and organic sediments // Mires and Peat. 2011. V. 7. P. 1–18.
Pereira P., Cerdà A., Jordán A., Martínez-Zavala L., Mataix-Solera J., Arcenegui V., Misiune I., Keesstra S., Novara A. Short-term vegetation recovery after a grassland fire in lithuania: The effects of fire severity, slope position and aspect // Land Degradation Development. 2016. V. 27. P. 1523–1534. https://doi.org/10.1002/ldr.2498
Preston C.M., Schmidt M.W.I. Black (pyrogenic) carbon: a synthesis of current knowledge and uncertainties with special consideration of boreal regions // Biogeosciences. 2006. V. 3(4). P. 397–420.
Reisser M., Purves R.S., Schmidt M.W.I., Abiven S. Pyrogenic carbon in soils: a literature-based inventory and a global estimation of its content in soil organic carbon and stocks // Frontiers Earth Sci. 2016. V. 4. P. 1–14. https://doi.org/10.3389/feart.2016.00080
Sartakov M.P., Novikov A.A., Chukhareva N.V. Study of humic acids in various types and kinds of peats at Khantymansi autonomous area – Ygra by 13C spectroscopy // Int. J. Pharmacy Technol. 2016. V. 8. № 2. P. 14204–14213.
Santin C., Doerr S.H., Jones M.W., Merino A., Warneke C., Roberts J.M. The relevance of pyrogenic carbon for carbon budgets from fires: Insights from the FIREX experiment // Global Biogeochem. Cycles. 2020. V. 34. P. e2020GB006647. https://doi.org/10.1029/2020GB006647
Sirin A.A., Medvedeva M.A., Makarov D.A., Maslov A.A., Joosten H. Multispectral satellite based monitoring of land cover change and associated fire reduction after large-scale peatland rewetting following the 2010 peat fires in Moscow Region (Russia) // Ecological Engineering. 2020. V. 158. 106044. https://doi.org/10.1016/j.ecoleng.2020.106044
Skjemstad J.O., Clarke P., Taylor J.A., Oades J.M., Neuman R.H. The removal of Magnetic Materials from surface soils. A solid state 13C CP/MAS n. m. r. // Aust. J. Soil Res. 1994. V. 32. P. 1215–1229. https://doi.org/10.1071/SR9941215
Van Reeuwijk L.P. (Ed.) Procedures for soil analysis. Technical Paper, 9. ISRIC, Wageningen. 2002.
Vergnoux A., Malleret L., Asia L., Doumenq P., Theraulaz F. Impact of forest fires on PAH level and distribution in soils // Environ. Res. 2011. V. 111. P. 193–198. https://doi.org/10.1016/j.envres.2010.01.008
Wiedemeier D.B., Brodowski S., Wiesenberg G.L.B. Pyrogenic molecular markers: Linking PAH with BPCA analysis // Chemosphere. 2015. V. 119. P. 432–437. https://doi.org/10.1016/j.chemosphere.2014.06.046
Yunker M.B., Macdonald R.W., Vingarzan R., Mitchell R.H., Goyette D., Sylvestre S. PAHs in the Fraser River basin: a critical appraisal of PAH ratios as indicators of PAH source and composition // Org. Geochem. 2002. V. 33. P. 489–515.
Дополнительные материалы отсутствуют.