Почвоведение, 2022, № 4, стр. 428-444
Изучение подвижности и биологической доступности цинка в почве с использованием 65Zn в условиях вегетационного лизиметрического эксперимента
В. С. Анисимов a, *, Л. Н. Анисимова a, А. И. Санжаров a, Р. А. Фригидов a, Д. В. Дикарев a, Ю. Н. Корнеев a, С. В. Коровин a, А. В. Саруханов a, А. В. Томсон a
a Всероссийский НИИ радиологии и агроэкологии
249030 Калужская область, Обнинск, Киевское ш., 109-й км, Россия
* E-mail: vsanisimov@list.ru
Поступила в редакцию 09.09.2021
После доработки 26.11.2021
Принята к публикации 29.11.2021
- EDN: FSHDHJ
- DOI: 10.31857/S0032180X22040037
Аннотация
С использованием вегетационного стенда, объединяющего в замкнутом цикле специальную лизиметрическую установку, заполненную дерново-подзолистой почвой легкого гранулометрического состава и дренажем, а также вегетационные сосуды с водной культурой ячменя, исследованы процессы перехода в водную фазу и поглощения растениями природного (стабильного) Zn и радиоактивного изотопа 65Zn. При этом процессы перехода цинка в водную фазу почвы и поглощения растениями хотя и разделены пространственно, но являются последовательно сопряженными. Установлены закономерности распределения Zn(65Zn) между различными формами (химическими фракциями) в почве с помощью методов параллельного и последовательного фракционирования. Относительное содержание стабильного Zn (по сравнению с валовым количеством) в подвижных и условно подвижных формах было в 2.1–6.5 раза меньше, чем относительное содержание радионуклида 65Zn и, наоборот, в 2.8–3.0 раза больше для консервативных (неподвижных) форм металла в почве. В динамике оценены концентрация Zn, удельная активность 65Zn, коэффициенты распределения и концентрирования природного Zn и 65Zn, накопление и вынос металла растениями. Определены величины коэффициентов обогащения природного (стабильного) Zn, содержащегося в последовательно извлекаемых химических фракциях, радиоизотопом 65Zn, рассчитана величина запаса подвижных соединений Zn в исследуемой почве.
ВВЕДЕНИЕ
Среди тяжелых металлов (ТМ), загрязняющих почву в результате антропогенного воздействия, наиболее распространенным является цинк [15, 34, 40, 48, 49]. Источниками загрязнения являются использование удобрений и осадков сточных вод в сельском хозяйстве, выбросы и сбросы горнодобывающей и металлургической промышленности, а также автомобильный транспорт [47, 56].
Вместе с тем Zn является одним из 17 необходимых элементов для растений со средним содержанием в сухой вегетативной массе 0.002% (20 ppm). Ионный радиус Zn2+ аналогичен радиусу Fe2+ и Mg2+, он может принимать участие в процессах изоморфного замещения этих элементов в структурах минералов [49]. Дефицит Zn отрицательно влияет на рост и созревание растений [28, 49], что приводит к потерям урожая и в наиболее тяжелых случаях к гибели растений. Часто дефицит цинка обусловлен не только низким содержанием металла в почве, но и влиянием типа почв, определяющим доступность его растениям [27, 29]. В работе [37] отмечается, что дефицит Zn наблюдается во всех почвах с низкой доступностью Zn, к которым относятся известкованные и сильнозафосфаченные почвы с высокими значениями pH.
Около 50% почв мира содержат недостаточное количество Zn [14]. Дефицит Zn отмечен для почв Бангладеш, Бразилии, Пакистана, Филиппин и Судана, стран Африки к югу от Сахары, Индии, Турции, западной Австралии, Китая, а также на Великих равнинах и в западных регионах Соединенных Штатов [28, 29].
Подвижность в почвах и доступность Zn растениям сильно зависят от соотношения различных форм нахождения (химических фракций) элемента в почвах. В кислых почвах растворимость Zn в основном контролируется процессами катионного обмена и адсорбции на глинистых минералах и органическом веществе почвы, при этом его биологическая доступность относительно высока. В почвах с нейтральной и щелочной реакцией подвижность и биологическая доступность Zn вследствие специфической сорбции органическим веществом, глинистыми минералами, оксидами Fe и Al, а также процессов хемосорбции и соосаждения уменьшаются [13, 14, 34, 56].
По степени подвижности и доступности растениям Зырин с соавт. [12] выделили 3 группы форм нахождения ТМ в почвах: 1) мобильные соединения – непосредственный источник и резерв питания растений, 2) фиксированные соединения – потенциальный резерв питания растений и 3) изоморфные примеси в минералах – стратегический резерв. Поскольку видоспецифический анализ соединений ТМ в почвах методами химического фракционирования провести невозможно, приходится ограничиваться анализом группового фракционного состава, определяемым выбранной схемой фракционирования и используемыми групповыми экстрагентами. Соответственно, классификация форм нахождения ТМ в почвах строится с учетом перехода соединений элементов в различные растворители [12].
К настоящему времени разработано большое количество методов определения фракционного состава ТМ в почвах. Все они используют специфичные реактивы для выделения отдельных групп соединений ТМ в почвах (обменных, легкорастворимых, связанных с органо-минеральными комплексными соединениями, связанных с органическим веществом, карбонатами, оксидами Fe, Mn и др.). При всем разнообразии данные методы можно разделить на две большие группы: параллельной и последовательной экстракций.
Методы параллельной экстракции [2, 5, 16, 17, 43] позволяют выделить основные формы нахождения ТМ в почвах по степени их доступности растениям: легкодоступная = (водорастворимая + обменная), доступная = (подвижная – (водорастворимая + обменная)), потенциально доступная = = (кислоторастворимая – подвижная), потенциальный резерв = (валовое количество – кислоторастворимая).
В то же время с помощью схем последовательного химического фракционирования ТМ [22, 30, 35, 36, 38, 39, 44–46, 48, 51, 57, 60] возможно не только оценить их подвижность и биологическую доступность, но и распределение по фракциям основных групп соединений и минералов в почвах (обменной, связанной с оксидами Al, Fe, Mn, карбонатами, фосфатами, сульфидами, органическим веществом, кристаллической матрицей почвенных минералов), а также оценить подвижность и биологическую доступность ТМ при изменении почвенных условий (pH, окислительно-восстановительного потенциала, влажности, солесодержания и др.).
Все вышеперечисленные методы позволяют исследователям лишь условно и с большой долей приближения решить главную задачу – оценить реальный запас подвижных и доступных растениям соединений ТМ. Фактически, корректное решение этой задачи возможно только с использованием метода изотопного разбавления [19, 24, 25, 31, 47, 55, 60]. Данный метод основан на законе идеального изотопного обмена [7] ионов внесенного радиоактивного или стабильного изотопа, выступающего в качестве метки, и ионов нативных стабильных изотопов исследуемого ТМ в системе почва–почвенный раствор–растение. Метод изотопного разбавления позволяет рассчитать: а) величину запасов (пулов) в почве общего количества подвижных соединений исследуемого ТМ − E-value (EТМ) и б) общего количества биологически доступных соединений ТМ − L-value (LТМ). Эти показатели определяют на основании отношения метки и стабильных изотопов ТМ соответственно: а) в почве и в равновесном почвенном растворе, б) в почве и в растениях. В теории EТМ и LТМ различаются на величину корневого захвата ТМ растениями в результате выделения ими органических кислот [33, 41, 42] и комплексонов [53, 58]. Зона воздействия последних ограничивается ризосферой и, в некоторой степени, прикорневой зоной <1 см.
Проблемы, связанные с недооценкой пула подвижных соединений ТМ в почве (EТМ) [31, 55], удалось преодолеть с помощью специального методического приема, получившего название isotope exchange kinetics (IEK), заключающегося в определении предельных величин параметров кривых, аппроксимирующих динамику изотопного обмена EТМ = f(t) в течение суток [19, 24, 26, 31, 55].
Метод изотопного разбавления, являясь источником ценных данных о величине запасов (пулов) подвижных и биологически доступных соединений ТМ в почве, не позволяет получить сведения о потенциальной подвижности в системе почва–почвенный раствор и биологической доступности различных форм нахождения ТМ. Для решения вышеуказанной задачи необходимо применение комплексного подхода, включающего совместное использование методов изотопного разбавления и последовательного фракционирования почвы, в которую предварительно внесена стабильная или радиоактивная метка ТМ. Подобные работы проводятся с целью установления источников и изучения вклада антропогенной составляющей в загрязнение почв ТМ, а также выявления трендов в трансформации форм их нахождения. Для этого анализируются изотопные отношения, например, 206Pb/207Pb, 66Zn/64Zn и др. для почвы в целом, для отдельных химических фракций (как в поверхностном слое, так и на различной глубине), а также для загрязняющих компонентов (пыли, аэрозолей, сбросных вод) от различных источников загрязнения [20, 40, 55, 59].
В то же время исследователи не уделяют должного внимания вопросам, связанным с оценкой потенциальной подвижности и биологической доступности ТМ на основании анализа изотопных отношений для отдельных химических фракций.
Цель работы: определение запасов подвижных и биологически доступных соединений нативного Zn с использованием в качестве радиоактивной метки 65Zn; оценка потенциальной подвижности и биологической доступности отдельных форм нахождения металла в почве в условиях, максимально приближенных к равновесным. Для этого разработана и апробирована на практике специальная проточная лизиметрическая установка циклического действия.
ОБЪЕКТЫ И МЕТОДЫ
Вегетационный эксперимент с водной культурой ячменя проводили с использованием специального стенда, включающего проточную лизиметрическую установку оригинальной конструкции (рис. 1, S1 ). Помимо лизиметрической установки циклического действия, обеспечивающей гравитационный сток почвенной влаги, стенд включал проточные вегетационные сосуды с почвенным раствором, в которые на специальных подставках в контейнерах с сетчатым дном (капроновая ткань), заполненных грубым песком, размещали проросшие семена растений; перистальтический насос; систему трубок, кранов и тройников-переходников; буферную емкость; источник освещения для растений. Сверху проточные лизиметры негерметично прикрывали крышкой из плексигласа с приспособлением для дождевания.
Рис. 1.
Структурно-динамическая схема стенда для изучения параметров миграции Zn (65Zn) в системе почва–почвенный раствор–растение: 1 – колонка из плексигласа с почвой и песком; 2 – вегетационный сосуд с растениями; 3 – перистальтический насос с компьютерным управлением; 4 – буферная емкость; 5 – тройник; 6 – стеклянный кран; 7 – лейка; 8 – сетка; 9 – почва; 10 – песок мелкий; 11 – прослойка грубого песка; 12 – перфорированная пластина и сетка; 13 – силиконовая пробка с отверстием для стеклянных трубок; 14 – силиконовые трубки.
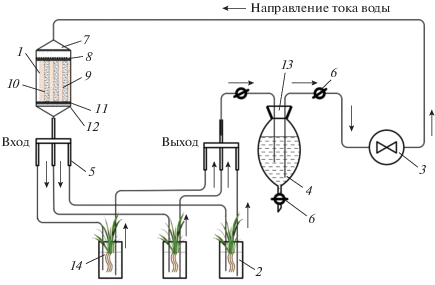
В качестве объектов исследования использовали ячмень (Hordeum vulgare L.) сорта Зазерский-85, а также дерново-подзолистую супесчаную почву (Albic Retisol (Loamic, Ochric)). Место отбора почвы д. Передоль Жуковского района Калужской области.
Физические и химические показатели почв (табл. 1) определяли общепринятыми методами [1, 3, 10]: pHKCl$\left( {{\text{р}}{{{\text{Н}}}_{{{{{\text{Н}}}_{{\text{2}}}}{\text{О}}}}}} \right)$ – потенциометрическим, в суспензии почвы в 1 М растворе KCl (дистиллированной воде) при соотношении твердой и жидкой фаз (т : ж) 1 : 2.5, гранулометрический состав почв – пипеточным методом Н.А. Качинского, содержание органического углерода – по методу Тюрина, гидролитическую кислотность – по Каппену, сумму поглощенных оснований – по Каппену–Гильковицу, содержание подвижных форм P2O5 – по Кирсанову в модификации ЦИНАО (0.2 M HCl, т : ж = 1 : 5). Обменные формы калия, кальция и магния извлекали из почв с помощью 1 M NH4Cl (pH 6.5) [3], CH3COONH4 (pH 7.0) – ацетатно-аммонийного буферного раствора (ААБ-7.0) [1], а также с помощью 1 M CH3COONH4 (pH 4.8) – ацетатно-аммонийного буферного раствора (ААБ-4.8), до отрицательной реакции на ионы Ca2+ [2, 12].
Таблица 1.
Основные характеристики исследуемой почвы
| Показатель | Дерново-подзолистая супесчаная почва | ||
|---|---|---|---|
| pHKCl | 5.05 ± 0.01 | ||
| ${\text{р}}{{{\text{Н}}}_{{{{{\text{Н}}}_{{\text{2}}}}{\text{О}}}}}$ | 6.04 ± 0.01 | ||
| Органический углерод, % | 1.0 ± 0.01 | ||
| Hг, смоль(+)/кг почвы | 1.89 ± 0.02 | ||
| Массовая доля фракции <0.01 мм в почве, % | 18.39 | ||
| Сумма обменных оснований, смоль(+)/кг почвы | 5.3 ± 0.1 | ||
| Zn валовый, мг/кг почвы | 41.2 ± 2.6 | ||
| Содержание обменных катионов, смоль(+)/кг почвы, извлекаемых: | Ca2+ | Mg2+ | K+ |
| 1 M NH4Cl (pH 6.5) | 5.70 ± 0.68 | 0.53 ± 0.05 | 0.19 ± 0.02 |
| 1 M CH3COONH4 (pH 7.0) | 5.21 ± 0.08 | 0.47 ± 0.10 | 0.17 ± 0.01 |
| 1 M CH3COONH4 (pH 4.8) | 5.20 ± 0.06 | 0.40 ± 0.09 | 0.15 ± 0.01 |
Предварительная подготовка почвы включала внесение в нее радионуклида 65Zn (τ1/2 = 224 сут) в количестве 200 кБк/кг в виде рабочего раствора 65Zn(II) без изотопного носителя – стабильного Zn. Рабочий раствор готовили из образцового раствора 65Zn(II) в 0.1 M HCl (Cyclotron Co., Ltd., паспорт № С-739-19), содержавшего на момент аттестации 42.4 МБк 65Zn. Суспензию тщательно перемешивали. Далее почву подсушивали до воздушно-сухого состояния и инкубировали при комнатной температуре на воздухе в течение полугода, регулярно (2 раза в месяц), увлажняя до полной влагоемкости. Окончательно почву доводили до воздушно-сухого состояния, растирали и пропускали через сито 2 мм. Подготовленную таким образом почву с внесенным радионуклидом послойно помещали в лизиметрическую установку, чередуя слои почвы и отмытого кварцевого мелкозернистого (0.4–0.8 мм) песка, являющегося дренажем. Направление ориентации слоев почвы/песка вертикальное (для обеспечения бесперебойной циркуляции раствора через лизиметр), толщина слоев 2.5 см. Сверху и снизу массив почва/песок последовательно переслаивали фракциями мелкого (0.4–0.8 мм) и грубого (1.5–3 мм) песка и защитной мелкоячеистой капроновой сеткой. Количество почвы в лизиметре 5 кг, столько же дренажа (крупного и мелкого песка). Отмытый кварцевый песок, использованный в опыте, имеет крайне низкую удельную поверхность (<0.01 м2/г) и практически нулевую емкость поглощения. Скорость тока влаги через перистальтический насос 4 см3/мин. Учитывая, что общий объем жидкой фазы в системе составлял около 5.5. дм3, раствор подвергался полной рекуперации, проходя через лизиметр, в течение суток.
После сборки лизиметрическую установку оборачивали светонепроницаемой пленкой. Приливали на поверхность почвы в лизиметре 2.0 дм3 деионизированной воды и уравновешивали систему почва–раствор в течение 5 мес., периодически возвращая стекающую из лизиметра воду обратно на поверхность почвы. Затем собирали вегетационный стенд, дополнительно вносили в систему 3.5 дм3 деионизированной воды, запускали перистальтический насос и оставляли систему в рабочем режиме для уравновешивания на 3 недели. Постоянный уровень лизиметрического раствора в вегетационных сосудах поддерживали, периодически доливая деионизированную воду на поверхность почвы в лизиметре (100–150 мл/сут). За неделю до начала вегетационного опыта добавляли питательные элементы в виде водных растворов солей (NH4NO3 и K2SO4) из расчета N100, и K100. Дополнительный фосфор не вносили, поскольку содержание его подвижных форм в почве было достаточным.
Растения выращивали в стеклянных вегетационных сосудах объемом 2 дм3 в 3-кратной повторности. Объем почвенного лизиметрического раствора в каждом сосуде был примерно 1.25 дм3. Перемешивание растворов осуществляли барботированием воздухом, непрерывно подаваемым в каждый вегетационный сосуд по тонким силиконовым трубкам с помощью маломощного компрессора. Для компенсации испаряющейся влаги общий объем ежедневно доливаемой деионизированной воды на поверхность почвы в лизиметре составлял 150–200 мл. В каждый вегетационный сосуд помещали пластиковый сепаратор на подставках с шестью большими отверстиями, в которые вставляли закрытые снизу капроновой тканью картриджи, заполненные крупным отмытым кварцевым песком (2–3 мм), касающиеся поверхности воды. В каждый картридж высаживали по 3 пророщенных в течение трех суток ростка ячменя. После появления корней снаружи картриджа последние приподнимали таким образом, чтобы дно их не касалось воды в сосуде. Между вегетационными сосудами и буферной емкостью за тройником устанавливали фильтр грубой очистки в виде трубчатой стеклянной воронки с пористой пластиной ПОР 40 (16–40 мкм) для задерживания органических остатков и водорослей, образующихся в вегетационных сосудах (на рис. 1 не показан). Продолжительность вегетационного опыта составляла 35 дней. Всего в ходе опыта провели 5 отборов растений – еженедельно. Из-за малой массы растительного материала количество отбираемых растений после первой недели опыта было удвоено.
В ходе вегетационного эксперимента определены в динамике значения следующих показателей (табл. 2):
Таблица 2.
Определяемые показатели активности 65Zn и концентрации Zn в исследуемых объектах
| Показатель* | Обозначение |
|---|---|
| Удельная активность 65Zn в почве, Бк/кг | Am65Znпочва |
| Удельная активность 65Zn в вегетативной массе и корнях растений, Бк/кг | Am65Znраст |
| Объемная активность 65Zn в фазе раствора, Бк/дм3 | Av65Zn |
| Концентрация цинка в почве, в вегетативной массе и корнях растений, мг/кг | [Zn]почва, [Zn]ВЧ, [Zn]корни |
| Коэффициент распределения 65Zn, дм3/кг | Kd65Zn = Am65Znпочва/Av65Znраствор |
| Коэффициент распределения Zn, дм3/кг | KdZn = [Zn]почва/[Zn]раствор |
| Коэффициент концентрирования 65Zn вегетативными частями растений, дм3/кг | KK65Zn = Am65ZnВЧ/Av(65Zn)раствор |
| Коэффициент концентрирования Zn вегетативными частями растений, дм3/кг | КК(Zn) = [Zn]ВЧ/[Zn]раствор |
| Удельная активность (65Zn/Zn), Бк/мг: | |
| – в растворе | Am(65Zn/Zn)раствор = Av65Zn/[Zn]раствор |
| – в почве, в отдельных химических фракциях (формах нахождения) элементов | Am(65Zn/Zn)фр№ = Am65Znфр№/[Zn]фр№ |
| – в вегетативных частях растений | Am(65Zn/Zn)ВЧ = Am65ZnВЧ /[Zn]ВЧ |
| – в корнях | Am(65Zn/Zn)корни = Am65Znкорни/[Zn]корни |
Удельная активность почвы, обусловленная присутствием радиоизотопа 65Zn $\left( {A_{m}^{{}}{\kern 1pt} {{\,}^{{65}}}{\text{Z}}{{{\text{n}}}_{{{\text{почва}}}}}} \right),$ на начало рассматриваемого вегетационного опыта составила 68700 ± 2800 Бк/кг.
Концентрацию Zn(65Zn) в корнях и вегетативных частях (ВЧ) растений ячменя определяли после озоления при температуре 500°C [5], общее содержание Zn в почве определяли после озоления при 500°C и последующего разложения образцов с помощью HClконц + HNO3конц + HFконц [8].
Элементный анализ проводили методами атомной абсорбции и оптической эмиссии с индуктивно-связанной плазмой с помощью спектрометров 140AA (Agilent) и Liberty II (Varian). Массовую/объемную удельные активности 65Zn определяли на γ-спектрометрическом комплексе в составе детектора и анализатора Ortec HPGe (с относительной эффективностью регистрации 40%) и программного обеспечения LSRM SpectraLine GP.
Непосредственно перед началом вегетационного опыта определяли формы нахождения цинка в почве, находящейся в лизиметре и имеющей влажность, равную наименьшей влагоемкости (табл. 3). Смешанный образец почвы получали путем объединения малых проб (m ≈ 5 г), извлеченных с помощью специального бурика, изготовленного из химически инертного материала (всего 10 уколов). Из объединенной пробы после тщательного ее усреднения путем разминания в герметично закрытом прочном полиэтиленовом пакете отбирали образцы на влажность, а также необходимое в соответствии с индивидуальной схемой фракционирования количество почвы (сырой, в пересчете на сухую массу).
Таблица 3.
Описание использованных методов параллельной и последовательной экстракции форм нахождения Zn(65Zn) в почве
| Форма нахождения Zn(65Zn)/Описание процедуры экстракции |
| Параллельная экстракция |
| Обменная/1 M CH3COONH4, pH 4.8 (ААБ-4.8) |
| Обменная и связанная в металлоорганических комплексах (ОМК)/ААБ-4.8 + 1% EDTA |
| Последовательная экстракция по методу Тессье в модификации Ферстнера |
| I. Обменная/1 M CH3COONH4 (pH 7.0) – ААБ-7.0 |
| II. Связанная с карбонатами/1 М CH3COONa (pH 5.0) |
| III. Связанная с легко восстанавливаемыми оксидами Mn (частично Fe)/0.1 M NH2OH–HCl в 0.01 M HNO3 |
| IV. Связанная с восстанавливаемыми оксидами Fe–Mn/0.1 M H2C2O4 + (NH4)2C2O4 буферный раствор (pH3.2–3.3) |
| V. Связанная с окисляемым органическим веществом и сульфидами/Смесь 0.02 M HNO3 + 30% H2O2 (v : v = 3 : 5), pH 2 |
| VI. Связанная с кристаллической матрицей первичных и вторичных почвенных минералов/Выпаривание с HNO3 (конц) при T = 95°C |
| VII. Остаточная (связанная с кристаллической матрицей первичных и вторичных почвенных минералов и не извлекаемая HNO3 (конц) при нагревании)/Определяют по разности между валовым количеством металла и общей удельной активностью 65Zn в почве и суммарным содержанием их во фракциях I–VI |
Подвижный Zn(65Zn) извлекали с помощью ААБ-4.8 в предложенной Зыриным с соавт. [12] модификации – последовательными исчерпывающими экстракциями до отрицательной реакции на Ca2+. Содержание подвижных и связанных в металлоорганических комплексах соединений Zn(65Zn) определяли методом, предложенным Минкиной с соавт. [45], также последовательными исчерпывающими экстракциями до отрицательной реакции на Ca2+. Данная схема параллельной экстракции ТМ из почв учитывает некоторые упущения предыдущей схемы. В частности, в группу непрочносвязанных соединений ТМ помимо соединений ТМ, экстрагируемых ААБ-4.8 и классифицируемых авторами как “обменные формы ТМ”, было предложено включить и соединения ТМ, связанные в металлоорганических комплексах (ОМК), для извлечения которых использовали групповой реагент ААБ-4.8 + 1% EDTA. Таким образом, разница в содержании ТМ, экстрагируемых из почв ААБ-4.8 + 1% EDTA и ААБ-4.8 представляет собой количество ТМ в виде комплексных соединений с органическим веществом почвы.
Содержание 65Zn(Zn), связанного с различными органо-минеральными фракциями, определяли методом Тессье в модификации Ферстнера [21, 22, 35, 51, 54, 60]. Полагаем, что в данном случае целесообразно, используя теоретические разработки, изложенные в работах [12, 45], объединить отдельные выделенные химические фракции цинка в почве в виде функциональной классификации: совокупность фракций I и II – подвижные формы нахождения (неспецифически сорбированные ионы и карбонаты), III–IV – условно подвижные формы нахождения (специфически сорбированные ионы гидрооксидами Fe, Mn), V – консервативные (фиксированные) формы нахождения (специфически сорбированные ионы, связанные с окисляемым органическим веществом), VI–VII – прочнофиксированные формы нахождения (связанные с кристаллической матрицей первичных и вторичных почвенных минералов).
Значения ключевого параметра, условно названного “удельной активностью Am65Zn/Zn” в лизиметрических водах, в отдельных химических фракциях (формах нахождения) цинка в почве, а также в частях растений были определены как отношения объемной (удельной) активности к концентрации стабильного Zn, содержащегося в соответствующих объектах исследования, Бк/мг. На основании данных об удельной активности 65Zn/Zn рассчитаны значения показателя, названного коэффициентом обогащения (KO) радиоактивной меткой 65Zn природного (стабильного) Zn, содержащегося в почве и растениях по отношению к главному компоненту модельной системы – лизиметрическому раствору, например: KOфр№(65Zn/Zn) = = Am(65Zn/Zn)фр№/Am(65Zn/Zn)раствор. Этот показатель принципиально отличается от известного в радиоэкологии показателя, называемого “наблюдаемым отношением”, или “коэффициентом дискриминации”. Последний представляет собой отношение удельной активности техногенного радионуклида к концентрации его природного неизотопного носителя (например, 90Sr/Ca) в данном и предшествующем звене миграционной цепочки.
Из-за сложного характера экспериментально установленной зависимости [Zn]раст = f(t) для вегетативной массы ячменя трудно подобрать идеальное уравнение для аппроксимации. В большинстве случаев зависимость изменения концентраций микроэлементов (включая цинк) в растениях (мг/кг сухой массы) от времени имеет вид одновершинной кривой с выраженной положительной асимметрией (крутая левая ветвь и полого ниспадающая правая). Подобная зависимость может быть удовлетворительно описана, например, с помощью уравнения Вуда (1), используемого в сельскохозяйственной практике [23].
(1)
${{\left[ {{\text{Zn}}} \right]}_{{{\text{раст}}}}}~ = a~{{t}^{b}}{\text{\;exp}}\left( { - c~t} \right),$Применительно к объекту исследования – ячменю – данное уравнение можно интерпретировать в рамках оценки динамики содержания цинка в растениях, как отражающее факт одновременного протекания конкурирующих процессов накопления (степенной сомножитель) и потери цинка растениями (экспоненциальный сомножитель).
Значения параметров a, b и c уравнения (1) подбирали с использованием компьютерной среды Sigma Plot 11. Точность аппроксимирующего уравнения (1), используемого для описания зависимости [Zn]раст(t) оценивалась с помощью t-критерия и коэффициентов детерминации R2. Статистический анализ экспериментальных данных проводили стандартными методами с использованием MS-Excel, на основании теоретических аспектов, изложенных в работах [4, 32, 50].
РЕЗУЛЬТАТЫ
Установлено, что уменьшение концентрации стабильного Zn и объемной активности 65Zn в лизиметрическом растворе со временем удовлетворительно описываются степенной функцией с отрицательным показателем вида [Zn]раствор = atb, где a и b – параметры, t – время, сут (рис. 2а, 2b).
Рис. 2.
Экспериментальные данные (среднее значение ± стандартное отклонение) для почвенного раствора в динамике: [Zn]стаб (а); объемная активность 65Zn (b); коэффициенты распределения (Kd) между твердой и жидкой фазами Zn (c), 65Zn (d); Am(65Zn/Zn)почв-раствор (e), Am(65Zn/Zn)ВЧ (f), Am(65Zn/Zn)корни (j).
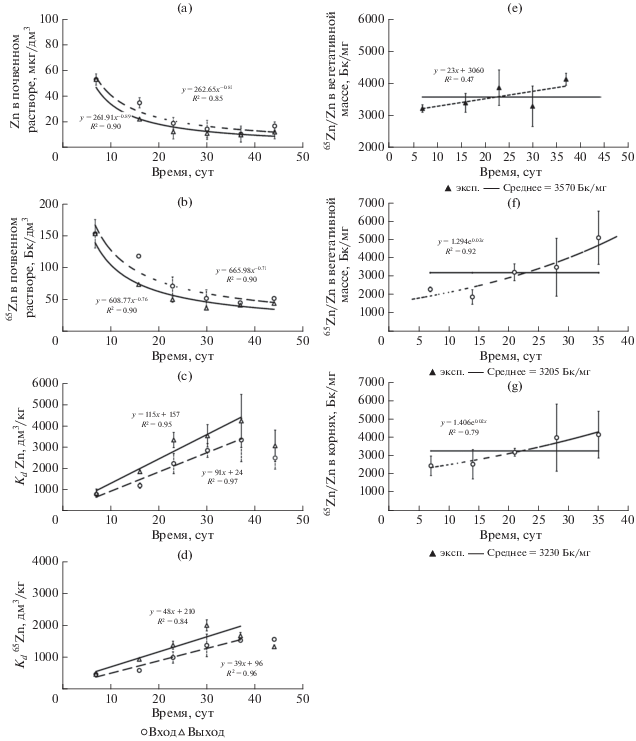
Значения параметров a и b и величины коэффициентов детерминации (R2) для Zn(65Zn) и в растворе на выходе из лизиметра перед вегетационными сосудами составили: 263, –0.81(0.85) и 666, –0.71(0.90); после выхода из вегетационных сосудов и грубой фильтрации: 262, –0.89(0.90) и 609, –0.76(0.90).
В течение вегетационного опыта в период до 35 сут происходит увеличение коэффициентов распределения как стабильного (природного), так и радиоактивного изотопов (рис. 2c, 2d). Динамика водно-миграционных показателей KdZn и Kd65Zn, удовлетворительно описывается линейными уравнениями типа Kd = at + b, где a (дм3/(кг сутb)) и b (дм3/кг) – параметры, t – время, сут. Так, знания коэффициентов распределения KdZn на входе в вегетационные сосуды в период с 1-х до 35-х суток увеличились с 780 ± 50 до 3340 ± 1020 дм3/кг. Для значений KdZn в растворе на входе в лизиметр (выходе из вегетационных сосудов) за соответствующий период времени изменения составили с 840 ± 200 до 4230 ± 1240 дм3/кг. Аналогично, значения коэффициентов распределения Kd65Zn на входе в вегетационные сосуды в период с 1-х до 35‑х суток увеличились с 460 ± 70 до 1530 ± 50 дм3/кг, а на выходе из вегетационных сосудов − с 460 ± 70 до 1670 ± 100 дм3/кг.
Важными показателями для оценки вклада конкретной формы нахождения цинка в миграционную цепочку почва–раствор–растение являются значения удельной активности 65Zn/Zn в исследуемых объектах. На рис. 2e–2j приведены данные по динамике удельной активности 65Zn/Zn в лизиметрическом растворе, вегетативных частях и корнях ячменя в пересчете на стабильный Zn, содержащийся в этом растворе, Бк/мг: Am(65Zn/Zn)раствор, Am(65Zn/Zn)ВЧ, Am(65Zn/Zn)корни. Средние за вегетационный период значения соответствующих показателей составили соответственно 3580 ± 390, 3210 ± 1250 и 3230 ± 780 Бк/мг.
В процессе вегетационного опыта наблюдалось существенное уменьшение в лизиметрическом растворе концентрации ионов $[{\text{NH}}_{4}^{ + }]$, [K+] и $[{\text{NO}}_{3}^{ - }]$ (мг/кг), в то время как средние (на входе и выходе из вегетационных сосудов) значения рН возрастали с 5 до 7 (рис. 3). В результате подщелачивания лизиметрического раствора его экстрагирующая способность по отношению к “свежевнесенному” 65Zn постепенно уменьшалась, но не так сильно, как по отношению к менее подвижному нативному цинку. Это привело к выраженным тенденциям увеличения значений Am(65Zn/Zn)раствор, Am(65Zn/Zn)ВЧ, Am(65Zn/Zn)корни в течение вегетационного периода (рис. 2e–2f).
Рис. 3
Динамика концентраций в почвенном растворе (среднее значение ± стандартное отклонение, n = 3): $[{\text{NH}}_{4}^{ + }]$ (a), [K+] (b) и $[{\text{NO}}_{3}^{ - }]$ (c), мг/кг; pH (d).
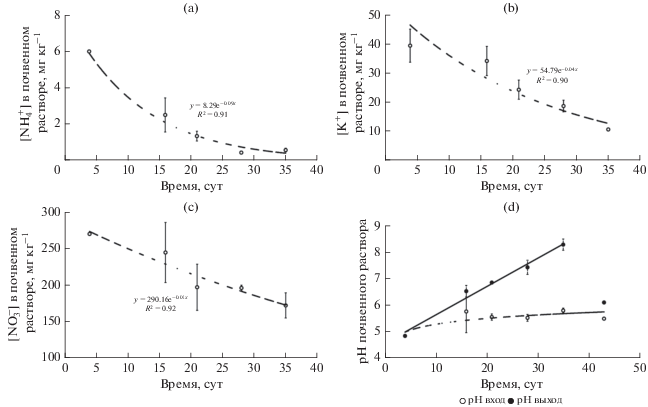
Для оценки подвижности в системе почва–раствор и потенциальной доступности растениям Zn(65Zn) исследовано распределение различных форм нахождения металла в почве. Результаты параллельного фракционирования почвы по схемам Крупского и Александровой в модификации Зырина [2, 12] и Минкиной с соавт. [45] с выделением подвижной и связанной с ОМК форм цинка свидетельствуют об отсутствии состояния равновесия 65Zn/Zn между различными химическими фракциями. Так, относительное содержание (по сравнению с валовым количеством) подвижной формы нативного Zn и 65Zn в исследуемой дерново-подзолистой почве составило 5.9 ± 0.4 и 30.3 ± 2.1% соответственно. В то же время содержание суммы подвижной и связанной с ОМК форм Zn и 65Zn было равно 11.0 ± 1.4 и 37.0 ± 1.2% соответственно. То есть в первом случае относительное содержание стабильного Zn было в 5.1 раза меньше, чем относительное содержание радионуклида 65Zn, а во втором – в 3.4 раза. Очевидно, что в условиях гипергенеза процесс уравновешивания в результате изотопного обмена между различными формами ТМ может занять очень длительное время, сопоставимое с геологическим веком.
Для того, чтобы более подробно изучить вклад различных форм нахождения Zn в состав жидкой фазы почв с использованием в качестве радиоактивной метки 65Zn, применили последовательную схему фракционирования отобранных образцов почв по методу Тессье в модификации Ферстнера. Результаты представлены на рис. 4. Сравнительный анализ данных показывает следующее соотношение различных форм нахождения стабильного Zn и радионуклида 65Zn (данные приведены в скобках) в почве, %: I – 5.9 ± 3.9 (1.9 ± 1.0); II – 14.3 ± ± 3.4 (2.2 ± 0.5); III – 32.5 ± 1.9 (7.8 ± 0.9); IV – 20.4 ± 2.6 (9.5 ± 0.9); V – 9.8 ± 1.4 (27.5 ± 4.2); VI – 12.2 ± 1.4 (41.1 ± 2.8); VII – 5.0 ± 2.7 (10.0 ± 6.8). Как следует из рис. 4а, 4b, относительное содержание подвижных и условно подвижных форм 65Zn в почве (фракции I–IV) значительно превышает содержание соответствующих форм стабильного (природного) изотопа Zn в 3.1, 6.5, 4.2 и 2.1 раза соответственно. В то же время значения относительного содержания консервативных и прочнофиксированных форм 65Zn в почве (фракции V – (VI + VII)) были значительно меньше, чем для Zn в 2.8 и 3.0 раза соответственно.
Рис. 4.
Относительное содержание (%) форм нахождения стабильного (природного) Zn (a) и 65Zn (b) в дерново-подзолистой почве, определяемых по методу Тессье в модификации Ферстнера; KO радионуклидом 65Zn стабильного Zn соответствующих фракций (форм нахождения) металла (c); кумулятивный KO суммы последовательно извлекаемых химических фракций нативного Zn радионуклидом 65Zn (d). Римскими цифрами I–VII обозначены формы нахождения цинка в почве, приведенные в табл. 3. 1 – формы нахождения Zn (65Zn), 2 – Zn (65Zn) в лизиметрическом растворе.
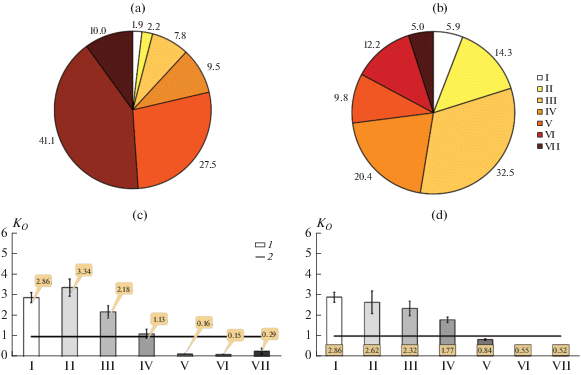
Значения коэффициентов обогащения (KO) соответствующих форм нахождения природного Zn радиоактивной меткой 65Zn по отношению к главному компоненту нашей модельной системы – лизиметрическому раствору на момент, соответствующий началу вегетационного опыта составляли: 2.86 ± 0.24, 3.34 ± 0.41, 2.18 ± 0.30, 1.13 ± 0.22, 0.16 ± 0.01, 0.15 ± 0.01, 0.29 ± 0.15 (рис. 4c). Само значение Am(65Zn/Zn)раствор было равно 3220 ± ± 110 Бк/мг. Секущая по значению ординаты 1.0 представляет собой KO (65Zn/Zn)раствор.
Полученные данные можно представить в виде кривой (рис. 4d), на которой каждое следующее значение KO представляет собой интегральную величину, где отношение суммарной удельной активности 65Zn данной и предыдущих фракций (Бк/кг почвы) к суммарной массовой доле соответствующих фракций стабильного Zn(мг/кг почвы) нормируется на удельную активность 65Zn/Zn в лизиметрическом растворе: KOΣфр(65Zn/Zn) = = Am(65Zn/Zn)Σфр/Am(65Zn/Zn)раствор. Значения KO суммы соответствующих форм нахождения природного Zn радиоактивной меткой 65Zn по отношению к лизиметрическому раствору составили: 2.86 ± 0.24 (фракция I), 2.62 ± 0.54 (Σфракций I–II), 2.32 ± 0.35 (Σфракций I–III), 1.77 ±0.13 (Σфракций I–IV), 0.84 ± 0.04 (Σфракций I–V), 0.55 ± 0.03 (Σфракций I–VI), 0.52 ± 0.02 (Σфракций I–VII). Секущая по значению ординаты 1.00 представляет собой KO (65Zn/Zn)раствор.
Данные по динамике накопления (концентрации) цинка в вегетативных частях ячменя (рис. 5а, 5b), имеют неоднозначный характер применительно к внесенному радионуклиду 65Zn и нативному стабильному Zn. Однако они показывают, что в обоих случаях содержание цинка в растениях, в целом, увеличивается в ходе онтогенеза.
Рис. 5.
Динамика концентрации Zn (а); удельной активности 65Zn (b); коэффициентов концентрирования (KK) (c), дм3/кг в сухой вегетативной массе ячменя (среднее ± стандартное отклонение, n = 3).
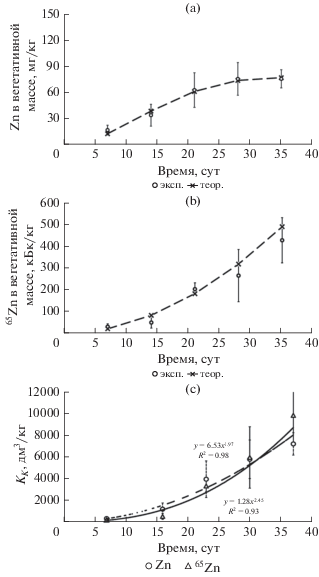
Как отмечалось выше, подобная зависимость может быть описана уравнением Вуда (1), отражающим взаимодействие конкурирующих процессов накопления в фитомассе и перераспределения Zn между разными частями растений, а также выноса элемента с опадом [15, 23]. Однако для сравнительно краткосрочных экспериментов (как в нашем случае 35 сут) ниспадающая часть кривой может быть не выражена. В нашем случае это наблюдалось в отношении Zn для корней (рисунок не приводится) и 65Zn для корней и ВЧ (рис. 5b). Таким образом, для аппроксимации зависимости Am65Znраст = f(t) в ряде случаев использовалась только усеченная часть уравнения Вуда с параметрами a и b. Значения параметров а (кБк/(кг сутb)) и b (сут–1) для ВЧ составили, соответственно, 0.51 ± 0.31 и 1.93 ± 0.18 (R2 = 0.96, n = = 13, ν = 11); для корней: a = 0.64 ± 1.66, b = 1.96 ± ± 0.75 (R2 = 0.56, n = 15, ν = 13).
Для природного Zn, наоборот, этот эффект был выражен (рис. 5а), но по другим причинам, а именно, из-за развития дефицита Zn в почвенном растворе и его подщелачивания (рН с 5.5 до 7.0) по мере прироста биомассы растений в ходе онтогенеза. Значения параметров а (кБк/(кг сутb)), b и c (сут–1), рассчитанные на основании уравнения (1) для ВЧ, составили соответственно а = 0.23 ± 0.39, b = 2.30 ± 0.80 и c = 0.07 ± 0.03 (R2 = 0.74, n = 26, ν = 24); для корней: а = 0.90 ± 0.99, b = 1.48 ± 0.32 (R2 = 0.76, n = 15, ν = 13).
Значения коэффициентов концентрирования (KK) Zn(65Zn) ожидаемо возрастали с увеличением возраста растений (рис. 5c). Это связано как с аккумулятивным эффектом при поглощении цинка растениями, так и с уменьшением содержания его в почвенном растворе в ходе эксперимента. Вследствие высокой вариабельности данных достоверного различия значений KK(Zn) и KK(65Zn) выявить не удалось.
ОБСУЖДЕНИЕ
Для стабильного Zn и радионуклида 65Zn установлено, что их концентрация и удельная активность, соответственно, в лизиметрическом растворе уменьшались со временем (рис. 2а, 2b). При этом содержание радиоизотопа и его стабильного изотопного носителя в растворе на выходе из лизиметра (на входе в вегетационные сосуды) было больше, чем на выходе из вегетационных сосудов, что объясняется поглощением цинка корнями ячменя. Уменьшение концентрации стабильного Zn и объемной активности радионуклида 65Zn в лизиметрическом растворе со временем связано как с истощением запаса водорастворимых форм металлов в почве в результате непрерывного поглощения корнями растений, не компенсируемого десорбцией Zn(65Zn) из почвенного поглощающего комплекса в раствор, так и с подщелачиванием раствора корневыми выделениями. Об этом свидетельствует увеличение значений Kd Zn(65Zn) со временем, по мере роста, развития растений и поглощения ими Zn(65Zn), а также на выходе из вегетационных сосудов.
Зависимости концентраций ионов аммония, калия и нитратов в лизиметрическом растворе от времени могут быть описаны экспоненциальными уравнениями. Следует отметить, что высокая концентрация нитратов приводила к увеличению щелочности квазиравновесного лизиметрического раствора в течение вегетационного периода. Последнее обусловлено способностью растений подщелачивать питательные растворы на свету, выделяя ионы ${\text{HCO}}_{3}^{ - }$ или OH– при наличии достаточного количества нитрат-ионов и малом содержании ионов аммония. В противном случае (избыток в питательном растворе катионов ${\text{NH}}_{4}^{ + }$ при недостатке ${\text{NO}}_{3}^{ - }$), наоборот, происходит подкисление среды в результате выделения корнями H+-ионов. Этот факт зафиксирован многими исследователями [6, 15, 18]. Он обусловлен соблюдением принципа электронейтральности при трансмембранном переносе анионов и катионов в симпласт корня.
Формы ТМ в почве, извлекаемые вытяжкой ААБ-4.8, принято классифицировать как подвижные. Однако это широкое определение, включающее в себя как неспецифически сорбированные ионы ТМ, то есть связанные с почвенным поглощающим комплексом электростатическими силами, так и легкорастворимые формы ТМ, связанные с карбонатами. Исследователи [11, 45, 52] предложили разделять неспецифически сорбированные почвами ТМ на легко обмениваемые, извлекаемые растворами нейтральных солей при pH 7.0, и трудно обмениваемые (извлекаемые, например, ААБ-4.8). Для почв, не содержащих карбонаты, вытяжку ААБ-4.8) можно использовать для оценки общих запасов обменных (неспецифически связанных) форм ТМ. Данные, приведенные в табл. 1, по количеству неспецифически связанных катионов Ca2+, Mg2+ и K+, содержащихся в исследуемой дерново-подзолистой почве и извлекаемых разными реагентами (1 M NH4Cl, ААБ-7.0, ААБ-4.8), полностью подтверждают эту гипотезу в отношении щелочных и щелочноземельных металлов.
Предложенная гипотеза позволяет классифицировать обменные формы ТМ на различные группы: присутствующие во внешнесферных комплексах (трудно обмениваемые ионы) и в диффузном слое (легко обмениваемые ионы) [11, 52].
Однако при этом остается очевидное сомнение в корректности использования растворов (даже концентрированных) нейтральных солей для извлечения обменно сорбированных катионов ТМ, относящихся к переходным металлам. Из-за склонности последних к гидролизу в процессе анализа в условиях нейтральной среды возможно их повторное осаждение в виде гидроксидов, что приводит к существенному уменьшению концентрации ТМ в анализируемых экстрактах. На существование такой проблемы обращали внимание Зырин с соавт. [12], отмечая, в частности, факт осаждения катионов Zn2+ в виде гидроксида цинка Zn(ОН)2 в почвенных растворах при рН больше 6.5. Поэтому полагаем, что при отсутствии свободных карбонатов, использование ААБ-4.8 дает корректные значения количества обменных форм Zn. Подтверждают данный вывод близкое значение (с поправкой на величину pH экстрагирующих растворов) содержание Zn извлекаемого как ААБ-4.8, так и ААБ-7.0 + 1 М CH3COONa (pH 5.0) в последовательной схеме по Тессье–Ферстнера.
Рассчитаны значения коэффициентов обогащения (KO) стабильного природного Zn, присутствующего в подвижной и суммарно в подвижной и связанной с ОМК формах, радиоактивной меткой 65Zn по отношению к главному компоненту нашей модельной системы – лизиметрическому раствору: (KOфр№(65Zn/Zn) = Am(65Zn/Zn)фр/Am(65Zn/Zn)раствор). Они составили 3.32 ± 0.01 (подвижная форма) и 2.21 ± 0.36 (сумма подвижной и связанной с ОМК форм). Таким образом, данные фракции почвенного стабильного Zn обогащены радиоактивным изотопом 65Zn значительно больше, чем фракция водорастворимого Zn, следовательно, они входят в пул соединений Zn в почвах, являющихся донором радиоизотопа для лизиметрического раствора.
Для обоснования этого и следующих утверждений необходимо упомянуть некоторые теоретические аспекты. В случае изотопного обмена 65Zn/Zn имеем дело с “идеальным изотопным обменом”, в котором участвуют изотопные атомы, тождественные по своим физико-химическим свойствам. Применительно к нашему случаю:
Для процессов идеального изотопного обмена характерны отсутствие элементных (химических) изменений, а также неизменность числа взаимодействующих частиц и их концентраций. Такие процессы приводят к возникновению новых изотопных разновидностей реагирующих форм, не отличающихся по свойствам (элементному составу, электронному и пространственному строению, энергии связей, теплоемкости, теплоте образования и др.). Причиной самопроизвольного протекания процессов идеального изотопного обмена является только увеличение энтропии системы, поскольку изменение ее энтальпии в данном случае будет равно нулю (ΔH = 0). С физической точки зрения увеличение энтропии системы при изотопном обмене соответствует переходу системы из более упорядоченного состояния (изотоп 65Zn находится в разных формах) к менее упорядоченному (изотоп равномерно распределен между формами, участвующими в процессе изотопного обмена), что соответствует смешению изотопов. При наступлении состояния равновесия при идеальном изотопном обмене ΔG0 = 0. Соответственно, ΔH0 = 0 и ΔS0 = 0, константа равновесия (Kр) =1 [4]. Для рассмотренного выше уравнения идеального изотопного обмена 65Zn/Zn это отношение будет выглядеть следующим образом:
(2)
${{K}_{р}} = ({{{{{{{[}^{{65}}}{\text{Zn}}]}}_{{{\text{почва}}}}}[{\text{Zn}}]{{)}_{{{\text{раствор}}}}})} \mathord{\left/ {\vphantom {{{{{{{[}^{{65}}}{\text{Zn}}]}}_{{{\text{почва}}}}}[{\text{Zn}}]{{)}_{{{\text{раствор}}}}})} {{{{({{{[{\text{Zn}}]}}_{{{\text{почва}}}}}{{[}^{{65}}}{\text{Zn}}])}}_{{{\text{раствор}}}}}}}} \right. \kern-0em} {{{{({{{[{\text{Zn}}]}}_{{{\text{почва}}}}}{{[}^{{65}}}{\text{Zn}}])}}_{{{\text{раствор}}}}}}} = 1.$Таким образом, состоянию равновесия при идеальном изотопном обмене соответствует равнораспределение изотопов между обменивающимися формами (включая водорастворимую, полностью переходящую в фазу почвенного раствора). Это приводит к идентичности изотопного состава обменивающихся форм:
(3)
$({{{{[}^{{65}}}{\text{Zn}}]} \mathord{\left/ {\vphantom {{{{[}^{{65}}}{\text{Zn}}]} {[{\text{Zn]}}{{)}_{{{\text{почва}}}}}}}} \right. \kern-0em} {[{\text{Zn]}}{{)}_{{{\text{почва}}}}}}} = ({{{{[}^{{65}}}{\text{Zn}}]} \mathord{\left/ {\vphantom {{{{[}^{{65}}}{\text{Zn}}]} {{\text{[Zn]}}{{{\text{)}}}_{{{\text{раствор}}}}}}}} \right. \kern-0em} {{\text{[Zn]}}{{{\text{)}}}_{{{\text{раствор}}}}}}},$в случае
(4)
$({{{{[}^{{65}}}{\text{Zn}}]} \mathord{\left/ {\vphantom {{{{[}^{{65}}}{\text{Zn}}]} {[{\text{Zn}}]{{)}_{{{\text{почва}}}}}}}} \right. \kern-0em} {[{\text{Zn}}]{{)}_{{{\text{почва}}}}}}} \ne {{({{[}^{{65}}}{\text{Zn}}]} \mathord{\left/ {\vphantom {{({{[}^{{65}}}{\text{Zn}}]} {{\text{[Zn]}}{{{\text{)}}}_{{{\text{раствор}}}}}}}} \right. \kern-0em} {{\text{[Zn]}}{{{\text{)}}}_{{{\text{раствор}}}}}}}$можно утверждать, что система еще не достигла состояния изотопного равновесия (но вполне может находиться в стационарном состоянии квазиравновесия).
Величина ([65Zn]/[Zn])почва/([65Zn]/[Zn])раствор = = KOпочва(65Zn/Zn). Вследствие ничтожности значений [65Zn]почва и [65Zn]раствор их принято выражать, соответственно, величинами удельной и объемной активностей радионуклида.
Чем больше значение KOпочва(65Zn/Zn), тем дальше от состояния изотопного равновесия находятся радиоактивный и природный стабильный изотопы цинка, присутствующие исследуемой почве в подвижных, условно подвижных и фиксированных формах с одной стороны, и водорастворимой форме, с другой стороны.
Жидкая фаза почвы–почвенный раствор является не только местом локализации “водорастворимой формы нахождения элементов”, но и важнейшей эффективной фазой почвы [9], на границе которой с твердыми фазами (минеральными и органическими частицами, корнями растений и др.) происходят процессы ионного обмена (трансформационная функция). При этом отдельные ионы могут, как активно сорбироваться из раствора определенными компонентами твердой фазы, так и десорбироваться в раствор другими компонентами. Направления реакций определяются соответствующими величинами химических потенциалов данного иона в почвенном растворе и в различных компонентах твердой фазы. Таким образом, состав почвенного раствора отражает сложившееся на определенный момент времени в неравновесной системе почва–почвенный раствор соотношение ионов во всех взаимодействующих с почвенным раствором компонентах твердой фазы (информационная функция). При этом раствор выступает в качестве связующего звена, благодаря которому опосредованно происходят реакции обмена ионов (например, рассматриваемых в настоящей работе изотопов цинка) между различными формами нахождения, локализованными в твердой фазе почвы (транспортная функция).
В том случае, если Am(65Zn/Zn)фр№ > > Am(65Zn/Zn)раствор, то есть коэффициент обогащения какой-либо формы нахождения Zn в почве радионуклидом 65Zn относительно почвенного раствора >1, то процесс изотопного обмена радионуклида между соответствующей формой нахождения и раствором смещен в сторону последнего. Место ионов 65Zn2+ в почве при этом занимают ионы природного стабильного изотопного носителя Zn2+. В случае, если Am(65Zn/Zn)фр№ < < Am(65Zn/Zn)раствор, происходит обратный процесс. Таким образом, через жидкую фазу, как уже отмечалось, происходит обмен Zn(65Zn) между конкурирующими местами связывания в твердой фазе почв, образующими с ионами цинка соответствующие формы нахождения. Концентрация [Zn] и объемная активность 65Zn в квазиравновесном почвенном (лизиметрическом) растворе отражают вклад различных форм их нахождения в исследуемой почве.
Прочность связывания катионов 65Zn2+ почвой отражают величины коэффициентов распределения между твердой и жидкой фазами. Следует отметить, что величина Kd, обычно получаемая исследователями в экспериментах является, по существу, интегральным показателем, отражающим вклад различных форм нахождения в процесс сорбции–десорбции катионов металлов, поскольку вычленить вклад отдельных форм в величину концентраций (объемной активности) исследуемых катионов невозможно. Результаты динамики значений Kd65Zn и KdZn, приведенные на рис. 2c, 2d, показывают, что спустя год после начала уравновешивания системы почва–раствор подвижность 65Zn остается, в среднем, почти в 2 раза больше, чем подвижность природного Zn. Полученные результаты подтверждает правило, согласно которому подвижность экзогенных соединений ТМ, включая цинк, всегда больше, чем природных [17].
Значения коэффициентов обогащения вышеуказанных подвижных и условно подвижных химических фракций Zn(I, II, III, IV) радиоактивной меткой 65Zn(KOфр№(65Zn/Zn)) = Am(65Zn/Zn)фр№/ Am(65Zn/Zn)раствор) были >1 (от 1.13 до 3.34), неподвижных (фиксированных) фракций (V, VI и VII) – <1 (0.16, 0.15 и 0.29 соответственно) (рис. 4c). Это позволяет предположить, что в системе почва–раствор из химических фракций I–IV ионы 65Zn2+ будут преимущественно десорбироваться в лизиметрический раствор, а во фракции V и VI + VII, наоборот, сорбироваться из него, что, постепенно будет приводить к уменьшению Am(65Zn/Zn) для первой группы фракций и увеличению для второй.
На диаграмме (рис. 4d) приведена кумулятивная зависимость отношения суммарной удельной активности 65Zn данной и предыдущих фракций (Бк/кг почвы) к суммарной массовой доле соответствующих фракций стабильного Zn (мг/кг почвы), нормированного на удельную активность (65Zn/Zn) в лизиметрическом растворе: KOΣфр(65Zn/Zn) = = Am(65Zn/Zn)Σфр/Am(65Zn/Zn)раствор. Очевидно, что значения данного кумулятивного показателя постепенно уменьшаются с последовательным увеличением количества фракций и для Σ(I–IV) KOΣфрI–IV = 1.77, а для Σ(I–V), KOΣфрI–V = 0.84 < 1.
Исходя из полученных результатов и предположения о возрастающей способности экстрагентов, используемых в методе последовательной экстракции, извлекать катионы цинка [46], можно рассчитать запас подвижного цинка в единице массы почвы – значение E-value: (EZn) = ΣС(Zn)фрI–IV = 8.80 ± 0.59 мг/кг (или 21.4 ± 1.4%). Соответствующее значение удельной активности 65Zn/Zn(Am(65Zn/Zn)ΣфрI–IV) равно 5700 ± 400 Бк/мг.
Обращает на себя внимание, что среднее за период вегетационного опыта значение Am(65Zn/Zn)раствор = = 3580 ± 390 Бк/мг < Am(65Zn/Zn)ΣфрI–IV. Значения последних величин различаются в 1.6 раза (в начале вегетационного эксперимента соотношение Am(65Zn/Zn) ΣфрI–IV/Am(65Zn/Zn)раствор было равно 1.8). Это позволяет сделать предположение о существовании медленного процесса изотопного обмена между подвижными и условно подвижными формами цинка с одной стороны, и неподвижными (фиксированными) с другой, посредством жидкой фазы исследуемой почвы – лизиметрического (почвенного) раствора. Факторами, позволившими зафиксировать данное явление, оказались повышенная влажность почвы, длительность периода инкубации влагонасыщенной почвы с внесенным 65Zn и, по-видимому, развитие естественных процессов, приводящих к повышению актуальной кислотности почвы. В дальнейшем, в ходе вегетационного опыта в результате жизнедеятельности растений, лизиметрический раствор обеднялся цинком и подщелачивался, что приводило к росту величины Am(65Zn/Zn)раствор до значений, близких к Am(65Zn/Zn)ΣфрI–IV (рис. 2e), фактически отражающей соотношение 65Zn/Zn в подвижных и условно подвижных формах в почве и их вклад в состав лизиметрического почвенного раствора.
Запас доступного растениям цинка (LZn), который, как отмечено выше, теоретически различается с EZn на величину корневого захвата металла растениями, в рамках данного вегетационного опыта оценить не представлялось возможным (из-за отсутствия непосредственного контакта корней растений с почвой).
Для балансовых расчетов и оценки вклада в процесс изотопного обмена цинка между различными формами в почве особый интерес представляют данные о суммарном выносе (ΣW) в ходе пяти отборов из системы почва–почвенный раствор как природного, так и радиоактивного изотопов цинка вегетативными частями и корнями ячменя. Результаты оказались следующими:
Таким образом, вынос природного Zn и радионуклида 65Zn в ходе вегетационного опыта из почвы тест-растениями был незначителен. В процентном отношении от общего количества Zn(65Zn), содержащегося в почве, он составил 0.34(0.69)%. Следовательно, оказать заметное влияние на соотношение форм нахождения цинка в почве вынос металла растениями не способен (разве только в отношении водорастворимых фракций Zn(65Zn), присутствующих в системе в незначительных количествах).
ЗАКЛЮЧЕНИЕ
В ходе вегетационного эксперимента с применением радиоактивного индикатора 65Zn, внесенного в исследуемую дерново-подзолистую супесчаную почву, изучены различные аспекты процесса миграции цинка в системе почва–лизиметрический раствор–растение. Для этого использовали специальный вегетационный стенд, включавший оригинальную лизиметрическую установку циклического действия, с помощью которой была реализована идея постоянной рекуперации питательного раствора, по химическому составу максимально приближающегося к почвенному. Это позволило получить ряд важных показателей, характеризующих подвижность и биологическую доступность цинка в квазиравновесных условиях в динамике. Установлено, что обогащение подвижных и условно подвижных форм природного Zn радиоактивным 65Zn в 1.13–3.34 раза превышало аналогичную величину для почвенного раствора на момент, соответствующий началу вегетационного опыта. В то же время обогащение консервативных и прочнофиксированных форм Zn в почве радионуклидом 65Zn по сравнению с лизиметрическим раствором было в 0.15–0.29 раза меньше. Анализ соотношений Am(65Zn/Zn)фр№/Am(65Zn/Zn)раствор позволил рассчитать величину запаса подвижных EZn соединений нативного цинка в единице массы исследуемой почвы: EZn ≅ ΣС(Zn)почва,фрI–IV = 8.80 ± 0.59 мг/кг (или 21.4 ± 1.4%).
К началу вегетационного опыта зафиксирован факт меньшего (в 1.8 раза) обогащения радионуклидом 65Zn нативного цинка, содержащегося в квазиравновесном почвенном растворе (после уравновешивания его с почвой в течение 1 года) по сравнению с цинком, содержащемся в сумме подвижных и условно подвижных фракций I–IV. В дальнейшем, в ходе вегетационного опыта в результате жизнедеятельности растений, почвенный (лизиметрический) раствор обеднялся цинком и подщелачивался, что приводило к увеличению величины Am(65Zn/Zn)раствор до значений, близких к Am(65Zn/Zn)ΣфрI–IV – величины, фактически отражающей соотношение 65Zn/Zn в подвижных и условно подвижных формах в почве и их превалирующий вклад в составе лизиметрического раствора в соответствующих условиях. Это свидетельствует о существовании медленного процесса изотопного обмена между подвижными и условно подвижными формами цинка с одной стороны, и неподвижными (фиксированными) с другой при непосредственном участии жидкой фазы исследуемой почвы – почвенного раствора.
Оценены в динамике переход в фазу почвенного раствора, накопление и вынос тест-растениями Zn(65Zn) и получены параметры соответствующих модельных аппроксимирующих уравнений. По результатам эксперимента рассчитаны суммарные выносы растениями (корнями и вегетативными частями) природного Zn и радионуклида 65Zn. В процентном отношении от общего количества Zn(65Zn) в почве они составили 0.34(0.69)%. Эти данные говорят о том, что вынос цинка растениями из почвы очень незначителен и не способен оказать заметное влияние на соотношение форм нахождения металла в почве.
Список литературы
Агрохимические методы исследования почв. М.: Наука, 1975. 656 с.
Анисимов В.С., Анисимова Л.Н., Фригидова Л.М., Дикарев Д.В., Фригидов Р.А., Kорнеев Ю.Н., Санжаров А.И., Арышева С.П. Оценка миграционной способности Zn в системе почва–растение // Почвоведение. 2018. № 4. С. 427–438.
Аринушкина Е.В. Руководство по химическому анализу почв. М.: Изд-во Моск. ун-та, 1970. 488 с.
Доспехов Б.А. Методика полевого опыта (с основами статистической обработки результатов исследований). М.: Агропромиздат, 1985. 351 с.
Методические указания по определению тяжелых металлов в почвах сельхозугодий и продукции растениеводства. М.: ЦИНАО, 1992. 61 с.
Най П.Х., Тинкер П.Б. Движение растворов в системе почва–растение. М.: Колос, 1980. 368 с.
Нефедов В.Д., Текстер Е.Н., Торопова М.А. Радиохимия. М.: Высшая школа, 1987. 271 с.
Обухов А.И., Плеханова И.О. Атомно-абсорбционный анализ в почвенно-биологических исследованиях. М.: Изд-во Моск. ун-та, 1991. 184 с.
Пинский Д.Л. Ионообменные процессы в почвах. Пущино, 1997. 166 с.
Практикум по агрохимии / Под ред. В.Г. Минеева. М.: Изд-во Моск. ун-та, 2001. 689 с.
Соколова Т.А., Трофимов С.Я. Сорбционные свойства почв. Адсорбция. Катионный обмен: учебное пособие по некоторым главам химии почв. Тула: Гриф и К, 2009. 172 с.
Химия тяжелых металлов, мышьяка и молибдена в почвах / Под ред. Н.Г. Зырина и Л.К. Садовниковой. М.: Изд-во Моск. ун-та, 1985. 208 с.
Adriano D.C. Trace elements in terrestrial environments. N.Y.: Springer-Verlag, 2001. 868 p.
Alloway B.J. Soil factors associated with zinc deficiency in crops and humans // Environ. Geochem. Health. 2009. V. 31. P. 537–548. https://doi.org/10.1007/s10653-009-9255-4
Barber S.A. Soil nutrient bioavailability: a mechanistic approach. N.Y.: John Wiley & Sons, 1995. 384 p.
Bauer T., Pinskii D., Minkina T., Mandzhieva S., Burachevskaya M., KalinitchenkoV., Barakhov A. Stabilization dynamics of easily and poorly soluble Zn compounds in the soil // Geochem.: Exploration, Environment, Analysis. 2019. V. 19. № 2. P. 184–192. https://doi.org/10.1144/geochem2017-086
Bauer T., Pinskii D., Minkina T., Nevidomskaya D., Mandzhieva S., Burachevskaya M., Chaplygin V., Popileshko Y. Time effect on the stabilization of technogenic copper compounds in solid phases of Haplic Chernozem // Sci. Total Environ. 2018. V. 626. P. 1100–1107. https://doi.org/10.1016/j.scitotenv.2018.01.134
Blossfeld S., Perriguey J., Sterckeman T. et al. Rhizosphere pH dynamics in trace-metal-contaminated soils, monitored with planar pH optodes // Plant Soil. 2010. V. 330. P. 173–184. https://doi.org/10.1007/s11104-009-0190-z
Echevarria G., Morel J.-L., Fardeau J.C., Leclerc E. Assessment of phytoavailability of nickel in soils // J. Environ. Quality. 1998. V. 27. P. 1064–1070. https://doi.org/10.2134/jeq1998.00472425002700050011x
Emmanuel S., Erel Y. Implications from concentrations and isotopic data for Pb partitioning processes in soils // Geochim. Cosmochim. Acta. 2002. V. 66. P. 2517– 2527.
Fernandez Albores A., Perez Cid B., Fernandez Gomez E., Falque Lopez E. Comparison between sequential extraction procedures and single extractions for metal partitioning in sewage sludge samples // Analyst. 2000. V. 125. P. 1353–1357. https://doi.org/10.1039/b001983f
Förstner U. Metal speciation-general concepts and applications // Int. J. Environ. Anal. Chem. 1993. V. 51. P. 5–23. https://doi.org/10.1080/03067319308027608
France J., Thornley J.H.M. Mathematical models in agriculture a quantitative approach to problems in agriculture and related sciences. London: Butterworths, 1985. 335 p.
Frossard Emmanuel, Sinaj Sokrat. The isotope exchange kinetic technique: A method to describe the availability of inorganic nutrients. Applications to K, P, S and Zn // Isotopes in Environmental and Health Studies. 1998. V. 34. P. 61–77. https://doi.org/10.1080/10256019808036360
Garforth J.M., Bailey E.H., Tye A.M., Young S.D., Lofts S. Using isotopic dilution to assess chemical extraction of labile Ni, Cu, Zn, Cd and Pb in soils // Chemosphere. 2016. V. 155. P. 534–541.
Gray C.W., McLaren R.G., Günther D., Sinaj S. An assessment of cadmium availability in cadmium-contaminated soils using isotope exchange kinetics // Soil Sci. Soc. Am. J. 2004. V. 68. P. 1210–1217.
Grusak M.A., Della Penna D. Improving the nutrient composition of plants to enhance human nutrition and health // Annu. Rev. Plant Biol. 1999. V. 50. P. 133–161. https://doi.org/10.1146/annurev.arplant.50.1.133
Hacisalihoglu G., Kochian L. How do some plants tolerate low levels of soil zinc? Mechanisms of zinc efficiency in crop plants // New Phytologist. 2003. V. 159. P. 341–350. https://doi.org/10.1046/j.1469-8137.2003.00826.x
Hacisalihoglu G. Zinc (Zn): The last nutrient in the alphabet and shedding light on Zn efficiency for the future of crop production under suboptimal Zn // Plants. 2020. V. 9. P. 1471. https://doi.org/10.3390/plants9111471
He Q., Ren Y., Mohamed I., Ali M., Hassan W., Zeng F. Assessment of trace and heavy metal distribution by four sequential extraction procedures in a contaminated soil // Soil Water. Res. 2013. № 8. P. 71–76.
Huang Z.-Y., Chen T., Yu J., Zeng X.-C., Huang Y.-F. Labile Cd and Pb in vegetable-growing soils estimated with isotope dilution and chemical extractants // Geoderma. 2011. V. 160. P. 400–407.
James G., Witten D., Hastie T., Tibshirani R. An introduction to statistical learning with applications in R. N.Y.: Springer, 2013. 426 p. https://doi.org/10.1007/978-1-4614-7138-7
Jones D.L., Darrah P.R. Role of root derived organic acids in the mobilization of nutrients from the rhizosphere // Plant and Soil. 1994. V. 166. P. 247–257.
Kabata-Pendias A. Trace elements in soils and plants. London: CRC Press, 2011. 505 p.
Kersten M., Förstner U. Chemical fractionation of heavy metals in anoxic estuarine and coastal sediments // Water Sci Technol. 1986. V. 18. P. 121–130.
Khadhar S., Sdiri A., Chekirben A., Aouzi R., Charef A. Integration of sequential extraction, chemical analysis and statistical tools for the availability risk assessment of heavy metals in sludge amended soils // Environ. Poll. 2020. V. 263 P. 114543. https://doi.org/10.1016/j.envpol.2020.114543
Kochian L.V. Zinc absorption from hydroponic solutions by plant roots // Zinc in soils and plants. Berlin: Kluwer Academic Publishers, 1993. P. 45–57.
Ladonin D.V. Fractional-isotopic composition of lead compounds in soils of the Kologrivskii forest reserve // Eurasian Soil Sci. 2018. V. 51. № 8. P. 929–937. https://doi.org/10.1134/S1064229318080069
Ladonin D.V. Heavy metal compounds in soils: Problems and methods of study // Eurasian Soil Sci. 2002. V. 35. № 6. P. 605–613.
Liu Y., Gao T., Xia Y., Wang Z., Liu C., Li S., Wu Q., Qi M., Lv Y. Using Zn isotopes to trace Zn sources and migration pathways in paddy soils around mining area // Environ. Poll. 2020. V. 267. P. 115616. https://doi.org/10.1016/j.envpol.2020.115616
Marschner H., Römheld V., Kissel M. Different strategies in higher-plants in mobilization and uptake of iron // J. Plant Nutr. 1986. № 9. P. 695–713.
Mench M., Martin E. Mobilization of cadmium and other metals from two soils by root exudates of Zea mays L., Nicotiana tabacum L. and Nicotiana rustica L. // Plant and Soil. 1991. V. 132. P. 187–196.
Minkina T., Nevidomskaya D., Bauer T., Linnik V., Shuvaeva V., Mandzhieva S., Soldatov A., Zubavichus Y., Trigub A. Quantitative speciation of Zn in technosols using chemical fractionation and X-ray absorption spectroscopy // Geochem.: Exploration, Environment, Analysis. 2019. № 19. V. 2. P. 101–109. https://doi.org/10.1144/geochem2017-106
Minkina T.M., Nevidomskaya D.G., Shuvaeva V.A., Soldatov A.V., Tsitsuashvili V.S., Zubavichus Y.V., Rajrut V.D., Burachevskaz M.V. Studying the transformation of Cu2+ ions in soils and mineral phases by the XRD, XANES, and sequential fractionation methods // J. Geochem. Explor. 2016. V. 184. P. 365–371. https://doi.org//10.1016/j.gexplo.2016.10.007
Minkina T.M., Mandzhieva S.S., Burachevskaya M.V., Bauer T.V., Sushkova S.N. Method of determining loosely bound compounds of heavy metals in the soil // Methods X. 2018. P. 5217–226. https://doi.org/10.1016/j.mex.2018.02.007
Morabito R. Extraction techniques in speciation analysis of environmental samples Fresenius // J. Anal Chem. 1995. V. 351. P. 378–385.
Nazif W., Marzouk E.R., Perveen S., Crout N.M.J., Young S.D. Zinc solubility and fractionation in cultivated calcareous soils irrigated with wastewater // Sci. Total Environ. 2015. P. 518–519. https://doi.org/10.1016/j.scitotenv.2015.03.016
Nevidomskaya D.G., Minkina T.M., Soldatov A.V. et al. Speciation of Zn and Cu in technosol and evaluation of a sequential extraction procedure using XAS, XRD and SEM–EDX analyses // Environ. Geochem. Health. 2021. V. 43. P. 2301–2315. https://doi.org/10.1007/s10653-020-00693-1
Pandey R. Mineral Nutrition of Plants // Plant Biology and Biotechnology: V. I: Plant Diversity, Organization, Function and Improvement. Springer, 2015. P. 499–538.
Prichard E., Barwick V. Quality assurance in analytical chemistry. England: John Wiley Sons Ltd., 2007. 293 p. https://doi.org/10.1002/9780470517772
Quevauviller Ph. (ed.) Methodologies in soil and sediment fractionation studies. Single and sequential extraction procedures. Cambridge: Royal Society of Chemistry, 2002. 180 p.
Sposito G. The Chemistry of Soils. N.Y.: Oxford University Press Inc., 2008. 329 p.
Suzuki M., Takahashi M., Tsukamoto T., Watanabe S., Matsuhashi S., Yazaki J., Kishimoto N., Kikuchi S., Nakanishi H., Mori S., Nishizawa N.K. Biosynthesis and secretion of mugineic acid family phytosiderophores in zinc-deficient barley // Plant J. 2006. V. 48. P. 85–97. https://doi.org/10.1111/j.1365-313X.2006
Tessier A., Campbell P.G.C., Bisson M. Sequential extraction procedure for the speciiation of particulate trace metals // Analyt. Chem. 1979. № 51. P. 844–851.
Tongtavee N., Shiowatana J., Ronald J. McLaren G., Colin W. Gray assessment of lead availability in contaminated soil using isotope dilution techniques // Sci. Total Environ. 2005. V. 348. P. 244–256. https://doi.org/10.1016/j.scitotenv.2004.12.066
Voegelin A., Tokpa G., Jacquat O., Barmettler K., Kretzschmar R. Zinc fractionation in contaminated soils by sequential and single extractions: Influence of soil properties and zinc content // J. Environ. Qual. 2008. V. 37. P. 1190–1200. https://doi.org/10.2134/jeq2007.0326
Wali A., Colinet G., Ksibi M. Speciation of heavy metals by modified BCR sequential extraction in soils contaminated by phosphogypsum in Sfax, Tunisia // Environ. Research, Engineering and Management. 2014. V. 70. № 4. P. 14–26. https://doi.org/10.5755/j01.erem.70.4.7807
Walter M., Oburger E., SchindleggerY., Hann S., Puschenreiter M., Kraemer S.M., Schenkeveld W.D.C. Retention of phytosiderophores by the soil solid phase – adsorption and desorption // Plant Soil. 2016. V. 404. P. 85–97. https://doi.org/10.1007/s11104-016-2800-x
Wong C.S.C., Li W.X.D. Pb contamination and isotopic composition of urban soils in Hong Kong // Sci. Total Environ. 2004. V. 319. P. 185–195.
Young S.D., Zhang H., Tye A.M., Maxted A., Thums C., Thornton I. Characterizing the availability of metals in contaminated soils // I. The solid phase: sequential extraction and isotopic dilution, Soil Use and Management. 2006. V. 21. P. 450–458. https://doi.org/10.1079/SUM2005348
Дополнительные материалы
- скачать ESM.docx
- Рис. S1. Стенд для изучения параметров миграции 65Zn(Zn) в системе почва – лизиметрический раствор – растение.


