Поверхность. Рентгеновские, синхротронные и нейтронные исследования, 2020, № 1, стр. 74-80
Влияние изокатионных аналогов CdBVI на свойства твердых растворов систем ZnS–CdBVI
И. А. Кировская a, *, Е. В. Миронова a, А. А. Григан a, А. О. Мурашова a
a Омский государственный технический университет
644050 Омск, Россия
* E-mail: kirovskaya@omgtu.ru
Поступила в редакцию 21.01.2019
После доработки 20.02.2019
Принята к публикации 20.02.2019
Аннотация
С использованием разработанной методики получены твердые растворы на основе систем ZnS–CdBVI (B = S, Se, Te), аттестованные как твердые растворы замещения со структурами сфалерита и вюрцита. Комплексно изучены объемные (кристаллохимические, структурные, электрофизические) и поверхностные (химический состав поверхности, кислотно-основные) свойства, определены природа, сила, концентрация активных (кислотных) центров, что обогатило сведения об алмазоподобных полупроводниках. Установлены закономерности изменения объемных и поверхностных свойств в зависимости от составов систем, расширяющие и облегчающие возможности поиска новых материалов для современной, в частности, сенсорной техники. Высказаны прогнозы относительно поиска новых материалов на основе изученных систем, даны практические рекомендации для изготовления датчиков.
ВВЕДЕНИЕ
Настоящая работа посвящена получению и исследованию объемных и поверхностных свойств многокомпонентных алмазоподобных полупроводников – твердых растворов систем ZnS–CdS, ZnS–CdSe, ZnS–CdTe. Исходя из уникальных свойств исходных бинарных соединений (электрофизических, оптических, оптоэлектрических), такие объекты должны быть перспективными материалами современной техники, в том числе нано-, сенсорной техники [1].
Для реализации таких возможностей необходимы, наряду с разработкой методик получения, знания объемных и особенно поверхностных свойств, установление закономерностей изменения свойств в зависимости от состава твердых растворов и характеристик бинарных компонентов. Это, несомненно, обеспечит прогнозируемый и потому менее затратный путь поиска новых материалов, а также расширит возможности их практического использования.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Исследуемые объекты представляли собой порошки (Sуд = 0.405–0.91 м2/г) ZnS, CdS, CdSe, CdTe и твердых растворов (ZnS)х(CdS)1 – х [2] (х = = 80, 38, 22, 6 мол. %); (ZnS)х(CdSe)1 – х (23, 39 мол. %); (ZnS)х(CdTe)1 – х (х = 2, 3, 96, 97 мол. %). Твердые растворы получали по разработанным методикам, базирующимся на изотермической диффузии исходных бинарных соединений в областях их взаимной растворимости, с использованием специальной программы температурного нагрева [3]. О завершении синтеза судили по результатам рентгенографических исследований, используемых затем для аттестации и определения структуры твердых растворов. Косвенно образование твердых растворов подтверждали данными УФ-, ИК-спектроскопических и электронно-микроскопических исследований.
Рентгенографические исследования проводили на дифрактометре Advance D8 фирмы BRUKER AXS (CuKα-излучение, λ = 0.154056 нм, Т = 293 К) по методике съемок в области дальних углов [4, 5] с использованием позиционно-чувствительного детектора Lynxeye. Для расшифровки полученных рентгенограмм и уточнения параметров решеток использовали базы данных ICDDIPDF-2 и программы ТОРАЗ 3.0 (Bruker) соответственно.
УФ-спектроскопические исследования выполняли на спектрофотометрах UV-2501 PC фирмы Shimadzu с приставкой диффузного отражения ISR-240A и SPECORD-40 в диапазоне 190–900 нм [6], ИК-спектроскопические – на фурье-спектрофотометре Инфра-ЛЮМ ФТ-02 с приставкой МНПВО [1], электронно-микроскопические – в растровом электронном микроскопе (РЭМ) JCM-5700, снабженном приставкой для энергодисперсионного анализа JED-2300 [7].
Поверхностные свойства (кислотно-основные) исследовали методами гидролитической адсорбции (определения водородного показателя изоэлектрического состояния поверхности рНизо), механохимии, неводного кондуктометрического титрования и ИК-спектроскопии многократного нарушенного полного внутреннего отражения [8–10].
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Результаты рентгенографических исследований свидетельствуют об образовании в системах ZnS–CdS, ZnS–CdSe, ZnS–CdTe (при заданных составах) твердых растворов замещения: на дифрактограммах наблюдается сдвиг линий, отвечающих твердым растворам, относительно линий бинарных компонентов при их постоянном числе (рис. 1); концентрационные зависимости параметров а, с кристаллических решеток, межплоскостных расстояний dhkl, а в системе ZnS–CdSe и плотности ρr преимущественно подчиняются закону Вегарда (рис. 2). Имеющие место отклонения от закона Вегарда концентрационных зависимостей ρr в системах ZnS–CdS, ZnS–CdTe допустимы в силу сложных внутренних процессов, сопровождающих образование твердых растворов. Об этом неоднократно было сказано ранее (например, [3]).
Рис. 1.
Дифрактограммы компонентов системы ZnS–CdSe: а – ZnS; б – (ZnS)0.39(CdSe)0.61; в – (ZnS)0.23(CdSe)0.77; г – CdSe.
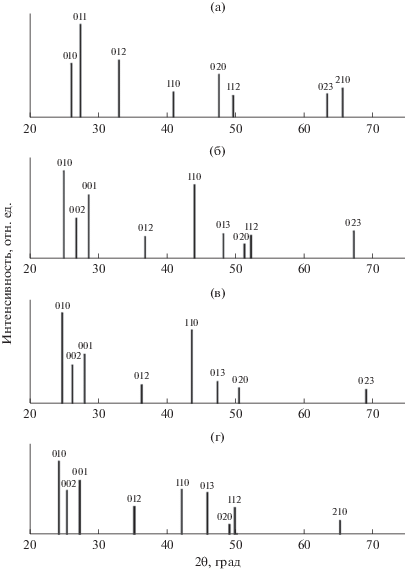
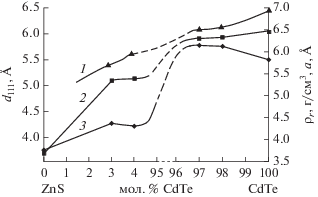
Рис. 2.
Зависимости от состава значений параметра а (1), межплоскостного расстояния d111 (2) и рентгеновской плотности ρr (3) кристаллических решеток компонентов системы ZnS–CdTe.
Дополнительно на образование твердых растворов замещения в изучаемых системах указали результаты УФ-, ИК-спектроскопических и электронно-микроскопических исследований. С увеличением содержания ZnS в системах наблюдается смещение относительного положения основного пика в УФ-спектрах и изменение его интенсивности (рис. 3), смещение ИК-полос, отвечающих валентным колебаниям молекулярно-адсорбированного СО2 и структурных гидроксильных групп (рис. 4), закономерно изменяются также ширина запрещенной зоны (∆Е), рассчитанная по УФ-спектрам ([6], рис. 3, 5), среднее число доминирующих частиц (nср), определенное по РЭМ-изображениям (рис. 6).
Рис. 3.
УФ-спектры отражения компонентов системы ZnS–CdTe: 1 – ZnS; 2 – (ZnS)0.97(CdTe)0.03; 3 – (ZnS)0.96(CdTe)0.04; 4 – (ZnS)0.03(CdTe)0.97; 5 – (ZnS)0.02(CdTe)0.98; 6 – CdTe.
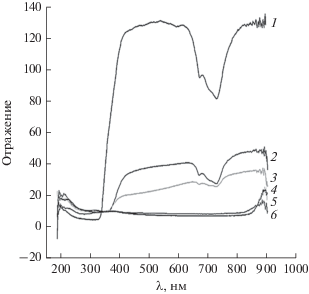
Рис. 4.
ИК-спектры поверхностей компонентов систем: a – ZnS–CdSe (1 – ZnS, 2 – (ZnS)0.39(CdSe)0.61, 3 – CdSe); б – ZnS–CdTe (1 – (ZnS)0.97(CdTe)0.03; 2 – (ZnS)0.96(CdTe)0.04; 3 – (ZnS)0.03(CdTe)0.97; 4 – (ZnS)0.02(CdTe)0.98; 5 – CdTe).
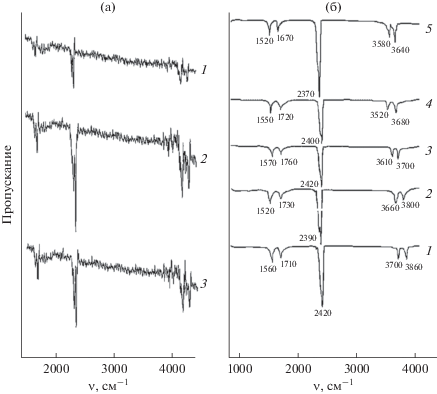
Рис. 5.
Зависимости от состава компонентов систем ZnS–CdS (а), ZnS–CdSe (б), ZnS–CdTe (в) ширины запрещенной зоны ∆Е (1), рентгеновской плотности ρr (2), pH изоэлектрического состояния поверхности (3).
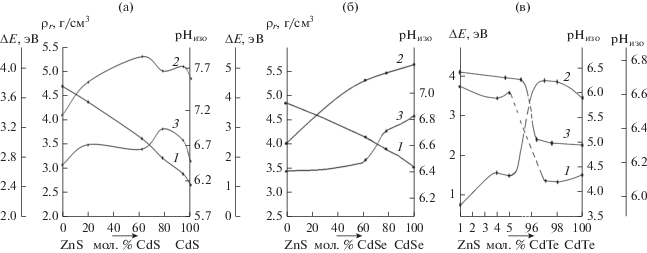
Рис. 6.
РЭМ-изображения в режиме фазового контраста порошков: ZnS (а); (ZnS)0.22(CdS)0.78 (б); CdS (в).

Согласно положению и распределению интенсивностей основных линий на дифрактограммах (рис. 1), компоненты систем ZnS–CdS, ZnS–CdSe имеют преимущественно гексагональную структуру вюрцита, компоненты системы ZnS–CdTe – преимущественно кубическую структуру сфалерита.
Комплексное исследование поверхностных (кислотно-основных) свойств позволило оценить силу, концентрацию, природу активных центров исходных (экспонированных на воздухе) поверхностей. По силе кислотных центров поверхности компонентов систем ZnS–CdS, ZnS–CdSe, ZnS–CdTe следует отнести к слабокислым: значения рНизо изменяются в общем пределе 6.29–6.86. Это позволяет говорить о некотором превалировании кислотных центров Льюиса и об ожидаемой повышенной адсорбционной активности по отношению к основным газам.
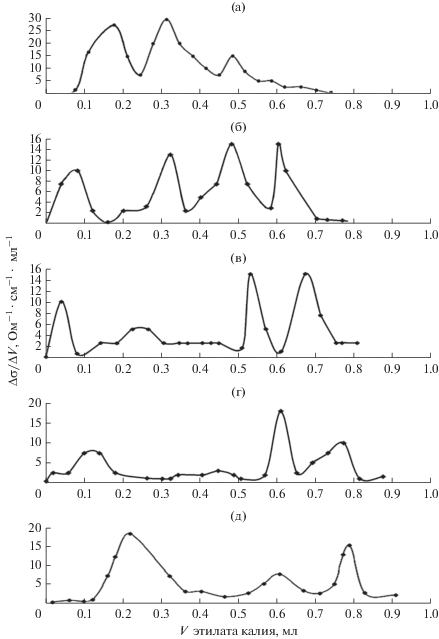
Для выяснения природы кислотных центров целесообразно обратиться к результатам неводного кондуктометрического титрования и механохимических исследований. Наличие на кривых неводного кондуктометрического титрования нескольких пиков (рис. 7) позволяет говорить об ответственности за кислотно-основное состояние поверхностей компонентов систем как центров Льюиса, так и центров Бренстеда, в роли которых выступают, соответственно, координационно-ненасыщенные атомы и адсорбированные молекулы воды, группы ОН–. Подтверждением могут служить такие факты, как наблюдаемое при диспергировании в воде крупнодисперсных порошков компонентов подкисление (уменьшение рНизо) и подщелачивание (увеличение рНизо), наличие в ИК-спектрах водных суспензий компонентов полос ионов S2–, ${\text{SO}}_{4}^{{2 - }},$ ${\text{SeO}}_{4}^{{2 - }},$ ${\text{TeO}}_{4}^{{2 - }},$ имеющих поверхностное происхождение [3, 9], а также наличие в ИК-спектрах исходных поверхностей и тем более в условиях адсорбции полос донорно-акцепторных связей H2O+σ–Me–σ, ${\text{CO}}_{2}^{{ + \sigma }}$–Me–σ, образованных с участием координационно-ненасыщенных атомов (рис. 4) [3, 11].
Рис. 7.
Дифференциальные кривые неводного кондуктометрического титрования компонентов системы ZnS–CdS, хранившихся на воздухе: а – ZnS; б – (ZnS)0.80(CdS)0.20; в – ZnS)0.38(CdS)0.62; г – (ZnS)0.06(CdS)0.94; д – CdS.
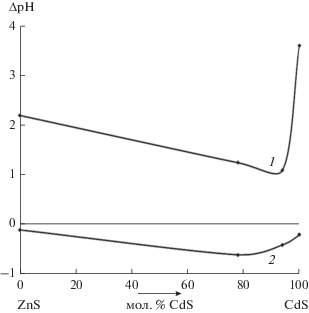
Участие координационно-ненасыщенных атомов как активных (кислотных) центров в образовании донорно-акцепторных связей указанного типа и повышенную активность поверхностей компонентов систем по отношению к основным газам подтверждает, наряду с ИК-спектрами, и характер воздействия основного газа (NH3, в отличие от кислотного СО) на рНизо (наблюдается рост) (рис. 8).
Рис. 8.
Зависимости изменений рН изоэлектрического состояния поверхностей компонентов системы ZnS–CdS под воздействиями NH3 (1) и CО (2) относительно рНизо поверхностей, обработанных в аргоне.
Особого внимания заслуживает влияние второго бинарного компонента CdBVI (B = S, Se, Te) в системах ZnS–CdBVI на особенности образующихся твердых растворов (ZnS)х(CdBVI)1 – х. Здесь логично проследить за “поведением” с изменением составов систем основных объемных (∆Е, ρr) и поверхностных (рНизо) свойств (рис. 5). Наблюдается преимущественно плавное изменение ширины запрещенной зоны ∆Е (уменьшение) во всех системах, плотности ρr (рост), рНизо (рост и уменьшение) в системах ZnS–CdSe, ZnS–CdTe с увеличением содержания второго бинарного компонента CdBVI. В системе ZnS–CdS при плавном изменении ширины запрещенной зоны с увеличением содержания CdS плотность ρr и рНизо изменяются экстремально (рис. 5). Такой факт может быть результатом конкурентного взаимного влияния обоих компонентов (ZnS и CdS) при образовании твердых растворов.
ЗАКЛЮЧЕНИЕ
В системах ZnS–CdS, ZnS–CdSe, ZnS–CdTe получены твердые растворы (ZnS)х(CdS)1 – х (х = = 80, 38, 22, 6 мол. %); (ZnS)х(CdSe)1 – х (23, 39 мол. %); (ZnS)х(CdTe)1 – х (х = 2, 3, 96, 97 мол. %) и изучены их свойства. Они изменяются по-разному в зависимости от содержания х. Критерием плавного или экстремального изменения свойств является ширина запрещенной зоны исходных бинарных соединений, образующих твердые растворы. При большей разнице в ширине запрещенной зоны (в системах ZnS–CdSe, ZnS–CdTe) наблюдается преимущественно плавное изменение свойств. При меньшей разнице в ширине запрещенной зоны бинарных компонентов (в системе ZnS–CdS) усиливается их конкурентное влияние, приводящее к экстремальному характеру изменения свойств.
Ширина запрещенной зоны коррелирует с другими объемными характеристиками, такими как разность электроотрицательностей, энергия атомизации, энтальпия образования, микротвердость, температура плавления и даже подвижность носителей тока, определяющих в конечном итоге прочность кристаллических решеток (табл. 1). Разница в этих характеристиках, как и в значениях ∆Е, сульфида цинка и вторых бинарных компонентов (CdS, CdSe, CdTe) нарастает в последовательности:
Таблица 1.
Физико-химические свойства соединений AIIBVI
| Соединение | Постоянная решетки, нм | Плотность, г/см3 | Температура плавления, °С | Микротвердость, МПа | Энтальпия образования, $\frac{{{\text{кДж}}}}{{{\text{моль}}}}$ | Энергия атомизации, $\frac{{{\text{кДж}}}}{{{\text{моль}}}}$ | Разность электро- отрицательностей (∆х) | Ширина запрещенной зоны (300 К), эВ | Подвижность носителей тока (298 К), $\frac{{{\text{с}}{{{\text{м}}}^{2}}}}{{{\text{В}}\,\,\cdot\,\,{\text{с}}}}$ | |
|---|---|---|---|---|---|---|---|---|---|---|
| электронов | дырок | |||||||||
| ZnS | а = 0.541 | 4.08 | 1830 | 1780 | – | 611 | 0.9 | 3.67 | 140 | 5 |
| CdTe (сфалерит) | а = 0.6474 | 5.86 | 1092 | 600 | –100.4 | 102 | 0.4 | 1.51 | 1800 | 600 |
| CdTe | а = 0.457 | |||||||||
| (вюрцит) | с = 0.747 | |||||||||
| CdSe | а = 0.43 с = 0.701 |
5.81 | 1258 | 900 | –136.9 | 423 | 0.8 | 1.74 | 600 | 50 |
| CdS | а = 0.413 с = 0.671 |
4.82 | 1750 | – | –144.4 | 532 | 0.8 | 2.42 | 350 | – |
Объемные характеристики бинарных полупроводников, как и ширина запрещенной зоны, определяют их взаимодействие при образовании твердых растворов.
Ожидаемая на основе кислотно-основных свойств повышенная адсорбционная активность полученных материалов по отношению к основным газам позволяет рекомендовать их для изготовления соответствующих датчиков.
Список литературы
Кировская И.А. Физико-химические свойства бинарных и многокомпонентных алмазоподобных полупроводников. Новосибирск: СО РАН, 2015. 367 с.
Кировская И.А., Миронова Е.В., Григан А.А., Ушаков О.В. // Физикохимия поверхности и защита материалов. 2018. Т. 54. № 5. С. 492.
Кировская И.А. Твердые растворы бинарных и многокомпонентных полупроводниковых систем. Омск: Изд-во ОмГТУ, 2010. 400 с.
Горелик С.С., Расторгуев Л.Н., Скаков Ю.А. Рентгенографический и электроннооптический анализ. М.: Металлургия, 1970. 107 с.
Смыслов Е.Ф. // Заводская лаборатория. Диагностика материалов. 2006. Т. 72. № 5. С. 33.
Косяченко А.А., Склярчук В.М., Склярчук О.В. // Физика и техника полупроводников. 2011. Т. 45. № 10. С. 1323.
Гоулдстейн Дж., Джой Д., Лифшин Э. и др. Растровая электронная микроскопия и рентгеновский микроанализ. Кн. 1. М.: Мир, 1984. 303 с.
Майдановская Л.Г. Каталитические реакции в жидкой фазе. Алма-Ата: Изд-во АН КазССР, 1963. С. 212.
Крешков А.П., Казарян Н.А. Кислотно-основное титрование в неводных растворах. М.: Химия, 1967. 192 с.
Кировская И.А. Поверхностные явления. Омск: Изд-во ОмГТУ, 2001. 175 с.
Kirovskaya I.A., Mironova E.V., Kosarev B.A., Nor P.E., Bukashkina T.L. // Russ. J. Phys. Chem. A. 2016. V. 90. № 10. P. 2029.
Дополнительные материалы отсутствуют.
Инструменты
Поверхность. Рентгеновские, синхротронные и нейтронные исследования


