Поверхность. Рентгеновские, синхротронные и нейтронные исследования, 2020, № 5, стр. 93-102
Влияние имплантации ионов углерода на поверхностные физико-химические свойства полилактида, гидроксиапатита и композита на их основе
О. А. Лапуть a, *, Д. А. Зуза a, b, **, И. В. Васенина a, c, ***
a Национальный исследовательский Томский государственный университет
634055 Томск, Россия
b Институт сильноточной электроники СО РАН
634050 Томск, Россия
c Физический институт им. П.Н. Лебедева РАН
119991 Москва, Россия
* E-mail: olesyalaput@gmail.com
** E-mail: zzdnl@yandex.ru
*** E-mail: ivpuhova@mail.ru
Поступила в редакцию 25.06.2019
После доработки 26.08.2019
Принята к публикации 29.08.2019
Аннотация
Представлены результаты исследования физико-химических свойств поверхности полилактида, гидроксиапатита и композита на их основе в соотношении компонентов 80 : 20, модифицированных ионами углерода с экспозиционными дозами облучения 1 × 1015 и 1 × 1016 ион/см2 при ускоряющем напряжении 20 кВ. Химический и элементный состав поверхности образцов исследовали методами инфракрасной и рентгеновской фотоэлектронной спектроскопии. Согласно полученным результатам, после ионной имплантации одновременно протекают процессы деструкции и сшивания макромолекул полилактида и полимера в композиционном материале. После ионно-лучевой обработки наблюдается изменение стехиометрии гидроксиапатита. Установлено, что внедрение ионов углерода способствует улучшению гидрофобных свойств материалов. Этот процесс сопровождается уменьшением свободной поверхностной энергии.
ВВЕДЕНИЕ
В настоящее время полилактид (ПЛ) считается наиболее перспективным и популярным материалом среди биосовместимых полимеров благодаря своим функциональным свойствам: низкому удельному весу, малой температуре обработки (по сравнению с металлами и стеклами), https://www.multitran.ru/c/m.exe?t=6831974_2_1&s1=enviromental%20friendlyэкологической безопасности (при разложении не образует токсичных соединений), высокой пригодности для печатания на 3D-принтерах и способности к формообразованию [1]. Полимеры и композиты на основе лактида, нашли всемирное применение в медицине, благодаря своей биосовместимости и способности разлагаться в живом организме без образования токсичных соединений. Перспективным для реконструкции дефектов костей является использование искусственных материалов, идентичных минеральному компоненту костного вещества. Такими материалами являются, например, композиты из фосфата кальция – гидроксиапатит (ГА), а также его комбинации с другими веществами в виде порошков, гранул, микрочастиц, пластин и т.д. Низкая механическая прочность ГА может быть улучшена путем введения полимерного компонента и получения композиционных материалов на основе ГА и биосовместимых полимеров, таких как полилактид. В организме такие полимеры деградируют до молочной кислоты, которая является нормальным метаболитом и не оказывает токсического воздействия на организм.
Обработка различных материалов ионными пучками является одним из важнейших направлений передовых современных промышленных технологий в виду широкого диапазона режимов ведения процесса [2, 3]. В поверхностных слоях при модифицировании происходят сложные физико-химические процессы, способные существенно изменить структуру и свойства поверхности материалов. Известно, что поверхностная модификация облучением пучками заряженных частиц изменяет физико-химические свойства полимеров вследствие процессов деструкции и сшивания полимерных цепей [4, 5]. В соответствии с принципами радиационной химии, при возбуждении макромолекул полимеров под действием ионизирующего излучения образуются свободные радикалы [6], которые затем могут взаимодействовать друг с другом или инициировать дальнейшие реакции сшивки между полимерными цепями, что приводит к изменениям физико-химических свойств материалов. При встрече двух радикалов может образоваться поперечная сшивка или произойти реструктуризация аморфной области в кристаллическую и наоборот [7]. Вместе с тем, передача цепи (при встрече радикала и макромолекулы) приводит к дальнейшему разрыву полимерной цепи [8]. Обычно оба эти процесса протекают одновременно для многих полимеров [9]. Идентификация этих процессов представляет сложную задачу.
В работе исследуются физико-химические характеристики композиционных материалов на основе полилактида и гидроксиапатита до и после имплантации ионов углерода. Выбор типа ионов обусловлен тем, что при облучении поверхности полимеров ионами углерода происходит активация их поверхности, что способствует улучшению физико-химических свойств материалов (повышение свободной поверхностной энергии, увеличение электропроводности и т.д.) [10, 11]. Исследования носят прикладной и фундаментальный характер, затрагивая вопросы практического применения поверхностно-модифицированных материалов, а также физико-химические основы процессов, протекающих в поверхностных слоях композиционных материалов с полимерной и неорганической составляющей.
Целью настоящей работы является изучение влияния имплантации ионов углерода при экспозиционных дозах облучения 1 × 1015 и 1 × 1016 ион/см2 на физико-химические свойства полимерных и композиционных материалов на основе полилактида и гидроксиапатита.
Согласно нашим предыдущим исследованиям [12], при экспозиционной дозе облучения 1 × × 1014 ион/см2 не наблюдается значительных изменений физико-химических свойств поверхности полимерных материалов, а при дозах выше 1 × 1016 ион/см2 происходит интенсивный рост углеродных частиц и их коалесценция, а также постепенная деградация полимерных материалов [13], что негативно сказывается на функциональных свойствах полимеров. Поэтому в настоящей работе выбран диапазон доз 1 × 1015–1 × 1016 ион/см2, который является оптимальным для улучшения физико-химических и механических характеристик. Энергия имплантируемых ионов углерода определялась произведением ускоряющего напряжения (20 кВ) на среднее значение заряда ионов (〈Q〉С = 1+) и при этом составила 20 кэВ.
МАТЕРИАЛЫ И МЕТОДЫ ИССЛЕДОВАНИЯ
Получение экспериментальных образцов полилактида, гидроксиапатита и композиционных материалов на их основе
Способы получения образцов ПЛ и композиционных материалов ПЛ/ГА в соотношении 80/20 описаны в [14]. Синтез ГА проводили жидкофазным методом под воздействием СВЧ-излучения при рН ~ 11 по схеме по запатентованной технологии [15] в соответствии с уравнением:
Формование таблеток ГА осуществлялось на лабораторном гидравлическом прессе ПГР-10 при давлении 100 бар, диаметр таблеток составлял 7 мм. После прессования таблетки подвергались отжигу при 800°С в течение 4-х часов. Композиционные материалы с дисперсным ГА были получены смешением раствора полилактида в хлороформе (с = 0.1 г/мл) и порошка гидроксиапатита (ГА) при постоянном перемешивании, массовое соотношение компонентов составляло 80% ПЛ и 20% ГА. Полученную суспензию обрабатывали ультразвуком в течение 20 мин с частотой 40 кГц, затем осаждали в пятикратном избытке этилового спирта и полученные волокна высушивали до полного испарения растворителя в сушильном шкафу при 40°С. Композиционный материал, а также волокна чистого полилактида подвергали механическому измельчению, затем формовали на лабораторном гидравлическом прессе ПГР-10 при давлении 100 бар; диаметр таблеток составлял 10 мм.
Модификацию полученных образцов ПЛ, ГА, ПЛ/ГА 80/20 проводили при помощи источника ионов MEVVA II [16]. Экспериментальный макет состоит из источника ионов на основе вакуумного дугового разряда, магнитного сепаратора, вакуумной камеры и коллектора ионов. Схема экспериментальной установки и принцип ее действия представлены в работе [17].
В процессе имплантации применялся пучок сепарированных однозарядных ионов углерода. Ток вакуумной дуги не превышал 200 А при длительности импульса 300 мкс и частоте импульсов 1 Гц. Ионно-лучевая обработка производилась до достижения экспозиционных доз 1 × 1015, 1 × × 1016 ион/см2 при ускоряющем напряжении 20 кВ, при этом энергия однозарядных ионов углерода равна 20 кэВ. Скорость набора экспозиционной дозы и средняя плотность мощности регулировались током ионного пучка и частотой следования разрядных импульсов и составляли 5 × × 1012 ион/(см2 · с) и 1.5 мВт/см2 соответственно. В процессе обработки ионными пучками образцы фиксировались на поверхности водоохлаждаемого коллектора, при этом их интегральная температура не превышала 20°С. Рабочее давление поддерживалось системой откачки на основе двух турбомолекулярных насосов на уровне Р = (1–2) × × 10–6 Toрр.
Методы исследования физико-химических и механических свойств образцов
Химический состав поверхности образцов изучали методом инфракрасной спектроскопии (ИК-спектроскопии) при помощи ИК-Фурье спектрометра Nikolet 5700 на приставке однократного НПВО (нарушенного полного внутреннего отражения) с разрешением 4 см–1.
Элементный состав поверхности исследовался методом рентгеновской фотоэмиссионной спектроскопии (РФЭС) с помощью PHIX-tool automated XPS microprobe. Образцы устанавливали на держатель с помощью, проводящей углеродной или медной ленты. Для РФЭС-анализа использовали монохромный источник рентгеновского излучения с рентгеновским пятном размером 400 мкм. В процессе анализа использовали стандартную систему компенсации заряда с низкой энергией электронов и ионов (≈0.1 эВ). На образцах выполнялась газовая кластерная очистка с использованием источника ионов MAGCIS.
Для оценки смачивания поверхности исходных образцов и после поверхностной модификации проводили измерение краевых углов при контакте с водой, глицерином и этиленгликолем методом лежащей капли и последующий расчет поверхностной энергии с помощью ПО DSA1 на приборе EasyDrop (KRUSS). Сначала измеряли краевые углы смачивания согласно уравнению Юнга–Дюпре [18]. Равновесная величина контактного угла определяется уравнением Юнга–Дюпре:
(1)
${{\sigma }_{{{\text{тв}} - {\text{г}}}}} = {{\sigma }_{{{\text{тв}} - {\text{ж}}}}} + {{\sigma }_{{{\text{ж}} - {\text{г}}}}}{\text{cos}}\theta ,$(2)
$\begin{gathered} {{\sigma }_{{{\text{тв}} - {\text{ж}}}}} = {{\sigma }_{{{\text{тв}} - {\text{г}}}}} + {{\sigma }_{{{\text{ж}} - {\text{г}}}}} - \\ --\,\,2\left( {\sqrt {\sigma _{{{\text{тв}} - {\text{г\;}}}}^{{\text{D}}}\sigma _{{{\text{ж}} - {\text{г}}}}^{{\text{D}}}} + \sqrt {\sigma _{{{\text{тв}} - {\text{г\;}}}}^{{\text{P}}}\sigma _{{{\text{ж}} - {\text{г}}}}^{{\text{P}}}} } \right). \\ \end{gathered} $(3)
$\frac{{{{\sigma }_{{{\text{ж}}--{\text{г}}}}}\left( {{\text{cos}}\theta + 1} \right)}}{{2\sqrt {\sigma _{{{\text{ж}}--{\text{г}}}}^{{\text{D}}}} }} = \frac{{\sqrt {\sigma _{{{\text{ж}}--{\text{г}}}}^{{\text{P}}}} }}{{\sqrt {\sigma _{{{\text{ж}}--{\text{г}}}}^{{\text{D}}}} }}\sqrt {\sigma _{{{\text{тв}}--{\text{г}}}}^{{\text{P}}}} + \sigma _{{{\text{тв}}--{\text{г}}}}^{{\text{D}}}.$РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Химический и элементный состав полимерных и композиционных материалов
Проведено исследование образцов полилактида, гидроксиапатита и композита ПЛ/ГА до и после воздействия ионами углерода методом инфракрасной спектроскопии. На ИК-спектре ПЛ (рис. 1) функциональным группам –СН3, –СН в полимере соответствуют валентные колебания с волновыми числами 2944 см–1 (симметричные колебания) и 2996 см–1 (асимметричные колебания). Дополнительно на ИК–спектре присутствуют валентные колебания карбонильной группы (–С=О) с соответствующим волновым числом 1759 см–1 и валентные колебания (–С(=О)–О) группы с волновыми числами 1456, 1186, 1093, 1045 см–1. Также в ИК-спектре ПЛ присутствуют деформационные колебания функциональной группы (–С–О–С–) с волновым числом 872 см–1. Смещения или образования новых полос в ИК-спектрах не обнаружено, что свидетельствует об отсутствии химических реакций в полимерном материале в условиях ионной имплантации. По результатам ИК-спектроскопии установлено, что спектры образцов, имплантированных ионами углерода, идентичны спектру исходного полилактида (рис. 1, табл. 1), в них присутствуют полосы поглощения, соответствующие колебаниям функциональных групп ПЛ.
Рис. 1.
ИК-спектры исходных и имплантированных ионами углерода с дозой 1 × 1016 ион/см2 образцов ПЛ, ГА и ПЛ/ГА.
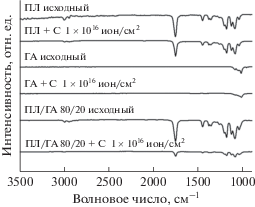
Таблица 1.
Полосы поглощения характеристических колебаний, наблюдаемых в ИК-спектрах ПЛ, ГА, и композита ПЛ/ГА 80/20
| Название группы | Частоты колебаний, см–1 |
|---|---|
| ν (С=О) | 1760–1750 |
| ν (СН3, СН) | 2995–2945, 2885–2980 |
| δ (СН3) | 1380–1360 |
| ν (О–Н) | 3500–2500 |
| ν (${\text{PO}}_{4}^{{3 - }}$) | 1030–1080, 960 |
| δ (${\text{PO}}_{4}^{{3 - }}$) | 630, 600, 570 |
| ν (С–О–С) | 1150–1060, 1075–1020, 920–800 |
На рис. 1 показано, что на ИК-спектрах гидроксиапатита как в исходном состоянии, так и после ионной имплантации наблюдается четыре полосы поглощения в области 965, 1025, 1055 и 1087 см–1, соответствующие валентным колебаниям ортофосфорных групп ${\text{РО}}_{4}^{{3--}}.$ Анализ полученных данных ИК-спектроскопии показал, что в спектрах, исходных и имплантированных ионами углерода образцов композита ПЛ/ГА 80/20 имеются полосы, характерные как для ПЛ, так и для ГА (рис. 1, табл.1). Смещений или новых полос не обнаружено, что свидетельствует о том, что новые химические связи между исходными компонентами материала в процессе получения композита и в условиях ионной имплантации не образуются. Установлено, что после имплантации ионами углерода наблюдается снижение интенсивности всех линий как для ПЛ, так и для композита, что, вероятно, связано с процессами сшивки в приповерхностных слоях материалов.
Элементный состав поверхности образцов полилактида, гидроксиапатита и композита ПЛ/ГА 80/20 в исходном состоянии и после имплантации ионов углерода исследован методом рентгеновской фотоэлектронной спектроскопии. Энергия связи пиков C1s и О1s относятся к химическим связям атомов углерода и кислорода, находящихся в соответствующих координационных состояниях, приведенных в табл. 2 [21]. В исходном образце ПЛ положение и форма линий в спектрах C1s и О1s соответствует справочным данным по энергиям связи электронов, находящихся на соответствующих уровнях углерода и кислорода в ПЛ. На рис. 2 представлены C1s и О1s РФЭ-спектры, полученные для чистой и имплантированной поверхности ПЛ.
Таблица 2.
РФЭС характеристики С1s и О1s в полилактиде
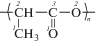 |
С1s | O1s | |||
|---|---|---|---|---|---|
| 1 | 2 | 3 | 1 | 2 | |
| Энергия связи, эВ | 285.00 | 286.98 | 289.06 | 532.25 | 533.66 |
Рис. 2.
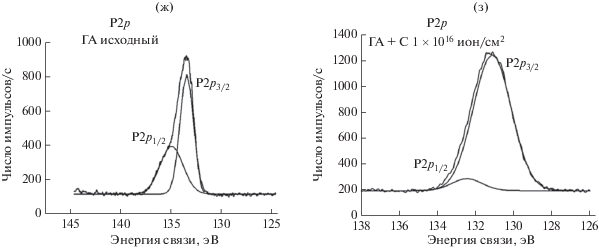
РФЭ-спектры образцов: а – линии С1s исходного ПЛ, б – линии С1s ПЛ + С 1 × 1016 ион/см2, в – линии О1s исходного ПЛ, г – линии О1s ПЛ + С 1 × 1016 ион/см2, д – линии Са2р исходного ГА, е – линии Са2р ГА + С 1 × × 1016 ион/см2, ж – линии Р2р исходного ГА, з – линии Р2р ГА + С 1 × 1016 ион/см2.
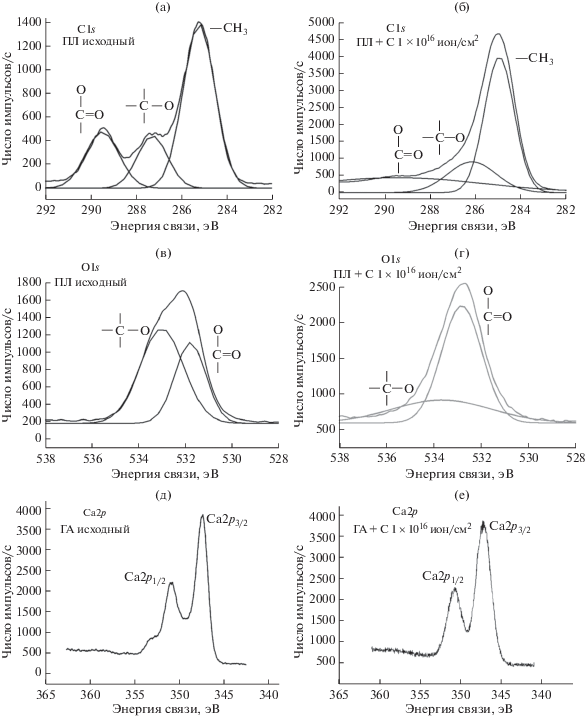
Рис. 2.
Окончание
После имплантации ионами углерода в поверхность ПЛ, смещений по энергиям связи или появления новых полос в спектрах C1s и О1s не обнаружено, что свидетельствует об отсутствии новых химических связей между исходными компонентами материала и внедряемыми примесями в процессе ионной имплантации. Однако соотношение площадей пиков в спектрах C1s после имплантации ионов углерода изменяется: площадь полосы, соответствующей углероду в координации –С=O увеличивается в 1.6 раз, а в спектре О1s – в 2.5 раза, что связано с процессами деструкции или окисления в поверхностных слоях ПЛ в процессе ионной имплантации. Ионно-лучевая обработка способствует увеличению содержания атомов углерода в полилактиде по рассчитанному соотношению атомных концентраций С/О (табл. 3). Увеличение доли углерода связано с процессами деструкции приповерхностных слоев полимера и образование углеродных (графитовых) кластеров.
Таблица 3.
Соотношение атомных концентраций элементов, поверхностная энергия и ее составляющие для образцов ПЛ, ГА, ПЛ/ГА 80/20
| Обозначение | Соотношение атомных концентраций элементов, aт. % | Поверхностная энергия, мН/м | |||
|---|---|---|---|---|---|
| С/О | Са/Р | Полярная | Дисперсионная | Общая | |
| ПЛ исходный | 0.78 | – | 31.16 ± 1.07 | 5.15 ± 0.38 | 36.30 ± 1.45 |
| ПЛ + С 1 × 1015 ион/см2 | – | – | 10.69 ± 0.40 | 13.87 ± 0.45 | 24.56 ± 0.85 |
| ПЛ + С 1 × 1016 ион/см2 | 2.14 | – | 4.29 ± 0.31 | 28.87 ± 0.97 | 33.16 ± 1.29 |
| ГА исходный | – | 1.33 | 79.40 ± 3.99 | 1.01 ± 0.15 | 80.96 ± 4.04 |
| ГА + С 1 × 1015 ион/см2 | – | – | 75.17 ± 1.53 | 6.24 ± 1.22 | 81.41 ± 1.94 |
| ГА + С 1 × 1016 ион/см2 | – | 1.00 | 30.62 ± 3.75 | 8.19 ± 0.90 | 38.81 ± 4.07 |
| ПЛ/ГА исходный | – | 1.19 | 19.88 ± 1.07 | 12.85 ± 0.79 | 32.73 ± 1.86 |
| ПЛ/ГА + С 1 × 1015 ион/см2 | – | – | 12.48 ± 0.49 | 13.47 ± 0.49 | 25.95 ± 0.98 |
| ПЛ/ГА + С 1 × 1016 ион/см2 | – | 1.14 | 16.02 ± 0.82 | 10.84 ±0 .63 | 26.87 ± 1.45 |
По данным РФЭС для образцов ГА (рис. 2) установлено, что имплантация ионов углерода приводит к уменьшению площади пика, соответствующего электронам на уровне P2p1/2 в 1.2 раза, а на уровне P2p3/2 к увеличению в 1.7 раз. Площади пиков в спектре атомов кальция Са2р незначительно уменьшается. Можно отметить фактически пропорциональное изменение соотношения основных элементов (кальция и фосфора) в гидроксиапатите до и после ионного облучения, следовательно, ионная имплантация оказывает влияние на стехиометрию гидроксиапатита. Рассчитанное соотношение атомных концентраций Са/Р = 1.33 (табл. 3) свидетельствуют о том, что, полученный в ходе эксперимента гидроксиапатит, согласно синтезу, относится к октокальциевому фосфату [22]. После имплантации ионов.
На углерода наблюдается изменение данного соотношения и стехиометрия меняется до дикальциевого фосфата (Са/Р = 1), что обусловлено деструкцией приповерхностных слоев материалов рис. 3 представлены РФЭ-спектры C1s, О1s, Са2р, Р2р исходного композита ПЛ/ГА 80/20 и после имплантации ионами углерода с дозой облучения 1 × 1016 ион/см2. Показано, что спектры C1s исходного и облученных ионами углерода образцов ПЛ/ГА 80/20 содержат линии связей электронов на 1s-энергетическом уровне углерода, находящегося в трех координационных состояниях, соответствующих полилактиду (табл. 2). В композите ПЛ/ГА 80/20 после имплантации углерода с дозой 1 × 1016 ион/см2 в 1.9 раз увеличивается площадь пика углерода С1s в координации СН3–СН–, площадь пика углерода С1s в координации –СН–С– уменьшается в 1.2 раза и площадь пика углерода С1s в координации –С=О уменьшается в 1.1 раз. Также в композите после имплантации ионами углерода уменьшается площадь пика углерода С1s в координации –С=О в 1.5 раз, а площадь пика углерода С1s в координации –СН–С– увеличивается в 3.2 раза. Установлено, что соотношение атомных концентраций Са/Р в композите ПЛ/ГА 80/20 не претерпевают значительных изменений после ионно-лучевой обработки.
Рис. 3.
РФЭ-спектры образцов: а – линии С1s исходного ПЛ/ГА, б – линии С1s ПЛ/ГА + С 1 × 1016 ион/см2, в – линии О1s исходного ПЛ/ГА, г – линии О1s ПЛ/ГА + С 1 × 1016 ион/см2, д – линии Са2р исходного ПЛ/ГА, е – линии Са2р ПЛ/ГА + С 1 × 1016 ион/см2, ж – линии Р2р исходного ПЛ/ГА, з – линии Р2р ПЛ/ГА + С 1 × 1016 ион/см2.
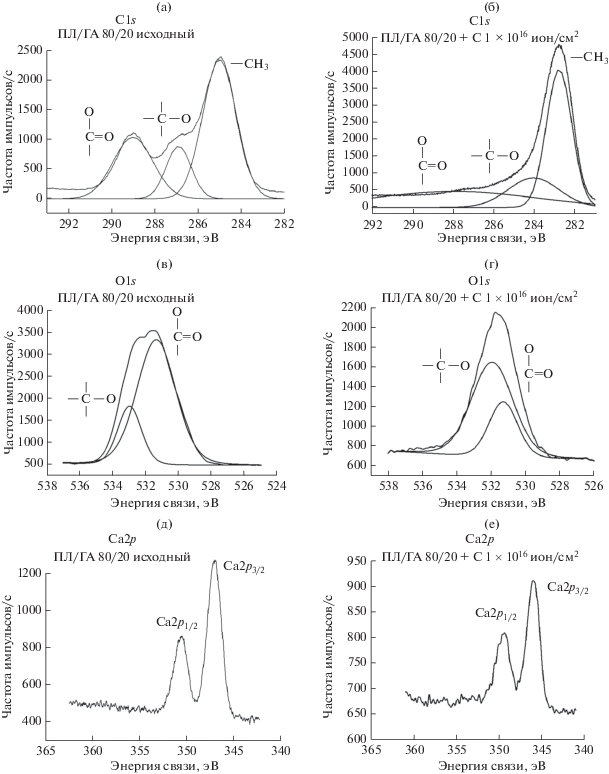
Рис. 3.
Окончание

Смачиваемость поверхности
Известно, что характеристики смачиваемости играют огромную роль в биохимических процессах, протекающих на границе костная ткань-жидкость живого организма. Измерения краевого угла смачивания поверхности ПЛ проводили методом лежащей капли при контакте с тремя жидкостями: вода, глицерин и этиленгликоль. Максимальное значение краевого угла смачивания при контакте с водой и этиленгликолем наблюдается для образца, модифицированного ионами углерода с экспозиционной дозой облучения 1 × 1016 ион/см2, и составляет 84° и 54° соответственно. При контакте с глицерином для образца, обработанного ионами углерода, наблюдается незначительное снижение краевого угла с 71 до 69° (рис. 4а, 4в). В целом, можно отметить, что материал после ионной имплантации становится более гидрофобным.
Рис. 4.
Краевые углы смачивания ПЛ, ГА и композита ПЛ/ГА при контакте с водой (а), глицерином (б), этиленгликолем (в).
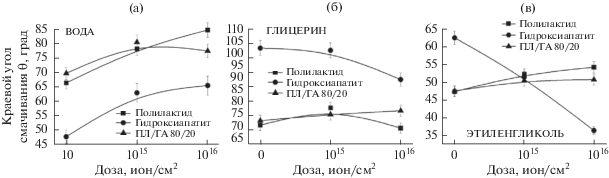
Гидроксиапатит является влаговпитывающим материалом, поэтому измерение краевого угла на его поверхности проводили за первые три секунды нанесения капли и брали средние значения. Тем не менее, удалось проследить устойчивую тенденцию к увеличению краевого угла при смачивании гидроксиапатита водой после ионной имплантации с увеличением дозы облучения с 47° до 86° (рис. 4а). В исходном состоянии ГА является олеофобным материалом, краевой угол смачивания глицерином составляют 102° (рис. 4б). При смачивании глицерином значения краевого угла для облученных образцов ГА незначительно отличаются от исходного. При смачивании образцов ГА этиленгликолем наблюдается линейная тенденция к уменьшению краевого угла с увеличением дозы облучения с 63° до 40°, следовательно, гидрофильность материала повышается (рис. 4в).
Значения краевого угла смачивания композиционного материала на основе полилактида и гидроксиапатита в соотношении 80 : 20 идентичны значениям для чистого полилактида. Наблюдаются такие же тенденции изменения характеристик смачиваемости: краевой угол незначительно увеличивается при контакте со всеми жидкостями (вода, глицерин, этиленгликоль) (рис. 4а–4в). После облучения композита ПЛ/ГА 80 : 20 ионами углерода значения краевого угла при смачивании всеми тремя жидкостями изменяются: для воды с 69° до 77°, глицерина с 73° до 77°, этиленгликоля с 47° до 51° (рис. 4а–4в).
Поверхностная энергия содержит две компоненты: дисперсионную (силы Ван-дер-Ваальса, другие неспецифические взаимодействия) и полярную (сильные взаимодействия атомов поверхности с адсорбируемыми молекулами жидкости и водородные связи). Установлено, что имплантация образцов ПЛ ионами углерода приводит к снижению полярной и повышению дисперсионной составляющей, при этом общая поверхностная энергия ПЛ уменьшается с увеличением дозы облучения с 36 до 33 мН/м (табл. 3).
Необходимо отметить, что общая поверхностная энергия гидроксиапатита уменьшается с увеличением дозы облучения ионов углерода с 81 до 39 мН/м, этот процесс сопровождается ростом дисперсионной составляющей и уменьшением полярной компоненты (табл. 3). Установлено, что после имплантации ионов углерода полярная и дисперсионная компоненты поверхностной энергии композита ПЛ/ГА 80/20 уменьшаются (табл. 3), при этом общая поверхностная энергия также снижается с 33 до 27 мН/м.
ЗАКЛЮЧЕНИЕ
Проведен комплекс исследований по влиянию имплантации ионов углерода с экспозиционными дозами облучения 1 × 1015 и 1 × 1016 ион/см2 на свойства полилактида, гидроксиапатита и композита на их основе с массовым соотношением компонентов 80 : 20. Показано, что поверхностное воздействие ионами углерода влияет на физико-химические характеристики (элементный состав, смачиваемость) и, соответственно, на энергетическое состояние поверхности материалов.
По результатам ИК-спектроскопии после ионной имплантации в спектрах полилактида наблюдаются характерные для данного материала полосы (–СН3, –СН, –С=О, –С–О–С–). В ИК-спектрах ГА присутствуют характерные для него линии, соответствующие валентным колебаниям ортофосфорных групп ${\text{РО}}_{4}^{{3--}}.$ При этом после имплантации ионами углерода наблюдается снижение интенсивности всех линий как для полилактида, так и для композита на их основе, что обусловлено процессами сшивки. По результатам РФЭС установлено, что площадь полосы ‒С=O увеличивается в 1.6 раз, что связано с процессами деструкции и окисления в условиях ионной имплантации. Вероятно, при ионной имплантации происходят одновременные процессы деструкции и сшивки полимерных макромолекул.
После имплантации ионов углерода смещений по энергиям связи или появления новых полос в спектрах C1s и О1s не обнаружено, что свидетельствует об отсутствии новых химических связей между исходными компонентами материала и внедряемыми примесями в процессе ионной имплантации. Показано, что ионная имплантация влияет на стехиометрию гидроксиапатита, что обусловлено деструкцией приповерхностных слоев материалов.
Обработка ионными пучками способствует изменению смачиваемости поверхности полимерных и композиционных материалов как полярными (вода, этиленгликоль), так и неполярными жидкостями (глицерин). Установлено, что после внедрения ионов углерода в полилактид, гидроксиапатит и композит ПЛ/ГА 80/20 наблюдается линейная тенденция к росту краевого угла при смачивании всеми тремя жидкостями с увеличением дозы облучения. Повышение краевого угла смачивания сопровождается снижением общей поверхностной энергии для всех материалов после имплантации. Уменьшение общей поверхностной энергии происходит за счет изменения соотношения ее компонент: полярная составляющая поверхностной энергии уменьшается, а дисперсионная компонента становится доминантной. Снижение значений свободной поверхностной энергии после внедрения ионов углерода, вероятно, связано с процессами деструкции в приповерхностных слоях материалов. Таким образом, материалы после ионной имплантации приобретают гидро- и олеофобные свойства.
Список литературы
Hu Y., Daoud W.A., Cheuk K.K.L., Lin C.S.K. // Materials. 2016. V. 9. № 3. P. 133.
Sviridov D.V. // Chemical Problems of The Development of New Materials and Technologies. 2003. V. 1. P. 88.
Popok V.N. // Rev. Adv. Mater. Sci. 2012. V. 30. P. 1.
Chapiro A. Radiation Chemistry of Polymeric Systems. London: Interscience, 1962.
Charlesby A. Radiation Chemistry Principles, Applications. N.Y.: VCH, 1987.
Mark H.F. Encyclopedia of Polymer Science and Engineering. Lincolnshire: Wiley, 1986. V. 4
Lovinger A.J. // ACS Symp. Ser. 1991. V. 475. Ch. 6. P. 84.
Pionteck J., Hu J., Pompe G., Albrecht V., Schulze U., Borsig E. // Polymer. 2000. V. 41. P. 7915.
Ichikawa T. // Nucl. Instrum. Methods Phys. Res. B. 1995. V. 105. P. 150.
Sokullu E., Ersoy F., Öztarhan A., Brown I. G. // Anatomy. 2015. V. 9. P. 135.
Schiller T.L., Sheeja D., McKenzie D.R., McCulloch D.G., Lau D.S.P., Burn S., Tay B.K. // Surf. and Coat. Technol. 2004. V. 177. P. 483.
Pukhova I.V., Savkin K.P., Laput O.A., Lytkina D.N., Botvin V.V., Medovnik A.V., Kurzina I.A. // Appl. Surf. Sci. 2017. V. 422. P. 856.
Степанов А.Л. // Журн. технич. физ. 2004. Т. 74. № 2. С. 1.
Shapovalova Y., Lytkina D., Rasskazova L., Filimoshkin A., Korotchenko N., Kurzina I., Kzhyshkowska J. Zhuk I., Gudima A. // Key Eng. Mater. 2016. V. 683. P. 475.
Коротченко Н.М., Рассказова Л.А. РФ Патент 2 507 151, 2014.
Brown I.G. // IEEE Trans. Nucl. Sci. 1985. V. 32. № 5. P. 1723.
Курзина И.А., Пухова И.В., Савкин К.П. // Известия высших учебных заведений: Физика. 2016. Т. 59. № 9/3. С. 252.
Mark J.E. Physical Properties of Polymers. Handbook. N.Y.: Springer, 2007.
Owens D., Wendt R. // J. Appl. Polym. Sci. 1969. V. 13. P. 1741.
Миронюк А.В. Придатко А.В., Сиволапов П.В., Свидерский В.А. // Восточно-Европейский журн. передовых технологий. 2014. Т. 1. № 6. С. 23.
Beamson G., Briggs D. High Resolution XPS of Organic Polymers. Chichester: Wiley, 1992.
Рассказова Л.А. Технология получения магний- и кремний-модифицированных гидроксиапатитов и биорезорбируемых композиционных материалов с использованием полимеров молочной кислоты. Дисс. … канд. тех. наук. Томск: ТТГУ, 2015. 137 с.
Дополнительные материалы отсутствуют.
Инструменты
Поверхность. Рентгеновские, синхротронные и нейтронные исследования


