Поверхность. Рентгеновские, синхротронные и нейтронные исследования, 2021, № 4, стр. 3-11
Селенсодержащие наносистемы на основе амфифильных молекулярных щеток с варьируемой степенью полимеризации боковых цепей в водных и органических средах
С. В. Валуева a, *, М. Э. Вылегжанина a, К. А. Митусова a, А. Я. Волков a, Т. К. Мелешко a, И. В. Иванов a, А. В. Якиманский a
a Институт высокомолекулярных соединений Российской академии наук
199004 Санкт-Петербург, Россия
* E-mail: svalu67@mail.ru
Поступила в редакцию 19.07.2020
После доработки 18.09.2020
Принята к публикации 25.09.2020
Аннотация
Методами атомно-силовой микроскопии, рентгеноструктурного анализа, УФ-видимой спектроскопии и динамического светорассеяния проведено сравнительное исследование наносистем на основе наночастиц биогенного элемента селена в нуль-валентной форме (Se0) и амфифильных молекулярных щеток (графт-СП) с гидрофобной основной полиимидной цепью и гидрофильными боковыми цепями полиметакриловой кислоты. Показана возможность регулирования морфологических и спектральных характеристик наноструктур Se0/графт-СП путем варьирования степени полимеризации m боковых цепей амфифильной молекулярной щетки. На примере “свободной” (не загруженной наночастицами Se0) амфифильной молекулярной щетки графт-СП с фиксированной степенью полимеризации боковых цепей (m = 270) показано влияние природы растворителя (вода, диметилформамид и хлороформ) на морфологию тонких пленок графт-СП на слюде.
ВВЕДЕНИЕ
Молекулярные полимерные щетки – особый вид привитых сополимеров с регулярно привитыми узкодисперсными боковыми цепями – привлекают большой интерес из-за их уникальных химических и физических свойств [1]. Активное развитие этого направления стало возможным благодаря последним достижениям в области так называемой контролируемой/“живой” (псевдоживой) полимеризации. Среди методов псевдоживой полимеризации при получении молекулярных щеток наиболее часто используют метод контролируемой радикальной полимеризации с переносом атома (Atom Transfer Radical Polymerization, ATRP), применяя стратегию “прививка от” [2]. Амфифильные молекулярные щетки эффективно используют в нанобиотехнологических разработках для создания на их основе наноконтейнеров в целях солюбилизации гидрофобных лекарственных препаратов или агентов и их адресной доставки [3–8]. В настоящей работе в качестве загружаемого агента использовали гидрофобные наночастицы биогенного элемента селена в нуль-валентной форме (Se0), обладающие комплексом уникальных биомедицинских свойств [8–12]. Несомненный интерес для использования в качестве наноконтейнеров представляют амфифильные молекулярные щетки с гидрофобной полиимидной основной цепью и гидрофильными боковыми цепями полиметакриловой кислоты (ПМАК), так как показано, что при высоких значениях степени полимеризации боковых цепей ПМАК и плотности их прививки эти щетки обладают хорошей растворимостью в воде и проявляют способность инкорпорировать в гидрофобную часть лекарственные препараты/агенты за счет гидрофобных взаимодействий [7, 8].
Целью настоящей работы являлось изучение морфологических и спектральных характеристик как свободных амфифильных молекулярных щеток графт-СП с основной полиимидной цепью и боковыми цепями ПМАК в растворителях различной природы (вода, диметилформамид и хлороформ), так и новых селенсодержащих наносистем Se0/графт-СП в воде методами атомно-силовой микроскопии (АСМ), рентгеноструктурного анализа (РСА), УФ-видимой спектроскопии и динамического светорассеяния (ДСР). В качестве полиимидных щеток в данной работе были использованы образцы графт-СП (рис. 1) с одинаковыми параметрами основной полиимидной цепи и максимальной плотностью прививки Z боковых цепей ПМАК (Z = 100 мол. %), но с варьируемой степенью полимеризации m боковых цепей.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Материалы
Для синтеза наночастиц селена использовались селенистая и аскорбиновая кислоты (“Вектон”, Санкт-Петербург). Вещества растворялись в апирогенной воде для инъекций.
Синтез молекулярных щеток с полиимидной основной цепью и боковыми цепями полиметакриловой кислоты. Образцы амфифильных молекулярных щеток графт-СП синтезировали в несколько стадий (как описано в работе [7]). Сначала полимеризацией трет-бутилметакрилата (ТБМА) на мультицентровом полиимидной макроинициаторе методом ATRP получали образцы щетки-прекурсора с боковыми цепями поли (трет-бутилметакрилата) (ПТБМА). Затем цепи ПТБМА путем кислотного гидролиза переводили в боковые цепи полиметакриловой кислоты, сохраняя их степень полимеризации. С целью получения образцов графт-СП с одинаковыми параметрами основной полиимидной цепи и одинаковой максимальной плотностью прививки боковых цепей для синтеза щеток прекурсора была использована одна партия полиимидного инициатора с инициирующими ATRP 2-бромизобутиратными группами в каждом повторяющемся звене (по данным 1Н ЯМР). Поскольку этот макроинициатор в дальнейшем формирует основную цепь образцов графт-СП, были определены его молекулярная масса, средняя степень поликонденсации n и индекс полидисперсности Đ (табл. 1). В табл. 1 также приведены экспериментальные условия получения молекулярных щеток-прекурсоров. Для расчета степени полимеризации m (табл. 1) и плотности прививки Z боковых цепей ПТБМА определяли конверсию мономера методом газовой хроматографии [13], а боковые цепи выделяли из образцов щеток прекурсора путем селективного щелочного гидролиза основной цепи [7]. На основе данных конверсии мономера и степеней полимеризации выделенных боковых цепей, определенных методом ГПХ, рассчитывали значения плотности прививки боковых цепей [14]. Все синтезированные образцы характеризовались 100% плотностью прививки боковых цепей Z (табл. 1).
Таблица 1.
Условия синтеза и молекулярно-массовые характеристики графт-СП (полимеризацию проводили в растворе в N-метил-2-пирролидоне, объемное соотношение растворитель/мономер = 3/1)
| № обр. | Условия синтеза графт-СП | Характеристики ПИ основной цепи | Характеристики боковых цепей ПТБМА | |||||||
|---|---|---|---|---|---|---|---|---|---|---|
| Мольное соотношение реагентов | T, °C | t, ч | Mn | n | Ð | Mn | m | Ð | Z | |
| 1 | ПИИ/CuCl/HMTETA/ТБМА = 1/1/1.5/200 | 50 | 1 | 31 200 | 49 | 2.5 | 8600 | 60 | 1.3 | 100 |
| 2 | ПИИ/CuCl2/dNbpy/Sn(EH)2/ТБМА = = 1/1.2/2.4/1/200 |
80 | 4 | 17 700 | 120 | 1.5 | 100 | |||
| 3 | ПИИ/CuCl/HMTETA/ТБМА = 1/1/1.5/400 | 50 | 6 | 39 500 | 270 | 1.3 | 100 | |||
Синтез наночастиц нуль-валентного селена. Синтез селенсодержащих наносистем Se0/графт-СП проводили на основе реакции восстановления селенистой кислоты H2SeO3 аскорбиновой кислотой C6H8O6 в водной среде в присутствии графт-СП:
при этом массовое соотношение ν компонентов Se0/графт-СП составляло ν = СSe/Сграфт-СП = 0.05. После завершения реакции раствор приобретал красновато-оранжевый цвет. Введение в реакционную среду графт-СП позволило получить стабильные растворы красновато-оранжевого цвета, сохраняющие свои физико-химические свойства в течение 2–3 мес., рН селен-содержащих растворов составляла 3.2–3.4.Методы исследования
Изучение морфологии селенсодержащих наносистем Se0/графт-СП методом атомно-силовой микроскопии (АСМ). Морфологические исследования амфифильных молекулярных щеток и соответствующих гибридных наносистем Se0/ графт-СП проводили на атомно-силовом микроскопе Nanotop NT-206 (ОДО “Микротестмашины”, Беларусь). Измерения выполняли в контактном режиме в атмосферных условиях с использованием кремниевых кантилеверов NSC11/AlBS с коэффициентом жесткости k = 3.0 Н/м и радиусом кривизны кончика острия 10 нм. Экспериментальные данные обрабатывали с помощью программы Surface Explorer. Растворы графт-СП и наносистем Se0/графт-СП наносили на слюду.
Рентгеноструктурный анализ (РСА). Съемка порошковых образцов графт-СП (рис. 2) была проведена на дифрактометре SEIFERT XRD 3003 TT при комнатной температуре. Использовали CuKα-излучение с длиной волны λ = 1.5406 Å.
Рис. 2.
Дифракционная картина для амфифильных молекулярных щеток графт-СП при варьировании степени полимеризации m боковых цепей ПМАК: кривая 1 – m = 60, кривая 2 – m = 120, кривая 3 – m = 270.

УФ/видимая спектроскопия. Измерения оптической плотности D водных растворов амфифильных молекулярных щеток графт-СП (рис. 3а) и соответствующих наносистем Se0/графт-СП (рис. 3б) проводили на спектрофотометре Specord M-40 (Карл Цейс Йена, Германия) в диапазоне длин волн от 185 до 900 нм в термостатируемом режиме, с толщиной фотометрического слоя 1 см.
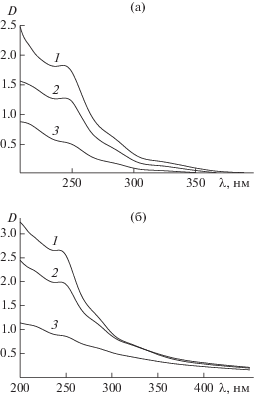
Рис. 3.
Оптические спектры поглощения свободных амфифильных молекулярных щеток графт-СП при варьировании степени полимеризации m боковых цепей полиметакриловой кислоты: 1 – m = 60, 2 – m = = 120, 3 – m = 270 (а). Оптические спектры поглощения гибридных наносистем Se0/графт-СП (ν = = CSe/Сграфт-СП = 0.05) при варьировании степени полимеризации m боковых цепей полиметакриловой кислоты: 1 – m = 60, 2 – m = 120, 3 – m = 270 (б).
Динамическое светорассеяние (ДСР). Гидродинамические радиусы Rh амфифильных молекулярных щеток графт-СП в различных растворителях определяли методом ДСР на корреляционном спектрометре PhotoCorComplex (источник света – гелий-неоновый лазер фирмы Сoherent мощностью 20 мВт с длиной волны λ = 632.8 нм) с программируемым коррелятором Photocor-FC (число каналов 288, ООО “Фотокор”, Россия). Анализ корреляционной функции осуществляли с помощью программы обработки данных динамического светорассеяния Dynals. Величины гидродинамических радиусов Rhрассчитывали из значений коэффициентов диффузии D* по уравнению Эйнштейна–Стокса: Rh = kT/6πη0D* (η0 – вязкость растворителя, k – константа Больцмана, T – температура).
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
По данным РСА (рис. 2) образцы “свободных” графт-СП (не загруженных наночастицами Se0) являются кристаллическими. Наиболее упорядоченным являлся образец с самой короткой боковой цепью (m = 60). На картине дифракции в области углов рассеяния 2Θ = 10°–40° наблюдается ряд накладывающихся друг на друга кристаллических рефлексов (рис. 2, кривая 1). При увеличении степени полимеризации m боковых цепей ПМАК степень упорядоченности снижается (рис. 2, кривые 2 и 3). Для образца с максимальной длиной боковых цепей (m = 270) на дифрактограмме в области углов 2Θ = 18°–35° наблюдается менее интенсивный широкий максимум, более похожий на аморфное гало (рис. 1, кривая 3).
На рис. 3а приведены оптические спектры поглощения в УФ- и видимой областях для свободных графт-СП при варьировании степени полимеризации m боковых цепей полиметакриловой кислоты. На спектрах четко прослеживается зависимость величины оптической плотности D от параметра m: по мере увеличения степени полимеризации боковых цепей величина оптической плотности падает. Это коррелирует с данными РСА, которые показывают, что с увеличением степени полимеризации m боковых цепей графт-СП степень упорядоченности снижается. Аналогичная зависимость по величине оптической плотности от параметра m наблюдается и для селенсодержащих наносистем Se0/графт-СП при ν = 0.05 (рис. 3б). Для более наглядного представления значения оптической плотности D при λ = = 244 нм (λ = 244 нм соответствует середине “плато” на оптических спектрах поглощения свободных графт-СП и соответствующих наносистем Se0/графт-СП) сведены в табл. 2. Спектральные данные, представленные в табл. 2, иллюстрируют гиперхромный эффект полосы поглощения при λ = 244 нм, наблюдаемый при переходе от свободных амфифильных молекулярных щеток графт-СП к наносистемам Se0/графт-СП. Это подтверждает эффект стабилизации наночастиц Se0 амфифильными молекулярными щетками графт-СП, так как согласно литературным данным пик поглощения для коллоидного селена наблюдается при λ = 256 нм [15]. Таким образом, в случае наносистем Se0/графт-СП имеет место суперпозиция вкладов в величину оптической плотности в диапазоне длин волн λ = 240–260 нм от графт-СП и наночастиц селена. Похожая картина наблюдалась для исследованных нами ранее селенсодержащих наносистем на основе амфифильных молекулярных щеток с варьируемой плотностью прививки Z боковых цепей ПМАК [16].
Таблица 2.
Величины оптической плотности D при λ = 240 нм (середина плато на оптических спектрах поглощения графт-СП и гибридных наносистем Se0/графт-СП (ν = CSe/Сграфт-СП = 0.05)) в зависимости от параметра m
| Графт-СП | D, отн. ед. при λ = 240 нм | Se0/графт-СП | D, отн. ед. при λ = 240 нм |
|---|---|---|---|
| m = 60 | 1.80 | m = 60 | 2.65 |
| m = 120 | 1.27 | m = 120 | 2.00 |
| m = 270 | 0.54 | m = 270 | 0.80 |
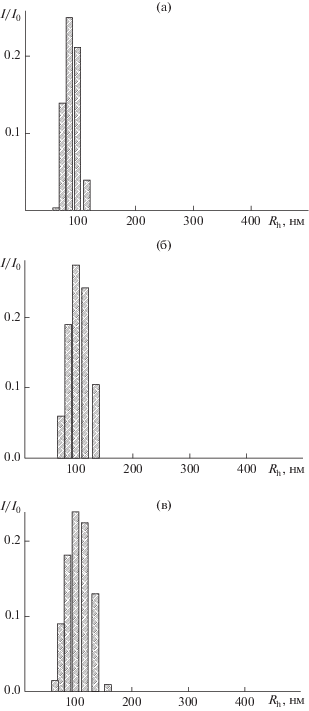
Учитывая, что чем сильнее взаимодействие поверхностных атомов с адсорбированными на НЧ макромолекулами, тем меньше размер частиц, при котором образуется устойчивая в растворе система [17], были сопоставлены величины гидродинамических радиусов наноструктур Rh, определенные методом ДСР для гибридных наносистем Se0/графт-СП (ν = 0.05), в зависимости от параметра m. Анализ данных показал, что величина гидродинамического радиуса селенсодержащих наноструктур Rh практически не зависит от параметра m: Rh = 105 нм (m = 60), Rh = 102 нм (m = 120) и Rh = 101 нм (m = 270). При этом для всех наносистем наблюдалось унимодальное распределение по гидродинамическим радиусам Rh с увеличением ширины распределения по мере возрастания параметра m (рис. 4). Важно отметить, что наблюдаемый для наносистем Se0/графт-СП факт отсутствия зависимости размеров Rh от параметра m кардинально отличается от того, что было зафиксировано для этих наносистем в случае варьирования плотности прививки Z боковых цепей полиметакриловой кислоты графт-СП [16]. В последнем случае четко прослеживалась тенденция уменьшения размеров наноструктур при увеличении параметра плотности прививки Z.
Рис. 4.
Гистограммы распределения по размерам (гидродинамический радиус) $R_{{\text{h}}}^{*}$ для наносистем Se0/графт-СП (ν = 0.05) при варьировании степени полимеризации m боковых цепей полиметакриловой кислоты: а – m = 60, б – m = 120, в – m = 270 в соответствии с относительной интенсивностью I/I0 динамического светорассеяния.
На рис. 5а, 5в, 5д представлены 3D-изображения поверхности тонких пленок, отлитых из водных растворов свободных амфифильных молекулярных щеток графт-СП с различной степенью полимеризации m боковых цепей, полученных методом АСМ. На 3D-изображениях (рис. 5а и 5в) для графт-СП при m = 60 и 120 наблюдаютcя структуры двух морфологических типов: отдельные сферические структуры диаметром DАСМ = = 80–120 и DАСМ = 80–160 нм (табл. 3); также четко визуализируются кольцевые агрегаты размером ~0.3–0.4 мкм, имеющие толщину до 100 нм. Совсем иная картина наблюдается для графт-СП при m = 270 (рис. 5д): видны объекты исключительно сферической формы диаметром 150–200 нм (табл. 3). Таким образом, для свободных щеток характерна тенденция увеличения размеров DАСМ с возрастанием степени полимеризации m боковых цепей. Расчетные математические параметры шероховатости пленок, отлитых из водных растворов графт-СП невелики, и имеют следующие значения: среднеарифметическая шероховатость составляет Ra = 0.5 нм (при m = 60 и 120), Ra = 1.2 нм (m = 270), среднеквадратичная шероховатость Rq = 0.7 нм (при m = 60 и 120) и Rq = 1.6 нм (m = 270) (табл. 3).
Рис. 5.
3D-изображения (размер скана 4 × 4 мкм) поверхности пленок, полученных из водных растворов свободных амфифильных молекулярных щеток графт-СП (а), (в), (д) и гибридных наносистем Se0/графт-СП (ν = CSe/Сграфт-СП = = 0.05) (б), (г), (е) с различной степенью полимеризации m боковых цепей полиметакриловой кислоты: m = 60 (а), (б), m = 120 (в), (г) и m = 270 (д), (е).

Таблица 3.
Размеры и параметры шероховатости, определенные методом АСМ для пленок, полученных на слюде из водных растворов графт-СП и гибридных наносистем Se0/графт-СП при варьировании параметра m
| Графт-СП | DАСМ, нм | Ra, нм | Rq, нм | Se0/графт-СП | DАСМ, нм | Ra, нм | Rq, нм |
|---|---|---|---|---|---|---|---|
| m = 60 | 80–120 | 0.5 | 0.7 | m = 60 | 80–120 | 0.9 | 1.5 |
| m = 120 | 80–160 | 0.5 | 0.7 | m = 120 | 70–100 | 0.5 | 0.7 |
| m = 270 | 150–200 | 1.2 | 1.6 | m = 270 | 50–100 | 1.5 | 2.7 |
На 3D-изображениях, полученных для селенсодержащих наносистем Se0/графт-СП при ν = = 0.05 (рис. 5б, 5г, 5е) морфологическая картина близка к той, что наблюдалось для свободных щеток: при m = 60 и 120 имеют место структуры двух морфологических типов: отдельные сферические структуры и кольцевые агрегаты (рис. 5б, 5г), а для графт-СП при m = 270 (рис. 5е) – только объекты сферической формы диаметром 50–100 нм (табл. 3). Однако, для селенсодержащих наносистем характерна тенденция уменьшения размеров DАСМ с возрастанием степени полимеризации m боковых цепей ПМАК (табл. 3). Это противоположно тому, что наблюдалось для свободных щеток и отличается от ситуации, наблюдаемой в растворе для наносистем Se0/графт-СП методом ДСР, по-видимому, наличие объектов разных морфологических типов при m = 60 и 120 не позволяет адекватно рассчитывать величины гидродинамических радиусов Rh из значений коэффицентов диффузии по уравнению Эйнштейна–Стокса. Параметры шероховатости для щеток, загруженных наночастицами селена имеют величины больше, чем для свободных щеток при тех же значениях параметра m (табл. 3).
Таким образом, синтезированы и исследованы новые гибридные селенсодержащие наносистемы на основе водорастворимых амфифильных молекулярных щеток с варьируемой степенью полимеризации m боковых цепей полиметакриловой кислоты. Широким спектром физических методов в растворе и в пленке были получены данные, свидетельствующие о влиянии параметра m на морфологические и спектральные характеристики наноструктур Se0/графт-СП. Полученные результаты составляют физико-химическую основу для модификации регулярно привитых амфифильных молекулярных щеток графт-ПС биогенными элементами в нуль-валентной форме.
Известно, что, варьируя физико-химические свойства растворителя (например, его диэлектрическую проницаемость ε), можно изменять конформацию щетки [18], и как следствие – надмолекулярную структуру объекта. В качестве объекта исследования в растворителях с различной диэлектрической проницаемостью (табл. 4): вода (ε = 81), диметилформамид (ДМФА) (ε = 36.7) и хлороформ (ε = 9.5) была выбрана амфифильная молекулярная щетка графт-СП со степенью полимеризации боковых цепей ПМАК m = 270. Сравнительное АСМ-исследование этой щетки в различных средах показало, что, меняя природу растворителя, можно кардинально изменять морфологическую картину поверхности пленок. Так из рис. 6 следует, что в пленке, отлитой из водного раствора, формируются дискретные сферические структуры диаметром 150–200 нм (рис. 6а); а в пленке, отлитой из ДМФА, образуются изотропные мицеллы размером ~0.5–2 мкм с набухающей короной, декорированные сферическими структурами диаметром 200–400 нм (рис. 6б); в случае хлороформа наблюдаются фибриллы, заполненные сферическими структурами диаметром 150–200 нм, образующие домены с преимущественной внутренней ориентацией (рис. 6в).
ЗАКЛЮЧЕНИЕ
Для исследованных селенсодержащих наносистем на основе водорастворимых амфифильных молекулярных щеток графт-СП с основной полиимидной цепью и боковыми цепями полиметакриловой кислоты методом УФ-видимой спектроскопии в воде установлен факт образования наночастиц Se0 в нуль-валентном состоянии.
Показана возможность регулирования морфологических и спектральных параметров селенсодержащих наносистем Se0/графт-СП путем варьирования степени полимеризации боковых цепей щетки (параметра m). Установлено, что в водном растворе изученных наносистем формируются преимущественно дискретные сферические наноструктуры, размеры которых определяются параметром m.
Установлено влияние природы растворителя (вода, диметилформамид и хлороформ) на морфологическую картину поверхности пленок, отлитых из соответствующих сред, содержащих “свободные” амфифильные молекулярные щетки графт-СП с фиксированной степенью полимеризации боковых цепей (m = 270): в пленке, отлитой из водного раствора, формируются дискретные сферические структуры, в пленке, отлитой из ДМФА, образуются изотропные мицеллы; в случае хлороформа наблюдаются фибриллы, заполненные сферическими структурами, образующие домены с преимущественной внутренней ориентацией.
Список литературы
Sheiko S.S., Sumerlin B.S., Matyjaszewski K. // Prog. Polym. Sci. 2008. V. 33. P. 759. https://doi.org/10.1016/j.progpolymsci.2008.05.001
Ilgach D.M., Meleshko T.K., Yakimansky A.V. // Polym. Sci. Ser. C. 2015. V. 57. № 1. P. 3. https://doi.org/10.1134/S181123821501004X
Tran T.-H., Nguyen C.T., Gonzalez-Fajardo L., Hargrove D., Song D., Deshmukh P., Mahajan L., Ndaya D., Lai L., Kasi R.M., Lu X. // Biomacromolecules. 2014. V. 15. P. 4363. https://doi.org/10.1021/bm5013822
Xie G., Martinez M.R., Olszewski M., Sheiko S.S., Matyjaszewski K. // Biomacromolecules. 2019. V. 20. P. 27. https://doi.org/10.1021/acs.biomac.8b01171
Pelras T., Mahon C.S., Müllner M.// Angew. Chemie Int. Ed. 2018. V. 57. P. 6982. https://doi.org/10.1002/anie.201711878
Ivanov I.V., Meleshko T.K., Kashina A.V., Yakimansky A.V. // Russ. Chem. Rev. 2019. V. 88. P. 1248. https://doi.org/10.1070/rcr4870
Yakimansky A.V., Meleshko T.K., Ilgach D.M., Bauman M.A., Anan’eva T.D., Klapshina L.G., Lermontova S.A., Balalaeva I.V., Douglas W.E .// J. Polym. Sci. Part A Polym. Chem. 2013. V. 51. № 20. P. 4267. https://doi.org/10.1002/pola.26846
Valueva S.V., Gasilova E.R., Meleshko T.K., Vylegzhanina M.E., Borovikova L.N., Yakimansky A.V. / Collection of materials of the V interdisciplinary scientific forum with international participation “New materials and promising technologies”. Moscow. 2019. V. 1. P. 468.
Валуева С.В., Боровикова Л.Н., Суханова Т.Е., Вылегжанина М.Э. // Статья в сборнике трудов VII Международной научно-практической конференции “Актуальные достижения европейской науки-2011”. София, Болгария. 2011. С. 13.
Валуева С.В., Боровикова Л.Н., Коренева В.В. и др. // Журн. физ. химии. 2007. Т. 81. № 1. С. 1329. ISSN: 0044-4537.
Валуева С.В., Азизбекян С.Г., Кучинский М.П. и др. // Нанотехника. 2012. № 4(32). С. 53.
Валуева С.В., Вылегжанина М.Э., Плющенко А.В. // Поверхность. Рентген., синхротр. и нейтрон. исслед. 2019. № 7. С. 27. ISSN: 1028-0960. DOI (Valueva S.V., Vylegzhanina M.E., Plyushchenko A.V. // ISSN 1027-4510, J. Surf. Investigation.: X-ray, Synchrotron Neutron Tech. 2019. V. 13. № 4. P. 586. https://doi.org/10.1134/S1027451019040177).https://doi.org/10.1134/S0207352819070175
Meleshko T.K., Ivanov I.V., Kashina A.V., Bogorad N.N., Simonova M.A., Zakharova N.V., Filippov A.P., Yakimansky A.V. // Polym. Sci. Ser. B. 2018. V. 60. № 1. P. 35. https://doi.org/10.1134/S1560090418010098
Meleshko T.K., Il’gach D.M., Bogorad N.N., Kukarkina N.V., Yakimansky A.V. // Polym. Sci. Ser. B. 2014. V. 56. № 2. P. 118. https://doi.org/10.1134/S1560090414020110
Бусев А.И. Колориметрические (фотометрические) методы определения неметаллов. М.: Изд-во иностранной литературы, 1963. 467 с.
Валуева С.В., Вылегжанина М.Э., Суханова Т.Е. // сборник статей XXV Международной научно-практической конференции “Фундаментальные и прикладные научные исследования: актуальные вопросы, достижения и инновации”, Пенза МЦНС “Наука и просвещение”. 2019. Часть 1. С. 13.
Kamat P.V. // J. Physical Chemistry B. 2002. V. 106. P. 7729.
Филиппов А.П., Беляева Е.В., Красова А.С. и др. // ВМС. Сер. А. 2014. Т. 56. № 4. С. 359.
Дополнительные материалы отсутствуют.
Инструменты
Поверхность. Рентгеновские, синхротронные и нейтронные исследования