Радиационная биология. Радиоэкология, 2019, T. 59, № 5, стр. 546-552
РОЛЬ ПРИРОДНЫХ ОРГАНИЧЕСКИХ ВЕЩЕСТВ В МИГРАЦИОННЫХ ПРОЦЕССАХ ТРИТИЯ
М. Я. Чеботина 1, *, Е. В. Поляков 2, В. П. Гусева 1
1 Институт экологии растений и животных УрО РАН
Екатеринбург, Россия
2 Институт химии твердого тела УрО РАН
Екатеринбург, Россия
* E-mail: Chebotina@ipae.uran.ru
Поступила в редакцию 31.05.2019
Аннотация
Приводятся данные о сорбции трития природной гуминовой кислотой в условиях лабораторного эксперимента. Установлено, что величина сорбции трития гуминовой кислотой зависит от времени экспозиции и концентрации кислоты в растворе. Полученные в эксперименте коэффициенты распределения радионуклида между кислотой и водной средой свидетельствуют о наличии изотопного эффекта при связывании кислотой трития и протия. Обсуждаются данные лабораторных экспериментов о вертикальной миграции трития в грунтах водоема-охладителя Белоярской АЭС в зависимости от температуры водной среды и времени взаимодействия. Показано, что примерно 10% трития входит в состав органического вещества грунта, остальная часть радионуклида перемещается в грунте в составе капиллярной и адсорбированной форм влаги.
Роль органического вещества в естественных водоемах заключается не только в обеспечении существования разнообразных жизненных форм организмов и интенсивности их биологической деятельности, но и в круговороте химических элементов в системе “вода–грунт–биота”. Природные органические вещества включают в себя гумусовые кислоты (гуминовые и фульвокислоты), неспецифические органические соединения, разлагающиеся остатки отмерших растений и животных и др. [1, 2]. Показано, что органические вещества, с одной стороны, хорошо накапливают значительную часть химических элементов, концентрируя их в твердой фазе органогенных пород (почв, сапропелей, торфов, горючих сланцев, углей и пр.) [3–5], а с другой – их растворимая компонента при определенных условиях среды способствует мобилизации микроколичеств редких и рассеянных элементов, переводя их в миграционное состояние [6, 7].
К настоящему времени изучение роли органического вещества в связывании трития касается в основном почвы и биоты [8–10], данные же о сорбции радионуклида природной гуминовой кислотой, являющейся важной составляющей органического вещества, в литературе отсутствуют. Исследование этой проблемы важно для оценки миграционной способности трития и возможных способов очистки природных сред, загрязненных радионуклидом.
Цель настоящей работы: 1 – изучить сорбцию трития природной гуминовой кислотой из водного раствора при разной ее концентрации и продолжительности эксперимента; 2 – исследовать вертикальную миграцию трития в водных грунтах, содержащих органическое вещество, при разных температурных условиях.
МАТЕРИАЛЫ И МЕТОДИКА
Материалом исследования служили дистиллированная вода, природная гуминовая кислота, два типа водного грунта (илистый сапропель и затопленная почва) Белоярского водохранилища и радионуклид тритий. Последний использовался в виде тритиевой воды (НТО), которая в исходном растворе содержала 0.1 МБк/л трития. Работу проводили на Биофизической станции Института экологии растений и животных УрО РАН. Было проведено несколько лабораторных опытов. В одном из них изучали сорбцию трития природной гуминовой кислотой в диапазоне концентраций от 0.02 до 0.18 мг/мл при времени взаимодействия 100 и 270 сут. Гуминовая кислота получена из подземной скважины № 36–РЭ г. Салехарда Тюменской области. Вода, содержащая гуминовую кислоту, гидрокарбонатно-хлоридно-натриевая слабоминерализованная. Концентрация гуминовой кислоты в воде составляла 850–990 мг/л, содержание нейтральных битумов <1.9 мг/л, кислых битумов <0.4 мг/л. При изучении сорбции трития гуминовой кислотой в стеклянные колбы с притертыми пробками наливали по 250 мл тритиевой воды, из них отбирали пробы для определения концентрации радионуклида. В зависимости от варианта опыта в сосуды добавляли по 5, 15 и 45 мл воды, содержащей гуминовую кислоту, что создавало ее концентрацию в растворе 0.02, 0.06 и 0.18 мг/мл соответственно. Контрольный вариант оставляли без гуминовой кислоты. В процессе проведения опыта из каждого экспериментального сосуда отбирали аликвоту раствора (10 мл) и осаждали гуминовую кислоту добавлением 200 мкг HCl с концентрацией 16 моль/л. Осадок гуминовой кислоты отделяли от раствора путем фильтрования через фильтр “синяя лента”. В контрольном растворе также добавляли аналогичный объем HCl с целью учета гашения трития от внесения кислоты. После отделения гуминовой кислоты из прозрачных растворов отбирали пробы по 1 мл в специальные флаконы для определения концентрации трития. Поглощение трития гуминовой кислотой определяли по разнице содержания радионуклида в растворе без добавления гуминовой кислоты и растворах с разной концентрацией гуминовой кислоты после ее осаждения. Коэффициенты распределения (КР) рассчитывали как отношение содержания радионуклида в гуминовой кислоте (имп/мин/мг) к его содержанию в воде (имп/мин/мл). Этот параметр использовали для интерпретации величины изотопного эффекта (тритий–протий), которые находятся в обратной зависимости: чем ниже КР, тем выше изотопный эффект.
Во второй серии опытов изучали вертикальную миграцию трития в грунтах Белоярского водохранилища. Для этой цели использовали стеклянные цилиндры высотой 23 см и диаметром 3.5 см. Исследовали переход радионуклида в грунт из водного раствора и из грунта в водную среду. В первом случае увлажненный грунт помещали на дно экспериментального сосуда, уплотняя его таким образом, чтобы исключить образование в нем воздушных прослоек, после чего сверху осторожно заливали раствор, содержащий тритий. Во втором случае на дно сосуда через воронку с удлиненным кончиком заливали раствор, содержащий тритий, таким образом, чтобы стенки верхней части сосуда не загрязнялись радионуклидом. После этого через воронку на дно засыпали сухой грунт до уровня меченного тритием раствора, затем сверху заливали чистую дистиллированную воду. Высота слоя грунта и воды была одинакова и составляла 10 см. Сосуды плотно закрывали пробками. В опытах с различной температурой воды экспериментальные сосуды разделяли на три партии, каждую из которых размещали в холодильнике (t = 4°С), на лабораторном столе (t = 17°С) и в термостате (t = 42°С). Продолжительность опытов варьировала от 0.5 до 3 лет. Из сосудов периодически отбирали пробы свободной воды, находящейся над грунтом.
Для исследования распределения трития в различных категориях влаги и органическом веществе грунта сосуды, заполненные грунтом и водой, меченной тритием, готовили как указано выше и выдерживали при температуре +4°С в течение 256 сут. Через определенные промежутки времени часть опытов разбирали: воду сливали, грунт полностью извлекали из сосудов и выделяли из него капиллярную и адсорбционную формы влаги. Для выделения капиллярной влаги навески грунта центрифугировали в пробирках с сетчатым дном на центрифуге ЦЛС-3 при скорости 5000 об/мин. Адсорбционную влагу отделяли путем отгонки в специальной печи при температуре 105°С. Органически связанный тритий определяли путем сжигания грунта при 600°С в той же печи с последующим улавливанием радионуклида после прохождения через систему охлаждения.
Для радиометрии пробы трития (1 мл) помещали в специальные пузырьки из бескалиевого стекла, куда добавляли по 10 мл сцинтилляционной жидкости ЖС-8. Тщательно закрытые пузырьки помещали в гнезда счетчика на 1 сут для стабилизации. Пробы в двух повторностях просчитывали по 2–3 раза на установке “Дельта-300” (США) и определяли концентрацию трития в относительных единицах (имп/мин/мл).
РЕЗУЛЬТАТЫ
На рис. 1 представлены полученные в эксперименте данные о распределении трития в системе “вода–гуминовая кислота” в зависимости от концентрации кислоты и времени экспозиции. Видно, что гуминовая кислота накапливает тритий из воды с КР < 1. Последнее свидетельствует о том, что при взаимодействии меченной тритием воды с гуминовой кислотой вследствие процессов изотопного обмена водорода происходит изотопное разбавление индикатора – трития.
Рис. 1.
Коэффициенты распределения трития в системе “вода–гуминовая кислота” в зависимости от времени экспозиции и концентрации гуминовой кислоты.
Fig. 1. Distribution coefficients of tritium in the “wate–humic acid” system depending on the exposure time and concentration of humic acid.
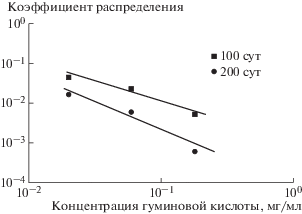
Данные рисунка свидетельствуют об увеличении изотопного эффекта с увеличением концентрации гуминовой кислоты. В частности, при изменении концентрации гуминовой кислоты от 0.02 до 0.18 мг/мл и экспозиции 100 сут КР снижается почти на порядок величин (от 0.046 до 0.005 соответственно), а при экспозиции 270 сут он снижается примерно в 27 раз (от 0.016 до 0.0006). Из рисунка также видно, что изотопный эффект зависит от времени экспозиции: для всех трех концентраций гуминовой кислоты и экспозиции 270 сут он больше, чем при 100-суточной экспозиции, о чем говорят более низкие значения КР в первом случае по сравнению со вторым.
Результаты проведенного эксперимента показали, что при концентрации гуминовой кислоты в растворе 0.18 мг/мл и длительности эксперимента 100 сут в состав гуминовой кислоты вошло ~20% трития, остальные ~80% радионуклида осталось в водной среде. При экспозиции 270 сут при той же концентрации гуминовой кислоты относительное содержание трития в гуминовой кислоте снизилось до 3%, при этом ~97% радионуклида оказалось в воде. По нашим предположениям, снижение содержания трития в гуминовой кислоте к окончанию эксперимента (270 сут) связано с ее нестабильностью во времени, в результате чего при воздействии соляной кислоты в момент осаждения гуминовой кислоты образуются низкомолекулярные фрагменты, уносящие тритий в анализируемый раствор. Однако это предположение требует дальнейшего исследования.
Во второй серии опытов исследовали вертикальную миграцию трития в водном грунте при различной температуре. Этот опыт моделировал условия водоема-охладителя, куда систематически поступают слаборадиоактивные стоки Белоярской АЭС, содержащие тритий [11], и где температура воды может изменяться от 4 до 30°С. Предполагается, что при сбросе повышенных концентраций трития в воду Белоярского водохранилища радионуклид мигрирует в глубь грунта, а при снижении содержания трития в воде он снова переходит из грунта в водную среду.
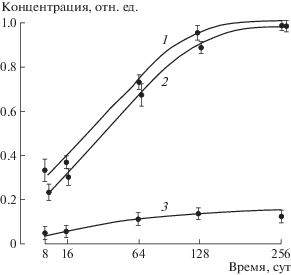
В первом эксперименте изучали содержание трития в различных категориях влаги и органическом веществе илистого сапропеля, при этом тритиевая метка помещалась в столб воды над грунтом. Поскольку со временем содержание радионуклида в воде над грунтом снижалось, это свидетельствовало о его миграции вниз колонки. При этом было установлено, что в процессе миграции тритий входит в различные категории влаги, а также в органическое вещество грунта. Как видно из рис. 2, основная часть радионуклида в данном грунте находится в капиллярной и адсорбированной формах влаги, которые по концентрации трития практически не различаются. Более 10% трития за время эксперимента вошло в состав органического вещества. Равновесное распределение радионуклида в системе “вода–грунт” установилось примерно в течение 8.5 мес. Наблюдение, проведенное через 3 года, показало, что за это время распределение трития между свободной водой, категориями влаги в грунте и органическим веществом практически не изменилось.
Рис. 2.
Изменение относительной концентрации трития в различных категориях влаги и органическом веществе илистого сапропеля при разном времени экспозиции: 1 – капиллярная влага; 2 – адсорбционная влага; 3 – органическое вещество.
Fig. 2. The change in the relative concentration of tritium in different categories of moisture and organic matter of silty sapropel at different exposure times: 1 – capillary moisture; 2 – adsorption moisture; 3 – organic matter.
В связи с вариабельностью температуры в водоеме-охладителе в лабораторном эксперименте было исследовано влияние температурного фактора на переход трития из воды в грунт и из грунта в водную среду. В работе использовали два типа грунта – илистый сапропель и затопленную почву. Первый из них имеет темно-серый цвет и содержит >90% органического вещества. Затопленная почва представляет собой грунт, сформировавшийся в процессе затопления почвы угодий и ее заиления с момента образования водоема-охладителя.
На рис. 3 и 4 в отн. ед. представлены данные эксперимента в диапазоне температур от 4 до 42°С. Видно, что процесс выравнивания концентраций трития в системе “вода–грунт” в обоих экспериментах состоит из двух стадий. На первой стадии продолжительностью до 80–100 сут вертикальная миграция радионуклида возрастает с увеличением температуры. На второй стадии (100–365 сут) процесс перехода практически не зависит от температуры. При этом кривые выходят на плато, что свидетельствует об установлении равновесия по тритию между водой и грунтом.
Рис. 3.
Переход трития из воды в грунт в зависимости от температуры водной среды: 1 – 4°С; 2 – 17; 3 – 42°С. а – затопленная почва; б – илистый сапропель.
Fig. 3. The transition of tritium from water to soil, depending on the temperature of the aquatic environment: 1 – 4°C; 2 – 17°C; 3 – 42°C. a – flooded soil; b – silt sapropel.
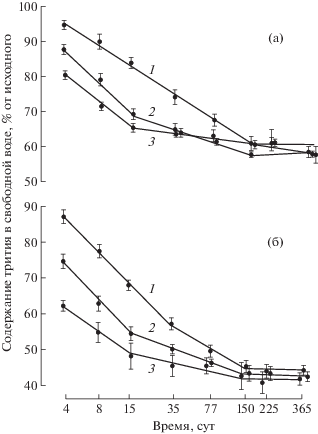
Рис. 4.
Переход трития из грунта в водную среду в зависимости от температуры: 1 – 4°С; 2 – 17; 3 – 42°С. а – затопленная почва; б – илистый сапропель.
Fig. 4. Transition of tritium from the soil to the aquatic environment, depending on temperature: 1 – 4°C; 2 – 17°C; 3 – 42°C. a – flooded soil; b – silt sapropel
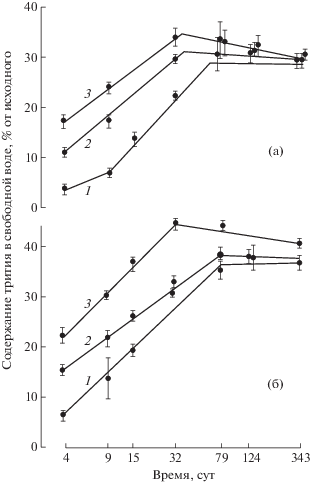
Из рис. 3 и 4 видно, что в равновесных условиях в опытах по сорбции трития грунтами из воды в илистый грунт переходит ~58% радионуклида, а в затопленную почву ~40% от его общего содержания (рис. 3). При десорбции в конце опыта ~60–70% трития остается в грунте и 30–40% переходит в свободную воду над грунтом (рис. 4).
Можно предположить, что миграция трития в вертикальном профиле грунта происходит за счет быстрой диффузии радионуклида в капиллярной и адсорбированной влаге, которая зависит от температуры, и медленного процесса взаимодействия радионуклида с ионообменным водородом органического вещества грунта, не зависящего или слабо зависящего от температурных условий. Весь процесс можно представить в виде решений двух уравнений:
уравнение второго закона Фика (диффузия трития в воде)
Расчет показал, что коэффициенты диффузии трития возрастают с повышением температуры водной среды (таблица 1) и не зависят от направления диффузии. Для илистого сапропеля они выше, чем для затопленной почвы. Илистый грунт характеризуется более высоким содержанием илистых частиц и большей обводненностью, поэтому сопротивление диффузии в нем меньше, чем в затопленной почве.
Таблица 1.
Зависимость коэффициентов диффузии трития от температуры Table 1. The dependence of the diffusion coefficients of tritium on temperature
| Тип грунта | Температура, °С | D, n × 10–5 см2/сек |
|---|---|---|
| Затопленная почва | 4 | 0.45 |
| 17 | 0.78 | |
| 42 | 1.96 | |
| Илистый сапропель | 4 | 1.2 |
| 17 | 2.2 | |
| 42 | 5.7 |
ОБСУЖДЕНИЕ
В условиях лабораторного эксперимента впервые установлена способность природной гуминовой кислоты связывать тритий, находящийся в водном растворе в виде тритиевой воды. При этом показано, что тритий сорбируется кислотой с КР < 1, что свидетельствует о наличии изотопного эффекта, т.е. дискриминации трития относительно протия. Наблюдаемый эффект обусловлен различиями в физических и химических свойствах изотопов водорода [12, 13]. В частности, установлено, что константы скоростей реакций различаются для аналогичных соединений, меченных и не меченных тритием [14]. Внедрение трития в биологические структуры, с одной стороны, дискриминируется, а с другой – инкорпорированный в соединения тритий удерживается дольше, чем немеченые соединения (цит. по [15]).
Установлено, что в условиях эксперимента изотопный эффект в системе “гуминовая кислота–тритиевая вода” увеличивался с возрастанием концентрации гуминовой кислоты (в интервале концентраций от 0.02 до 0.18 мг/мл) и времени экспозиции (от 100 до 270 сут).
В порядке обсуждения полученных данных следует подчеркнуть, что в ряде работ при изучении поглощения трития биологическими объектами (гидробионтами из природных водоемов и выращенными в лаборатории при различных условиях культивирования, а также другими живыми организмами) производилась оценка распределения радионуклида между органическим веществом тканей (ОВТ) и свободной тканевой водой (СТВ) [16–19] и др.]. В целом приведенные в работах результаты подтверждают наличие изотопного эффекта при поглощении трития органическим веществом тканей (ОВТ/СТВ < 1), который проявляется преимущественно для водных объектов [16]. Однако в ряде случаев, особенно для наземных растений и продуктов питания, наблюдался обратный эффект – повышенное содержание трития в органическом веществе по сравнению со свободной тканевой водой (ОВТ/СТВ > 1). С нашей точки зрения, случаи повышенного накопления трития в органическом веществе тканей можно объяснить рядом причин: временем экспозиции объекта в тритиевой воде, флуктуациями концентраций трития в воде, особенно в районах поступления радионуклида от предприятий ЯТЦ и испытаний ядерного оружия, атмосферными выпадениями, сезонными вариациями, химической формой соединений трития, источниками поступления трития в биоту (вода, осадки, пища), методическими особенностями эксперимента и другими причинами.
В опытах по исследованию вертикальной миграции трития в водных грунтах, содержащих органическое вещество, показано, что основная часть трития передвигается в грунте в составе капиллярной и адсорбционной форм влаги, при этом скорость диффузии увеличивается с возрастанием температуры водной среды. Примерно 10% трития входит в состав органического вещества грунта. В условиях эксперимента равновесное распределение трития в системе “свободная вода–органическое вещество грунта” устанавливается примерно в течение 1.5–4 мес. от начала эксперимента. Зависимость скорости вхождения радионуклида в состав органического вещества грунта от температуры водной среды в данной работе не установлена и требует дальнейшего исследования. По результатам экспериментов по сорбции трития гуминовой кислотой получен патент на изобретение № 2680507.
Список литературы
Орлов Д.С. Химия почв. M.: МГУ, 1985. 376 с. [Orlov D.S. Himiya pochv. M.: MGU, 1985. 376 s. (In Russian)]
Шоба В.Н., Чудненко К.В. Ионообменные свойства гумусовых кислот // Почвоведение. 2014. № 8. С. 921–931. [Shoba V.N., Chudnenko K.V. Ionoobmennye svojstva gumusovyh kislot // Pochvovedenie. 2014. № 8. S. 921–931. (In Russian)]
Потапова И.А., Вишняков В.В., Пурыгин П.П. и др. Выделение гуминовых кислот из бурых углей и их применение для рекультивации нефтезагрязненных земель // Изв. Самарского науч. центра РАН. Спец. вып. ХIII конгр. “Экология и здоровье человека”. 2008. Т. 1. С. 215–218. [Potapova I.A., Vishnyakov V.V., Purigin P.P., Simakova S.A., Vorob’ov L.V. Vydelenie guminovyh kislot iz buryh uglej i ih primenenie dlya rekultivacii neftezagryaznennyh zemel // Izvestiya Samarskogo nauch. centra RAN. Specialnyj vypusk. HSH kongress ”Ehkologiya i zdorove cheloveka“. Rep. Samara Sci. Center of RAS. Special issue. Of the XIII Congress “Ecology and Health”. 2008. V. 1. S. 215–218. (In Russian)]
Водяницкий Ю.Н. Тяжелые и сверхтяжелые металлы в загрязненных почвах. М.: ГНУ Почвенный институт им. Докучаева, 2008. 95 с. [Vodjanitski Yu.N. Tyazhelye i sverhtyazhelye metally v zagryaznennyh pochvah . M.: GNU Pochvennyj institut im. Dokuchaeva, 2008. 95 s. (In Russian)]
Перминова И.В. Гуминовые вещества – вызов химикам XXI века // Химия и жизнь. 2008. № 1. С. 50–56. [Perminova I.V. Guminovye veshchestva – vyzov himikam XXI veka // Himiya i zhizn. 2008. № 1. S. 50–56. (In Russian)]
Моисеенко Т.И., Дину М.И., Гашкина Н.А., Кремлева Т.А. Формы нахождения металлов в природных водах и их комплексообразование с гуминовым веществом // ДАН. 2012. Т. 442. № 5. С. 691–685. [Moiseenko T.I., Dinu M.I., Gashkina N.A., Kremleva T.A. Formy nahozhdeniya metallov v prirodnyh vodah i ih kompleksoobrazovanie s guminovym veshchestvom // DAN. 2012. V. 442. № 5. S. 691–685. (In Russian)]
Чеботина М.Я., Поляков Е.В., Гусева В.П. и др. Влияние растворимой гуминовой кислоты на коэффициенты распределения химических элементов в системе вода–планктон // Водное хозяйство России. 2015. № 5. С. 94–102. [Chebotina M.Y., Polyakov E.V., Guseva V.P., Volkov I.V., Khlebnikov N.A. Vliyanie rastvorimoj guminovoj kisloty na koehfficienty raspredeleniya himicheskih ehlementov v sisteme voda–plankton // Vodnoe hozyajstvo Rossii. 2015. № 5. S. 94–102. (In Russian)]
Qin Zhanga, Lin Dua, Zhong-qin Daid et al. Studies of particle size distribution of non-exchangeable organically bound tritium activities in the soil around Qinshan Nuclear Power Plant // J. Envir. Radioact. 2018. V. 192. P. 362–387.
Eyrollea F., Ducrosa L., Le Dizèsa S. et al. An updated review on tritium in the environment // J. Environ. Radioact. 2018. V. 181. P. 128–137.
Renard H., Maro D., Le Dizes S. et al. Tritium forms discrimination in ryegrass under constant tritium exposure: From seed germination to seedling autotrophy // J. Environ. Radioact. 2017. V. 177. P. 194–205.
Чеботина М.Я. Тритий в воде Белоярского водохранилища в период работы трех энергоблоков АЭС // Водное хозяйство России. 2010. № 4. С. 58–73. [Chebotina M.Ya. Tritij v vode Beloyarskogo vodohranilishcha v period raboty trekh ehnergoblokov AEHS // Vodnoe hozyajstvo Rossii. 2010. № 4. S. 58–73. (In Russian)]
Дерпгольц В.Ф. Мир воды. Л.: Недра, 1979. С. 27. [Derpgol’c V.F. Mir vody. L.: Nedra, 1979. S. 27. (In Russian)]
Jones W.M. Vapor pressures of tritium oxide and deuterium oxide. Interpretation of isotope effect // J. Chem. Phys. 1968. V. 48. P. 207.
Weston R.E. Kinetic and equilibrium isotope effects of tritium substitution // Tritium (Eds A.A. Moghissi, M.W. Carter.). CONF 710809, Messenger Graphics, Phoenix, AZ and Los Vegas. NV, 1973. P. 289.
Рачинский В.В., Ленский Л.А. Исследование взаимодействия меченой тритием воды с почвами. Сообщение 1 // Изв. ТСХА. 1965. Вып. 1. С. 133–144. [Rachinskyi V.V., Lenskyi L.A. Issledovanie vzaimodejstviya mechenoj tritiem vody s pochvami. Soobshchenie 1 // Izv. TSKHA. 1965. № 1. S. 133–144. (In Russian)]
Le Goff P., Fromm M., Vichot L. et al. Isotopic fractionation of tritium in biological systems // Environ. Int. 2014. V. 65. P. 116–126.
Boyer C., Vichot L., Fromm M. et al. Tritium in plants: A review of current knowledge // Environ. Experim. Bot. 2009. V. 67. P. 34–51.
Krištof R., Košenina S., Zorko B., Kožar Logar J. Tritium in organic matter around Krsˇko Nuclear Power Plant // J. Radioanal. Nucl. Chem. 2017. V. 314. P. 675–679.
Jean-Baptiste P., Fourre E., Baumier D., Dapoigny A. Environmental OBT/TFWT revisited // Fusion Sci. Technol. 2011. V. 60. P. 1248–1251.
Дополнительные материалы отсутствуют.
Инструменты
Радиационная биология. Радиоэкология


