Радиотехника и электроника, 2021, T. 66, № 11, стр. 1125-1132
Влияние финишной обработки поверхности GaAs на свойства границ раздела Au–GaAs
Т. А. Брянцева a, *, Ю. В. Гуляев b, В. Е. Любченко a, И. А. Марков a, Ю. А. Тен a
a Фрязинский филиал Института радиотехники и электроники им. В.А. Котельникова РАН
141120 Фрязино, Московской обл., пл. Введенского, 1, Российская Федерация
b Институт радиотехники и электроники им. В.А. Котельникова РАН
125009 Москва, ул. Моховая 11, корп. 7, Российская Федерация
* E-mail: bryantseva44@mail.ru
Поступила в редакцию 04.02.2021
После доработки 17.05.2021
Принята к публикации 21.06.2021
Аннотация
Исследована поверхность GaAs в зависимости от способов предэпитаксиальной обработки. Показано, что известные методы обработки поверхности с применением кислотных или щелочных травителей с последующим отжигом в вакуумной камере приводят к различным результатам по составу приповерхностного слоя. Обнаружено, что большую роль при финишной отмывке GaAs играют физико-химические свойства воды на стадии нейтрализации травящего раствора. При этом из оставшихся капель на поверхности GaAs на стадии высушивания может выпадать либо тонкий слой оксида GaAs (при использовании деионизованной воды), либо слой перекристаллизованного GaAs (при использовании безреагентно модифицированной воды).
ВВЕДЕНИЕ
Процесс формирования тонкопленочных структур Au-GaAs путем испарения золота в вакууме является одним из широко используемых методов получения выпрямляющих и невыпрямляющих контактов при создании приборов на основе GaAs [1]. Изготовление полупроводниковых приборов на основе GaAs потребовало существенной проработки и решения вопросов взаимодействия поверхности полупроводника с окружающей средой на различных этапах изготовления и использования. Эти же технологии используются и при создании микрополосковых антенн и интегральных схем СВЧ на основе GaAs [2]. При создании планарной логопериодической антенны, например, необходимо получение однородного слоя золота довольно большой площади с минимальными токами утечек и стабильными в работе.
Вместе с тем осаждение пленок металла, как известно, приводит к заметным изменениям структуры и состава самого приповерхностного слоя GaAs [3–6].
Установлено, что при осаждении Au на поверхность GaAs на границе Au-GaAs формируется слой, включающий в себя помимо золота Ga и As.
Источником Ga и As является приповерхностный слой исходного GaAs [4–6], вследствие чего граница металл-полупроводник оказывается в области температур, близких к температуре кристаллизации и/или плавления.
Чтобы добиться требуемых условий формирования границ раздела контактов металл-арсенид галлия применяются различные методы предэпитаксиальной обработки поверхности GaAs. Непременным этапом осаждения пленок, как правило, является предварительная очистка поверхности подложки. Иногда требуется шлифовка, полировка, удаление приповерхностного слоя с помощью химического травления, для чего используются специальные кислотные или щелочные растворы [7]. К методам предэпитаксиальной подготовки поверхности относятся и способы специального конструирования поверхности с заданными свойствами [8–12].
Естественно предположить, что процессы финишной отмывки поверхности GaAs, в том числе в деионизованной воде, так же как и способы ее высушивания, перед осаждением металла играют значительную роль в формировании границ раздела металл–полупроводник.
С этой целью исследовалась возможность использования финишной отмывки поверхности GaAs с применением безреагентно модифицированной воды (БМВ) [13, 14].
1. МЕТОДИКА И ТЕХНИКА ЭКСПЕРИМЕНТА
Исследования поверхности GaAs проводились с использованием как пластин толщиной ~300 мкм полуизолирующего арсенида галлия с нанесенными предварительно встречно-штыревыми контактами из алюминия, так и транзисторных структур GaAs: эпитаксиально выращенные пленки GaAs с концентрацией электронов n ~ 9.7 × 1016 см–3, толщиной ~0.3 мкм на сильно легированной подложке с n ~ 1018 см–3. Использовались также пленки GaAs с n ~ (1014–1017) см–3, выращенные на пластинках из полуизолирующего арсенида галлия.
Поверхность образцов исследовали после промывания как в изопропиловом спирте, так и в концентрированном растворе соляной кислоты, и в 7 H2SO4 : 1 H2O2 : 1 H2O с дальнейшим промыванием в воде. При этом была использована деионизованная, и/или БМВ, подверженная предварительно воздействию физических полей. Состояние поверхности (100) GaAs изучали как с помощью дифракции быстрых электронов (ДБЭ), так и оже-спектроскопии. Применялись также методы тонкого химического анализа с использованием метода калориметрии и ПАВ-диагностики [4, 15, 16].
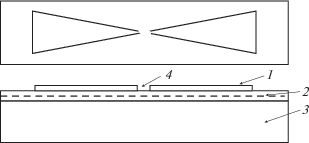
С целью создания контактов металл–полупроводник на поверхность (100) GaAs наносили пленки золота путем испарения в вакууме (порядка 10–7 Тор). Осаждение Au производили через трафарет, выполненный из тонкой пластинки вольфрама либо в виде двух полосок с расстояниями между ними 3 мм, либо в виде планарных логопериодических антенн (рис. 1).
Рис. 1.
Микрополосковая антенна: пленка золота на поверхности эпитаксиальной n – i-структуры из арсенида галлия: 1 – контактный слой Au; 2 – пленка n‑GaAs с обедненным слоем; 3 – подложка из i-GaAs, 4 – зазор между контактами.
Электрофизические свойства контактов определяли путем измерения поверхностного сопротивления и вольт-амперных характеристик (ВАХ). В случае изготовления логопериодических антенн сопротивление образцов измеряли между ближайщими выступами на лепестках антенны.
2. ЭКСПЕРИМЕНТАЛЬНЫЕ ДАННЫЕ И ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
2.1. Взаимодействие поверхности GaAs с окружающей средой
Природный слой оксида на (100) GaAs. Природный слой оксида, образующийся на поверхности пленок GaAs сразу после роста и выдержки на воздухе в течение 2–3 часов, как известно, является сложным комплексным соединением. В состав слоя оксида помимо галлия и мышьяка входят углерод и кислород. Так, например, с помощью оже-спектроскопии обнаружено, что в состав приповерхностного слоя (100) GaAs с n ~ 1018 см–3 еще до осаждения золота входят такие элементы как O (14.2 ат. %), С (20.3 ат. %), Ga (30.2 ат. %), As (28.5 ат. %). Толщина слоя оксида достигает в среднем толщины 20…100 Å и зависит от условий роста пленок арсенида галлия и окружающей атмосферы. Затем поверхность GaAs пассивируется. Состав и толщина приповерхностного слоя зависят от способа предэпитаксиальной обработки перед осаждением пленок металла.
Диагностика поверхности GaAs на воздухе с помощью поверхностных акустических волн (ПАВ). С помощью ПАВ было исследовано изменение состояния поверхности (111) GaAs под воздействием света (белого) в зависимости от времени выдержки [4]. Поверхность образца промывали в изопропиловом спирте и выдерживали на воздухе под воздействием света лампы накаливания, расположенной на расстоянии 25 см от источника. Лампа накаливания, как известно, часто используется для высушивания поверхности образцов после финишной отмывки. Как показали исследования, зависимость скорости распространения ПАВ от времени облучения имеет ступенчатый характер.
Наблюдения дискретной зависимости ${{\Delta V} \mathord{\left/ {\vphantom {{\Delta V} V}} \right. \kern-0em} V}$ от времени облучения связано, по-видимому, с изменением состава слоя оксида. Этот факт подтверждается известными данными преобразования окисных слоев на поверхности GaAs, когда возможны следующие реакции превращения: ${\text{Ga}} + 4{\text{O}}{{{\text{H}}}^{ - }} = {\text{Ga}}({\text{OH}})_{4}^{ - } + 3{\text{e}}.$ При разложении гидрата ${\text{GaOOH}}$ при 300°С можно получить β-модификацию ${\text{G}}{{{\text{a}}}_{{\text{2}}}}{{{\text{O}}}_{{\text{3}}}}{\text{,}}$ при 400°С − ${\text{G}}{{{\text{a}}}_{{\text{2}}}}{{{\text{O}}}_{{\text{3}}}}$ α-модификации со структурой типа корунда [17]. При этом может меняться и проводимость окисных слоев. Известно, что ${\text{G}}{{{\text{a}}}_{{\text{2}}}}{{{\text{O}}}_{{\text{3}}}}$ обладает полупроводниковыми свойствами и под воздействием света может иметь электрическую проводимость, что естественно оказывает значительное влияние на поглощение ПАВ. Все эти окисные модификации метастабильны и переходят в устойчивую β-модификацию ${\text{G}}{{{\text{a}}}_{{\text{2}}}}{{{\text{O}}}_{{\text{3}}}}{\text{.}}$
Состав поверхности после химической обработки и отжига в вакууме. В то же время исследования поверхности GaAs с помощью ДБЭ после химической обработки и отжига при Т = 550°С показали для всех рассматриваемых образцов GaAs наличие кубической фазы GaAs. В некоторых случаях на электронограммах появлялись линии Кикучи. Это означает, что сразу же после травления на поверхности GaAs присутствует окисный слой, который затем после температурной обработки становится аморфным и прозрачным для электронов. Причем его состав определяется способом обработки поверхности, в частности, зависит от состава кислотного травителя. Состав приповерхностного слоя в этом случае, как будет показано ниже, зависит от способа роста GaAs и концентрации электронов.
2.2. Состояние (100) GaAs после осаждения Au
Следует отметить, что при эффективной толщине d ~ 10 Å пленка Au не сплошная и часть поверхности GaAs свободна от островков золота. В табл. 1 приведены данные по структуре и составу поверхности вне участков, покрытых Au.
Таблица 1.
Реконструкция поверхности GaAs с Au d ~ 10 Å в зависимости от способа предварительной отработки, концентрации электронов n и температуры подложки Tп во время осаждения
| n, cм–3 | Химическая обработка |
Нагрев (отжиг*) | Tп, °C | Реконструкция | |
|---|---|---|---|---|---|
| тип | особенности | ||||
| 1016 | 7H2SO4 : 1H2O2 : 1H2O | Отжиг, остывание 5 мин | 200 | 1 | – |
| 1016 | 7H2SO4 : 1H2O2 : 1H2O | Отжиг, остывание 5 мин, нагрев перед осаждением при 200°C, 20 мин | 200 | 2 | – |
| 1014…1017 | 7H2SO4 : 1H2O2 : 1H2O | Отжиг, остывание 20 мин | 50 | 2 | На электронограммах также рефлексы от Ga2O3 δ- и γ-модификаций |
| 1014…1018 | 7H2SO4 : 1H2O2 : 1H2O | Без отжига или нагрева | 20 | 3 | – |
| 1014 | HCl | Отжиг, остывание 20 мин | 50 | 1 | – |
| 1016…1017 | HCl | Отжиг, остывание 20 мин | 50 | 2 | На электронограммах сильный некогерентный фон + рефлексы от Ga2O3 α- и β-модификаций |
| 1016 | HCl | Отжиг, остывание 5 мин | 200 | 2 | На электронограммах рефлексы от δ-Ga2O3 |
| 1014…1017 | HCl | Без отжига или нагрева | 20 | 2 или 3 | На электронограммах рефлексы от Ga2O3 α- и β-модификаций |
При исследованиях с помощью ДБЭ отмечаются три различных типа структуры поверхности (100) GaAs:
тип 1 – образование дефектного монокристаллического слоя: на электронограммах двойные рефлексы кубической фазы GaAs и рефлексы, характерные для гексагональной фазы GaAs с характерным размером межплоскостного расстояния d ~ 3.5 Å;
тип 2 – появление поликристаллической или текстурированной фазы GaAs (возможно с гексагональной структурой);
тип 3 – образование слоя GaAs с мозаичной монокристаллической структурой – видны четко выраженные пятна GaAs.
Тип реконструкции зависит от способа подготовки поверхности, поскольку толщина и плотность окисного слоя зависят от состава травителя.
К примеру, после отработки в растворе H2SO4 может образоваться рыхлый аморфный слой Ga2O3⋅4/3SO3⋅3H2O, а после обработки в HCl образуются тонкий плотный окисел Ga2O3 и легколетучий окисел As2O3. Отжиг перед осаждением, как правило, разрушает или удаляет окисную пленку, но при медленном охлаждении наличие остаточных газов может привести к образованию более плотного окисла. Под воздействием потока, осаждаемого Au, поверхность GaAs, свободная от загрязнений, становится дефектной. Наличие плотного окисла на поверхности GaAs приводит к образованию поликристаллической фазы, по-видимому, в соответствии с реакцией
Из табл. 1 видно, что структура и состав пленки Au с эффективной толщиной d ~ 10 Å определяются способом предварительной обработки GaAs. Так, монокристаллическая фаза Au становится превалирующей после обработки в растворе H2SO4, а после обработки в HCl преобладает поликристаллическая фаза Au. Окисный слой, образуемый остаточными газами вакуумной камеры, по-видимому, разрушается при осаждении Au, поэтому доля монокристаллической фазы становится заметной.
В табл. 2 приведены данные по содержанию элементов на поверхности (100) GaAs при осаждении золота с d ~ 10 Å в вакууме в зависимости от обработки в щелочном растворе и в изопропиловом спирте. Как видим, в состав приповерхностного слоя помимо золота входят Ga, As, С и О. Оказалось, что наибольшее количество кислорода обнаруживается на поверхности образцов, вообще не подверженных обработке, тогда как наибольшее количество углерода наблюдается после обработки в щелочном травителе. Наибольшее количество Au в процентном отношении при этом наблюдается в случае обработки в изопропиловом спирте. В случае без предварительной обработки образца количество Ga на поверхности наибольшее и превышает количество As.
Таблица 2.
Результаты исследования с помощью оже-спектроскопии состава поверхности (100) GaAs с n ~ 1018 см–3, покрытой пленкой Au d ~ 10 Å
| Способ обработки | Содержание элементов, ат. % | ||||
|---|---|---|---|---|---|
| Au | Ga | As | C | O | |
| Без обработки | 12.6 | 28.3 | 22.4 | 21.7 | 15.1 |
| В Na(OH)3 | 13.9 | 24.3 | 24.7 | 26 | 11.2 |
| В изопропиловом спирте | 31.1 | 19.4 | 14.6 | 24.5 | 10.4 |
Соотношение Ga : As ≈ 1 при обработке в щелочном травителе. При этом наименьшее количество Ga и As наблюдается при обработке поверхности в изопропиловом спирте и количество Ga превышает количество As.
Ниже приведен элементный состав поверхности арсенида галлия, покрытого слоем Au c d ~ 50 Å после предварительной обработки в соляной кислоте и отжига в вакууме:
Au (18.4 ат. %), O (12.3 ат. %), С (42.2 ат. %), Ga (19.2 ат. %), As (8.0 ат. %). Как видим, в состав поверхности входит галлий, количество которого превышает количество мышьяка, а содержание углерода превышает количество кислорода.
Вместе с тем из справочных данных следует, что GaAs стехиометрического состава устойчив к кислороду из воздуха и к парам воды до ~600°С, медленно реагирует с соляной кислотой с выделением арсина AsH3 [18]. Вследствие воздействия растворами щелочей разлагается. Галлий и мышьяк тоже медленно растворяются в воде и в соляной кислоте. Однако их оксиды и гидриды хорошо растворяются в воде и в кислоте, в частности в соляной кислоте. Следует отметить, что в случае добавления воды в кювету с раствором HCl для нейтрализации кислоты раствор резко разогревается до кипения (103°С).
2.3. Реакция взаимодействия соляной кислоты с арсенидом галлия
Анализ раствора HCl после взаимодействия с GaAs. С помощью метода калориметрии [15, 16] был проведен химический анализ на содержание Ga и As в природном слое оксида GaAs, уходящего в раствор концентрированной HCl после травления в течение 1 ч. Количество мышьяка в растворе менялось в зависимости от концентрации электронов в пленках и способов выращивания GaAs. Однако после отжига образцов при Т = 550°С количество галлия в кислотном растворе значительно увеличилось и превысило содержание мышьяка. В табл. 3 представлен состав по Ga и As, уходящих в раствор соляной кислоты.
Таблица 3.
Содержание Ga и As (мкг/см2) в растворе HCl по отношению к эталону (*)
| Способ получения образцов* | Концентрация электронов n в GaAs |
Ga | As |
|---|---|---|---|
| 1 | 8.6 × 1014 cм–3 (100) | Х.х. ** | 0.29 |
| 2 | 2.5 × 1014 cм–3 (111) | 1.3 | 0.22 |
| 3 | 1 × 1015 cм–3 (100) | 2.76 | 1.8 |
| 4 | Полуизолир. (100) | 1.44 | 3.65 |
* Образцы получены газотранспортным методом (1); образцы получены с помощью жидкофазной эпитаксии (2, 3); образцы были вырезаны из слитка, вырезанного методом Чохральского, поверхность образцов подвергалась шлифовке и полировке с использованием химико-динамического метода (4). ** Холостой ход определяли по растворению кусочка кристалла, отколотого от монокристалла GaAs, выращенного методом Чохральского.
Следует отметить, что продукты реакции взаимодействия поверхности GaAs с HCl при получении и росте эпитаксиальных пленок GaAs с использованием химических транспортных реакций с H2 в качестве газа-носителя [18] хорошо изучены. Взаимодействие арсенида галлия с соляной кислотой осуществляется по формуле
(1)
$\begin{gathered} 4{\text{GaAs}} + 4{\text{HCl}} \leftrightarrow \\ \leftrightarrow 4{\text{GaCl}} + 4{\text{As}} + 2{{{\text{H}}}_{{\text{2}}}}\,\,\left( {900 \to 759^\circ {\text{С}}} \right). \\ \end{gathered} $При этом GaAs получают в горячей зоне (900°С) по реакции
(2)
$2{\text{Ga}} + 2{\text{AsC}}{{{\text{l}}}_{3}} + 3{{{\text{H}}}_{2}} \leftrightarrow {\text{GaAs}} + 6{\text{HCl}}.$Используют также процесс при 700°С
(3)
${\text{Ga}}{{\left( {{{{\text{C}}}_{{\text{2}}}}{{{\text{H}}}_{{\text{5}}}}} \right)}_{3}} + {\text{As}}{{{\text{H}}}_{3}} \to {\text{GaAs}} + 3{{{\text{C}}}_{{\text{2}}}}{{{\text{H}}}_{{\text{6}}}}.$Нейтрализация раствора HCl деионизованной водой. Как известно, вода, в том числе и деионизованная, является хорошим растворителем полярных веществ (рН = 7.0) и при этом обладает высоким поверхностным натяжением и относительно высокой вязкостью.
При нормальных условиях вода слабо диссоциирована и в ней присутствуют в небольших количествах протоны (ионы гидроксония H3O+) и гидроксильные ионы OH−. Как известно, воду иногда рассматривают как кислоту и основание одновременно (катион H+ и анион OH−). В отсутствие посторонних веществ в воде одинаковая концентрация гидроксид-ионов и ионов водорода [18]. Судя по всему, при нейтрализации раствора HCl с растворенными в ней ионами Ga+ и As– и молекулами природного оксида GaAs путем добавления воды сильно полярные молекулы H2O сольватируют ионы: образуют гидраты и кристаллогидраты. При этом положительно заряженные участки молекулы растворяемого вещества притягивают атомы кислорода и создают молекулы типа GaOOH, а отрицательно заряженные – атомы водорода, AsH3.
При нейтрализации кислоты в составе водного раствора могут оставаться ионы и молекулы растворенного оксида, поскольку вода является хорошим растворителем. В то же время со стороны воздушной атмосферы в ней могут растворяться такие газы, как N2, O2, Ar, CO2, He, H2.
На стадии слива водного раствора с поверхности GaAs, вследствие большой вязкости и большой величины поверхностного натяжения H2O на поверхности GaAs остается практически одна большая куполообразная капля, хорошо связанная с поверхностью (хорошая смачиваемость). То есть внутреннее давление со стороны молекул воды на поверхность остаточного слоя H2O в капле становится больше атмосферного. Вследствие этого легко летучие компоненты, в частности арсин, покидают поверхность капли. Эту остаточную воду высушивают либо феном, либо с помощью фильтровальной бумаги, либо с помощью лампы накаливания, что может приводить к выпадению осадка на поверхности GaAs в виде Ga(OH)3, который при определенных условиях может перейти в Ga2O3. Таким образом, на стадии высушивания воды на поверхности GaAs могут оказаться (высаживаться) растворенные в ней элементы в виде тонкого слоя оксида, состоящего из соединений галлия и мышьяка с кислородом и углеродом. Химическое осаждение арсенида галлия из газовой фазы в системе GaAs–H2O–H2 и термодинамические характеристики этой системы были рассмотрены в работе [19].
Реакции водного раствора с поверхностью арсенида галлия. Реакция взаимодействия паров воды с арсенидом галлия может происходить, например, при кипении раствора HCl + H2O на стадии вливания воды в концентрированный раствор HCl в соответствии с реакцией:
(4)
${\text{GaAs}} + 3{{{\text{H}}}_{{\text{2}}}}{\text{O}} \leftrightarrow {\text{As}}{{{\text{H}}}_{{\text{3}}}} + {\text{Ga}}{{\left( {{\text{OH}}} \right)}_{{\text{3}}}}.$Однако арсин сравнительно нестоек и медленно разлагается даже при комнатной температуре на водород и элементарный мышьяк. То есть арсин, оказавшийся в капле раствора HCl + H2O, может улетать с поверхности воды. Причем формирование выпуклой поверхности остаточной капли способствует его удалению. В то же время известно [18], что в присутствии CO2 или паров воды формируется диоксид галлия. Последующее увеличение температуры ведет к реакции диспропорционирования Ga2O:
(5)
$3{\text{G}}{{{\text{a}}}_{{\text{2}}}}{\text{O}} \leftrightarrow 4{\text{Ga}} + {\text{G}}{{{\text{a}}}_{{\text{2}}}}{{{\text{O}}}_{3}}.$На стадии высушивания воды на поверхности GaAs могут оказаться (высаживаться) растворенные в ней элементы в виде тонкого слоя [19]:
(6)
$\begin{gathered} 2{\text{GaA}}{{{\text{s}}}_{{{\text{(тв)}}}}} + {{{\text{H}}}_{{\text{2}}}}{{{\text{O}}}_{{{\text{(газ)}}}}} \leftrightarrow \\ \leftrightarrow {{{\text{H}}}_{{{\text{2(газ)}}}}} + {\text{G}}{{{\text{a}}}_{{\text{2}}}}{{{\text{O}}}_{{{\text{(газ)}}}}} + {\text{A}}{{{\text{s}}}_{{{\text{2(газ)}}}}}, \\ \end{gathered} $(7)
$\begin{gathered} \frac{2}{3}{\text{GaA}}{{{\text{s}}}_{{\left( {{\text{тв}}} \right)}}} + {{{\text{H}}}_{{\text{2}}}}{{{\text{O}}}_{{\left( {{\text{газ}}} \right)}}} \leftrightarrow \\ \leftrightarrow {{{\text{H}}}_{{{\text{2}}\left( {{\text{газ}}} \right)}}} + \frac{2}{3}{\text{G}}{{{\text{a}}}_{{\text{2}}}}{{{\text{O}}}_{{{\text{3}}\left( {{\text{тв}}} \right)}}} + {\text{A}}{{{\text{s}}}_{{{\text{2}}\left( {{\text{газ}}} \right)}}}, \\ \end{gathered} $(8)
$2{\text{GaA}}{{{\text{s}}}_{{\left( {{\text{тв}}} \right)}}} + {{{\text{H}}}_{{\text{2}}}}{{{\text{O}}}_{{\left( {{\text{газ}}} \right)}}} \leftrightarrow 2{\text{G}}{{{\text{a}}}_{{\left( {\text{ж}} \right)}}} + {\text{A}}{{{\text{s}}}_{{{\text{2}}\left( {{\text{газ}}} \right)}}}.$Общее давление, при котором происходит газотранспортный химический процесс, равен Р, тогда сумма парциальных давлений газовых компонентов будет равна:
(9)
${{P}_{\sum }} = P\left( {{{{\text{H}}}_{{\text{2}}}}} \right) + P\left( {{{{\text{H}}}_{{\text{2}}}}{\text{O}}} \right) + P\left( {{\text{G}}{{{\text{a}}}_{{\text{2}}}}{\text{O}}} \right) + P{\text{A}}{{{\text{s}}}_{2}} = P.$При этом в химические реакции вступает только часть молей присутствующих в растворе реагентов. При использовании деионизованной воды давление внутри остаточной капли Р, как было указано выше, превышает атмосферное и реакция (7) сдвигается в сторону образования Ga2O3. В результате этого реакция высаживания арсенида галлия на подложку не происходит. В наиболее применимом на практике случае, когда идет реакция с образованием GaAs, давление Р равно атмосферному.
Обработка в БМВ. В отличие от деионизованной воды БМВ, бидистиллят, подвергнутый безреагентному (т.е. без привлечения химических реагентов) воздействию различными физическими полями, приобретает аномальные свойства. Одним из свойств этой воды является ее метастабильный характер. При отсутствии в ее составе щелочных элементов показатель pH может достигать значений 9…11. При этом электропроводность такой воды в 8…30 раз превышает электропроводность ее химического аналога. Как полагают, в этом случае кислотно-основные свойства воды будут определяться отношением концентраций сольватированных, не входящих в состав кластерных ионов протонов и гидроксилов, и выполняется неравенство: (m + 1)OH− > (l + 1)H+. То есть среда обладает щелочными свойствами при отсутствии в ее составе щелочных элементов, вследствие чего происходит дополнительная диссоциация молекул воды и образуются протонофильные H+(H2O)p и отрицательные OH−(H2O)n кластерные ионы.
В случае нейтрализации раствора HCl (с находящимся в нем образцом) с помощью вливания в кювету воды, типа БМВ, на стадии слива образуются мелкие капельки, покрывающие поверхность GaAs, которые легко слетают с поверхности. Данный факт объясняется физико-химическими свойствами БМВ. Прежде всего следует отметить, что БМВ является более хорошим растворителем, чем деионизированная вода, и обладает меньшей вязкостью по сравнению с обычной водой, соответственно, меньшим поверхностным натяжением и большим коэффициентом смачивания. Вместе с тем окружающий воздух оказывает давление на поверхность водной пленки. При этом атомы кислорода и углерода из воздуха оказывают парциальное давление на пленку воды, достигая равновесия. В этом случае давление со стороны атмосферы комнаты Р близко или равняется давлению P∑ внутри слоя воды.
Кроме того, реакции с образованием кислотных соединений в модифицированной воде способны нейтрализовать ее щелочные свойства, преобразуя БМВ в простую воду. Уменьшается и ее способность к растворению компонентов. Уменьшение растворимости приводит к выпадению GaAs (скорее всего, мелкокристаллического) из раствора на поверхность арсенида галлия в согласии с реакциями (3) и (6). Метастабильная вода, превращаясь в обычную воду, плохо смачивает поверхность выпавшего GaAs, свободного от окислов. Вследствие этого вода в виде капелек слетает с поверхности. Возможными реакциями с образованием кислотных соединений являются такие реакции, как указаны ниже. Как известно, при растворении оксида мышьяка(III), образуется гидроксид мышьяка(III) или мышьяковистая кислота [18]: As2О3 + 3Н2О = 2As(OH)3. Гидроксид мышьяка(III) амфотерен, но у него преобладают кислотные свойства. Кроме того, в воде растворяются такие соединения, как окись углерода. Часть молекул СО2 взаимодействует с водой с образованием угольной кислоты, которая в свою очередь подвергается частичной диссоциации: ${\text{СО}}_{3}^{{2 - }}$ + 2Н+ = = Н2CO3; ${\text{СО}}_{3}^{{2 - }}$ + 2Н+ = Н2O + CO2↑.
2.4. Электрофизические свойства контактов
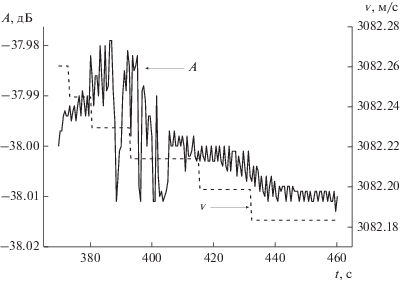
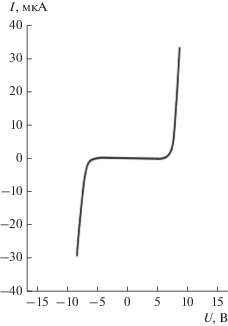
При нанесении планарных контактов на (100)GaAs с n ~ 9.7 × 1016 см–3 в виде двух параллельных полосок Au после обработки в деонизованной воде было обнаружено, что между ними формируется плохой выпрямляющий контакт. Лучшую ВАХ, присущую диодам Шоттки, показали образцы, промывавшиеся после обработки поверхности в HCl сразу же в БМВ (рис. 3). Образец перед осаждением Au при этом не отжигался в вакуумной камере ни до осаждения, ни после него. Осаждение Au проводили при Тподл ~ 20°С. Если же образец подвергался отжигу в вакуумной камере перед осаждением, то ВАХ показывали зависимость, характерную для омического контакта.
Измерение планарного сопротивления R между двумя сформированными металлическими контактами показало, что величина сопротивления в случае применения в качестве финишной очистки в БМВ имеет следующие значения: в одном направлении сопротивление составляет R1 = 87 кОм, в обратном направлении R2 = 277 кОм. Это намного превышает сопротивление между контактными слоями в случае применения деионизованной воды: R1 = 43 кОм, R2 = 162 кОм.
ЗАКЛЮЧЕНИЕ
Таким образом, можно сделать следующие выводы. Структура и состав слоя оксида, формирующегося на поверхности пленок арсенида галлия, определяются как способом роста полупроводника, концентрацией примесей, так и методами очистки поверхности. Методы очистки поверхности с использованием травящего раствора определяют в дальнейшем процессы формирования границ контактных слоев металл–полупроводник и их свойства. Значительную роль при этом играют способы нейтрализации раствора на стадии высушивания. Разбавление кислоты простой деионизованной водой может приводить к формированию диэлектрического слоя типа Ga2(C2O4)3 или Ga2O3 на поверхности арсенида галлия. Нейтрализация раствора кислоты с помощью БМВ при высушивании, скорее всего, приводит к покрытию поверхности арсенида галлия тонким слоем GaAs, свободного от окислов. Отсюда и различия в величине сопротивления приповерхностных слоев, что значительно сказывается на свойствах вольт-амперных характеристик изготавливаемых контактов.
Список литературы
Родерик Э.Х. Контакты металл–полупроводник. М.: Радио и связь, 1982.
Любченко В.Е., Брянцева Т.А., Марков И.А. и др. // РЭ. 2016. Т. 61. № 8. С. 824.
Тонкие пленки. Взаимная диффузия и реакции / Под ред. Дж. Мейера. М.: Мир, 1982.
Брянцева Т.А., Любченко В.Е., Любченко Д.В. и др. // РЭ. 2009. Т. 54. № 5. С. 4.
Брянцева Т.А., Бобылев М.И., Лебедева З.М. и др. // Физикохимия поверхности и защита материалов. 2012. Т. 48. № 1. С. 39.
Брянцева Т.А., Любченко Д.В., Марков И.А. и др. // Неорган. материалы. 2009. Т. 45. № 8. С. 901.
Травление полупроводников. Сб. статей. / Под ред. С.Н. Горина. М.: Мир, 1965.
Lioubtchenko D.V., Briantseva T.A., Markov I.A. et al. // Defect and Diffusion Forum. 2007. V. 261–262. P. 25.
Поута Дж.М., Фоти Г., Джекобсон Д.К. Модифицирование и легирование поверхности лазерными, ионными и электронными пучками. М.: Машиностроение, 1987.
Фомина Л.В., Безносюк С.А. // Нанотехника. 2006. № 4. С. 26.
Безрядин Н.Н., Котов Г.И., Арсентьев И.Н. и др. // Физика и техника полупроводников. 2012. Т. 46. № 6. С. 756.
Орлов А.М., Явтушенко И.О., Махмуд-Ахунов М.Ю. // Физика твердого тела. 2016. Т. 58. № 4. С. 792.
Гуляев Ю.В., Еремин С.М., Марков, И.А. и др. // Журн. радиоэлектроники. 2005. № 11. http://jre.cplire.ru/jre/nov05/1/text.html
Gulyev Yu.V., Markov I A., Ten Yu.A. // Physics of Wave Phenomena. 2020. V. 28. № 2. P. 98.
Брянцева Т.А, Бобылев М.А., Лебедева З.М. и др. // Зав. лаборатория. Диагностика материалов. 2012. № 2. С. 41.
Briantseva T.A., Lebedeva Z.M., Markov I.A. et al. // Appl. Surface Sci. 1999. V. 1. № 43. P. 223.
Химия и технология редких и рассеянных элементов. Ч. 1 / Под ред. К.А. Большакова. М.: Высшая школа, 1976.
Химическая энциклопедия. М.: Сов. энциклопедия, 1988. Т. 1.
Барыбин А.А., Томилин В.И., Шаповалов В.И. Физико-технологические основы макро-, микро- и наноэлектроники. М.: Физматлит, 2011.
Дополнительные материалы отсутствуют.
Инструменты
Радиотехника и электроника