Теоретические основы химической технологии, 2019, T. 53, № 6, стр. 681-688
Сравнительный анализ схем разделения реакционных смесей получения эпихлоргидрина в присутствии различных растворителей
Е. А. Охлопкова a, *, А. В. Фролкова a
a МИРЭА – Российский технологический университет (Институт тонких химических технологий
им. М.В. Ломоносова)
Москва, Россия
* E-mail: ea.okhl@ya.ru
Поступила в редакцию 22.04.2019
После доработки 10.06.2019
Принята к публикации 17.06.2019
Аннотация
На основе термодинамико-топологического анализа диаграмм фазового равновесия реакционных смесей, образуемых в процессе жидкофазного эпоксидирования аллилхлорида водным раствором пероксида водорода в среде органического растворителя в присутствии гетерогенного катализатора, предложены две принципиальные технологические схемы разделения. В качестве растворителей рассмотрены два низших спирта: метанол и пропанол-2. Обе схемы направлены на выделение всех компонентов в чистом виде и основаны на использовании специальных методов разделения: экстрактивной ректификации с диметилсульфоксидом (разделение пар компонентов аллилхлорид–метанол и пропанол-2–вода) и сочетания ректификации и расслаивания (разделение бинарных смесей аллилхлорид–вода и вода–эпихлоргидрин). Рассчитаны материальные балансы схем разделения смесей конкретного состава (рассматривается один состав для обеих смесей). Для определения параметров работы ректификационных колонн (число ступеней разделения, тарелка питания, флегмовое число) проведен вычислительный эксперимент с использованием программного комплекса Aspen Plus®. Предпочтение отдавалось параметрам, обеспечивающим получение всех веществ чистотой, отвечающей ГОСТ, при минимальных энергозатратах. Схема разделения смеси с пропанолом-2 содержит на одну колонну меньше, характеризуется меньшим суммарным числом ступеней разделения (на 32 теоретические тарелки) и меньшими (на 11%) энергозатратами по сравнению со схемой разделения смеси с метанолом. Кроме того, проведение реакции эпоксидирования при избытке пропанола-2 (концентрация спирта должна быть не меньше 68 мас. %) позволяет значительно упростить схему выделения целевого продукта эпихлоргидрина, что невозможно для системы с метанолом.
ВВЕДЕНИЕ
Эпихлоргидрин является важным продуктом основного органического синтеза, на основе которого получают краски, лаки, синтетические волокна, ионообменные смолы, эпихлоргидриновые каучуки и др. Разработка технологии получения эпихлоргидрина (ЭХГ) и выделения целевого продукта из реакционной смеси является актуальной задачей, обусловленной необходимостью создания отечественного производства данного органического продукта [1–4]. Сравнительный анализ различных методов получения ЭХГ (хлоргидринные, окислительные и методы с использованием пероксидных соединений) [4] показал перспективность использования жидкофазного эпоксидирования аллилхлорида водным раствором пероксида водорода в среде органического растворителя в присутствии гетерогенного катализатора (гранулированного титансодержащего силиката) [5–7]. Роль растворителя в данной реакции – гомогенизация раствора для обеспечения взаимодействия аллилхлорида и пероксида водорода на поверхности катализатора, а также охлаждение реакционной массы (процесс получения ЭХГ экзотермичен) [7]. В качестве растворителя рассматриваются низшие спирты: метанол (М), этанол (Э), пропанол-2 (П2), пропанол-1 (П1), бутанол-1 (Б) [8], для которых наблюдаются следующие показатели химического превращения: выход ЭХГ при 30% концентрации пероксида водорода составляет 29.1, 28.1, 26.9, 25.9 и 23.9% соответственно; начальная скорость образования целевого продукта выше для первых трех представителей ряда спиртов (М, Э и П2) [3]. Дальнейшие исследования реакционной составляющей авторы [2, 3] проводили исключительно для метанола, ввиду того, что отдельные показатели химического превращения несколько выше (хотя и незначительно) по сравнению с другими спиртами. Авторы сформулировали рекомендации по содержанию спирта в реакционной массе (55–60 мас. %). Нижний предел обусловлен необходимостью проведения реакции в гомогенном растворе (ниже 55% смесь расслаивается), превышение верхнего предела может нежелательным образом сказаться на технологической схеме разделения (“значительно усложняет последующую стадию выделения целевого продукта” [2, 3]). Исследования реакционной и разделительной составляющих технологии получения ЭХГ в присутствии остальных спиртов не проводились.
Ранее в работах [9, 10] был проведен анализ структур диаграмм парожидкостного равновесия реакционных смесей, содержащих аллилхлорид (АХ), воду (В), ЭХГ, растворитель (М, Э, П2, П1, Б), 3-хлор-1,2-пропандиол (ХПД) и пероксид водорода (ПВ). Оценка возможности разделения смесей, содержащих различный растворитель, показала, что пропанол-2 может составить конкуренцию токсичному метанолу в процессе получения ЭХГ. Данный факт обусловлен тем, что фазовая диаграмма системы с П2 содержит меньше азеотропов и сепаратрис по сравнению с системами с этанолом, пропанолом-1 и бутанолом-1, а также характеризуется благоприятным для разделения взаимным расположением сепаратрис и областей двухфазного расслаивания. Однако в работе [10] не приведены схемы разделения и результаты расчета процесса ректификации, подтверждающие данное утверждение.
Целью настоящей работы является синтез и сравнительный анализ принципиальных технологических схем разделения реакционных смесей получения эпихлоргидрина в присутствии метанола (пропанола-2) (рассматриваются схемы полного разделения смесей с получением всех веществ чистотой, отвечающей ГОСТ). В качестве метода исследования используется вычислительный эксперимент с применением программного продукта Aspen Plus®. Полный набор параметров бинарного взаимодействия уравнения NRTL, позволяющий воспроизводить физико-химические свойства реальных объектов с относительной ошибкой, не превышающей 3–5%, получен нами ранее и опубликован в работе [10].
ТЕОРЕТИЧЕСКАЯ ЧАСТЬ
При исследовании шестикомпонентных реакционных смесей было показано, что 3-хлор-1,2-пропандиол и пероксид водорода могут быть объединены в тяжелокипящую фракцию (ТКФ), поскольку последние не образуют азеотропов с остальными компонентами [10]. Следовательно, на первом этапе разделения можно отделить ТКФ от остальных компонентов. Данный прием позволяет снизить размерность решаемой задачи и упростить дальнейший анализ структуры диаграммы парожидкостного равновесия. Для оценки возможности дальнейшего разделения смеси на рис. 1 приведены структуры диаграмм фазового равновесия четырехкомпонентных систем (равновесие жидкость–пар приведено при атмосферном давлении, жидкость–жидкость при атмосферном давлении и 20°С) и точки состава смеси (F), подлежащей разделению.
Рис. 1.
Диаграммы фазового равновесия систем аллилхлорид (АХ)–растворитель–вода (В)–эпихлоргидрин (ЭХГ): (а) – метанол (М); (б) – пропанол-2 (П2); F – состав смеси, подлежащий разделению (расположен за сепаратрическим многообразием).
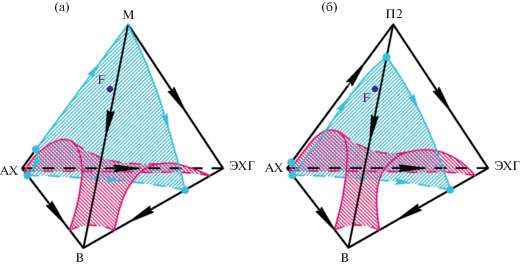
В качестве исходного рассматривается состав (в мас. %), полученный авторами [2, 3] для реакционной смеси с метанолом (АХ – 16.66, М – 61.61, В – 10.88, ЭХГ – 10.15, ПВ – 0.01, ХПД – 0.39). Для смеси с пропанолом-2 соотношение концентраций компонентов может измениться, однако, ввиду того, что реакционная составляющая пока не изучена, в качестве исходного будет рассмотрен вышеприведенный состав.
Для разделения четырехкомпонентных смесей состава F предлагается использовать первое заданное разделение: в дистилляте будет выделяться смесь, отвечающая составу азеотропа АХ–М для системы с метанолом (в кубе – смесь М–В–ЭХГ) и АХ–В – для системы с пропанолом-2 (в кубе – смесь П2–В–ЭХГ) (рис. 2). Для разделения дистиллятных потоков предлагается использование комплекса экстрактивной ректификации (смесь АХ–М); флорентийского сосуда и ректификационной колонны (смесь АХ–В). Ограниченная взаимная растворимость аллилхлорида и воды позволяет выделить аллилхлорид после флорентийского сосуда как самостоятельный продуктовый поток (99.05 мас. %).
Рис. 2.
Принципиальные схемы разделения смесей аллилхлорид (АХ)–вода (В)–растворитель–эпихлоргидрин (ЭХГ)–тяжелокипящая фракция (ТКФ): (а) – метанол (М); (б) – пропанол-2 (П2).
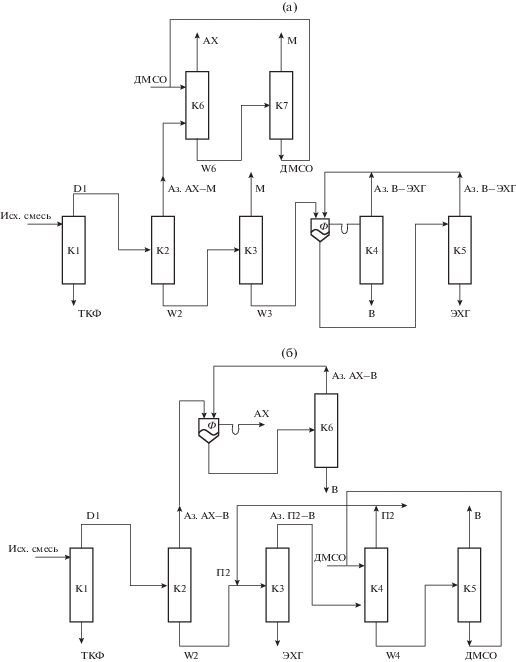
Для системы с метанолом смесь, образующаяся в кубе колонны К2 (рис. 2а), после полного отделения метанола (колонна К3) поступает в комплекс, состоящий из флорентийского сосуда и двух колонн для разделения пары компонентов В–ЭХГ.
Для системы с пропанолом-2 точка состава смеси кубового потока колонны К2 (рис. 2б) расположена вблизи сепаратрисы, порожденной седловидным азеотропом В–ЭХГ, что затрудняет дальнейшее разделение. По этой причине принято решение организовать направленный поток по пропанолу-2 с целью создания более благоприятных условий для разделения (полное выделение ЭХГ) (рис. 3).
Рис. 3.
Особенность расположения точки состава смеси П2–В–ЭХГ (W2 – схема рис. 2б) и сепаратрисы, порожденной азеотропом В–ЭХГ.
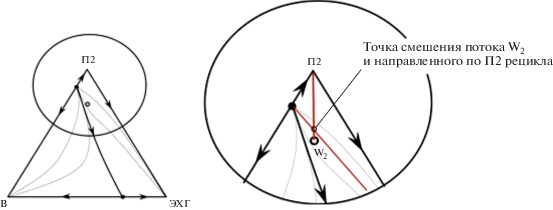
Для разделения азеотропной пары П2–В также предлагается комплекс экстрактивной ректификации (рис. 2 – колонны К4 и К5).
Для экстрактивной ректификации смесей аллилхлорид–метанол и пропанол-2–вода на основе анализа литературы [11] выбран ряд промышленных растворителей: диметилсульфоксид (ДМСО), N,N-диметилформамид (ДМФА), этиленгликоль, N-метилпирролидон. Оценка селективности потенциальных экстрактивных агентов (ЭА) проводилась на основе расчета коэффициента относительной летучести пар компонентов при различной концентрации ЭА.
ВЫЧИСЛИТЕЛЬНЫЙ ЭКСПЕРИМЕНТ
В программном комплексе Aspen Plus® проведен расчет парожидкостного равновесия и определены значения коэффициентов относительной летучести пар компонентов АХ–М и П2–В в присутствии выбранных ЭА (рис. 4).
Рис. 4.
Изменение коэффициента относительной летучести компонентов при увеличении концентрации экстрактивных агентов: (а) – аллилхлорид (АХ)–метанол (М); (б) – пропанол-2 (П2)–вода (В); 1 – ДМСО, 2 – ДМФА, 3 – этиленгликоль, 4 – N-метилпирролидон.
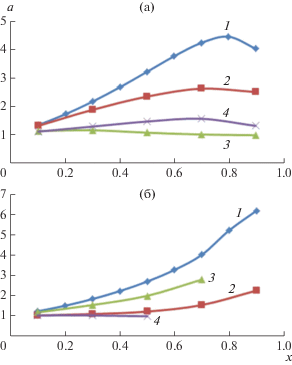
Анализ зависимостей, приведенных на рис. 4, показал, что наиболее селективным разделяющим агентом для обеих пар компонентов является диметилсульфоксид. Дальнейшие расчеты процесса ректификации проведены для этого ЭА.
В табл. 1 и 2 приведены материальные балансы (на 100 кг/ч исходной смеси) предложенных схем разделения, представленных на рис. 2, а также параметры работы ректификационных колонн и энергозатраты. Критерием выбора параметров работы колонн (эффективность колонны – число теоретических тарелок (N), тарелка подачи исходной смеси и ЭА (NF и NЭА) (нумерация тарелок с верха колонны), флегмовое число (R), энергозатраты, кВт (Q)) являются минимальные энергозатраты, при которых возможно получение веществ чистотой, отвечающей ГОСТ [12–14].
Таблица 1.
Параметры работы ректификационных колонн схемы разделения, приведенной на рис. 2а
| Колонна | N | NF (NЭА) | R | D, кг/ч | W, кг/ч | XD, мас. % | XW, мас. % | Q, кВт |
|---|---|---|---|---|---|---|---|---|
| 1 | 7 | 1 | – | 99.30 | 0.70 | 16.78 | 0.00 | 29.74 |
| 62.04 | 0.00 | |||||||
| 10.96 | 0.10 | |||||||
| 10.22 | 0.00 | |||||||
| 0.00 | 99.90 | |||||||
| 2 | 23 | 6 | 11.95 | 18.92 | 80.38 | 88.00 | 0.01 | 3.27 |
| 11.89 | 73.85 | |||||||
| 0.05 | 13.52 | |||||||
| 0.05 | 12.62 | |||||||
| 3 | 55 | 48 | 4.50 | 59.44 | 20.94 | 0.02 | 0.00 | 100.20 |
| 99.70 | 0.48 | |||||||
| 0.13 | 51.53 | |||||||
| 0.15 | 47.99 | |||||||
| Соотношение потоков, покидающих сепаратор, составляет 1.37 (водный слой/орг. слой) | ||||||||
| 4 | 10 | 1 | – | 3.44 | 10.80 | 0.00 | 0.00 | 2.09 |
| 7.56 | 0.09 | |||||||
| 22.67 | 99.91 | |||||||
| 69.77 | 0.00 | |||||||
| 5 | 9 | 1 | – | 0.44 | 10.09 | 0.00 | 0.00 | 0.63 |
| 4.55 | 0.30 | |||||||
| 22.73 | 0.00 | |||||||
| 72.73 | 99.70 | |||||||
| 6 | 25 | 17 (2) | 1.61 | 16.73 | 29.20 | 99.04 | 0.27 | 1.76 |
| 0.90 | 7.19 | |||||||
| 0.00 | 0.03 | |||||||
| 0.00 | 0.03 | |||||||
| 0.06 | 92.47 | |||||||
| Соотношение потоков D2 и ЭА составляет 1/1.4 | ||||||||
| 7 | 32 | 17 | 2.94 | 2.11 | 27.03 | 0.30 | 0.03 | 2.81 |
| 99.70 | 0.00 | |||||||
| 0.00 | 0.03 | |||||||
| 0.00 | 0.04 | |||||||
| 0.00 | 99.90 | |||||||
Таблица 2.
Параметры работы ректификационных колонн схемы разделения, приведенной на рис. 2б
| Колонна | N | NF (NЭА) | R | D, кг/ч | W, кг/ч | XD, мас. % | XW, мас. % | Q, кВт |
|---|---|---|---|---|---|---|---|---|
| 1 | 12 | 1 | – | 99.30 | 0.70 | 16.78 | 0.00 | 25.13 |
| 62.04 | 0.00 | |||||||
| 10.96 | 0.00 | |||||||
| 10.22 | 0.10 | |||||||
| 0.00 | 99.90 | |||||||
| 2 | 22 | 7 | 12.82 | 17.33 | 81.97 | 96.02 | 0.02 | 2.98 |
| 0.63 | 75.03 | |||||||
| 3.29 | 12.58 | |||||||
| 0.06 | 12.37 | |||||||
| 3 | 35 | 27 | 2.26 | 89.58 | 10.17 | 0.02 | 0.00 | 78.23 |
| 88.47 | 0.30 | |||||||
| 11.51 | 0.00 | |||||||
| 0.00 | 99.70 | |||||||
| Соотношение потоков П2 рецикла и W2 составляет 1/4.57 | ||||||||
| 4 | 40 | 20 (2) | 1.00 | 79.38 | 91.20 | 0.03 | 0.00 | 9.96 |
| 99.70 | 0.10 | |||||||
| 0.08 | 11.24 | |||||||
| 0.00 | 0.00 | |||||||
| 0.19 | 88.66 | |||||||
| Соотношение потоков D3 и ЭА составляет 1/0.9 | ||||||||
| 5 | 13 | 5 | 0.45 | 10.26 | 80.94 | 0.00 | 0.00 | 8.30 |
| 0.10 | 0.10 | |||||||
| 99.90 | 0.00 | |||||||
| 0.00 | 0.00 | |||||||
| 0.00 | 99.90 | |||||||
| Соотношение потоков, покидающих сепаратор, составляет 25.45 (орг. слой/водный слой) | ||||||||
| 6 | 7 | 4 | 1.00 | 0.12 | 0.53 | 83.33 | 0.00 | 0.69 |
| 1.25 | 0.10 | |||||||
| 12.50 | 99.90 | |||||||
| 0.00 | 0.00 | |||||||
Суммарные энергозатраты составили 140.5 и 125.3 кВт для схем, приведенных на рис. 2а и 2б соответственно.
ЗАКЛЮЧЕНИЕ
Сравнительный анализ структур диаграмм парожидкостного равновесия реакционных смесей получения эпихлоргидрина в присутствии метанола или пропанола-2 показал, что система с метанолом содержит на один азеотроп меньше по сравнению с системой с пропанолом-2, однако наличие дополнительного азеотропа (АХ–П2) не влияет на структуру схемы разделения смеси. Диаграммы парожидкостного равновесия обеих систем содержат по одному двухмерному сепаратрическому многообразию, разбивающему симплекс на две области дистилляции.
Для исходного состава смеси (концентрация растворителя составляет 61.61 мас. %) предложены две принципиальные схемы разделения, направленные на выделение всех компонентов в чистом виде (для корректного сравнения схем). Схема разделения смеси с пропанолом-2 содержит на одну колонну меньше, что обусловлено ограниченной взаимной растворимостью аллилхлорида и воды и отсутствием необходимости доочистки АХ (его концентрация в составе равновесного жидкого слоя 99.05 мас. %). Суммарная эффективность ректификационных колонн (суммарное число ступеней разделения) также ниже для схемы разделения пропанольной смеси (129 против 161); энергозатраты для данной схемы ниже на 11%. В схеме (б) на рис. 2 имеется направленный поток по спирту для перевода состава смеси, подаваемого в колонну К3, в благоприятную для разделения область. Следует отметить, что при незначительном увеличении содержания пропанола-2 в исходной смеси (т.е. проведение реакции при небольшом избытке П2) – до 68 мас. % – можно отказаться от направленного рецикла, что также благоприятным образом скажется на энергозатратах.
Если рассматривать схемы разделения, направленные только на выделение целевого продукта – эпихлоргидрина, то в случае метанольной системы потребуется минимум четыре колонны, в случае системы с пропанолом-2 – три. Следует также отметить, что реализация второго заданного разделения с целью выделения ЭХГ в схеме разделения метанольной смеси невозможна ни при каких условиях (данные ограничения связаны с особенностью расположения сепаратрического многообразия).
Результаты настоящей работы подтверждают, что при разработке технологии получения органических продуктов следует применять комплексный подход, направленный на исследование как реакционной, так и разделительной составляющей. В технологии получения эпихлоргидрина эпоксидированием аллилхлорида в среде растворителя пропанол-2 может стать альтернативой токсичному метанолу; более того, его применение может привести к снижению энергоемкости процесса.
Работа выполнена при финансовой поддержке Российского научного фонда (проект № 16-19-10632).
ОБОЗНАЧЕНИЯ
| D | дистиллятный поток, кг/ч |
| N | число теоретических тарелок |
| NF | номер теоретической тарелки питания |
| Q | энергозатраты на кипятильник, кВт |
| R | флегмовое число |
| W | кубовый поток, кг/ч |
| XD | состав дистиллятного потока, мас. % |
| XW | состав кубового потока, мас. % |
| x | массовая доля компонента в жидкой фазе |
| α | коэффициент относительной летучести |
Список литературы
Сулимов А.В., Данов С.М., Овчарова А.В., Обрывалина А.Н., Теляшев Р.Г., Овчаров А.А., Балашов А.Л. Инновационные процессы получения эпихлоргидрина // Нефтегазохимия. 2013. № 1. С. 32.
Сулимов А.В. Разработка научных основ и технологий получения гетероциклических кислородсодержащих соединений. Дис. … докт. техн. наук. М.: МИТХТ, 2013.
Овчарова А.В. Разработка технологии получения эпихлоргидрина. Дис. … канд. хим. наук. М.: РХТУ, 2012.
Охлопкова Е.А., Серафимов Л.А., Фролкова А.В. Методы получения эпихлоргидрина // Хим. технол. 2017. Т. 18. № 8. С. 341.
Хофен В., Брассе К., Франке Р., Катцер Р. Способ получения эпихлоргидрина. Пат. 2456279 РФ. 2012.
Данов С.М., Сулимов А.В., Овчаров А.А., Сулимова А.В. Способ получения гранулированного титансодержащего цеолита. Пат. 2422360 РФ. 2011.
Сулимов А.В., Данов С.М., Овчарова А.В., Овчаров А.А., Флид В.Р., Леонтьева С.В., Флид М.Р., Трушечкина М.А. Изучение закономерностей процесса эпоксидирования аллилхлорида в среде метанола в присутствии экструдированного титансодержащего силиката // Изв. Акад. наук. Сер. хим. 2016. № 2. С. 469.
Данов С.М., Сулимов А.В., Сулимова А.В. Влияние природы растворителя на процесс эпоксидирования аллилхлорида пероксидом водорода на титансодержащем силикате // Журн. прикл. хим. 2008. Т. 81. № 11. С. 1847.
Охлопкова Е.А., Серафимов Л.А., Фролкова А.В. Разделение многокомпонентной системы, образующейся в производстве эпихлоргидрина // Тонкие хим. технол. 2016. Т. 11. № 6. С. 36.
Фролкова А.В., Охлопкова Е.А., Фролкова А.К. Фазовое равновесие реакционных смесей получения эпихлоргидрина в присутствии растворителей // Теор. осн. хим. технол. 2019. Т. 53. № 2. С. 138.
Гайле А.А., Сомов В.Е., Залищевский Г.Д. Селективные растворители. Разделение и очистка углеводородсодержащего сырья. СПб.: ХИМИЗДАТ, 2008.
ГОСТ 2222-95. Метанол технический. Технические условия. Взамен ГОСТ 2222-78. М.: Изд-во стандартов, 2001.
ГОСТ 9805-84. Спирт изопропиловый. Технические условия. Взамен ГОСТ 9805-76. М.: Изд-во стандартов, 1986.
ГОСТ 12844-74. Эпихлоргидрин технический. Технические условия. Взамен ГОСТ 12844-67. М.: Государственный комитет СССР по стандартам, 1975.
Дополнительные материалы отсутствуют.
Инструменты
Теоретические основы химической технологии


