Теоретические основы химической технологии, 2023, T. 57, № 5, стр. 495-506
Разделение промышленной смеси продуктов фторирования декалина или нафталина. Разработка технологии очистки перфтор(7-метилбицикло[4.3.0]нонана) от близкокипящих примесей методом гетероазеотропной ректификации
А. В. Полковниченко a, *, Е. В. Лупачев a, **, А. В. Кисель a, С. Я. Квашнин a, Н. Н. Кулов a
a Институт общей и неорганической химии им. Н.С. Курнакова РАН
Москва, Россия
* E-mail: anzakhlevniy@rambler.ru
** E-mail: egorlu91@gmail.com
Поступила в редакцию 14.07.2023
После доработки 20.07.2023
Принята к публикации 23.07.2023
- EDN: MGWEPC
- DOI: 10.31857/S0040357123050172
Аннотация
В работе рассмотрен процесс выделения перфтор(7-метилбицикло[4.3.0]нонана) (МБЦН) из промышленной смеси продуктов фторирования декалина или нафталина. Согласно экспериментальным данным, ректификационное разделение позволяет концентрировать МБЦН до фракции с содержанием основного компонента более 0.950 масс. д., после чего эффективность процесса начинает быстро снижаться; при достижении концентрации 0.975 масс. д. разделения уже практически не наблюдается (величина коэффициента разделения ${{K}_{{{\text{sep}}}}}$ → 1). В настоящей работе предложен и на полупромышленной ректификационной колонне периодического действия реализован процесс очистки МБЦН методом гетероазеотропной ректификации с применением ацетона (Ац) как разделяющего агента. Данный метод позволяет существенно интенсифицировать финальную стадию очистки и повысить содержание МБЦН с 0.950 до более чем 0.998 масс. д., массовая доля отбора обогащенной фракции составляет более 0.85 от загрузки, выход по продукту более 88%. В работе приведены значения коэффициентов разделения между дистиллятом и кубовым продуктом и коэффициентов обогащения для целевого и примесных компонентов; для бинарной системы МБЦН–Ац определены данные о фазовом равновесии жидкость-жидкость и характеристики гетероазеотропа.
1. ВВЕДЕНИЕ
Основным методом промышленного производства перфтордекалина (ПФД) является процесс электрохимического фторирования декалина или нафталина. В промышленности его осуществляют в две стадии [1]. Первая стадия – фторирование в “мягких” условиях, что позволяет защитить углеродную цепь. На второй стадии, чтобы избавиться от частично фторированных молекул, содержание которых строго регламентируется, реакционную смесь обрабатывают молекулярным фтором. Это приводит к побочным реакциям разрушения углеродной цепи части молекул и как следствие к образованию примесей.
В рамках исследования процесса получения и очистки ПФД был опубликован ряд работ о структуре побочных продуктов электрохимического фторирования декалина или нафталина [2–4], а также рассмотрены свойства основных составляющих продуктовой смеси [5–8]. Однако, механизмы реакций образования побочных продуктов и вид этих продуктов все еще недостаточно изучены, так как идентификация последних требует спектрального анализа образцов, многие из которых так и не были получены в чистом виде. То есть, эталонные образцы на практике как правило недоступны, а данные о спектральных и физико-химических свойствах отсутствуют в литературе, что делает крайне проблематичным направленный поиск методов интенсификации процесса выделения этих соединений.
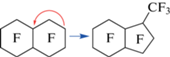
Перфтор(7-метилбицикло[4.3.0]нонан) (МБЦН) является одним из идентифицированных примесных компонентов промышленной смеси близкокипящих пространственных и структурных изомерных продуктов реакции электрохимического фторирования декалина или нафталина [9]. МБЦН образуется при разрушении углеродной цепи ПФД с последующей частичной радикальной реакцией замыкания цикла (рис. 1). МБЦН также является побочным продуктом фторирования бутилбензола [10], где в качестве продуктов реакции по аналогии с процессом фторирования декалина или нафталина образуются цис-ПФД, транс-ПФД и перфтор(бутилциклогексан).
Рис. 1.
Механизм побочной реакции разрыва углеродной цепи перфтордекалина с последующей частичной радикальной реакцией замыкания цикла и образованием перфтор(7-метилбицикло[4.3.0]нонана).
Следует отметить, что ряд перфторированных алициклических веществ, которые являются побочными продуктами процесса электрохимического фторирования декалина или нафталина, имеют свою собственную коммерческую ценность. Они используются: в качестве мономеров при производстве лиофобной полимерной пленки; как индикаторы для оценки утечки в результате улавливания CO2 в истощенном нефтяном резервуаре; в оптических элементах, включая линзы, фокусным расстоянием которых можно управлять с помощью электрического поля [11–15]. Сам МБЦН потенциально применим в медицине: как компонент кровезаменителя [16–19]; компонент нано эмульсий для маркировки и визуализации клеток при магнитно-резонансной и оптической томографии [20, 21]; для обеспечения тепловой визуализации и мониторинга теплового физиологического состояния живого организма (термография с помощью ядерного магнитного резонанса (ЯМР)) [22]; для неинвазивного создания газовой карты животного in vivo [23].
Целью настоящей работы является разработка финальной стадии технологии очистки перфтор(7-метилбицикло[4.3.0]нонана) – компонента промышленной смеси изомерных продуктов реакции электрохимического фторирования декалина или нафталина.
2. МАТЕРИАЛЫ И МЕТОДЫ
В качестве объекта исследования в настоящей работе рассмотрена фракция МБЦН (CAS No. 75262-86-1) с содержанием целевого компонента (${{X}_{{{\text{МБЦН}}}}}$) в диапазоне от 0.950 до 0.975 масс. д. Сама фракция [0.950; 0.975] масс. д. была получена ректификацией промышленных образцов смеси с исходным содержанием основного компонента около 0.80 масс. д.
Примесные компоненты в исследуемых образцах с содержанием основного компонента от 0.950 до 0.975 масс. д. можно разбить на следующие группы:
1. Идентифицированные: ПФД, от 0.004 до 0.025 масс. д.;
2. Неидентифицированные:
2.1. Основная примесь (main imp.), от 0.012 до 0.028 масс. д.;
2.2. Суммарные прочие примеси (∑other imp.), от 0.0001 до 0.008 масс. д. (до 10 соединений).
Следует отметить, что идентификация указанных выше примесей на настоящем этапе исследований невозможна ввиду недостатка справочной информации и отсутствия концентрированных образцов этих примесей для спектрального анализа.
Для интенсификации процесса очистки МБЦН использовали метод гетероазеотропной ректификация. В качестве потенциальных гетероазеотропообразующих разделяющих агентов (РА) были рассмотрены ацетон (Ац) (CAS No. 67-64-1, ≥0.995 масс. д.) и диметилформамид (ДМФА) (CAS No. 68-12-2, ≥ 0.990 масс. д.). Эксперименты проводили при атмосферном давлении (P) на полупромышленной ректификационной колонне периодического действия с эффективностью в 85 теоретических ступеней разделения. Описание ректификационной колонны и ее схема приведены в работе [24]. В ходе эксперимента в куб колонны загружали от 7 до 9 кг разделяемой смеси; в случае гетероазеотропной ректификации в куб колонны дополнительно загружали 1 л РА. В течении эксперимента каждые два часа отбирали порядка 60–70 мл дистиллята (в случае гетероазеотропной дистилляции осуществляется отбор нижней, фторорганической фазы дистиллята); каждые 8 отборов объединялись и образовывали фракцию дистиллята (Fr). Анализу подвергали исходную смесь (F), фракции дистиллята (Fr), сумму всех Fr (∑D) и конечный кубовый продукт (W). Для определения качественного и количественного состава образцов использовали газовую хроматографию (Agilent 6890N, капиллярная колонка Restek RTX-1701 RK12054) и ЯМР-спектроскопию (Bruker AVANCE-300 radiospectrometer). В случае гетероазеотропной дистилляции растворенный в образцах РА предварительно удалялся экстрагированием водой.
Фазовое равновесие жидкость–жидкость определяли методом “точки помутнения” (cloud point method). Массы навесок определяли на Mass Comparator MC-1000 с точностью ±5 × 10–4 г.
Характеристики гетероазеотропа определяли на ректификационной колонне, описанной выше. Для эксперимента использовали МБЦН с содержанием основного компонента ≥0.998 масс. д. В качестве исходной брали бинарную смесь МБЦН–Ац по составу предположительно отвечающему составу гетероазеотропа. В ходе эксперимента колонну выводили в стационарный режим в течении 40 мин, после чего начинали отбор дистиллята при флегмовом числе равном 0. Поток дистиллята собирался в приемной емкости. Объем дистиллята, полученный в первые 5 мин после начала отбора, удаляли. Далее каждые 3 мин фракции дистиллята отбирали для определения состава. Дистиллят представлял собой двухфазную системы; верхняя фаза – ацетоновая, нижняя фаза – МБЦН. Собранные таким образом образцы термостатировали в делительной воронке в течении 12 ч, после чего фазы разделялись и взвешивались. Состав фаз определялся на основании данных о фазовом равновесии жидкость–жидкость. Полученные данные были использованы для расчета состава гетероазеотропа.
3. ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
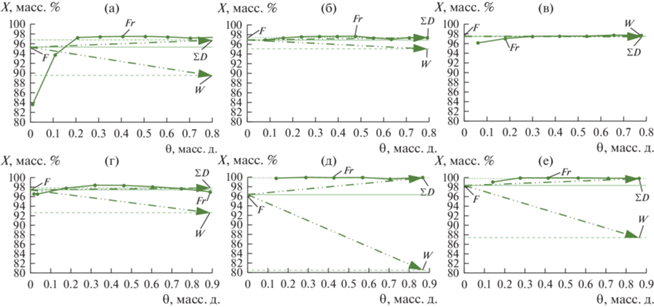
Экспериментальные данные по ректификационному разделению фракций МБЦН с исходным содержанием основного компонента более 0.950 масс. д. представлены в табл. 1 и табл. 2. Зависимости состава фракций дистиллята (Fr), суммарных отобранных дистиллятов (∑D) и итоговых кубовых продуктов (W) от доли отбора (θ) (уравнение (1)) приведены на рис. 2–5.
(1)
$\begin{array}{*{20}{c}} {\Theta = {{\sum {{m}_{{Fr}}}} \mathord{\left/ {\vphantom {{\sum {{m}_{{Fr}}}} {{{m}_{F}}}}} \right. \kern-0em} {{{m}_{F}}}},} \end{array}$Таблица 1.
Экспериментальные данные по очистке МБЦН на полупромышленной ректификационной колонне при атмосферном давлении. Составы фракций дистиллята
| W | D | $X_{{Fr}}^{i}$, маcс. % | Доля отбора, масс. д. | |||||
|---|---|---|---|---|---|---|---|---|
| Идентифицированные | Неидентифицированные | |||||||
| T, °C | P, кПа | T, °C | P, кПа | МБЦН | ПФД | main imp. | ∑ other imp. | |
| Эксперимент No. 1. Ректификация без РА | ||||||||
| F | 95.359 | 2.493 | 1.305 | 0.843 | – | |||
| 136.1 | 100.4 | 132.2 | 100.4 | 83.706 | 1.821 | 0.952 | 13.521 | 0.01 |
| 136.6 | 100.8 | 134.1 | 100.3 | 93.788 | 1.537 | 1.187 | 3.488 | 0.11 |
| 137.1 | 100.5 | 135.3 | 100.4 | 97.298 | 1.233 | 1.230 | 0.239 | 0.21 |
| 136.8 | 100.7 | 135.0 | 100.4 | 97.475 | 1.072 | 1.290 | 0.163 | 0.31 |
| 136.7 | 100.5 | 135.1 | 100.4 | 97.561 | 0.939 | 1.346 | 0.154 | 0.41 |
| 137.1 | 100.5 | 135.6 | 100.4 | 97.547 | 0.854 | 1.442 | 0.157 | 0.51 |
| 136.7 | 100.5 | 135.5 | 100.4 | 97.458 | 0.824 | 1.540 | 0.178 | 0.60 |
| 138.1 | 100.5 | 135.6 | 100.4 | 97.226 | 0.992 | 1.535 | 0.247 | 0.70 |
| 143.0 | 100.5 | 136.4 | 100.5 | 97.335 | 0.876 | 1.476 | 0.313 | 0.80 |
| Эксперимент No. 2. Ректификация без РА | ||||||||
| F | 96.925 | 1.058 | 1.659 | 0.358 | – | |||
| 137.7 | 103.1 | 134.8 | 99.9 | 96.967 | 0.879 | 1.368 | 0.786 | 0.08 |
| 139.5 | 100.7 | 136.7 | 100.0 | 97.344 | 1.038 | 1.213 | 0.405 | 0.16 |
| 137.2 | 100.4 | 135.7 | 99.9 | 97.590 | 0.913 | 1.306 | 0.191 | 0.24 |
| 137.4 | 100.5 | 135.9 | 100.0 | 97.658 | 0.734 | 1.460 | 0.148 | 0.32 |
| 137.5 | 100.6 | 136.1 | 100.0 | 97.644 | 0.641 | 1.581 | 0.134 | 0.40 |
| 137.5 | 100.5 | 136.1 | 100.1 | 97.703 | 0.523 | 1.614 | 0.160 | 0.48 |
| 137.5 | 100.3 | 136.2 | 100.3 | 97.358 | 0.505 | 1.674 | 0.463 | 0.55 |
| 137.6 | 100.4 | 136.5 | 100.3 | 97.070 | 0.385 | 2.052 | 0.493 | 0.63 |
| 137.9 | 100.3 | 136.6 | 100.2 | 97.373 | 0.367 | 2.111 | 0.149 | 0.71 |
| 141.6 | 100.2 | 136.8 | 100.1 | 97.407 | 0.323 | 2.069 | 0.201 | 0.79 |
| Эксперимент No. 3. Ректификация без РА | ||||||||
| F | 97.512 | 0.990 | 1.311 | 0.187 | – | |||
| 135.9 | 100.7 | 133.9 | 100.7 | 96.154 | 2.130 | 0.987 | 0.729 | 0.06 |
| 136.5 | 100.5 | 134.9 | 100.5 | 97.034 | 1.614 | 1.065 | 0.287 | 0.18 |
| 136.9 | 100.6 | 135.4 | 100.5 | 97.465 | 1.261 | 1.088 | 0.186 | 0.30 |
| 136.6 | 100.9 | 135.1 | 100.9 | 97.546 | 1.169 | 1.125 | 0.160 | 0.42 |
| 136.3 | 100.9 | 134.7 | 100.8 | 97.543 | 1.103 | 1.215 | 0.139 | 0.54 |
| 136.1 | 100.8 | 134.8 | 100.8 | 97.771 | 0.802 | 1.311 | 0.116 | 0.66 |
| 138.8 | 100.8 | 135.3 | 100.7 | 97.734 | 0.656 | 1.567 | 0.043 | 0.78 |
| Эксперимент No. 4. Гетероазеотропная ректификация в присутствии ДМФА | ||||||||
| F | 97.410 | 0.894 | 1.505 | 0.191 | – | |||
| 122.0 | 100.4 | 119.1 | 100.4 | 96.592 | 0.622 | 1.011 | 1.775 | 0.02 |
| 121.7 | 100.5 | 118.8 | 100.5 | 96.558 | 0.692 | 0.876 | 1.874 | 0.04 |
| 119.7 | 100.4 | 118.9 | 100.4 | 97.794 | 0.547 | 0.904 | 0.755 | 0.18 |
| 120.9 | 100.5 | 118.1 | 100.2 | 98.418 | 0.525 | 0.884 | 0.173 | 0.32 |
| 120.9 | 100.8 | 118.2 | 100.8 | 98.341 | 0.528 | 1.013 | 0.118 | 0.46 |
| 121.2 | 100.6 | 119.3 | 100.6 | 98.063 | 0.583 | 1.198 | 0.156 | 0.60 |
| 121.5 | 100.6 | 119.3 | 100.5 | 97.705 | 0.637 | 1.517 | 0.141 | 0.75 |
| 130.5 | 100.3 | 119.9 | 100.3 | 97.002 | 0.660 | 2.053 | 0.285 | 0.89 |
| Эксперимент No. 5. Гетероазеотропная ректификация в присутствии Ац | ||||||||
| F | 96.400 | 0.689 | 2.845 | 0.066 | – | |||
| 58.1 | 101.3 | 54.5 | 99.2 | 99.855 | 0 | 0 | 0.145 | 0.14 |
| 58.7 | 101.9 | 54.2 | 99.9 | 99.999(5) | 0 | 0 | 0.000(5) | 0.29 |
| 59.9 | 102.1 | 54.2 | 100.2 | 99.931 | 0 | 0 | 0.069 | 0.43 |
| 60.2 | 102.1 | 54.3 | 100.1 | 100 | 0 | 0 | 0 | 0.57 |
| 56.3 | 101.9 | 54.3 | 100.0 | 99.658 | 0 | 0 | 0.342 | 0.71 |
| 59.5 | 102.0 | 54.3 | 99.9 | 100 | 0 | 0 | 0 | 0.87 |
| Эксперимент No. 6. Гетероазеотропная ректификация в присутствии Ац | ||||||||
| F | 98.379 | 0.399 | 1.206 | 0.016 | – | |||
| 58.7 | 102.1 | 54.5 | 99.7 | 99.139 | 0 | 0 | 0.861 | 0.14 |
| 59.3 | 102.1 | 54.3 | 99.4 | 99.999 | 0 | 0 | 0.001 | 0.28 |
| 60.2 | 102.1 | 53.9 | 99.4 | 100 | 0 | 0 | 0 | 0.41 |
| 60.5 | 102.1 | 53.7 | 99.5 | 100 | 0 | 0 | 0 | 0.56 |
| 59.9 | 102.0 | 53.8 | 99.5 | 99.921 | 0 | 0 | 0.079 | 0.71 |
| 70.3 | 101.8 | 53.9 | 99.4 | 99.928 | 0 | 0 | 0.072 | 0.87 |
| u(T) = ±1.5°C; u(P) = ±1.25 кПа; u(X) = 0.05 маcс. % | ||||||||
Таблица 2.
Экспериментальные данные по очистке МБЦН на полупромышленной ректификационной колонне при атмосферном давлении. Составы продуктовых потоков
| Поток | X, маcс. % | Доля отбора, масс. д. |
|||
|---|---|---|---|---|---|
| Идентифицированные | Неидентифицированные | ||||
| МБЦН | ПФД | main imp. | ∑ other imp. | ||
| Эксперимент No. 1. Ректификация без РА | |||||
| ∑D | 96.791 | 1.051 | 1.375 | 0.783 | 0.80 |
| F | 95.359 | 2.493 | 1.305 | 0.843 | |
| W | 89.557 | 7.720 | 1.114 | 1.609 | |
| Эксперимент No. 2. Ректификация без РА | |||||
| ∑D | 97.412 | 0.631 | 1.645 | 0.312 | 0.79 |
| F | 96.925 | 1.058 | 1.659 | 0.358 | |
| W | 95.066 | 2.690 | 1.712 | 0.532 | |
| Эксперимент No. 3. Ректификация без РА | |||||
| ∑D | 97.411 | 1.180 | 1.210 | 0.199 | 0.78 |
| F | 97.512 | 0.990 | 1.311 | 0.187 | |
| W | 97.516 | 0.555 | 1.739 | 0.190 | |
| Эксперимент No. 4. Гетероазеотропная ректификация в присутствии ДМФА | |||||
| ∑D | 97.835 | 0.583 | 1.249 | 0.333 | 0.89 |
| F | 97.410 | 0.894 | 1.505 | 0.191 | |
| W | 92.616 | 3.353 | 3.306 | 0.725 | |
| Эксперимент No. 5. Гетероазеотропная ректификация в присутствии Ац | |||||
| ∑D | 99.912 | 0 | 0 | 0.088 | 0.87 |
| F | 96.400 | 0.689 | 2.845 | 0.066 | |
| W | 80.537 | 3.782 | 15.681 | 0 | |
| Эксперимент No. 6. Гетероазеотропная ректификация в присутствии Ац | |||||
| ∑D | 99.835 | 0 | 0 | 0.165 | 0.87 |
| F | 98.379 | 0.399 | 1.206 | 0.016 | |
| W | 87.344 | 2.167 | 10.489 | 0 | |
| u(X) = 0.05 маcс. % | |||||
Рис. 4.
Зависимость содержания основной неидентифицированной примеси (main imp.) (X, маcс. %) в продуктовых потоках от доли отбора θ согласно данным табл. 1 и табл. 2: (а) – Эксперимент No. 1; (б) – Эксперимент No. 2; (в) – Эксперимент No. 3; (г) – Эксперимент No. 4; (д) – Эксперимент No. 5; (е) – Эксперимент No. 6.
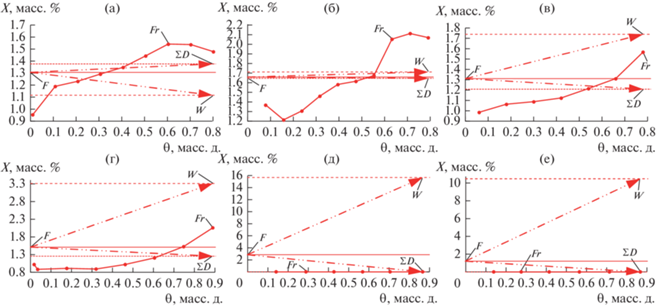
Рис. 5.
Зависимость содержания суммы прочих неидентифицированных примесей (∑other imp.) (X, маcс. %) в продуктовых потоках от доли отбора θ согласно данным табл. 1 и табл. 2: (а) – Эксперимент No. 1; (б) – Эксперимент No. 2; (в) – Эксперимент No. 3; (г) – Эксперимент No. 4; (д) – Эксперимент No. 5; (е) – Эксперимент No. 6.
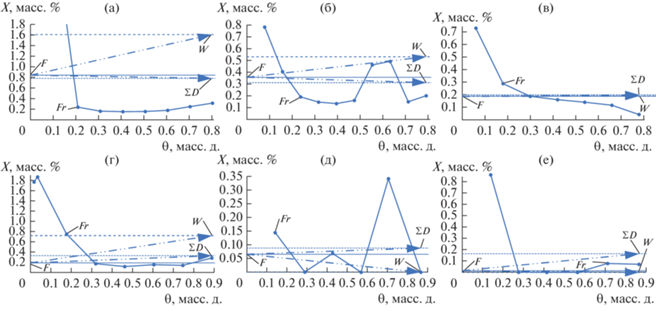
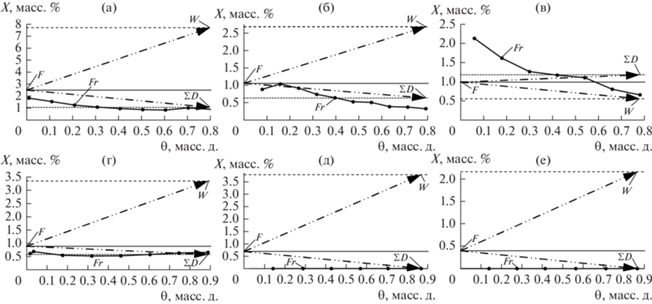
По данным табл. 2 были рассчитаны значения коэффициентов разделения Ksep (уравнение (2)) и обогащения Kenr (уравнение (3)). Зависимости величин Ksep и Kenr от содержания целевого компонента в исходной смеси приведены в Табл. 3 и показаны на рис. 6 и 7, соответственно.
(2)
$\begin{array}{*{20}{c}} {{{K}_{{{\text{sep}}}}} = \frac{{\left( {{{X_{{\sum D}}^{i}} \mathord{\left/ {\vphantom {{X_{{\sum D}}^{i}} {\left( {1 - X_{{\sum D}}^{i}} \right)}}} \right. \kern-0em} {\left( {1 - X_{{\sum D}}^{i}} \right)}}} \right)}}{{\left( {{{X_{W}^{i}} \mathord{\left/ {\vphantom {{X_{W}^{i}} {\left( {1 - X_{W}^{i}} \right)}}} \right. \kern-0em} {\left( {1 - X_{W}^{i}} \right)}}} \right)}},} \end{array}$(3)
$\begin{array}{*{20}{c}} \begin{gathered} K_{{{\text{enr}}}}^{{\sum D/F}} = \frac{{\left( {{{X_{{\sum D}}^{i}} \mathord{\left/ {\vphantom {{X_{{\sum D}}^{i}} {\left( {1 - X_{{\sum D}}^{i}} \right)}}} \right. \kern-0em} {\left( {1 - X_{{\sum D}}^{i}} \right)}}} \right)}}{{\left( {{{X_{F}^{i}} \mathord{\left/ {\vphantom {{X_{F}^{i}} {\left( {1 - X_{F}^{i}} \right)}}} \right. \kern-0em} {\left( {1 - X_{F}^{i}} \right)}}} \right)}}{\text{\;or}} \\ {\text{\;}}K_{{{\text{enr}}}}^{{W/F}} = \frac{{\left( {{{X_{W}^{i}} \mathord{\left/ {\vphantom {{X_{W}^{i}} {\left( {1 - X_{W}^{i}} \right)}}} \right. \kern-0em} {\left( {1 - X_{W}^{i}} \right)}}} \right)}}{{\left( {{{X_{F}^{i}} \mathord{\left/ {\vphantom {{X_{F}^{i}} {\left( {1 - X_{F}^{i}} \right)}}} \right. \kern-0em} {\left( {1 - X_{F}^{i}} \right)}}} \right)}}, \\ \end{gathered} \end{array}$Таблица 3.
Значения коэффициентов разделения (Ksep) и коэффициентов обогащения (Kenr) рассчитанные по данным табл. 2
| No. эксп. | Эксперимент No. 1. Ректификация без РА |
Эксперимент No. 2. Ректификация без РА |
Эксперимент No. 3. Ректификация без РА |
|||||||||
| Комп. | МБЦН | ПФД | main imp. | ∑ other imp. | МБЦН | ПФД | main imp. | ∑ other imp. | МБЦН | ПФД | main imp. | ∑ other imp. |
| $X_{F}^{i}$ | 95.359 | 2.493 | 1.305 | 0.843 | 96.925 | 1.058 | 1.659 | 0.358 | 97.512 | 0.990 | 1.311 | 0.187 |
| $K_{{{\text{enr}}}}^{{\frac{{\sum D}}{F}}}$ | 1.47 | 0.59 | 0.99 | 0.87 | 1.19 | 0.42 | 1.05 | 0.93 | 0.96 | 1.19 | 0.92 | 1.07 |
| $K_{{{\text{enr}}}}^{{\frac{W}{F}}}$ | 0.42 | 2.58 | 1.03 | 1.49 | 0.61 | 3.27 | 0.85 | 1.92 | 1.00 | 0.56 | 1.33 | 1.02 |
| ${{K}_{{{\text{sep}}}}}$ | 3.52 | 0.23 | 0.96 | 0.59 | 1.95 | 0.13 | 1.24 | 0.48 | 0.96 | 2.14 | 0.69 | 1.05 |
| No. Эксп. | Эксперимент No. 4. Гетероазеотропная ректификация в присутствии ДМФА | Эксперимент No. 5. Гетероазеотропная ректификация в присутствии Ац | Эксперимент No. 6. Гетероазеотропная ректификация в присутствии Ац | |||||||||
| Комп. | МБЦН | ПФД | main imp. | ∑ other imp. | МБЦН | ПФД | main imp. | ∑ other imp. | МБЦН | ПФД | main imp. | ∑ other imp. |
| $X_{F}^{i}$ | 97.410 | 0.894 | 1.505 | 0.191 | 96.400 | 0.689 | 2.845 | 0.066 | 98.379 | 0.399 | 1.206 | 0.016 |
| $K_{{{\text{enr}}}}^{{\frac{{\sum D}}{F}}}$ | 1.20 | 0.65 | 0.83 | 1.74 | 42.26 | 0 | 0 | 1.34 | 9.96 | 0 | 0 | 10.49 |
| $K_{{{\text{enr}}}}^{{\frac{W}{F}}}$ | 0.33 | 3.85 | 2.24 | 3.82 | 0.15 | 5.67 | 6.35 | 0 | 0.11 | 5.54 | 9.59 | 0 |
| ${{K}_{{{\text{sep}}}}}$ | 3.60 | 0.17 | 0.37 | 0.46 | 273.46 | 0 | 0 | $\infty $ | 87.55 | 0 | 0 | $\infty $ |
Рис. 6.
Зависимость величины коэффициента разделения (Ksep) от содержания целевого компонента в исходной смеси согласно данным Табл. 3. (а) МБЦН; (б) ПФД; (в) main imp.; (г) ∑other imp. (I) Весь диапазон; (II) область малых значений Ksep. $\bigcirc $ – без разделяющего агента; $\square $ – в присутствии ДМФА; $\vartriangle $ – в присутствии ацетона.
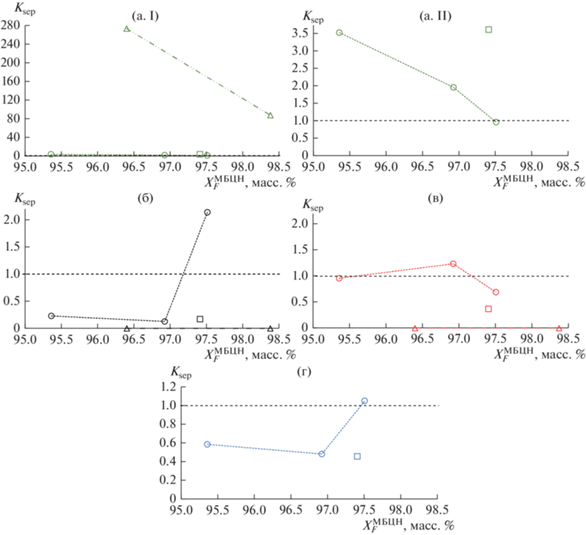
Рис. 7.
Зависимость величины коэффициента обогащения (Kenr) от содержания целевого компонента в исходной смеси согласно данным Табл. 3. (а) МБЦН; (б) ПФД; (в) main imp.; (г) ∑other imp. (I) Весь диапазон; (II) область малых значений Kenr. Синий – $K_{{{\text{enr}}}}^{{W/F}}$; красный – $K_{{{\text{enr}}}}^{{\sum D/F}}$. $\bigcirc $ – без разделяющего агента; $\square $ – в присутствии ДМФА; $\vartriangle $ – в присутствии ацетона.
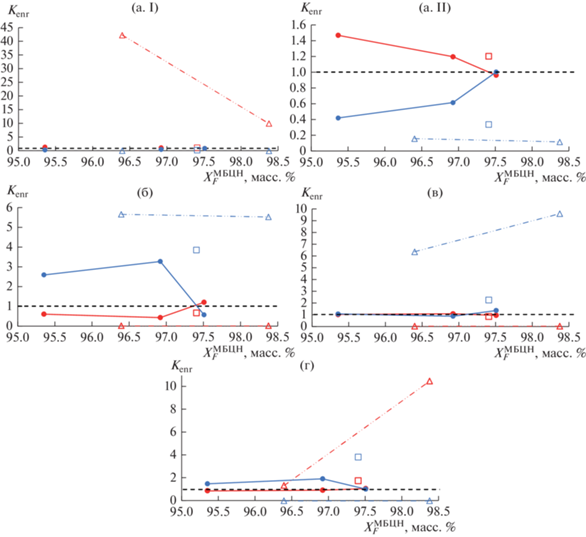
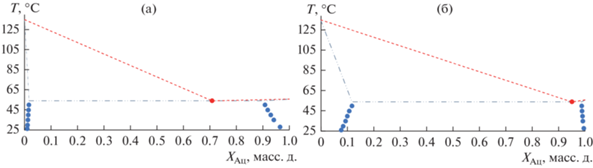
Экспериментальные данные о фазовом равновесии жидкость–жидкость в системе МБЦН–Ац в диапазоне температур от 25 до 50°С приведены в табл. 4; характеристики гетероазеотропа при атмосферном давлении для системы МБЦН–Ац приведены в табл. 5; Вид фазовой диаграммы жидкость–жидкость–пар изображен на рис. 8.
Представленные результаты были частично доложены и обсуждены на ECP 2023 [25].
Таблица 4.
Данные о фазовом равновесии жидкость-жидкость для системы МБЦН–Ац при атмосферном давлении 100.0 кПа
| T, °C | XАц, масс. д. | Фаза МБЦН xАц, мол. д. | Δ мол. д. | XАц, масс. д. | Фаза Ац xАц, мол. д. | Δ мол. д. |
|---|---|---|---|---|---|---|
| 26.2 ± 0.1 | 0.0105 | 0.0778 | ±0.0028 | – | – | – |
| 28.0 ± 0.1 | – | – | – | 0.9659 | 0.9956 | ±0.0002 |
| 30.0 ± 0.1 | 0.0116 | 0.0852 | ±0.0008 | – | – | – |
| 35.0 ± 0.1 | 0.0129 | 0.0939 | ±0.0013 | 0.9419 | 0.9923 | ±0.0002 |
| 40.0 ± 0.1 | 0.0138 | 0.1004 | ±0.0006 | 0.9309 | 0.9908 | ±0.0002 |
| 45.0 ± 0.1 | 0.0150 | 0.1081 | ±0.0008 | 0.9193 | 0.9891 | ±0.0001 |
| 50.0 ± 0.1 | 0.0166 | 0.1183 | ±0.0006 | 0.9090 | 0.9876 | ±0.0002 |
4. ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
Данные, приведенные в табл. 1 и табл. 2 наиболее полно отражают термодинамические ограничения на процесс ректификационного разделения. Наибольшую сложность вызывает отделение ПФД и так называемой “основной неидентифицированной примеси” (main imp.). Из данных табл. 2 и рис. 2а–2в следует, что при содержании МБЦН в исходной смеси ($X_{F}^{{{\text{МБЦН}}}} \approx 0.950$ масс. д.) метод обычной ректификации еще позволяет концентрировать целевой компонент в дистилляте. Однако, согласно данным табл. 3, когда содержание МБЦН в исходной смеси приближается к $X_{F}^{{{\text{МБЦН}}}} \approx 0.975$ масс. д., метод обычной ректификации становится неэффективным ($K_{{{\text{sep}}}}^{{{\text{МБЦН}}}} \to 1$ рис. 6a; $K_{{{\text{enr}}}}^{{{\text{МБЦН}}}} \to 1$ рис. 7а). Примесные ПФД (рис. 3а–3в) и main imp. (Рис. 4а–4в) все еще частично перераспределяются между кубовым продуктом и дистиллятом; при этом происходит инверсия величин Ksep (рис. 6б, 6в) и Kenr (рис. 7б, 7в). Для ∑other imp. (рис. 5а–5в) Ksep → 1 (рис. 6г) и Kenr → 1 (рис. 7г).
Добавление ДМФА несущественно, но все же интенсифицирует процесс разделения (рис. 2г) фракции МБЦН с содержанием целевого компонента $X_{F}^{{{\text{МБЦН}}}} \approx $ 0.975 масс. д. ($K_{{{\text{sep}}}}^{{{\text{МБЦН}}}}$ → 3.6 (рис. 6а); $K_{{{\text{enr}}}}^{{{\text{МБЦ}}{{{\text{Н}}}_{{W/F}}}}}$ → 0.33 и $K_{{{\text{enr}}}}^{{{\text{МБЦ}}{{{\text{Н}}}_{{\sum D/F}}}}}$ → 1.2 (рис. 7а)). ПФД (рис. 3г) и main imp. (рис. 4г) концентрируются в кубе колонны (Ksep < 1 рис. 6б, 6в), обогащение также происходит по кубовому продукту ($K_{{{\text{enr}}}}^{{W/F}}$ > 1 и $K_{{{\text{enr}}}}^{{\sum D/F}}$ < 1 рис. 7б, 6в). В случае ∑other imp. (табл. 2, табл. 3 и рис. 5г) наблюдается расхождение материального баланса; дать качественную оценку рассчитанных величин Ksep и Kenr для ∑other imp. не представляется возможным.
Согласно экспериментальным данным процесс гетероазеотропной ректификации в присутствии Ац оказался более эффективным по сравнению с ДМФА (рис. 2г и рис. 2д). Для фракций с $X_{F}^{{{\text{МБЦН}}}}$ = [0.964; 0.984] мол. д. интенсификация процесса разделения происходит на порядок:
• для МБЦН Ksep = [273.46; 87.55] (рис. 6а), $K_{{{\text{enr}}}}^{{W/F}}$ = [0.15; 0.11] и $K_{{{\text{enr}}}}^{{\sum D/F}}$ = [42.26; 9.96] (рис. 7а);
• ПФД (рис. 3д, 3е) и main imp. (рис. 4д, 4е) фактически отсутствуют в дистилляте и полностью концентрируются в кубе колонны Ksep → 0 (рис. 6б, 6в), $K_{{{\text{enr}}}}^{{{\text{ПФ}}{{{\text{Д}}}_{{W/F}}}}}$ ≈ 5.5, $K_{{{\text{enr}}}}^{{{\text{main\;imp}}{{.}_{{W/F}}}}}$ ≈ 10.0 и $K_{{{\text{enr}}}}^{{\sum D/F}}$ → 0 (рис. 7б, 7в).
• ∑other imp. в основном концентрируются в потоке дистиллята в начале гетероазеотропной ректификации (θ < 0.2 рис. 5д, 5е); они могут быть удалены из разделяемой смеси с первыми фракциями дистиллята. Для процесса в целом анализ по ∑other imp. (рис. 5д, 5е) показывает их полное отсутствие в кубе колонны Ksep → ∞ (табл. 3), $K_{{{\text{enr}}}}^{{W/F}}$ → 0 и $K_{{{\text{enr}}}}^{{\sum D/F}}$ ≈ [1.34; 10.49] (рис. 7г).
Таким образом, добавление Ац позволяет повысить концентрацию МБЦН с $X_{F}^{{{\text{МБЦН}}}} \approx $ ≈ 0.964 масс. д. до $X_{{\sum D}}^{{{\text{МБЦН}}}} > 0.998$ масс. д.; доля отбора данной фракции превышает 0.85 масс. д. от загрузки, выход по продукту составляет более $\eta = \frac{{{{m}_{{\sum D}}}X_{{\sum D}}^{{{\text{МБЦН}}}}}}{{{{m}_{F}}X_{F}^{{{\text{МБЦН}}}}}} > 88\% $.
В рамках настоящей работы для системы МБЦН–Ац были также получены данные о фазовом равновесии жидкость-жидкость в диапазоне температур от 25 до 50°C (табл. 4) и определены характеристика гетероазеотропа (табл. 5). Растворимости Ац в МБЦН (${{x}_{{{\text{Ац}}}}} = 0.0778 \to 0.1183$ мол. д.) и МБЦН в Ац (${{x}_{{{\text{Ац}}}}} = 0.9956 \to 0.9876$ мол. д.) растут с увеличением температуры; состав гетероазеотропа при атмосферном давлении существенно смещен в сторону Ац. Полученные данные (рис. 8) могут позволить оценить потери Ац в процессе отбора целевого компонента и рассчитать количество гетероазеотропообразующего агента, требуемого для организации компенсационного потока РА, что необходимо для разработки технологической схемы.
5. ЗАКЛЮЧЕНИЕ
Основной сложностью при разработке процессов разделения промышленной смеси изомерных продуктов реакции электрохимического фторирования декалина или нафталина является недостаток в научной литературе данных, прежде всего по составу реакционной смеси, свойствам ее составляющих и топологии фазовой диаграммы. Ввиду отсутствия таких данных поиск методов разделения происходит эмпирически и опирается на самые общие теоретические предпосылки. Тем не менее, несмотря на отсутствие полной номенклатуры примесей, в настоящей работе удалось предложить эффективный метод очистки МБЦН. Эффект был достигнут за счет добавления гетероазеотропообразующего агента Ац. Для бинарной смеси МБЦН–Ац также были получены экспериментальные данные о фазовом равновесии жидкость–жидкость и определены характеристики гетероазеотропа при атмосферном давлении.
Экспериментальные результаты настоящей работы представляют собой технологическое решение в рамках процесса очистки перфторированных циклоалканов и включают в себя ряд справочных данных, необходимых для его реализации.
Исследование выполнено за счет гранта Российского научного фонда № 22-29-00791, https://rscf.ru/project/22-29-00791/.
ОБОЗНАЧЕНИЯ
| Ац | ацетон |
| ДМФА | диметилформамид |
| МБЦН | перфтор(7-метилбицикло[4.3.0]нонан) |
| ПФД | перфтордекалин |
| РА | разделяющий агент |
| ЯМР | ядерный магнитный резонанс |
| F | исходная смесь |
| Fr | фракция дистиллята |
| ${{K}_{{{\text{enr}}}}}$ | коэффициент обогащения |
| ${{K}_{{{\text{sep}}}}}$ | коэффициент разделения |
| m | масса, г |
| main imp. | основная неидентифицированная примесь |
| P | давление, кПа |
| T | температура, °С |
| u | стандартная неопределенность |
| W | кубовый продукт |
| X | состав, масс. д. (маcс. %) |
| x | состав, мол. д. |
| ∑D | суммарный отобранный дистиллят |
| ∑other imp. | сумма прочих неидентифицированных примесей |
| $\eta $ | выход по продукту |
| θ | доля отбора, масс. д. |
| ИНДЕКСЫ | |
| i | компонент |
Список литературы
Aleshinskii V.V., Novikova M.D., Shabalin D.A. Method of Producing Perfluorocycloalkanes // Patent No. RU 2451006 C1. 20 May 2012. https://patents.google.com/patent/RU2451006C1
Gervits L.L., Snegirov V.F., Makarov K.N., Galakhov M.V., Mukhin V.Yu. Non-Chair Conformation of Cis Isomers of 1,4-Disubstituted Perfluorocyclohexanes // Bull. Acad. Sci. USSR Div. Chem. Sci. 1987. V. 36. P. 2664–2665. https://doi.org/10.1007/BF00957267
Gervits L.L. Perfluorocarbon-Based Blood Substitutes Russian Experience // Fluor. Med. 21st Century. 1994. Paper 22. P. 1–9. https://www.researchgate.net/publication/350153316_Perfluorocarbon-Based_Blood_Substitutes_Russian_Experience
Kambur P.S., Pashkevich D.S., Alekseev Yu.I., Yampolskii Yu.P., Alentev A.Yu. Interaction of Perfluorinated Fluids with Fluorine in Gas-Liquid Reactor // Russ. J. Appl. Chem. 2019. V. 92. № 5. P. 661–666. https://doi.org/10.1134/S1070427219050124
Moshnyag A.V., Khoroshilov A.V., Selivanova D.I., Aksenova D.M. Thermodynamics of Dissolved Nitrogen, Nitrous Oxide, and Ammonia in Perfluorodecalin // Russ. J. Phys. Chem. A. 2017. V. 91. № 11. P. 2117–2120. https://doi.org/10.1134/S0036024417100260
Moshnyaga A.V., Khoroshilov A.V., Semyashkin M.P., Mel’nikov V.V. Density of N2O Solutions in Perfluorodecalin As a Function of Concentration // Russ. J. Phys. Chem. A. 2018. V. 92. № 4. P. 719–723. https://doi.org/10.1134/S0036024418040222
Hassanalizadeh R., Nelson W.M., Naidoo P., Ramjugernath D. Measurement and Modeling of the Solubility of Tetrafluoromethane in Either Perfluoroheptane or Perfluorodecalin // J. Chem. Eng. Data. 2020. V. 65. № 10. P. 4862–4868. https://doi.org/10.1021/acs.jced.0c00461
Deepika D., Pandey S. Density and Dynamic Viscosity of Perfluorodecalin-Added n-Hexane Mixtures: Deciphering the Role of Fluorous Liquids // Liquids. 2023. V. 3. № 1. P. 48–56. https://doi.org/10.3390/liquids3010005
Polkovnichenko A.V., Lupachev E.V., Kisel’ A.V., Kvashnin S.Ya., Kulov N.N. Perfluoro(7-Methylbicyclo[4.3.0]Nonane) and Perfluoro(Butylcyclohexane): Physicochemical, Thermophysical, and Spectral Data // J. Chem. Eng. Data. 2023. V. 68. № 3. P. 499–517. https://doi.org/10.1021/acs.jced.2c00588
Wen-Zheng G., Wen-Juan C., Yu-Qing H., Wei-Yuan H. Study on the Vapour Phase Fluorination of Butyl Benzene with Cobalt Trifluoride // Acta Chimica Sinica. 1987. V. 45. № 7. P. 720–723. http://sioc-journal.cn/Jwk_hxxb/EN/Y1987/V45/I7/720
Hynes A.M., Shenton M.J., Badyal J.P.S. Plasma Polymerization of Trifluoromethyl-Substituted Perfluorocyclohexane Monomers // Macromolecules. 1996. V. 29. № 1. P. 18–21. https://doi.org/10.1021/ma950647h
Wells A.W., Diehl J.R., Bromhal G., Strazisar B.R., Wilson T.H., White C.M. The Use of Tracers to Assess Leakage from the Sequestration of CO2 in a Depleted Oil Reservoir, New Mexico, USA // Applied Geochemistry 2007. V. 22. №. 5. P. 996–1016. https://doi.org/10.1016/j.apgeochem.2007.01.002
Tuffin R., Paari O.L., Baker P., Brown C., Sage I.C. Material Combination // Patent No. EP3334801A1. 20 June 2018. https://patents.google.com/patent/EP3334801A1
Dionisio K.L., Phillips K., Price P.S., Grulke C.M., Williams A., Biryol D., Hong T., Isaacs K.K. The Chemical and Products Database, a Resource for Exposure-Relevant Data on Chemicals in Consumer Products // Scientific Data. 2018. 5. Article number: 180125. https://doi.org/10.1038/sdata.2018.125
Tuffin R., Paari O.L., Baker P., Brown C., Sage I.C. Material Combination // Patent No. EP3334801B1. 27 May 2020. https://patents.google.com/patent/EP3334801B1
Moore R.E., Clark L.C. Jr., Miller M.L. Synthesis and Biological Activity of Perfluoroadamantane and Some Closely Related Compounds // International Congress Series. 1979. 486 (Proc. Int. Symp. Perfluorochem. Blood Substitutes). P. 69–79. https://scifinder-n.cas.org/searchDetail/reference/ 64b11cf93459c50ab262f7cc/referenceDetails
Clark L.C. Jr., Moore R.E. Selecting Perfluorocarbon Compounds for Synthetic Blood // Patent No. US4289499 A. 15 September 1981. https://patents.google.com/patent/US4289499A
Rirando C.K.J., Robaato E.M. Determination of Critical Solution Temperatures of Perfluorocarbons // Patent No. JP55095868 A. 21 July 1980. https://worldwide.espacenet.com/patent/search/family/ 025491089/publication/JPS5595868A?q =JPS5595868A
Moore R.E., Clark L.C. Jr. Synthesis and Physical Properties of Perfluorocompounds Useful as Synthetic Blood Candidates // Oxygen Carrying Colloidal Blood Substitutes. 1982. (Int. Symp. Perfluorochem. Blood Substitutes, 5th). P. 50–60. https://scifinder-n.cas.org/searchDetail/reference/ 64b1334c3459c50ab2644c98/referenceDetails
Chung B.H., Lim, Y.T. Cell Labeling and Imaging Using Multifunctional Perfluorocarbon Nanoemulsion // Patent No. WO2009128610 A2. 22 October 2009. https://patents.google.com/patent/WO2009128610A2
Cacheris W.P., Richard T.J., Grabiak R.C., Lee A.C. Paramagnetic Complexes of N-Alkyl-N-Hydroxylamides of Organic Acids and Emulsions Containing Same for Magnetic Resonance Imaging (MRI) // Patent No. US5614170A. 25 March 1997. https://patents.google.com/patent/US5614170A
Ackerman J.L., Clark L.C. Jr., Thomas S.R. Methods for Detecting and Imaging a Temperature of an Object by Nuclear Magnetic Resonance // Patent No. US4558279A. 10 December 1985. https://patents.google.com/patent/US4558279A
Clark L.C. Jr. NMR Compositions for Indirectly Detecting a Dissolved Gas in an Animal // Patent No. US4775522A. 10 April 1988. https://patents.google.com/patent/US4775522A
Kulov N.N., Polkovnichenko A.V., Lupachev E.V., Rastunova I.L., Magomedbekov E.P. Fractionation of D/H and 18O/16O Water Isotopes in a Packed Distillation Column // Theor. Found. Chem. Eng. 2020. V. 54. P. 389–396. https://doi.org/10.1134/S0040579520030094
Polkovnichenko A.V., Lupachev E.V., Kisel’ A.V., Kvashnin S.Y., Kulov N.N. Perfluoro(7-methylbicyclo[4.3.0]-nonane) Purification from Close-Boiling Impurities by Heteroazeotropic Distillation Method. Eng. Proc. 2023, 37, 72. https://doi.org/10.3390/ECP2023-14621
Дополнительные материалы отсутствуют.
Инструменты
Теоретические основы химической технологии