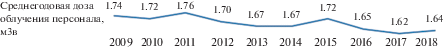Вестник РАН, 2021, T. 91, № 6, стр. 550-559
РОЛЬ РАДИОБИОЛОГИИ И РАДИАЦИОННОЙ МЕДИЦИНЫ В ОБЕСПЕЧЕНИИ ЗАЩИТЫ ОТ ВОЗДЕЙСТВИЯ ИОНИЗИРУЮЩИХ ИЗЛУЧЕНИЙ (ОТЕЧЕСТВЕННЫЙ ОПЫТ)
Л. А. Ильин a, *, А. С. Самойлов a, **
a Государственный научный центр Федеральный медицинский биофизический центр
им. А.И. Бурназяна ФМБА России
Москва, Россия
* E-mail: la_ilin@mail.ru
** E-mail: asamoilov@fmbcfmba.ru
Поступила в редакцию 30.12.2020
После доработки 30.12.2020
Принята к публикации 12.01.2021
Аннотация
В статье представлен отечественный опыт научных исследований по радиационной медицине, радиобиологии, радиотоксикологии, радиационной защите и сохранению здоровья работников атомной отрасли и населения, проживающего в районе расположения радиационно-опасных объектов Российской Федерации.
Кроме того, авторы уделяют внимание истории формирования и этапам становления радиационной медицины и радиобиологии в нашей стране, а также современным проектам и перспективам дальнейшего совершенствования медико-санитарного обеспечения работников атомной промышленности.
В нашей стране началом систематизированных исследований в области радиобиологии, радиотоксикологии, радиационной медицины и радиационной безопасности следует считать 29 июня 1946 г. [1]. Именно тогда специальным Постановлением Совета Министров СССР была создана радиационная лаборатория в качестве самостоятельного научно-исследовательского учреждения в системе Академии медицинских наук, в дальнейшем переименованная в Институт биофизики, который в настоящее время является Государственным научным центром им. А.И. Бурназяна Федерального медико-биологического агентства.
Уже в феврале 1947 г. президентом Академии медицинских наук Н.Н. Аничковым и директором этой лаборатории, членом-корреспондентом АМН СССР Г.М. Франком был представлен доклад о предлагаемых направлениях и планах работ радиационной лаборатории, который был заслушан на заседании научно-технического совета (НТС) Первого главного управления Совета Министров СССР, отвечавшего за разработку и создание атомного оружия в СССР. В обсуждении доклада приняли активное участие председатель НТС, научный руководитель атомного проекта академик И.В. Курчатов и крупнейшие учёные в этой области – академики Н.Н. Семёнов, Ю.Б. Харитон, И.К. Кикоин и другие.
В интересах исторической объективности следует отметить, что в конце 1946 г. в посёлке Сунгуль на Урале в недрах 9-го Управления НКВД была создана, к сожалению, мало кому известная и в настоящее время, совершенно секретная Лаборатория “Б”, в которой работали расконвоированные учёные, отобранные из лагерей ГУЛАГа, интернированные немецкие специалисты и вольнонаёмные научные сотрудники [2].
По имеющимся данным, к работам, начатым в радиационной лаборатории Института биофизики, с 1950-х годов было привлечено более 30 институтов и лабораторий Академии наук, Министерства здравоохранения, Министерства обороны, Минсредмаша, кафедр и лабораторий Минвуза. Координацию их деятельности осуществляла Проблемная комиссия № 1 союзного значения и секция № 5 НТС Минсредмаша [3].
Таким образом, история формирования радиационной медицины и радиобиологии в нашей стране связана с разработкой ядерного оружия и становлением атомной индустрии. У истоков развития названных наук стояли выдающиеся учёные и организаторы здравоохранения: член-корреспондент Академии наук СССР Г.М. Франк, академики Академии медицинских наук СССР А.А. Летавет, Ф.Г. Кротков, Е.И. Смирнов.
Одним из ведущих направлений научных исследований в области радиационной медицины и радиоэпидемиологии стало изучение отдалённых последствий облучения персонала и населения, включая оценку риска онкологических и генетических эффектов. Эта задача решается путём создания медико-дозиметрических регистров (МДР), социальная значимость которых определяется уникальным сочетанием накопленного исторического опыта отечественной радиационной медицины и современных высокоэффективных компьютерных технологий.
К основным медико-дозиметрическим регистрам можно отнести:
• Региональный регистр облучённых лиц из населённых пунктов бассейна реки Теча;
• Отраслевой регистр лиц, имеющих профессиональные заболевания;
• Отраслевой МДР ликвидаторов последствий аварии на ЧАЭС – работников Министерства атомной энергетики и промышленности;
• Регистр острых лучевых поражений человека;
• Региональный МДР персонала Сибирского химического комбината (Северск);
• Региональный МДР персонала Горно-химического комбината (Железногорск);
• Национальный радиационно-эпидемиологический Чернобыльский регистр (Обнинск).
На основе регистра персонала Производственного объединения “Маяк” создана объединённая когорта, насчитывающая около 57 тыс. работников, для которых имеются оценки доз внешнего излучения, а для части работников оценены уровни воздействия инкорпорированного плутония. Изучение отдалённых последствий облучения у этой когорты – приоритетное направление мирового уровня новизны.
В ГНЦ ФМБЦ им. А.И. Бурназяна ФМБА России с 1985 г. ведутся не имеющий аналогов в мире регистр и база данных по острым лучевым поражениям человека [4, 5]. На основе этих данных в 2016–2019 гг. выпущены русская и английская версии единственного в мире атласа “Острая лучевая болезнь человека” [6, 7], содержащего уникальные данные по клинической картине и дозиметрическим характеристикам более 150 лиц с острыми радиационными поражениями.
Проблеме научной разработки методов и способов защиты населения, оказавшегося в орбите радиационного воздействия аварийных объектов, всегда уделялось большое внимание. Огромный опыт, накопленный в России, освещён в многочисленных публикациях [3, 8]. В качестве примера приведём книгу “Крупные радиационные аварии: последствия и защитные меры”, переведённую на английский и японский языки [9], и фундаментальное издание “Радиационная медицина. Руководство для врачей-исследователей и организаторов здравоохранения” в четырёх томах под общей редакцией академика Л.А. Ильина [10].
Известно, что клиника ГНЦ ФМБЦ им. А.И. Бурназяна ФМБА России в силу многих причин имеет богатый опыт диагностики, лечения и медицинской реабилитации больных острой лучевой болезнью [10, т. 2]. На основании этого опыта впервые в мировой практике были разработаны классификация различных форм лучевых поражений как от внешнего, так и внутреннего облучения человека, принципы биодозиметрии и цитогенетические методы, а также предложены эффективные схемы лечения костномозговой формы острой лучевой болезни и местных лучевых поражений [6, 11].
Сегодня одно из активно развивающихся инновационных направлений – лечение местных лучевых поражений мезенхимальными стволовыми клетками в сочетании с микрохирургической техникой. Получены обнадёживающие экспериментальные результаты: разработанная ГНЦ ФМБЦ им. А.И. Бурназяна методика ускоряет заживление раневой поверхности в 2 и более раз. Подробнее с ними можно ознакомиться в международном рецензируемом журнале “Cells” от сентября 2020 г., где опубликована совместная статья специалистов ГНЦ ФМБЦ им. А.И. Бурназяна и Института ядерной и радиационной безопасности Франции [12].
В последние годы приоритетными являются научные исследования в области молекулярных, биохимических и генетических механизмов формирования лучевого поражения и пострадиационного восстановления, поскольку учёные сосредоточили свои усилия на исследовании роли ДНК и систем её репарации как одного из ключевых элементов живых систем. Радиобиологами изучались молекулярные и клеточные механизмы гибели облучённых клеток. Эти работы представляют значительный интерес как для формирования концептуальных основ патогенеза радиационных поражений, так и для разработки адекватных методов и способов профилактики и терапии лучевых поражений [13–16].
В настоящее время для выполнения задач по обеспечению радиационной безопасности персонала и населения крайне необходимы новые высокочувствительные технологии биодозиметрии, которые превосходят традиционно используемые цитогенетические тесты. Сейчас разрабатываются технологии биодозиметрии радиационных воздействий, позволяющие повысить порог чувствительности до 30–50 мГр, что крайне актуально для восстановления доз как у стажированных сотрудников, так и в результате радиационных аварий [17–20].
Широкомасштабные экспериментальные исследования в области радиотоксикологии выполнены отечественными учёными-медиками с участием физиков-дозиметристов. Детально изучена радиотоксикология основных биологически значимых радионуклидов: плутония-239, полония-210, цезия-137, стронция-90, йода-131 и др. [21–23]. Оценены поражающие дозы на критические органы и красный костный мозг, разработаны радиозащитные препараты [24].
На основе исследований по радиотоксикологии предложены и внедрены в практику радиофармпрепараты в качестве основы ядерной медицины и лекарственные соединения для предотвращения инкорпорации радиоактивных веществ и стимуляции их выведения из организма. В 1972 г. профессором Н.Н. Суворовым и его сотрудниками было синтезировано химическое соединение из группы биологических аминов [25]. Лекарственные формы этого соединения испытывались на различных воинских контингентах, включая экипажи двух атомных подводных лодок, возвратившихся с боевого дежурства. Этот радиопротектор получил официально название индралин, а его лекарственная форма в таблетках для перорального применения – Б-190, в честь А.И. Бурназяна. Масштаб проводимых доклинических и клинических экспериментальных исследований радиопротектеров сопоставим с масштабом современных исследований в области лечения новой коронавирусной инфекции. Неслучайно многие проводят аналогию между COVID и радиацией: оба врага невидимы, оба представляют серьёзную опасность для жизни и здоровья людей. В настоящее время Б-190 является табельным препаратом профилактического и немедленного применения при гамма- и гамма-нейтронном облучении на объектах ГК “Росатом”, Минобороны, МЧС и в других организациях. Препарат Б-190 включён также в противоаварийную аптечку персонала ГК “Росатом”. В качестве радиопротектора экстренного действия, применяемого в течение 2–3 часов после облучения, рекомендован также бета-лейкин отечественного производства, а в качестве средства комплексного лечения острой лучевой болезни – оригинальный препарат на основе ДНК – дезоксинат (деринат).
В отечественной линейке средств защиты от инкорпорации наиболее биологически значимых радионуклидов разработаны: препарат стабильного йода (KJ) в дозировке для взрослых и детей – при воздействии радионуклидов йода; сорбент ферроцин – для связывания в желудочно-кишечном тракте радиоактивного цезия; ионообменные сорбенты адсобар и полисурмин – для поглощения радионуклидов стронция. Для ускорения выведения из организма радиоактивных веществ применяются комплексообразующие препараты: оксатиол для борьбы с инкорпарацией полония-210, пентацин-ДТПА (тринатрийкальциевая соль дитилентриаминпентауксусной кислоты) и соответственно цинковая соль этого соединения – цинкацин для стимуляции выведения радиоактивных изотопов редкоземельных элементов, плутония и трансплутониевых элементов.
Среди различных методов и способов защиты человека от техногенного облучения исключительная роль принадлежит регламентации (нормированию) радиационного воздействия на людей и жёсткому соблюдению соответствующих правил. Инициатором этих работ был И.В. Курчатов. В начале 1949 г. он поручил Институту биофизики разработку и обоснование временных предельно допустимых уровней облучения профессиональных работников от воздействия осколочных радионуклидов – продуктов деления урана и плутония. Заодно Игорь Васильевич передал учёным института сведения, в то время строго секретные, о свойствах этих радиоактивных веществ.
В 1952 г. при Министерстве здравоохранения СССР была создана Национальная Комиссия по радиационной защите, основной задачей которой стала разработка общегосударственных норм радиационной безопасности, выполнение которых было обязательным для всех предприятий, где применялись, производились, перерабатывались, хранились и транспортировались радиоактивные вещества. В 1960 г. были утверждены первые допустимые уровни, затем – “Нормы радиационной безопасности” и “Основные санитарные правила обеспечения радиационной безопасности”. На основе многолетнего опыта радиационно-гигиенического сопровождения работ на всех звеньях ядерного топливного цикла были разработаны “Санитарные правила проектирования предприятий и установок атомной промышленности” и “Санитарные правила проектирования и эксплуатации атомных станций”. В настоящее время нами завершена подготовка нового регулирующего документа – Санитарных правил “Обеспечение радиационной безопасности при выводе из эксплуатации блока атомной станции”.
В результате внедрения в практику этих документов, при строгом соблюдении производственной дисциплины на объектах ГК “Росатом” в настоящее время, по данным дозиметрического мониторинга, среднегодовая доза облучения персонала не превышает установленной нормами радиационной безопасности (2009) величины – 20 мЗв в год – и составляет доли от этого значения (рис. 5).
Рис. 1.
Основоположники радиационной медицины и радиобиологии Г.М. Франк, А.А. Летавет, Ф.Г. Кротков, Е.И. Смирнов

Рис. 2.
Академик РАН, почётный президент ГНЦ ФМБЦ им. А.И. Бурназяна ФМБА России Л.А. Ильин с изданием “Радиационные аварии”

Опыт радиационно-гигиенических работ в период создания и функционирования предприятий атомной индустрии определил требования учёных-медиков о необходимости создания трёхзональной системы при планировании, строительстве и эксплуатации соответствующих объектов. Речь идёт о последовательности прохождения работников из так называемых грязных зон радиоактивного загрязнения в чистые помещения под постоянным дозиметрическим контролем. Внедрение этого принципа защиты от радиации сыграло огромную роль в обеспечении радиационной безопасности работников атомной отрасли.
Относительно соблюдения регламентов, о которых говорилось выше, можно привести следующий факт: по сравнению с 2000 г. число работников ядерного топливного цикла, имеющих индивидуальную эффективную дозу облучения 20 мЗв/год, к сегодняшнему дню сократилось с 547 человек практически до единичных случаев. Напомним, что под дозиметрическим контролем в ГК “Росатом” состоят 65 600 специалистов. За последние 23 года среди работников корпорации не было зафиксировано случаев острой лучевой болезни – лишь два случая местных радиационных поражений были установлены в 2012 г.
Благодаря реализации научно обоснованной системы медицинского обслуживания и санитарно-гигиенического регулирования в области радиационной безопасности показатели профессиональной заболеваемости, которые с учётом данных ведомственного регистра о профессиональных заболеваниях среди работников ГК “Росатом” в сравнении с профессиональной заболеваемостью в других отраслях промышленности весьма невысоки, а вклад заболеваний, которые можно связать с радиационным фактором, составляют единицы процентов. Это единичные случаи: на протяжении многих лет ионизирующее излучение выступает в качестве причины профессиональных заболеваний (онкологических) только у стажированных работников в горнорудном уранодобывающем производстве.
В последние годы по инициативе руководства Госкорпорации “Росатом” выполняется амбициозная программа, получившая название “Прорыв”, посвящённая ядерным энерготехнологиям нового поколения и новой платформе ядерной энергетики. Это создание замкнутого ядерного топливного цикла на базе реакторов на быстрых нейтронах, работающих на новом виде ядерного топлива – смешанном нитридном уран-плутониевом топливе. Располагая большим опытом исследований по медико-гигиеническому и дозиметрическому сопровождению разработки технологий и производства оксидного уран-плутониевого топлива и регенерированного урана, учёные и специалисты ГНЦ ФМБЦ им. А.И. Бурназяна в настоящее время изучают радиационную обстановку и готовят медико-технические требования к обеспечению радиационной безопасности персонала опытного демонстрационного комплекса, создаваемого на одном из атомных комбинатов. Следующим этапом будет обоснование проектных решений и требований для обеспечения радиационной безопасности при промышленной реализации проекта “Прорыв” для профессиональных работников и населения, проживающего в зоне его влияния.
В рамках дальнейшего совершенствования медико-санитарного обеспечения работников атомной индустрии приоритетными являются следующие научно-практические направления:
• совершенствование и разработка новых медико-санитарных технологий, направленных на обеспечение радиационной безопасности;
• завершение создания единой системы радиационно-гигиенического реагирования и медицинских аспектов защиты людей в случае радиационных аварий;
• дальнейший поиск и разработка методов и средств профилактики и лечения лучевой патологии человека, включая инновационные биомедицинские технологии;
• совершенствование методологии изучения отдалённых последствий облучения персонала радиационно-опасных объектов и населения;
• осуществление специалистами ФМБА России международного взаимодействия по ядерному обнаружению, ситуационному реагированию и противодействию ядерному терроризму [26]; это новое научное направление – медико-биологическая ядерная криминалистика;
• постепенный переход к профилактическому направлению в отношении выявления профессиональных и социально-значимых заболеваний, вносящих основной вклад в трудопотери атомной отрасли.
Одно из важнейших направлений в области защиты человека от воздействия радиоактивных веществ – научные исследования и разработки с целью создания средств индивидуальной защиты. В начальный период становления атомной отрасли, когда концентрация радиоактивных аэрозолей в воздухе рабочих зон в большинстве случаев превышала нормативные значения в сотни и тысячи раз, актуальной задачей было создание средств защиты органов дыхания. Примером успешного решения этой проблемы стало создание в конце 1950-х годов знаменитых одноразовых респираторов ШБ-1 “Лепесток” из так называемой петряновской фильтрующей ткани (по имени выдающегося отечественного учёного академика И.В. Петрянова-Соколова). Их эффективность при малом сопротивлении дыханию достигала 99%. Эта работа была отмечена Ленинской премией [27].
К началу 2019 г. выпуск ШБ-1 “Лепесток” достиг 6 млрд экземпляров, и он с успехом используется во многих отраслях промышленности. На рисунке 7 представлены разработанные при участии специалистов Института биофизики изолирующие костюмы для работы с радиоактивными веществами, в том числе с принудительной подачей воздуха. Отвечая на запросы времени, ГНЦ ФМБЦ им. А.И. Бурназяна совместно с НИЦ эпидемиологии и микробиологии им. Н.Ф. Гамалея Минздрава России создали технологию радиационной обработки спецодежды, используемой при работе с коронавирусной инфекцией, с целью её повторного применения в случае чрезвычайных ситуаций.
Обращаясь к проблеме радиационных аварий, отметим, что, по данным регистра ФМБЦ им. А.И. Бурназяна, в СССР в общей сложности произошло 352 радиационных аварии в учреждениях гражданского профиля и на объектах Минсредмаша, Министерства атомной энергетики и промышленности и Министерства обороны (табл. 1). Общее число инцидентов составило 748 случаев, из них острая лучевая болезнь (ОЛБ) различной степени тяжести установлена у 352 человек, было зарегистрировано 70 летальных исходов. Наибольшее число случаев ОЛБ – 134, произошло в результате аварии на Чернобыльской АЭС. Речь идёт о двух контингентах – свидетелях аварии и пожарных. Среди так называемых ликвидаторов – контингента, привлечённого к аварийным работам на ЧАЭС и в 30-километровой зоне, случаев ОЛБ установлено не было, равно как и у населения, проживавшего в зонах радиоактивного загрязнения [4, 5].
Таблица 1.
Регистр радиационных аварий и инцидентов на территории СССР и России, 1949–2016 гг.
| Вид инцидента | Число инцидентов | Число пострадавших | ||
|---|---|---|---|---|
| всего | с ОЛБ | умершие | ||
| Инциденты с источниками излучений | 90 | 154 | 45 | 15 |
| Рентгеновские установки и ускорители | 43 | 52 | – | – |
| Реакторные инциденты и потеря контроля над критичностью делящегося материала (без ЧАЭС 1986 г.) | 33 | 82 | 73 | 13 |
| Чернобыльская авария 1986 г. | 1 | 134 | 134 | 28 |
| Случаи с МЛП на ПО “Маяк” (1949–1956) | 168 | 168 | – | – |
| Аварии на атомных подводных лодках и нештатные ситуации на ядерных испытаниях | 5 | 141 | 93 | 12 |
| Другие инциденты | 12 | 17 | 7 | 2 |
| Итого | 352 | 748 | 352 | 70 |
Через год после событий в Чернобыле Институт биофизики направил фундаментальный отчёт в Научный комитет по действию атомной радиации Организации Объединённых Наций – наиболее авторитетный в мире научный орган в этой области. В докладе Генеральной Ассамблее ООН в 1988 г. этот комитет следующим образом оценил деятельность учёных-медиков: “Представленная СССР информация является исчерпывающей и очень ценной. Комитет считает, что он в долгу перед всеми авторами за их готовность поделиться своим опытом и желает отметить их профессиональное мастерство и человеческое сострадание, проявленное в связи со столь трагическими обстоятельствами” [28].
Проблеме научной разработки методов и способов защиты населения, оказавшегося в орбите радиационного воздействия аварийных объектов, всегда уделялось большое внимание. Следует напомнить, что ещё за 19 лет до чернобыльской аварии отечественными учёными на основании собственных экспериментальных данных и испытаний на добровольцах была составлена и утверждена Минздравом СССР “Инструкция по йодной профилактике в случае радиационных аварий на ядерных реакторах”, а в 1970 г. Минздрав СССР утвердил несекретные “Временные методические указания для разработки мероприятий по защите населения в случае аварий ядерных реакторов”, подготовленные также под руководством Института биофизики [29].
В рамках анализа радиационных аварий чернобыльская катастрофа, прежде всего в силу её масштабов, занимает особое место. Напомним, что в результате этой аварии радиоактивному загрязнению (внутри изолинии 1 Кюри/км2) подверглась территория европейской части СССР площадью около 150 тыс. км2, на которой проживало порядка 6.2 млн человек. В кратчайшие сроки было необходимо решить задачу выработки научно обоснованной стратегии действий государства по защите населения в этой беспрецедентной и жизненно важной ситуации. Группой учёных, работавших на аварийном объекте в сотрудничестве со специалистами Госкомгидромета и агропромышленного комплекса под научным руководством академиков Л.А. Ильина и Ю.А. Израэля, впервые в мировой практике в течение двух недель после аварии были разработаны “Рекомендации по критериям возможности проживания населения, необходимости отселения и временной эвакуации на территории, подвергшейся радиоактивному загрязнению в результате аварии на ЧАЭС”. В этом документе, утверждённом на высшем уровне 22 мая 1986 г., были установлены аварийные регламенты облучения населения – 100 мЗв за первый год после аварии (с последующим снижением этой величины) и впервые осуществлено зонирование территорий по уровням гамма-излучения на местности. В зонах с высокими уровнями радиоактивного загрязнения (зоны жёсткого контроля), где без принятия мер ограничения дозовые нагрузки на людей могли превысить 100 мЗв/год, проживало 273 тыс. человек в 789 населённых пунктах. В этих зонах, согласно Рекомендациям, были введены способы ограничения жизнедеятельности населения – запрет на потребление молока и местных пищевых продуктов с заменой на “чистые” продукты, преимущественное пребывание людей в зданиях, а не на открытой местности и т.п. В результате удалось снизить дозовую нагрузку в 3 раза по сравнению с установленными регламентами. Обеспечение радиационной безопасности населения, проживавшего в зонах радиоактивного загрязнения, потребовало многочисленных расчётов допустимых уровней внутреннего облучения (100 мЗв общего облучения – временный аварийный норматив). В этот же период были разработаны методические рекомендации по радиационно-гигиеническому контролю на местах и на предприятиях по производству пищевых продуктов.
Мероприятия по защите людей, включая анализ радиационной обстановки и дозовые нагрузки на население пострадавших районов, позволили учёным-медикам сделать предварительный прогноз возможных отдалённых последствий в виде онкологической заболеваемости [3]. Этот прогноз свидетельствовал о крайне малой вероятности заболеваний радиационно индуцированными лейкозами и солидарными раками, за исключением ожидаемого роста числа злокачественных опухолей щитовидной железы среди детей. В последнем случае свою негативную роль сыграли причины административного, организационного, бюрократического характера, помешавшие практической реализации разработанных задолго до чернобыльской аварии методов и способов йодной профилактики и других рекомендаций. Указанные выше прогнозы были подтверждены рядом зарубежных и отечественных специалистов.
В результате аварии на ЧАЭС также остро встал вопрос о судьбе трёхмиллионного населения г. Киева – столицы Украины, так как 7 мая 1986 г. Политбюро ЦК Украины планировало эвакуацию всего детского населения, а следовательно и большинства взрослых в не затронутые радиацией районы. Основываясь на научных данных о радиационной обстановке и её прогнозе Ю.А. Израэль и Л.А. Ильин на заседании Политбюро выступили против этого предложения. В результате эта акция с очевидными тяжёлыми социально-экономическими последствиями была предотвращена, а обоснованность позиции учёных в дальнейшем полностью подтвердилась.
В заключение хотелось бы отметить, что впервые за всю историю нашей страны Российская академия наук посвящает Научную сессию Общего собрания юбилейной дате отдельной отрасли. История Атомного проекта свидетельствует, скорее, не о вкладе Академии наук в развитие атомной отрасли, а о её приоритетной роли в этом эпохальном начинании. Пророческие слова выдающегося российского учёного-физиолога академика И.П. Павлова, сказанные им более 100 лет тому назад, в 1914 г., как никогда созвучны проблемам сегодняшнего дня: “Что нам, русским, нужно сейчас в особенности – это пропаганда научных стремлений, обилие научных средств и страстная научная работа. Очевидно, что наука становится главнейшим рычагом жизни народов; без неё нельзя удержать ни самостоятельность, ни, тем более, достойного положения в мире”.
Список литературы
Наука и общество: история советского Атомного проекта (40–50-е годы) / Труды международного симпозиума ИСАП-96. М.: ИздАТ, 1997.
Емельянов Б.М. Лаборатория “Б”. Сунгульский феномен / Б.М. Емельянов, В.С. Гаврильченко. Снежинск: Изд-во РФЯЦ–ВНИИТФ, 2000.
Ильин Л.А. Реалии и мифы Чернобыля. 2-е изд. испр. и доп. М.: НПП “ALARA”, 1996.
Ильин Л.А., Соловьёв В.Ю. Непосредственные медицинские последствия радиационных инцидентов на территории бывшего СССР // Медицинская радиология и радиационная безопасность. 2004. № 6. С. 37–48.
Соловьёв В.Ю., Самойлов А.С., Бушманов А.Ю., Ильин Л.А. Острые радиационные поражения у пострадавших в радиационных инцидентах на территории бывшего СССР 1949–1991 гг. и Российской Федерации 1992–2015 гг. (обзор) // Ядерные технологии на страже здоровья: сборник тезисов Международного научно-практического форума. М.: ФГБУ ГНЦ ФМБЦ им. А.И. Бурназяна ФМБА России, 2016. С. 24–26.
Барабанова А.В., Баранов А.Е., Бушманов А.Ю. и др. Острая лучевая болезнь человека. Атлас / Под ред. А.С. Самойлова и В.Ю. Соловьёва. М.: ФГБУ ГНЦ ФМБЦ им. А.И. Бурназяна ФМБА России, 2016–2017.
Atlas. Acute radiation syndrom / A.V. Barabanova, A.E. Baranov, A.Yu. Bushmanov et al. / Ed. by A.S. Samoilov and V.Yu. Soloviev. M.: SRC–FMBC. 2019.
Аветисов Г.М., Антипин Е.Б., Барабанова А.В. и др. Организация санитарно-гигиенических и лечебно-профилактических мероприятий при радиационных авариях: руководство / Под ред. Л.А. Ильина. М.: Всероссийский центр медицины катастроф “Защита” Росздрава, 2005.
Алексахин Р.М., Булдаков Л.А., Губанов В.А. и др. Крупные радиационные аварии: последствия и защитные меры / Под ред. Л.А. Ильина, В.А. Губанова. М.: ИздАТ, 2001.
Радиационная медицина. Руководство для врачей-исследователей и организаторов здравоохранения: в 4-х томах / Под общей ред. Л.А. Ильина. М.: ИздАТ, 1999–2004.
Гуськова А.К., Галстян И.А., Гусев И.А. Авария на Чернобыльской атомной станции (1986–2011): последствия для здоровья, размышления врача / Под общей ред. А.К. Гуськовой. М.: ФМБЦ им. А.И. Бурназяна, 2011.
Brunchukov V., Astrelina T., Usupzhanova D. et al. Evaluation of the Effectiveness of Mesenchymal Stem Cells of the Placenta and Their Conditioned Medium in Local Radiation Injuries // Cells. 2020. № 9 (12). 2558.
Озеров И.В., Осипов А.Н. Особенности индукции и репарации двунитевых разрывов ДНК в клетках млекопитающих при действии редкоионизирующего излучения с различной мощностью дозы. М.: ФГБУ ГНЦ ФМБЦ им. А.И. Бурназяна ФМБА России, 2016.
Tsvetkova A., Ozerov I.V., Pustovalova M. et al. γH2AX, 53BP1 and Rad51 protein foci changes in mesenchymal stem cells during prolonged X-ray irradiation // Oncotarget. 2017. № 8(38). P. 64317–64329.
Osipov A.N., Grekhova A., Pustovalova M. et al. Activation of homologous recombination DNA repair in human skin fibroblasts continuously exposed to X-ray radiation // Oncotarget. 2015. № 6(29). P. 26876–26885.
Babayan N., Vorobyeva N., Grigoryan B. et al. Low repair capacity of DNA double-strand breaks induced by laser-driven ultrashort electron beams in cancer cells // International Journal of Molecular Sciences. 2020. № 21(24). pii 9488.
Rapid Diagnosis in Populations at Risk from Radiation and Chemicals / Ed. by A. Cebulska-Wasilewska, A.N. Osipov and F. Darroudi. IOS Press. V. 73. NATO Science for Peace and Security Series – E: Human and Societal Dynamic. November 2010.
Pustovalova M., Astrelina T.A., Grekhova A. et al. Residual γH2AX foci induced by low dose x-ray radiation in bone marrow mesenchymal stem cells do not cause accelerated senescence in the progeny of irradiated cells // Aging (Albany NY). 2017. № 9 (11). P. 2397–2410.
Osipov A.N., Pustovalova M., Grekhova A. et al. Low Doses of X-rays Induce Prolonged and ATM-independent Persistence of γH2AX Foci in Human Gingival Mesenchymal Stem Cells // Oncotarget. 2015. № 6(29). P. 27275–27287.
Ulyanenko S., Pustovalova M., Koryakin S. et al. Formation of γH2AX and pATM Foci in Human Mesenchymal Stem Cells Exposed to Low Dose-Rate Gamma-Radiation // International Journal of Molecular Sciences. 2019. № 20(11). P. 2645.
Ильин Л.А., Архангельская Г.В., Константинов Ю.О., Лихтарев И.А. Радиоактивный йод в проблеме радиационной безопасности / Под ред. Л.А. Ильина. М.: Атомиздат, 1972.
Абрамов Ю.В. и др. Плутоний. Радиационная безопасность / Под общей ред. Л.А. Ильина. М.: ИздАТ, 2005.
Борисов Н.Б., Ильин Л.А., Маргулис У.Я. и др. Радиационная безопасность при работе с полонием-210 / Под ред. И.В. Петрянова, Л.А. Ильина. М.: Атомиздат, 1980.
Калистратова В.С., Беляев И.К., Жорова И.К. и др. Радиобиология инкорпорированных радионуклидов / Под ред. В.С. Калистратовой. Изд. 2-е, переработанное. М.: ГНЦ ФМБЦ им. А.И. Бурназяна ФМБА России, 2016.
Ильин Л.А., Рудный Н.М., Суворов Н.Н. и др. Индралин – радиопротектор экстренного действия. Противолучевые свойства. Фармакология, механизм действия, клиника. М.: ГНЦ ФМБЦ им. А.И. Бурназяна ФМБА России, 1994.
Грачёв М.И., Ильин Л.А., Квачева Ю.Е. и др. Медицинские аспекты противодействия радиологическому и ядерному терроризму / Под общей ред. Л.А. Ильина. М.: ГНЦ ФМБЦ им. А.И. Бурназяна ФМБА России, 2018.
Петрянов И.В., Кощеев Ф.С., Басманов П.И. и др. Лепесток. Лёгкие респираторы. 2-е изд., перераб. и доп. М.: Наука, 2015.
Резолюции 43-й сессии Генеральной Ассамблеи ООН (1988–1989 годы) https://www.un.org/ru/ga/43/docs/43res.shtml
Дибобес И.К., Ильин Л.А., Козлов В.М. и др. Временные методические указания для разработки мероприятий по защите населения в случае аварии ядерных ректоров. М., 1971.
Дополнительные материалы отсутствуют.