Высокомолекулярные соединения (серия С), 2022, T. 64, № 2, стр. 251-264
АМИНО- И СУЛЬФОСОДЕРЖАЩИЕ МОЛЕКУЛЯРНЫЕ ЩЕТКИ НА ОСНОВЕ ОЛИГОЭТИЛЕНГЛИКОЛЬ(МЕТ)АКРИЛАТОВ – СИНТЕЗ И СВОЙСТВА В РАСТВОРАХ
А. С. Симагин a, b, М. В. Савинова a, Д. М. Каморин a, b, *, О. А. Казанцев a, Д. В. Орехов a, М. А. Симонова c, С. В. Орехов a
a Нижегородский государственный технический университет им. Р.Е. Алексеева
603950 Нижний Новгород, Минина, 24, Россия
b Национальный исследовательский Нижегородский государственный университет им. Н.И. Лобачевского
603022 Нижний Новгород, пр. Гагарина, 23, Россия
c Институт высокомолекулярных соединений Российской академии наук
199004 Санкт-Петербург, Большой пр., 31, Россия
* E-mail: d.kamorin@mail.ru
Поступила в редакцию 25.04.2022
После доработки 05.07.2022
Принята к публикации 19.07.2022
- EDN: FEVDWV
- DOI: 10.31857/S2308114722700169
Аннотация
Радикальной сополимеризацией в растворах (вода, этилацетат, толуол) метакриловых эфиров, содержащих олигоэтиленгликолевые и(или) олигопропиленгликолевые блоки разной длины и порядка расположения, с 2-акриламидо-2-метилпропансульфокислотой или N-(3-диметиламинопропил)метакриламидом синтезированы амфифильные сульфо- или аминосодержащие молекулярные щетки. При сополимеризации с 2-акриламидо-2-метилпропансульфокислотой в воде композиционная однородность образующихся сополимеров значительно возрастает по мере повышения концентрации исходных растворов. Показано практически отсутствующее влияние строения макромономеров на константы их сополимеризации с N-(3-диметиламинопропил)метакриламидом в органических растворителях. Синтезированные аминосодержащие молекулярные щетки проявляют стимулчувствительные свойства в водных растворах, причем порядок расположения гидрофильного и гидрофобного блоков в боковых цепочках макромолекул влияет на зависимости температуры фазовых переходов от концентрации полимеров и рН.
ВВЕДЕНИЕ
В последние двадцать лет олиго(этиленгликоль)(мет)акрилаты (ОЭГ-МА) стремительно вошли в число наиболее исследуемых мономеров, что связано с несколькими факторами [1–14]. Во-первых, такие макромономеры обладают высокой (на уровне широко используемых алкил(мет)акрилатов) активностью в радикальной гомо- и сополимеризации; на их основе могут быть легко синтезированы полимеры самого разного состава, архитектуры, молекулярно-массовых характеристик [5–7]. Для разработки методов получения полимеров с заданными свойствами были изучены закономерности как традиционной [8, 9], так и разных вариантов контролируемой радикальной полимеризации [15–17] с участием ОЭГ-МА разного строения. Во многих исследованиях последних лет по этой теме образующиеся полимеры отнесены к классу молекулярных щеток, получаемых методом “прививка через” [18, 19]. Вторым фактором популярности ОЭГ-МА можно назвать доступность исходного сырья и относительную простоту технологий их получения, что, в случае выявления высокой эффективности действия соответствующих сополимеров, делает возможным организацию их рентабельного производства. Данное обстоятельство продемонстрировал пример применения карбоксилатных сополимеров ОЭГ-МА в качестве суперпластификаторов для бетона [20]. Третьей и наиболее важной причиной интереса к ОЭГ-МА служат уникальные свойства их (со)полимеров, которые, благодаря сочетанию гидрофобной основной цепи макромолекул и гидрофильному блоку олигоэтиленгликоля (ОЭГ) в боковой цепи, обладают ярко выраженной амфифильностью и в водных растворах проявляют термочувствительные свойства (т.е. осуществляют обратимые фазовые переходы в узких температурных интервалах) [3, 14, 21]. При этом низшие критические значения температуры растворения или определяемые при заданной концентрации полимера значения температуры фазовых переходов (ТФП) легко регулируются изменением длины ОЭГ-блока либо введением в полимер дополнительных гидрофобных (обычно, высших н-алкильных) фрагментов в молекулах исходных ОЭГ-МА, либо сополимеризацией с алкилметакрилатами или н-алкилакриламидами [21–23]. Поэтому фазовые переходы могут осуществляться в заданных температурных интервалах, в том числе соответствующих температуре человеческого тела [9, 24]. В сочетании с такими свойствами ОЭГ-содержащих полимеров, как биосовместимость и биоразлагаемость, это привело многих исследователей к оценке сополимеров ОЭГ-МА в качестве наиболее перспективных наноносителей для контролируемой доставки лекарственных веществ в организме по сравнению с другими полимерами, в том числе получаемыми на основе N-изопропилакриламида (предыдущего лидера своеобразного “рейтинга перспективности”) [25, 26]. В целом, возможность регулирования поведения (со)полимеров ОЭГ-МА в растворителях за счет варьирования их гидрофильно-гидрофобных свойств определяет задачи многих проводимых исследований. Для контролируемой доставки лекарственных веществ в организме важными свойствами таких полимеров являются ТФП, формирование и распад мицеллярных наноконтейнеров, проницаемость макромолекул через липофильные слои и т.д. Еще одним развиваемым направлением исследований выступает разработка каталитических систем на основе сополимеров ОЭГ-МА [27, 28], и в этом случае рассматриваются не только их амфифильные свойства, но и возможность введения аминных, сульфокислотных и других групп, способных как непосредственно оказывать каталитический эффект, так и обеспечивать связывание полимера с другими активными компонентами каталитических систем. Кроме того, введение ионогенных групп придает сополимерам ОЭГ-МА рН-чувствительные свойства, что дополнительно расширяет возможности применения материалов в различных целях. Новым направлением исследований является также более мягкое регулирование амфифильного баланса сополимеров ОЭГ-МА путем введения в их состав умеренно гидрофобных блоков олигопропиленгликоля (ОПГ) [29, 30], дополнительным достоинством которых, по сравнению с гидрофобными н-алкильными блоками, считаются биосовместимость и биоразлагаемость.
В настоящей работе впервые рассмотрены особенности радикальной сополимеризации в растворителях ОЭГ- и(или) ОПГ-содержащих метакриловых эфиров разного строения с 2-акриламидо-2-метилпропансульфокислотой (АПСК) или N-(3-диметиламинопропил)метакриламидом (ДАПА) с образованием амфифильных ионогенных молекулярных щеток четырех типов – сульфо- или аминосодержащих полимеров с моноблоками ОЭГ или ОПГ в боковых цепочках (МЩ-I, МЩ-II), а также с диблочными боковыми цепочками при разном расположении ОЭГ- и ОПГ-фрагментов относительно основной макромолекулярной цепи (МЩ-III, МЩ-IV):
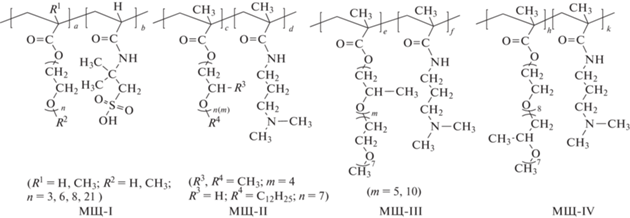
Таким образом, для синтеза молекулярных щеток использован метод “прививка через” [18] – радикальная сополимеризация с участием макромономеров, что позволяет четко контролировать состав и структуру получаемых продуктов. Кроме закономерностей синтеза щеток, в работе рассмотрено влияние их состава и структуры на растворимость в органических растворителях и в воде (в том числе в зависимости от температуры и рН).
В использованных далее обозначениях мономеров и полимеров среднее содержание звеньев в ОЭГ- и ОПГ-блоках показано как индекс в Еn и Рm соответственно. В обозначениях исходных макромономеров слева направо приводятся количество атомов углерода в концевом углеводородном радикале (для концевой гидроксильной группы указано Н), затем – последовательно расположенные от этого радикала ОЭГ- и(или) ОПГ-блоки (Еn и(или) Рm), далее обозначен метакрилоильный (М) или акрилоильный (А) полимеризующийся фрагмент. Например, общая структура метоксиолиго(этиленгликоль)метакрилатов представлена как С1ЕnМ. При обозначении составов сополимеров показаны использованные сомономеры, а в скобках дано мольное содержание кислотных или аминных звеньев в полимере. Пример – молекулярная щетка типа МЩ-I для случая сополимера С1Е8М и АПСК при содержании сульфокислотных звеньев 50% имеет обозначение С1Е8М–АПСК(50).
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
В работе использовали ДАПА и АПСК фирмы “Sigma Aldrich”. Исходные (мет)акриловые макромономеры синтезировали по методике [10] методом этерификации метакриловой или акриловой кислот соответствующими спиртами, содержащими ОЭГ- и(или) ОПГ-блоки. Для синтеза додетоксиолиго(этиленгликоль)метакрилатов (R4 = С12Н25), содержащих 7 или 10 этиленгликолевых звеньев, применяли промышленные этоксилированные жирные спирты, марок АЛМ-7 и АЛМ-10 соответственно (Общество с ограниченной ответственностью “Завод синтанолов”, Россия). Методы синтеза остальных исходных спиртов описаны в работе [10]. Молекулярную массу и среднее содержание звеньев в ОЭГ- и ОПГ-блоках рассчитывали по данным спектроскопии ЯМР 1Н и по гидроксильному числу (согласно ISO 4326:1980). Для определения состава синтезированных исходных спиртов и макромономеров (а также выделенных полимеров) применяли метод спектроскопии ЯМР 1Н с использованием прибора “Agilent DD2 400”.
Синтез молекулярных щеток
Радикальную сополимеризацию макромономеров с АПСК проводили в водных растворах при суммарной начальной концентрации мономеров (Σ[М]0) 15–70 мас. % и температуре 60°С в присутствии персульфата калия как инициатора (0.5–1.0 мол. % от суммы мономеров) и тиогликолевой кислоты в качестве регулятора молекулярной массы (0.8–3.0 мас. % от суммы мономеров). Радикальную гомогенную сополимеризацию макромономеров с ДАПА осуществляли в этилацетате или толуоле при суммарной концентрации мономеров 20–50 мас. % и температуре 70–85°С в присутствии 2,2'-азобисизобутиронитрила в качестве инициатора (1 мас. % от суммы мономеров). После завершения синтеза сополимеры выделяли из реакционной смеси высаждением в холодный гексан.
Методы определения состава, молекулярно-массовых характеристик молекулярных щеток и их поведения в растворах
При проведении сополимеризации определяли динамику изменения концентрации обоих сомономеров, что позволяло построить кинетические кривые и вычислить составы сополимеров, образующихся при любых конверсиях. Адекватность метода подтверждали соответствием расчетных значений составов сополимеров, определенным экспериментально методом спектроскопии ЯМР 1Н для выделенных из реакционных смесей образцов полимеров. Содержание ДАПА в реакционных смесях устанавливали методом газовой хроматографии на приборе “Хромос ГХ-1000” (Россия) с использованием капиллярной колонки “VB-1” (0.32 мм × 30 м, температура испарителя и детектора – 250°С). Содержание АПСК и метоксиолиго(этиленгликоль)(мет)акрилатов находили методом высокоэффективной жидкостной хроматографии (ВЭЖХ) на приборе “Хромос ЖХ-301” (Россия), оснащенном спектрофотометрическим детектором и колонкой “Cosmosil 5C18-MS-II” (4.6 × 250 мм), элюент – смесь фосфатного буфера (рН 3) и водного раствора ацетонитрила (87 об. %) в объемном соотношении 1 : 1, расход 0.6 мл/мин (30°С). Определение концентрации высших алкоксиолиго(этиленгликоль)метакрилатов и ОПГ-содержащих макромономеров ВЭЖХ выполняли на приборе “Shimadzu Prominence” (Япония), оснащенном рефрактометрическим и УФ-детекторами с использованием соответственно колонки “Kromasil C-18” (4.6 × 250 мм), элюент – ацетонитрил, расход 0.9 мл/мин (55°C) и колонки “Kromasil NH2” (4.6 × 250 мм), элюент – циклогексан, расход 1.5 мл/мин (25°C).
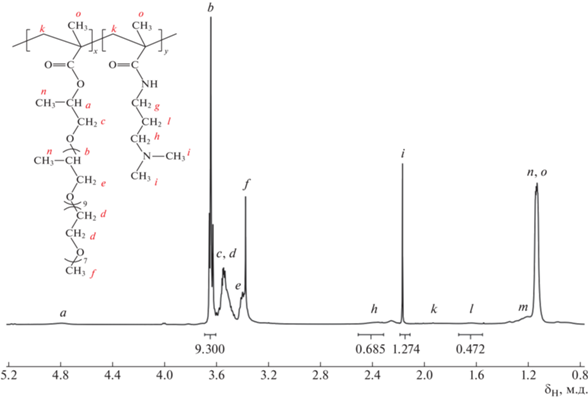
Структура и состав полученных сополимеров подтверждали методом спектроскопии ЯМР 1H на приборе “Agilent DD2 NMR400 WB” (400 MГц) в дейтерохлороформе. Пример спектра сополимера С1Е7Р10М и ДАПА (МЩ-III) представлен на рис. 1. Соотношение мономерных звеньев в составе полимера определяли путем сравнения площадей протонов b в составе С1Е7Р10М (9.3 протона на звено) с суммарной площадью протонов h, i, l в составе ДАПА (10 протонов на звено). В соответствии с представленным примером спектра соотношение звеньев макромономера и ДАПА составило 80.4 : 19.6 при исходном мольном соотношении мономеров в реакционной смеси 80 : 20.
В случае сополимеризации макромономеров и ДАПА методом Фейнмана–Росса рассчитывали относительные активности сомономеров (детали методики вычислений описаны в работе [9]). На основе полученных данных по динамике изменения состава сополимеров по мере роста конверсии [31] вычисляли значения фактора композиционной неоднородности Ф (чем выше значение Φ, тем более неоднородным является сополимер):
Молекулярные массы и коэффициенты полидисперсности Р для синтезированных полимеров типа МЩ-II–МЩ-IV находили методом гель-проникающей хроматографии с использованием прибора “Хромос ЖК-301”, оснащенного рефрактометрическим детектором и двумя последовательно расположенными эксклюзионными колонками “Phenogel 50A” и “Phenogel 10E3A” фирмы “Phenomenex” (с диапазоном измерений молекулярной массы полимеров от 1 × 102 до 7.5 × 104), элюент – тетрагидрофуран. Для расчета молекулярной массы полимеров применяли калибровку по полистиролу. В случае полимеров типа МЩ-I использовали колонку “Phenomenex Biosep-3000” (элюент – водный раствор 0.25 моль/л NaNO3 и 0.01 KH2PO4), для калибровки применяли полиэтиленгликолевые стандарты.
Для характеристики термо- и рН-чувствительных свойств полимеров в водных растворах устанавливали температуру фазового перехода (ТФП, во многих публикациях последних лет используется также термин “температура помутнения”). Значения ТФП определяли по положению максимума первой производной s-образной зависимости оптического пропускания водных растворов полимеров от температуры [32]. Оптическое светопропускание измеряли с использованием фотоколориметра КФК-2 на длине волны 670 нм при скорости нагревания растворов 1–2 град/мин.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Исследование сополимеризации олиго(этиленгликоль)(мет)акрилатов и АПСК
При сополимеризации АПСК с различными гидрокси- или метоксиолиго(этиленгликоль)метакрилатами в относительно разбавленных водных растворах (при начальной суммарной концентрации сомономеров Σ[М]0 = 15 мас. %) сульфокислотный мономер расходовался с заметно меньшей скоростью. Примеры кинетических кривых расхода сомономеров представлены на рис. 2а. Такое соотношение активностей соответствует известным закономерностям сополимеризации в других системах типа метакриловый эфир–N-замещенный акриламид. Например, для пары метилметакрилат–N-метилакриламид константы сополимеризации составляют 3.30 и 0.28 соответственно (растворитель – этанол) [33]. Однако нами было отмечено, что при повышении концентрации сомономеров (при неизменном их начальном мольном соотношении) относительные активности ОЭГ-содержащих макромономеров и АПСК заметно выравниваются (рис. 2б).
Рис. 2.
Влияние Σ[М]0 на динамику роста конверсии сомономеров К при сополимеризации эквимольного количества С1Е21М (1) и АПСК (2) в воде; Σ[М]0 = 15 (а) и 70 мас. % (б).

Аналогичные концентрационные эффекты были зафиксированы ранее для сополимеризации АПСК с акриламидом в водных растворах [34], и повышение относительной активности сульфокислотного акриламида было объяснено влиянием резко усиливающейся при повышенных значениях концентрации ассоциацией молекул этого мономера как между собой, так и с растущими макрорадикалами. Вероятно, аналогичные факторы определяют проявление концентрационного эффекта и при сополимеризации АПСК с ОЭГ-содержащими макромономерами.
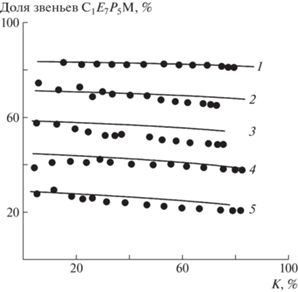
Наличие концентрационных эффектов при синтезе молекулярных щеток типа МЩ-I может быть использовано для повышения их композиционной однородности. На рис. 3а на примере системы С1Е8М–АПСК проиллюстрировано влияние конверсии и суммарной исходной концентрации сомономеров (при их эквимольном начальном соотношении) на составы образующихся сополимеров. Однако для таких систем (типа метакрилат–АПСК), несмотря на выравнивание относительных активностей сомономеров по мере роста Σ[М]0, не удается получить молекулярные щетки с высокой степенью однородности по составу. Это количественно показывают значения факторов композиционной неоднородности Ф – они вычислены для сополимеров, синтезированных при высоких значениях конверсии сомономеров. На рис. 4 видно, что при росте начальных значений концентрации сомономеров значения Ф для сополимеров метакриловых макромономеров и АПСК могут быть снижены в ~2 раза – с 80–90 до 45–54 (композиционную однородность можно считать высокой при значениях Ф < 10). Аналогичные данные получены для сополимеров гидроксиолиго(этиленгликоль)метакрилата и метоксиолиго(этиленгликоль)метакрилата с увеличенной (до 21 звена) длиной ПЭГ-цепочки.
Рис. 3.
Влияние конверсии и суммарной исходной концентрации сомономеров (при их эквимольном начальном соотношении) на состав образующихся сополимеров С1Е8М–АПСК (а) и С1Е3А–АПСК (б); Σ[М]0 = 15 (1), 35 (2) и 70 мас. % (3).

Рис. 4.
Влияние суммарной исходной концентрации мономеров (при их начальном эквимольном соотношении) на значения факторов композиционной неоднородности Ф синтезированных сополимеров С1Е8М–АПСК (1) и С1Е3А–АПСК (2).

Гораздо более однородные щетки удалось получить при замене метакриловых макромономеров на акриловые. На рис. 5 представлены примеры кинетических кривых расхода сомономеров при сополимеризации метоксиолиго(этиленгликоль)акрилата и АПСК при начальной их суммарной концентрации 15 и 70 мас. %. Если посмотреть на рис. 3б, то хорошо видно, как по мере использования более концентрированных исходных смесей происходит выравнивание кривой зависимости состава от конверсии, и при значениях Σ[М]0 = 70 мас. % от начального этапа реакции до практически полного исчерпания мономеров образуются молекулярные щетки, чей состав соответствует составу исходной мономерной смеси. Кривая 2 на рис. 4 демонстрирует, что показатель Ф при этом достигает очень низкого значения 0.1, что свидетельствует об образовании сополимера с очень высокой композиционной однородностью. Таким образом, сополимеризация как метакриловых, так и акриловых ОЭГ-содержащих макромономеров с АПСК в высококонцентрированных водных растворах позволяет синтезировать сульфосодержащие молекулярные щетки с гораздо более высокой композиционной однородностью по сравнению с синтезом в более разбавленных растворах.
Рис. 5.
Влияние Σ[М]0 на динамику роста конверсии сомономеров при сополимеризации эквимольного количества С1Е3А (1) и АПСК (2) в воде; Σ[М]0 = 15 (а) и 70 мас. % (б).

Полимеризационные системы с подобными эффектами относятся к неклассическим (“особым”) [34, 35]. Для таких систем нельзя определить адекватные константы сополимеризации, позволяющие с достаточной точностью рассчитать дифференциальные или средние составы сополимеров при любых заданных конверсиях и начальных значениях концентрации сомономеров. Следует также отметить, что композиционная однородность может существенно влиять на такие свойства амфифильных сополимеров, которые определяются именно оптимальным соотношением гидрофильных и гидрофобных свойств. Например, как показано в работе [22], для амфифильных сополимеров олиго(этиленгликоль)метакрилатов, способных к образованию ферментоподобных мономолекулярных мицелл (“single chain nanoparticles”) с узким распределением по размерам, одним из обязательных требований выступает высокая композиционная однородность полимеров.
Закономерности сополимеризации ОЭГ- и ОПГ-содержащих макромономеров с ДАПА
При синтезе аминосодержащих молекулярных щеток методом сополимеризации с ДАПА все исследуемые макромономерные метакриловые эфиры проявляли более высокую активность (при любых исходных соотношениях сомономеров), однако скорость расходования аминного метакриламида была лишь незначительно ниже как при низких, так и при высоких начальных суммарных значениях концентрации сомономеров. На рис. 6 представлены примеры кинетических кривых, полученных при синтезе молекулярных щеток типа МЩ-III (а) и МЩ-II (б).
Рис. 6.
Зависимости конверсии сомономеров от времени при сополимеризации эквимольного количества С1Е7Р5М (1) или С12Е7М (3) с ДАПА (2, 4); Σ[М]0 = 20 мас. %.

Второй важной особенностью, отличающей аминосодержащие полимеризационные системы от описанных выше (включающих сульфокислотный мономер), является очень небольшое влияние суммарной начальной концентрации сомономеров на составы образующихся сополимеров (рис. 7), которые были близки к составам исходных мономерных смесей в ходе всего процесса. В количественной форме это нашло отражение в значениях Ф, которые составили 10 и менее для всех синтезированных аминосодержащих молекулярных щеток.
Рис. 7.
Влияние конверсии и суммарной исходной концентрации сомономеров (при их эквимольном начальном соотношении) на состав образующихся сополимеров С12Е7М–ДАПА (а) и С1Р7Е8М–ДАПА (б). Σ[М]0 = 20 (1) и 50 мас. % (2).

Основной причиной отсутствия концентрационного эффекта стало применение в данной серии экспериментов малополярных органических растворителей, не склонных к сильным ассоциативным взаимодействиям с молекулами органических веществ. В таких растворителях ассоциация мономеров менее выражена, и влияние ассоциативных факторов в рассматриваемых системах не проявилось. Это сделало целесообразным вычисление и адекватное использование констант сополимеризации. Были проведены синтезы в широком интервале соотношений мономеров, и диаграммы состава сополимеров, образующихся при низких значениях конверсии (не более 10%), показаны на рис. 8.
Рис. 8.
Диаграммы состава сополимеров типа МЩ-II, МЩ-III, МЩ-IV. Обозначения точек, полученных при сополимеризации ДАПА с макромономерами С1Р4М (1), С1Е7Р5М (2), С1Е7Р10М (3), С1Р7Е8М (4) и С1Е7М (5).

Как видно из табл. 1, рассчитанные методом Фейнмана–Росса относительные активности сомономеров мало отличаются при изменении состава макромономеров и образовании молекулярных щеток типов МЩ-II–МЩ-IV. Вычисленные константы сополимеризации для всех аминосодержащих полимеризационных систем позволяют довольно точно описать как начальные составы сополимеров, так и полученные при глубоких степенях превращения (при использовании различных соотношений и суммарных значений концентрации исходных сомономеров). В качестве примера на рис. 9 представлены зависимости состава сополимера С1Е7Р5М–ДАПА от конверсии, построенные по экспериментальным данным и расчетным, определенным на основе констант сополимеризации.
Таблица 1.
Константы сополимеризации макромономеров разного строения (r1) и ДАПА (r2) в этилацетате или толуоле
| Макромономеры | Растворитель | r1 | r2 |
|---|---|---|---|
| С1Р4М | Этилацетат | 1.47 ± 0.13 | 0.60 ± 0.04 |
| С1Е7Р5М | Этилацетат | 1.32 ± 0.05 | 0.66 ± 0.02 |
| С1Е7Р10М | Этилацетат | 1.42 ± 0.11 | 0.92 ± 0.05 |
| С1Р7Е8М | Этилацетат | 1.24 ± 0.09 | 0.71 ± 0.03 |
| С12Е7М | Толуол | 1.15 ± 0.05 | 0.60 ± 0.02 |
Поведение синтезированных молекулярных щеток в растворах
Все синтезированные сульфосодержащие молекулярные щетки типа МЩ-I имели низкие молекулярные массы (значения среднечисленных молекулярных масс синтезированных полимеров составляли от 3800 до 6800), не растворялись в углеводородах, ацетонитриле, но хорошо растворялись в воде, N,N-диметилформамиде и диметилсульфоксиде. При небольшой доле звеньев АПСК указанные сополимеры также растворимы в тетрагидрофуране, а при содержании звеньев сульфокислоты 50% и более являются нерастворимыми в указанном растворителе. В водных растворах многие гомополимеры различных ОЭГ-МА проявляют термочувствительные свойства. Например, гомополимер метоксиолиго(этиленгликоль)метакрилата, содержащий в среднем 7.2 оксиэтильных звеньев, имеет значение ТФП 82°С [16]. Однако введение в аналогичный полимер (n = 8) 5 мол. % (или более) гидрофильных звеньев АПСК привело к потере термочувствительных свойств и растворимости полимера в воде во всем исследованном диапазоне температуры. Не демонстрировали такие свойства и все другие синтезированные щетки типа МЩ-I. Вероятно, для придания сульфосодержащим молекулярным щеткам термочувствительных свойств необходимо сбалансировать их амфифильность путем введения дополнительных гидрофобных фрагментов.
В табл. 2 представлены условия синтеза и молекулярно-массовые характеристики синтезированных аминосодержащих сополимеров. Все синтезированные щетки типов МЩ-II–МЩ-IV не растворимы в неполярном гексане и растворимы в более полярном толуоле, а также таких органических растворителях, как этилацетат, тетрагидрофуран и ацетонитрил. В воде при нормальных условиях большинство полимеров растворяется, но многие из них при нагревании растворов до определенных значений температуры теряют растворимость. Это выражается в помутнении растворов, что сопровождается резким понижением коэффициента светопропускания – со 100% до 0 (рис. 10). При охлаждении растворы вновь становятся прозрачными. Таким образом, в водных растворах такие молекулярные щетки проявляют термочувствительные свойства по типу НКТР. Для синтезированных аминосодержащих сополимеров характерны и pH-чувствительные свойства, поскольку значения ТФП изменяются в зависимости от рН. Были выявлены интересные особенности, связанные с влиянием состава и строения молекулярных щеток (длины гидрофильных ОЭГ- и(или) гидрофобных ОПГ-блоков, порядка их расположения в диблочных боковых цепочках, содержания аминных звеньев) на значения ТФП при различных рН и концентрации полимеров.
Таблица 2.
Составы (для низких значений конверсии) и молекулярно-массовые характеристики (для высоких) синтезированных аминосодержащих сополимеров; М2 = ДАПА
| Полимер, № | М1 | М1 : М2 | Σ[M]0, мас. % | m1 : m2* | Mn** | Ð** |
|---|---|---|---|---|---|---|
| 1 | С12Е7М | 80 : 20 | 20 | 85 : 14 | 15 746 | 1.70 |
| 2 | С12Е7М | 50 : 50 | 20 | 62 : 38 | 7892 | 1.23 |
| 3 | С12Е7М | 35 : 65 | 20 | 46 : 54 | 10 037 | 1.36 |
| 4 | С1Е7Р5М | 80 : 20 | 20 | 86 : 14 | 5900 | 1.63 |
| 5 | С1Е7Р5М | 65 : 35 | 20 | 74 : 26 | 5950 | 1.50 |
| 6 | С1Е7Р5М | 50 : 50 | 20 | 58 : 42 | 3800 | 1.43 |
| 7 | С1Е7Р10М | 95 : 5 | 30 | 96 : 4 | 16 800 | 1.61 |
| 8 | С1Е7Р10М | 90 : 10 | 30 | 93 : 7 | 15 900 | 1.73 |
| 9 | С1Е7Р10М | 80 : 20 | 20 | 86 : 14 | 10200 | 1.36 |
| 10 | С1Е7Р10М | 65 : 35 | 20 | 68 : 32 | 8950 | 1.37 |
| 11 | С1Е7Р10М | 50 : 50 | 20 | 54 : 46 | 6900 | 1.24 |
| 12 | С1Р7Е8М | 95 : 5 | 30 | 96 : 4 | 9500 | 1.41 |
| 13 | С1Р7Е8М | 90 : 10 | 30 | 92 : 8 | 9100 | 1.31 |
| 14 | С1Р7Е8М | 80 : 20 | 20 | 83 : 17 | 8000 | 1.26 |
| 15 | С1Р7Е8М | 65 : 35 | 20 | 70 : 30 | 6850 | 1.20 |
| 16 | С1Р7Е8М | 50 : 50 | 20 | 55 : 45 | 5800 | 1.12 |
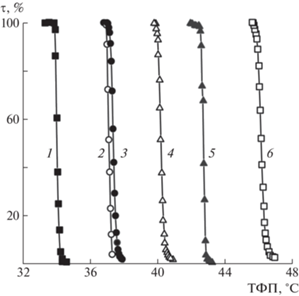
Рис. 10.
Примеры зависимости степени светопропускания τ от температуры для водных растворов сополимеров С1Е7Р10М (1, 2, 5) или С1Р7Е8М (3, 4, 6) и ДАПА при содержании аминных звеньев 5 (1, 3), 10 (2, 4) и 20 мол. % (5, 6). Концентрация – 1.0 мас. %.
Известно, что в большинстве случаев значения ТФП понижаются при росте концентрации термочувствительных полимеров в водных растворах. Это характерно, например, для подробно исследованных термочувствительных (со)полимеров N-изопропилакриламида или сополимеров метоксиолиго(этиленгликоль)(мет)акрилатов с высшими алкилметакрилатами. Данный эффект связан с тем, что при повышении концентрации усиливаются межмолекулярные взаимодействия (особенно между гидрофобными фрагментами макромолекул), что способствует образованию и укрупнению агрегатов макромолекул с дальнейшей потерей ими растворимости. В результате, образование водонерастворимой фазы в более концентрированных растворах происходит при менее высоких значениях температуры. Однако в ряде случаев значения ТФП зависят от концентрации полимеров очень слабо, что свидетельствует о преобладании внутримолекулярных гидрофобных взаимодействий даже при повышенных значениях концентрации. Такие эффекты выявлены, например, для некоторых производных гидроксиэтилцеллюлозы [36] и поли(N,N-бис-(2-метоксиэтил)акриламида [37], для модифицированных полилактидов, содержащих ОЭГ-цепочки [38]. В каждом из перечисленных случаев, это наблюдалось только для определенных составов полимеров, что указывает на нетривиальность подобных зависимостей и их реализации лишь при определенных характеристиках амфифильных термочувствительных полимеров.
Именно такой вариант найден для нейтральных растворов синтезированных молекулярных щеток типа МЩ-III (рис. 11а), причем постоянство значений ТФП при разных значениях концентрации полимеров наблюдалось при различном содержании звеньев ДАПА (в интервале 0–20%). Для аминосодержащих сополимеров двух других типов такой эффект отсутствовал – значения ТФП понижались при повышении концентрации. Соответствующий пример показан на рис. 11б для сополимера типа МЩ-IV. Понижение ТФП происходило и в кислых водных растворах – для сополимера додетоксиолиго(этиленгликоль)метакрилата (n = 7) и ДАПА (тип МЩ-II) оно составило 3.2°С при росте концентрации от 0.1 до 1.0 мас. % На рис. 12 для 1%-ных нейтральных растворов сополимеров, содержащих диблочные боковые цепочки, показано, что при данных условиях порядок расположения ОЭГ- и ОПГ-блоков не оказывал влияния на характер и степень изменения температуры фазовых переходов при повышении содержания аминных звеньев с 5 до 20 мол. %.
Рис. 11.
Зависимости значений ТФП от концентрации сополимеров С1Е7Р10М (а) или С1Р7Е8М (б) с ДАПА в водных растворах (рН 6.7) при содержании аминных звеньев 5 (1, 4), 10 (2, 5) и 20 мол. % (3, 6).

Рис. 12.
Влияние содержания аминосодержащих звеньев в сополимерах С1Е7Р10М (1) или С1Р7Е8М (2) с ДАПА на значения ТФП в водных растворах (рН 6.7). Концентрация – 1.0 мас. %.

Важным свойством синтезированных молекулярных щеток можно назвать проявление ими pH-чувствительных свойств в водных растворах, причиной которых выступают кислотно-основные взаимодействия с участием аминогрупп. На рис. 13 представлены данные по влиянию рН среды на температуру фазовых переходов сополимеров с близким общим соотношением гидрофильных и гидрофобных блоков, но разным порядком их расположения в диблочных боковых цепочках. По мере повышения кислотности среды увеличивается доля протонированных аминогрупп, а повышение содержания положительно заряженных аммониевых групп в макромолекулах повышает их гидрофильность. Поэтому в кислых средах значения ТФП для обоих типов сополимеров заметно увеличиваются, причем отдичия между однотипными полимерами с разным содержанием звеньев ДАПА значительно возрастают. В щелочных средах (при приближении к рН 12), напротив, происходит резкое сближение значений ТФП для однотипных молекулярных щеток, содержащих 5, 10 или 20% звеньев ДАПА. В этих условиях в макромолекулах практически не содержатся гидрофильные аммониевые группы, а незаряженные аминогруппы имеют амфифильный характер и не оказывают заметного влияния на общий гидрофильно-гидрофобный баланс макромолекул.
Рис. 13.
Влияние значений рН водных растворов на значения ТФП сополимеров С1Е7Р10М (а) или С1Р7Е8М (б) с ДАПА при содержании аминных звеньев 5 (1, 4), 10 (2, 5) и 20 мол. % (3, 6). Концентрация – 1.0 мас. %.

Наблюдается и некоторое влияние порядка расположения ОЭГ- и ОПГ-блоков в боковых цепочках. Когда “наружными” являются гидрофобные блоки (МЩ-IV), т.е. гидрофильный ОЭГ-блок расположен между двумя гидрофобными цепочками (основной цепью макромолекулы и ОПГ-блоком в боковой цепи), то степень влияния подкисления среды на значения ТФП заметно увеличивается (особенно при возрастании содержания аминогрупп в полимере). Например, при изменении рН от 6.7 до 2.6 для сополимера С1Р7Е8М–ДАПА(20), имеющего “наружные” гидрофобные ОПГ-цепочки, ТФП возрастает на 48°С (и полимер вплотную подходит к границе потери термочувствительных свойств), а для сополимера С1Е7Р10М–ДАПА(20), содержащего “наружные” гидрофильные ОЭГ-цепочки – только на 19°С. Еще одним отличием можно назвать прохождение зависимости ТФП от рН через явно выраженный минимум в случае сополимеров типа МЩ-IV с небольшим содержанием ДАПА (рис. 13б), особенно он заметен при содержании аминных звеньев 5%. Для сополимера типа МЩ-III (рис. 13а) с таким же содержанием аминных звеньев зависимость имеет едва выраженный минимум, а для полимера с 10% звеньев ДАПА экстремум вообще отсутствует.
Можно предположить, что зафиксированные для молекулярных щеток МЩ-III и МЩ-IV (имеющих разные порядки расположения ОЭГ- и ОПГ-блоков в боковых цепочках) отличия в зависимостях ТФП от концентрации полимеров и от рН водных растворов связаны с различными преобладающими конформациями макромолекул. Известно [24], что сополимеры метоксиолиго(этиленгликоль)метакрилатов с высшими алкилметакрилатами и с высшими алкоксиолиго(этиленгликоль)метакрилатами в воде образуют мицеллы разных типов. В первом случае, это классические мицеллы с гидрофобным ядром и подвижной гидрофильной “короной”, а во втором – мицеллы “цветочного” типа, поскольку в звеньях высших алкоксиолиго(этиленгликоль)(мет)акрилатов все ОЭГ-цепочки, связанные с двух сторон с гидрофобными фрагментами ядра мицеллы, образуют гидрофильные “петли” – “лепестки цветка”. Аналогично, синтезированные в настоящей работе молекулярные щетки МЩ-III могут образовывать мицеллы классического типа, а молекулярные щетки МЩ-IV – “цветочные”. В первом случае, подвижная гидрофильная “ОЭГ-корона” занимает бóльший объем и лучше препятствует как объединению мицелл в более крупные агрегаты, так и протонированию аминогрупп макромолекул (находящихся на поверхности “ядра”) с образованием ионов аммония, повышающих гидрофильность макромолекулы. В результате, повышение концентрации полимеров не приводит к формированию укрупненных агрегатов (и, как следствие, к понижению ТФП), а рост кислотности среды менее сильно повышает температуру фазовых переходов. В “цветочных” мицеллах гидрофильная “ОЭГ-корона” с обеих сторон связана с гидрофобным “ядром”, что должно повышать ее компактность и уменьшать препятствия для “внешних” взаимодействий с участием компонентов “ядра”. С этим могут быть связаны зафиксированные для полимеров типа МЩ-IV понижение ТФП при повышении концентрации и более резкое повышение ТФП в сильнокислой среде.
Амфифильные молекулярные щетки типа МЩ-II, которые содержат в макромономерных звеньях только ОЭГ-блок и концевой додецильный радикал, имеющий ярко выраженные гидрофобные свойства, проявляют термочувствительность в водных растворах в гораздо более узком интервале условий по сравнению с полимерами типа МЩ-III и МЩ-IV, в боковых цепочках которых гидрофобные функции выполняют ОПГ-блоки. Так, при эквимольном соотношении звеньев додетоксиолиго(этиленгликоль)метакрилата (С12Е7М) и ДАПА такие молекулярные щетки в нейтральной и щелочной среде не растворяются в воде и становятся водорастворимы только в сильно кислой среде (рН 2.6), но не подвергаются фазовым переходам при нагревании вплоть до температуры кипения растворителя. Уменьшение содержания макромономерных звеньев в сополимерах С12Е7М и ДАПА (до соотношения 30 : 70 или 10 : 90) обеспечивает растворимость в воде при всех значениях рН. Однако такие полимеры не выпадают в осадок при нагревании водных растворов с рН 2.6 или 6.4. Лишь в слабоосновной среде (рН 9.2) они начинают проявлять термочувствительные свойства, и значения ТФП составляют 79.4°С (30 : 70) и 48.2°С (10 : 90). Такие же свойства в водных растворах (при тех же рН) продемонстрировали и аналогичные сополимеры, в которых гидрофильная ОЭГ-цепочка увеличена на три звена.
ЗАКЛЮЧЕНИЕ
Таким образом, определены условия синтеза композиционно-однородных сульфо- или аминосодержащих молекулярных щеток методом гомогенной радикальной сополимеризации в растворителях мономеров АПСК или ДАПА с амфифильными макромономерными (мет)акриловыми эфирами, содержащими гидрофильные (ОЭГ-) и гидрофобные (ОПГ-, н-додецильные) блоки разной длины и порядка расположения. При синтезе сульфосодержащих сополимеров в водных растворах выявлен сильный концентрационный эффект – влияние исходных значений концентрации сомономеров (при их неизменном соотношении) на состав образующихся сополимеров. При синтезе аминосодержащих сополимеров в толуоле или этилацетате отсутствие концентрационного эффекта позволяет использовать найденные для пяти полимеризационных систем коэффициенты относительной активности сомономеров для адекватного вычисления состава молекулярных щеток при любых значениях конверсии, соотношениях и концентрации сомономеров. Строение макромономеров практически не влияет на синтез аминосодержащих щеток, но порядок расположения ОЭГ- и ОПГ-блоков в боковых цепочках отражается на особенности фазовых переходов полученных стимулчувствительных сополимеров в водных растворах – зависимости ТФП от концентрации полимеров и от значений рН.
Работа выполнена при финансовой поддержке Российского научного фонда в рамках проектов № 20-13-00161 (исследования аминосодержащих полимеров) и № 21-73-00271 (исследования сульфосодержащих полимеров).
Список литературы
Lutz J.-F., Hoth A., Schade K. // Des. Monomers Polym. 2009. V. 12. № 4. P. 343.
Lutz J.-F. // J. Polym. Sci. A. 2008. V. 46. № 11. P. 3459.
Badi N. // Prog. Polym. Sci. 2017. V. 66. P. 54.
Sundararajan S., Samui A.B., Kulkami P.S. // React. Funct. Polym. 2018. V. 130. P. 43.
Liu M., Leroux J.-C., Gauthier M.A. // Prog. Polym. Sci. 2015. V. 48. P. 111.
Neugebauer D. // Polym. Int. 2007. V. 56. № 12. P. 1469.
Terashima T., Sugita T., Fukae K., Sawamoto M. // Macromolecules. 2014. V. 47. P. 589.
Zhang J., Liao B., Meng Y., Li S., Lin X., Huang J., Pang H. // J. Dispers. Sci. Technol. 2020. V. 41. № 4. P. 628.
Orekhov D.V., Kamorin D.M., Simagin A.S., Arifullin I.R., Kazantsev O.A., Savinova M.V., Sivokhin A.P. // Polym. Bull. 2021. V. 78. № 10. P. 5833.
Orekhov D.V., Kazantsev O.A., Orekhov S.V., Sivokhin A.P., Kamorin D.M., Simagin A.S., Savinova M.V., Bolshakova E.A., Korotaev M.S. // J. Appl. Polym. Sci. 2021. V. 138. № 38. P. 50982.
Orekhov D.V., Kamorin D.M., Rumyantsev M., Kazantsev O.A., Sivokhin A.P., Gushchin A.V., Savinova M.V. // Coll. Surf. A. 2015. V. 481. P. 20.
Kazantsev O.A., Kamorin D.M., Orekhov D.V., Sivokhin A.P. // Des. Monomers Polym. 2015. V. 18. № 4. P. 378.
Orekhov D.V., Kazantsev O.A., Sivokhin A.P., Savinova M.V. // Eur. Polym. J. 2018. V. 100. P. 18.
Kazantsev O.A., Orekhov D.V., Sivokhin A.P., Kamo-rin D.M., Savinova M.V. // Des. Monomers Polym. 2017. V. 20. P. 136.
Zhang X., Dai Y. // Polym. Chem. 2019. V. 10. № 18. P. 2212.
Sivokhin A.P., Orekhov D.V., Kazantsev O.A., Gubanova O.V., Kamorin D.M., Zarubina I.S., Bolshakova E.A. // Polym. J. 2021. V. 53. P. 655.
Sivokhin A., Orekhov D., Kazantsev O., Sivokhina O., Orekhov S., Kamorin D., Otopkova K., Smirnov M., Karpov R. // Polymers. 2022. V. 14. № 1. P. 137.
Ilgach D.M., Meleshko T.K., Yakimansky A.V. // Polymer Science C. 2015. V. 57. № 1. P. 3.
Ivanov I.V., Meleshko T.K., Kashina A.V., Yakimansky A.V. // Russ. Chem. Rev. 2019. V. 88. № 12. P. 1248.
Xiang S., Gao Y., Shi C. // Adv. Civ. Eng. 2020. ID 8810443.
Vancoillie G., Frank D., Hoogenboom R. // Prog. Polym. Sci. 2014. V. 39. № 6. P. 1074.
Hattori G., Hirai Y., Sawamoto M., Terashima T. // Polym. Chem. 2017. V. 8. P. 7248.
Shibata M., Matsumoto M., Hirai Y., Takenaka M., Sawamoto M., Terashima T. // Macromolecules. 2018. V. 51. № 10. P. 3738.
Matsumoto M., Takenaka M., Sawamoto M., Terashima T. // Polym. Chem. 2019. V. 10. № 36. P. 4954.
Kröger A.P.P., Hamelmann N., Juan A. // ACS Appl. Mater. Int. 2018. V. 10. № 37. P. 30946.
Pia A., Kröger P., Paulusse M.J. // J. Control. Release. 2018. V. 286. P. 326.
Rubio-Cervilla J., Gonzalez E., Pomposo J. // Nanomaterials. 2017. V. 7. № 10. P. 1.
De-La-Cuesta J., Asenjo-Sanz I., Latorre-Sánchez A. // Eur. Polym. J. 2018. V. 109. P. 447.
Kamorin D.M., Simagin A.S., Orekhov D.V., Kazantsev O.A., Bolshakova E.A., Sivokhin A.P., Savinova M.V., Ore-khov S.V. // Polym. Bull. 2021 (in press).
Simonova M., Kamorin D., Kazantsev O., Nepomnyashaya M., Filippov A. // Polymers. 2021. V. 13. № 16. P. 2715.
Мягченков В.А, Френкель С.Я. Композиционная неоднородность сополимеров. Ленинград: Химия, 1988.
Kuckling D., Doering A., Krahl F., Arndt K.-F. // Polym. Sci. Compreh. Ref. 2012. V. 8. P. 377.
Leoni A., Franco S., Saini G. // Makromol. Chem. 1973. V. 165. № 1. P. 97.
Kazantsev O.A., Shirshin K.V., Sivohin A.P., Igolkin A.V., Goncharova O.S., Kamorin D.M. // J. Polym. Res. 2012. V. 19. № 6. P. 1.
Семчиков Ю.Д., Смирнова Л.А. // Высокомолек. соед. Б. 1999. Т. 41. № 4. С. 734.
Dai M., Tian Y., Fan J., Ren J., Liu Y., Rahman M., Ju B., Ren X., Ma H. // BioRes. 2019. V. 14. № 4. P. 7977.
Hechenbichler M., Laschewsky A., Gradzielski M. // Coll. Polym. Sci. 2021. V. 299. P. 205.
Zhang P., She P., He J., Xiang Z., Li Z., Caob Y., Zhang X. // React. Funct. Polym. 2019. V. 142. P. 128.
Дополнительные материалы отсутствуют.
Инструменты
Высокомолекулярные соединения (серия С)