Водные ресурсы, 2020, T. 47, № 4, стр. 368-379
Особенности состава поверхностных вод бассейна р. Кучерлы (Горный Алтай)
Е. В. Бородина a, *, У. О. Бородина a
a Институт геологии и минералогии им. В.С. Соболева СО РАН
630090 Новосибирск, Россия
* E-mail: borev@igm.nsc.ru
Поступила в редакцию 28.06.2018
После доработки 22.12.2019
Принята к публикации 24.12.2019
Аннотация
Представлены результаты количественного определения растворенных форм 41 элемента методом масс-спектрометрии с индуктивно-связанной плазмой (ICP-MS), а также pH, Eh и минерализации в озерах и водотоках бассейна р. Кучерлы. Обильные дожди, повышающие уровень водообмена, и поступление талых вод ледников и снежников – определяющие факторы в динамике физико-химических показателей. В исследованных реках и озерах бассейна Кучерлы наблюдается превышение ПДК вредных веществ для водных объектов рыбохозяйственного значения по Al, Fe, Zn и ПДК в питьевой воде по Al, Sb.
ВВЕДЕНИЕ
В условиях высокогорных регионов сохраняется пресная вода высокого качества, и они крайне чувствительны к изменению климата [33], поэтому их исследование имеет большое значение. Особый интерес вызывает изучение динамики экологического состояния горных озер, поскольку эти водные экосистемы могут быть использованы в качестве индикатора глобальных изменений окружающей среды [32]. Отдаленные горные озера минимально затронуты антропогенными загрязнителями, что позволяет изучить их геохимические свойства – определить исходные фоновые концентрации микроэлементов и других химические параметры. Отсутствие антропогенного загрязнения делает эти озера идеальной естественной лабораторией для изучения природных биогеохимических циклов микроэлементов [31]. Горные хребты – естественные барьеры для атмосферного переноса, здесь осаждение переносимого в атмосфере материала может происходить в виде пыли или примесей, растворенных в атмосферных осадках [28]. Снежный покров нивальной зоны аккумулирует твердые осадки, которые выносят из атмосферы химические вещества как природного, так и техногенного происхождения. Изучение содержания тяжелых металлов в атмосфере и озерной воде важно из-за их токсического воздействия на людей, водные биоценозы и геохимический баланс экосистем. На концентрации металлов в атмосфере влияют такие их антропогенные источники, как почвенная пыль, сжигание биомассы и топлива [30].
На сегодняшний день известно очень мало современных исследований озер и рек высокогорных районов Горного Алтая из-за их труднодоступности. При этом следует отметить недостаточную изученность химического состава особо охраняемых водных объектов, в частности бассейна р. Кучерлы (рис. 1). Кучерла – правый приток р. Катуни – образуется от слияния рек Мюшту-Айры и Кони-Айры, ее длина – 50 км. По долине реки проходят популярные туристские маршруты к озерам Кучерлинскому, Дарашколь, к ледникам горы Белуха, гроту Куйлю.
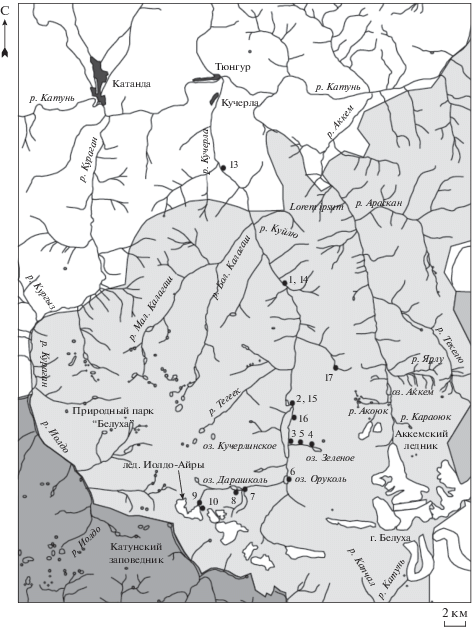
Рис. 1.
Картосхема места расположения особо охраняемых природных территорий в верховьях р. Катуни [7]. Точками отмечены места отбора образцов: 1 – В-1-16; 2 – B-2-16; 3 – B-3-16; 4 – В-4-16; 5 – B-5-16; 6 – B-6-16; 7 – B-7-16; 8 – B-8-16; 9 – B-9-16; 10 – B-10-16; 13 – В-22-17; 14 – В-23-17; 15 – В-24-17; 16 – В-25-17; 17 – б/Обр-4-17.
Рельеф долины р. Кучерлы типично горный, а в его южной части – альпийский, представлен гребнями-антиклиналями и глубокими долинами, образовавшимися за счет новейших тектонических движений на неровном складчатом основании палеозоя. В рельефе хорошо выражены формы древнего и современного оледенения – карлинги, кары, трогообразные долины, гряды, моренные холмы. Территория бассейна Кучерлы сложена метаморфизованными серо- и зеленосланцевыми породами горноалтайской серии нижнего палеозоя и метасланцевой формацией верхнего протерозоя, развитыми в центральной части Холзунско-Чуйской структурно-формационной зоны, прорванными небольшими интрузиями основного и кислого состава [13]. В верхней части бассейна Кучерлы, в долине выше оз. Кучерлинского, а также в долине р. Иолдо-Айры отмечены площадные шлиховые ореолы рассеяния монацита [15].
Бассейн р. Кучерлы занимает большую часть природного парка “Белуха”. Для этого района характерен резко континентальный климат с суровой, многоснежной зимой и сравнительно жарким коротким летом. Средняя температура января –25°С, июля +13°С [13]. Инструментальные метеорологические наблюдения в парке ведутся на двух станциях – Аккем и Каратюрек, расположенных на абсолютных высотах соответственно 2050 и 2600 м. В долинах у верхней границы леса (Аккем) среднегодовая температура воздуха составляет –5.4°С, средняя температура июля +8.3°С, а на платообразных вершинах (Каратюрек) среднегодовая температура –6.3°С, средняя температура июля +6.3°С. Норма годовых осадков на станции Каратюрек 736 мм, в долине Аккем 628 мм. На побережье Кучерлинского озера средняя температура января –17оС, июля +10°С, годовая сумма осадков 550 мм. В нивально-гляциальной зоне Белухи за год выпадает >1000 мм осадков. Максимальные суммы осадков приурочены к летним месяцам. Жидкие осадки преобладают над твердыми до высоты 2300 м, на высоте 3000 м твердые осадки составляют 80%. С октября по апрель осадки выпадают только в твердом виде [16, 17].
Кучерлинское озеро – крупнейший в Горном Алтае водоем ледникового происхождения. С 1978 г. озеро имеет статус памятника природы республиканского значения, подтвержденный в 1996 г. [13]. Основной целью создания памятника природы было сохранение в естественном состоянии его уникального природного комплекса: высокогорных ландшафтов, флоры и фауны на его площади, качества природной воды озера, а также поддержание экологического баланса сопредельных с ним территорий. Для сохранения памятника природы “Озеро Кучерлинское” необходимо поддержание естественных природных комплексов и уникальной экосистемы озера, проведение научных исследований, фоновый экологический мониторинг экосистемы озера [13]. Цель настоящей работы – исследование состава и физико-химических свойств поверхностных вод бассейна р. Кучерлы, а также оценка экологического состояния памятника природы “Озеро Кучерлинское”.
МЕТОД ИССЛЕДОВАНИЯ
Представлены результаты количественного определения 41 элемента в воде рек, озер и в талых ледниковых водах бассейна р. Кучерлы. Концентрации растворенных форм металлов определены методом ICP-MS, относительная погрешность ≤10%. В 2016 г. анализы образцов В-1-16–В-17-16 выполнены на масс-спектрометре высокого разрешения “ELEMENT” (фирма “Finnigan MAT”, Германия) в Центре коллективного пользования Многоэлементных и изотопных исследований СО PAН (Новосибирск, аналитик И.В. Николаева); в 2017 г. анализы образцов В-22-17–В-25-17 – на квадрупольном масс-спектрометре с индуктивно-связанной плазмой “Agilent 7500a” (США) и атомно-абсорбционном спектрофотометре “АА280FS” (США) в ИХТТМ СО РАН (Новосибирск, аналитик С.С. Шацкая). Отбор проб воды проводился в период с 13 по 23 августа 2016 г. и с 16 по 29 июля 2017 г. Пробы отбирались в соответствии с нормативными документами [1, 19, 23] в местах максимального водообмена – в зоне прибоя или течения, на открытой воде, вдали от застойных прибрежных зон, на расстоянии 1–3 м от берега, с глубины 0.5 м, чтобы уменьшить влияние неоднородности концентраций микроэлементов по площади поверхности и по глубине озера. Не допускалось взмучивание донных отложений. В 2016 г. пробы отбирали в чистую одноразовую полиэтиленовую посуду [5, 6, 14, 23], в 2017 г. – в стерильные одноразовые полипропиленовые пробирки (фирма “Corning”, США). Емкости и крышки предварительно ополаскивали не менее трех раз отбираемой для анализа водой [1, 20]. На месте отбора пробы фильтровали через мембранные фильтры и консервировали очищенной азотной кислотой, которая использовалась в дальнейшем при выполнении масс-спектрального анализа этих образцов. Пробы снега и фирна отбирали на глубине 10 см в стерильные одноразовые полипропиленовые пробирки. После отбора пробы снега и фирна были растоплены при комнатной температуре, профильтрованы через мембранные фильтры, законсервированы очищенной азотной кислотой и помещены в такие же стерильные одноразовые полипропиленовые пробирки, как и пробы воды.
Для фильтрации применялись одноразовые шприцевые фильтрующие насадки “Minisart NML” (фирма “Sartorius”, Германия) с размером пор 0.45 мкм. Фильтрат подкислялся до pH < 2 из расчета 3–5 мл концентрированной азотной кислоты на 1 л пробы [5, 6, 19]. Пробы транспортировали в темных контейнерах, хранили в прохладном месте, анализировали ранее чем через 1 мес. с момента отбора [5, 6, 23].
В ходе полевых работ были исследованы физико-химические характеристики водных объектов – температура, pH, окислительно-восстановительный потенциал (ОВП, Eh), электропроводность и общая минерализация. Измерения проводились в точках отбора проб с помощью приборов: PH-200, ORP-200 и COM-100 (производитель “HM Digital”, Южная Корея). Высокая точность полученных данных гарантирована техническими характеристиками приборов. PH-200 позволяет измерять pH в диапазоне 0–14 (погрешность ± 0.1 pH). ORP/Redox-метр ORP-200 измеряет ОВП в диапазоне от – 999 до +1000 мВ с точностью ±0.5% (±2мВ). COM-100 предназначен для измерения общей минерализации, электропроводности и температуры воды, диапазон измерения минерализации 0–8560 ppm (мг/л), электропроводности – 0–9990 мкСм/см, температуры – 0–80°C, погрешность ±2%.
ФИЗИКО-ХИМИЧЕСКИЕ ХАРАКТЕРИСТИКИ ВОДНЫХ ОБЪЕКТОВ
В табл. 1 приведены основные физико-химические характеристики водных объектов бассейна р. Кучерлы. В пробах, полученных в июле 2017 г., величина pH ≤ 6.5–7.2, ОВП – 47–88 мВ, минерализация – 19.0–34.2 мг/л, электропроводность – 30.0–53.5 мкСм). В августе 2016 г. pH менялось в диапазоне 7.3–8.3, ОВП – 173–222 мВ, минерализация – 9.4–23.9 мг/л, электропроводность – 14.8–37.2 мкСм. При этом минерализация и электропроводность проб, отобранных в одних и тех же точках в 2016 и 2017 гг., имеют сходные значения. Температура поверхностного слоя воды р. Кучерлы и оз. Кучерлинского в июле 2017 г. составляла +14.2–(+15.0)°С, в верховьях р. Текелюшки вблизи ледника +7.5°С. В августе 2016 г. температура воды в р. Кучерле была +11.4°С, а в озерах Кучерлинском и Дарашколь – не превышала +7.6–(+9.3)°С.
Таблица 1.
Физико-химические показатели водных объектов (1 – р. Кучерла, среднее течение; 2 – оз. Кучерлинское, исток р. Кучерлы; 3 – оз. Кучерлинское, восточный берег; 4 – оз. Зеленое, северо-западный берег, исток руч. Зеленого; 5 – руч. Зеленый, среднее течение; 6 – оз. Оруколь (пойма р. Кучерлы); 7 – оз. Дарашколь, исток р. Йолдо-Айры; 8 – оз. Дарашколь, южный берег; 9 – верховья р. Йолдо-Айры вблизи ледника Иолдо-Айры; 10 – ледник Иолдо-Айры, снег, фирн; 11 – р. Кокса, с. Усть-Кокса; 12 – р. Катунь, с. Усть-Кокса; 13 – р. Кучерла, урочище Елань; 14 – р. Кучерла, среднее течение; 15 – оз. Кучерлинское, исток р. Кучерлы; 16 – оз. Кучерлинское, северо-восточный берег; 17 – р. Текелюшка, верхнее течение, водораздельный хребет рек Аккема и Кучерлы; 18 – р. Катунь, с. Усть-Кокса; 19 – скважина, с. Усть-Кокса; 20 – скважина, берег р. Катуни, с. Усть-Кокса; 13.08.16 – дата отбора пробы воды; б/Обр-1 – физико-химические показатели водных объектов исследованы без отбора проб; высота над уровнем моря [7]; минер., мг/л – минерализация; эл. пров., мкСм – электропроводность)
| Показатель | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
|---|---|---|---|---|---|---|---|
| 13.08.2016 | 14.08.2016 | 15.08.2016 | 15.08.2016 | 15.08.2016 | 16.08.2016 | 17.08.2016 | |
| B-1-16 | B-2-16 | B-3-16 | B-4-16 | B-5-16 | B-6-16 | B-7-16 | |
| Высота, м | 1270 | 1689 | 1689 | 2293 | 2100 | 1733 | 2133 |
| t возд., °С | 26.5 | 11.2 | – | – | – | 13.5 | 12.1 |
| t воды, °С | 11.4 | 7.6 | 8.4 | – | – | – | 7.8 |
| Минерализация, ppm | 21.1 | 19.6 | 20.8 | 23.9 | 23.9 | 20.0 | 13.7 |
| Электропроводность, мкСм | 32.9 | 30.3 | 32.5 | 36.8 | 37.2 | 31.2 | 21.7 |
| pH | 8.2 | 8.3 | 8.1 | 8.0 | 7.9 | 7.7 | 7.9 |
| ОВП (Eh), мВ | 173 | 182 | 221 | 195 | 222 | 202 | 189 |
| Показатель | 8 | 9 | 10 | 11 | 12 | 13 | 14 |
| 17.08.2016 | 18.08.2016 | 18.08.2016 | 23.08.2016 | 23.08.2016 | 26.07.2017 | 26.07.2017 | |
| B-8-16 | B-9-16 | B-10-16 | B-16-16 | B-17-16 | В-22-17 | В-23-17 | |
| Высота, м | 2133 | 2500 | 2500 | 980 | 980 | 1000 | 1270 |
| t возд., °С | 21.0 | – | – | – | 27 | 23 | 26.3 |
| t воды, °С | 9.3 | – | – | – | 14.2 | 15.0 | 14.2 |
| Минерализация, ppm | 14.6 | 9.4 | 13.9 | 108 | 36.5 | 20.3 | 21.4 |
| Электропроводность, мкСм | 21.9 | 14.8 | 21.6 | 163 | 56.0 | 33.0 | 33.0 |
| pH | 7.9 | 7.3 | 6.5 | 8.5 | 8.2 | 7.2 | 6.5 |
| ОВП (Eh), мВ | 184 | 212 | 233 | 170 | 180 | 88 | 67 |
| Показатель | 15 | 16 | 17 | 18 | 19 | 20 | |
| 27.07.2017 | 27.07.2017 | 29.07.2017 | 16.07.2017 | 22.08.2016 | 16.07.2017 | ||
| В-24-17 | В-25-17 | б/Обр-4-17 | б/Обр-1-17 | б/Обр-5-16 | б/Обр-2-17 | ||
| Высота, м | 1689 | 1689 | 2500 | 980 | 980 | 980 | |
| t возд., °С | 20.5 | 20.5 | 9.5 | 26 | – | 26 | |
| t воды, °С | 14.4 | 14.6 | 7.5 | 17.0 | – | 19.8 | |
| Минерализация, ppm | 19.0 | 20.1 | 34.2 | 23.2 | 250 | 42.5 | |
| Электропроводность, мкСм | 30.0 | 31.3 | 53.5 | 36.4 | 377 | 64.3 | |
| pH | 6.7 | 7.0 | 6.9 | 6.6 | 8.4 | 6.7 | |
| ОВП (Eh), мВ | 47 | 50 | 62 | 32 | 174 | 33 |
Физико-химические показатели снега и фирна ледника Иолдо-Айры отличаются от показателей талых вод, потоки которых дают начало р. Иолдо-Айры. Для снега и фирна характерны более высокие минерализация (13.9 мг/л), электропроводность (21.6 мкСм), ОВП (233 мВ), но более низкая величина pH (6.5), чем для вод, стекающих с ледника: минерализация (9.4 мг/л), электропроводность (14.8 мкСм), ОВП (212 мВ), pH (7.3). Воды в верховьях р. Иолдо-Айры имеют наименьшие минерализацию и электропроводность из всех исследованных объектов бассейна р. Кучерлы, а наибольшие значения зафиксированы в верховьях р. Текелюшки (минерализация 34.2 мг/л, электропроводность 53.5 мкСм), а также в руч. Зеленом и оз. Зеленом (минерализация 23.9 мг/л, электропроводность 36.8–37.2 мкСм).
В табл. 1 собраны данные по физико-химическим характеристикам вод рек Катуни, Коксы и грунтовых вод в районе с. Усть-Кокса. В июле 2017 г. минерализация в р. Катуни была 23.2 мг/л (электропроводность 36.4 мкСм). Минерализация грунтовых вод из скважины на берегу р. Катуни составляла 42.5 мг/л (электропроводность 64.3 мкСм). Значения pH были в пределах 6.6–6.7, ОВП – 32–33 мВ. В августе 2016 г. минерализация в р. Катуни составляла 36.5 мг/л (электропроводность 56.0 мкСм), в р. Коксе – 108 мг/л (электропроводность 163 мкСм), а в воде из скважины – 250 мг/л (электропроводность 377 мкСм). При этом pH и ОВП всех трех объектов близки: pH – 8.2–8.5, ОВП – 170–180 мВ.
ХИМИЧЕСКИЙ СОСТАВ ВОДЫ БАССЕЙНА КУЧЕРЛЫ
Лимнологическая экосистема оз. Кучерлинского – проточная с замедленным водообменом и гидрокарбонатной кальциевой водой [13]. В табл. 2 приведены содержания растворенных форм элементов в водных объектах бассейна р. Кучерлы. Эти значения варьируют в широких пределах – от 3.2 мг/л в истоке р. Иолдо-Айры до 35.1 мг/л в талых водах снега и фирна с поверхности ледника Иолдо-Айры, в реках и озерах – не превышают 8–5 мг/л. Преобладающий компонент состава воды изученных рек и озер бассейна Кучерлы – Ca, его массовая доля по отношению к другим катионам 75–67%. Содержание основных катионов убывает в следующей последовательности: Ca > > K > Si > Mg > Na > Fe > Al > Sr > Zn, а их сумма составляет 99.5–99.8% общего количества. Другое соотношение катионов наблюдается в составе снега и фирна ледника Иолдо-Айры. Здесь преобладает K (80%), а также Mg, Na, Ca (в сумме составляют 98.7%). Остальные катионы располагаются так в порядке убывания их содержаний: Fe > Al > P > Zn > Mn > > Ba > Sr > Sb. Состав воды рек Катуни и Коксы по набору основных катионов сходен с составом рек и озер бассейна Кучерлы; Катунь: Ca (68%) > Si > Na > > Mg > K > Sr > Fe > Al (в сумме составляют 99.8%), остальные элементы: Zn > Mn > Ba > Sb > > Ag > Mo > Rb > U > W; Кокса: Ca (81%) > Mg > > Si > Na > K > Sr > Mn (в сумме составляют 99.9%), остальные элементы: Ba > Sb > Zn > P > > U > Mo. Концентрации основных ионов и микроэлементов в талой воде на поверхности ледника низкие, но увеличиваются в подледниковых потоках из-за взаимодействия воды с горными породами [29]. Так, в воде в верховьях р. Йолдо-Айры и в других реках и озерах бассейна Кучерлы следующее содержание: Si – в 6–2 раза, Ca – в 4–2 раза, Sr и Mo – в 5–2 раза выше, чем в леднике Иолдо-Айры. При этом в леднике происходило накопление ряда элементов: Na, Mg, Al, P, K, Mn, Fe, Co, Cu, Zn, Rb, Cd, Ba. Их содержание в поверхностном слое снега и фирна гораздо выше, чем в воде, стекающей с ледника, а также в реках и озерах бассейна Кучерлы: Na – в 10–3, Mg – в 25–5, Al – в 3–2, K – в 143–42, Mn – в 39–8, Fe – в 3–2, Zn – в 21–3, Rb – в 5–2, Ba – в 24–7 раз. Содержание в составе льда и снега таких элементов, как Na, Mg, P, K, Ba, и, соответственно, общая минерализация могут увеличиваться в результате “процессов трансформации первоначального химического состава под влиянием процессов испарения и конденсации на поверхности ледника, а также таяния и повторного замерзания воды, происходящего в теплое время года” [27]. Ледники представляют собой резервуары осажденных из атмосферы микроэлементов как природного, так и техногенного происхождения, которые выделяются во время таяния [29]. Кроме того, значительная часть элементов в составе льда и снега может быть привнесена из подстилающих горных пород.
Таблица 2.
Результаты ИСП-МС-определения содержания растворенных форм элементов в водных пробах, мкг/л (1 – р. Кучерла, среднее течение; 2 – оз. Кучерлинское, исток р. Кучерлы; 3 – оз. Кучерлинское, восточный берег; 4 – оз. Зеленое, северо-западный берег, исток руч. Зеленого; 5 – руч. Зеленый, среднее течение; 6 – оз. Оруколь (пойма р. Кучерлы); 7 – оз. Дарашколь, исток р. Йолдо-Айры; 8 – оз. Дарашколь, южный берег; 9 – верховья р. Йолдо-Айры вблизи ледника Иолдо-Айры; 10 – ледник Иолдо-Айры, снег, фирн; 11 – р. Кокса, с. Усть-Кокса; 12 – р. Катунь, с. Усть-Кокса; 13 – р. Кучерла, урочище Елань; 14 – р. Кучерла, среднее течение; 15 – оз. Кучерлинское, исток р. Кучерлы; 16 – оз. Кучерлинское, северо-восточный берег; 17 – ПО-16 – пределы обнаружения для анализов, выполненных в 2016 г. (B-1-16–B-17-16); 18 – ПО-17 – в 2017 г. (B-22-17–B-25-17); 19 – [22]: 1 – полифосфаты (олиготрофные водоемы), 2 – для водоемов с минерализацией до 100 мг/л; 20 – ПДК питьевой воды согласно: 1 – [25]; 2 – [3]; 3 – [9, 10]; 4 – [4]; 21 – первая категория [26]; 22 – высшая категория [26]; подчеркнуты показатели, превышающие ПДК)
| Компонент | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| 13.08.2016 | 14.08.2016 | 15.08.2016 | 15.08.2016 | 15.08.2016 | 16.08.2016 | 17.08.2016 | 17.08.2016 | |
| B-1-16 | B-2-16 | B-3-16 | B-4-16 | B-5-16 | B-6-16 | B-7-16 | B-8-16 | |
| Na | 568 | 386 | 396 | 349 | 328 | 429 | 289 | 318 |
| Mg | 474 | 415 | 430 | 646 | 612 | 511 | 182 | 186 |
| Al | 50.1 | 43.9 | 49.9 | 61.3 | 29.9 | 59.5 | 31.0 | 51.0 |
| Si | 645 | 569 | 494 | 473 | 449 | 536 | 376 | 419 |
| P | 3.8* | 3.2* | 5.6* | 5.2* | 3.1* | 4.3* | 3.7* | 5.9* |
| K | 676 | 542 | 572 | 541 | 577 | 555 | 504 | 513 |
| Ca | 5170 | 4391 | 4611 | 5809 | 5465 | 4392 | 3478 | 3712 |
| Sc | <0.01 | <0.01 | <0.01 | <0.01 | <0.01 | 0.03 | <0.01 | <0.01 |
| Ti | 1.4* | 1.2* | 1.5* | 2.6* | 1.7* | 1.6* | <1 | 1.7* |
| V | 0.26* | 0.20* | 0.20* | 0.22* | 0.22* | 0.25* | 0.26* | 0.26* |
| Cr | 0.41* | 0.78 | 0.63 | 0.83 | 0.39* | 0.98 | 0.34* | 0.26* |
| Mn | 2.2 | 2.4 | 4.3 | 3.5 | 1.6 | 3.5 | 6.1 | 6.6 |
| Fe | 57 | 48 | 57 | 68 | 36 | 73 | 40 | 65 |
| Co | <0.05 | <0.05 | <0.05 | <0.05 | <0.05 | 0.06* | <0.05 | <0.05 |
| Cu | 0.70* | 0.52* | 0.70* | 0.73* | 0.71* | 0.47* | 0.54* | 0.75 |
| Zn | 12.4 | 11.9 | 4.6 | 4.6 | 3.1 | 5.8 | 19.7 | 12.1 |
| Rb | 0.67 | 0.58 | 0.70 | 0.82 | 0.77 | 0.77 | 0.38 | 0.49 |
| Sr | 28.5 | 26.7 | 28.1 | 40.8 | 40.8 | 26.2 | 16.7 | 16.8 |
| Mo | 0.88 | 0.83 | 0.73 | 0.83 | 0.87 | 0.90 | 0.80 | 0.63 |
| Cd | <0.01 | <0.01 | <0.01 | <0.01 | 0.01* | <0.01 | 0.01* | <0.01 |
| Sb | 2.9 | 8.7 | 14.5 | 13.6 | 0.30 | 2.4 | 0.33 | 0.11 |
| Te | <0.001 | 0.01 | 0.01 | <0.001 | <0.001 | 0.01 | 0.01 | <0.001 |
| Ba | 1.6 | 1.2 | 1.4 | 1.9 | 1.6 | 1.3 | 1.7 | 2.3 |
| W | 0.07 | 0.07 | 0.08 | 0.02* | 0.02* | 0.08 | 0.02* | 0.02* |
| Pb | 0.08* | 0.07* | 0.07* | 0.08* | 0.55 | 0.08* | 0.10* | 0.12* |
| Bi | 0.002* | 0.002* | 0.002* | 0.002* | 0.002* | 0.003 | 0.001* | 0.002* |
| U | 0.15 | 0.12 | 0.18 | 0.90 | 0.84 | 0.15 | 0.28 | 0.33 |
| Сумма | 7696 | 6452 | 6673 | 8024 | 7554 | 6605 | 4952 | 5313 |
| Компонент | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 |
| 18.08.2016 | 18.08.2016 | 23.08.2016 | 23.08.2016 | 26.07.2017 | 26.07.2017 | 27.07.2017 | 27.07.2017 | |
| B-9-16 | B-10-16 | B-16-16 | B-17-16 | В-22-17 | В-23-17 | В-24-17 | В-25-17 | |
| Li | – | – | – | – | 0.047 | 0.100 | 0.310 | 0.100 |
| Na | 175 | 1716 | 1690 | 1139 | – | – | – | – |
| Mg | 127 | 3185 | 3012 | 1094 | – | – | – | – |
| Al | 14.8* | 99.4 | 5.5* | 23.0 | 87.0 | 54.0 | 140 | 5.9 |
| Si | 217* | 114* | 2006 | 1450 | 990 | 800 | 790 | 550 |
| P | 4.3* | 79.6 | 7.3 | 3.9* | – | – | – | – |
| K | 197 | 28 141 | 522 | 367 | – | – | – | – |
| Ca | 2375 | 1539 | 31 442 | 9056 | – | – | – | – |
| Sc | <0.01 | <0.01 | <0.01 | <0.01 | 0.045 | 0.027 | 0.100 | – |
| Ti | <1 | 2.7* | <1 | <1 | 4.3 | 2.5 | 4.8 | 0.89 |
| V | 0.15* | 0.32 | 0.20* | 0.16* | 0.31 | 0.27 | 0.36 | 0.05 |
| Cr | 0.23* | 0.63 | <0.2 | 0.30* | – | – | – | – |
| Mn | 7.8 | 61.9 | 103 | 8.0 | 4.1 | 2.5 | 4.7 | 2.2 |
| Fe | 13* | 103 | 12* | 29.8 | 130 | 81.0 | 180 | 56.0 |
| Co | <0.05 | 0.33 | <0.05 | <0.05 | 0.04 | – | 0.05 | – |
| Cu | <0.25 | 2.80 | 0.53* | 0.41* | – | – | – | – |
| Zn | 3.7 | 67.0 | 8.1 | 8.2 | – | – | – | – |
| Ga | – | – | – | – | 0.140 | – | – | – |
| Ge | – | – | – | – | – | – | 0.092 | – |
| Rb | 0.15* | 1.93 | 0.18* | 0.34 | 0.52 | 0.46 | 0.72 | 0.44 |
| Sr | 18.4 | 9.0 | 153 | 53.0 | 23.0 | 20.0 | 21.0 | 21.0 |
| Y | – | – | – | – | 0.050 | – | 0.099 | – |
| Mo | 0.34 | 0.17 | 0.40 | 0.36 | – | – | – | – |
| Ag | – | – | – | 0.40 | – | 0.45 | – | 0.55 |
| Cd | <0.01 | 0.07 | <0.01 | <0.01 | – | – | – | – |
| Sb | 3.4 | 5.8 | 12.7 | 2.9 | – | – | – | – |
| Te | <0.001 | 0.010 | <0.001 | <0.001 | – | – | – | – |
| Ba | 0.67 | 16.4 | 17.3 | 5.1 | 0.58 | – | – | – |
| Ce | – | – | – | – | 0.71 | 0.69 | 1.10 | 0.63 |
| Pr | – | – | – | – | 0.073 | 0.075 | 0.130 | 0.070 |
| Nd | – | – | – | – | 0.51 | 0.51 | 0.66 | 0.50 |
| Sm | – | – | – | – | – | – | 0.054 | – |
| Eu | – | – | – | – | 0.027 | – | – | – |
| Gd | – | – | – | – | – | 0.049 | 0.088 | 0.068 |
| Dy | – | – | – | – | 0.033 | – | – | – |
| Ho | – | – | – | – | 0.010 | 0.009 | – | – |
| Ta | – | – | – | – | – | – | 0.011 | 0.011 |
| W | 0.01* | 0.02* | 0.02* | 0.03 | 0.07 | – | – | – |
| Pb | <0.05 | 0.54 | 0.10* | 0.12* | 0.19 | 0.54 | 3.5 | 0.29 |
| Bi | 0.002* | 0.007 | <0.001 | <0.001 | 1.000 | 0.900 | 1.100 | 1.200 |
| U | 0.010 | 0.060 | 0.520 | 0.110 | 0.110 | 0.086 | 0.200 | 0.100 |
| Сумма | 3159 | 35 147 | 38 993 | 13 243 | – | – | – | – |
| Компонент | 17 | 18 | 19 | 20 | 21 | 22 | ||
| ПО-16 | ПО-17 | приказ | ПДК | первая | высшая | |||
| Li | – | 0.001 | 80 | 301, 2 | 30 | 30 | ||
| Na | 10 | – | 120 000 | 200 0001–3 | 200 000 | 20 000 | ||
| Mg | 3 | – | 40 000 | 50 0002 | 65 000 | 5000–50 000 | ||
| Al | 5 | 1 | 40 | 2002 | 200 | 100 | ||
| Si | 100 | 0.001 | – | 10 0001, 2 | 10 000 | 10 000 | ||
| P | 2 | 1 | 501 | 35001, 2 | – | – | ||
| K | 30 | – | 10 0002 | 12 0003 | 20 000 | 2000–20 000 | ||
| Ca | 500 | – | 180 000 | 100 0003 | 130 000 | 25 000–80 000 | ||
| Sc | 0.01 | 0.001 | – | – | – | – | ||
| Ti | 1 | 0.001 | 60 | 1002 | – | – | ||
| V | 0.1 | 0.01 | 1 | 1001, 2 | – | – | ||
| Cr | 0.2 | – | 20 | 501, 2, 4 | 50 | 30 | ||
| Mn | 0.2 | 0.001 | 10 | 1001, 2 | 50 | 50 | ||
| Fe | 5 | 0.1 | 100 | 3001, 2 | 300 | 300 | ||
| Co | 0.05 | 0.01 | 10 | 1001, 2 | 100 | 100 | ||
| Cu | 0.25 | 0.1 | 1 | 10001, 4 | 1000 | 1000 | ||
| Zn | 1 | 1 | 10 | 10002 | 5000 | 3000 | ||
| Ga | – | 0.001 | – | – | – | – | ||
| Ge | – | 0.001 | – | – | – | – | ||
| Rb | 0.1 | 0.001 | 100 | 1001, 2 | – | – | ||
| Sr | 1 | 1 | 400 | 70001, 2 | 7000 | 7000 | ||
| Y | – | 0.001 | – | – | – | – | ||
| Mo | 0.01 | 0.01 | 1 | 704 | 70 | 70 | ||
| Ag | 0.01 | 0.01 | – | 501, 2 | 25 | 25 | ||
| Cd | 0.01 | 0.005 | 5 | 11, 2 | 1 | 1 | ||
| Sb | 0.005 | 0.005 | – | 52 | 5 | 5 | ||
| Te | 0.001 | 0.0005 | – | 101 | – | – | ||
| Ba | 0.1 | 0.1 | 740 | 1001 | 700 | 100 | ||
| Ce | – | 0.001 | – | – | – | – | ||
| Pr | – | 0.001 | – | – | – | – | ||
| Nd | – | 0.001 | – | – | – | – | ||
| Sm | – | 0.001 | – | 241 | – | – | ||
| Eu | – | 0.001 | – | 3001 | – | – | ||
| Gd | – | 0.001 | – | – | – | – | ||
| Dy | – | 0.001 | – | – | – | – | ||
| Ho | – | 0.001 | – | – | – | – | ||
| Ta | – | 0.001 | – | – | – | – | ||
| W | 0.01 | 0.005 | 0.8 | 501, 2 | – | – | ||
| Pb | 0.05 | 0.01 | 6 | 102 | 10 | 5 | ||
| Bi | 0.001 | 0.0005 | – | 1001, 2 | – | – | ||
| U | 0.001 | 0.001 | – | 154 | – | – |
Содержание Na, Mg, Al, Si, K, Ca, Fe, Zn, Rb, Sr, Mo, Ba, U в реках бассейна Кучерлы увеличивается в направлении от верхней части водосбора вниз. Так, состав воды р. Кучерлы в среднем течении отличается от состава воды высокогорной части бассейна (верховья р. Йолдо-Айры) и истока р. Кучерлы в среднем в 2–3 раза большим содержанием этих элементов, а значит, они, вероятно, поступают в воду в результате выщелачивания горных пород, слагающих водосбор (табл. 2).
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
Кучерла берет начало у ледников Белухи. Питание реки преимущественно снеговое (до 50%), а потому максимальный сток наблюдается во время таяния снежников и сезонного снежного покрова. Дождевое питание не превышает 20, а грунтовое – 30% стока. Характерно высокое половодье в июне–июле и низкая межень в зимне-весенний период [13]. Время проведения гидрохимических исследований соответствует как периоду наиболее интенсивного таяния ледников и снежников с максимальным уровнем стояния вод на реках (с 16 по 29 июля 2017 г.), так и периоду постепенного уменьшения объемов снеготаяния и снижения уровня рек (с 13 по 23 августа 2016 г.). Вероятно, изменения характера питания водотоков повлияли на физико-химические показатели поверхностных вод.
Низкие величины pH в июле 2017 г. (6.5–7.2, нейтральная среда [21]) могут быть связаны с тем, что значительную долю стока рек бассейна Кучерлы в это время составляют кислые снежно-ледниковые воды и дождевые осадки. В период наиболее интенсивного поступления кислых вод в водоем возможно значительное уменьшение величины рН воды. С прекращением поступления кислых осадков водоем переходит в обычное состояние – рН поднимается до первоначальных значений [18]. Понижение pH поверхностных вод в условиях усиленного увлажнения в середине лета может быть также связано с попаданием в водотоки и водоемы большого количества гумусовых кислот из насыщенных ими почв лесной зоны. Дождевые осадки дренируют верхний слой почвы и вымывают растворы с высоким содержанием гумусовых кислот в реки и озера. К середине августа с понижением температуры воздуха таяние снежников замедляется и объем снежно-ледникового стока снижается. В то же время в питании рек увеличивается доля грунтовых вод. Для поверхностных водоемов, находящихся в равновесии с карбонатом кальция и диоксидом углерода, содержащимся в атмосферном воздухе, рН воды должен составлять 7.3–8.4 [18]. Такие показатели наблюдались в августовских пробах 2016 г. – pH 7.3–8.3 (нейтральная и слабощелочная среда [21]) (табл. 1).
ОВП природных водоемов зависит главным образом от концентрации растворенного в воде кислорода. Концентрация кислорода определяет направление и скорость процессов химического и биохимического окисления органических и неорганических соединений. На его содержание в воде влияют противоположно направленные процессы: одни увеличивают концентрацию кислорода, другие уменьшают ее. К процессам, обогащающим воду кислородом, относятся: поступление в водоемы насыщенных кислородом дождевых и снеговых вод, выделение кислорода водной растительностью в процессе фотосинтеза. Интенсивность продуцирования кислорода снижается при понижении температуры, уменьшении прозрачности воды и количества биогенных веществ. К процессам, уменьшающим содержание кислорода в воде, относятся биохимические (дыхание бактерий) и химические (окисление органических и неорганических веществ) реакции [8].
В июле поверхностные воды бассейна Кучерлы насыщаются кислородом за счет талых снежно-ледниковых вод и атмосферного кислорода дождевых осадков. Олиготрофные водные объекты бассейна, такие как озера Кучерлинское, Дарашколь, Цветные, – глубокие, с холодной, слабо прогреваемой в летнее время водой, бедны планктоном и питательными веществами, а потому процессы фотосинтеза с выработкой кислорода в них протекают слабо, при этом кислород интенсивно расходуется на биохимические процессы. В оз. Кучерлинском вода мутная и прозрачность ≤1 м, что препятствует выработке кислорода. Это связано с близостью ледников в верховьях рек Мюшту-Айры и Кони-Айры. В озеро попадает большое количество взвеси за счет продуктов таяния ледников и размываемых береговых отложений, а дно покрыто толстым слоем ила.
Повышение содержания гумусовых кислот в водоеме может привести к резкому снижению концентрации растворенного кислорода, идущего на их окисление. Главные источники поступления гумусовых кислот в природные воды – почвы и торфяники, из которых они вымываются дождевыми и болотными водами [8, 12, 24]. В летнее время, особенно после обильных дождей, берега рек и озер бассейна Кучерлы большей частью заболочены. Специфика окислительно-восстановительного режима переувлажненных почв – развитие химических и биохимических (микробиологических) восстановительных процессов и падение Eh почвы до низких или даже отрицательных значений [2]. Значительная часть гумусовых кислот вносится в водоемы вместе с пылью и образуется непосредственно в водоеме в процессе трансформации “живого органического вещества” [12, 24]. Низкие значения ОВП (47–88 мВ) поверхностных вод бассейна Кучерлы в июле 2017 г. соответствуют переходной окислительно-восстановительной геохимической обстановке, которая определяется величинами Eh от 0 до +100 мВ, неустойчивым геохимическим режимом. Такие значения характерны для воды с переменным составом солей и часто меняющимся содержанием кислорода [11]. В августе 2016 г. ОВП поверхностных вод составлял 173–222 мВ, что соответствует окислительной геохимической обстановке (Eh > +100 – (+150) мВ), которая характеризуется присутствием в воде растворенного кислорода, а также ряда элементов в высшей форме своей валентности [11]. В этот период интенсивность водообмена снижается и, соответственно, уменьшается количество гумусовых веществ, смываемых с берегов в реки и озера со склонов гор. Понижение температуры воды в августе и, как следствие, увеличение растворимости кислорода в воде также способствуют ее обогащению кислородом.
Для выявления связи между содержаниями элементов в исследованных реках и озерах бассейна Кучерлы построены матрицы парных корреляций. Для выборки проб 2016 г. установлены следующие статистически значимые (r > 0.7) корреляционные связи между элементами: Na, Mg, Al, Si, K, Ca, Cr, Mn, Fe, Rb, Sr, Mo, W, U. Корреляционная зависимость может быть косвенным показателем существования единых источников поступления этих элементов. Содержания Zn, Sb, Ba не имеют корреляционной связи с содержаниями других элементов. Для проб 2017 г. установлены следующие корреляционные связи (r > 0.7): Li, Al, Si, Sc, Ti, V, Mn, Fe, Rb, Sr, Ce, Pr, Nd, Gd, Pb, Bi, U.
Содержания растворенных форм элементов в исследованных реках и озерах бассейна Кучерлы в некоторых случаях выше установленных нормативов ПДК вредных веществ. ПДК для водных объектов рыбохозяйственного значения [22] были превышены в большинстве объектов по Al (3.5–1.1 ПДК), в р. Кучерле и оз. Кучерлинском – по Fe (1.8–1.3 ПДК) и Zn (1.2 ПДК), в оз. Дарашколь – по Zn (2.0–1.2 ПДК). Зафиксировано превышение ПДК в питьевой воде в истоке р. Кучерлы – по Al (1.4 ПДК [26]) и Sb (1.7 ПДК [3, 26]), в озерах Кучерлинском и Зеленом – по Sb (2.9–2.7 ПДК [3, 26]). Содержание в составе снега и фирна следующих элементов превышает нормативные показатели: Al (2.5 ПДК [22]), P (1.6 ПДК [22]), K (2.8 ПДК [22], 2.3 ПДК [9, 10], 1.4 ПДК [26]), Mn (6.2 ПДК [22], 1.2 ПДК [26]), Fe (1 ПДК [22]), Cu (2.8 ПДК [22]), Zn (6.7 ПДК [22]), Sb (1.2 ПДК [3, 26]). В воде р. Коксы в окрестностях с. Усть-Кокса зафиксировано высокое содержание Mn (10 ПДК [22], 1 ПДК [3, 25], 2 ПДК [26]), Sb (2.5 ПДК [3, 26]) (табл. 2).
ЗАКЛЮЧЕНИЕ
Вода в бассейне Кучерлы ультрапресная, нейтральная до слабощелочной, относится к кальциевой группе. В июле 2017 г. величины pH (6.5–7.2) были ниже, чем в августе 2016 г. (7.3–8.3). ОВП поверхностных вод в августе 2016 г. соответствовал окислительной (173–222 мВ), а в июле 2017 г. – переходной геохимической обстановке (47–88 мВ). При этом определяющие факторы в динамике физико-химических показателей, вероятно, – обильные дожди, повышающие уровень водообмена, а также поступление талых вод ледников и снежников с низкими значениями pH. Кислые дождевые осадки дренируют верхний слой почвы и вымывают в реки и озера растворы с высоким содержанием гумусовых кислот, способствующие понижению pH и ОВП поверхностных вод.
Содержания Na, Mg, Al, Si, K, Ca, Fe, Zn, Rb, Sr, Mo, Ba, U увеличиваются в направлении от верхней части водосбора р. Кучерлы вниз, поэтому, вероятно, эти элементы поступают в воду в результате выщелачивания горных пород. Анализ корреляционных матриц содержания растворенных форм элементов выявил прямые корреляционные связи (r > 0.7): Li, Na, Mg, Al, Si, K, Ca, Sc, Ti, V, Cr, Mn, Fe, Rb, Sr, Mo, Ce, Pr, Nd, Gd, W, Pb, Bi, U, что может означать наличие общих путей поступления элементов в водные объекты из природных источников. Выщелачивание химических элементов из горных пород и почв – определяющий фактор формирования состава природных вод бассейна Кучерлы при меньшем влиянии атмосферных осадков. Содержания Zn, Sb, Ba не имеют корреляционной связи с содержаниями других элементов. Отсутствие корреляции может быть связано с дополнительным поступлением элементов из обогащенных этими элементами пород.
В исследованных реках и озерах бассейна Кучерлы наблюдается превышение ПДК вредных веществ для водных объектов рыбохозяйственного значения по Al (в р. Кучерле, озерах Кучерлинском, Зеленом, Оруколь, Дарашколь), Fe (в р. Кучерле, оз. Кучерлинском), Zn (в р. Кучерле, озерах Кучерлинском, Дарашколь) и ПДК в питьевой воде по Al (в оз. Кучерлинском), Sb (в озерах Кучерлинском и Зеленом). В снеге и фирне ледника Иолдо-Айры ПДК для водных объектов рыбохозяйственного значения превышены по Al, P, K, Mn, Fe, Cu, Zn, а ПДК в питьевой воде – по K, Mn, Sb. В р. Коксе (с. Усть-Кокса) ПДК в питьевой воде превышены по Mn и Sb.
Авторы выражают искреннюю благодарность А.А. Князеву, А.В. Полукарову, М.Е. Бочкарeву, Н.В. Лукьянчиковой (ИХБФМ СО РАН) за помощь в проведении экспедиционных работ, И.В. Николаевой (ИГМ СО РАН), С.С. Шацкой (ИХТТМ СО РАН) за помощь в аналитических исследованиях.
Список литературы
Борисова Е.А. Анализ воды: методическое пособие. Ижевск: УдГУ, 2013. 30 с.
Вомперский С.Э. Болота и заболоченные леса в свете задач устойчивого природопользования. Материалы совещания. 1999. [Электронный ресурс] URL: https://myzooplanet.ru/bolotovedenie_905/bolota-zabolochennyie-lesa-svete-zadach.html. (01.01.2020)
ГН 2.1.5.1315-03 Предельно допустимые концентрации химических веществ в воде водных объектов хозяйственно-питьевого и культурно-бытового водопользования. М., 2003. 154 с.
ГН 2.1.5.2280-07 Предельно допустимые концентрации химических веществ в воде водных объектов хозяйственно-питьевого и культурно-бытового водопользования. Гигиенические нормативы. Дополнения и изменения № 1 к ГН 2.1.5.1315-03. М.: ФЦГиЭ Роспотребнадзора, 2008. 11 с.
ГОСТ 31861-2012 Вода. Общие требования к отбору проб. Межгосударственный стандарт. М.: Стандартинформ, 2013. 36 с.
ГОСТ 31870-2012 Вода питьевая. Определение содержания элементов методами атомной спектрометрии. Межгосударственный стандарт. М.: Стандартинформ, 2013. 18 с.
Государственная геологическая карта Российской Федерации. 1 : 200 000. Сер. Алтайская. Лист М-45-77. СПб., 2001.
Гусева Т.В., Заика Е.А., Виниченко В.Н., Молчанова Я.П., Аверочкин Е.М. Гидрохимические показатели состояния окружающей среды. Справочные материалы. М.: СоЭС, 2000. 148 с.
Директива 80/778/EEC от 15.07.1980 о качестве питьевой воды, предназначенной для употребления человеком // Журн. Европейского Сообщества. 1980. L229. С. 11–29.
Директива 98/83/ЕС от 03.11.1998 о качестве воды, предназначенной для употребления человеком // Журн. Европейского Сообщества. 1998. OJ L 330. 23 с.
Зверев В.П. Гидрогеохимия осадочного процесса. М.: Наука, 1993. 176 с.
Зенин А.А., Белоусова Н.В. Гидрохимический словарь. Л.: Гидрометеоиздат, 1988. 240 с.
Кадастр особо охраняемых природных территорий Республики Алтай / Под ред. A.M. Маринина. Барнаул: Азбука, 2014. 456 с.
Карандашев В.К., Туранов А.Н., Орлова Т.А., Лежнев А.Е., Носенко С.В., Золотарева Н.И., Москвина И.Р. Использование метода масс-спектрометрии с индуктивно-связанной плазмой в элементном анализе объектов окружающей среды // Заводская лаборатория. Диагностика материалов. 2007. Т. 73. № 1. С. 12–22.
Карта полезных ископаемых Республики Алтай. 1 : 1 000 000. СПб.: ВСЕГЕИ, 2006.
Катунский биосферный заповедник. Тр. / Под ред. Т.В. Яшиной. Барнаул: Пять плюс, 2006. Вып. 2. 80 с.
Красная книга Республики Алтай. Особо охраняемые территории и объекты / Отв. ред. А.М. Маринин. Горно-Алтайск: Госкомэкология Республики Алтай, ГАГУ, 2000. 272 с.
Крупнова Т.Г., Сухарев Ю.И. Химия окружающей среды. Учебное пособие. Челябинск: Изд-во ЮУрГУ, 2005. Ч. 2. 36 с.
МУК 1.2. 2743-10 Порядок отбора проб для выявления и идентификации наноматериалов в водных объектах. Методические указания // Экол. ведомости. 2010. № 11.
МУК 4.1. 1469-03 Атомно-абсорбционное определение массовой концентрации ртути в питьевой, природных и сточных водах. Сб. методических указаний. М.: ФЦ госсанэпиднадзора Минздрава России, 2004. 59 с.
Никаноров А.М. Гидрохимия. Учебное пособие. СПб.: Гидрометеоиздат, 2001. 448 с.
Приказ Федерального агентства по рыболовству от 18.01.2010 № 20 “Об утверждении нормативов качества воды водных объектов рыбохозяйственного значения, в том числе нормативов предельно допустимых концентраций вредных веществ в водах водных объектов рыбохозяйственного значения”. М., 2010. 214 с.
Р 52.24.353-2012 Отбор проб поверхностных вод суши и очищенных сточных вод. Рекомендации. Ростов-на-Дону: ГУ ГХИ, Росгидромет, 2012. 35 с.
Руководство по химическому анализу поверхностных вод суши / Под ред. А.Д. Семенова. Л.: Гидрометеоиздат, 1977. 541 с.
СанПиН 2.1.4.1074-01 Питьевая вода. Гигиенические требования к качеству воды централизованных систем питьевого водоснабжения. Контроль качества. М.: Минздрав России, 2002. 67 с.
СанПиН 2.1.4.1116-02 Питьевая вода. Гигиенические требования к качеству воды, расфасованной в емкости. Контроль качества. М.: Минздрав России, 2002. 40 с.
Фролова Н.Л., Повалишникова Е.С., Ефимова Л.Е. Комплексные исследования водных объектов Горного Алтая (на примере бассейна р. Мульты) – 75 лет спустя // Изв. РАН. Сер. геогр. 2011. № 2. С. 113–126.
Brahney J., Ballantyne A.P., Kociolek P., Leavitt P.R., Farmer G.L., Neff J.C. Ecological changes in two contrasting lakes associated with human activity and dust transport in western Wyoming // Limnol. Oceanogr. 2015. V. 60 (2). P. 678–695.
Carling G.T., Rupper S.B., Fernandez D.P., Tingey D.G., Harrison C.B. Effect of Atmospheric Deposition and Weathering on Trace Element Concentrations in Glacial Meltwater at Grand Teton National Park, Wyoming, U.S.A. // Arctic, Antarctic, and Alpine Res. 2017. V. 49(3). P. 427–440.
Manan A., Ying H.C., Xinxin G., Xing-Min Z. Microwave assisted digestion followed by ICP-MS for determination of trace metals in atmospheric and lake ecosystem // J. Environ. Sci. 2017. V. 55. P. 1–10.
Sander S.G., Anderson B., Reid M.R., Kim J.P., Hunter K.A. Trace metal chemistry in the pristine freshwater Lake Hauroko, Fiordland, New Zealand // Microchem. J. 2013. V. 111. P. 74–81.
Santolaria Z., Arruebo T., Urieta J.S., Lanaja F.J., Pardo A., Matesanz J., Rodriguez-Casals C. Hydrochemistry dynamics in remote mountain lakes and its relation to catchment and atmospheric features: the case study of Sabocos Tarn, Pyrenees // Environ. Sci. Pollut. Res. 2015. V. 22. P. 231–247.
Zaharescu D.G., Palanca-Solerb A., Hoodac P.S., Tanased C., Burgheleaa C.I., Lestere R.N. Riparian ecosystem in the alpine connectome. Terrestrialaquatic and terrestrial-terrestrial interactions in high elevation lakes // Preprint version bioRxiv. 2015. https://doi.org/10.1101/035576
Дополнительные материалы отсутствуют.


