Водные ресурсы, 2022, T. 49, № 6, стр. 701-707
Динамика содержания железа в воде Рыбинского водохранилища на современном этапе
Н. Г. Отюкова *
Институт биологии внутренних вод им. И.Д. Папанина РАН
152742 пос. Борок, Ярославской обл., Россия
* E-mail: ong70@mail.ru
Поступила в редакцию 12.04.2021
После доработки 01.10.2021
Принята к публикации 29.03.2022
- EDN: SZOVFY
- DOI: 10.31857/S0321059622060116
Аннотация
В Рыбинском водохранилище (Верхняя Волга) в 2012–2019 гг. исследована динамика содержания валового и растворенного железа общего в поверхностном и придонном горизонтах. Определены сезонные и межгодовые вариации в концентрациях железа в водоеме. С помощью корреляционного анализа показано, что существует достоверная положительная связь между содержанием валового и растворенного железа общего и объемом водного стока. Дана сравнительная характеристика полученных данных с ретроспективными. Отмечено, что за последние годы не произошло существенных изменений содержания валового железа в водохранилище, полученные концентрации железа сопоставимы с таковыми более ранних периодов.
Наличие железа в природных водах обусловлено высоким его кларком. Природные условия на водосборе, выщелачивание горных пород, грунтовые воды, антропогенное воздействие – определяющие факторы формирования содержания железа в поверхностных водах.
Биогенные вещества, в частности железо, в воде – один из важнейших факторов биологической продуктивности водоема. Изменения содержания железа влияют на развитие гидробионтов, так как оно входит в состав молекул порфинов и белков, участвующих в транспорте кислорода. Железо содержится в составе ферментов, ответственных за окислительно-восстановительные реакции в живом организме [15], и оказывает существенное влияние на биодоступность многих химических элементов [13]. Дефицит железа в воде либо снижение его биодоступности приводят к угнетению развития фитопланктона [12].
Содержание железа > ПДК (0.3 мг/дм3 для водных объектов хозяйственно-питьевого и культурно-бытового назначения) существенно ухудшает органолептические свойства воды, делает ее малопригодной для использования. В воде с повышенным содержанием железа создаются благоприятные условия для развития железобактерий, продукты жизнедеятельности которых являются канцерогенами. Повышенное содержание железа также негативно влияет на гидробионтов. Гидроксиды железа, образующиеся в щелочной среде, вызывают отравление рыб. За массовую гибель гидробионтов отвечают соединения железа(II), связывающие растворенный в воде кислород.
В водных объектах железо содержится в широких диапазонах концентраций. В речных водах его содержание 10–1400, в морских 0.06–0.44 мкг/дм3 [14]. Содержание железа в поверхностных водах повышается с увеличением концентрации растворенного органического вещества, поэтому в водоемах с болотным питанием концентрации этого компонента могут достигать 20–30 мг/дм3 [16].
Для бассейна Верхней Волги характерны обширные заболоченные территории, благодаря которым в воду поступает большое количество органического вещества. Основную массу железа в Волгу вносят ее притоки, воды которых маломинерализованы и содержат большее количество органических веществ. Так, малый приток Рыбинского водохранилища р. Ильд, берущая начало в заболоченной местности, характеризуется высокими цветностью, концентрацией органического вещества, железа [7]. А приток оз. Плещеево руч. Язевка (Ярославская обл.), питающийся преимущественно болотными водами, характеризуется запредельным содержанием органического вещества (бихроматная окисляемость – 114 мгО/дм3, перманганатная окисляемость – 90 мгО/дм3, цветность – 750 град.) и железа (валового Feвал – 11.2, растворенного общего Feраств – 5.59 мг/дм3) [6, 8].
Главная миграционная форма железа в природных водах – взвешенная Feвзв с частицами размером >0.45 мкм [1]. Во взвешенном веществе железо может переноситься как в органической, так и в минеральной форме. В зависимости от морфологии и гидродинамики водоема Feвзв либо потребляется фитопланктоном, либо осаждается. Растворенное железо может находиться в ионной форме, в виде комплексных соединений с минеральными и органическими веществами [1].
Цель работы – анализ межгодовой динамики содержания Feвал и Feраств в воде Рыбинского водохранилища за период 2012–2019 гг.; изучение зависимости содержания форм железа от объема водного стока; сопоставление полученных новых данных с ретроспективными.
МАТЕРИАЛЫ И МЕТОДЫ
Рыбинское водохранилище находится в границах трех административных областей – Ярославской, Вологодской и Тверской. Бассейн водохранилища расположен в пределах лесной зоны, в подзоне южной тайги, значительные площади занимают “ополья”. Древние осадочные породы, выступающие на поверхность в районе водохранилища, нижнетриасовые континентальные отложения представлены пестроцветными глинами и мергелями. Рельеф побережья плоский, слабо расчлененный. Климат на побережье характеризуется умеренно теплым летом, умеренно холодной зимой и достаточным увлажнением [9].
Гидрохимическая характеристика водохранилищ требует прежде всего знания исходных данных о химизме речных вод, за счет которых происходит его наполнение и питание. В водохранилище вода уже в других условиях подвергается изменениям, при которых главную роль играет взаимодействие воды с дном. Особенно сильно влияние дна проявляется в первые годы после образования водохранилища, когда активно протекает переработка растительного и почвенного покрова суши.
Рыбинское водохранилище имеет площадь зеркала при нормальном подпорном уровне (НПУ = 102 м) 4550 км2, объем – 25.4 км3, среднюю глубину – 5.6 м, коэффициент водообмена – 1.9 год–1. Оно замыкает бассейн Верхней Волги [11]. Рыбинское водохранилище – водоем преимущественно весеннего наполнения, доля весеннего притока составляет до 48% годового притока поверхностных вод [9]. Волжский плес водохранилища заполняется в основном водами Волги в период половодья. Воды Шексны и Мологи заполняют соответствующие плесы, формируя водные массы Центрального плеса, который составляет 70% объема водохранилища.
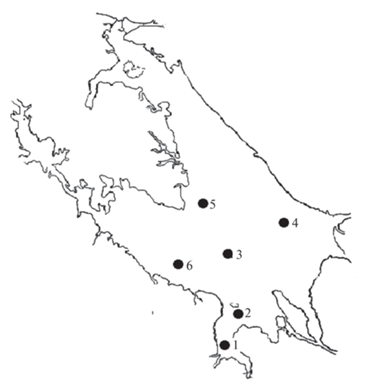
Исследования проведены на шести стандартных глубоководных (до 14 м) станциях Рыбинского водохранилища: Наволок (58°22′ с.ш., 38°23′ в.д.), Средний Двор (58°31′ с.ш., 38°19′ в.д.), Измайлово (58°27′ с.ш., 38°30′ в.д.), Брейтово (58°19′ с.ш., 37°57′ в.д.) – Центрального плеса; Коприно (58°04′ с.ш., 38°18′ в.д.) и Молога (58°13′ с.ш., 38°27′ в.д.) – Волжского плеса, принимающего воды р. Волги (рис. 1).
Рис. 1.
Картосхема территории расположения станций отбора проб на Рыбинском водохранилище. 1 – Коприно, 2 – Молога, 3 – Наволок, 4 – Средний Двор, 5 –Измайлово, 6 – Брейтово.
Пробы воды для анализа отбирали с поверхностного (0.5 м от поверхности) и придонного (0.5 м от дна) горизонтов батометром Рутнера в период открытой воды с периодичностью в среднем 1–2 раза в месяц. В зимнее время съемки были эпизодическими. Содержание Feвал (сумма Feраств и Feвзв) и Feраств (сумма истинно растворенного и коллоидного железа) определяли фотометрическим методом с орто-фенантролином. Погрешность метода в диапазоне содержания 0.1–1.0 мг/дм3 – 20%. Feраств определяли в фильтрате, полученном фильтрованием пробы через мембранный фильтр “Synpor” с диаметром пор 0.45 мкм. Feвзв вычисляли по разности между содержанием Feвал и Feраств. Данные по объему водного стока Рыбинского водохранилища приведены на основе материалов Рыбинской гидрометеорологической обсерватории “Ярославского центра по метеорологии мониторингу окружающей среды”.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
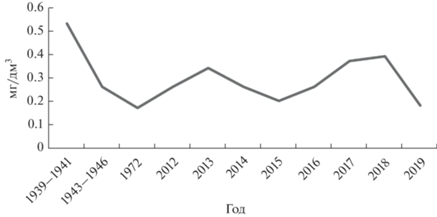
Изучение содержания железа в водной толще Рыбинского водохранилища проводилось в разные годы, но, к сожалению, исследователи не всегда указывали метод его определения. Первые данные по содержанию железа в воде Рыбинского водохранилища получены в 1939 г. – за два года до начала его функционирования. На базе биологического стационара “Борок” А.П. Щербаковым были начаты исследования по гидрохимии рек Волги, Мологи и Шексны, образующих водоем. Концентрации железа определяли методом с роданистым аммонием и в среднем за год в период 1939–1941 гг. они составили, мг/дм3: в Волге – 0.71, в Мологе – 0.61 и в Шексне – 0.71 [10]. С 1943 г. на Рыбинском водохранилище гидрохимические наблюдения стали систематическими. Feвал определялось колориметрическим методом с роданистым калием. Среднегодовые концентрации железа за 1943–1944 гг. в воде водохранилища составляли 0.3–0.5 мг/дм3. В 1945–1946 гг. количество железа снизилось, что объясняется постепенным становлением водохранилища. При этом максимальное содержание железа приходилось на паводок, минимальное – на летнюю межень. Далее от осени к зиме вновь отмечено накопление железа [3]. В начале 1970-х гг. вышла монография “Рыбинское водохранилище” [9], где обобщены все данные по содержанию железа со времени становления водоема. Осредненные годовые концентрации Feвал в основных реках, питающих водохранилище, следующие, мг/дм3: в Волге – 0.36, в Мологе – 0.88 и в Шексне – 0.51. В водохранилище содержание железа составляло 0.19 мг/дм3, что гораздо меньше, чем в смеси речных вод (0.50 мг/дм3). Установлено, что в водохранилище аккумулируется большая часть поступающего в него железа [9].
За исследованный период (2012–2019 гг.) осредненная внутригодовая концентрация Feвал в поверхностном слое водохранилища составляет 0.3 мг/дм3, что в 3 раза превышает ПДК водных объектов рыбохозяйственного значения (0.1 мг/дм3). Feраств находится в концентрациях 0–0.42 мг/дм3 (табл. 1).
Таблица 1.
Средние за исследованный период концентрации железа (мг/дм3) по сезонам в воде Рыбинского водохранилища
| Год | Сезон | Поверхностный горизонт | Придонный горизонт | ||||||
|---|---|---|---|---|---|---|---|---|---|
| Feвал | Feраств | Feвзв | Feраств/Feвзв | Feвал | Feраств | Feвзв | Feраств/Feвзв | ||
| 2012 | Весна | 0.49 | 0.22 | 0.27 | 0.82 | Пробы не отбирались | |||
| Лето | 0.24 | 0.10 | 0.14 | 0.71 | |||||
| Осень | 0.19 | 0.05 | 0.21 | 0.24 | |||||
| 2013 | Весна | 0.56 | 0.33 | 0.23 | 1.44 | 0.61 | 0.43 | 0.18 | 2.39 |
| Лето | 0.28 | 0.14 | 0.14 | 1.0 | 0.45 | 0.18 | 0.27 | 0.67 | |
| Осень | 0.46 | 0.10 | 0.36 | 0.28 | 0.44 | 0.11 | 0.33 | 0.33 | |
| Зима | 0.19 | 0.09 | 0.10 | 0.90 | 0.38 | 0.19 | 0.19 | 1.0 | |
| 2014 | Весна | 0.37 | 0.10 | 0.27 | 0.37 | 0.39 | 0.09 | 0.30 | 0.30 |
| Лето | 0.21 | 0.04 | 0.17 | 0.24 | 0.36 | 0.05 | 0.31 | 0.16 | |
| Осень | 0.31 | 0.01 | 0.30 | 0.03 | 0.44 | 0.02 | 0.42 | 0.05 | |
| Зима | 0.21 | 0.13 | 0.08 | 1.63 | 0.57 | 0.20 | 0.37 | 0.54 | |
| 2015 | Весна | 0.21 | 0.04 | 0.17 | 0.24 | 0.25 | 0.05 | 0.20 | 0.25 |
| Лето | 0.27 | 0.05 | 0.22 | 0.23 | 0.37 | 0.07 | 0.30 | 0.23 | |
| Осень | 0.23 | 0.11 | 0.12 | 0.92 | 0.30 | 0.09 | 0.21 | 0.43 | |
| Зима | 0.06 | 0.03 | 0.03 | 1.0 | 0.13 | 0.07 | 0.06 | 1.17 | |
| 2016 | Весна | 0.29 | 0.13 | 0.16 | 0.81 | 0.40 | 0.13 | 0.27 | 0.48 |
| Лето | 0.17 | 0.04 | 0.13 | 0.31 | 0.26 | 0.06 | 0.20 | 0.30 | |
| Осень | 0.30 | 0.07 | 0.23 | 0.30 | 0.31 | 0.07 | 0.24 | 0.29 | |
| Зима | 0.23 | 0.09 | 0.14 | 0.64 | 0.38 | 0.16 | 0.22 | 0.73 | |
| 2017 | Весна | 0.46 | 0.32 | 0.14 | 2.29 | 0.53 | 0.33 | 0.20 | 1.65 |
| Лето | 0.31 | 0.15 | 0.16 | 0.94 | 0.43 | 0.15 | 0.28 | 0.54 | |
| Осень | 0.35 | 0.17 | 0.18 | 0.94 | 0.43 | 0.18 | 0.25 | 0.72 | |
| Зима | 0.38 | 0.28 | 0.10 | 2.80 | 0.57 | 0.28 | 0.29 | 0.97 | |
| 2018 | Весна | 0.54 | 0.42 | 0.12 | 3.50 | 0.56 | 0.45 | 0.11 | 4.09 |
| Лето | 0.30 | 0.19 | 0.11 | 1.73 | 0.43 | 0.20 | 0.23 | 0.87 | |
| Осень | 0.32 | 0.09 | 0.23 | 0.39 | 0.43 | 0.10 | 0.33 | 0.30 | |
| 2019 | Весна | 0.18 | 0.10 | 0.08 | 1.25 | 0.26 | 0.09 | 0.17 | 0.53 |
| Лето | 0.14 | 0.05 | 0.09. | 0.56 | 0.49 | 0.07 | 0.44 | 0.16 | |
| Осень | 0.23 | 0 | 0.23 | 0 | 0.38 | 0.01 | 0.37 | 0.03 | |
Концентрации Feвал в весенний период – максимальные с последующей тенденцией снижения летом и в большинстве случаев повышения осенью. В зимнюю межень содержание Feвал либо остается на осеннем уровне, либо снижается. Такие изменения вызваны характером питания водохранилища в разные сезоны. В половодье в водохранилище с речными потоками поступают преимущественно поверхностно-склоновые воды. Они богаты органическими веществами, содержащими в значительном количестве гуминовые вещества и железоорганические комплексы, что обеспечивает максимальные концентрации Feвал и Feраств. В этот период нет интенсивного фотосинтеза, что также способствует высокому содержанию железа. Для водохранилищ Днепровского каскада повышенное содержание железа также обусловлено высокими концентрациями гумусовых веществ, с которыми железо образует прочные комплексные соединения [4]. В летнюю межень питание водохранилища в основном происходит за счет атмосферных осадков и грунтовых вод с более высоких горизонтов, содержащих меньше железа, также оно активно потребляется растительными организмами. В это время под воздействием ультрафиолета идет осаждение взвешенных веществ вместе с гумусовыми органическими веществами. Перечисленные факторы способствуют снижению концентрации железа в воде водохранилища в летне-осеннее время. При сопоставлении современных данных по содержанию Feвал в Рыбинском водохранилище с более ранними не установлено каких-либо существенных различий (рис. 2).
В подледный период питание водохранилища происходит исключительно за счет грунтовых вод, которые по сравнению с поверхностно-склоновыми имеют меньше растворенных органических веществ и, соответственно, железоорганических комплексов. В зимнюю межень наблюдается снижение концентраций Feвал в поверхностном горизонте водохранилища (табл. 1).
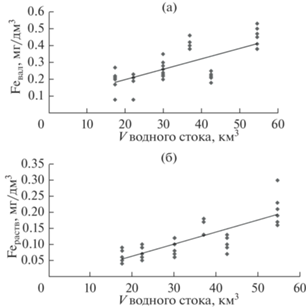
Между Feвал, Feраств и объемом водного стока выявлена достоверная положительная корреляционная связь (r = 0.76 и r = 0.87, р < 0.05 соответственно) (рис. 3).
Рис. 3.
Корреляционное поле зависимости Feвал (а) и Feраств (б) от объема водного стока V в Рыбинском водохранилище в 2012–2019 гг.
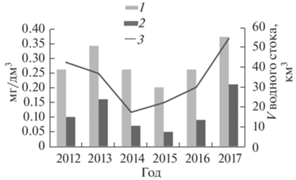
Ранее установлено, что объем годового стока определяет общее количество органического вещества в водохранилище [5]. Соответственно, можно заключить, что объем годового стока определяет и количество Feвал и Feраств в водохранилище (рис. 4).
Рис. 4.
Зависимость содержания Feвал и Feраств от объема водного стока V в воде Рыбинского водохранилища. 1 – Feвал, 2 – Feраств, 3 – Vстока.
Соотношение Feраств/Feвзв – показатель, позволяющий получить представление о формах нахождения железа в водоеме. Весной, когда железо-гумусовые комплексы составляют значительную часть растворенного железа, в водохранилище оно может доходить до 3.5, что свидетельствует о доминировании растворенных форм железа над взвешенными. Летом и осенью преобладающей формой железа была взвешенная, в зимнюю межень Feраств/Feвзв = 0.64–2.8, т. е. в разные годы исследования могла преобладать как растворенная форма железа, так и взвешенная. Отмечено, что наименьшее значение Feраст/Feвзв характерно для периодов с минимальным уровнем водного стока, а наибольшие – с максимальным. Статистический анализ выявил обратную корреляционную связь между Feвзв и объемом водного стока (r = –0.35).
На протяжении всего периода исследования в водохранилище наблюдалась вертикальная стратификация железа с наибольшим его содержанием у дна и наименьшим – в поверхностном горизонте. Максимальная стратификация отмечена зимой и летом 2019 г., когда концентрации между горизонтами различались в 1.5–2.7 и 3.5 раза соответственно. На содержание железа влияют анаэробные условия, возникающие в гиполимнионе водохранилища. Большие концентрации железа у дна – следствие минерализации органических веществ (отмерший планктон). В работе [9] отмечено существенное влияние процесса седиментации на содержание железа в Рыбинском водохранилище. При исследованиях микроскопических компонентов взвесей обнаружили большое количество железистых частиц. Минеральная часть взвесей состоит в основном из гидратов окиси железа [2]. Причина седиментации железа – распад железо-органических соединений, в составе которых растворенное железо находится в тесной связи с органическим веществом. Также в водохранилище минерализуется треть всей массы аллохтонного органического вещества. В зависимости от сезона содержание железа в придонных слоях колеблется в широких пределах: Feвал – от 0.13 до 0.61, Feраств – от 0.01 до 0.43 мг/дм3. В условиях продолжительного ледостава и дефицита растворенного кислорода увеличение концентрации этого компонента происходит в зимнюю межень. Холодные кислые растворы обогащаются железом за счет грунтов.
ВЫВОДЫ
Изучение межгодовой динамики валового и растворенного железа общего выявило его достоверную положительную корреляционную связь с объемом водного стока (соответственно r = 0.76 и r = 0.87, p < 0.05), что может свидетельствовать о преобладающей роли последнего в формировании содержания железа в воде Рыбинского водохранилища. Анализ динамики содержания железа валового за многолетний период показал, что за последние годы в его содержании в водохранилище не произошло существенных изменений, полученные новые данные сопоставимы с ретроспективными. В водохранилище отмечена вертикальная стратификация железа с максимальным содержанием у дна и минимальным – в поверхностном горизонте. В Рыбинском водохранилище определяющие факторы содержания железа – объем водного стока и седиментация.
На протяжении всего периода исследований вне зависимости от сезона концентрация железа валового превышала ПДК водных объектов рыбохозяйственного значения. Повышенное содержание железа в воде Рыбинского водохранилища обусловлено природными условиями на водосборе, а именно – значительно заболоченными территориями, откуда берут начало притоки, питающие водоем.
Автор выражает благодарность Л.А. Кучай (ИБВВ им. И.Д. Папанина РАН) за помощь в обработке данных.
Список литературы
Глаголева М.А. Формы миграции элементов в речных водах // К познанию диагенеза осадков. М., 1959. С. 5–28.
Зиминова Н. А. Состав взвесей Рыбинского водохранилища // Тр. Инст. биол. внутр. вод АН СССР. М.; Л.: Наука, 1965. Вып.7 (10). С. 100–111.
Кудрявцев Д.Д. Материалы к гидрохимической характеристике Волжского отрога Рыбинского водохранилища 1943–1946 гг. // Тр. биол. ст. Борок. 1950. Вып. 1. С. 35–78.
Линник П.Н., Жежеря В.А., Линник Р.П. Железо в природных поверхностных водах Украины: содержание, особенности миграции и биологическая роль // Гидробиол. журн. 2018. Т. 54. № 3. С. 70–88.
Литвинов А.С., Степанова И.Э. Зависимость содержания органического вещества и биогенных элементов от гидрологических условий в Рыбинском водохранилище // Водное хоз-во России. 2015. № 3. С. 20–31.
Отюкова Н.Г. Гидрохимический режим притоков озера Плещеево Ярославская область) // Тр. ИБВВ. Борок: ИБВВ РАН, 2020. Вып. 90 (93). С. 27–32.
Отюкова Н.Г. Динамика содержания железа в речных аквальных комплексах (на примере реки Ильд бассейна Рыбинского водохранилища) // Тр. ИБВВ. Ярославль: Филигрань, 2016. Вып. 75 (78). С. 75–81.
Отюкова Н.Г. Органическое вещество в водных объектах особо охраняемых природных территорий на примере притоков оз. Плещеево (Ярославская обл.) и р. Таденки Приокско-Террасного биосферного заповедника (Московская обл.) // Вод. ресурсы. 2021. Т. 48. № 3. С. 344–353.
Рыбинское водохранилище и его жизнь. Л.: Наука, 1972. 364 с.
Щербаков А.П. Гидрохимический режим Волги, Мологи и Шексны в районе Рыбинского водохранилища (до наполнения водохранилища) // Тр. биол. ст. Борок. Л., 1950. Вып. 1. С. 7–34.
Экологические проблемы Верхней Волги. Ярославль: ЯГТУ, 2001. 427 с.
Chen M., Wang W.-X. Accelerated uptake by phytoplankton of iron bound to humic acids // Aquat. Biol. 2008. V. 3. P. 155–166.
Lofts S., Tipping E., Hamilton-Taylor J. The chemical speciation of Fe(III) in freshwaters // Aquat. Geochem. 2008. V. 14. P. 337–358.
Rabajczyk A., Namiesnik J. Speciation of iron in the aquatic environment // Water Environ. Res. 2014. V. 86. № 8. P. 741–758.
Vuori K.-M. Direct and indirect effects of iron on river ecosystems // Ann. Zool. Fennici. 1995. V. 32. P. 317–329.
Wotter S.E.T., Niencheski L.F.H., Milani M.R. Chemical speciation and dissolved iron in the pore water of Patos lagoon sediments – Brazil // Portugaliae Electrochimica Acta. 2011. V. 29. № 3. P. 155–163.
Дополнительные материалы отсутствуют.