Физикохимия поверхности и защита материалов, 2019, T. 55, № 1, стр. 43-47
Особенности температурной зависимости электрического сопротивления оксида графена
А. А. Бабаев 1, *, М. Е. Зобов 1, Д. Ю. Корнилов 2, С. В. Ткачев 2, Е. И. Теруков 3, В. С. Левицкий 4
1 Федеральное государственное бюджетное учреждение наук Институт физики
им. Х.И. Амирханова Дагестанского научного центра РАН
367003 Махачкала, Россия
2 ООО “АкКо Лаб”
Москва, Россия
3 Федеральное государственное бюджетное учреждение наук
Физико-технический институт им. А.Ф. Иоффе РАН
194021 Санкт-Петербург,, Россия
4 ООО “НТЦ тонкопленочных технологий в энергетике”
194064 Санкт-Петербург,, Россия
* E-mail: babaev-arif@mail.ru
Поступила в редакцию 23.03.2018
После доработки 17.05.2018
Принята к публикации 21.06.2018
Аннотация
Исследованы температурная зависимость электрического сопротивления оксида графена в процессе непрерывного нагрева и охлаждения в атмосфере в интервале температур 300–550 K и спектры комбинационного рассеяния света. В интервале 300–370 K сопротивление постоянно в процессе охлаждения и последующем нагреве термостабильно. Температурная зависимость сопротивления в области 370–550 K меняется по активационному закону. Уменьшение сопротивления с ростом температуры связано с удалением функциональных кислородсодержащих групп, что подтверждается результатами исследования спектров комбинационного рассеяния света.
ВВЕДЕНИЕ
В настоящее время наблюдается большой интерес к изучению функциональных свойств оксида графена, поскольку он является перспективным материалом для многих отраслей индустрии, имеет высокий коммерческий потенциал, выступает в качестве сырья для получения самого графена.
Оксид графена, представляющий собой случайным образом распределенные по поверхности подложки небольшие островки графена с sp2-гибридизированными связями, окруженные обширными областями с sp3-связями, функционализированные кислородосодержащими группами (эпоксидные, гидроксильные, карбонильные и карбоксильные) [1]. Для широкого использования оксида графена требуется, в том числе, и проведение его восстановления до графена [2, 3]. Термообработка является одним из эффективных способов восстановления оксида графена, в результате которой удается значительно снизить содержание кислородосодержащих групп в оксиде графена [3].
Несмотря на значительные успехи в развитии методов получения графена и оксида графена, достигнутые в последние годы, создание технологии воспроизводимого формирования материала на различных подложках по-прежнему остается нерешенной задачей. Технологические ограничения имеющихся методов получения графена или не позволяют получать одиночные слои углеродных атомов большой площади [4], либо приводят к образованию материала с мозаичной структурой, состоящей из взаимно развернутых мелких (около 20–30 нм) фрагментов [5].
Одним из перспективных способов получения графена, позволяющего преодолеть указанные ограничения, является метод химического расщепления природного или пиролитического графита, который уже содержит в своей структуре графеновые листы [6]. Возможность применения подобного расщепления определяется способностью графита к интеркаливанию. Этот процесс приводит к увеличению расстояния между графеновыми слоями в структуре графита и в дальнейшем к его окислению. Наиболее распространенным методом химического расщепления графита является его окисление в жидкой среде с помощью перманганата калия, приводящее к образованию оксида графита [7]. Оксид графита (гидроокись графита, графитовая кислота) не имеет постоянного состава и при максимальной степени окисления его брутто-формула может варьировать в пределах от С2О до СОН, т.е. представляет собой (C2O)x(COH)x –1, где 0 < х < 1. Оксид графита состоит из стопок окисленных графеновых листов, по обе стороны и по краям которых находятся кислородсодержащие группы. Действие ультразвуковой обработки на оксид графита приводит к образованию оксида графена [8]. Оксид графена образует устойчивые дисперсии в гидрофильных растворителях, легко восстанавливается, частично теряя кислородсодержащие группы при нагреве, интенсивном освещении или при действии химических восстановителей. В результате восстановления оксида графена образуется графен. Это обстоятельство открывает возможность получения графеновых пленок на любых смачиваемых водой подложках путем осаждения пленок оксида графена из водных суспензий и последующего восстановления.
Следует отметить, что опубликованные результаты исследований, выполненных в целом ряде работ [9, 10], указывают на наличие существенных ограничений, препятствующих созданию технологии получения графена по выше обсуждаемой технологии. Важным препятствием для воспроизводимого получения графена является неоднородность синтезируемого оксида графена. Для решения данной задачи необходимо обеспечить условия предельного окисления графита и конроля образования в чешуйках оксида графена многочисленных дефектов углеродного слоя, связанных со сменой гибридизации углерода с sp2 на sp3 при взаимодействии с кислородом [9]. Следовательно, указанные обстоятельства существенным образом ограничивают возможности использования оксида графита при получении графена для структур электронных приборов [11].
В настоящее время оксид графена получают окислением графита известными хорошо отработанными методами: Броди [11], Штауденмайера [12] и Хаммерса [13], причем последний способ и его модификации являются наиболее распространенными. Обсуждаемые методы позволяют получать образцы оксида графена с различными физическими параметрами из-за различных концентраций дефектов.
В данной работе приводятся результаты исследования температурной зависимости сопротивления оксида графена (ООО “АкКо Лаб”,), в процессе непрерывного нагрева и охлаждения в атмосфере аргона в интервале температур 300–550 K.
ПОЛУЧЕНИЕ ОКСИДА ГРАФЕНА И МЕТОДИКА ИЗМЕРЕНИЙ
Исследуемые пленки были получены из водной дисперсии оксида графена с концентрацией 1 мг/мл путем нанесения на предметные стекла методом спин-коатинга при скорости вращения 5000 об./мин. Подача дисперсии оксида графена на поверхность подложки производилась по 0.1 мл.
Очистка стеклянных подложек проводилась в несколько стадий, содержащих следующие виды обработки:
– отмывка поверхностно-активным веществом (ПАВ);
– ополаскивание деионизованной водой (ДВ);
– выдержка в водном растворе 20% NaOH при комнатной температуре, в течение 20 мин;
– ополаскивание ДВ;
– выдержка в водном растворе 5% HF при комнатной температуре в течение 5 мин;
– ополаскивание ДВ;
– обработка в ультразвуковой ванне в течение 10 мин;
– ополаскивание ДВ;
– сушка на воздухе в течение 1 ч.
Исходным веществом для получения оксида графена служил китайский природный графит высокой чистоты (99.9% С), раздробленный в шаровой мельнице до фракции 200–300 мкм.
Оксид графена получали по модифицированному методу Хаммерса, приведенному в [14] (в перерасчете на 1 г природного графита).
Для получения водной дисперсии оксида графена использовали навеску массой 0.15 г, которую помещали в цилиндрический стакан объемом 250 мл, добавляли 150 мл деионизованной воды, затем производилась ультразвуковая обработка (частота 20.4 кГц, удельная мощность 0.1–1 Вт/см3) в течение 15 мин.
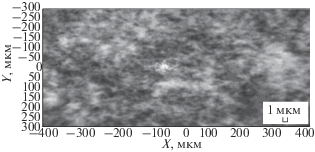
Содержащиеся в дисперсии чешуйки оксида графена латеральным размером от 0.1 до 4 мкм и толщиной до 1.5 нм (менее 10 графеновых слоев) были охарактеризованы современными физико-химическими методами анализа, результаты которых представлены в [14].
Методом рентгенофазового анализа установлено наличие уширенного интенсивного рефлекса, характерного для оксида графена (2θ = 11.5°). Согласно данным молекулярной спектроскопии, в спектрах оксида графена присутствуют следующие пики: D-полоса (~1320 см–1), G-полоса, характеризующая колебания системы sp2 углеродных связей (~1582 см–1), 2D-полоса (~2720 см–1). Считается, что появление D-полосы для оксида графена свидетельствует об образовании дефектной структуры по отношению к графиту. Методами СЭМ, АСМ, ПЭМ показано, что оксид графена имеет слоистую структуру; латеральные размеры чешуек оксида графена варьируются от 100 нм до 4 мкм, максимальная толщина составляет 1.5 нм (менее 10 графеновых слоев). Данные ИК-спектроскопии и РФЭС свидетельствуют о наличии различных функциональных кислородсодержащих групп в структуре ГО: С=O, С–O, –OH, C–OH, C(O)C. Методом С,H,N-анализа определено массовое содержание элементов в составе оксида графена, (мас. %): С (58.0 ± 1.0), H (1.5 ± ± 0.5), O (39.0 ± 1.0), N (0); мольное содержание С/O ~ 2/1.
Исходные образцы проявляли диэлектрические свойства с сопротивлением более 10 ГОм с большой шириной запрещенной зоны более 3 эВ. В качестве контактов использована серебряная паста. Расстояние между контактами 1.7 мм. Измерения температурной зависимости сопротивления исследовалось при непрерывном нагреве и охлаждении со скоростью 1–1.5 K в минуту. Спектры комбинационного рассеяния света (КРС) получены при помощи спектрометра LabRamHR 800 при комнатной температуре. Длина волны возбуждения при измерении спектров КРС составляла 532 нм. Мощность излучения в пучке лазера 2–3 мВт для предотвращения перегрева образца. Измерения сопротивления выполнены на четырех образцах двухзондовым методом, используя прибор Терраомметр Е6-13А.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
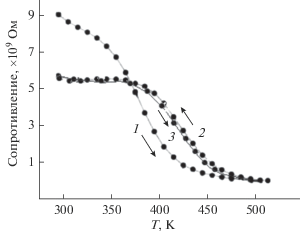
На рис. 2. представлены результаты исследования температурной зависимости сопротивления в режиме динамического нагрева – 1 и охлаждения – 2 и последующего нагрева. Видно, что в процессе нагрева и охлаждения исходного оксида графена сопротивление уменьшается от 9 × 109 до 5.6 × 109 Oм при комнатной температуре, а в интервале температур 300–550 K сопротивление уменьшается до 0.8 × 109 Ом. В температурном интервале 370–550 K сопротивление меняется по активационному закону. В процессе охлаждения оксида графена в области температур 300–370 K сопротивление оксида графена постоянно. На температурной зависимости сопротивления наблюдается гистерезис. При последующем нагреве оксида графена сопротивление изменяется по кривой 2 рис. 2. Для объяснения полученных результатов проведены исследования оксида графена методом комбинационного рассеивания, который дает информацию о внутримолекулярных, межмолекулярных взаимодействиях и релаксационных процессах.
Рис. 2.
Температурная зависимость сопротивления оксида графена в процессе нагрева – 1, охлаждения – 2 и последующего нагрева – 3.
Элементарная ячейка графена содержит 2 атома углерода, поэтому существует шесть фононных ветвей: три акустических (А) и три оптических (О). Четыре из этих фононных ветвей (две акустические и две оптические) отвечают за планарные колебания атомов углерода в плоскости слоев (i), а остальные две отвечают за колебания в плоскости, перпендикулярной слоям (о). Колебания в плоскости слоев, подразделяются на колебания вдоль (L) или поперек (Т) связи С–С. Основной вклад в спектр КР дают iLO и iTO колебания. Схема, показывающая электронную дисперсию графена вблизи уровня Ферми в точках K и K' гексагональной зоны Бриллюэна, и дисперсионные кривые в зоне Бриллюэна приведены в работе [15].
Линия G в спектре КРС соответствует рассеянию света в Г-точке зоны Бриллюэна на оптическом фононе симметрии E2g, порожденном планарными колебаниями атомов углерода в плоскости слоев [16]. Эта полоса является дважды вырожденной и существует для всех углеродных материалов, имеющих sр2-гибридизацию. Процесс возникновения этой линии можно пояснить следующим образом: падающий фотон с энергией Еex резонансно возбуждает виртуальную электрон-дырочную пару, затем электрон или дырка рассеиваются на iLO или iTO фононе с энергией Ерп, и рекомбинируют с испусканием фотона с энергией Ept = Еех – Ерп. Для графена линия G вырождена, однако это вырождение может быть снято применением одноосной деформации к графеновому слою или при сворачивании графенового листа в углеродную нанотрубку. В этом случае произойдет расщепление линии G [17, 18].
Спектральная линия 2D обусловлена резонансным рассеянием света с участием двух фононов с одинаковой энергией, но противоположным направлением импульса. Рассеяние происходит в К-точке зоны Бриллюэна и вызвано симметричными колебаниями растяжения-сжатия графенового кольца. Падающий фотон возбуждает электрон-дырочную пару вблизи K-точки зоны Бриллюэна. Электрон неупруго рассеивается на iTO фононе в точку K'. Поскольку в процессе КРС должны выполняться законы сохранения энергии и импульса, то электрон обязан рассеяться обратно в K-точку прежде, чем произойдет рекомбинация с дыркой. В случае 2D-линии обратное рассеяние электрона происходит за счет второго iTO фонона. Аналогичный процесс может происходить и для дырки. Эти процессы получили название двойного резонанса, так как появление и рассеяние фотона и первый или второй процесс рассеяния фононов совпадают с электронными уровнями в графене.
Другой важной особенностью в спектрах КРС Г является линия D, появление которой обусловлено рассеянием на дефектах. Эта линия, также как и 2D, возникает при рассеянии на iTO фононе вблизи K-точки зоны Бриллюэна [19, 20], однако, в отличие от G и 2D линий, для выполнения закона сохранения импульса необходим дефект. В этом случае, электрон неупруго рассеивается на iTO фононе в K' точку, а затем упруго рассеивается на дефекте обратно в K-точку [21, 22]. Поскольку процесс рассеяния происходит с участием одного фонона, то частотный сдвиг для D-линии составляет половину значения от 2D-линии. Дефектом может являться любое нарушение симметрии решетки графена, например, sр3-дефекты [23], вакансии [24, 25], границы зерен [26] и др. [27–29].
На рис. 3а приведены типичные спектры КРС оксида графена. Видно, что в спектрах КРС присутствуют типичные узкие линии с положением максимума вблизи 1320 см–1 (линия D) и 1582 см–1 (линия G), а также 2D-полоса ~ 2720 см–1.
Рис. 3.
Спектры комбинационного рассеяния оксида графена а) до и после нагрева и охлаждения при Т = = 300 K. б) массив спектров КРС как функция числа слоев, расположенные по степени возрастания их интенсивности.

На рис. 3б приведен массив спектров КРС образца оксида графена. Интенсивность спектров КРС в различных точках слоя оксида графена существенно меняется и зависит от толщины слоя. Однако во всех спектрах существуют две основные D и G линии. Используя результаты работы [30], авторы которой показали зависимость толщины слоя оксида графена от интенсивности линии G в спектрах КРС, определили толщину слоя оксида графена в диапазоне от 1 до 10 слоев.
Природа данных пиков связана с колебаниями sp3-гибридизированных (полоса D) и sp2 – (полоса G) фрагментов углеродной сетки [31, 32]. Отношение интенсивностей D и G полос (ID/IG) пропорционально количественному отношению областей со связями углерода sp3-гибридизации и областей со связями углерода sp2-гибридизации, а также количественному отношению атомов кислорода и атомов углерода (О/С) в структуре оксида графена [33]. С увеличением температуры оксида графена отношение интенсивности (ID/IG) уменьшается от 1 до 0.95 (рис. 3), свидетельствует о том, что в оксиде графена уменьшается содержание кислорода и увеличивается доля областей углеродной сетки с sp2-связями. Высокая интенсивность и значительная ширина линии D в спектрах КРС указывает на большую концентрацию структурных дефектов. Используя результаты работы [34], в которой была предложена модель и методы расчета концентрации структурных дефектов в графене, нами была определена концентрация дефектов в структуре оксида графена Nd ~ ~ 1 × 1014c см–2. Удаление кислородсодержащих функциональных групп сопровождается уменьшением электрического сопротивления, приводит к изменению структуры оксида графена, в результате наблюдается гистерезисное поведение температурной зависимости сопротивления, которое исчезает при последующем нагреве. Из-за сильной связи кислорода с углеродом в интервале температур 300–370 K сопротивление оксида графена термостабильно. Дальнейшее уменьшение сопротивления от 0.8 × 109 Ом будет сопровождаться при более высоких температурах, свыше 550 K.
ЗАКЛЮЧЕНИЕ
Получены слои оксида графена с латеральными размерами чешуек от 0.1 до 4 мкм. Результаты исследования спектров КРС, в частности уменьшение интенсивности D полосы после термообработки от 1 до 0.95, связано с уменьшением содержания кислородосодержащих групп. Сопротивление оксида графена уменьшается с ростом температуры за счет уменьшения содержания кислородсодержащих групп. В интервале температур 300–370 K сопротивление оксида графена термостабильно. При этих температурах кислородсодержащие группы находятся в сильно связанном состоянии с углеродом. Для большего уменьшения кислородосодержащие группы, необходимы более высокие температуры.
Список литературы
Singh V., Joung D., Zhai L. et al. // Proress in Material Science. 2011. V. 56. P. 1178.
Pei S., Cheng Hu-M. // Carbon. 2012. V. 50. P. 3210.
Stankovich S., Dikin D., Finer R.D. et al. // Carbon. 2007. V. 45. P. 1558.
Allen M.J., Tung V.C., Kaner R.B. // Chem. Rev. 2010. V. 110. № LP. 132.
Bae S., Kim H., Lee Y. et al. // Nat. Nanotechnol. 2010. V. 5. № 8. P. 574–578.
Novoselov K., Fal V., Colombo L., Gellert P. et al. // Nature. 2012. V. 490. № 7419. P. 192–200.
Offeman R., Hummers W. // J. Am. Chem. Soc. 1958. V. 80. P. 1339–1339.
Bao Q., Eda G., Chhowalla M. // Nat. Chem. 2010. V. 2. № 12. P. 1015–1024.
Park S., Ruoff R.S. // Nat. Nanotechnol. 2009. V. 4. № 4. P. 217–224.
Chen W., Yan L. // Nanoscale. 2010. V. 2. P. 559.
Eda G., Fanchini G., Chhowalla M. // Nat. Nanotechnol. 2008. V. 3. № 5. P. 270–274.
Soldano C., Mahmood A., Dujardin E. // Carbon. 2010. V. 48. № 8. P. 2127–2150.
Brodie B.C. // Ann. Chim. Phys., 1860, 59. P. 466–472.
Ткачев С.В., Буслаева Е.Ю., Наумкин А.В. и др. // Неорганические материалы. 2012. Т. 48. № 8. С. 909–915.
Beams R., Cancado L.G., Novotny L. // J. Phys. Condens. Matter. 2015. V. 27. P. 083002.
Nemanich R.J., Solin S.A. // Phys. Rev B. 1979. V. 20. P. 392.
Ni Z.H., Chen W., Fan X.F. et al. // Phys. Rev. B. 2008. V. 77. P. 115416.
Jorio A., Souza Filho A.G., Dresselhaus G. et al. // Phys. Rev. B. 2002. V. 65. P. 155412.
Thomsen C., Reich S. // Phys. Rev. Lett. 2000. V. 85. P. 5214.
Das A., Chakraboty B., Sood A.K. // Bull. Mater. Sci. 2008. V. 31. P. 579.
Saito R., Jorio A., Souza Filho A.G. et al. // Phys. Rev. Lett. 2001. V. 88. P. 027401.
Pimenta M.A., Dresselhaus G., Dresselhaus M.S. et al. // Phys. Chem. Chem. Phys. 2007. V. 9. P. 1276.
Eckmann A., Felten A., Mishchenko A. et al. // Nano Lett. 2012. V. 12. P. 3925.
Lucchese M.M., Stavale F., Ferreira E.H.M et al. // Carbon. 2010. V. 48. P. 1592.
Cancado L.G., Jorio A., Ferreira E.H.M et al. // Nano Lett. 2001. V. 11. P. 3190.
Lespade P., Marchand A., Couzi M. et al. // Carbon. 1984. V. 22. P. 375.
Casiraghi C., Hartschuh A., Qian H. et al. // Nano Lett. 2009. V. 9. P. 1433.
Beams R., Cancado L.G., Novotny L. // Nano Lett. 2011. V. 11. P. 1177.
Cancado L.G., Pimenta M.A., Neves B.R.A. et al. // Phys. Rev. Lett. 2004. V. 93. P. 247401.
Diez-Betriu X., Alvarez-Garsia S., Botas C. et al. // J. Mater. Chem. C 2013. V. LP. 6905.
Kudin K.N., Ozbas B., Schniepp H.C. et al. // NanoLetters. 2008. V. 8. P. 36.
Александров Г.Н., Смагулова С.А., Капитонов А.Н. и др. // Российские нанотехнологии. 2014. Т. 9. С. 18.
Lucchese M.M., Stavale F., Ferreira E.H.M. et al. // Carbon. 2010. V. 48. P. 1592.
Yang K., Hи K., Wang Y., Yu T. // Carbon. 2013. V. 52. P. 528.
Дополнительные материалы отсутствуют.
Инструменты
Физикохимия поверхности и защита материалов