Физикохимия поверхности и защита материалов, 2020, T. 56, № 5, стр. 509-515
Синтез, строение и фотофизические свойства новых 15-краун-5-замещенных порфиринатов галлия(III) и индия(III)
А. Ю. Чернядьев 1, *, А. Ю. Цивадзе 1
1 Институт физической химии и электрохимии им. А.Н. Фрумкина РАН
119991 Москва, Ленинский проспект, 31, Россия
* E-mail: chernyadyev@mail.ru
Поступила в редакцию 19.02.2020
После доработки 02.04.2020
Принята к публикации 09.04.2020
Аннотация
Получены новые мезо-тетра(бензо-15-краун-5)порфинаты индия(III) и галлия(III). Строение комплексов установлено по данным спектральных методов. Проведен сравнительный анализ люминесцентных свойств новых соединений при температуре 298 и 77 К. Установлено, что при температуре 298 К краун-порфиринаты индия(III) и галлия(III) проявляют флуоресцентные свойства, а фосфоресцентное свечение при данной температуре полностью отсутствует у обоих комлексов. При температуре жидкого азота (77 K) оба комплекса обладают как флуоресцентным, так и фосфоресцентным свечением. Полученные соединения могут представлять интерес как люминесцентные сенсоры температуры по соотношению интенсивности переходов флуоресценции и фосфоресценции в диапазоне 77–203 К. Энергетическое положение триплетных уровней молекул краун-порфиринатов индия(III) и галлия(III) указывает на способность новых соединений генерировать синглетный молекулярный кислород. Новые соединения, очевидно, могут представлять интерес и как фотосенсибилизаторы для ФДТ опухолей.
ВВЕДЕНИЕ
Краунзамещенные порфирины представляют интерес как соединения, способные образовывать супрамолекулярные ассоциаты с катионами щелочных и щелочноземельных металлов, катионом аммония [1, 2], а также и с нейтральными молекулами, такими как фуллерены [3]. Супрамолекулярные ассоциаты краун-порфиринов с катионами металлов могут представлять интерес как перспективные соединения для транспорта катионов металлов через клеточную мембрану [4], а ассоциаты краун-порфиринатов металлов c фуллеренами представляют интерес как активные компоненты композиционных фотовольтаических преобразователей [3, 5]. Ранее нами было установлено, что краун-порфиринаты родия(III), палладия(IV) со средним по величине “эффектом тяжелого атома” в полимерной основе (полистирол) обладают свойствами люминесцентных сенсоров температуры по изменению соотношения интенсивности фосфоресцентного и флуоресцентного свечения молекул [6, 7]. Такие композиционные материалы (порфиринат металла в полистироле) можно наносить на поверхность исследуемых обьектов при условии химического сродства полимерной основы по отношению к исследуемой поверхности. Также возможно нанесение молекул порфирината металла без полимерной основы на поверхность пористых материалов (глина) или имеющих сложный рельеф поверхности с углублениями (силикагель), в которых могут разместиться молекулы краун-порфирината металла, которые представляют собой диски диаметром ~2.5 нм. Однако без полимерной основы приходится решать проблему контакта кислорода воздуха с молекулами красителя путем вакуумирования образца или помещения в атмосферу инертного газа. Диапазон измеряемых температур с помощью краун-порфиринатов палладия(IV) и родия(III) в полистироле оказался весьма широким – от 77 до 358 К, что позволяет использовать такие сенсоры в условиях Арктики, а также для анализа температуры микро- и нанообьектов с помощью люминесцентного микроскопа [6, 7]. Определенный интерес представляет анализ люминесцентных свойств менее токсичных и более доступных краун-порфиринатов металлов непереходного ряда, обладающих сопоставимым по величине “эффектом тяжелого атома” по сравнению с катионами Pd4+ и Rh3+. В данной работе нами были получены новые 15-краун-5-замещенные порфиринаты металлов непереходного ряда – индия(III) и галлия(III), установлено строение новых соединений и проведен анализ люминесцентных свойств новых соединений в растворе диметилформамида при 298 К и в полимерной основе (полистирол) в диапазоне температур 77–298 К.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
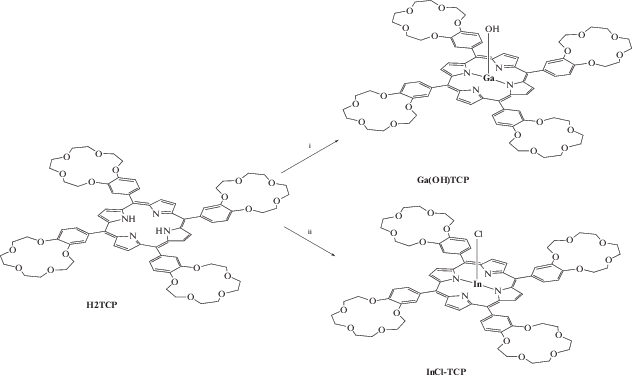
Как известно, порфиринаты галлия(III) можно получить при кипячении свободного основания порфирина и хлорида галлия(III) в диметилформамиде [8], однако реакция осложняется образованием хлорината галлия(III), что снижает выход целевого продукта. Аналогичная проблема возникает при получении порфиринатов индия(III) методом кипячения исходного свободного основания порфирина и хлорида индия(III) в диметилформамиде или феноле [9]. Авторами работ [10, 11] был предложен альтернативный метод получения порфиринатов галлия(III) и порфиринатов индия(III), который не осложнен побочным образованием хлоринов и позволяет получать порфиринаты данных металлов c выходом, близким к количественному. В данном методе в качестве растворителя применяется уксусная кислота, обладающая более низкой темпераутрой кипения по сравнению с диметилформамидом или фенолом, в качестве основания для нейтрализации образующихся в ходе реакции сильных кислот (HCl, H2SO4) применяется ацетат натрия [10, 11]. Для получения 15-краун-5-замещенных порфиринатов галлия(III) и индия(III) нами был применен данный метод с той лишь модификацией, что в качестве растворителя используется смесь диметилформамида с уксусной кислотой, поскольку 15-краун-5-замещенный порфирин (H2TCP) слабо растворим в уксусной кислоте. Модифицированная методика также позволила получить краун-порфиринаты галлия(III) и индия(III) c близким к количественному выходом (схема 1 , эксп. часть).
i) GaCl3 . xH2O, Na+OAc–, HOAc, ДМФ, ∆
ii) InСl3, Na+OAc–, HOAc, ДМФ, ∆
Схема 1 . Синтез 15-краун-5-порфиринатов галлия(III) и индия(III).
Строение поученных порфиринатов галлия(III) и индия(III) было установлено по данным MALDI TOF масс-спектрометрии и ЭСП. В масс-спектре краун-порфирината галлия(III) Ga(OH)TCP наблюдаетсяся основной сигнал, соответствующий катиону GaTCP+, сигнал молекулярного иона Ga(OH)TCP+ и сигнал димера GaTCPP-O-GaTCP+ низкой интенсивности (эксп. часть). Наличие этих сигналов характерно для порфиринатов алюминия(III), галлия(III), содержащих гироксид-анион [8, 9] и хорошо согласуется с предложенным строением полученного соединения (схема 1 ). В масс-спектре InCl-TCP наблюдается только сигнал иона InTCP+, сигналы ионов In(OH)P+ и InTCP-O-InTCP+ в спектре не регистрируются, что косвенно подтверждает наличие хлорид-аниона в составе молекулы комплекса как ацидолиганда. Обработка полученного комплекса 10% водным аммиаком с последующим разбавлением и проведением реакции с нитратом серебра(I) приводит к образованию белого осадка, что прямо подтверждает наличие хлорид-иона в качестве ацидолиганда в составе полученного порфирината индия(III). В ЭСП краун-порфиринатов галлия(III) Ga(OH)TCP и индия(III) InCl-TCP по сравнению с исходным 15-краун-5-замещенным порфирином H2TCP наблюдается батохромный сдвиг полосы Соре (рис. 1, табл. 1) и уменьшение числа Q-полос до двух для порфиринатов металлов по сравнению с четырьмя Q-полосами поглощения у свободного порфирина в силу повышения симметрии молекулы при комплексообразовании [12].
Рис. 1.
Спектры поглощения 15-краун-5-замещенных порфиринатов галлия(III) (а) и индия(III) (б) в диметилформамиде.
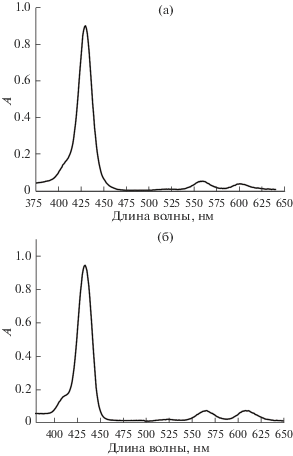
Таблица 1.
Фотофизические характеристики 15-краун-5-замещенных порфиринов в растворе диметилформамида при температуре 298 К
| Соединение | ЭСП, λmax, нм | Спектр флуоресценции, λmax, нм | Квантовый выход флуоресценции, % |
|---|---|---|---|
| H2TCP | 427, 519, 556, 595, 645 | 657, 724 | 14.8 |
| Al(OH)TCP | 431, 560, 603 | 608, 661 | 13.1 |
| Ga(OH)TCP | 430, 558, 601 | 611, 664 | 8.2 |
| InCl-TCP | 435, 565, 609 | 616, 670 | 3.4 |
15-Краун-5-порфиринаты галлия(III) и индия(III) при температуре 298 К в полистироле или в растворе диметилформамида обладают только флуоресцентным типом свечения (рис. 2). В спектрах флуоресценции наблюдаются два перехода эмиссии, близко соответствующие правилу зеркальной симметрии по отношению к Q-полосам поглощения Ga(OH)TCP и InCl-TCP (рис. 1). Квантовый выход флуоресценции уменьшается с ростом заряда ядра катиона металла в ряду Al(OH)TCP-Ga(OH)TCP-InCl-TCP (табл. 1), что хорошо согласуется с ростом “эффекта тяжелого атома” в ряду катионов Al3+, Ga3+, In3+, который согласно теории обмена энергией между триплетными и синглетными электронными уровнями молекул с ростом заряда ядра катиона металла должен приводить к уменьшению квантового выхода флуоресценции за счет увеличения вероятности переходов интеркомбинационной конверсии [13–15].
Рис. 2.
Спектры флуоресценции 15-краун-5-замещенных порфиринатов галлия(III) (а) и индия(III) (б) в диметилформамиде при температуре 298 К.
Интересно отметить, что 15-краун-5-порфиринаты галлия(III) и индия(III) в полистироле не обладают фосфоресцентным свечением при температуре 298 К. Переходы фосфоресценции для этих соединений становятся заметными лишь при охлаждении образцов ниже 203 К. При охлаждении образцов до температуры жидкого азота (77 К) интенсивность переходов фосфоресценции Ga(OH)TCP и InCl-TCP становится сопоставимой с интенсивностью переходов флуоресценции (рис. 3). Характер изменений интенсивности фосфоресценции при изменении температуры 15-краун-5-порфиринатов галлия(III) и индия(III) резко отличается от свойств фосфоресцентного свечения полученных нами ранее 15-краун-5-порфиринатов родия(III) [7] и палладия(IV) [6], которые обладают фосфоресцентными свойствами в полистироле как при 77 К, так и при 298 К. При этом эффект тяжелого атома катионов In3+, Rh3+, Pd4+ весьма близок в силу близких значений заряда ядра этих катионов. Отсутствие фосфоресцентного свечения у 15-краун-5-порфиринатов галлия(III) и индия(III) в полистироле при температуре выше 203 К может обьясняться относительно слабым связыванием катиона металла непереходного ряда (Ga3+, In3+) с порфириновым циклом, что может приводить к значительному вкладу колебательной безызлучательной релаксации возбужденных триплетных уровней при повышении температуры, в то время как катионы переходных металлов (Rh3+, Pd4+) могут образовывать прочные связи с порфириновым лигандом с участием d-электронов катиона металла, что уменьшает вероятность колебательной безызлучательной деградации уровня T1 (схема 2 ) молекул порфиринатов платиновых металлов и тем самым способствует реализации излучательных переходов фосфоресценции при высоких температурах [16, 17]. Краун-порфиринаты галлия(III) и индия(III) Ga(OH)TCP и InCl-TCP, очевидно, могут применяться как сенсоры температуры по соотношению интенсивности переходов фосфоресценции и флуоресценции, однако лишь при низких температурах в отличие от 15-краун-5-порфиринатов родия(III) и палладия(IV), для которых диапазон измеряемых температур составляет 77–358 К [6, 7].
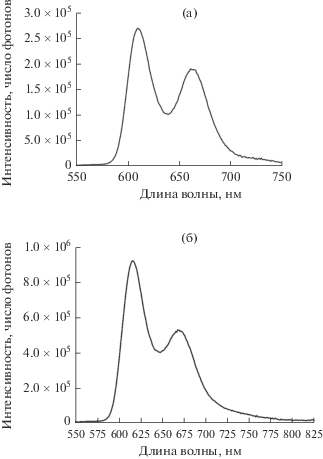
Рис. 3.
Переходы флуоресценции (560–720 нм) и фосфоресценции (720–850 нм) 15-краун-5-замещенных порфиринатов галлия(III) (а) и индия(III) (б) в полистироле при температуре 77 К.

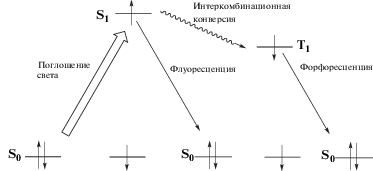
Схема 2 . Электронные переходы поглощения, интеркомбинационной конверсии, флуоресценции и фосфоресценции в молекулах Ga(OH)TCP и InCl-TCP.
Комплексы Ga(OH)TCP и InCl-TCP могут представлять интерес и как фотосенсибилизаторы генерации синглетного молекулярного кислорода из “обычного” триплетного кислорода воздуха, поскольку триплетные уровни (схема 2 ) порфиринатов индия(III) и галлия(III) лежат выше по энергии (787 нм для InCl-TCP, 753 нм для Ga(OH)TCP, рис. 3), чем триплет-синглетный переход молекулы кислорода при ~1250 нм [18], то есть соблюдается необходимое энергетическое условие для генерации синглетного кислорода молекулой фотосенсибилизатора. Другое условие, связанное с достаточно высоким временем жизни триплетного состояния молекул фотосенсибилизатора, очевидно, тоже выполняется для данных соединений, так как катионы индия(III) и галлия(III) обладают средним эффектом тяжелого атома [13, 19], за счет чего молекула фотосенсибилизатора достаточно долго находится в возбужденном триплетном состоянии, чтобы произошло взаимодействие с молекулой триплетного кислорода.
Третье условие применимости фотосенсибилизатора в ФДТ опухолей, связанное с “попаданием” спектра поглощения фотосенсибилизатора в фототерапевтическое окно (красный и ближний ИК-диапазон световых волн) для Ga(OH)TCP и InCl-TCP также выполняется, поскольку оба соединения имеют полосу поглощения в диапазоне 600–650 нм. Активность соединений Ga(OH)TCP и InCl-TCP как фотосенсибилизаторов генерации синглетного кислорода подтверждается наблюдением характерного спектра люминесценции триплетного кислорода [18] при фотовозбуждении 10–4 М растворов Ga(OH)TCP и InCl-TCP в хлороформе (рис. 4). При продувке образцов азотом данное свечение исчезает и появляется вновь при последующей продувке воздухом, что дополнительно подтверждает принадлежность данного спектра люминесценции молекулам синглетного кислорода. Очевидно, что новые 15-краун-5-порфиринаты галлия(III) и индия(III) могут представлять интерес как фотосенсибилизаторы генерации синглетного молекулярного кислорода для ФДТ онкологоческих заболеваний, а также для деструкции инфицированных вирусом клеток или очагов бактериальной инфекции.
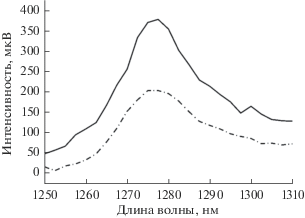
Рис. 4.
Спектры люминесценции синглетного кислорода, зарегистрированные при возбуждении светом с длиной волны 605 нм 10–4 М растворов Ga(OH)TCP (кривая сверху) и InCl-TCP (кривая снизу) в хлороформе.
Работа выполнялась в рамках госзадания по теме госзадания “Физикохимия функциональных материалов на основе архитектурных ансамблей металл-оксидных наноструктур, многослойных наночастиц и пленочных нанокомпозитов”. Регистрационный номер НИОКТР АААА-А19-119031490082-6, а также при поддержке Программы фундаментальных научных исследований Президиума Российской академии наук № 14 “Актуальные проблемы физикохимии поверхности и создания новых композитных материалов”, проект “Новые наноразмерные люминесцентные сенсоры температуры на основе порфиринатов металлов”.
Список литературы
Цивадзе А.Ю. // Успехи химии. 2004. Т. 73. № 1. С. 6–26.
Thanabal V., Krishnan V. // Inorg. Chem. 1982. V. 21. P. 3606.
D’Souza F., Chitta R., Gadde S., Zandler M. // J. Phys. Chem. A. 2006. V. 110. P. 4338.
Thanabal V., Krishnan V. // J. Amer. Chem. Soc. 1982. V. 104. P. 3643.
Цивадзе А.Ю., Чернядьев А.Ю., Ванников А.В. // патент RU 2469440, дата публикации 10.12.2012.
Чернядьев А.Ю., Котенев В.А., Цивадзе А.Ю. // Физикохимия поверхности и защита материалов. 2015. Т. 51. № 6. С. 609.
Чернядьев А.Ю., Котенев В.А., Цивадзе А.Ю. // Физикохимия поверхности и защита материалов. 2019. Т. 55. № 6. С. 635.
Чернядьев А.Ю., Цивадзе А.Ю. // Физикохимия поверхности и защита материалов. 2018. Т. 54. № 6. С. 1086.
Стужина О.В., Ломова Т.Н. // Журн. физ. химии. 2008. Т. 82. С. 216.
Bhatti M., Bhatti W. // Inorg. Nucl. Chem. Lett. 1972. V. 8. P. 133.
Kadish K.M., Cornillon J.L. // Inorg. Chem. 1987. V. 26. P. 4167.
Аскаров К.А., Березин Б.Д., Евстигнеева Р.П. и др. Порфирины: структура, свойства, синтез. М.: Наука, 1985. 333 с.
Соловьев К.Н., Борисевич Е.А. // Успехи физических наук. 2005. Т. 175. № 3. С. 247.
Ельяшевич М.А. Атомная и молекулярная спектроскопия. М.: Физматгиз, 1962.
Ermolaev V.L., Sveshnikova E.B. // Acta Phys. Pol. 1968. V. 34. P. 771.
Лакович Дж. Основы флуоресцентной спектроскопии. М.: Мир, 1986. 496 с.
Чернядьев А.Ю., Логачева Н.М., Цивадзе А.Ю. // Журн. неорг. хим. 2005. Т. 50. № 4. С. 615.
Krasnovsky A.A. // J. Photochemistry and Photobiology A: Chemistry, 2018. V. 354. P. 11.
Harriman A. // J. Chem. Soc., Faraday Trans. 2. 1981. V. 77. P. 1281.
Гордон А., Форд Р. Спутник химика. М.: Мир, 1976. 541 с.
Дополнительные материалы отсутствуют.
Инструменты
Физикохимия поверхности и защита материалов