Физикохимия поверхности и защита материалов, 2020, T. 56, № 5, стр. 463-466
Теория объемного заполнения микропор при температурах выше критических для адсорбтивов
А. М. Толмачев 1, *, Т. А. Кузнецова 1, П. Е. Фоменков 1, М. Р. Гумеров 1
1 Московский государственный университет имени М.В. Ломоносова, Химический факультет
119991 Москва, ГСП-1, Ленинские горы, д. 1, стр. 3, Россия
* E-mail: amtolmach@yandex.ru
Поступила в редакцию 24.10.2019
После доработки 27.11.2019
Принята к публикации 04.12.2019
Аннотация
На основании численного эксперимента доказано, что теория объемного заполнения микропор может быть распространена на анализ адсорбционных равновесий при сверхкритических температурах. Уточнены температурные зависимости основных параметров теории.
ВВЕДЕНИЕ
Теория объемного заполнения микропор (ТОЗМ) [1], признанная и широко используемая во всем мире, была развита М.М. Дубининым и сотр. во второй половине XIX века для описания и анализа адсорбции паров на микропористых адсорбентах.
М.М. Дубинин стремился распространить ТОЗМ на область температур выше критических для адсорбтивов, но экспериментальных данных для перехода от стандартных состояний, используемых при Т < Ткр (предельная адсорбция a0(T) и давление насыщенного пара адсорбтива Рs(T)) к стандартным состояниям при Т > Ткр, не было.
Только в последние годы молекулярно-динамические расчеты адсорбционных равновесий при переходе к температурам выше критических позволили решить эту важную термодинамическую проблему.
ПОЛУЧЕННЫЕ РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
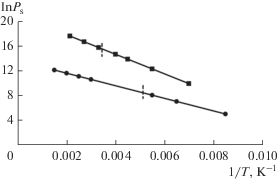
В наших работах [2, 3] при использовании численного эксперимента было доказано, что при температурах выше критической для адсорбтивов логарифм стандартного давления (lnP*(Т)), равновесный с предельной адсорбцией a0(T), линейно зависит от 1/Т и эта зависимость является продолжением аналогичной зависимости при температурах ниже критической для адсорбтива, как показано на рис. 1.
Рис. 1.
Зависимости lnPs (Р*) от обратной температуры для метана (◼) и ксенона (⚫) при температурах ниже и выше критических. Пунктиром обозначены Ткр.
Этот результат позволяет распространить уравнения ТОЗМ (а также уравнения решеточной модели [4, 5], стехиометрической теории адсорбции (СТА) [6] и т.п.), полученных ранее для температур, ниже критических, на описание абсолютных изотерм адсорбции газов, что очень важно для современных адсорбционных технологий, поскольку параметры этих уравнений являются весьма информативными характеристиками соответствующих адсорбционных систем.
Соответствующие уравнения: Дубинина–Радушкевича (активные угли) (1) и Дубинина–Астахова (цеолиты) (2) представлены ниже:
(2)
$\ln a = \ln {{a}_{0}} - {{\left( {\frac{{RT}}{{{{E}_{0}}}}} \right)}^{3}}{{\ln }^{3}}\frac{{P{\kern 1pt} {\text{*}}(T)}}{P}.$В уравнениях (1), (2) и далее: а, a0 – равновесные при давлении Р и “предельная” при стандартном давлении пара Рs при Т < Ткр и (Р*) при Т > Ткр адсорбция (моль кг–1); Е0 (кДж моль–1) – характеристическая энергия адсорбции.
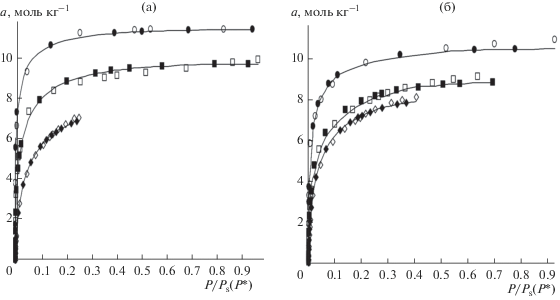
В качестве примера на рис. 2а, 2б приведены экспериментальные изотермы ксенона и их описание уравнениями (1) и решеточной модели в широком интервале температур ниже и выше критической для ксенона (Ткр = 289.6 К).
Рис. 2.
Экспериментальные (сплошные кривые) и рассчитанные по уравнениям (1) (⚫, ◼, ◆) и решеточной модели (⚪, ⬜, ◇) изотермы адсорбции (а (моль кг–1) = f(Р/Рs(Р*)) ксенона при температурах (а): 177.7 (⚫, ⚪), 273.1 (◼, ⬜), 393 (◼, ⬜) и (б): 216.2 (⚫, ⚪), 313 (◼, ⬜), 353 К (◆, ◇).
Обработка большого количества изотерм в широком интервале температур и давлений позволила уточнить некоторые положения ТОЗМ.
Для расчетов по уравнениям (ТОЗМ) (1), (2) при высоких давлениях изначально предполагалась необходимость использования летучестей. Проверка, проведенная нами в широком интервале изменения температур больших критических и соответствующих достаточно больших давлений, показала, что в использовании летучестей нет необходимости, поскольку уравнения ТОЗМ получены без использования метода активностей (летучестей) для расчета зависимостей концентраций (а не активностей) адсорбата (а, моль кг–1) от равновесного давления. Как видно из данных табл. 1 значения а0 для азота и кислорода при расчетах с использованием относительных летучестей (f/fст) начинают расти с температурой при температурах больших критических, в то время как при расчетах с относительными давлениями (Р/Р*) а0 закономерно уменьшаются и совпадают со значениями, рассчитанными по уравнениям решеточной модели ($а_{0}^{*}$).
Таблица 1.
Зависимости а0 от температуры для адсорбции азота и кислорода на активном угле АУК при расчетах по уравнению (1) с использованием относительных летучестей и давлений
| Т, К | Азот | Кислород | ||||
|---|---|---|---|---|---|---|
| а0(f) | а0(Р) | $a_{0}^{*}$ | а0(f) | а0(Р) | $a_{0}^{*}$ | |
| 177.7 | 11.3 | 12 | 12 | 12.5 | 13.5 | 13.4 |
| 216.2 | 10.8 | 11.0 | 11.0 | 11.1 | 12.2 | 12.0 |
| 243 | 11.4 | 11.0 | 10.8 | 10.7 | 11.6 | 11.2 |
| 273.1 | 11.9 | 10.6 | 10.6 | 11.1 | 11.1 | 10.5 |
| 313 | 12.5 | 10.5 | 10.5 | 11.2 | 10.3 | 9.9 |
| 353 | – | 10.4 | 10.3 | – | 10.0 | 9.5 |
| 393 | – | 10.3 | 10.1 | – | 9.7 | 9.3 |
На основании этих данных все дальнейшие расчеты по уравнениям (1), (2) следует проводить с использованием относительных давлений, что значительно упрощает их использование.
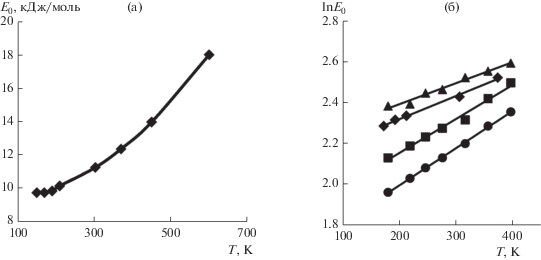
Данные, приведенные в табл. 2 и на рис. 3а, 3б, показывают, что температурная инвариантность (постоянство Е0) приближенно выполняется только в ограниченном интервале температур меньших критических, а при более высоких температурах характеристическая энергия экспоненциально возрастет с увеличением температуры.
Таблица 2.
Зависимость характеристической энергии от температуры при адсорбции метана на активном угле БАУ-10
| Т (К) | а0 (1) | Е0 |
|---|---|---|
| Метан | ||
| 150 | 11.3 | 10.0 |
| 170 | 10.9 | 9.8 |
| 190 | 10.7 | 10.1 |
| 210 | 9.9 | 10.3 |
| 303 | 8.4 | 11.3 |
| 370 | 7.6 | 12.4 |
| 450 | 7.3 | 13.2 |
Рис. 3.
(а) Зависимость характеристической энергии адсорбции метана от температуры на активном угле ПАУ-10; (б) Зависимость lnE0 от температуры для адсорбции метана (◆), криптона (◼), ксенона (▲) и кислорода (⚫) на активном угле АУК.
В этой связи все закономерности, установленные в ТОЗМ (связь Еi0 через парахоры, связь ширины щели в активных углях и Е0, бензола), выполняются только при Т < Ткр.
Отметим, что, как было показано нами [2, 3], в соответствии с уравнением Дубинина–Николаева [7] $\ln {{a}_{0}}$ является линейной функцией температуры в широком интервале температур ниже и выше критических для адсорбтивов
что подтверждает корректность выбора Р*. Заметим дополнительно, что использование Р* в уравнениях решеточной модели также подтверждает корректность его расчета [5, 6].Таким образом, как и мечтал М.М. Дубинин, ТОЗМ в результате последних разработок может быть применена и при обработке данных по адсорбции газов в широком интервале изменения температур и давлений.
Отметим в заключение, что распространение ТОЗМ на сверхкритические температуры означает возможность соответствующих переходов во всех уравнениях и теориях, основанных на использовании в качестве “стандартного давления” – давления насыщенных паров адсорбтивов (уравнения, полученные в рамках решеточных моделей, стехиометрическая теория адсорбции и т.п.). Так, например, в компьютерном банке данных, разработанном и поддерживаемом нами [8], соответствующие данные обрабатываются с учетом этой возможности.
Список литературы
Dubinin M.M. // Progress in surface and membrane Sci. New York:Acad. Press. 1975. V. 9. P. 1.
Фоменков П.Е., Гумеров М.Р., Толмачев А.М. // Физикохимия поверхности и защита материалов. 2018. Т. 54. № 4. С. 374.
Толмачев А.М., Кузнецова Т.А., Крюченкова Н.Г., Фоменков П.Е. // Физикохимия поверхности и защита материалов. 2015. Т. 51. № 4. С. 339.
Толмачев А.М., Годовиков И.А., Кузнецова Т.А. // Физикохимия поверхности и защита материалов. 2012. Т. 48. № 2. С. 145.
Толмачев А.М., Фирсов Д.А., Крюченкова Н.Г., Кузнецова Т.А. // Физикохимия поверхности и защита материалов. 2019. Т. 55. № 3. С. 234.
Toлмaчeв A.M. // Lanqmuir. 1991. № 7. P. 1400.
Николаев К.М., Дубинин М.М. // Изв. АНСССР. Отд. хим. наук. 1958. С. 65.
Толмачев А.М., Годовиков И.А., Кузнецова Т.А., Крюченкова Н.Г., Фирсов Д.А. // http://www.adsbank.chem.msu.ru.
Дополнительные материалы отсутствуют.
Инструменты
Физикохимия поверхности и защита материалов


