Физикохимия поверхности и защита материалов, 2021, T. 57, № 1, стр. 41-49
Выявление закономерностей сорбционного связывания ионов кадмия пектиновыми веществами из водных растворов
С. В. Алеева 1, *, О. В. Лепилова 1, С. А. Кокшаров 1
1 Федеральное государственное бюджетное учреждение науки Институт химии растворов им. Г.А. Крестова Российской академии наук
153045 Иваново, ул. Академическая, 1, Россия
* E-mail: sva@isc-ras.ru
Поступила в редакцию 12.12.2019
После доработки 10.09.2020
Принята к публикации 17.09.2020
Аннотация
Методом ИК-спектроскопии полимерных пленок оценено комплексное влияние сорбции ионов кадмия на состояние пектиновых веществ по изменению полос поглощения, формируемых валентными колебаниями связи С–О карбоксильных групп пектатов, а также деформационными колебаниями связи О–Н вторичных гидроксилов и валентными колебаниями карбонила в сложноэфирных группах. Проведен анализ изотерм адсорбции Cd2+ при 293–308 К. Для образцов пектина, выделенных из биомассы лопуха Arctium lappa L., ревеня Rheum и цитрусовых культур, а также для модельных субстратов пектината, пектата и пектовой кислоты на их основе получено адекватное описание сорбционного процесса с помощью модели сорбции Ленгмюра. Определены термодинамические параметры адсорбции, которые количественно характеризуют связывание кадмия по механизмам ионного обмена с группами –СООН, катионного замещения с группами –СООСа1/2 и координационных взаимодействий с участием спиртовых гидроксилов и карбонильного кислорода метоксилированных галактуронатных звеньев.
ВВЕДЕНИЕ
Решение проблем экологии неразрывно связано с необходимостью сокращения объемов сточных вод, загрязненных различными химическими токсикантами, включая соли тяжелых металлов. Одним из высокотоксичных металлов, содержащихся в водных стоках, является кадмий, который наряду с мышьяком, свинцом, ртутью отнесен к 1 классу опасности. Согласно СанПин 2.1.4.1074-01 предельно допустимая концентрация кадмия в воде хозяйственно-питьевого и культурно-бытового водопользования составляет 0.001 мг/дм3. Наиболее интенсивными источниками загрязнения окружающей среды кадмием являются металлургия, гальванотехника, лакокрасочные производства. Повышенный уровень антропогенного загрязнения окружающей среды ионами Cd2+ отмечается для процессов сжигания твердого и жидкого топлива.
С 2010 по 2016 г. сброс загрязненных стоков в России снижен с 16.5 до 14.7 млрд м3. Однако их доля в общем объеме водоотведения составляет примерно 1/3 [1]. Более 75% в указанных объемах составляют промышленные стоки с недостаточной степенью очистки. Их количество в течение указанного периода также сокращено с 13.1 до 11.3 млрд м3, но темпы снижения недостаточны. Для ускоренного развития водоочистных технологий существенное значение имеет совершенствование сорбционных методов, в том числе с применением биополимерных сорбентов [2, 3].
В числе достоинств природных сорбентов отмечают доступность, дешевизну, простоту изготовления, применения и утилизации, а среди ограничительных факторов – недостаточную селективность и невысокую сорбционную емкость [4]. Часто адсорбционные свойства растительных материалов рассматривают лишь в отношении к основному полимерному компоненту – целлюлозе – с поиском методов ее целенаправленной модификации [5, 6]. В частности считают [7], что связывание ионов металлов обеспечивают карбоксильные группы, которые в целлюлозе могут присутствовать при 1, 2, 3 и 6 атомах углерода пиранозного цикла:
В природной целлюлозе СООН-группы практически отсутствуют и могут появляться в результате химической обработки растительного сырья для очистки целлюлозы от примесей. Использование окислительной деструкции целлюлозы может быть оправдано, например, для модификации хлопковых волокон [8], содержащих 95–98% целлюлозы. Для многих видов растительного сырья сорбционные свойства обусловлены присутствием нецеллюлозных полисахаридов [9, 10]. Например, повышенный уровень карбоксильной кислотности биомассы стебля топинамбура (0.82 мг-экв/г) [7] обусловлен присутствием в субстрате 8–10 мас. % полиуронидных соединений.
Комплексообразующую способность пектинов преимущественно связывают с участием во взаимодействиях галактуронатных звеньев с незамещенной карбоксильной группой. В модельных исследованиях часто применяют пектовые кислоты, состоящие в основном из деметоксилированной полигалактуроновой кислоты. Этерификация карбоксилов понижает реакционную способность биополимера. В частности, высокометоксилированные пектины связывают ионы Pb2+ в 1.7 слабее, особенно в кислой среде [11].
Часть галактуронатных звеньев в растительных пектинах присутствует в виде кальциевой соли. Ионы Са2+ образуют межцепные связи, обеспечивая поперечную сшивку макромолекул пектина [12, 13]. Это не исключает возможность участия кальций-пектатных форм в сорбционном связывании неорганических поллютантов в связи с легкостью протекания замены Са2+ на ионы тяжелых d- и f-металлов. По уровню проявляемого сродства к пектовой кислоте ионы располагаются в возрастающей последовательности: К+ < Mg2+ < < Ca2+ < Ni2+ < Pb2+ < Co2+ < Zn2+ < Cu2+ < Mn2+. При этом по величине сродства к низкометоксилированному пектину ионы кадмия превышают показатель для ионов свинца: 0.051 и 0.017 ммоль/г соответственно [14].
Настоящая работа продолжает изучение связи между сорбционными свойствами и характеристиками молекулярного строения пектинов. Ранее на примере препаратов растительного пектина и модельных субстратов на их основе выявлены закономерности изменения кинетических характеристик и адсорбционной емкости по кальцию [15]. Показано, что вклад в суммарную сорбционную емкость незамещенного галактуронатного звена превышает активность кальций-пектатных форм и метилгалактуронатных звеньев в 10 и 13 раз соответственно. Предполагается, что различия отражают участие в сорбционном процессе рассматриваемых структурных фрагментов по механизмам ионного обмена, катионного замещения и координационного связывания.
В развитие применяемых подходов к получению пектиновых субстратов с целенаправленным изменением состояния карбоксильных групп и выявлением отклика в изменении их сорбционной активности проведена оценка закономерностей влияния химического строения полиуронидов на проявление сорбционных свойств в отношении растворов солей кадмия. Результаты позволят расширить представления о природе и механизмах протекания взаимодействий и методах управления системой для максимального использования ресурсов, которыми обладают биополимерные растительные материалы с разнообразным сочетанием адсорбционных центров.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
В работе применены коммерческий препарат цитрусового пектина PC (производитель Yantai Andre Pectin, Китай), а также пектины лопуха Arctium lappa L. (PAL) и ревеня Rheum (PR), выделение и идентификация которых проведена в соответствии с описанием в работе [15].
В качестве дополнительных модельных сорбентов использованы препараты пектинатов, пектатов и пектовой кислоты, которые применяются для количественной оценки долевого содержания в пектине галактуронатных звеньев с незамещенной карбоксильной группой (unsubstituted group, Gug), а также в метилгалактуронатной (methylgalacturonate group, Gmg) и кальций-пектатной (calcium pectate, Gcp) формах. Получение модельных сорбентов и анализ карбоксильных групп в полимерах осуществлены в соответствии с рекомендациями [16]. Параметры молекулярного строения исследуемых субстратов представлены в табл. 1. Содержание форм галактуронатных звеньев выражено в долевом соотношении к их общему количеству, принимаемому за единицу.
Таблица 1.
Параметры химического строения сравниваемых образцов пектина и модельных препаратов на их основе
| Образец пектина |
Долевое соотношение форм галактуронатных звеньев в субстратах | ||||||
|---|---|---|---|---|---|---|---|
| пектин | пектинат | пектовая кислота | пектат | ||||
| Gug | Gmg | Gсp | Gmg | Gсp | Gug | Gсp | |
| PAL | 0.30 | 0.46 | 0.24 | 0.46 | 0.54 | 1 | 1 |
| PR | 0.28 | 0.53 | 0.19 | 0.53 | 0.47 | 1 | 1 |
| PC | 0.15 | 0.68 | 0.17 | 0.68 | 0.32 | 1 | 1 |
Для исследования изменения состояния пектинов при сорбции ионов кадмия использован метод ИК-спектроскопии полимерных пленок. Анализ образцов проведен на спектрофотометре AVATAR-360 в режиме на пропускание в области частот 400–2000 см–1. Выделение пектиновых веществ из исходной суспензии и после ее обработки в растворе сульфата кадмия осуществляли путем осаждения полимера 96%-ным этанолом. Отделяемый пектиновый коагулят промывали 70 и 96%-ным этанолом и сушили при 303 K. Для получения пленок 10 мл водного раствора пектина с концентрацией 6 г/л выливали на шаблон из фторопласта площадью 60 cм2 и высушивали на воздухе. Поверхностная плотность получаемых пленок составляла 1.0 ± 0.1 мг/см2.
Для нивелирования колебания толщины пленки испытуемых образцов при анализе спектрограмм использован прием оценки изменения интенсивности характеристических полос поглощения в относительном выражении к полосе внутреннего стандарта. В качестве внутреннего стандарта выбрана полоса валентных колебаний связей С–С и С–О в пиранозном цикле νas(С–С) = 1020 см–1, характеризующая содержание мономерных звеньев.
Показатель относительной оптической плотности dDi для адсорбционных центров в исследуемых образцах с учетом внутреннего стандарта рассчитывали по формуле:
где D1020 – оптическая плотность полосы внутреннего стандарта.Величину оптической плотности D в максимуме полосы внутреннего стандарта и i-той полосы колебаний для соответствующих функциональных групп, участвующих в адсорбционном процессе, определяли из соотношения:
где I0, I – интенсивность соответственно падающего и прошедшего света.Величину I0 определяли с использованием приема построения базисной линии, позволяющей учесть различия толщины анализируемых пленок и изменений величины фона, обусловленных дефектами их поверхности. Базисную линию строили через минимумы поглощения при 1850 и 860 см–1, полностью охватывая зону измерений.
Для получения изотерм сорбции проведены серии экспериментов с варьированием начальной концентрации Cd2+ в рабочем растворе сульфата кадмия (квалификация “х. ч.”) в интервале 1–50 ммоль/л при фиксированном значении рН 4.5 с термостатированием в интервале 293–308 K. Остаточное содержание Cd2+ в растворе определяли методом атомно-адсорбционной спектроскопии на спектрофотометре AAS-3 по ГОСТ 24596.11-2015. По кинетике взаимодействия Cd2+ и пектина установлена продолжительность выхода системы на сорбционное равновесие – 1 час. По истечение необходимого времени сорбент отделяли центрифугированием и определяли равновесную концентрацию ионов кадмия в супернатанте. Равновесную сорбционную емкость пектиновых субстратов (А, ммоль/г) вычисляли по формуле:
(3)
$А = {{V({{C}_{0}} - {{С}_{P}})} \mathord{\left/ {\vphantom {{V({{C}_{0}} - {{С}_{P}})} m}} \right. \kern-0em} m},$Обработка изотерм поглощения Cd2+ образцами пектиновых сорбентов для описания молекулярной адсорбции на полимерах осуществлена с применением модели Ленгмюра. Уравнение изотермы Ленгмюра имеет следующий вид:
(4)
$А = {{{{A}_{m}}{{K}_{L}}{{C}_{P}}} \mathord{\left/ {\vphantom {{{{A}_{m}}{{K}_{L}}{{C}_{P}}} {\left( {1 + {{K}_{L}}{{C}_{P}}} \right),}}} \right. \kern-0em} {\left( {1 + {{K}_{L}}{{C}_{P}}} \right),}} $Для определения параметров Аm и KL использовали линейную форму уравнения (4):
(5)
${{{{С}_{P}}} \mathord{\left/ {\vphantom {{{{С}_{P}}} A}} \right. \kern-0em} A} = {{\left( {{{K}_{L}}{{A}_{m}}} \right)}^{{ - 1}}} + {{{{C}_{P}}} \mathord{\left/ {\vphantom {{{{C}_{P}}} {{{A}_{m}}}}} \right. \kern-0em} {{{A}_{m}}}}.$Представление экспериментальных данных в координатах СР/А = f(CР) линейного уравнения (5) позволяет графически определить значения Аm и KL соответственно по тангенсу угла наклона и свободному члену линейной зависимости.
Из величины константы KL определяли параметры коэффициента распределения ионов металла между фазой раствора и фазой полимерного материала KD:
Сопоставление термодинамических параметров сорбции проведено по показателям свободной энергии Гиббса (ΔG, кДж/моль), внутренней энергии (ΔH, кДж/моль) и энтропии адсорбции (ΔS, Дж/K моль). Расчеты выполнены в соответствии с фундаментальным уравнением термодинамики:
где R – универсальная газовая постоянная (R = = 8.314 Дж/K моль); T – температура, K.Предполагая, что ΔH в узком исследованном интервале температур не зависит от температуры, уравнение (7) можно представить в интегральном виде:
(8)
$\ln {{K}_{D}} = - {{\Delta H} \mathord{\left/ {\vphantom {{\Delta H} {RT}}} \right. \kern-0em} {RT}} + {\text{const}}{\text{.}}$Тепловой эффект сорбции определяли графически из уравнения прямой линии в координатах Аррениуса lnKD = f(1/T).
ΔS рассчитывали из уравнения термодинамики (7).
Математическая обработка экспериментальных данных проведена с использованием программы Statgraphics PLUS 2000 Professional.
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
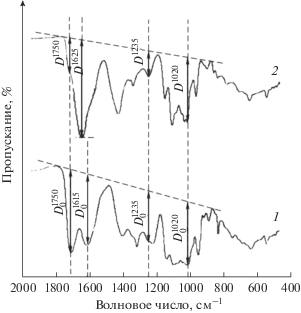
Оценка изменения ИК-спектров пектиновых веществ при сорбционном связывании катионов Cd2+ демонстрирует комплексных характер взаимодействий с участием нескольких реакционных центров полимера. На рис. 1 приведены спектрограммы пленок пектина ревеня PR до и после обработки раствором сульфата кадмия. Выделены пики валентных колебаний, отражающие отклик структурных элементов макромолекулы:
– 1235 см–1 – деформационные колебания связи в спиртовой ОН-группе вторичных гидроксилов галактуронатных звеньев δ(ОН);
– 1610–1625 см–1 – валентные колебания связи С–О карбоксильных групп пектатов с ионами металлов νas(СОО–);
– 1750 см–1 – валентные колебания карбонила в сложноэфирных группах νas(С=О).
Представленные в табл. 2 результаты обработки ИК-спектров демонстрируют однотипные отклики для всей совокупности полимерных субстратов и получаемых адсорбционных комплексов. Основные отклонения зафиксированы для карбоксильных групп, обеспечивающих ковалентное связывание катионов кадмия. Полоса валентных колебаний связи С–О после сорбции Сd2+ смещается в сторону увеличения волнового числа с 1615 до 1625 см–1 и возрастает по амплитуде. Для комплекса Cd-РR величина относительной оптической плотности dD1625 в 2.2 раза превышает значение dD1615 для исходного образца РR. При переходе к соответствующим пикам для образцов на основе РC и РAL прирост относительной оптической плотности составляет 1.9 и 2.4 раза. Усиление эффекта согласуется с потенциальной способностью препаратов к связыванию металла не только за счет перевода незамещенной формы галактуронатных звеньев в пектат кадмия, но и замещения катиона в кальций-пектатных фрагментах (см. табл. 1).
Таблица 2.
Изменение характеристических полос поглощения ИК-спектров пектиновых веществ при адсорбционном связывании ионов кадмия
| Образец | Оптическая плотность | Относительная оптическая плотность | |||||||
|---|---|---|---|---|---|---|---|---|---|
| D1020 | D1615 | D1625 | D1235 | D1750 | dD1615 | dD1625 | dD1235 | dD1750 | |
| PAL | 0.468 | 0.355 | 0.271 | 0.459 | 0.76 | 0.58 | 0.98 | ||
| Cd-PAL | 0.512 | 0.855 | 0.148 | 0.149 | 1.67 | 0.29 | 0.29 | ||
| PR | 0.433 | 0.364 | 0.234 | 0.355 | 0.84 | 0.54 | 0.82 | ||
| Cd-PR | 0.494 | 0.998 | 0.133 | 0.133 | 2.02 | 0.27 | 0.27 | ||
| PС | 0.476 | 0.305 | 0.291 | 0.566 | 0.64 | 0.61 | 1.19 | ||
| Cd-PС | 0.467 | 0.569 | 0.135 | 0.149 | 1.22 | 0.29 | 0.32 | ||
Сорбция кадмия приводит к уменьшению амплитуды полосы деформационных колебаний гидроксильных групп галактуронатного звена. Для всех адсорбционных комплексов получено одинаковое снижение величины dD1235 в 2–2.1 раза, что характеризует равные возможности участия вторичных гидроксилов в координационных взаимодействиях с Cd2+ не зависимо от исходного состояния пектиновых веществ.
Изменение амплитуды пика валентных колебаний связи С=О в сложноэфирных группах позволяет считать карбонильный кислород метоксилированных звеньев активным участником комплексообразования. Снижение величины dD1750 нарастает с 3 раз для комплекса Сd-РAL до 3.4 и 3.7 раза при переходе соответственно к образцам на основе РR и РС. Увеличение эффекта коррелирует с величиной долевого содержания мономерных звеньев Gmg в сопоставляемых образцах пектиновых веществ (см. табл. 1).
На рис. 2 продемонстрирован ход зависимостей равновесной сорбции ионов кадмия от концентрации Cd2+ в термостатируемом растворе для сравниваемых препаратов пектина и модельных субстратов на основе образца РR. Аналогичные исследования проведены для температурного интервала 293–308 К.
Рис. 2.
Изотермы сорбции ионов кадмия сравниваемыми образцами пектина (1–3) и модельными препаратами на основе пектина ревеня (2 *–2 ***) при 303 К: 1 – PR; 2 – PАL; 3 – PС; 2 * – пектовая кислота; 2 ** – пектат; 2 *** – пектинат.
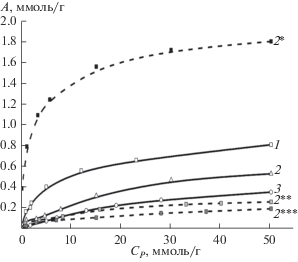
Зависимости, полученные для каждой из исследуемых биополимерных систем, имеют традиционный вид изотермы адсорбции Ленгмюра для случая химического взаимодействия между поглощаемым веществом и частицами адсорбента. Представленные данные отражают характерную для всех условий сорбционного эксперимента тенденцию к нарастанию величины равновесного поглощения в ряду PC < PR < PAL. При этом ход изотермы адсорбции модельным образцом пектовой кислоты многократно превышает уровень значений для базового препарата РR. В свою очередь результаты сорбции модельным субстратом пектата кальция уступают показателям исходного биополимера, но превосходят сорбционную способность пектината.
Аналитическое описание изотерм равновесной адсорбции кадмия на биополимерных материалах осуществлено путем интерпретации результатов в координатах линейного уравнения Ленгмюра СР/А = f(CР). Высокую степень аппроксимации экспериментальных данных отражают значения коэффициентов детерминации R2, указанные в табл. 3.
Таблица 3.
Результаты анализа сорбционной способности исследуемых препаратов пектиновых веществ в отношении ионов кадмия по модели Ленгмюра при 303 K
| Образцы сорбентов | R2 | Аm, ммоль/г | KL, л/ммоль | |
|---|---|---|---|---|
| PC | 0.986 | 0.35 | 0.048 | |
| PAL | 0.996 | 0.84 | 0.196 | |
| PR | 0.983 | 0.54 | 0.065 | |
| Модельные субстраты на основе РR | Пектовая кислота | 0.995 | 1.79 | 0.535 |
| Пектат | 0.995 | 0.26 | 0.125 | |
| Пектинат | 0.986 | 0.19 | 0.088 | |
Применение модели Ленгмюра позволяет охарактеризовать процесс сорбции по двум ключевым показателям: константа адсорбционного равновесия KL и предельная сорбция Аm. Достигаемый уровень Аm отражает количество активных центров в молекулярной цепи полиуронида, которые могут взаимодействовать с Cd2+. Величина константы KL характеризует изменение энергии взаимодействия с сорбентом. С ростом показателя KL увеличивается сродство сорбируемого вещества к адсорбционным центрам биополимера, повышается прочность возникающих связей в системе “сорбент–металл”. Расчетные параметры моделирования равновесных закономерностей адсорбционного процесса для сравниваемых биополимерных материалов даны в табл. 3. Анализ показал, что выбранный вариант зависимости удовлетворяет условиям адекватности, поскольку различие расчетной величины Аm и экспериментальных значений сорбционной емкости сорбентов (см. рис. 2) не превышает 5%.
Нетрудно проследить связь между расчетной величиной предельной сорбции и характеристиками молекулярного строения исследуемых пектинов. Возрастание показателя Аm симбатно увеличению содержания свободных карбоксильных групп и кальций пектатных форм при снижении доли метоксилированных звеньев в цепи полиуронида. Данные для модельных субстратов позволяют сопоставить роль структурных фрагментов макромолекулы как в плане изменений доступности адсорбционных центров, так и проявляемого к ним сродства сорбируемого вещества.
Получаемые в рамках модели Ленгмюра результаты еще не дают представления о механизме взаимодействий в системах. Вместе с тем выявленные значения константы адсорбционного равновесия KL позволяют перейти к термодинамическому описанию процесса и количественно охарактеризовать роль структурных компонентов полимера в суммарном результате реализации различных механизмов хемосорбции.
На рис. 3 приведены температурные зависимости адсорбционного равновесия в координатах Аррениуса для базовых образцов и для модельных субстратов. Интерпретация данных проведена с применением коэффициента распределения ионов металла между фазами раствора и полимерного материала KD, величина которого определена исходя из данных константы KL по уравнению (6). Представленные результаты свидетельствуют о высокой степени аппроксимации расчетных параметров KD всех полимерных сорбентов (R2 > 0.98), что обеспечивает корректное определение основных энергетических составляющих в соответствии с фундаментальными уравнениями термодинамики (7)–(8). Результаты обработки зависимостей представлены в табл. 4.
Рис. 3.
Температурная зависимость адсорбционного равновесия для исследуемых образцов пектинов (a) и для модельных препаратов на основе полиуронида ревеня (б); 1 – PR; 2 – PАL; 3 – PС; 2* – пектовая кислота; 2** – пектат; 2*** – пектинат.
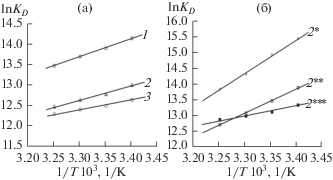
Таблица 4.
Термодинамические параметры сорбции ионов кадмия пектиновыми веществами
| Препараты пектина |
ΔH, кДж/моль |
ΔS, Дж/(К моль) |
ΔG, кДж/моль | |||
|---|---|---|---|---|---|---|
| 293 К | 298 К | 303 К | ||||
| Пектин | PC | –15.01 | 48.39 | –29.19 | –29.43 | –29.67 |
| PR | –22.59 | 26.07 | –30.22 | –30.35 | –30.48 | |
| PAL | –30.95 | 7.14 | –33.04 | –33.07 | –33.11 | |
| Пектовая кислота | PC | –80.67 | –155.81 | –35.28 | –34.57 | –33.94 |
| PR | –79.88 | –153.17 | –35.00 | –34.24 | –33.47 | |
| PAL | –80.27 | –154.49 | –35.17 | –34.40 | –33.83 | |
| Пектат | PC | –54.74 | –72.63 | –33.74 | –33.37 | –32.91 |
| PR | –54.34 | –71.30 | –33.45 | –33.09 | –32.73 | |
| PAL | –54.19 | –70.77 | –33.33 | –32.97 | –32.51 | |
| Пектинат | PC | –10.69 | 50.00 | –25.34 | –25.59 | –25.84 |
| PR | –20.35 | 20.74 | –26.43 | –26.53 | –26.63 | |
| PAL | –24.94 | 14.34 | –28.71 | –28.78 | –28.85 | |
Для всех рассматриваемых субстратов поглощение Cd2+ протекает самопроизвольно (ΔG < 0) и сопровождается выделением тепла (ΔН < 0). Для образцов с однородным составом функциональных группировок – пектовой кислоты и пектата – протекание процесса сорбции более эффективно при низких температурах. При нагревании систем наблюдается уменьшение свободной энергии Гиббса. Максимальная амплитуда различий зафиксирована для варианта сорбции Cd2+ на незамещенных карбоксилах пектовой кислоты. Экзотермический эффект сорбции и достигаемый уровень энтальпии для пектовой кислоты свидетельствуют о протекании хемосорбционных взаимодействий с образованием стабильных хелатных структур; сорбция кадмия практически необратима.
Подобная характеристика применима и для образцов пектата из разных препаратов пектина. Меньший уровень показателей ΔН и ΔG обусловлен более существенными энергозатратами на вытеснение из субстрата ионов кальция.
Отрицательные значения структурной (энтропийной) составляющей сорбции для пектовой кислоты и пектата отражают утрату молекулами адсорбтива при взаимодействии определенного количества степеней свободы, включая способность к перемещению по адсорбирующей поверхности, к вращательным и колебательным движениям. В наибольшей степени этот эффект проявляется при переходе пектовой кислоты в состояние пектата кадмия. В этом случае резко ограничивается сегментальная подвижность и молекул полимера, уменьшается возможное число конформаций пиранозных звеньев. Для кальций-пектатной формы результат ионного замещения выражен в меньшей степени, поскольку в исходном виде она уже обладает высокой степенью упорядоченности.
Для пектина и пектината, являющихся полимерами со смешанным составом функциональных групп, с повышением температуры свободная энергия процесса нарастает. По-видимому, в этом случае определяющий вклад вносят метоксилированные звенья полимерной цепи. Хемосорбция для таких систем менее выражена. Показатель энтальпии снижается при уменьшении содержания формы Gug в сравниваемых препаратах пектина, а также при увеличении содержания формы Gmg, что обусловлено низким уровнем теплового эффекта для случаев образования координационной связи (10–15 кДж/моль).
Характеризуя энтропийный фактор в рассматриваемых системах, следует отметить, что при связывании кадмия пектинами и пектинатами зафиксировано возрастание показателя и переход в область положительных значений (ΔS > 0). По-видимому, это отражает наименьшую стабильность адсорбционного комплекса на основе координационного связывания ионов металла этерифицированными участками полимерной цепи.
Для поиска корреляций между величиной теплоты адсорбции и строением пектиновых субстратов сформирован подход к оценке вклада структурных фрагментов в величину показателя ΔН с помощью многопараметровой зависимости общего вида:
Величину причленных множителей удалось определить путем последовательного усложнения состава рассматриваемых биополимерных систем с учетом данных табл. 1 и 4.
Для группы двухкомпонентных пектинатов на основе пектинов из цитрусового сырья и ревеня вклад метоксилированной и кальций-пектатной форм структурных звеньев отражает система уравнений (10), которая трансформируется в равенство (11):
(10)
$\left\{ \begin{gathered} \Delta {{H}^{{{{P}_{C}}}}} = {{x}_{1}}G_{{mg}}^{{{{P}_{C}}}} + {{x}_{2}}G_{{cp}}^{{{{P}_{C}}}} \hfill \\ \Delta {{H}^{{{{P}_{R}}}}} = {{x}_{1}}G_{{mg}}^{{{{P}_{R}}}} + {{x}_{2}}G_{{cp}}^{{{{P}_{R}}}}, \hfill \\ \end{gathered} \right.$(11)
${{x}_{1}} = \frac{{\Delta {{H}^{{{{P}_{C}}}}} - {{x}_{2}}G_{{ср}}^{{{{P}_{C}}}}}}{{G_{{mg}}^{{Pc}}}} = \frac{{\Delta {{H}^{{{{P}_{R}}}}} - {{x}_{2}}G_{{ср}}^{{{{P}_{R}}}}}}{{G_{{mg}}^{{{{P}_{A}}}}}}.$Выражение (11) позволяет определить величину множителя x2 = –54.87, которая должна быть неизменной для всех видов пектиновых веществ с учетом постоянства значений ΔН в исследуемой группе пектатов (см. табл. 4). Используя значение x2 при решении уравнений системы (10), получаем численные варианты множителя x1 = 10.10 для пектината на основе РС и x1 = 10.32 для пектината на основе РR.
Верификация расчета значений х1 с использованием зависимости для пектината на основе пектина лопуха: $\Delta {{H}^{{{{P}_{{AL}}}}}} = {{x}_{1}}G_{{mg}}^{{{{P}_{{AL}}}}} + {{x}_{2}}G_{{cp}}^{{{{P}_{{AL}}}}}$ − дает численный вариант множителя x1 = 10.56 для пектината на основе РAL. Среднее значение множителя при показателе Gmg в уравнении (9) составляет 10.33 при величине отклонений в дисперсии менее 3%.
Проверка корректности определения множителя х2 проведена с учетом соблюдения зависимости $\Delta H = {{x}_{2}}G_{{cp}}^{{}}$ по результатам сорбции ионов кадмия модельными препаратами пектатов на основе исследуемых образцов пектина. Полученные значения показателя составили –54.74 для пектата РС, –54.34 для пектата РR и –54.19 для пектата РAL. Таким образом, отличия расчетных значений х2 для исследуемой группы пектатов от величины, полученной из системы уравнений (10) для пектинатов не превышают 2.0%.
Решая систему уравнений (12) для сорбции кадмия образцами пектиновых препаратов с учетом средних значений x1 и x2 находим численные варианты множителя х3:
(12)
$\left\{ \begin{gathered} \Delta {{H}^{{{{P}_{С}}}}} = {{x}_{1}}G_{{mg}}^{{{{P}_{С}}}} + {{x}_{2}}G_{{cp}}^{{{{P}_{С}}}} + {{x}_{3}}G_{{ug}}^{{{{P}_{С}}}}\,\,\,\,\,\,\, \Rightarrow {{x}_{3}} = - 84.71 \hfill \\ \Delta {{H}^{{{{P}_{R}}}}} = {{x}_{1}}G_{{mg}}^{{{{P}_{R}}}} + {{x}_{2}}G_{{cp}}^{{{{P}_{R}}}} + {{x}_{3}}G_{{ug}}^{{{{P}_{R}}}}\,\,\,\,\,\,\, \Rightarrow {{x}_{3}} = - 80.03 \hfill \\ \Delta {{H}^{{{{P}_{{AL}}}}}} = {{x}_{1}}G_{{mg}}^{{{{P}_{{AL}}}}} + {{x}_{2}}G_{{cp}}^{{{{P}_{{AL}}}}} + {{x}_{3}}G_{{ug}}^{{{{P}_{{AL}}}}} \Rightarrow {{x}_{3}} = - 82.55. \hfill \\ \end{gathered} \right.$Полученные значения сопоставлены с условиями реализации зависимости $\Delta H = {{x}_{3}}G_{{ug}}^{{}}$ по результатам сорбции Cd2+ модельными препаратами пектовой кислоты. Соответствующие значения показателя х3 составляют –80.67; –79.88 и –80.27 для модельных субстратов на основе РС, РR и РAL. Отклонения результатов от среднего значения х3 = –81.35 не превышают 3%.
ЗАКЛЮЧЕНИЕ
Таким образом, обобщенная математическая модель для описания влияния химического строения пектина на величину теплового эффекта сорбции Cd2+ имеет вид:
Величина причленных множителей отражает уровень тепловых эффектов адсорбции катионов кадмия по механизмам:
– ионного обмена на незамещенных карбоксильных группах (–81.35 кДж/моль);
– катионного замещения на участках галактуронатных звеньев в кальций-пектатной форме (–54.87 кДж/моль);
– координационного связывания с участием адсорбционных центров метилгалактуронатных звеньев (10.33 кДж/моль).
Величина множителя при Gmg отражает протекание взаимодействия по механизму физической сорбции. Примечателен положительный вклад структурных фрагментов Gmg в суммарную величину энтальпии сорбции кадмия многокомпонентными биополимерными материалами. Очевидно, в этом случае процесс сорбции контролируется внутренней диффузией Cd2+ в структуре полимера, которая ускоряется с повышением температуры. Это обстоятельство определяет эндотермический характер связывания ионов металлов на метоксилированных участках полимера, что проявляется в температурной зависимости параметра ΔG для пектинов и пектинатов (см. табл. 4).
Полученная модель адсорбционной активности пектиновых веществ обладает высокой прогностической способностью и позволяет оценить внутреннюю энергию процесса сорбции для любого соотношения форм мономерных галактуронатных звеньев в структуре полимера. Результаты исследований являются обоснованием для развития технологических подходов к повышению сорбционных свойств пектинсодержащих сорбентов, в частности, за счет проведения биокатализируемых процессов деметоксилирования полимера с использованием ферментов пектинэстераза.
Исследования проведены в рамках Государственного задания Института химии растворов им. Г.А. Крестова РАН (проект № 012012 60483). В работе использована приборная база Центра коллективного пользования научным оборудованием “Верхневолжский региональный центр физико-химических исследований”.
Список литературы
http://water-rf.ru/water/gosdoc/31.html
Lipatova I.M., Makarova L.I., Yusova A.A. // Chemosphere. 2018. V. 212. P. 1155–1162. https://doi.org/10.1016/j.chemosphere.2018.08.158
Al-Homaidan A.A., Al-Qahtani H.S., Al-Ghanayem A.A. et al. // Saudi J. Biol. Sci. 2018.V. 25. № 8. P. 1733–1738. https://doi.org/10.1016/j.sjbs.2018.07.011
Ahmaruzzaman Md. // Adv. Colloid Interface Sci. 2008. V. 143. P. 48–67. https://doi.org/10.1016/j.cis.2008.07.002
Titov V.A., Stokozenko V.G., Titova Yu.V. et al. // High Energ. Chem. 2015. V. 49 № 6. P. 459–464. https://doi.org/10.1134/S0018143915050148
O’Connell D.W., Birkinshaw C., O’Dwyer T.F. // J. Appl. Polym. Sci. V. 99. № 6. P. 2888–2897. https://doi.org/10.1002/app.22568
Никифорова Т.Е., Козлов В.А. // Физикохимия поверхности и защита материалов. 2016. Т. 52. № 3. С. 243–271. https://doi.org/10.7868/S0044185616030219
Никифорова Т.Е., Багровская Н.А., Козлов В.А. и др. // Химия растительного сырья. 2009. № 1. С. 5–14.
Алеева С.В., Лепилова О.В., Курзанова П.Ю. и др. // Изв. вузов. Химия и хим. технология. 2018. Т. 61. № 2. С. 80–85. https://doi.org/10.6060/tcct.20186102.5512
Qin F., Wen B., Shan X.Q. et al. // Environ. Pollut. V. 144. P. 669–680, https://doi.org/10.1016/j.envpol.2005.12.036
Khotimchenko M., Kovalev V., Khotimchenko Yu. // J. Hazard. Mater. 2007. V. 149. P. 693–699. https://doi.org/10.1016/j.jhazmat.2007.04.030
Assifaoui A., Lerbret A., Uyen H.T. et al. // Soft Mater. 2015. V. 11. № 3. P. 551–560. https://doi.org/10.1039/c4sm01839g
Лепилова О.В., Алеева С.В., Кокшаров С.А. // Журн. прикл. химии. 2018. Т. 91. Вып. 1. С. 68–73. https://doi.org/10.1134/S1070427218010147
Ленская К.В. // Автореф. … канд. биол. наук: 14.00.25. Владивосток: ВГМУ. 2007. 22 с.
Алеева С.В., Чистякова Г.В., Лепилова О.В. и др. // Журн. физ. химии. 2018. Т. 92. № 8. С. 1308–1315. https://doi.org/10.1134/S0036024418080022
Алеева С.В., Чистякова Г.В., Кокшаров С.А. // Изв. вузов. Химия и хим. технология. 2009. Т. 52. № 10. С. 118–121.
Дополнительные материалы отсутствуют.
Инструменты
Физикохимия поверхности и защита материалов