Физикохимия поверхности и защита материалов, 2021, T. 57, № 3, стр. 227-230
О согласовании данных численного и физического эксперимента при исследованиях адсорбции газов и паров в микропорах активных углей
А. М. Толмачев 1, *, Т. А. Кузнецова 1, П. Е. Фоменков 1
1 Московский государственный университет имени М.В. Ломоносова, Химический факультет
Москва, Россия
* E-mail: amtolmach@yandex.ru
Поступила в редакцию 28.09.2020
После доработки 11.01.2021
Принята к публикации 12.01.2021
Аннотация
Рассмотрены условия проведения молекулярно-динамических расчетов изотерм адсорбции газов и паров в микропорах активных углей, обеспечивающие количественное совпадение расчетных и экспериментальных изотерм.
ВВЕДЕНИЕ
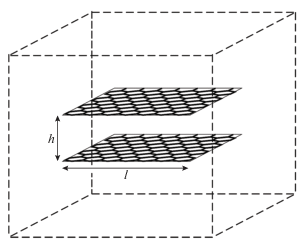
Прежде всего отметим, что описание изотерм адсорбции, полученных в результате физического эксперимента теоретическими уравнениями, выведенными на основании каких либо моделей, дает удовлетворительные результаты, как правило, только при относительно больших степенях заполнения объема микропор адсорбатом (Θ > 0.2–0.3). Это связано с тем, что модельные уравнения предполагают выполнение условий модели во всем интервале адсорбции, а в реальном микропористом адсорбенте всегда наблюдается “неидеальность” адсорбента, в виду небольших различий в ширинах щелевидных микропор, наличием структурных и энергетических неоднородностей. Например, уравнения решеточной модели, основанные на предположении, что микропоры образованы двумя строго параллельными слоями графена имеют вид [1]:
(1)
$\begin{gathered} \ln \frac{{{{X}_{1}}{\text{ }}(n)[1 - {{Y}_{1}}{\text{ }}]}}{{{{Y}_{1}}[1 - {{X}_{1}}{\text{ }}(n)]}} + 2\frac{{{{\varepsilon }_{{01}}}}}{{kT}} - \\ - \,\,\frac{{{{\varepsilon }_{{11}}}}}{{kT}}6{{X}_{1}}{\text{ }}(1) - \frac{{\varepsilon _{{11}}^{*}}}{{kT}}12{{Y}_{1}} = 0, \\ \end{gathered} $Эти уравнения количественно описывают экспериментальные изотермы при температурах меньших и больших критических для различных адсорбтивов на разных активных углях в широком интервале заполнений (Θ > 0.2–0.3), но при малых заполнениях наблюдаются заметные отклонения от экспериментальных данных. Это хорошо видно из данных табл. 1, в которой приведены относительные расхождения (∆ = $~\frac{{{{a}_{{{\text{экс}}}}} - {{a}_{{{\text{рас}}}}}}}{{{{a}_{{{\text{экс}}}}}}} \times 100\% $) рассчитанных и экспериментальных изотерм при различных степенях насыщения (Θ) микропористых активных углей.
Таблица 1.
Относительные расхождения (∆) при описании экспериментальных изотерм уравнениями (1)–(3) при различных степенях насыщения (Ɵ) микропористых активных углей
| Xe-ACC, 243 K | CH4-Exsorb, 323 K | CO2-AC, 308 K | C2H6-AC, 293 K | N2-AC-Nor, 298 К | |||||
|---|---|---|---|---|---|---|---|---|---|
| Ɵ | ∆ | Ɵ | ∆ | Ɵ | ∆ | Ɵ | ∆ | Ɵ | ∆ |
| 0.03 | 62.7 | 0.14 | 13 | 0.13 | 5.6 | 0.18 | 12 | 0.05 | 6.5 |
| 0.38 | –3.0 | 0.2 | 3.2 | 0.2 | 3.1 | 0.44 | 6.0 | 0.17 | 0.4 |
| 0.47 | –1.7 | 0.26 | 2.6 | 0.33 | –1.3 | 0.52 | 1.2 | 0.27 | –0.8 |
| 0.54 | 0.41 | 0.31 | –0.4 | 0.37 | –0.9 | 0.68 | –0.7 | 0.35 | –0.3 |
| 0.59 | 0.19 | 0.36 | –0.4 | 0.45 | –0.4 | 0.72 | –0.3 | 0.39 | –0.5 |
| 0.64 | 0.90 | 0.44 | –1.6 | 0.55 | 0.4 | 0.76 | 0.0 | 0.47 | 0 |
| 0.73 | 0.82 | 0.58 | –1.2 | 0.65 | 0.4 | 0.79 | –1.5 | 0.53 | 0.1 |
| 0.86 | –2.9 | 0.72 | 1.5 | 0.72 | 0.2 | 0.81 | –2.1 | 0.6 | –0.6 |
| 0.94 | 0.72 | 0.82 | 1.6 | 0.81 | 0.1 | 0.92 | 0.3 | 0.79 | 0.4 |
| 0.97 | 1.3 | 0.98 | 0 | 0.93 | 0.3 | 0.94 | 0.70 | 0.88 | 0.6 |
Очевидно, что количественного совпадения результатов численного (всегда модельного) и физического эксперимента можно также ожидать при Θ > 0.2–0.3.
ПОЛУЧЕННЫЕ РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Методика молекулярно-динамического эксперимента подробно описана ранее [3]. Отметим лишь, что расчеты проводились в модельной ячейке, в которую помещалась микропора, образованная двумя параллельными графеновыми пластинами 5 × 5 нм.
Изотермы адсорбции в микропоре получались в виде зависимостей числа адсорбированных молекул (m) от равновесного давления Р. Расчеты проводились до достижения предельных адсорбций (ms) при стандартных давлениях (давлении насыщенного пара адсорбтива – Рs при T < Tкр и Р * при Т > Ткр [4]).
Наши расчеты показали, что для количественного совпадения изотерм адсорбции в микропористых активных углях в широком интервале температур меньших и больших критических для адсорбтивов, рассчитанных методом молекулярной динамики и полученных в физических экспериментах необходимо соблюдение следующих условий.
Прежде необходимо согласовать величины адсорбции в модельной микропоре и реальном адсорбенте. Для этого необходимо проводить расчет в модельной поре ограниченных размеров, поскольку в этом случае можно определить число модельных микропор в реальном адсорбенте делением объема микропор адсорбента (W, см3) на объем микропоры (V, см3).
Однако, определение W по соотношению W = = a0/ρ (a0 – предельная адсорбция при стандартном давлении) связано с использованием плотности адсорбатов (ρ), которая, как правило, неизвестна. Поэтому сравнение изотерм точнее проводить в относительных величинах адсорбции
(4)
${m \mathord{\left/ {\vphantom {m {{{m}_{s}}}}} \right. \kern-0em} {{{m}_{s}}}} = {a \mathord{\left/ {\vphantom {a {{{a}_{0}}}}} \right. \kern-0em} {{{a}_{0}}}}~$(5)
$a = {{{{a}_{0}}m} \mathord{\left/ {\vphantom {{{{a}_{0}}m} {{{m}_{s}}\,\,({\text{моль}}\,\,{{{\text{г}}}^{{--1}}})}}} \right. \kern-0em} {{{m}_{s}}\,\,({\text{моль}}\,\,{{{\text{г}}}^{{--1}}})}} = f({P \mathord{\left/ {\vphantom {P {{{P}_{s}}}}} \right. \kern-0em} {{{P}_{s}}}}(P*)).$Вторым, очень важным условием является выбор универсального силового поля и соответствие ширины модельной и реальной щелей, которые и определяют энергию взаимодействия адсорбат–адсорбент.
Ширина щели (h) рассчитывается по уравнению теории объемного заполнения микропор [5]:
(6)
$h\,\,({\text{нм}}) = \frac{{24\,\,({\text{кДж}}\,\,{\text{нм}})}}{{{{E}_{{{\text{0,бенз}}}}}\,\,({\text{кДж}})}},\,\,\,\,\frac{{{{E}_{{{\text{0,бенз}}}}}}}{{{{E}_{{{\text{0,}}i}}}}} = \frac{{{{\Pi }_{{{\text{бенз}}}}}}}{{{{\Pi }_{i}}}},$Характеристическая энергия адсорбции определялась при обработке экспериментальных изотерм по уравнению Дубинина–Радушкевича [5].
Наши расчеты подтвердили справедливость этой формулы, если под величиной (h) принимать расстояние между центрами атомов углерода в графеновых поверхностях, ограничивающих модельную микропору.
Это подтверждается, например, данными табл. 2, в которой при ширине поры, рассчитанной по (6) (h = 0.8 нм), наблюдается хорошее совпадение рассчитанных и экспериментальных изотерм для разных адсорбтивов, а при ширине поры равной 1.0 нм наблюдается заметное отклонение соответствующих изотерм (левая колонка) для этанола.
Таблица 2.
Относительные расхождения (Δ) рассчитанных и экспериментальных изотерм при различных степенях насыщения (Ɵ) микропористых активных углей при 293 К (Т < Ткр). Ширина поры по (6) – 0.8 нм
| C2H5OH, АУ-1 h = 1.0 нм | C2H5OH, АУ-1 h = 0.8 нм | C6H6, АУ-1 h = 0.8 нм | Изо-C8H18, АУ-1 h = 0.8 нм | C3H6, АУ-1 h = 0.8 нм | |||||
|---|---|---|---|---|---|---|---|---|---|
| Ɵ | ∆ | Ɵ | ∆ | Ɵ | ∆ | Ɵ | ∆ | Ɵ | ∆ |
| 0.28 | 6.5 | 0.31 | 2.5 | 0.35 | 2.1 | 0.38 | 3.0 | 0.25 | 3.2 |
| 0.35 | 7.4 | 0.37 | –1.6 | 0.40 | 2.3 | 0.44 | 2.7 | 0.31 | 2.7 |
| 0.42 | 7.8 | 0.41 | –1.0 | 0.46 | 1.9 | 0.51 | 2.3 | 0.40 | 2.2 |
| 0.54 | 6.1 | 0.52 | 0.7 | 0.50 | 1.6 | 0.59 | –0.8 | 0.45 | 0.8 |
| 0.64 | 6.8 | 0.62 | 1.9 | 0.57 | 1.2 | 0.65 | –1.3 | 0.51 | –05 |
| 0.69 | 7.3 | 0.66 | 2.3 | 0.61 | 1.3 | 0.71 | 1.0 | 0.56 | 0.5 |
| 0.75 | 6.7 | 0.73 | 1.9 | 0.69 | 2.5 | 0.77 | 2.1 | 0.61 | 0.8 |
| 0.81 | 7.0 | 0.79 | 2.2 | 0.76 | 2.1 | 0.81 | 2.4 | 0.74 | 2.0 |
| 0.86 | 7.5 | 0.84 | 2.1 | 0.82 | 1.8 | 0.89 | 2.5 | 0.81 | 2.6 |
| 0.95 | 6.9 | 0.91 | 1.8 | 0.92 | 2.0 | 0.96 | 1.8 | 0.90 | 1.8 |
Однако, необходимо заметить, что соотношения (6) нуждаются в дополнительном уточнении интервала ширин пор, для которых оно применимо. Так, например, наши расчеты [6] показали, что плотность адсорбата достаточно резко меняется при переходе от ширины поры, в которой умещается один слой адсорбата, к более широким порам, допускающим размещение двух и более слоев адсорбата. Характеристическая адсорбция при этом изменяется почти в два раза. Такие расчеты могут быть проведены методом молекулярной динамики.
Что касается выбора универсального силового поля, то в общем случае необходима изотерма данного адсорбтива на каком-либо микропористом активном угле для подбора силового поля, которое потом может быть использовано и на других активных углях в широком интервале температур.
Наши расчеты [7] показали, что при расчетах изотерм адсорбции органических веществ (метан, этилен, бензол, этанол и т.д.) количественное совпадение изотерм наблюдается при использовании универсального силового поля OPLS-AA [8].
В дополнение к данным табл. 2 приведем данные, полученные для различных адсорбтивов при температурах выше критических.
Таблица 3.
Относительные расхождения (Δ) рассчитанных и экспериментальных изотерм при различных степенях насыщения (Ɵ) микропористых активных углей. Ширины микропор рассчитаны по уравнению (6)
| CH4-ПАУ-10, 170 К, h = 1.1 нм | CH4-ПАУ-10, 240 К, h = 1.1 нм | CH4-ПАУ-10, 303 К, h = 1.1 нм | C2H6,Nuxit, 333 К, h = 1.2 нм | C3H8,Nuxit, 373 К, h = 1.2 нм | |||||
|---|---|---|---|---|---|---|---|---|---|
| Ɵ | ∆ | Ɵ | ∆ | Ɵ | ∆ | Ɵ | ∆ | Ɵ | ∆ |
| 0.28 | 2.9 | 0.21 | 3.2 | 0.25 | 3.3 | 0.31 | 3.0 | 0.34 | 3.3 |
| 0.35 | 1.8 | 0.31 | 2.6 | 0.34 | 2.8 | 0.38 | 2.6 | 0.41 | 2.6 |
| 0.43 | –0.2 | 0.37 | 1.8 | 0.40 | 1.3 | 0.45 | 2.1 | 0.51 | –0.1 |
| 0.48 | –0.1 | 0.44 | 2.3 | 0.45 | –0.1 | 0.53 | 1.2 | 0.55 | –0.2 |
| 0.53 | 0.3 | 0.54 | 1.8 | 0.51 | –0.2 | 0.61 | 0.23 | 0.60 | 0.4 |
| 0.57 | 1.1 | 0.60 | 2.2 | 0.55 | 0.3 | 0.65 | –0.20 | 0.64 | 0.9 |
| 0.62 | 1.6 | 0.65 | 2.4 | 0.58 | 1.2 | 0.69 | –0.1 | 0.71 | 1.4 |
| 0.73 | 2.1 | 0.69 | 1.8 | 0.66 | 2.1 | 0.75 | 0.7 | 0.76 | 1.9 |
| 0.82 | 1.9 | 0.74 | 1.4 | 0.76 | 1.9 | 0.84 | 1.3 | 0.85 | 1.6 |
| 0.90 | 2.0 | 0.91 | 2.0 | 0.90 | 2.5 | 0.93 | 2.1 | 0.95 | 2.1 |
Отметим дополнительно, что ранее было показано [7, 9], что количественное совпадение рассчитанных и экспериментальных изотерм компонентов смесей также наблюдается при соблюдении описанных выше условий.
ЗАКЛЮЧЕНИЕ
Отметим в заключение, что численный эксперимент имеет очевидные преимущества перед физическим экспериментом. Кроме технических (необходимость адсорбционных установок, позволяющих получать изотермы адсорбции в широком интервале температур и давлений) есть еще одно важное обстоятельство. В численном эксперименте рассчитываются абсолютные изотермы адсорбции индивидуальных газов и паров или компонентов смесей, в то время как в физическом эксперименте всегда получаются избыточные изотермы, которые необходимо пересчитывать в абсолютные на основе приближенных моделей адсорбционной фазы [10]. Это особенно сложно делать при адсорбции смесей газов или паров [11].
Список литературы
Кузнецова Т.А., Толмачев А.М., Крюченкова Н.Г., Фирсов Д.А., Фомкин А.А. // Физикохимия поверхности и защита материалов. 2013. Т. 49. № 4. С. 339.
Толмачев А.М. // Адсорбция газов, паров и растворов. 2012. М. Изд. “Граница”. 239 с.
Толмачев А.М., Анучин К.М., Фоменков П.Е., Гумеров М.Р. // ЖСХ. 2018. Т. 59. № 8. С. 2013.
Фоменков П.Е., Гумеров М.Р., Толмачев А.М. // Физикохимия поверхности и защита материалов. 2018. Т. 54. № 4. С. 374.
Dubinin M.M. // Progress in surface and membrane Sci. New York: Acad. Press. 1975. V. 9. P. 1.
Толмачев А.М., Анучин К.М., Фоменков П.Е., Крюченкова Н.Г., Фирсов Д.А. // Физикохимия поверхности и защита материалов. 2017. Т. 53. № 2. С. 132.
Анучин К.М. // Дис. … канд. хим. наук. Москва. ИФХЭ РАН. 2011 г.
Jorgensen W.L., Maxwell D.S., Tirado-Rives J. // J. Am. Chem. Soc. 1996. 118, 11225.
Гумеров М.Р., Фоменков П.Е., Крюченкова Н.Г., Толмачев А.М. // Физикохимия поверхности и защита материалов. 2019. Т. 55. № 2. С. 115.
Fomkin A.A. // Adsorption. 2005. V. 11. № 3. P. 425.
Толмачев А.М., Гумеров М.Р., Кузнецова Т.А., Фоменков П.Е. // Физикохимия поверхности и защита материалов. 2020. Т. 56. № 5. С. 459.
Дополнительные материалы отсутствуют.
Инструменты
Физикохимия поверхности и защита материалов