Электрохимия, 2023, T. 59, № 1, стр. 29-42
Саморазряд суперконденсаторов (обзор)
Ю. М. Вольфкович *
Институт физической химии и электрохимии им. А.Н. Фрумкина РАН
119991 Москва, Россия
* E-mail: yuvolf40@mail.ru
Поступила в редакцию 04.06.2022
После доработки 09.07.2022
Принята к публикации 30.08.2022
- EDN: JZJCCN
- DOI: 10.31857/S0424857023010267
Аннотация
Была рассмотрена литература по следующим вопросам: преимущества электрохимических суперконденсаторов (ЭХСК) перед аккумуляторами. Показано, что основным недостатком ЭХСК является быстрый саморазряд. Проведено исследование саморазряда ЭХСК; были описаны методы исследования саморазряда, влияние на саморазряд функциональных углеродных групп (ФГ), механизмы саморазряда и математическое моделирование саморазряда. Была описана разработка новых устройств суперконденсаторов для минимизации саморазряда, а именно добавки в электролит, твердотельные суперконденсаторы, ЭХСК с ионообменными мембранами, использование беспримесных электролитов, методы химической модификации электродов для замедления саморазряда. Было проведено исследование саморазряда ЭХСК с электродами на основе активированной углеродной (АУ) ткани СН 900 компании Kuraray с водным электролитом 1 М MgSO4. Установлено, что скорость саморазряда через ~70 мин после его начала пропорциональна напряжению заряда. Зависимость же скорости саморазряда через 2000 мин после его начала от напряжения имеет минимум. Этот минимум объясняется, во-первых, существенным вкладом в емкость псевдоемкости фарадеевских редокс-реакций ФГ, а во-вторых, само наличие этих групп увеличивает скорость саморазряда. В области низких напряжений доминирует первый фактор, а в области высоких напряжений – второй фактор.
1. ВВЕДЕНИЕ
Согласно общепринятому определению, впервые сформулированному Конвеем, электрохимическими суперконденсаторами (ЭХСК) называются электрохимические устройства, в которых протекают квазиобратимые электрохимические зарядно-разрядные процессы, и форма гальваностатических зарядных и разрядных кривых которых близка к линейной, т.е. близка к виду соответствующих зависимостей для обычных электростатических конденсаторов [1]. ЭХСК имеют ряд существенных преимуществ перед аккумуляторами: практически бесконечная циклируемость, намного более высокая удельная мощность, принципиальная возможность получения энергетического КПД, приближающегося к 100%. В противоположность этому, энергетический КПД у аккумуляторов существенно ограничен поляризацией электродных реакций [2].
2. ПРЕИМУЩЕСТВА СУПЕРКОНДЕНСАТОРОВ ПЕРЕД АККУМУЛЯТОРАМИ
Промышленность ЭХСК в настоящее время испытывает бурный рост, что стимулирует исследования и внедрение их в новые области практического применения [1, 2]. ЭХСК имеют много преимуществ перед аккумуляторами: намного более длительное время работы, практически бесконечная циклируемость (от сотен тысяч до миллиона циклов, в то время как у аккумуляторов – только несколько сотен или тысяч циклов), намного более высокая удельная мощность, сравнительная дешевизна, возможность функционирования в широком диапазоне времен заряда–разряда и температур, экологичность и др. Очень важным преимуществом ЭХСК перед аккумуляторами является принципиальная возможность получения КПД по энергии (отношение энергии разряда к энергии заряда), приближающегося к 100%. Это может быть достигнуто в случае практического доминирования вклада емкости двойного электрического слоя (ДЭС) в полную емкость ЭХСК, что имеет место в двойнослойных суперконденсаорах (ДСК) [3]. В противоположность этому, величина КПД по энергии у аккумуляторов очень ограничена поляризацией электродных реакций. Возможность получения энергетического КПД, приближающегося к 100%, создает перспективу применения ЭХСК для сглаживания пиковых нагрузок электрических сетей.
Еще одним преимуществом ЭХСК является использование их для опреснения воды методом емкостной деионизации воды (ЕДВ), в котором используются такие же электрохимические ячейки с двумя электродами на основе высокодисперсных углеродных материалов (ВДУМ) с высокой площадью удельной поверхности 500–2500 м2 г–1, использующиеся также в ЭХСК [4, 5]. Метод ЕДВ требует минимальных энергетических затрат по сравнению со всеми другими опреснительными методами, в том числе и перед наиболее распространенным в промышленности методом обратного осмоса.
3. ОСНОВНОЙ НЕДОСТАТОК ЭХСК – БЫСТРЫЙ САМОРАЗРЯД
Существенным недостатком суперконденсаторов является их быстрый саморазряд, выражающийся в снижении напряжения и запасенной энергии после заряжения и размыкания внешней электрической цепи [4, 5]. В подавляющем большинстве публикаций, посвященных ЭХСК (а их уже многие тысячи), в рекламных целях отсутствует упоминание о саморазряде, поэтому очень важным является систематическое исследование этого вредного явления и выработка мер, снижающих скорость саморазряда, а значит, способствующих расширению применения ЭХСК в различных областях народного хозяйства и обороны.
В [6, 7] предположено, что явление саморазряда свидетельствует о том, что ЭХСК находится в неравновесном состоянии и стремится к термодинамическому равновесию. Был сделан вывод о том, что саморазряд – это неизбежная проблема для ЭХСК с углеродными электродами. В работах [8, 9] было установлено, что потери напряжения в диапазоне 5–60% происходят в течение двух недель и что скорость саморазряда зависит от таких факторов, как начальное напряжение, температура, продолжительность заряда и предыстория.
4. МЕТОДЫ ИЗМЕРЕНИЯ САМОРАЗРЯДА
4.1. Измерение профилей напряжения
На рис. 1 приведены кривые профилей саморазряда, т.е. зависимости изменения напряжения от времени для разных начальных напряжений для коммерческих ЭХСК марки Supercup с ацетонитрильным, т.е. неводным, электролитом [9].
Рис. 1.
Зависимости U(t)–U(0) от времени, где U(0) – начальное напряжение, U(t) – текущее напряжение для коммерческого ЭХСК марки Supercup с ацетонитрильным электролитом [9].

Из этого рисунка видно, скорость уменьшения напряжения со временем после размыкания электрической цепи, характеризующая саморазряд, возрастает с увеличением начального напряжения U(0). В работе [9] была развита простая математическая модель, объясняющая механизмы спада напряжения и токи утечки. Было также показано, что саморазряд увеличивается при повышении температуры.
На рис. 2 приведены типичные профили саморазряда для двух ЭХСК с блокировкой электродов и без нее. Оба конденсатора потенциостатически заряжались до 2.0 В в течение 18 ч до напряжения холостого хода [9]. В этой работе было также исследовано применение ультратонкого слоя электроосажденного поли (п-фениленоксида) (PPO) в качестве блокирующего слоя для уменьшения тока утечки, т.е. саморазряда. Полимер сначала осаждали на стеклоуглеродный электрод. Из этого рисунка видно, что цель уменьшения саморазряда была таким образом достигнута.
Рис. 2.
Профиль саморазряда в двух ЭХСК с блокировкой (with PPO) и без нее (without PPO). Оба суперконденсатора заряжались до 2.0 В в течение 18 ч до напряжения холостого хода [10].

4.2. Измерение токов утечки
Измерение тока утечки заключается в задании определенного напряжения ЭХСК и измерении изменения тока во времени. Обычно через какое-то, часто длительное время эта падающая зависимость выходит на плато, которое характеризует ток утечки. Чем больше величина тока утечки, тем больше саморазряд. На рис. 3 приведены зависимости токов утечки при различных напряжениях с течением времени: (а) 1 и (б) 1.2 В [11].
Рис. 3.
Токи утечки при различных напряжениях с течением времени: (а) 1 В, (б) 1.2 В [11]. (Обозначения: Pure – чистый образец, т.е. без добавок.)

В [11] было проведено сравнительное электрохимическое исследование ЭХСК, содержащего водный электролит 1 М Li2SO4 и ЭХСК с жидкокристаллической (ЖК) добавкой 2% 4-n-пентил-4'-цианобифенил (5CB). В результате было показано, что ЭХСК, содержащий ЖК-добавку 5CB, проявляет пониженный саморазряд и меньший ток утечки без ущерба для емкостных характеристик при различных исходных напряжениях по сравнению с поведением устройства без 5CB. Объяснение этих различий в саморазряде заключалось в более медленной диффузии ионов, которая затрудняет саморазряд и снижает ток утечки. Ток утечки пропорционален скорости фарадеевской реакции. Скорость переноса электрона зависит от потенциала редокс-реакции. Согласно уравнению Тафеля, скорость фарадеевской реакции экспоненциально связана с перенапряжением и приводит к тому, что ток утечки увеличивается экспоненциально с увеличением напряжения. В идеале, при отсутствии фарадеевских реакций ток утечки равен нулю. При этом емкость равна емкости ДЭС.
4.3. Измерение импеданса
В целом ряде работ саморазряд исследовался методом электрохимического импеданса [12–19]. На рис. 4 приведены измеренные и вычисленные частотные зависимости импеданса для ЭХСК с применением ультратонкого блокирующего слоя электроосажденного поли (п-фениленоксида) (PPO) для уменьшения саморазряда [13].
Рис. 4.
Измеренные (measured) и вычисленные (simulated) частотные характеристики импеданса СК с РРО (w) и без РРО (wо) [13].

Эти зависимости рассчитывались путем использования эквивалентной электрической схемы, изображенной на рис. 5.
Рис. 5.
Электрическая эквивалентная схема для ЭХСК, где Ceq – емкость ДЭС, Rs – последовательное сопротивление, Rp – параллельное сопротивление [13].

Из рис. 4 видно, что применение блокирующего слоя приводит к увеличению импеданса в диапазоне частот от 10–2 до 103 Гц.
5. МЕХАНИЗМЫ САМОРАЗРЯДА
На основании исследования ЭХСК с различными углеродными материалами были установлены следующие механизмы саморазряда.
5.1. Перераспределение катионов и анионов в пористом электроде по толщине и по порам разных размеров [20–22]
Длительное заряжение позволяет ионам равномерно распределяться по порам разных размеров и по толщине электродов, и поэтому падение напряжения в период покоя (холостого хода) после заряжения существенно снижается. Данная модель способна предсказывать влияние продолжительности заряжения, начального напряжения и температуры на спад напряжения холостого хода [20–22]. Перераспределение заряда обусловлено разницей в доступности ионов к внутренней поверхности электрода. При более высоком начальном напряжении ЭХСК демонстрируют больший саморазряд, однако при достаточно длительном времени предварительного удержания заряда скорость саморазряда мала. Восстановление напряжения было обнаружено в ЭХСК с графеновыми электродами даже после полного разряда за счет механизма перераспределения заряда [24].
5.2. Окисление углерода
В работах [25, 26] было установлено, что окисление углерода и перераспределение заряда – это процессы, направленные на снижение градиентов потенциала в электродах, и они являются основными механизмами, связанными с саморазрядом в кислотно-водных электролитах. Различить эти механизмы оказывается сложной задачей, поскольку оба процесса характеризуются аналогичными профилями саморазряда. Для того чтобы решить эту проблему, была разработана новая экспериментальная методика. Было установлено, что перераспределение заряда является основным механизмом саморазряда с меньшим вкладом (17% от исходного саморазряда) процесса окисления углерода в графеновых электродах [24]. Была установлена корреляция между саморазрядом и скоростью окисления углерода. В процессе окисления активированной углеродной (АУ) ткани Spectracarb 2225 углерод окисляется до CO2 и развивает функциональность поверхности со связями C–O и C=O. Очевидно, что при больших величинах зарядного напряжения положительный электрод больше окисляется и это приводит к ускорению саморазряда. Это видно из рис. 6, на котором показаны зависимости напряжения от корня квадратного от времени (t1/2) для углеродного ЭХСК SCA272 с органическим электролитом для четырех начальных напряжений [22].
Рис. 6.
Кривые зависимостей напряжения от t1/2 для ЭХСК SCA272 в течение 120 мин саморазряда для четырех начальных напряжений [22].

Первоначально функциональные группы (ФГ) C–O образуются преимущественно во время заряжения электрода; при саморазряде в основном образуются ФГ C=O. При повторных циклах заряда/разряда происходит истощение активных центров окисления углерода. Следовательно, удаление этих активных участков поверхности посредством электрохимического окисления существенно снижает саморазряд положительных углеродных электродов в ЭХСК с водными электролитами [26]. Следует отметить, что указанное влияние ФГ на саморазряд в данном случае имеет место для ЭХСК с неводным электролитом.
5.3. Челночный перенос ионов – продуктов редокс-реакций с одного электрода на другой и обратно [1, 22, 28–31]
Распространенным случаем такого челночного переноса является процесс, обусловленный наличием в электролите примесей ионов железа. Ионы Fe+3 вследствие электромиграции переносятся на отрицательный электрод, на котором они восстанавливаются до Fe+2; затем они мигрируют на положительный электрод, на котором окисляются до Fe+3, и т.д. Источником ионов железа в электролите в основном является зола или коррозия корпуса ЭХСК. В [32] было исследовано влияние на саморазряд аналогичного челночного механизма, обусловленного многовалентными ионами марганца и титана. Ионы переменной валентности могут содержаться не только в виде примесей в электролите, но также в виде противоионов ФГ в АУ. Челночный перенос ионов может ограничиваться на разных стадиях [21, 23, 26, 27, 32]:
3а – на стадии поляризации электродных реакций, зависящей от каталитической активности этих реакций;
3б – на стадии барьера в виде ДЭС;
3в – на стадиях диффузионного и электрического переноса ионов между электродами. В работах [26] было показано, что диффузионно-контролируемый механизм за счет примесей наблюдался при E > 1.4 В для положительного электрода и при E < 1.2 В для отрицательного электрода.
Согласно Конвею [1], скорости саморазряда определяются следующими механизмами процессов:
(а) Если саморазряд контролируется диффузией ионов, являющихся продуктами перезаряжения, или редокс-реакций примесей, например, Fe2+/Fe3+, или других ионов элементов с переменной валентностью, то зависимость падения напряжения U от логарифма времени (lgt) будет линейной:
где А – энергия, t – время, θ – константа интегрирования.(б) Если саморазряд контролируется полубесконечной диффузией в пористом электроде с участием примесей, то падение потенциала во времени определяется зависимостью от квадратного корня:
(2)
${{U}_{t}} = {{U}_{1}} - \frac{{2zFS{{D}^{{{1 \mathord{\left/ {\vphantom {1 2}} \right. \kern-0em} 2}}}}{{\pi }^{{{1 \mathord{\left/ {\vphantom {1 2}} \right. \kern-0em} 2}}}}c{{t}^{{{1 \mathord{\left/ {\vphantom {1 2}} \right. \kern-0em} 2}}}}}}{c},$(в) Если саморазряд обусловлен током утечки “короткого замыкания” между двумя электродами, например вследствие погрешностей в сборке батареи биполярных суперконденсаторов, то зависимость lnUi от t будет линейной:
где R – омическое сопротивление току утечки.Здесь следует отметить, что механизм саморазряда вследствие челночного переноса ионов переменной валентности с одного электрода на другой и обратно в неводных электролитах играет существенно меньшую роль по сравнению с водными электролитами вследствие существенно меньшей растворимости ионов в неводных электролитах.
На рис. 7 изображено снижение напряжения вследствие саморазряда на электроде из углеродной ткани СН900 относительно стандартного водородного электрода (с. в. э.) от следующих исходных потенциалов: +0.7, +0.9, +1.1, +1.3 и +1.35 В в электролите 5.0 М H2SO4, после заряжения током 10 мА [1]. Из рисунка видно, что в этом случае саморазряд соответствует уравнению (1), т.е. механизму (а).
Рис. 7.
Снижение напряжения вследствие саморазряда на электроде из углеродной ткани относительно с.в.э. от следующих исходных потенциалов: +0.7, +0.9, +1.1, +1.3 и +1.35 В в электролите 5.0 М H2SO4, после длительного заряжения током 10 мА [1].

5.4. Перенос ионов из мест с высокой концентрацией в места с более низкой концентрацией [32]
Было установлено, что для углеродных электродов с большой концентрацией ФГ процесс саморазряда протекает быстрее [9, 22, 33, 34]. В работах [35, 36] были описаны новые методы химической модификации электродов для снижения саморазряда, обусловленного наличием определенных ФГ. В [33] был исследован саморазряд для однослойных углеродных наноторубок (ОСУНТ) с большим количеством ФГ и было установлено, что саморазряд с исходного напряжения 1 В протекает быстрее в первые 0.5 ч и еще 4.15 ч до 0.5 В, т.е. до “периода полусаморазряда”.
В [35] саморазряд исследовали с помощью электродов, состоящих из многослойных углеродных нанотрубок (МСУНТ) трех диаметров: 20, 30 и 50 нм. Характеристики диффузии, полученные на основе разработанной модели, согласуются с измеренными скоростями саморазряда, которые повышаются с увеличением диаметра МСУНТ. Было также установлено, что процессы саморазряда зависят от распределения пор по размерам. Показано также, что процесс саморазряда существенно связан с площадью удельной поверхности электродов [36]. Удаление активных участков поверхности в результате электрохимического циклирования значительно уменьшает саморазряд, испытываемый за счет положительных углеродных электродов ЭХСК с водными электролитами. Это показано в [25] для ЭХСК с электродами из восстановленного оксида графена (ВОГ).
Поскольку выводы о механизмах саморазряда и, в основном, о его количественных характеристиках существенно зависят от вида электродных материалов, то во многих публикациях было проведено исследование саморазряда ЭХСК с электродами на основе различных углеродных материалов.
6. МАТЕМАТИЧЕСКОЕ МОДЕЛИРОВАНИЕ САМОРАЗРЯДА
В ряде публикаций математическое моделирование саморазряда было основано на разработке адекватной эквивалентной электрической схемы. Метод электрохимического импеданса является очень информативным для исследования процесса саморазряда ЭХСК [37, 38]. Обычные эквивалентные электрические схемы конденсаторов имеют основное последовательное сопротивление (RC-ветвь) и параллельное сопротивление тока утечки [37]. Параллельное сопротивление Rp отвечает за время саморазряда конденсатора [37‒39]. В работе [40] были предложены модели с тремя параллельными ветвями, причем одна из этих ветвей содержит элемент постоянного сдвига фаз (CPE).
В [41] на основании исследования ЭХСК марки A600 F компании Nesscap было установлено, что процесс саморазряда определяется рядом параметров, таких как исходное напряжение, температура и продолжительность заряда. В зависимости от этих параметров наблюдали небольшое падение напряжения на 5–15% в течение 48 ч после начала саморазряда. Была развита сложная электрическая модель для учета эффектов перераспределения ионов, происходящих в ЭХСК. Длительный заряд позволяет ионам более равномерно распределяться по толщине электродов и по порам разных радиусов. Вследствие этого падение напряжения в период покоя после заряжения значительно уменьшается. Модель дает возможность предсказывать влияние продолжительности заряда, начального напряжения и температуры на снижение напряжения холостого хода. На рис. 8 показана разработанная в данной работе эквивалентная электрическая схема саморазряда двойнослойного суперконденсатора (ДСК), которая учитывает сопротивление и емкость микропор, мезопор и макропор а также сопротивление электролита, углерода и емкость ДЭС [41].
На рис. 9 продемонстрировано влияние времени заряжения на спад напряжения холостого хода при продолжительности заряда 15 мин, 2 ч и 5 дней. Как видим, при продолжительности заряжения 2 ч и 5 дней падение напряжения через 50 ч соответственно равны 6 и 3%. Это очень незначительный саморазряд [41].
Рис. 9.
Влияние времени заряжения на спад напряжения холостого хода при продолжительности заряда 15 мин, 2 ч и 5 дней [41].

Другой подход к моделированию процесса саморазряда ЭХСК был разработан в [42], а именно аналитический подход. Была получена система уравнений, учитывающих заряжение ДЭС, уравнение для саморазряда с учетом уравнения Тафеля. На рис. 10 показаны экспериментальные и расчетные кривые профиля саморазряда с блокирующим слоем и без него. В качестве блокирующего слоя для снижения саморазряда использовался ультратонкий электроосажденный слой поли (п-фениленоксида) (PPO).
Рис. 10.
Экспериментальные (сплошные линии) и рассчитанные (Simulation – пунктир) кривые профиля саморазряда с блокирующим слоем (With blocking layer – красный цвет) и без него (No blocking layer – синий цвет) [42].

Из этого рисунка можно сделать следующие выводы: 1) применение блокирующего слоя существенно снижает саморазряд; 2) рассчитанные кривые практически идеально совпадают с соответствующими экспериментальными кривыми, что свидетельствует о корректности разработанной математической модели для описания саморазряда.
7. РАЗРАБОТКА НОВЫХ СУПЕРКОНДЕНСАТОРОВ ДЛЯ ПОВЫШЕНИЯ ИХ ХАРАКТЕРИСТИК И МИНИМИЗАЦИИ САМОРАЗРЯДА
7.1. Введение специальных добавок в электролит
Специальные добавки вводились в электролит для увеличения вязкости, которое приводит к увеличению сопротивления и снижает саморазряд. В [32] в электролит вводили жидкие кристаллы 4-n-пентил-4'-цианобифенил (5CB) для подавления саморазряда ДСК. Когда ДСК заряжен, то электрическое поле в ДЭС вблизи поверхности электрода индуцирует выравнивание молекул 5CB, вызывая значительно повышенную вязкость жидкости с помощью так называемого электрореологического эффекта. В результате диффузия ионов затрудняется и скорость саморазряда уменьшается. Было показано, что при добавлении 2% 5CB в неводный электролит TEMABF4/ацетонитрил скорость снижения напряжения разомкнутой цепи и ток утечки уменьшались более чем на 80%. В [43] жидкокристаллическую добавку 5CB вводили в ЭХСК с водным электролитом 1 М Li2SO4. Полученные результаты показали, что ЭХСК, содержавший добавку 5CB, проявлял пониженный саморазряд и ток утечки без ущерба для емкостных характеристик при различных исходных напряжениях по сравнению с поведением без 5CB. Объяснение влияния этой добавки на саморазряд заключалось в изменении эффективной проводимости композитного электролита при приложенных напряжениях. В результате ЭХСК продемонстрировал более медленную диффузию ионов, которая приводила к уменьшению саморазряда и тока утечки.
В работе [44] в качестве добавки к электролиту был использован лиотропный жидкий кристалл (LLC) для подавления саморазряда суперконденсаторов за счет электрореологического эффекта LLC. Этот жидкий кристалл, образованный триблок-сополимером Pluronic L64 в ионной жидкости [Bmim] BF4, проявляет диэлектрическую анизотропию и может переориентировать ионы в электрическом поле, вызывая повышенную вязкость и более медленную диффузию ионов. Было показано, что добавление 5 об. % LLC в неводный электролит TEMABF4/ацетонитрил позволяет снизить скорость саморазряда при комнатной температуре на 32% по сравнению с ЭХСК без LLC. Жидкий кристалл LLC также может снизить скорость саморазряда суперконденсаторов даже при 50°C из-за его стабильности в относительно широком диапазоне температур.
В [45] добавка на основе изоцианата 2-изоцианатоэтилметакрилат (ICEMA) полимеризовалась двумя методами: электрополимеризацией in situ (EP) и радикальной полимеризацией (RP) на электроде из активированного угля (AУ) для уменьшения диффузии и саморазряда. Хотя радикально-полимеризационный метод (RP) продемонстрировал существенное подавление саморазряда, однако он показал резкое увеличение всех параметров импеданса и ухудшенные возможности заряда/разряда. Метод же EP не имеет этот недостаток и продемонстрировал сохраненную емкость и подавление саморазряда.
7.2. Твердотельные суперконденсаторы
Другими новыми типами ЭХСК для существенной минимизации саморазряда являются твердотельные суперконденсаторы. Существует ряд вариантов создания твердотельных ЭХСК. В [46] был разработан твердотельный ЭХСК с использованием цвиттерионного гелевого электролита. Этот электролит наделяет твердотельные ЭХСК низким саморазрядом во время работы при разомкнутой цепи, сохраняя при этом высокие электрические характеристики во время работы в замкнутой цепи. В данной работе был использован поли(пропилсульфонат диметиламмоний пропилметакриламид) (PPDP) для изготовления полицвиттерионного гелевого электролита со структурной формулой
При этом использовались электроды на основе графена. Симметричный суперконденсатор (ССК) заряжался до 1.0 В при постоянной плотности тока 100 мкА см–1, а затем выдерживался при этом напряжении в течение 1.33 ч, чтобы гарантировать, что ССК полностью заряжен. После этого измерялся спад напряжения в условиях холостого хода. Время саморазряда при снижении напряжения наполовину было 12 ч для ССК на основе PPDP и почти в 2 раза дольше, чем у ССК на основе поливинилового спирта. Было установлено, что цвиттерионный гелевый электролит может применяться на практике для подавления диффузии ионов в условиях разомкнутой цепи. Это уменьшение обусловлено уменьшением активности воды вследствие сильной гидратации полицвиттер-иона. Диффузия ионов подавляется из-за их электростатического взаимодействия с цвиттерионными группами. Этот механизм действует для всех цвиттерионных гелевых электролитов, поскольку подобные механизмы, рассмотренные в работе [46], могут быть обобщены на цвиттерионный гелевый электролит, применяемый в других ЭХСК для решения проблемы удовлетворения противоположных требований: минимизации саморазряда при сохранении электрохимических характеристик.
В работе [20] редокс-медиатор метиленовый синий (MB) был введен в смесь поливинилового спирта и поливинилпирролидона (ПВС/PVP), чтобы приготовить гелевый полимерный электролит (ПВС–PVP–H2SO4–MB) для квазитвердотельного ЭХСК. Электрохимические свойства такого суперконденсатора с гелевым полимерным электролитом оценивали методами циклической вольтамперометрии, гальваностатического метода, спектроскопии электрохимического импеданса и измерений саморазряда. При добавлении медиатора MB удельная емкость электрода ЭХСК с электролитом ПВС–PVP–H2SO4–MB составляла в H2SO4 328 Ф г–1, увеличиваясь на 164% по сравнению с таковой у нелегированной системы MB при той же плотности тока 1 А г–1. Плотность энергии ЭХСК увеличивалась с 3.2 до 10.3 Вт ч кг–1. Квазитвердотельный ЭХСК показал отличную циклируемость в течение 2000 циклов заряда/разряда. В работе [47] сообщалось об электрохимических свойствах, таких как саморазряд, ток утечки, и результатах испытаний по поддержанию напряжения твердотельных симметричных ЭХСК на основе восстановленного оксида графена (ВОГ), сепаратора на основе фильтра марки Whatman и гелевого электролита (поливиниловый спирт/Na2SO4). Испытания симметричных ЭХСК продемонстрировали широкое окно потенциалов (1.2 В), достаточно высокую удельную емкость 110.3 мА ч г–1 при плотности тока 1 А г–1, высокую плотность энергии 22.1 Вт ч кг–1 и очень высокую плотность мощности 7304.5 Вт кг–1. Кроме того, этот ЭХСК показал высокую стабильность 89.4% после 10 000 циклов гальваностатического заряда/разряда и 82.3% емкости после 20 ч саморазряда. Этот суперконденсатор показал также небольшой ток утечки 0.029 мА.
В [36] сообщалось о создании твердотельных батарей на основе гибких микро-суперконденсаторов (МСК) с электродами, состоящими из узорчатого многослойного графена (МГ), функционализированных многослойных углеродных нанотрубок (МСУНТ) и гелевого электролита из поливинилового спирта (ПВС)–H3PO4. Такой МСК показал поверхностную емкость 2.54 мФ см–2 при скорости сканирования 10 мВ с–2, что в 150 раз выше, чем у МСК с электродами из МГ. Поверхностная энергия и плотность мощности также были значительно увеличены за счет использования электродов МГ/МСУНТ. Кроме того, не наблюдалось ухудшения электрохимических характеристик при повторяющейся выпуклой и вогнутой формах изгиба МСК с радиусом изгиба 2.3 мм. Кроме того, как выходное напряжение, так и суммарная емкость МСК могут контролироваться через последовательное или параллельное соединение нескольких MCK планарного типа для работы высоковольтных светодиодов. Эти МСК продемонстрировали сниженный саморазряд.
7.3. Суперконденсаторы с ионообменными мембранами
В последние годы были начаты исследования по использованию ионообменных мембран (ИОМ) в ЭХСК [48–51]. Это обусловлено удобной для практики твердотельной конструкцией таких ЭХСК, а также уменьшением саморазряда. В [47] были исследованы твердотельные гибридные суперконденсаторы (ГСК) АУ/MnO2 с электродами, нанесенными на углеродную нановолокнистую тканевую основу. Они показали стабильную производительность в водной среде для диапазона напряжений 0–1.6 В, низкий саморазряд и хорошие емкостные характеристики 138 и 134 Ф г–1 с пористой бумагой и мембраной Нафион соответственно. Твердотельный ГСК показал очень низкий саморазряд даже после длительных испытаний на долговечность в течение 270 ч. Другим важным заключением этой работы явилось стабильное рабочее напряжение 1.6 В, т.е. выше потенциала разложения воды (1.23 В), без заметного выделения кислорода и процессов деградации электродов.
В [49] было исследовано электрохимическое поведение мембран Нафион в твердотельных ЭХСК с композитами: восстановленный оксид графена (ВОГ)–мембрана Нафион–УН–полипиррол. Мембраны Нафион 117 были применены в качестве сепараторов при приготовлении твердотельных симметричных ЭХСК в 1 М LiCl. Была получена удельная емкость 258.3 Ф г–1 при скорости развертки напряжения 10 мВ с–1. Также были получены величины плотности энергии и плотности мощности 10 Вт ч кг–1 и 6031 Вт кг–1 соответственно. В [49] было описано изготовление неводного механически прочного протонопроводящего гель-полимерного электролита. Этот электролит был основан на мономере 2-гидроксиметил-метакрилат, смешанном с двумя различными растворителями (пропиленкарбонат и N,N-диметилформамид). Композитный углеродный электрод был изготовлен путем смешивания АУ YP80-F с АУ Kuraray Chemical Co., LTD и с 5 вес. % связующего полиливилиден фторида – гексафторпропилена. В результате было показано, что электрохимические характеристики изменяются в зависимости от состава гелевого электролита. В результате была получена удельная емкость 90 Ф г–1 при 20°C. Эти исследования проводились в широком диапазоне температур от –40 до 80°C.
Хотя в большинстве работ по ЭХСК с ИОМ применялись протонообменные мембраны, однако в ряде работ были исследованы ЭХСК с анионообменными мембранами в среде OH–. В [50] были исследованы ЭХСК в щелочной среде с проводимостью по анионам ОН– в полимерной матрице, а также установлены несколько интересных взаимосвязей между свойствами полимерного электролита и характеристиками твердотельного ЭХСК. Полимерные электролиты с ионной проводимостью по OH– были подразделены на два типа: анионообменные мембраны и щелочные полимерные электролиты. ЭХСК, использующие щелочные электролиты, обычно содержали пористые сепараторы, такие как полипропилен (PP), полиэтилен (PE) или полиамид, которые впитывали электролит в поры, являясь электрическим изолятором между электродами. В результате исследования были установлены несколько важных свойств ИОМ, которые повлияли на производительность ЭХСК, химическую стабильность и поглощение электролита. Снижение производительности во времени было следствием испарения воды, и был предложен способ уменьшения этого эффекта. Чтобы создать экономически обоснованный, легкий, тонкий и гибкий твердый ЭХСК с анионообменной мембраной, полимерные электролиты должны удовлетворять следующим требованиям: большая ионная проводимость; широкое окно напряжения; способность достигать надежных контактов электрод/электролит; механическая прочность, химическая стабильность при длительном циклировании [51].
7.4. Использование беспримесных электролитов
Как следует из вышеизложенного, одним из основных механизмов саморазряла является челночный перенос ионов – продуктов окислительно-восстановительных реакций, с одного электрода на другой и обратно. Типичным случаем такого челночного переноса ионов является процесс, вызванный присутствием в растворе электролита примесей ионов железа. Поэтому важнейшей мерой для существенного уменьшения скорости саморазряда является достижение беспримесной чистоты электролита. Основным источником примесей в электролите ЭХСК с АУ-электродами является зола, состоящая из неорганических компонентов, содержащаяся в прекурсорах из растительных материалов: древесины, скорлупы орехов, кокосов и т.п. Для удаления золы ее растворяют в концентрированных кислотах. Кардинальным решением этой проблемы является применение прекурсоров из синтетических полимеров, например полиэтилена, полиакрилонитрила и т.п. Другим способом получения беспримесных электролитов является использование в качестве электродов карбидных углей.
Производители коммерческих ЭХСК предпринимают необходимые меры, чтобы практически исключить наличие примесей в электролитах с целью минимизации саморазряда. Например, в [52] проводились измерения саморазряда для коммерческого ЭХСК Maxwell BCAP 3000 с номинальной емкостью 3000 Ф и напряжением 2.7 В. Исследования осуществлялись при следующих температурах: 278, 293, 308 и 323 К и при начальных напряжениях: 2.7, 2.4, 2.1, 1.8 и 1.5 В. На рис. 11 показаны результаты измерений саморазряда такого ЭХСК. Из этого рисунка следует, что для не очень высоких температур (278, 293 и 308 К) саморазряд был ничтожен на протяжении более 100 000 с. Следует отметить, что столь низкий саморазряд был получен для ЭХСК с неводным электролитом.
Рис. 11.
Профили саморазряда ЭХСК Maxwell BCAP 3000 при разных температурах и начальных напряжениях [52].

Из этого рисунка видно, что падение напряжения на клеммах увеличивается с увеличением исходного напряжения и температуры. Аналогичные результаты получены в [53]. Ничтожный саморазряд был достигнут также для коммерческих ЭХСК A600 F компании Nesscap.
7.5. Методы химической модификации электродов для снижения саморазряда
В [25] было показано, что устранение активных центров поверхности посредством электрохимического или химического окисления существенно снижает скорость саморазряда положительных углеродных электродов в водных ЭХСК. Для суперконденсаторов с электродами на основе ВОГ было показано, что вольт-амперное циклирование в определенном диапазоне потенциалов очищает поверхность электродов от ФГ и существенно снижает саморазряд. Было также установлено, что этот метод применим к СК с другими ВДУМ.
8. САМОРАЗРЯД СУПЕРКОНДЕНСАТОРА С ЭЛЕКТРОДАМИ НА ОСНОВЕ АКТИВИРОВАННОЙ УГЛЕРОДНОЙ ТКАНИ
В работе [54] было проведено исследование саморазряда ЭХСК с электродами на основе активированной углеродной (АУ) ткани СН 900 компании Kuraray с водным электролитом 1 М MgSO4. Элементный состав положительного и отрицательного электродов после электрохимической обработки до 1.6 В стал радикально различаться между собой. Это было установлено методом элементного анализа. На положительном электроде возникла очень большая концентрация водорода и кислорода, что объясняется образованием функциональных поверхностных групп (ФГ). Установлено, что логарифм скорости саморазряда через ~70 мин после его начала пропорционален напряжению заряда. Зависимость же скорости саморазряда через 2000 мин после его начала от напряжения имеет минимум. Этот минимум объясняется действием двух противонаправленных механизмов. Во-первых, существенный вклад в емкость вносит псевдоемкость фарадеевских редокс-реакций ФГ, а во-вторых, само наличие этих групп увеличивает скорость саморазряда. В области низких напряжений доминирует первый фактор, а в области высоких напряжений – второй фактор.
На основании импедансных измерений для области малых времен саморазряда разработана эквивалентная электрическая схема ячейки ЭХСК. Показано, что сопротивление тока утечки уменьшается при увеличении напряжения, что согласуется с измерениями скорости саморазряда. Показано, что скорость саморазряда ЭХСК после 2000 заряд-разрядных циклов меньше по сравнению с соответствующей для исходного состояния ячейки, что объясняется наличием ФГ. На рис. 12 приведены кривые падения напряжения ячейки ЭХСК во времени за первые 2 ч саморазряда после 3-часового заряжения при разных напряжениях: 1 – 1000; 2 – 1200; 3 – 1400; 4 – 1600 мВ. На вкладке приведена зависимость логарифма скорости саморазряда от напряжения заряда через 4000 с. Из рис. 12 следует, что логарифм скорости саморазряда пропорционален напряжению заряда.
Рис. 12.
Снижение напряжения ячейки ЭХСК во времени за первые 2 ч саморазряда после 3-часового заряжения при разных напряжениях: 1 – 1000; 2 – 1200; 3 – 1400; 4 – 1600 мВ. На вкладке приведена зависимость скорости саморазряда через 4000 с, от напряжения заряда [54].

На рис.13 продемонстрировано снижение напряжения ячейки ЭХСК во времени до напряжения, соответствующего половине напряжения заряда, при напряжениях заряда: 1 – 1000; 2 – 1200; 3 – 1400; 4 – 1600 мВ. На вкладке приведена зависимость скорости саморазряда через 2000 мин от напряжения заряда. Интересно, что кривая на вкладке имеет минимум (при напряжении 1.4 В) в отличие от соответствующей кривой на рис. 12, имеющей возрастающий характер. Различие условий измерений этих кривых заключается в том, что кривые на рис. 12 измерены через 66.7 мин (4000 с) после заряда, а кривые на рис. 13 измерены через 2000 мин после заряда.
Рис. 13.
Снижение напряжения ячейки ЭХСК во времени до напряжения, соответствующего половине напряжения заряда. Напряжение заряда: 1 – 1000; 2 – 1200; 3 – 1400; 4 – 1600 мВ. На вкладке зависимость скорости саморазряда через 2000 мин, от напряжения заряда [54].
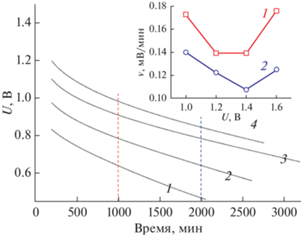
Следовательно, механизм саморазряда резко изменяется во времени. Как показано в работе [54], при малых временах (до 66.7 мин) важной составляющей саморазряда является двойной электрический слой. При больших же временах саморазряда химический состав поверхности существенно изменяется вследствие генерации большого количества ФГ. Наличие минимума на вкладке рис. 13 свидетельствует о действии двух противонаправленных механизмов. Во-первых, согласно [55, 56], в ЭХСК с АУ-электродами существенный вклад в емкость вносит псевдоемкость фарадеевских редокс-реакций функциональных поверхностных групп, а во-вторых, само наличие этих групп увеличивает скорость саморазряда (см. Введение). Следовательно, в интервале напряжений от 1.0 до 1.4 В доминирует влияние первого фактора, а в интервале напряжений от 1.4 до 1.6 В доминирует влияние второго фактора.
На рис. 14 приведено сравнение динамики спада напряжения после 3-часового заряжения ячейки ЭХСК при напряжении 1000 мВ для: 1 – исходного состояния ячейки; 2 – после 2000 заряд-разрядных циклов в интервале 1600–500 мВ. На вкладке дано сравнение ЦВА в этих условиях. Как видим, скорость спада напряжения после 2000 заряд-разрядных циклов в интервале 1600–500 мВ (кривая 2 на основном рисунке) меньше по сравнению со скоростью спада напряжения для исходного состояния ячейки (кривая 1 на основном рисунке). Это можно объяснить, во-первых, тем, что в процессе циклирования возрастает концентрация ФГ, и, во-вторых, тем, что влияние этих групп в основном сводится к повышению емкости вследствие фарадеевских редокс-реакций этих групп. Это согласуется с рисунком на вкладке, согласно которому форма ЦВА-кривой после 2000 заряд-разрядных циклов в интервале 1600–500 мВ (кривая 2) свидетельствует о существенном вкладе фарадеевской емкости, в то время как форма ЦВА-кривой для исходного состояния (кривая 1) имеет классический вид для ДЭС [1, 2].
Рис. 14.
Сравнение динамики спада напряжения после 3-часового заряжения ячейки ЭХСК при напряжении 1000 мВ для: 1 – исходного состояния ячейки; 2 – после 2000 заряд-разрядных циклов в интервале 1600–500 мВ. На вкладке сравнение ЦВА в этих условиях [54].

ЗАКЛЮЧЕНИЕ
Была рассмотрена литература по следующим вопросам:
– Преимущества ЭХСК перед аккумуляторами. Показано, что основным недостатком ЭХСК является быстрый саморазряд.
– Проведено исследование саморазряда ЭХСК; были описаны методы исследования саморазряда, влияние на саморазряд функциональных углеродных групп (ФГ), механизмы саморазряда и математическое моделирование саморазряда.
– Была описана разработка новых устройств суперконденсаторов для минимизации саморазряда, а именно добавки в электролит, твердотельные суперконденсаторы, ЭХСК с ионообменными мембранами, использование беспримесных электролитов, методы химической модификации электродов для замедления саморазряда.
– Было проведено исследование саморазряда суперконденсатора (ЭХСК) с электродами на основе активированной углеродной (АУ) ткани СН 900 компании Kuraray с водным электролитом 1 М MgSO4. Элементный состав положительного и отрицательного электродов после электрохимической обработки до 1.6 В стал радикально различаться между собой.
– Установлено, что скорость саморазряда через ~70 мин после его начала пропорционален напряжению заряда. Зависимость же скорости саморазряда через 2000 мин после его начала от напряжения имеет минимум. Этот минимум объясняется действием двух противонаправленных механизмов. Во-первых, существенный вклад в емкость вносит псевдоемкость фарадеевских редокс-реакций ФГ, а во-вторых, само наличие этих групп увеличивает скорость саморазряда. В области низких напряжений доминирует первый фактор, а в области высоких напряжений – второй фактор.
Следует отметить сходства и различия между саморазрядом ЭХСК с водными и неводными электролитами. Ряд механизмов саморазряда в той или иной степени присущ ЭХСК с обоими этими типами электролитов, однако, один из основных механизмов – саморазряд, вследствие челночного переноса ионов переменной валентности с одного электрода на другой и обратно в неводных электролитах играет намного меньшую роль по сравнению с водными электролитами вследствие существенно меньшей растворимости ионов в неводных электролитах. Это проявляется, в частности, в очень малом саморазряде для ряда коммерческих ЭХСК с неводными электролитами.
Список литературы
Conway, B., Electrochemical Supercapacitors: Scientific Fundamentals and Technological Applications, Berlin: Springer Science & Business Media, 2013.
Bagotsky, V.S., Skundin, A.M., and Volfkovich, Yu.M., Electrochemical Power Sources. Batteries, Fuel Cells, Supercapacitors, N.J.: Jhon Wiely & Sons Inc. Publisher, 2015.
Volfkovich, Yu.M., Bograchev, D.A., Rychagov, A.Yu., Sosenkin, V.E., and Chaika, M.Yu., Supercapacitor carbon electrodes with high capacitance, J. Solid State Electrochem., 2015, vol. 19, p. 1.
Oren, Y., Capacitive deionization (CDI) for desalination and water treatment–past, present and future (a Review), Desalination, 2008, vol. 228, p. 10.
Вольфкович, Ю.М., Электрохимические суперконденсаторы (обзор). Электрохимия. 2021. Т. 57. С. 197. [Volfkovich, Yu. M., Electrochemical Supercapacitors (a Review), Russ. J. Electrochem., 2021, vol. 57, p. 311.]
Вольфкович, Ю.М, Сердюк, Т.М. Электрохимические конденсаторы. Электрохимия. 2002. Т. 38. С. 1043. [Volfkovich, Yu.M. and Serdyuk, T.M., Electrochemical capacitors, Russ. J. Electrochem., 2002, vol. 38, p. 935.]
Fic, K., Meller, M., Menzel, J., and Frackowiak, E., Specific carbon/iodide interactions in electrochemical capacitors monitored by EQCM technique, Electrochim. Acta, 2016, vol. 206, p. 496.
Yang, X., Fei, B., Ma, J., Liu, L., Liu, X., Yang, S., Tian, G., Jiang, Z., Yang, S., Tian, G., and Jiang, Z., Porous nanoplatelets wrapped carbon aerogels by pyrolysis of regenerated bamboo cellulose aerogels as supercapacitor electrodes, Carbohydrate Polymers, 2018, vol. 180, p. 385.
Kowal, J., Avaroglu, E., Chamekh, F., and Šenfelds, A., Detailed analysis of the self-discharge of supercapacitors, J. Power Sources, 2011, vol. 196, p.573.
Diab, Y., Venet, P., Gualous, H., and Rojat, G., Self-discharge characterization and modeling of electrochemical capacitor used for power electronics, IEEE Transactions on Power Electronics, 2008, vol. 24, p. 510.
Kurzweil, P. and Shamonin, M., State-of-charge monitoring by impedance spectroscopy during long-term self-discharge of supercapacitors and Lithium-Ion batteries, Batteries, 2018, vol. 4, p. 35.
Liu, K., Yu, C., Guo, W., Ni, L., Yu, J., Xie, Y., and Wang, Z., Recent research advances of self-discharge in supercapacitors: Mechanisms and suppressing strategies, J. Energy, 2021, vol. 58, p. 94.
Tevi, T., Yaghoubi, H., Wang, J., and Takshi, A., Understanding performance limitation and suppression of leakage current or self-discharge in electrochemical capacitors: a review, J. Power Sources, 2013, vol. 241, p. 586.
Shen, J.F., He, Y.J., and Ma, Z.F., A systematical evaluation of polynomial based equivalent circuit model for charge redistribution dominated self-discharge process in supercapacitors, J. Power Sources, 2016, vol. 303, p. 294.
Saha, P. and Khanra, M., Equivalent circuit model of supercapacitor for self-discharge analysis. comparative study. 2016. Internat. Conf. on Signal, India. https://doi.org/10.1109/SCOPES.2016.7955667
Brouji, H.E., Vinassa, J.M., and Briat, O., Ultracapacitors self discharge modelling using a physical description of porous electrode impedance. IEEE 2008, Vehicle Power and Propulsion Conf. IEEE. Harbin, China. https://doi.org/10.1109/VPPC.2008.4677493
Bamgbopa, M.O., Belaineh, D., Mengistie, D.A., Edberg, J., Engquist, I., Berggren, M., and Tybrandt, K., Modelling of heterogeneous ion transport in conducting polymer supercapacitors, J. Mater. Chem. A, 2021, vol. 9, p. 2184.
Rizoug, N. and Bartholomeus, P., Modeling and characterizing supercapacitors using an online method, IEEE Transactions on Industrial Electronics, 2010, vol. 57, p. 3980.
Huang, M., Wu, M. Qiu, Z., Fan, L., Lin, J., and Lin, Y., A redox-mediator-doped gel polymer electrolyte applied in quasi-solid-state supercapacitors, J. Appl. Polym. Sci., 2014, vol. 131, p. 39784.
Wang, H., Zhou, Q., Yao, D., and Ma, H., Suppressing the Self-Discharge of Supercapacitors by Modifying Separators with an Ionic Polyelectrolyte, Adv. Mater. Interfaces, 2018, vol. 5, p. 1701547.
Ricketts, B.W. and Ton-That, C., Self-discharge of carbon-based supercapacitors with organic electrolytes, J. Power Sources, 2000, vol. 89, p. 64.
Ceraolo, M. and Lutzemberger, G., State-of-charge evaluation of supercapacitors, J. Energy Storage, 2017, vol. 11, p. 211.
Yang, H. and Zhang, Y., Ammonia and related chemicals as potential indirect hydrogen storage materials, J. Power Sources, 2011, vol. 196, p. 8173.
Davis, M.A. and Andreas, H.A., Identification and isolation of carbon oxidation and charge redistribution as self-discharge mechanisms in reduced graphene oxide electrochemical capacitor, Carbon, 2018, vol. 139, p. 299.
Oickle, A.M., Tom, J., and Andreas, H.A., Carbon oxidation and its influence on self-discharge in aqueous electrochemical capacitors, Carbon, 2016, vol. 110, p. 232.
Okhay, O., Tkach, A., Staiti, P., and Lufrano, F., Long term durability of solid-state supercapacitor based on reduced graphene oxide aerogel and carbon nanotubes composite electrodes, Electrochim. Acta, 2020, vol. 353, p. 136540.
Andreas, H.A., Black, J.M., and Oickle, A.A., Self-discharge in manganese oxide electrochemical capacitor electrodes in aqueous electrolytes with comparisons to faradaic and charge redistribution models, Electrochim. Acta, 2014, vol. 140, p. 116.
Yumak, T., Bragg, D., and Sabolsky, E.M., Cost-effective synthesis of NiCo2O4@nitrogen-doped carbon nanocomposite using waste PET plastics for high-performance supercapacitor, Appl. Surface Sci., 2019, vol. 469, p. 983.
Rafik, F., Gualous, H., Gallay, R., and Crausaz, A., Frequency, thermal and voltage supercapacitor characterization and modeling, J. Power Sources, 2007, vol. 165, p. 928.
Kazaryan, S.A., Litvinenko, S.V., and Kharisov, G.G., Self-discharge of heterogeneous electrochemical supercapacitor of PbO2|H2SO4|C related to manganese and titanium ions, J. Electrochem. Soc., 2008, vol. 155, p. A464.
Xia, M., Nie, J., Zhang, Z., Lu, X., and Wang, Z.L., Facile and fast synthesis of SnO2 quantum dots for high performance solid-state asymmetric supercapacitor, J. Power Sources, 2018, vol. 47, p. 43.
Zhang, Q., Cai, C., Qin, J., and Wei, B., Tunable self-discharge process of carbon nanotube based supercapacitors, Nano Energy, 2014, vol. 4, p. 14.
Miniguano, H., Barrado, A., Fernández, C., Zumel, P., and Lázaro, A., A general parameter identification procedure used for the comparative study of supercapacitors models, Energies, 2019, vol. 12, p. 1.
Subramanian, S., Johny, M.A., Neelanchery, M.M., and Ansari, S., Self-discharge and voltage recovery in graphene supercapacitors, IEEE Transactions on Power Electronics, 2018, vol. 33, p. 10410.
Yun, J., Kim, D., Lee, G., and Ha, J.S., All-solid-state flexible micro-supercapacitor arrays with patterned graphene/MWNT electrodes, Carbon, 2014, vol. 79, p. 156.
Satpathy, S., Dhar, M., and Bhattacharyya, B.K., Why supercapacitor follows complex time-dependent power law and does not obey normal exponential (e–t(RC)) rule? J. Energy Storage, 2020, vol. 31, p. 101606.
Schneuwly, A. and Gallay, R., Properties and applications of supercapacitors from the state-of-the-art to future trends, Proceeding PCIM, 2000, vol. 2, p. 1.
Ghanbari, T., Moshksar, E., Hamedi, S., Rezaei, F., and Hosseini, Z., Self-discharge modeling of supercapacitors using an optimal time-domain based approach, J. Power Sources, 2021, vol. 495, p. 229787.
Musolino,V., Piegari, L., Tironi, E., A comparative study of a PEMFC, Battery, Super-capacitor based energy source owing to hybrid vehicle, IEEE Transactions on Industrial Electronics, 2012, vol. 60, p. 112.
Kaus, M., Kowal, J., and Sauer, D.U., Modelling the effects of charge redistribution during self-discharge of supercapacitors, Electrochim. Acta, 2010, vol. 55, p. 7516.
Tevi, T. and Takshi, A., Modeling and simulation study of the self-discharge in supercapacitors in presence of a blocking layer, J. Power Sources, 2015, vol. 273, p. 857.
Haque, M., Li, Q., Smith, A.D., and Kuzmenko, V., Self-discharge and leakage current mitigation of neutral aqueous-based supercapacitor by means of liquid crystal additive, J. Power Sources, 2020, vol. 453, p. 227897.
Liu, M., Xia, M., Qi, R., Ma, Q., Zhao, M., and Zhang, Z., Lyotropic Liquid Crystal as an Electrolyte Additive for Suppressing Self-Discharge of Supercapacitors, ChemElectrochem., 2019, vol. 6, p. 2531.
Chung, J., Park, H., and Jung, C., Electropolymerizable isocyanate-based electrolytic additive to mitigate diffusion-controlled self-discharge for highly stable and capacitive activated carbon supercapacitors, Electrochim. Acta, 2021, vol. 369, p. 137698.
Ge, K. and Liu, G., Suppression of self-discharge in solid-state supercapacitors using a zwitterionic gel electrolyte, Chem. Commun., 2019, vol. 55, p. 7167.
Mishra, R.K., Choi, G.J., Sohn, Y., Lee, S.H., and Gwag, J.S., Reduced graphene oxide based supercapacitors: Study of self-discharge mechanisms, leakage current and stability via voltage holding tests, Mater. Letters, 2019, vol. 253, p. 250.
Paleo, A.J., Stait, P., Brigandì, A., Ferreira, F.N., Rocha, A.M., and Lufrano, F., Supercapacitors based on AC/MnO2 deposited onto dip-coated carbon nanofiber cotton fabric electrodes, Energy Storage Materials, 2018, vol. 12, p. 204.
Hosseini, M.G., Rasouli, H., Shahryari, E., and Naji, L., Electrochemical behavior of a Nafion-membrane-based solid-state supercapacitor with a graphene oxide—multiwalled carbon nanotube–polypyrrole, J. Appl. Polym. Sci., 2017, vol. 13, p. 44926.
Łatoszynska, A.A., Taberna, P. Simon, P., and Wieczorek, W., Plasticized polymer blend electrolyte based on chitosan for energy storage application: Structural, circuit modeling, morphological and electrochemical properties, Electrochim. Acta, 2017, vol. 242, p. 31.
Li, J. Qiao, J., and Lian, K., Hydroxide ion conducting polymer electrolytes and their applications in solid supercapacitors: a review, Energy Storage Materials, 2020, vol. 24, p. 6.
Liu, K., Yu, C., Guo, W., Ni, L., Yu, J., Xie, Y., and Wang, Z., Recent research advances of self-discharge in supercapacitors: Mechanisms and suppressing strategies, J. Energy Chemistry, 2021, vol. 58, p. 94.
Shen, J.F., He, Y.J., and Ma, Z.F., A systematical evaluation of polynomial based equivalent circuit model for charge redistribution dominated self-discharge process in supercapacitors, J. Power Sources, 2016, vol. 303, p. 294.
Zhongxue, L.I. and Fu, W., Diagnostic identification of self-discharge mechanisms for carbon-based supercapacitors with high energy density. IEEE 2011. Asia-Pacific Power and Energy Engineering Conf. (APPEEC). https://doi.org/10. 1109/APPEEC. 2011. 5748403
Volfkovich, Yu.M., Rychagov, A.Yu., Mikhalin, A.A., Sosenkin, V.E., Kabachkov, E.N., Shulga, Yu.M., and Michtchenko, A., Self-discharge of a supercapacitor with electrodes based on activated carbon cloth, J. Electroanal. Chem., 2022, vol. 910, p. 116198.
Shulga, Yu.M., Baskakov, S.A., Baskakova, Yu.V., Lobach, A.S., Kabachkov, E.N., Volfkovich, Yu.M., Sosenkin, V.E., Shulga, N.Yu., Nefedkin, S.I., Kumar, Y., and Michtchenko, A., J. Alloys and Compounds, 2018, vol. 730, p. 88.
Shulga, Yu.M., Baskakov, S.A., Baskakova, Yu.V., Lobach, A.S., Volfkovich, Yu.M., Sosenkin, V.E., Shulga, N.Yu., Parkhomenko, Y.N., Michtchenko, A., and Kumar, Y., Microporous and Mesoporous Materials, 2017, vol. 245, p. 24.
Дополнительные материалы отсутствуют.




