Журнал аналитической химии, 2020, T. 75, № 5, стр. 449-457
Применение пьезоэлектронного носа для оценки состояния дыхательной системы у телят по легколетучим соединениям
Т. А. Кучменко a, А. А. Шуба a, *, Р. У. Умарханов a, Е. В. Дроздова a, А. Е. Черницкий b
a Воронежский государственный университет инженерных технологий,
факультет экологии и химической технологии
394000 Воронеж, просп. Революции, 19, Россия
b Всероссийский научно-исследовательский ветеринарный институт патологии,
фармакологии и терапии
394087 Воронеж, ул. Ломоносова, 114Б, Россия
* E-mail: an-mishina@yandex.ru
Поступила в редакцию 29.01.2019
После доработки 22.03.2019
Принята к публикации 02.12.2019
Аннотация
Обсуждаются выбор и применение массива пьезосенсоров для оценки состояния органов дыхания у телят по составу равновесной газовой фазы над конденсатом выдыхаемого воздуха. Рассмотрена взаимосвязь между выходными регистрируемыми, расчетными данными массива сенсоров и состоянием дыхательной системы животного, установленным по результатам клинических и лабораторных исследований. Описаны особенности химического состава равновесной газовой фазы над пробами конденсата выдыхаемого воздуха в норме и при воспалениях. Полученные результаты позволяют рекомендовать массив пьезосенсоров с выбранными модификаторами, регистрируемые и расчетные параметры “электронного носа” для разработки способа экспресс-диагностики воспалительных заболеваний органов дыхания у телят по составу легколетучей фракции конденсата выдыхаемого воздуха.
Современным направлением диагностики является определение ранних маркеров, предшествующих развитию клинических признаков заболевания, для повышения эффективности профилактических и лечебных мероприятий. В ветеринарной медицине наибольшую сложность представляет диагностика воспалительных заболеваний органов дыхания (ВЗОД) у телят [1]. Клиническое проявление и характер патологоанатомических изменений при ВЗОД различной этиологии у телят первого месяца жизни часто однотипны независимо от вызвавшего болезнь возбудителя [1]. Традиционные гематологические и биохимические маркеры воспаления, такие как изменения лейкограммы, скорости оседания эритроцитов, повышение концентрации белков острой фазы в сыворотке крови, для ранней диагностики ВЗОД у телят оказываются малоинформативными в силу их неспецифичности [2]. Актуальным направлением в диагностике является разработка и применение неинвазивных способов, которые позволяют безболезненно и быстро проводить процедуру обследования, оценивать состояние органов дыхания и при необходимости корректировать профилактические и лечебные мероприятия.
Выдыхаемый воздух у телят насыщен водяными парами, которые могут быть конденсированы при охлаждении. Помимо водяных паров, конденсат выдыхаемого воздуха (КВВ) содержит целый ряд соединений различной природы: пептиды, жирные кислоты, углеводы, макро- и микроэлементы и др., которые в виде аэрозоля переносятся из нижних отделов респираторного тракта при дыхании. Изменения состава КВВ у телят, отражающие нарушения в работе легких, возникают уже при угрозе развития ВЗОД [1, 2]. Показано, что химический состав КВВ коррелирует с состоянием дыхательной системы и течением заболевания (хроническое, острое) [1], поэтому диагностика ВЗОД по составу КВВ у телят представляет особый научный и практический интерес. Однако концентрации веществ, которые содержатся в КВВ у телят и характеризуют различные параметры состояния дыхательной системы, чрезвычайно малы и не всегда могут быть выявлены традиционными лабораторными тестами.
Известно, что возможно уловить небольшие различия в составе проб и малые содержания легколетучих веществ сенсорными системами типа “электронный нос”, в том числе на основе модифицированных пьезокварцевых резонаторов [3]. Это позволило поставить задачу применения массива сенсоров для ранжирования проб конденсата выдыхаемого воздуха по результатам анализа равновесной газовой фазы (РГФ) над ними.
Цель исследования – выбрать массив пьезосенсоров, потенциально информативные качественные, количественные характеристики из матрицы данных “электронного носа” для установления значимых различий в составе РГФ над пробами конденсата выдыхаемого воздуха телят и ранжирования их на группы по наличию и характеру течения ВЗОД.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
В качестве объектов исследования выбраны пробы конденсата выдыхаемого воздуха телят, как условно здоровых, так и с субклиническим и острым течением ВЗОД, замороженные в жидком азоте (табл. 1). Конденсат выделяемого воздуха у телят (n = 6) собирали в утренние часы до кормления с помощью специального устройства [4]. Во время процедуры сбора КВВ учитывали объем выдыхаемого теленком воздуха. Сразу после сбора пробы КВВ замораживали и хранили до проведения исследований в жидком азоте при –196°C. Всех телят подвергали детальному клиническому исследованию с обязательным лабораторным контролем во Всероссийском научно-исследовательском ветеринарном институте патологии, фармакологии и терапии: проводили бактериологические и молекулярно-генетические (ПЦР) исследования носовых и трахеальных смывов, определяли гематологические (лейкограмма) показатели воспаления в крови и КВВ (концентрация малонового альдегида, уровень pH) [2]. Состояние телят при ВЗОД оценивали по балльной системе, разработанной в Университете Висконсин-Мэдисон (США) [5]. Размораживание пробирок проводили при комнатной температуре в емкостях с притертыми полистирольными крышками в течение 2 ч. Размороженные пробы перед анализом выдерживали при температуре 20 ± 1°С в течение 30 мин.
Таблица 1.
Вещества-маркеры в выдыхаемом воздухе и его конденсате при патологических процессах дыхательной системы и рекомендованные покрытия сенсоров
| Патология органов дыхания | Вещества-маркеры в выдыхаемом воздухе или его конденсате | Рекомендованные чувствительные покрытия для сенсоров |
|---|---|---|
| Хроническая обструктивная болезнь легких | 2-Гидроксиизомасляная кислота, ацетогидроксибутановая кислота, пиридин [12] | Tween, ДЦГ18К6 [18] |
| Воспаление | Этан, пентан, СО, NO, Н2О2, этилен, изопрен, альдегиды [13–15] | МУНТ, ПЭГ-2000 [19, 20] |
| Бактериальная обсемененность | Этанол, метанол, ароматические соединения, цианиды, карбоновые кислоты [15–17] | ПЭГ-2000, ПДЭГС, MO [19, 21, 22] |
| Деструктивные процессы в тканях | CS2, серосодержащие соединения, алкиламины [14, 15, 17] | ТХ-100, ПДЭГС, БКС [8, 21–24] |
Исследовали состав равновесной газовой фазы над конденсатом объемом 3 мл при 20 ± 1°C в статическом режиме на анализаторе газов МАГ-8 с массивом из восьми разноселективных пьезосенсоров (ООО ‘СНТ’, Россия). Фиксировали выходные сигналы пьезосенсоров – относительные изменения частоты колебания каждого пьезосенсора (ΔFi, Гц) во времени с шагом в 1 с в виде хроночастотограмм, аналитические сигналы (ΔFmax,i, Гц) в программном обеспечении МАG-Soft [6].
В качестве селективных покрытий пьезокварцевых резонаторов (ПКР) (ОАО “Пьезо”, Москва, базовая частота 10.0 МГц) для создания сенсоров выбрали фазы, формирующие на электродах ПКР стабильные пленки, обеспечивающие низкий уровень шумов пьезосенсоров, в том числе: полиэтиленгликоль ПЭГ-2000 (ПЭГ-2000 – сенсор 1), дициклогексано-18-краун-6 (ДЦГ18К6 – сенсор 2), метиловый оранжевый (МО – сенсор 3), тритон Х-100 (ТХ-100 – сенсор 4), бромкрезоловый синий (БКС – сенсор 5), многостенные углеродные нанотрубки, карбоксилированные азотной кислотой (МУНТ – сенсор 6), полидиэтиленгликоль сукцинат (ПДЭГС – сенсор 7), Tween 40 (Tween – сенсор 8). Все фазы производства компании “Alfa Aesar” (США). Пьезосенсоры изготавливали по описанной ранее методике [7]. Для стабилизации неполимерных реагентов применяли подложку из МУНТ массой 1–2 мкг. МУНТ синтезировали в Институте особо чистых материалов (Черноголовка) [8].
Для оценки постоянства состава РГФ над пробами КВВ применяли расчeтные параметры :
1) параметр эффективности сорбции $A_{{ij}}^{{\max }}$ [9]:
(1)
$A_{{ij}}^{{\max }} = {{\Delta {{F}_{{{\text{max}},i}}}} \mathord{\left/ {\vphantom {{\Delta {{F}_{{{\text{max}},i}}}} {\Delta {{F}_{{{\text{max}},j}}}}}} \right. \kern-0em} {\Delta {{F}_{{{\text{max}},j}}}}},$2) параметры интегрального аналитического сигнала массива сенсоров – фигуры “визуальных отпечатков” максимальных откликов [10]: minj, характеризующий соотношение проекций сигналов сенсоров с пленками i и n на сигнал сенсора с пленкой j, и αinj – угол между этими проекциями, выраженный в радианах, которые рассчитывали по формулам:
(2)
${{m}_{{inj}}} = \frac{{\sqrt {\Delta F_{{\max ,i}}^{2} + \Delta F_{{\max ,j}}^{2} - \Delta {{F}_{{\max ,i}}}\Delta {{F}_{{\max ,j}}}\sqrt 2 } }}{{\sqrt {\Delta F_{{\max ,j}}^{2} + \Delta F_{{\max ,n}}^{2} - \Delta {{F}_{{\max ,j}}}\Delta {{F}_{{\max ,n}}}\sqrt 2 } }},$(3)
$\begin{gathered} {{\alpha }_{{inj}}} = \\ = \arcsin \left( {\frac{{\Delta {{F}_{{\max ,i}}}\sqrt 2 }}{{2\sqrt {\Delta F_{{\max ,i}}^{2} + \Delta F_{{\max ,j}}^{2}} - \Delta {{F}_{{\max ,i}}}\Delta {{F}_{{\max ,j}}}\sqrt 2 }}} \right) + \\ + \,\arcsin \left( {\frac{{\Delta {{F}_{{\max ,n}}}\sqrt 2 }}{{2\sqrt {\Delta F_{{\max ,j}}^{2} + \Delta F_{{\max ,n}}^{2}} - \Delta {{F}_{{\max ,j}}}\Delta {{F}_{{\max ,n}}}\sqrt 2 }}} \right), \\ \end{gathered} $Для оценки степени идентичности двух наборов расчетных параметров, соответствующих откликам сенсоров для проб от условно здорового животного и из других диагностических групп, применяли параметр подобия δ [11], рассчитываемый в Excel. Для расчетов и построений типичных “визуальных отпечатков” применяли статистически надежные средние значения откликов сенсоров (n = 3, P = 0.95).
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Первым важным этапом при разработке подхода для анализа различных биопроб химическими пьезосенсорами является выбор чувствительных пленок измерительных элементов, позволяющих количественно увидеть различие в составе и малых концентрациях легколетучих соединений (ЛЛС) в РГФ над биопробами. Для этого путем анализа литературы определили вещества-маркеры (биомаркеры) в выдыхаемом воздухе или конденсате, характерные для патологических процессов в органах дыхания (табл. 1). Данные биомаркеры не являются строго специфичными для дыхательной системы, однако заметное повышение их концентрации в выдыхаемом воздухе (до уровня 10–100 ppb) связано в основном с патологией органов дыхания. Накопленные нашей научной группой результаты по сорбции различных классов ЛЛС на тонких пленках и покрытиях сорбционных фаз разной природы позволяют рекомендовать сорбенты для создания химических пьезосенсоров (табл. 1). Ранее неоднократно обсуждались селективность, чувствительность сенсоров с пленками хроматографических фаз и индикаторов. Совместное применение нескольких сенсоров без разделения смесей паров не обеспечивает изменения избирательности по сигналам сенсоров. Более того, методология “электронных носов”, напротив, принципиально отличается от других подходов в мультисенсорных системах (глаз, язык) неопределенностью этих традиционных характеристик. Решение задачи селективного микровзвешивания на относительно неселективных пленках успешно решается применением идентификационных параметров. Именно экстремальные значения параметров в выборке соединений обеспечивают их распознавание в смесях. Полученный массив сенсоров позволяет с высокой чувствительностью сорбировать различные классы летучих веществ, включая биомаркеры заболеваний органов дыхания, и следовательно, должен быть эффективен для решения поставленной задачи.
Для оценки стабильности работы пьезосенсоров и погрешности детектирования в закрытой ячейке использовали подход на основе карт Шухарта [25, 26]. Стабильность оценивали по откликам сенсора с пленкой Tween в парах РГФ над раствором уксусной кислоты с концентрацией 0.5 об. % (n = 30), так как ранее установлено, что данное покрытие проявляет наибольшую чувствительность к парам кислот и наименее устойчиво по дрейфу базовой линии из предложенного массива сенсоров. На первом этапе проверяли гипотезу о нормальном распределении значений откликов пьезосенсоров в выборках при помощи критерия согласия χ2 Пирсона [25, 26]. Проверку нормальности закона распределения проводили на уровне значимости α = 0.1. Установлено, что выборка значений отклика сенсора подчиняется нормальному распределению в парах уксусной кислоты небольших концентраций, поэтому для оценки стабильности работы измерительных элементов массива “электронного носа” использовали контрольные карты Шухарта среднего и выборочных стандартных отклонений при детектировании паров уксусной кислоты [24, 25].
Построение и анализ контрольных карт позволяет сделать вывод, что пьезосенсоры с пленкой Tween при микровзвешивании паров уксусной кислоты работают стабильно. Погрешность измерения в закрытой ячейке детектирования не превышает 10%, при этом на долю прибора (электрические схемы) приходится до 2%.
Выбранный массив сенсоров применили для оценки состояния дыхательной системы у 6 телят по составу летучих соединений КВВ. Регистрируемые и расчетные параметры массива сенсоров “электронного носа” сравнивали с клинико-физиологическим статусом, установленным традиционным методом анализа. По результатам клинических и лабораторных исследований телят разделили на 3 группы: 1) “здоровые со стороны дыхательной системы” – группа I, 2) “с клиническими признаками поражения органов дыхания” – острый бронхит и бронхопневмония – группа II, 3) “с субклиническим течением ВЗОД” – субклинический бронхит и трахеобронхит – группа III. Результаты клинических и лабораторных исследований телят представлены в табл. 2.
Таблица 2.
Результаты биохимического анализа проб конденсата выдыхаемого воздуха и крови исследуемых телят
| Группа телят | “Здоровые со стороны дыхательной системы” | “С субклиническим течением ВЗОД” | “С клиническими признаками поражения органов дыхания” | |||
|---|---|---|---|---|---|---|
| Номер пробы | 1 | 2 | 5 | 6 | 3 | 4 |
| Клиническая оценка состояния телят, баллы | 0 | 1.0 | 2.0 | 5.0 | 10.0 | 8.0 |
| Температура, °С | 38.8 | 39.0 | 38.9 | 39.6 | 40.5 | 39.0 |
| Дыхательный объем, мл | 587 | 409 | 624 | 633 | 271 | 296 |
| Гематологические признаки воспаления | –* | – | + | – | + | + |
| Микробиоценоз верхних дыхательных путей | – | Геном патогенных микоплазм | E. coli O26, O8; Ent. faecalis; Asp. flavus; аденовирус |
Ent. faecalis; Penicillium spp.; Asp. fumigatus; геном патогенных микоплазм | ||
| Малоновый диальдегид в ВВ, нМ/100 л ВВ | 0.121 | 0.084 | 0.210 | 0.180 | 0.251 | 0.390 |
| рН КВВ | 7.35 | 7.32 | 7.34 | 7.58 | 7.63 | 7.66 |
| Общие Ig, г/л | 19.3 | 19.2 | 19.6 | 18.5 | 25.7 | 30.0 |
Рассмотрим взаимосвязь выходных данных массива сенсоров с диагностическим статусом телят по ранее предложенному подходу “от простого к сложному”, определяемому сложностью их обработки [27].
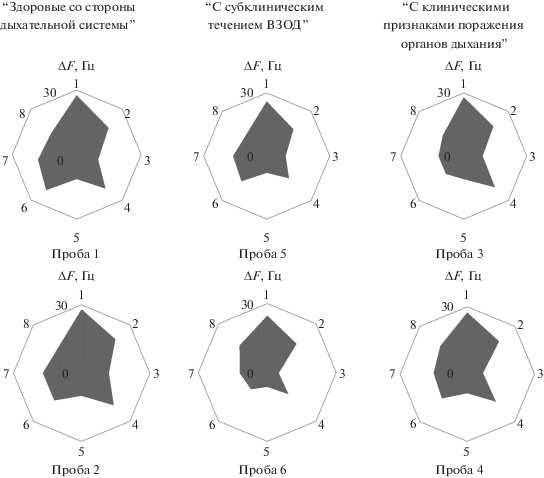
Первичной аналитической информацией, получаемой при анализе пробы с применением массива сенсоров, являются максимальные сигналы сенсоров и “визуальные отпечатки”, построенные по ним. Известно, что форма “визуального отпечатка” определяется качественным составом летучей фракции пробы и соотношением концентраций различных классов соединений, а сравнение абсолютных сигналов сенсоров позволяет оценить долю различных веществ в пробе. На первом уровне обработки данных были получены “визуальные отпечатки” максимальных сигналов сенсоров в равновесной газовой фазе над пробами КВВ (рис. 1). Установлено, что форма “визуальных отпечатков” максимальных сигналов сенсоров отличается незначительно для всех проб, однако можно выделить особенности, характерные для каждой диагностической группы. Для группы I “здоровы со стороны дыхательной системы” максимальные значения откликов характерны для сенсоров с пленками ПЭГ-2000 и ДЦГ18К6, что свидетельствует о наличии в РГФ над пробами КВВ здоровых животных паров воды и легких полярных кислородсодержащих веществ. Наибольшие значения откликов также характерны для сенсора с покрытием из МУНТ, что связано с большим содержанием легких газов в КВВ здоровых телят при интенсивном легочном обмене. В группе II “с клиническими признаками поражения органов дыхания” отмечается значительное увеличение сигналов для сенсора с пленкой ТХ-100, что указывает на увеличение в пробах общего содержания летучих веществ, особенно гетероатомных. Для этой группы при остром течении ВЗОД характерно, согласно исследованиям [15], накопление альдегидов, насыщенных углеводородов, тиолов, что отражает изменение откликов этого сенсора. При этом уменьшаются сигналы сенсоров с пленками БКС и ПДЭГС, что указывает на уменьшение содержания летучих аминов в пробах КВВ для телят с острым течением заболевания. Это указывает на явное преобладание в РГФ метаболитов патогенной микрофлоры, что доказывается присутствием в пробах по результатам микробиологических исследований энтерококков и патогенных грибов (табл. 2). Для проб КВВ от телят из группы III “с субклиническим течением ВЗОД” характерны более значительные различия в форме “визуальных отпечатков” максимальных сигналов сенсоров, при этом проба 5 может быть отнесена к группе условно здоровых животных, а проба 6 к группе больных. Это связано с различным состоянием телят из этой группы, при этом по результатам лабораторных испытаний проба 5 ближе к пробам из группы I, так как по клиническому осмотру у животного наблюдаются незначительные отклонения от нормы. По клиническим признакам животное, у которого отобрана проба 6, относится к группе II. А микробиологические показатели биопроб для этого животного обнаруживают умеренной рост патогенной микрофлоры. Таким образом, в группу III объединены пробы, значительно отличающиеся друг от друга по клиническим и лабораторным показателям, с возможностью самопроизвольного перехода из субклинического состояния к выздоровлению (проба 5) или острому течению ВЗОД (проба 6). Для пробы 6, помимо сигналов сенсоров с пленками ПЭГ-2000, ДЦГ18К6, значителен отклик сенсора с пленкой Tween, что указывает на увеличение содержания в РГФ веществ с кислотными свойствами при прогрессировании заболевания [13].
Рис. 1.
“Визуальные отпечатки” максимальных сигналов сенсоров в равновесной газовой фазе над пробами конденсата выдыхаемого воздуха. По кругу указаны номера сенсоров в массиве. По радиальным осям отложены сигналы сенсоров в диапазоне 0–30 Гц.
Для более детальной оценки постоянства состава РГФ над пробами КВВ и соотношения в них отдельных групп соединений рассчитывали параметры сорбции по формулам (1)–(3) (второй уровень обработки данных), наиболее простым из которых является параметр эффективности сорбции $A_{{ij}}^{{{\text{max}}}}.$ Из всех возможных параметров $A_{{ij}}^{{{\text{max}}}}$ в табл. 3 представлены только те, которые позволяют дифференцировать пробы телят из группы I от проб из группы II.
Таблица 3.
Параметры эффективности сорбции $A_{{ij}}^{{{\text{max}}}}$ (±0.02) для проб конденсата выдыхаемого воздуха
| $A_{{ij}}^{{{\text{max}}}}$ | “Здоровые со стороны дыхательной системы” | “С клиническими признаками поражения органов дыхания” | “С субклиническим течением ВЗОД” | Идентифицируемые вещества/значение параметра $A_{{ij}}^{{{\text{max}}}}$ ± d (критерий совпадения) [9] | |||
|---|---|---|---|---|---|---|---|
| 1 | 2 | 3 | 4 | 5 | 6 | ||
| $A_{{14}}^{{{\text{max}}}}$ (∆F(ПЭГ 2000)/∆F(ТХ-100)) | 2.0 | 1.8 | 1.6* | 1.9 | 2.4 | 2.8 | Диэтиламин/1.5 ± 0.2 |
| $A_{{16}}^{{{\text{max}}}}$ (∆F(ПЭГ 2000)/∆F(МУНТ)) | 2.0 | 2.3 | 4.0 | 2.5 | 2.2 | 2.3 | Алифатические амины/0.3 ± 0.2 |
| $A_{{17}}^{{{\text{max}}}}$ (∆F(ПЭГ 2000)/∆F(ПДЭГС)) | 1.7 | 1.6 | 2.3 | 1.8 | 1.6 | 2.1 | Аммиак/0.2 ± 0.1 |
| $A_{{35}}^{{{\text{max}}}}$∆F(МО)/∆F(БКС)) | 1.4 | 1.5 | 0.9 | 1.0 | 1.5 | 1.3 | – |
| $A_{{68}}^{{{\text{max}}}}$ (∆F(МУНТ)/∆F(Tween) | 0.9 | 0.8 | 0.5 | 0.6 | 0.9 | 0.6 | Этанол/0.6 ± 0.1 |
Установлено, что для параметров $A_{{14}}^{{{\text{max}}}}$ наибольшие значения характерны для проб из группы III “с субклиническим течением ВЗОД” (табл. 3), что указывает на преобладание в газовой фазе над пробами КВВ полярных кислородсодержащих веществ по сравнению с полярными гетероатомными соединениями. По параметрам $A_{{16}}^{{{\text{max}}}},$ $A_{{17}}^{{{\text{max}}}}$ у телят из группы “с клиническими признаками поражения органов дыхания” в РГФ над пробами КВВ содержание спиртов, альдегидов, кетонов больше, чем легких газов и летучих аминов. Также для этой группы характерно меньшее содержание ароматических и алифатических аминов, аммиака, чем летучих органических кислот в РГФ над пробами КВВ по параметрам $A_{{35}}^{{{\text{max}}}},$ $A_{{68}}^{{{\text{max}}}}.$ Ранее установлено, что параметры $A_{{ij}}^{{{\text{max}}}}$ при определенных условиях являются идентификационными для ЛЛС [8]. По установленным ранее идентификационным параметрам $A_{{ij}}^{{{\text{max}}}}$ [9] в РГФ над пробами КВВ от телят из группы II “с клиническими признаками поражения органов дыхания” идентифицированы диэтиламин и этанол, которые являются биомаркерами наличия патогенных микроорганизмов и деструктивных процессов в тканях (табл. 1).
Выделять отдельно разные диагностические группы только по параметрам $A_{{ij}}^{{{\text{max}}}}$ ненадежно, поэтому рассчитаны параметры, отражающие особенности геометрии “визуальных отпечатков” максимальных сигналов сенсоров. Данные параметры отражают особенности взаимодействия газов и паров с тремя различными пленками сорбентов одновременно, что позволяет в зависимости от природы пленок использовать их как более специфические интегральные характеристики взаимодействия, выраженные в числовой форме. В табл. 4 представлены только те параметры minj и αinj, которые позволяют по их значениям выделить одну или несколько диагностических групп. Установлено, что параметры m136, m137 для группы телят “здоровые со стороны дыхательной системы” принимают наименьшие значения, поэтому можно предположить незначительное преобладание в РГФ над пробами полярных соединений некислотной природы по сравнению с аминами и легкими газами. Для группы телят “с клиническими признаками поражения органов дыхания” параметр m157 имеет наибольшие значения, что связано со значительным преобладанием в РГФ над пробами КВВ спиртов, альдегидов по сравнению с легкими летучими аминами. Увеличение содержания полярных гетероатомных соединений основной природы в РГФ над пробами КВВ характеризует субклиническое течение ВЗОД, что отражается в наибольших значениях параметра m145 (табл. 4).
Таблица 4.
Расчетные параметры особенностей формы “визуальных отпечатков” m и α (±0.02) максимальных сигналов сенсоров для проб конденсата выдыхаемого воздуха
| Группа телят | Номер пробы | m136 | m137 | m145 | m157 | m237 | α126 | α134 | α135 | α234 | α247 | α346 | α347 | α356 | α357 | α358 | α478 | α578 |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| I | 1 | 2.26 | 1.84 | 1.97 | 1.83 | 1.20 | 2.36 | 2.60 | 1.86 | 2.77 | 2.95 | 1.91 | 2.12 | 2.80 | 2.71 | 2.74 | 2.07 | 1.47 |
| 2 | 2.32 | 1.77 | 1.71 | 1.82 | 1.26 | 2.11 | 2.71 | 1.92 | 2.89 | 2.74 | 1.69 | 2.10 | 3.03 | 2.76 | 2.84 | 2.13 | 1.49 | |
| II | 3 | 2.95 | 2.17 | 1.58 | 2.14 | 1.33 | 2.09 | 2.41 | 2.39 | 2.61 | 2.20 | 1.16 | 1.49 | 2.23 | 2.61 | 2.61 | 2.59 | 1.97 |
| 4 | 2.89 | 2.02 | 1.92 | 2.02 | 1.41 | 2.09 | 2.29 | 2.18 | 2.39 | 2.82 | 1.40 | 1.76 | 2.65 | 2.42 | 2.35 | 2.42 | 1.79 | |
| III | 5 | 2.43 | 1.79 | 2.48 | 1.77 | 1.15 | 2.28 | 2.51 | 1.83 | 2.70 | 2.98 | 2.22 | 2.48 | 2.80 | 2.65 | 2.71 | 1.78 | 1.36 |
| 6 | 2.63 | 2.37 | 2.90 | 2.33 | 1.62 | 2.20 | 2.31 | 1.86 | 2.38 | 2.80 | 1.99 | 2.08 | 2.56 | 2.52 | 2.42 | 2.42 | 1.87 |
По максимальным значениям параметров α134, α234 можно выделить группу телят “здоровые со стороны дыхательной системы”. Исходя из геометрического смысла параметра αinj, можно предположить равное содержание в РГФ над пробами КВВ полярных веществ кислотной природы и гетероатомных соединений. По минимальным значениям параметров α346, α347, α356, α357, α358 можно выделить группу телят “с клиническими признаками поражения органов дыхания”, что указывает на преобладание в РГФ над пробами КВВ тяжелых полярных гетероатомных соединений, включая ароматические амины.
Отметим, что значимое разделение всех диагностических групп возможно только по параметрам m136 и α346, так как рассчитанный критерий сравнения Крускала−Уоллиса (Н) для каждого параметра является статистически значимым (Н = 4.571 = Н3, 2, 0.1). Следовательно, сигналы сенсоров с пленками ПЭГ-2000, МО, ТХ-100, МУНТ характеризуются максимальной дифференцирующей способностью при диагностике заболеваний органов дыхания у телят. Однако ранжирование проб по одному из выделенных параметров ненадежно, поэтому для разделения проб на диагностические группы по совокупности рассчитанных параметров применили параметр подобия δ [10], который оценивает степень идентичности двух наборов переменных, характеризует в случае откликов пьезосенсоров близость химического качественного и количественного состава смесей ЛЛС. Чем меньше δ, тем ближе по составу смеси [10].
В качестве стандартной выборки параметров для сравнения взяты данные, полученные для пробы 1, для которой все клинические и лабораторные показатели соответствуют норме, включая отсутствие внутриклеточных патогенов (вирусы, микоплазмы) (табл. 2). Рассчитаны 4 вида параметров подобия δ для наборов данных анализируемых проб. Выбраны наборы: максимальных сигналов сенсоров ΔFmax (δΔF), параметров эффективности сорбции $A_{{ij}}^{{{\text{max}}}}$ (δА), параметров minj (δm) и αinj (δα) (табл. 5).
Таблица 5.
Параметры подобия наборов выходных данных массива сенсоров для равновесной газовой фазы над пробами конденсата выдыхаемого воздуха
| Номер пробы, группа телят | δΔF ± 0.056 | Правильность ранжирования |
δА | Правильность ранжирования |
δm | Правильность ранжирования |
δα | Правильность ранжирования |
|---|---|---|---|---|---|---|---|---|
| 1, I – стандарт | 0 | –* | 0 | – | 0 | – | 0 | – |
| 2, I | 0.028 | + (группа I) | ~0 | + (группа I) | 0.015 | + (группа I) | 0.004 | + (группа I) |
| 5, III | 0.032 | – (группа I) | 0.075 | ± (группа I, III) | 0.049 | ± (группа I, III) | 0.006 | – (группа I) |
| 4, II | 0.104 | – (группа III) | 0.025 | – (группа I) | 0.129 | + (группа II) | 0.036 | + (группа II) |
| 3, II | 0.118 | – (группа III) | 0.162 | + (группа II) | 0.139 | + (группа II) | 0.038 | + (группа II) |
| 6, III | 0.264 | – (группа II) | 0.137 | – (группа II) | 0.294 | – (группа II) | 0.013 | + (группа III) |
Предварительно для наиболее значимо меняющейся регистрируемой величины $\left( {\Delta {{F}_{{{\text{max}}}}}} \right)$ с учетом допустимой вариации откликов сенсоров (±1 Гц) рассчитали отклонение значения параметра подобия ΔδΔF, превышение которого определяет значимое различие в выборке и отнесение пробы к другой диагностической группе. Для аналитического сигнала пьезосенсоров ΔδΔF составляет ±0.056. С учетом этого по величинам δΔF пробы 2–6 отнесены к группам I–III (табл. 5). Кроме выборки для пробы 2, ни для одной пробы не получен верный прогноз клинического состояния. Аналогично проанализированы и ранжированы пробы по наборам расчетных показателей ($А_{{ij}}^{{\max }},$ minj, αinj) (табл. 5).
По величинам параметров подобия δА пробы из группы I (“здоровы со стороны дыхательной системы”) не отличаются друг от друга (табл. 5); ложно к этой группе относится по этому параметру проба 4. Проба 6 также ложно отнесена к группе II, кроме того, неоднозначно принятие решения по состоянию для пробы 5. Параметр δА для малой выборки не позволяет выделить все пробы с тяжелым течением ВЗОД, но он более информативен, чем δΔF.
Наибольшие различия между пробами отражают параметры minj, и наибольшие значения параметров подобия δm характерны при расчете по их наборам (табл. 5). Прогноз состояния по набору параметров minj ложен для пробы 6, которая отнесена к группе II, тем не менее, по результатам лабораторных исследований состояние биопроб от животного 6 соответствует группе больных животных со слабо выраженными клиническими признаками. Аналогичное неустойчивое ранжирование характерно для пробы 5, наиболее близкой к пробам из группы I.
Критерии подобия, рассчитанные по параметрам αinj (δα) характеризуются минимальными значениями (табл. 5), однако их значения увеличиваются в соответствии с нарастанием клинических признаков заболевания. Ложным является отнесение только пробы 5 к группе I. Из всех регистрируемых клинических и лабораторных характеристик для этой пробы завышено содержание лейкоцитов в крови. Только этот параметр не позволил изначально отнести ее к группе I. С учетом этого прогноз и оценка состояния дыхательных путей телят по результатам пьезокварцевого микровзвешивания массивом из восьми сенсоров РГФ над конденсатом выдыхаемого воздуха наиболее предпочтителен по наборам параметров αinj, minj.
С учетом всех параметров отсутствует ошибка при оценке состояния дыхательных путей для пробы 2 (группа I) и минимальна для пробы 3 (группа II), отобранной у теленка с ярко выраженными клиническими и лабораторными (патогенные микроорганизмы) признаками воспаления. Главным ограничением применения параметра подобия для ранжирования по качественным характеристикам состава смесей биомаркеров в РГФ над КВВ является то, что пьезосенсорами детектируются не все соединения из смеси, а лишь те, которые взаимодействуют с пленками сорбентов.
Для проверки предлагаемого подхода дополнительно проанализированы пробы КВВ от 20 телят с разным диагностическим статусом. Установлено, что по параметрам подобия δ правильность ранжирования проб составляет 83%, а чувствительность определения наличия ВЗОД у телят – 93%.
По всем регистрируемым и расчетным параметрам оценка состояния дыхательных путей путем анализа РГФ над пробами КВВ массивом пьезосенсоров больше связана с результатами лабораторных исследований, чем с клиническими. Поскольку клинические проявления заболевания наступают позже и свидетельствуют о протекании острой фазы, при которой требуется не профилактическое, а направленное эффективное лечение, предварительная оценка состояния здоровья животных с помощью массива пьезосенсоров является более ценной.
* * *
Массив неселективных химических пьезосенсоров можно применять для анализа проб КВВ малого объема без предварительной их подготовки. Установлено, что сигналы сенсоров с пленками ПЭГ-2000, МО, ТХ-100, МУНТ характеризуются максимальной дифференцирующей способностью при определении патологии органов дыхания у телят. Наибольшими диагностическими и ранжирующими свойствами характеризуются расчетные характеристики (αinj, minj) массива сенсоров. Основным преимуществом подхода являются простота работы и обслуживания массива сенсоров, возможность эксплуатации во внелабораторных условиях. Правильность и чувствительность предлагаемого подхода диагностики состояния дыхательной системы у телят составляет 83 и 93% соответственно. Для оценки надежности необходимо увеличить выборку животных с более подробным изучением их клинико-физиологического статуса для исключения заболеваний и патологических состояний других органов и систем.
Работа выполнена при финансовой поддержке гранта РНФ № 18-76-10015.
Список литературы
Шабунин С.В., Шахов А.Г., Черницкий А.Е., Золотарев А.И., Рецкий М.И. Респираторные болезни телят: современный взгляд на проблему // Ветеринария. 2015. № 5. С. 3.
Черницкий А.Е., Ефанова Л.И., Золотарев А.И., Шахов А.Г., Шабунин С.В., Рецкий М.И. Методическое пособие по прогнозированию и ранней диагностике респираторных болезней у телят. Воронеж: Издательство “Истоки”, 2013. 48 с.
Кучменко Т.А. Химические сенсоры на основе пьезокварцевых микровесов / Проблемы аналитической химии. Т. 14 / Под ред. Власова Ю.Г. М.: Наука, 2011. С. 127.
Черницкий А.Е., Рецкий М.И., Золотарев А.И. Устройство для сбора конденсата выдыхаемого воздуха у животных. Патент РФ № 134772. Заявка № 2013135753/14 от 30.07.2013. Опубл. 27.11.2013.
McGuirk S.M. Disease management of dairy calves and heifers // Veterinary Clinics of North America: Food Animal Practice. 2008. V. 24. № 1. P. 139.
Кучменко Т.А. Инновационные решения в аналитическом контроле: учеб пособие. Воронеж: Воронеж. гос. технол. акад., ООО “СенТех”, 2009. 252 с.
Кучменко Т.А., Мишина А.А. Особенности сорбции паров аминов на тонких пленках кислотно-основных индикаторов // Журн. аналит. химии. 2011. Т. 66. № 8. С. 816. (Kuchmenko T.A., Mishina A.A. Sorption specifics of volatile amines on thin films of acid-base indicators // J. Analyt. Chem. 2011. V. 66. № 8. P. 701.)
Кучменко Т.А., Умарханов Р.У., Гражулене С.С., Заглядова С.В., Шкинев В.М. Микроструктурные исследования сорбционных слоев масс-чувствительных сенсоров для детектирования азотсодержащих соединений // Поверхность. Рентгеновские, синхротронные и нейтронные исследования. 2014. № 4. С. 9.
Кучменко Т.А., Шуба А.А., Бельских Н.В. Пример решения идентификационных задач в методе пьезокварцевого микровзвешивания смесей некоторых органических соединений // Аналитика и контроль. 2012. Т. 16. № 2. С. 151.
Кучменко Т.А., Шуба А.А. Информативность выходных сигналов “электронного носа” на пьезосенсорах // Аналитика и контроль. 2017. Т. 21. № 2. С. 71.
Иванов М.Г. Размерность и подобие. М.: Долгопрудный, 2013. 68 с.
Breg L., Nussbaumer-Ochsner Y., Sinues P. M-L., García-Gómez D., Suter Ya., Gaisl T., Stebler N., Gaugg M.T., Kohler M., Zenobi R. Real-time mass spectrometric identification of metabolites characteristic of chronic obstructive pulmonary disease in exhaled breath // Clin. Mass Spectrom. 2018. V. 7. № 1. P. 29.
Kim K.-H., Jahan S.A., Kabir E. A review of breath analysis for diagnosis of human health// Trends Anal. Chem. 2012. V. 33. № 1. P. 1.
Cathcart M.P., Hughes K.J. The application of exhaled breath gas and exhaled breath condensate analysis in investigation of lower respiratory tract in veterinary medicine: A review // Vet. J. 2012. V. 191. № 2. P. 282.
Zhou M., Liu Y., Duan Y. Breath biomarkers in diagnosis of pulmonary diseases // Clin. Chim. Acta. 2012. V. 413. № 10. P. 1770.
Miekisch W., Schubert J.K., Noeldge-Schomburg G.F.E. Diagnostic potential of breath analysis – focus on volatile organic compounds // Clin. Chim. Acta. 2004. V. 347. № 1. P. 25.
Mazzatenta A., Giulio C.D., Pokorski M. Pathologies currently identified be exhaled biomarkers // Respir. Physiol. Neurobiol. 2013. V. 187. № 2. P. 128.
Коренман Я.И., Попова Н.Н., Кучменко Т.А. Сенсорометрическое определение карбоновых кислот С1–С3 в воздухе // Журн. аналит. химии. 2008. Т. 63. № 1. С. 94. (Korenman Ya.I., Popova N.N., Kuchmenko T.A. Determination of C1–C3 carboxylic acids in air using a sensor // J. Analyt. Chem. 2008. V. 63. № 1. P. 85.)
Кучменко Т.А., Семенякина Н.В., Коренман Я.И. Оценка сродства некоторых сорбентов к алифатическим спиртам// Журн. прикл. химии. 1999. Т. 72. № 8. С. 1285. (Kuchmenko T.A., Semenyakina N.V., Korenman Ya.I. Estimation of the affinity of some sorbents for aliphatic alcohols by piezoelectric crystal microweighing // Russ. J. Appl. Chem. 1999. V. 72. № 8. P. 1355.)
Кучменко Т.А., Умарханов Р.У., Кочетова Ж.Ю., Бельских Н.В. Разработка датчика, газоанализатора и детектора аммиака на основе пьезосенсора // Журн. аналит. химии. 2012. Т. 67. № 11. С. 1032. (Kuchmenko T.A., Umarkhanov R.U., Kochetova Zh.Yu., Bel’skikh N.V. Development of a piezosensor-based transducer, gas analyzer and ammonia detector // J. Analyt. Chem. 2012. V. 67. № 11. Р. 930.)
Кучменко Т.А., Умарханов Р.У. Особенности микровзвешивания следовых содержаний алкиламинов на полимерных и твердотельных тонких пленках // Журн. аналит. Химии. 2013. Т. 68. № 4. С. 397. (Kuchmenko T.A., Umarkhanov R.U. Peculiarities of microweighing of trace quantities of alkylamines on polymer and solid–state thin films // J. Analyt. Chem. 2013. V. 68. № 4. P. 368.)
Попова Н.Н., Коренман Я.И., Кучменко Т.А. Определение муравьиной и уксусной кислот в воздухе методом пьезокварцевого микровзвешивания // Журн. прикл. химии. 2007. Т. 80. № 6. С. 977. (Popova N.N., Korenman Ya.I., Kuchmenko T.A. Determination of formic and acetic acids in air by piezoelectric microweighing // Russ. J. Appl. Chem. 2007. V. 80. № 6. P. 955.)
Кучменко Т.А., Кочетова Ж.Ю., Силина Ю.Е., Коренман Я.И., Кулин Л.А., Лапицкий И.В. Определение концентраций сероводорода в потоке газа применением пьезодетектора // Журн. аналит. химии. 2007. Т. 62. № 8. С. 866. (Kuchmenko T.A., Kochetova Zh.Yu., Silina Yu.E., Korenman Ya.I., Kulin L.A., Lapitskii I.V. Determination of trace amounts of hydrogen sulfide in a gas flow using a piezoelectric detector // J. Analyt. Chem. 2007. V. 62. № 8. Р. 781.)
Кучменко Т.А., Шуба А.А., Тюркин И.А., Битюкова В.В. Оценка состояния биологических проб по составу равновесной газовой фазы с применением мультисенсорной системы // Журн. аналит. химии. 2014. Т. 69. № 5. С. 534. (Kuchmenko T.A., Shuba A.A., Tyurkin I.A., Bityukova V.V. Estimation of the state of biological samples by the composition of the headspace using a multisensor system // J. Analyt. Chem. 2014. V. 69. № 5. Р. 485.)
Статистические методы. Контрольные карты Шухарта: ГОСТ Р 50779.42-99. М.: Стандартинформ, 2008. 32 с.
Гмурман В.Е. Теория вероятностей и математическая статистика. М.: Высшая школа, 2003. 479 с.
Кучменко Т.А., Шуба А.А., Битюкова В.В., Матвеева Н.А. Применение массива химических сенсоров для оценки наличия новообразований по запаху крови // Журн. аналит. химии. 2018. Т. 73. № 1. С. 60. (Kuchmenko T.A., Shuba A.A., Bityukova V.V., Matveeva N.A. Application of a chemical sensor array to assessing the presence of neoplasms by blood smell // J. Analyt. Chem. 2018. V. 73. № 1. Р. 91.)
Дополнительные материалы отсутствуют.
Инструменты
Журнал аналитической химии


