Журнал аналитической химии, 2020, T. 75, № 6, стр. 516-520
Определение диэтилтиокарбамата на твердой фазе волокнистого катионообменника в Cu-форме методом спектроскопии диффузного отражения
В. П. Дедкова a, *, О. П. Швоева a, А. А. Гречников a
a Институт геохимии и аналитической химии им. В.И. Вернадского Российской академии наук
119991 Москва, ул. Косыгина, 19, Россия
* E-mail: Dedva@yandex.ru
Поступила в редакцию 04.03.2019
После доработки 23.04.2019
Принята к публикации 07.12.2019
Аннотация
Методом спектроскопии диффузного отражения изучено взаимодействие диэтилдитиокарбамата натрия (ДЭДТК) с ионами меди, сорбированными на дисках волокнистого катионообменника ПАНВ–КУ-2. Определены условия получения носителя в Cu-форме. Изучена зависимость величины аналитического сигнала от условий сорбции ДЭДТК: рН раствора, времени контакта раствора с носителем, объема раствора и концентрации ДЭДТК в растворе. Сняты спектры диффузного отражения носителя ПАНВ–КУ-2–Cu и комплекса ДЭДТК с Cu в фазе ПАНВ–КУ-2. Наибольший аналитический сигнал наблюдается при 450 нм. Отмечена вероятность образования комплексов Cu(ДЭДТК) и Cu(ДЭДТК)2 на поверхности сорбента в зависимости от концентрации ДЭДТК в растворе. Показана возможность использования носителя ПАНВ–КУ-2–Cu для сорбции и определения 0.1–0.6 мкг/мл ДЭДТК в щелочных растворах (рН 7–10) измерением коэффициента диффузного отражения дисков при 450 нм. Методика апробирована на модельных растворах водопроводной воды.
Дитиокарбаматы (дитиокарбаминаты) широко применяют в аналитической химии в качестве органических реагентов на многие элементы. Они также нашли применение в медицине, биологии, химической технологии, металлургии в качестве ускорителя вулканизации резиновых смесей на основе каучуков, в качестве спиновой ловушки свободных радикалов и ингибиторов некоторых металлозависимых ферментов, как антиоксиданты. В сельском хозяйстве они известны как химический класс пестицидов, которые широко используют для борьбы с различными заболеваниями растений. Из производных дитиокарбаматов в качестве пестицидов применяют соли диметилдитиокарбаминой и этиленбисдитиокарбаминовой кислот: тирам, ТМТД, поликарбоцин, цинеб, манкоцеб и др. Они обладают аналогичным механизмом действия, но существенно отличаются по токсикологическим свойствам и поведению в окружающей среде. Тирам и манеб используют как фунгициды в качестве протравителей семян. Различные аспекты применения и определения дитиокарбаматов рассмотрены в монографии [1]. Дитиокарбаматы являются аллергенами, вызывающими дерматит, бронхиальную астму и другие заболевания. В почве и воде период их сохранности достигает двух месяцев [1–5].
Определение дитиокарбаматов может быть выполнено большинством известных методов, которые подробно рассмотрены в монографиях [1, 2]. Однако многие способы определения требуют разложения образца с переводом дитиокарбамата в форму какого-либо соединения серы, чаще всего в сульфат или сероуглерод [3–5]. При определении дитиокарбаматов используют метод газохроматографического парофазного анализа. Остаточные количества дитиокарбаматных пестицидов в почве и воде определяют после кислотного гидролиза путем кипячения с НСl в присутствии хлорида олова(II), очистки серной кислотой от сопутствующих соединений выделяющегося сероуглерода, поглощения его метанольным раствором КОН с образованием метилдитиокарбамината калия. Далее спектрофотометрически определяют продукт реакции с ионами меди. В обзоре [5], посвященном обеспечению безопасности пищевых продуктов, для определения дитиокарбаматов использовали метод газовой хроматографии–масс-спектрометрии после пробоподготовки кислотным разложением и экстракции изооктаном. Определяемые количества остаточных дитиокарбаматов в почве и воде составляют 0.005–0.05 мг/л, 0.01–0.1 мг/кг. Предельно допустимая концентрация в воде водоемов составляет 0.01мг/л [3–5].
В ряде работ описано определение органических соединений на твердой поверхности сорбента. Исследована сорбция ионных ассоциатов катионных красителей и комплексов металлов с 1,10-фенантролином на пенополиуретане [6]. Предложены тест-методики для определения анионных и катионных ПАВ, фенолов, 1-нафтола. Изучена [7] возможность определения тиосоединений на пенополиуретане, модифицированном наночастицами золота, выполнено определение 1–6 мкг/мл цистеина методом спектроскопии диффузного отражения при 540 нм с пределом определения 0.4 мкг/мл. Достоинства метода заключаются в простоте, экспрессности, доступности оборудования и легкости реализации тест-варианта. Получены [8] молекулярно-импринтированные белки, иммобилизованные на поверхности кремнеземов с привитыми иминодиацетатными и 2-карбоксиэтильными группами, для сорбционного концентрирования метиленового синего, бромтимолового синего и гидрохинона. Изучена их сорбционная емкость и селективность извлечения органических реагентов. Новые экспресс-методы [9] определения димедрола основаны на сорбции сульфоназо, конго красного и их ионных ассоциатов с димедролом на немодифицированном пенополиуретане. Ионные ассоциаты органических реагентов с димедролом сорбируются при рН 5–10, при этом сорбции азокрасителей не происходит.
В настоящей работе изучено взаимодействие ДЭДТК с ионами меди, сорбированными на волокнистом катионообменике ПАНВ–КУ-2, с целью нахождения условий определения ДЭДТК на твердой фазе методом спектроскопии диффузного отражения.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Растворы, реагенты, сорбенты. Использовали реактивы квалификации х. ч. или ч. д. а. Растворы солей металлов (0.01 М) готовили по известным методикам растворением соответствующих нитратов или хлоридов. Разбавлением получали растворы необходимой концентрации. Использовали растворы CuCl2 в 0.01 M HCl с содержанием меди 1 мг/мл. 0.01%-ный раствор ДЭДТК готовили ежедневно растворением 0.010 г ДЭДТК натрия в 100 мл воды.
В качестве твердой фазы использовали полиакрилонитрильное волокно, наполненное тонкодисперсным катионообменником КУ-2 (НИИСВ, Тверь). Диски диаметром 20 мм и массой 25–30 мг, промытые 1 М HCl и водой, хранили в дистиллированной воде. Диски ПАНВ–КУ-2 в Сu-форме получали перемешиванием 100 мл растворов с рН 5, содержащих 10–50 мкг меди, с десятью дисками ПАНВ–КУ-2 в течение 15 мин. Растворы сливали, диски промывали 50 мл воды, заливали водой и использовали для изучения.
Для создания необходимой кислотности анализируемого раствора применяли 0.1 M растворы HCl и NaOH.
Аппаратура. Параметры диффузного отражения регистрировали на колориметре Пульсар (ОКБА “Химавтоматика”, Чирчик). В качестве аналитического сигнала использовали разность коэффициентов диффузного отражения в условиях опыта (ΔR = R1 – R2) дисков ПАНВ–КУ-2–Cu (R1) и дисков после взаимодействия с анализируемым раствором (R2).
Кислотность растворов контролировали стеклянным электродом (потенциометр рН-673). Растворы перемешивали устройством ЛАБ-ПУ-02.
Методика эксперимента. В конические колбы емк. 100 мл помещали 20 мл анализируемого раствора в изучаемых условиях сорбции, вносили по 1 диску ПАНВ–КУ-2–Сu и перемешивали в течение заданного времени. Диски вынимали и измеряли коэффициент диффузного отражения. При динамическом режиме сорбции растворы прокачивали через диск и измеряли аналитический сигнал.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Диэтилдитиокарбамат образует окрашенные комплексы со многими элементами: Cu, Ni, Co, U(VI), Bi и др. [1, 2, 10]. Разработаны методики сорбционно-спектроскопического и тест-определения меди, основанные на сорбции меди на полиакрилонитрильном волокне, наполненном катионобменником КУ-2, образовании комплексов меди с ДЭДТК и регистрации окраски комплексов визуально или методом диффузно-отражательной спектроскопии [11–13]. В данном исследовании поставлена обратная задача: использовать эту систему для определения в растворе диэтилдитиокарбамата. Полиакрилонитрильные волокна, наполненные ионообменником, хорошо себя зарекомендовали при определении ионов металлов и анионов сорбционно-спектроскопическими и тест-методами. При определении сложных органических соединений их ранее не использовали.
Нами исследовано взаимодействие ДЭДТК с ионами меди, сорбированными на волокнистом ионообменнике ПАНВ–КУ-2. Медь хорошо сорбируется на ПАНВ–КУ-2 из водных растворов в области рН 2–5. Изучено влияние количества меди в водном растворе на образование комплексов меди с ДЭДТК на твердой фазе.
Зависимость аналитических сигналов комплексов на носителе, содержащем 5, 10 и 20 мкг меди на диск, от концентрации ДЭДТК в растворе представлена на рис. 1. Видно, что аналитические сигналы не зависят от содержания меди на носителе (5–20 мкг/диск) в диапазоне концентраций ДЭДТК в растворе 0.5–2.5 мкг/мл. Для дальнейших исследований использовали диски ПАНВ–КУ-2, содержащие 10 мкг Cu/диск носителя.
Рис. 1.
Зависимость аналитических сигналов комплексов Сu–ДЭДТК от концентрации диэтилдитиокарбамата натрия в растворе при содержании меди на носителе, мкг/мл: 1 – 5, 2 – 10, 3 – 20. рН 8, V = 20 мл, 450 нм, время перемешивания растворов с носителем – 20 мин.

Зависимость аналитического сигнала от рН раствора диэтилдитиокарбамата представлена на рис. 2. Аналитический сигнал достигает максимального значения при использовании раствора ДЭДТК с рН 10–11. Следует отметить, что в растворе экстракционно-фотометрическое определение меди с ДЭДТК выполняют при рН 9.0.
Рис. 2.
Зависимость аналитических сигналов от рН раствора диэтилдитиокарбамата. Носитель с содержанием 10 мкг Cu/диск, ДЭДТК – 2 мкг/мл, V = 20 мл, 450 нм.

Выбор режима сорбции диэтилдитиокарбамата. Изучена зависимость аналитического сигнала от объема раствора ДЭДТК в статическом и динамическом режимах сорбции и от времени перемешивания растворов ДЭДТК с диском ПАНВ–КУ-2–Сu. Данные представлены на рис. 3. При увеличении объема раствора от 20 до 250 мл при перемешивании диска носителя в растворе в течение 15 мин аналитический сигнал уменьшается в ~3 раза. Сигнал снижается в значительно меньшей степени при использовании динамического режима сорбции. Для дальнейшего изучения выбрали статический вариант сорбции ДЭДТК при перемешивании 50 мл раствора с диском носителя в течение 20 мин (рис. 3, кривая 3). Это позволяет одновременно выполнять сорбцию ДЭДТК из нескольких растворов и таким образом сократить продолжительность анализа. Однако для увеличения чувствительности определения можно использовать динамический вариант сорбции из объема 250 мл.
Рис. 3.
Зависимость аналитических сигналов от режима сорбции. ПАНВ–КУ-2–Сu c содержанием 10 мкг Сu/диск, ДЭДТК – 30 мкг: 1 – 20–250 мл, время сорбции 15 мин; 2 – 20–250 мл, скорость прокачивания раствора через диск 5 мл/мин; 3 – 50 мл, время сорбции 3–30 мин.

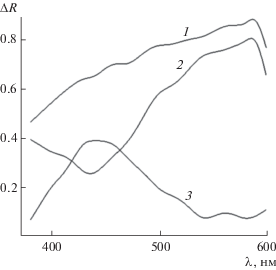
Спектры диффузного отражения носителя ПАНВ–КУ-2–Cu и комплекса меди с ДЭДТК в фазе носителя представлены на рис. 4. Как видно, аналитические сигналы максимальны при 430–450 нм. Это согласуется с условиями спектрофотометрического определения меди с ДЭДТК, которое выполняют при 435 нм.
Рис. 4.
Спектры диффузного отражения: 1 – носитель ПАНВ–КУ-2–Cu (R1), 2 – комплекс Cu–ДЭДТК на твердой фазе ПАНВ–КУ-2 (R2), 3 – аналитический сигнал ΔR = R1 – R2. сДЭДТК = 1 мкг/мл, V = 50 мл, рН 10, время перемешивания 20 мин.
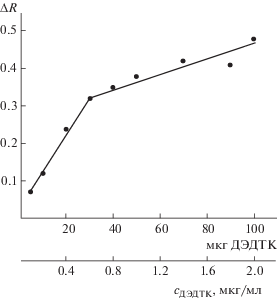
Зависимость аналитических сигналов от концентрации диэтилдитиокарбамата в растворе показана на рис. 5. В диапазонах концентраций ДЭДТК 0.1–0.6 мкг/мл и 0.6–2 мкг/мл наблюдаются линейные зависимости величины аналитического сигнала от концентрации с различными наклонами. Появление двух участков на градуировочном графике, по-видимому, можно объяснить образованием на твердой фазе комплексов Cu(ДЭДТК) и Cu(ДЭДТК)2. Коэффициенты градуировочной зависимости на первом участке a = 0.02, b = 0.51, на втором – a = 0.26, b = 0.11. Первый участок графика можно использовать для определения концентрации ДЭДТК в диапазоне 0.1–0.6 мкг/мл по уравнению с (мкг/мл) = (ΔR – 0.02)/0.51. Предел обнаружения, оцененный по 3s-критерию, составил 0.1 мкг/мл.
Рис. 5.
Зависимость аналитического сигнала от концентрации диэтилдитиокарбамата натрия в растворе. Статический режим сорбции, рН 10, V = 50 мл, время перемешивания 20 мин, 450 нм.
Проведенное исследование показало возможность определения ДЭДТК на твердой фазе ПАНВ–КУ-2–Cu при содержании 10 мкг Cu в одном диске путем сорбции ДЭДТК из водных щелочных растворов с рН 10. Концентрацию ДЭДТК определяют методом диффузной отражательной спектроскопии по желтой окраске дисков при 450 нм. Методика апробирована на модельных растворах водопроводной воды с добавками ДЭДТК.
Методика определения диэтилдитиокарбамата в водопроводной воде. Для нивелирования жесткости анализируемой воды работу выполняют с использованием 0.02 М раствора NаСl и при рН 7.0 ± 0.1, поскольку при подщелачивании до рН 10 наблюдается образование осадка.
Градуировочный график. В 20 мл 0.02 М растворов NаСl вводят 0, 10, 20, 40, 60, 80, 100 мкг ДЭДТК, что соответствует содержанию 0, 0.5, 1.0, 2.0, 3.0, 4.0, 5.0 мкг/мл ДЭДТК в растворе. Создают рН 7 добавлением 0.1 М НСl, вносят диски ПАНВ–КУ-2–Cu и перемешивают в течение 20 мин. Диски вынимают и измеряют коэффициенты диффузного отражения при 450 нм (R2). Диск с содержанием 0 мкг ДЭДТК (R1). Коэффициенты градуировочного графика: a = 0.07, b = = 0.04, ΔR = R1 – R2.
Методика анализа. К 20 мл анализируемой пробы воды прибавляют 0.4 мл 1 М раствора NаСl, создают рН 7.0 ± 0.1 добавлением 0.1 М НСl, вносят диск ПАНВ–КУ-2–Cu и перемешивают в течение 20 мин. Диск вынимают и измеряют R2 при 450 нм. Содержание ДЭДТК в воде рассчитывают по формуле: с (мкг/мл) = (ΔR – 0.07)/0.04.
Примеры анализа проб водопроводной воды представлены в табл. 1. При определении 1.0–4.0 мкг/мл ДЭДТК в модельных растворах водопроводной воды значения sr не превышают 0.2, предел обнаружения ДЭДТК, оцененный по 3s-критерию, составляет 0.2 мкг/мл. Анализ пяти проб воды занимает не более 30 мин.
Список литературы
Бырько В.М. Дитиокарбаматы. М.: Наука, 1984. 342 с.
Упор Э., Мохаи М., Новак Д. Фотометрические методы определения следов неорганических соединений. М.: Мир, 1985. 359 с.
ГОСТ Р51357-99 (ИСО 6466-83). Москва. Определение содержания остаточных количеств дитиокарбаматных пестицидов. М.: Издательство стандартов, 2000. 10 с.
Методические указания МУК 4.1.2997-12. Определение остаточных количеств дитиокарбаматов (тирама, цинеба, манкоцеба, метирама) в почве и воде методом газохроматографического парофазного анализа. М.: Федеральный центр гигиены и эпидемиологии Роспотребнадзора, 2013. 24 с.
Амелин В.Г., Лаврухина О.И. Обеспечение безопасности пищевых продуктов средствами химического анализа // Журн. аналит. химии. 2017. Т. 72. № 1. С. 3. (Amelin V.G., Lavrukhina O.I. Food Safety Assurance Using Methods of Chemical Analysis // J. Analyt. Chem. 2017. V. 72. № 1. P. 1.)
Дмитриенко С.Г., Пяткова Л.Н., Золотов Ю.А. Сорбция ионных ассоциатов на пенополиуретане и ее применение в сорбционно-спектроскопических и тест-методах анализа // Журн. аналит. химии. 2002. Т. 57. № 10. С. 1036.
Исаченко А.И., Апяри В.В., Дмитриенко С.Г., Волков П.А. Пенополиуретан, модифицированный наночастицами золота, и его перспективы для определения тиосоединений / Тез. докл. III съезда аналитиков России. Москва. 8–13 октября 2017 г. С. 214.
Булатова Е.В., Таныкова Н.Г., Петрова Ю.Ю., Беклемишев М.К. Молекулярный импринтинг красителей и фенолов в белок, иммобилизованный на поверхности кременезема / Тез. докл. III съезда аналитиков России. Москва. 8–13 октября 2017 г. С. 283.
Османова М.М., Мирзаева Х.А. Новые экспресс-методы определения димедрола / Тез. докл. III съезда аналитиков России. Москва. 8–13 октября 2017 г. С. 33.
Саввин С.Б., Дедкова В.П., Швоева О.П. Сорбционно-спектроскопические и тест- методы определения ионов металлов с органическими реагентами на твердой фазе ионообменников // Успехи химии. 2000. Т. 69. № 3. С. 203. (Savvin S.B., Dedkova V.P., Shvoeva O.P. Sorption-spectroscopic and test methods for the determination of metal ions on the solid-phase of ion-exchange materials // Russ. Chem. Rev. 2000. V. 69. № 3. P. 187.)
Швоева О.П., Дедкова В.П., Саввин С.Б. Применение двухслойных носителей для сорбционно-спектроскопического определения хрома(VI), меди(II) и никеля(II) из одной пробы в проточной системе // Журн. аналит. химии. 2001. Т. 56. № 3. С. 287. (Shvoeva O.P., Dedkova V.P., Savvin S.B. Use of two-layer supports for the sorption-spectrometric determination of chromium(VI), copper(II), and nickel(II) from a single sample in a flow sistem // J. Analyt. Chem. 2001. V. 56. № 3. P. 253.)
Дедкова В.П., Швоева О.П., Саввин С.Б. Тест-метод определения Cu(II), Ni(II) и Cr(VI) и из одной пробы // Журн. аналит. химии. 2001. Т. 56. № 8. С. 851. (Dedkova V.P., Shvoeva O.P., Savvin S.B. Test determination of Cu(II), Ni(II), and Cr(VI) in a single sample // J. Analyt. Chem. 2001. V. 56. № 8. P. 758.)
Швоева О.П., Дедкова В.П., Саввин С.Б. Сорбционно-спектроскопический метод многоэлементного анализа. Определение Cr(VI), V(V), Ni(II) и Cu(II) из одной пробы на двухслойном носителе // Журн. аналит. химии. 2010. Т. 65. № 7. С. 716. (Shvoeva O.P., Dedkova V.P., Savvin S.B. Adsorption-spectroscopic method for multielement analysis: Determination of Co(II), V(V), Ni(II) and Cu(II) from one sample using a two-layer absorbent // J. Analyt. Chem. 2010. V. 65. № 7. P. 699.)
Дополнительные материалы отсутствуют.
Инструменты
Журнал аналитической химии


