Журнал аналитической химии, 2021, T. 76, № 9, стр. 850-858
Проточное фракционирование во вращающейся спиральной колонке при разработке стандартных образцов природных наночастиц
М. С. Ермолин a, *, А. И. Иванеев a, П. С. Федотов a
a Институт геохимии и аналитической химии им. В.И. Вернадского Российской академии наук
119991 Москва, ул. Косыгина, 19, Россия
* E-mail: ermolin@geokhi.ru
Поступила в редакцию 02.04.2021
После доработки 15.04.2021
Принята к публикации 21.04.2021
Аннотация
Изучение свойств и состава природных наночастиц является важной проблемой аналитической химии. В настоящее время стандартные образцы природных наночастиц отсутствуют, что осложняет изучение роли наночастиц в тех или иных процессах, в том числе геохимических, а также делает практически невозможным сопоставление результатов, полученных разными исследователями. В данной работе наночастицы каолинита, монтмориллонита и мусковита изучены как потенциальные стандартные образцы природных наночастиц. Для выделения и характеризации минеральных наночастиц предложен комплекс аналитических методов, включающий проточное фракционирование частиц во вращающейся спиральной колонке, лазерную дифракцию, сканирующую электронную микроскопию, атомно-эмиссионную спектрометрию с индуктивно связанной плазмой. Показано, что согласно данным лазерной дифракции 93–98% выделенных частиц имеют размер от 40 до 300 нм, 2–7% частиц имеют размер до 830 нм. Размеры выделенных частиц подтверждены методом сканирующей электронной микроскопии. Исходя из содержания алюминия, оценена концентрация минеральных наночастиц в выделенных суспензиях. Изучена агрегационная устойчивость наночастиц в 5 мМ фосфатных буферных растворах при pH 6, 7 и 8. Показано, что наночастицы мусковита устойчивы при pH 7 и 8 в течение как минимум четырех недель, тогда как наночастицы монтмориллонита обладают схожей устойчивостью только при pH 8. Для наночастиц каолинита наблюдалась существенная агрегация при всех изучаемых значениях pH буферных растворов. Полученные экспериментальные результаты позволили уточнить проблемы и оценить перспективы разработки стандартных образцов природных наночастиц.
Проблема исследования микрочастиц (частиц размером от 1 до 100 мкм) в наземных, воздушных и водных экосистемах давно привлекает внимание ученых [1], однако наночастицы размером 1–100 нм остаются малоизученными [2], что обусловлено рядом методологических сложностей, связанных с их идентификацией, выделением, характеризацией и анализом. При этом в силу уникальных свойств наночастиц, в том числе развитой поверхности, высокой реакционной способности, высокой проникающей способности в живые организмы и подвижности в окружающей среде, их поведение может существенно отличаться от поведения микрочастиц и заметно влиять на живые организмы, кинетику геохимических реакций и биогеохимические циклы в целом [3].
Наночастицы окружающей среды в зависимости от источника происхождения делят на три группы: синтетические (engineered nanoparticles), случайные (incidental nanoparticles) и природные (natural nanoparticles) [4–6]. Природные наночастицы образуются в результате естественных процессов, таких как вулканические извержения, процессы выветривания, пожары. Случайные (техногенные) наночастицы являются побочным продуктом жизнедеятельности человека; к ним, прежде всего, относят наночастицы выбросов промышленных предприятий и автомобилей. Стремительное развитие нанотехнологий неизбежно приводит к попаданию в окружающую среду синтетических наночастиц, намеренно созданных человеком для тех или иных целей. Водные системы и почвы являются основными резервуарами для синтетических наночастиц, попадающих в окружающую среду с бытовыми и технологическими стоками, а также атмосферными осадками.
Для оценки потенциального воздействия природных, случайных и синтетических наночастиц на окружающую среду можно сравнить их потоки в окружающей среде [5]. По оценкам, ежегодное поступление синтетических наночастиц в окружающую среду составляет порядка 0.3 млн тонн [7]. Ежегодный выброс случайных наночастиц в атмосферу оценивается примерно в 1–10 млн тонн [5]. Казалось бы, количества синтетических и случайных наночастиц, выбрасываемых в окружающую среду, весьма внушительны, однако эти значения значительно меньше по сравнению с вкладом природных наночастиц. Например, ежегодный вклад пылевых бурь и извержений вулканов в общее количество природных наночастиц составляет порядка 320 и 22 млн тонн соответственно [5, 6]. Наибольший вклад в общий поток природных наночастиц в окружающей среде вносят процессы выветривания почв. Глины считаются основным резервуаром природных наноматериалов, на их долю приходится порядка 107–108 млн тонн наночастиц [5, 6]. Основными переносчиками силикатных наночастиц в окружающей среде являются грунтовые воды, реки, ледники, ветер и океанские течения. Реки ежегодно переносят порядка 103–104 млн тонн природных наночастиц в Мировой океан [5, 6].
Таким образом, с одной стороны, рассматриваемая научная проблема носит фундаментальный биогеохимический характер с точки зрения, например, изучения транспорта химических элементов и веществ, связанных с наночастицами, как на региональном, так и глобальном уровне. С другой стороны, характеризация и анализ природных наночастиц является важной проблемой аналитической химии, обусловленной сложностью их выделения для последующего исследования [2]. В настоящее время в большей степени изучены поведение и транспорт в окружающей среде именно синтетических наночастиц, тогда как природные наночастицы незаслуженно остаются малоизученными. Одной из основных причин этого является отсутствие стандартных образцов природных наночастиц, что значительно осложняет процесс их изучения. Отсутствие стандартных образцов природных наночастиц также делает практически невозможным сопоставление результатов, полученных разными исследователями, и оценку их правильности.
В общем, можно выделить следующие основные этапы разработки стандартных образцов природных наночастиц:
– выбор и отбор природного образца;
– пробоподготовка и выделение наночастиц из полидисперсного природного образца;
– оценка агрегационной и химической устойчивости наночастиц;
– характеризация наночастиц.
В первую очередь, выбор стандартных образцов природных наночастиц должен основываться на потребностях исследователей в моделировании и изучении тех или иных природных процессов на наноразмерном уровне. Особый интерес представляют наночастицы, которых больше всего в окружающей среде. Таким образом, силикатные наночастицы, которые наиболее широко распространены в окружающей среде, могут в первую очередь рассматриваться как потенциальные стандартные образцы природных наночастиц. Как уже упомянуто выше, глины считаются основным резервуаром природных наночастиц [5]. Глинистые минералы являются одним из основных компонентов почв и широко распространены в водных экосистемах. Значительную часть поверхности суши Земли занимают пустыни, а пылевые бури являются основным источником природных наночастиц в окружающей среде [4]. Основным компонентом песка пустыни является кварц, поэтому пустыни можно рассматривать как резервуар природных наночастиц кварца.
Стандартные образцы природных наночастиц могут быть двух типов. Первый тип – наночастицы конкретных минералов, например каолинита, монтмориллонита, кварца. Такие наночастицы однородны с точки зрения их элементного состава и структуры. Второй тип – наночастицы сложных гетерогенных образцов (например, пустынные пески, вулканический пепел), которые содержат наночастицы различных минералов. Изучение и разработка стандартных образцов второго типа значительно сложнее, но также возможны. Например, ранее наночастицы вулканического пепла были успешно выделены, охарактеризованы и количественно проанализированы [8]. Кроме того, показано, что наночастицы вулканического пепла обладают высокой устойчивостью в водной среде [9].
Природные наночастицы нельзя синтезировать в лаборатории, поэтому важнейшим этапом разработки стандартных образцов природных наночастиц является их выделение из природных образцов. Выделение наночастиц осложняется их низким содержанием в полидисперсных природных образцах (порядка 10–2% или менее) [10, 11]. Следовательно, методы разделения должны позволять работать с достаточно большим количеством полидисперсного природного образца. Следует отметить, что эффективность разделения также играет важную роль. Показано, что метод проточного фракционирования частиц во вращающейся спиральной колонке (ВСК) имеет преимущества с точки зрения эффективности разделения по сравнению с мембранной фильтрацией и седиментацией [12]. Кроме того, показана возможность масштабирования процесса разделения в ВСК без снижения его эффективности [13], что очень важно для приготовления больших объемов суспензий наночастиц.
Самая важная проблема при разработке стандартных образцов (размера и состава) природных наночастиц – это их агрегационная и химическая устойчивость при хранении. Поскольку разделение наночастиц осуществляют в жидкой среде, получаемый продукт разделения представляет собой суспензию. Хранение наночастиц в сухом виде – более предпочтительный способ, исключающий воздействие дисперсионной среды на наночастицы. Возможно высушивание (например, лиофилизация) суспензии наночастиц, при этом важным аспектом является возвращение суспензии в исходное состояния после повторного диспергирования. Также частицы должны быть достаточно устойчивы после повторного диспергирования для проведения исследований. В этом случае ключевую роль играет агрегационная устойчивость наночастиц. Агрегация наночастиц сильно зависит от pH и ионной силы дисперсионной среды. Важно, чтобы стандартные образцы природных наночастиц хранились в условиях, близких к природным, например, без стабилизации сильными органическими поверхностно-активными веществами. После такой стабилизации изучать поведение наночастиц в условиях, близких к природным, не имеет смысла. Наночастицы – это метастабильные объекты, способные к различным химическим превращениям, в том числе к растворению. Таким образом, постоянство химического состава наночастиц также является важнейшим аспектом проблемы.
Характеризацию и анализ природных наночастиц необходимо проводить с использованием взаимодополняющих аналитических методов. В настоящее время существуют различные методы характеризации и анализа наночастиц: сканирующая/просвечивающая электронная микроскопия, динамическое светорассеяние, лазерная дифракция (или статическое светорассеяние), методы проточного фракционирования в поперечном силовом поле, атомно-эмиссионная и масс-спектрометрия с индуктивно связанной плазмой. В целом характеризация и анализ природных наночастиц не является проблемой при условии получения устойчивых суспензий с достаточной концентрацией наночастиц.
Таким образом, разработка стандартных образцов природных наночастиц является насущной задачей аналитической химии. Цель настоящей работы – выделение минеральных наночастиц методом проточного фракционирования частиц в ВСК, характеризация их размера и морфологии, а также оценка устойчивости наночастиц в водных средах. Исследование проведено на примере частиц каолинита, монтмориллонита и мусковита.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Образцы и реагенты. Для выделения наночастиц использовали готовые порошки каолинита (КЛТ), монтмориллонита (ММТ) и мусковита (МСТ) из коллекции минералов Почвенного института им. В.В. Докучаева. Для приготовления фосфатных буферных растворов использовали следующие реактивы: NaH2PO4 (≥99.0%) и Na2HPO4·12H2O (≥99.0%). Деионизированную воду (18.2 МOм см, Millipore, Франция) использовали на всех этапах исследования.
Выделение минеральных наночастиц из полидисперсных образцов. Наночастицы выделяли из полидисперсных порошков минералов методом проточного фракционирования частиц в ВСК [10, 11]. Перед процедурой разделения готовили суспензии минералов, содержащие 0.1 г минерала и 10 мл фосфатного буферного раствора (5 мМ). Для каждого образца минерала готовили три суспензии при pH 6.0, 7.0 и 8.0. После этого приготовленные суспензии обрабатывали в ультразвуковой ванне Bandelin Sonorex DT 52 в течение 10 мин.
Суспензии вводили в ВСК, предварительно заполненную жидкостью-носителем. В качестве жидкости-носителя использовали фосфатный буферный раствор со значением pH, соответствующим pH разделяемой суспензии. Выделение наночастиц проводили при скорости вращения 800 об/мин и скорости потока жидкости-носителя 0.3 мл/мин. Элюирование частиц контролировали на выходе из ВСК при помощи спектрофотометра Thermo Scientific GENESYS 10S UV-Vis при длине волны 254 нм. В ходе фракционирования выделяли 20 мл суспензии минеральных наночастиц.
Оценка размера и морфологии минеральных наночастиц. Распределение минеральных наночастиц по размерам в суспензиях изучали методом лазерной дифракцией (ЛД) на приборе Shimadzu SALD-7500nano сразу после фракционирования, чтобы избежать агрегирования. Размер и морфологию выделенных наночастиц также изучали методом сканирующей электронной микроскопии (СЭМ, Tescan Mira LMU).
Оценку агрегационной устойчивости минеральных наночастиц осуществляли путем измерения их размерного распределения методом ЛД в течение 28 дней. В ходе оценки долгосрочной агрегационной устойчивости наночастиц суспензии хранили в темноте при 4°C. Перед каждым измерением суспензии обрабатывали в ультразвуковой ванне в течение 10 мин.
Оценка концентрации минеральных наночастиц в суспензиях. Для оценки концентрации минеральных наночастиц в выделенных суспензиях определяли алюминий методом атомно-эмиссионной спектрометрии с индуктивно связанной плазмы (АЭС-ИСП, Thermo Scientific iCAP 6500 Duo) после кислотного разложения суспензий. Подробно процедура разложения и анализа минеральных частиц описана в работе [14].
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Размерное распределение минеральных наночастиц. Размерные распределения наночастиц КЛТ, ММТ и МСТ представлены на рис. 1. Наночастицы КЛТ имеют бимодальное размерное распределение с максимумами при 160 и 550 нм. Первая популяция частиц имеет размер в диапазоне от 45 до 300 нм, а вторая – от 460 до 830 нм. Необходимо отметить, что содержание частиц во второй популяции незначительно и варьируется в диапазоне от 1.5 до 6.3%. Выявлено влияние pH на размерное распределение наночастиц КЛТ. Согласно данным ЛД, содержание частиц во второй популяции (460–830 нм) уменьшается с увеличением pH. Кроме того, с увеличением pH увеличивается содержание частиц размером <100 нм. Наблюдаемый эффект можно объяснить стабилизацией наночастиц КЛТ при повышении pH. Однако данный эффект незначителен и может быть также отнесен к погрешностям измерений.
Рис. 1.
Размерное распределение наночастиц каолинита, монтмориллонита и мусковита, выделенных методом проточного фракционирования частиц во вращающейся спиральной колонке.
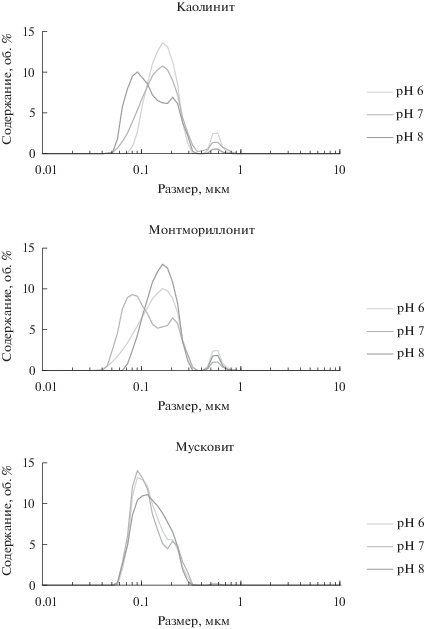
Наночастицы ММТ имеют бимодальное размерное распределение, которое включает две популяции частиц размером 40–300 и 460–830 нм. Содержание частиц во второй популяции варьируется в диапазоне от 2.8 до 6.5%. Следует отметить, что при pH 7 профиль распределения первой популяции (40–300 нм) имеет плечо на правом склоне, что можно отнести к погрешностям измерений. В целом существенного влияния pH на размерное распределение наночастиц ММТ не выявлено.
Согласно данным ЛД, размерное распределение наночастиц МСТ имеет диапазон от 60 до 300 нм с максимумом порядка 90–110 нм (в зависимости от pH). Необходимо отметить, что при pH 6 и 8 также наблюдали вторую популяцию частиц МСТ размером 520–660 нм, однако содержание этих частиц незначительно и составляет всего 0.02% при pH 6 и 0.44% при pH 8.
Таким образом, показано, что размерные распределения наночастиц КЛТ, ММТ и МСТ схожи и главным образом (не менее чем на 93.5%) состоят из частиц размером <300 нм. Частицы размером >300 нм также присутствуют в выделенных суспензиях минеральных наночастиц при различных pH, однако их содержание, как правило, невелико (менее 6.5%), а в случае МСТ и вовсе незначительно (менее 0.44%). Значительного влияния pH на размерное распределение выделенных минеральных наночастиц не выявлено. Важно отметить, что в основе метода ЛД лежит допущение о сферичности измеряемых частиц. Природные наночастицы редко имеют сферическую форму, поэтому возможны погрешности измерения размеров. Следовательно, необходима характеризация морфологии выделяемых наночастиц методом сканирующей электронной микроскопии.
Морфология минеральных наночастиц. Микрофотографии наночастиц каолинита, монтмориллонита и мусковита представлены на рис. 2. Как видно, большинство наночастиц КЛТ имеют размер порядка 100–300 нм, при этом также присутствуют частицы размером около 50 и 500 нм. Наночастицы ММТ имеют размер в диапазоне от 60 до 200 нм; кроме того, обнаружены частицы ММТ размером порядка 500 нм. Размер наночастиц МСТ варьируется приблизительно от 50 до 300 нм, при этом большинство наночастиц МСТ имеют размер около 100 нм. В целом микрофотографии наночастиц минералов хорошо согласуются с соответствующими распределениями по размерам. Что касается морфологии наночастиц, наночастицы КЛТ имеют пластинчатую форму. Напротив, наночастицы ММТ и МСТ имеют псевдосферическую форму.
Рис. 2.
Микрофотографии наночастиц каолинита (а), монтмориллонита (б) и мусковита (в), выделенных методом проточного фракционирования частиц во вращающейся спиральной колонке.

Агрегационная устойчивость минеральных наночастиц. Устойчивость минеральных наночастиц изучали в приближенных к естественным условиях, а именно, при pH и ионной силе дисперсионной среды, соответствующим поверхностным водам. Как правило, pH поверхностных вод колеблется в диапазоне от 6.0 до 8.5, а ионная сила составляет порядка 1–5 мМ. Агрегационную устойчивость минеральных наночастиц оценивали в 5 мМ фосфатных буферных растворах при pH 6.0, 7.0 и 8.0.
Устойчивость минеральных наночастиц оценивали путем измерения размерного распределения методом ЛД в течение четырех недель. Для упрощения и удобства сравнения результатов гранулометрического анализа суспензий наночастиц размерные распределения были преобразованы, а именно разделены на три размерных диапазона (<0.3, 0.3–1.0 и >1 мкм). Таким образом, сравнивали содержания минеральных наночастиц в каждом размерном диапазоне. Преобразованные (разделенные на три размерных диапазона) размерные распределения наночастиц КЛТ, ММТ и МСТ представлены на рис. 3. Показано, что наночастицы КЛТ агрегируют при хранении, при этом агрегация значительно зависит от pH фосфатного буферного раствора (рис. 3а). Установлено, что агрегационная устойчивость наночастиц КЛТ увеличивается с увеличением pH дисперсионной среды. При pH 8 за четыре недели хранения суспензии содержание наночастиц КЛТ размером <0.3 мкм снизилось примерно на 10%, при этом содержание частиц (агрегатов) размером >1 мкм увеличилось также на 10%; изменение содержания частиц размером 0.3–1.0 мкм в течение хранения было незначительным. При pH 7 содержание наночастиц КЛТ (<0.3 мкм) снизилось за четыре недели хранения приблизительно на 18–27%, при этом содержание микронных агрегатов (>1 мкм) увеличилось приблизительно на 19–25%. Также наблюдалось незначительное увеличение содержания частиц размером 0.3–1.0 мкм. Продемонстрировано, что наночастицы КЛТ неустойчивы в 5 мМ фосфатном буферном растворе при pH 6. После четырех недель хранения содержание наночастиц КЛТ (<0.3 мкм) снизилось с 99 до 8%, а содержание частиц КЛТ размером 0.3–1.0 мкм увеличилась с 1.5 до 15%. Содержание микронных агрегатов (>1 мкм) при этом после четырех недель хранения составило 77%.
Рис. 3.
Преобразованные размерные распределения наночастиц каолинита (а), монтмориллонита (б) и мусковита (в), полученные в течение четырех недель хранения суспензий.
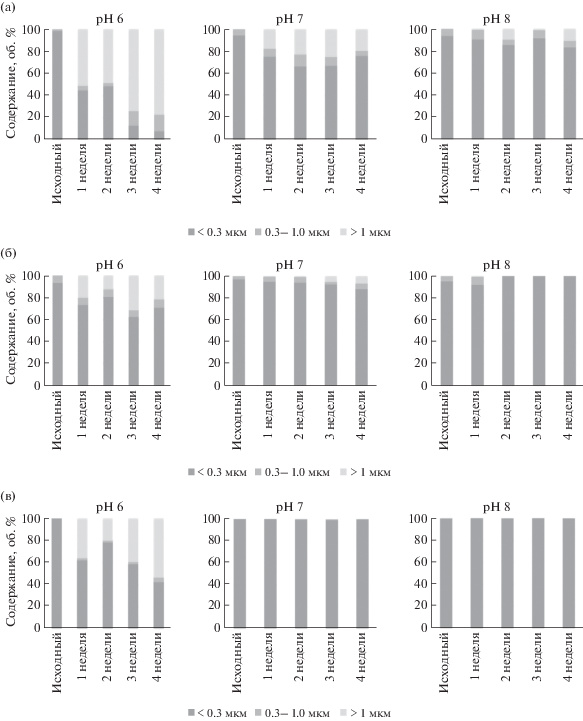
Наночастицы ММТ и МСТ продемонстрировали схожую агрегационную устойчивость при долгосрочном хранении. Показано, что устойчивость частиц ММТ и МСТ увеличивается с увеличением pH дисперсионной среды (рис. 3б, 3в). При pH 6 после четырех недель хранения содержание наночастиц (<0.3 мкм) в суспензиях снизилось с 93 до 71% для ММТ и со 100 до 42% для МСТ. Содержание субмикронных частиц (0.3–1.0 мкм) при этом изменилось незначительно; хранение в основном приводило к образованию агрегатов микронного размера. При pH 7 наблюдали незначительную агрегацию наночастиц ММТ; агрегаты микронного размера (6.5%) появились после четырех недель хранения. Установлено, что при pH 8 наночастицы ММТ обладают высокой агрегационной устойчивостью, в то время как наночастицы МСТ устойчивы при pH 7 и 8. Продемонстрировано, что размерное распределение наночастиц ММТ (pH 8) и МСТ (pH 7 и 8) сохранялось в течение четырех недель хранения суспензий. Наблюдаемые незначительные колебания доли субмикронных частиц (0.3–1.0 мкм) вероятнее всего вызваны погрешностями измерений методом ЛД.
Таким образом, показано, что агрегационная устойчивость наночастиц КЛТ, ММТ и МСТ зависит от pH дисперсионной среды. Устойчивость наночастиц повышается с увеличением pH. Наночастицы МСТ при pH 7 и 8, а также наночастицы ММТ при pH 8 продемонстрировали высокую агрегационную устойчивость и оставались стабильными в течение как минимум четырех недель. Агрегационная устойчивость исследуемых минеральных наночастиц возрастает в следующем порядке: каолинит < монтмориллонит < мусковит.
Концентрация наночастиц в выделенных суспензиях. Концентрацию наночастиц КЛТ, ММТ и МСТ в анализируемых суспензиях можно оценить по концентрации алюминия. Установлено, что содержание алюминия в выделенных суспензиях КЛТ, ММТ и МСТ составило 7.3 ± 0.1, 66.3 ± 1.7, 11.3 ± 0.4 мг/л соответственно. Согласно минеральному составу, содержание алюминия в КЛТ, ММТ и МСТ составляет около 20%, поэтому концентрация минеральных наночастиц в разделенных суспензиях может составлять около 37, 332 и 57 мг/л соответственно. Следует отметить, что концентрацию наночастиц можно увеличить за счет увеличения массы разделяемого образца. В данной работе наночастицы выделяли из 0.1 г полидисперсных образцов минералов. Масса разделяемого образца для аналитической ВСК (объемом 20–25 мл) может быть увеличена до 1 г, что позволит получить более концентрированные суспензии. Необходимо отметить, что увеличение концентрации частиц также может повлиять на их устойчивость.
* * *
Создание стандартных образцов природных наночастиц является насущной потребностью современной аналитической химии окружающей среды. В настоящей работе наночастицы каолинита, монтмориллонита и мусковита изучены в качестве потенциальных стандартных образцов природных наночастиц. Минеральные наночастицы успешно выделены, охарактеризованы и проанализированы. Особое внимание уделено агрегационной устойчивости наночастиц, поскольку хранение стандартных образцов природных наночастиц является важной проблемой. Показано, что наночастицы мусковита устойчивы в 5 мМ фосфатном буферном растворе при pH 7 и 8 в течение как минимум четырех недель. Для наночастиц монтмориллонита такая же устойчивость наблюдается только при pH 8. Выявлено, что наночастицы каолинита в значительной степени агрегируют при pH 6, 7 и 8. В целом устойчивость наночастиц монтмориллонита и мусковита в течение четырех недель является многообещающим результатом. Однако оценка устойчивости в течение более длительного периода (например, в течение нескольких месяцев) требует дополнительных исследований. Кроме этого, важное значение имеет изучение возможности высушивания суспензий природных наночастиц и повторного диспергирования с сохранением исходных свойств частиц (например, размерного распределения). Исследования в этой области будут в дальнейшем продолжены.
Исследование выполнено при поддержке Российского научного фонда (проект № 20-73-00299). Авторы искренне благодарны Ольге Борисовне Роговой (Почвенный институт им. В.В. Докучаева, Москва) за предоставление образцов минералов, а также Василию Константиновичу Карандашеву (Институт проблем технологии микроэлектроники и особочистых материалов РАН, Черноголовка) за разложение и анализ суспензий наночастиц. Исследование соответствует теме № 0116-2019-0010 ГЕОХИ РАН.
Список литературы
Buffle J., van Leeuwen H.P. Environmental Particles. Boca Raton: CRC Press, 1992. 576 p.
Ermolin M.S., Fedotov P.S. Separation and characterization of environmental nano- and submicron particles // Rev. Anal. Chem. 2016. V. 35. № 4. P. 185.
Wang Y. Nanogeochemistry: Nanostructures, emergent properties and their control on geochemical reactions and mass transfers // Chem. Geol. 2014. V. 378–379. № 1. P. 1.
Buzea C., Pacheco I.I., Robbie K. Nanomaterials and nanoparticles: Sources and toxicity // Biointerphases. 2007. V. 2. № 4. P. MR17.
Hochella M.F., Mogk D.W., Ranville J., Allen I.C., Luther G.W., Marr L.C., McGrail B.P., Murayama M., Qafoku N.P., Rosso K.M., Sahai N., Schroeder P.A., Vikesland P., Westerhoff P., Yang Y. Natural, incidental, and engineered nanomaterials and their impacts on the Earth system // Science. V. 363. № 6434. P. 1414.
Hochella M.F., Aruguete D., Kim B., Madden A.S. Naturally occurring inorganic nanoparticles: General assessment and a global budget for one of earth’s last unexplored major geochemical components // Nat. Nanostruct. 2012. P. 1.
Keller A.A., Lazareva A. Predicted releases of engineered nanomaterials: From global to regional to local // Environ. Sci. Technol. Lett. 2013. V. 1. № 1. P. 65.
Ermolin M.S., Fedotov P.S., Malik N.A., Karandashev V.K. Nanoparticles of volcanic ash as a carrier for toxic elements on the global scale // Chemosphere. 2018. V. 200. P. 16.
Ermolin M.S., Dzherayan T.G., Vanifatova N.G. Stability of volcanic nanoparticles using combined capillary zone electrophoresis and laser diffraction // Environ. Chem. Lett. 2021. V. 19. № 1. P. 751.
Ермолин М.С., Федотов П.С., Иванеев А.И., Карандашев В.К., Федюнина Н.Н., Еськина В.В. Выделение и количественный анализ наночастиц дорожной пыли // Журн. аналит. химии. 2017. Т. 72. № 5. С. 448. (Ermolin M.S., Fedotov P.S., Ivaneev A.I., Karandashev V.K., Fedyunina N.N., Eskina V.V. Isolation and quantitative analysis of road dust nanoparticles // J. Anal. Chem. 2017. V. 72. № 5. P. 520.)
Ермолин М.С., Федотов П.С., Карандашев В.К., Шкинев В.М. Методология выделения и элементного анализа наночастиц вулканического пепла // Журн. аналит. химии. 2017. Т. 72. № 5. С. 462. (Ermolin M.S., Fedotov P.S., Karandashev V.K., Shkinev V.M. Methodology for separation and elemental analysis of volcanic ash nanoparticles // J. Anal. Chem. 2017. V. 72. № 5. P. 533.)
Ivaneev A.I., Faucher S., Ermolin M.S., Karandashev V.K., Fedotov P.S., Lespes G. Separation of nanoparticles from polydisperse environmental samples: comparative study of filtration, sedimentation, and coiled tube field-flow fractionation // Anal. Bioanal. Chem. 2019. V. 411. № 30. P. 8011.
Fedotov P.S., Ermolin M.S., Katasonova O.N. Field-flow fractionation of nano- and microparticles in rotating coiled columns // J. Chromatogr. A. 2015. V. 1381. P. 202.
Ivaneev A.I., Faucher S., Fedyunina N.N., Karandashev V.K., Ermolin M.S., Fedotov P.S., Lespes G. Reliability of the direct ICP-MS analysis of volcanic ash nanoparticles // Int. J. Environ. Anal. Chem. 2019. V. 99. № 4. P. 369.
Дополнительные материалы отсутствуют.
Инструменты
Журнал аналитической химии


