Журнал аналитической химии, 2022, T. 77, № 5, стр. 446-453
Сорбционные возможности магнитного композита на основе модифицированных углеродных нанотрубок, синтезированных на различных катализаторах
С. С. Гражулене a, *, Н. И. Золотарева a, А. Н. Редькин a
a Институт проблем технологии микроэлектроники и особочистых материалов Российской академии наук
142432 Московская обл., Черноголовка, ул. Академика Осипьяна, 6, Россия
* E-mail: grazhulene@mail.ru
Поступила в редакцию 22.06.2021
После доработки 14.09.2021
Принята к публикации 15.10.2021
- EDN: IKNTSP
- DOI: 10.31857/S0044450222050036
Аннотация
На примере сорбции ионов Ag(I), Au(III) и Pd(II) из водных растворов изучена зависимость сорбционных возможностей магнитных сорбентов МНЧ@УНТ от соотношения образующих его компонентов: наночастиц магнетита (МНЧ) и углеродных нанотрубок (УНТ), синтезированных методом каталитического пиролиза паров этанола на различных катализаторах группы железа. Показано, что сорбционная емкость всех типов композитов растет с увеличением содержания в них УНТ по отношению к МНЧ. Установлено, что оптимальное соотношение компонентов в композите для всех УНТ, полученных на различных катализаторах и имеющих различную морфологию, равно 10 : 1. При этом соотношении композит имеет максимальную сорбционную емкость по отношению к изучаемым ионам, которая составляет 6.5, 6.1 и 5.5 мг/г для сорбции Ag(I), Au(III) и Pd(II) соответственно, и достаточную намагниченность для разделения фаз в магнитном поле. Показано, что модификация УНТ магнитными наночастицами позволяет использовать образовавшийся композит не только в статическом, но и в динамическом варианте твердофазной экстракции; ранее применение индивидуальных УНТ, полученных на кобальтовом и железном катализаторах, не дало положительных результатов. В динамическом режиме можно использовать большие объемы анализируемых растворов, достигаются более высокие коэффициенты концентрирования по сравнению со статическим режимом, а также более низкие пределы определения элементов после выпаривания элюатов на графитовом порошке. Для всех видов композита выполнена сравнительная метрологическая оценка результатов определения элементов методом дуговой атомно-эмиссионной спектроскопии. Полученные пределы определения элементов составляют n × 10–7 мас. % (Kконц = 200).
Метод магнитной твердофазной экстракции (МТФЭ), заключающийся в сорбции ионов металлов или органических соединений на магнитном сорбенте с последующим отделением сорбента от раствора с помощью постоянного магнита, находит все более широкое применение в аналитической химии [1]. Разделение фаз с помощью магнита позволяет избежать трудоемких процессов фильтрования или центрифугирования, которые обычно используются для разделения фаз в статических методах твердофазной экстракции, и значительно упростить и ускорить процесс извлечения определяемых веществ из растворов. Магнитные сорбенты представляют собой материалы, в которых наночастицы оксидов железа внедрены в немагнитные матрицы. Одним из перспективных магнитных сорбентов является МНЧ@УНТ, состоящий из магнитных наночастиц магнетита (МНЧ) и углеродных нанотрубок (УНТ). Благодаря высокой удельной поверхности, быстрому массообмену, полноте сорбции и десорбции, а также возможности многократной регенерации, магнитные нанокомпозиты МНЧ@УНТ с успехом используются в аналитической практике для концентрирования, а также для очистки объектов окружающей среды [2–4]. Нанокомпозит МНЧ@УНТ устойчив как в кислой, так и в щелочной средах, поэтому может использоваться для извлечения определяемых веществ из раствора в широком диапазоне pH. Обычно его получают путем адсорбции предварительно синтезированных МНЧ поверхностью УНТ, так как этот способ является наиболее простым и экономичным [5, 6]. Как правило, для синтеза УНТ используют метод каталитического пиролиза паров (chemical vapor deposition, CVD) ацетилена [7], изобутана [8] или этанола [9] на различных катализаторах. Наши предыдущие исследования [10] показали, что полученные на никелевом катализаторе УНТ(Ni), а также кислотно модифицированные УНТ могут успешно применяться в качестве сорбентов в твердофазной экстракции (ТФЭ) как в статическом, так и в динамическом режимах. Использование УНТ, полученных на кобальтовом (УНТ(Co)) и железном (УНТ(Fe)) катализаторах затруднено в статическом режиме из-за сложности разделения фаз и практически невозможно в динамическом варианте ТФЭ в связи с трудностью заполнения хроматографической колонки из-за ватообразной консистенции этих материалов. Причина этого явления – различная морфология УНТ, полученных в различных условиях синтеза, в частности с катализаторами разных типов. В то же время синтез на железном и кобальтовом катализаторах экономически более привлекателен в связи с гораздо бóльшим по сравнению с никелевым катализатором валовым выходом продукта реакции – УНТ, что особенно важно в технологии и при концентрировании примесей из больших объемов водных сред в аналитической практике.
В связи с изложенным выше задачей настоящего исследования являлось нахождение и сопоставление возможностей использования в качестве сорбентов УНТ различных морфологий: УНТ(Ni), УНТ(Fe), УНТ(Co). Для решения этой задачи модифицировали УНТ магнитными наночастицами и изучали зависимости сорбционных возможностей композитов от соотношения в них УНТ и МНЧ в статическом и динамическом режимах ТФЭ. Особый интерес представляло изучение возможности использования УНТ(Co) и УНТ(Fe), модифицированных магнитными наночастицами, и в динамическом варианте ТФЭ, который позволяет достигать более низкие пределы обнаружения определяемых ионов металлов по сравнению со статическим за счет использования для анализа больших объемов водных растворов.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Для синтеза магнетита использовали свежеприготовленные растворы хлоридов железа(III) и (II) при их соотношении 2 : 1, содержащие 11.7 г FeCl3·6H2O и 4.3 г FeCl2·4H2O. Синтез МНЧ проводили в трехгорлой круглодонной колбе емк. 200 мл при 80°С в атмосфере инертного газа аргона при интенсивном перемешивании в течение одного часа. Затем в раствор быстро добавляли 20 мл 25–30%-ного раствора NH3 до достижения pH 10. После охлаждения осадок удерживали в колбе с помощью магнита, промывали деионизованной водой и этанолом до pH 7, высушивали до сухого остатка в сушильном шкафу при 60°С, перемешивали в ступке из оргстекла и помещали в бюкс, а затем в эксикатор для хранения.
Углеродные нанотрубки синтезировали по разработанной нами методике CVD [9]. УНТ осаждали на поверхности никелевого, кобальтового или железного катализатора, который после синтеза отмывали 30%-ной HNO3. Полученные образцы УНТ промывали деионизованной водой, высушивали и проводили окислительную модификацию путем кипячения УНТ в конц. HNO3 oc. ч. в течение полутора часов. Затем УНТ отмывали от кислоты деионизованной водой до pH 7, высушивали и использовали для синтеза композита.
Магнитный сорбент МНЧ@УНТ синтезировали в конической колбе емк. 100 мл, в которую помещали по 100 мг заранее полученных МНЧ и УНТ. Заливали их 30 мл деионизованной воды и перемешивали при комнатной температуре на качалке с возвратно-поступательным движением в течение 30 мин. Образующийся магнитный сорбент удерживали в колбе магнитом, а не связавшиеся с МНЧ углеродные нанотрубки сливали в кварцевую чашку. Оставшийся в колбе полученный сорбент дважды промывали деионизованной водой и промывные воды сливали в ту же чашку. Сливы выпаривали, а сухой остаток высушивали под ИК-лампой и взвешивали, определяя таким образом количество не связавшихся в композит УНТ. По разности масс исходных и не связанных в композит УНТ определяли количество УНТ в магнитном сорбенте. Полученный магнитный сорбент оставляли в колбе во влажном состоянии и использовали для изучения сорбции ионов металлов из водных растворов.
Состав синтезированных порошков МНЧ и МНЧ@УНТ изучали методом рентгенофазового анализа на дифрактометре Bruker D2 PHAZER (СoKα1-излучение) в виде суспензии в вазелиновом масле. При расшифровке рентгенограмм использовали банк данных “Power Diffraction File (PDF-2)”. Магнитные характеристики МНЧ и композита определяли при комнатной температуре на вибрационном магнитометре EG&G Princeton Applied Research, model 155. Для исследования морфологии образцов композитов МНЧ@УНТ, в состав которых входили УНТ, полученные на различных катализаторах, применяли просвечивающий электронный микроскоп (ПЭМ) JEOL JEM-2100 при ускоряющем напряжении 200 кВ.
Для изучения сорбции ионов металлов из водных растворов 50 мл раствора помещали в коническую колбу емк. 100 мл, где уже находилось 200 мг магнитного сорбента, и перемешивали на качалке в течение 20 мин. Необходимое значение pH раствора создавали добавлением 10%-ного раствора NH3 или 5%-ной HNO3.
После окончания процесса сорбции сорбент с извлеченными из раствора ионами металлов удерживали в колбе магнитом, а раствор сливали в кварцевую чашку с 500 мг графитового порошка, выпаривали досуха под ИК-лампой и анализировали. Сорбированные ионы Ag(I), Au(III) и Pd(II) элюировали 6 мл 1 М HNO3 при постоянном перемешивании в течение 30 мин. Затем сорбент вновь удерживали в колбе магнитом, а элюат сливали в другую кварцевую чашку с 500 мг графитового порошка, упаривали досуха под ИК-лампой и анализировали.
В случае сорбции в динамическом режиме для приготовления колонки 80 мг магнитного сорбента МНЧ@УНТ засыпали во фторопластовую трубку длиной 30 и внутренним диаметром 2.5 мм через фторопластовую воронку. Верх и низ колонки закрывали пробками из стекловолокна. Колонку промывали раствором 1 М HNO3, затем деионизованной водой и 3 мл буферного раствора с pH 5.5–6.0. Анализируемый раствор пропускали через колонку со скоростью 2 мл/мин, используя перистальтический насос. Ионы металлов элюировали с колонки 4 мл 1 М HNO3. Элюат сливали в кварцевую чашку с 500 мг графитового порошка, упаривали досуха под ИК-лампой и анализировали.
Магнитный сорбент регенерировали путем обработки его в течение 15 мин 0.5 М HNO3 и промывания деионированной водой.
В качестве исходных растворов исследуемых элементов использовали одноэлементные стандартные растворы High Purity Standarts (США) с концентрацией элементов 1000 ppm. Рабочие растворы исследуемых элементов необходимой концентрации готовили разбавлением исходных деионизованной водой.
Для построения изотерм сорбции и определения сорбционной емкости сорбента готовили серию растворов с концентрацией исследуемых элементов от 10 до 70 мкг/мл. Из каждого раствора отбирали аликвоту 50 мл и при pH 6 проводили сорбцию на 200 мг сорбента до достижения сорбционного равновесия. Сорбент с извлеченными из раствора ионами металлов удерживали в колбе магнитом, а раствор сливали в кварцевую чашку с 500 мг графитового порошка, выпаривали досуха под ИК-лампой и анализировали.
Содержание элементов определяли методом атомно-эмиссионной спектрометрии (АЭС) в дуге постоянного тока силой 10 А на дифракционном спектрографе PGS-2 с решеткой 651 штр/мм, обеспечивающей обратную линейную дисперсию 0.74 нм/мм. В работе использовали графитовый порошок особой чистоты марки ОСЧ 8-4. Пробу набивали в кратер нижнего электрода (анода). Кратер имел глубину и диаметр 4 мм, толщину стенок 1 мм. Конец верхнего электрода (катода) был заточен на конус. Расстояние между электродами составляло 4 мм. Использовали трехлинзовую систему освещения щели. Для регистрации эмиссионных спектров использовали разработанную в лаборатории фотоэлектрическую систему регистрации на основе линеек приборов с зарядовой связью. Анализ выполняли, применяя государственные стандартные образцы на основе графитового порошка (комплект СОГ-21, УГТУ-УПИ). Для расчета содержания элементов в растворе их концентрацию в графитовом порошке делили на коэффициент концентрирования, который определяли как соотношение масс анализируемого раствора и графитового порошка.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Для решения поставленных задач синтезировали составляющие композит компоненты: МНЧ, УНТ(Ni), УНТ(Fe), УНТ(Co), из которых получали композиты МНЧ@УНТ методами, изложеными в “Экспериментальной части”, а также описанными нами ранее [10, 11]. Магнитный композит получали в две стадии при 80°С в атмосфере аргона. Этот метод получения, с нашей точки зрения, является более удобным и экономичным, чем одностадийный, а также позволяет управлять соотношением между УНТ и МНЧ в композите. Дифрактограмма порошка МНЧ показала, что его состав соответствуют однофазному магнетиту Fe3O4 (карточка PDF 11-614). Средний размер частиц МНЧ составил 15.0 нм [11]. Методом ПЭМ установили, что средний диаметр частиц композита составляет 35–55, 45–85, 90–145 нм для УНТ(Ni), УНТ(Co) и УНТ(Fe) соответственно.
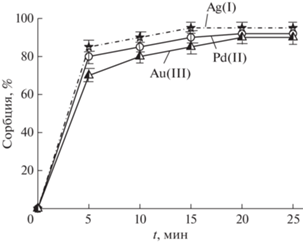
Сорбционные возможности полученных сорбентов изучали по отношению к ионам Au(III), Ag(I) и Pd(II) из азотнокислых растворов. Для определения времени достижения сорбционного равновесия в статическом режиме изучали распределение исследуемых элементов между сорбентом и водным раствором в зависимости от времени контакта фаз. Установили, что максимальная сорбция всех исследуемых ионов металлов на сорбентах происходит в течение 20 мин (рис. 1).
Рис. 1.
Зависимость сорбции Au(III), Ag(I) и Pd(II) на МНЧ@УНТ от времени контакта с сорбентом (pH 6).
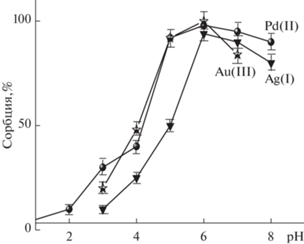
Оптимальное значение pH сорбции элементов в статическом и динамическом режимах составило рН 6. Характер зависимости сорбции от pH аналогичен для всех типов сорбентов, содержащих УНТ: УНТ(Ni), УНТ(Co) и УНТ(Fe), поэтому на рис. 2 приведены кривые лишь для МНЧ@УНТ(Ni).
Рис. 2.
Зависимость сорбции Au(III), Ag(I) и Pd(II) на МНЧ@УНТ(Ni) от pH раствора (концентрация сорбируемых ионов металлов 10 мкг/мл, объем раствора 10 мл).
Степень извлечения ионов металлов на магнитных сорбентах (табл. 1) составила 90–95%. Содержание сорбированных на композите ионов металлов определяли по разности содержаний в исходном растворе и в сливе. По разности между количеством сорбированных ионов и их содержанием в элюате определяли количество десорбированных ионов. Оптимальное время элюирования сорбированных ионов 6 мл 1 М HNO3 при постоянном перемешивании на качалке составило 30 мин.
Таблица 1.
Степень извлечения ионов Au(III), Ag(I) и Pd(II) из водного раствора магнитным сорбентом МНЧ@УНТ, содержащим углеродные нанотрубки различных морфологий, в оптимальных условиях сорбции и элюирования (n = 4, P = 0.95)
| Параметр сорбции | МНЧ@УНТ(Ni) | МНЧ@УНТ(Co) | МНЧ@УНТ(Fe) | ||||||
|---|---|---|---|---|---|---|---|---|---|
| Ag(I) (sr = 0.14) |
Au(III) (sr = 0.16) |
Pd(II) (sr = 0.15) |
Ag(I) (sr = 0.15) |
Au(III) (sr = 0.18) |
Pd(II) (sr = 0.16) |
Ag(I) (sr = 0.17) |
Au(III) (sr = 0.19) |
Pd(II) (sr = 0.18) |
|
| Введено, мкг | 50.0 | 50.0 | 50.0 | 50.0 | 50.0 | 50.0 | 50.0 | 50.0 | 50.0 |
| Сорбция, мкг | 48.5 ± 10.8 | 47.0 ± 12.0 | 48.0 ± 11.4 | 47.5 ± 11.3 | 46.0 ± 11.3 | 47.5 ± 12.1 | 47.0 ± 12.7 | 46.0 ± 14.0 | 47.0 ± 13.5 |
| Десорбция, мкг | 47.5 ± 10.5 | 45.5 ± 11.6 | 46.0 ± 11.0 | 46.5 ± 11.1 | 44.5 ± 12.7 | 46.0 ± 11.7 | 45.5 ± 12.3 | 45.0 ± 13.4 | 45.0 ± 12.9 |
| Степень извлечения, % | 95.0 | 91.0 | 92.0 | 93.0 | 90.0 | 92.0 | 91.0 | 90.0 | 90.0 |
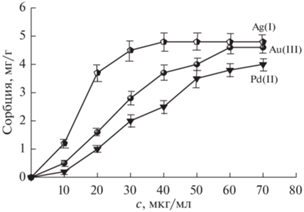
На рис. 3 приведены изотермы сорбции (при комнатной температуре) ионов Au(III), Ag(I) и Pd(II) на МНЧ@УНТ(Ni). Аналогичный вид имеют изотермы сорбции для УНТ(Co) и УНТ(Fe). Полученные величины сорбционной емкости всех типов магнитных сорбентов по отношению к благородным металлам в зависимости от соотношения компонентов приведены в табл. 2. Как видно, с уменьшением содержания МНЧ в композитах их сорбционная емкость увеличивается. Соотношение компонентов, соответствующее сорбентам с максимальной емкостью, равно 10 : 1 для всех композитов, содержащих УНТ, полученных на различных катализаторах. При таком соотношении намагниченность всех исследованных композитов еще достаточна для отделения сорбента от анализируемого раствора с помощью магнита. Как и следовало ожидать, максимальным значением емкости относительно всех элементов обладает МНЧ@УНТ(Ni), а минимальной – МНЧ@УНТ(Fe). Сорбционная емкость МНЧ@УНТ(Co) имеет промежуточное значение.
Таблица 2.
Сорбционная емкость композита МНЧ@УНТ (мг/г) с углеродными нанотрубками различных морфологий по отношению к ионам Au(III), Ag(I) и Pd(II) в зависимости от соотношения образующих его компонентов (n = 4, P = 0.95)
| Соотношение УНТ : МНЧ |
МНЧ@УНТ(Ni) | МНЧ@УНТ(Co) | МНЧ@УНТ(Fe) | ||||||
|---|---|---|---|---|---|---|---|---|---|
| Ag(I) (sr = 0.14) | Au(III) (sr = 0.16) | Pd(II) (sr = 0.15) | Ag(I) (sr = 0.15) | Au(III) (sr = 0.18) | Pd(II) (sr = 0.16) | Ag(I) (sr = 0.17) | Au(III) (sr = 0.19) | Pd(II) (sr = 0.18) | |
| 1 : 1 | 3.5 ± 0.8 | 3.4 ± 0.9 | 3.0 ± 0.7 | 2.9 ± 0.7 | 2.7 ± 0.8 | 2.3 ± 0.6 | 2.0 ± 0.5 | 1.5 ± 0.4 | 1.3 ± 0.4 |
| 2 : 1 | 4.6 ± 1.0 | 4.5 ± 1.1 | 4.0 ± 1.0 | 3.8 ± 0.9 | 3.5 ± 1.0 | 3.0 ± 0.8 | 2.5 ± 0.7 | 2.0 ± 0.6 | 2.0 ± 0.6 |
| 5 : 1 | 5.8 ± 1.3 | 5.6 ± 1.4 | 5.1 ± 1.2 | 4.8 ± 1.1 | 4.6 ± 1.3 | 3.8 ± 1.0 | 3.4 ± 0.9 | 2.3 ± 0.7 | 2.5 ± 0.7 |
| 10 : 1 | 6.5 ± 1.4 | 6.1 ± 1.6 | 5.5 ± 1.3 | 5.2 ± 1.2 | 5.0 ± 1.4 | 4.0 ± 1.0 | 3.7 ± 1.0 | 2.7 ± 0.8 | 2.8 ± 0.8 |
Механизм сорбции ионов металлов на окислительно-функционализированных УНТ не раз дискутировался в работах ученых различных стран и обсуждался нами в обзоре [12]. К настоящему времени утвердилось мнение, что механизм сорбции включает несколько физических и химических процессов, преобладающим из которых является ионный обмен между ионами металлов в водной фазе и протонами карбоксильных и карбонильных групп функционализированных УНТ. При этом известно, что при обработке УНТ более сильными окислителями (конц. HNO3, KMnO4) на поверхности нанотрубок образуются преимущественно карбоксильные функциональные группы. В большинстве работ обсуждается влияние на сорбционные свойства УНТ условий окисления: типа окислителя, температуры и времени обработки, кислотности среды или pH растворов, концентрации металлов. Введенные функциональные группы повышают отрицательный заряд поверхности углерода, соответственно увеличивая катионообменную емкость УНТ. Однако нами показано [10–12], что при одних и тех же условиях функционализации существенную роль играет морфология УНТ, определяющая способность к функционализации (введению кислородосодержащих групп), а следовательно, к повышению сорбционных свойств полученного материала. В свою очередь, морфология УНТ зависит от условий синтеза: температуры и типа катализатора. Именно это, по-видимому, является фундаментальной причиной существенного различия сорбционных свойств УНТ, функционализированных в одинаковых условиях, но полученных при разных условиях синтеза (в одном и том же CVD методе синтеза). Логично предположить, что более дефектные УНТ будут более восприимчивы к воздействию сильных окислителей при модификации, что подтверждается на практике. В УНТ, полученных на никелевом катализаторе, концентрация дефектов существенно больше, что облегчает введение кислородсодержащих групп. При синтезе УНТ на железном и кобальтовом катализаторах образуются более совершенные структуры, затрудняющие ввод кислородсодержащих групп, о чем свидетельствует более низкая кислотность поверхности, полученная после обработки конц. HNO3.
В то же время более разветвленная морфология УНТ влияет, видимо, и на электростатический механизм сорбции, внося определенный вклад в общую величину сорбции.
Поскольку нами показано, что определяющий вклад в величину сорбции на синтезированных магнитных сорбентах вносят УНТ [13], приведенные выше рассуждения по сорбции на УНТ можно отнести и к сорбции на композите, что подтверждено нами экспериментально в настоящей работе. Таким образом, различие в поведении магнитных сорбентов можно объяснить различающейся морфологией входящих в состав композита УНТ, полученных на различных катализаторах.
Показано [14], что в композите на основе УНТ(Ni) поверхность частиц шероховатая, имеются многочисленные изгибы и переплетения друг с другом. В композите МНЧ@УНТ(Fe) нанотрубки более прямые, имеют винтообразную форму и практически не переплетены между собой. В композите МНЧ@УНТ(Co) нанотрубки имеют как упорядоченные, так и скрученные участки, т.е. поверхность нанотрубок, выращенных как на кобальтовом, так и на железном катализаторах, существенно более гладкая, чем в случае никелевого. Магнитные частицы располагаются, как правило, в местах изгибов и дефектов УНТ. Таким образом, можно заключить, что сорбционная емкость магнитного композита по отношению к исследованным элементам тем выше, чем менее упорядочена структура УНТ, входящих в его состав.
Вторая важная часть работы состояла в выяснении возможности использования магнитных сорбентов с УНТ всех морфологий в динамическом режиме ТФЭ. Известно, что динамический вариант ТФЭ позволяет использовать для анализа большие объемы растворов и тем самым обеспечивает более низкие пределы обнаружения ионов металлов по сравнению со статическим вариантом благодаря высоким коэффицентам концентрирования. Было интересно выяснить, позволит ли модификация УНТ магнитными наночастицами использовать их в динамическом режиме ТФЭ. Установлено, что МНЧ@УНТ(Co) и МНЧ@УНТ(Fe), в отличие от индивидуальных УНТ(Co) и УНТ(Fe), легко можно засыпать в колонку через воронку, если с противоположного конца колонки расположить магнит. Вначале через колонку с композитом пропускали буферный раствор с pH 5.5–6.0, а затем анализируемый раствор, содержащий определяемые ионы металлов. Оптимальная скорость пропускания раствора и элюирования с помощью 6 мл 1 М HNO3 составляла 2 мл/мин. Элюат выпаривали на графитовом порошке ос. ч. и анализировали методом АЭС в дуге постоянного тока.
Для расчета количества ионов металлов в анализируемом растворе их содержание в концентрате на графитовом порошке делили на коэффициент концентрирования (Kконц), который определяли как соотношение массы анализируемого раствора к массе графитового порошка, на котором выпаривался элюат. Были достигнуты пределы определения элементов (сlim) на уровне 10–7 мас. % (табл. 3), которые оценивали по нижней точке градуировочного графика, найденной с приемлемой точностью [15]. Правильность результатов определения Au(III), Ag(I) и Pd(II) в водном растворе после их предварительного концентрирования на магнитном сорбенте динамическим методом ТФЭ проверяли методом введено–найдено. Результаты (табл. 3) свидетельствуют об отсутствии систематической погрешности в результатах определений.
Таблица 3.
Проверка правильности и пределы определения Au(III), Ag(I) и Pd(II) в водных растворах дуговым атомно-эмиссионным методом после их предварительного концентрирования на магнитных сорбентах в динамическом режиме (n = 4, Р = 0.95, объем раствора 100 мл, Kконц = 200)
| Элемент | Введено, мкг |
МНЧ@УНТ(Ni) | МНЧ@УНТ(Co) | МНЧ@УНТ(Fe) | сlim, мас. % |
|||
|---|---|---|---|---|---|---|---|---|
| найдено, мкг |
sr | найдено, мкг |
sr | найдено, мкг |
sr | |||
| Ag(I) | 10.0 | 9.2 ± 2.0 | 0.14 | 9.0 ± 2.1 | 0.15 | 8.8 ± 2.4 | 0.17 | 1 × 10–7 |
| Au(III) | 10.0 | 8.7 ± 2.1 | 0.16 | 8.8 ± 2.4 | 0.18 | 8.4 ± 2.5 | 0.19 | 5 × 10–7 |
| Pd(II) | 10.0 | 9.0 ± 2.1 | 0.15 | 9.2 ± 2.2 | 0.16 | 8.7 ± 2.5 | 0.18 | 3 × 10–7 |
Магнитный композит легко регенерируется 1 М HNO3 и может многократно использоваться для извлечения исследуемых ионов металлов из водных растворов. Для подтверждения этого изучали сорбцию ионов Au(III), Ag(I) и Pd(II) из водных растворов при pH 6 на регенерированных сорбентах. В табл. 4 приведены результаты сорбции только для ионов Ag(I), так как для остальных ионов получили аналогичные закономерности. Как видно, один и тот же последовательно регенерируемый сорбент МНЧ@УНТ можно использовать для извлечения исследуемых ионов из водных растворов не менее 10 раз. И лишь после этого его сорбционная способность начинает заметно уменьшаться. Дополнительно постоянно контролировали количество магнитных частиц, которые могли бы перейти в раствор из сорбента в процессе сорбции и элюирования исследуемых ионов. Для этого определяли содержание железа в каждом сливе и элюате. Установлено, что количество растворившихся магнитных частиц в процессе проведения одного цикла сорбции и десорбции очень незначительно и находится на уровне 5 × 10–3 мг. Потеря массы магнитных частиц после 10 циклов сорбции–десорбции составляла лишь 5 × 10–2 мг, что никак не сказывается на устойчивости и сорбционных возможностях магнитного сорбента.
Таблица 4.
Степень извлечения ионов Ag(I) из водного раствора магнитным сорбентом МНЧ@УНТ(Ni) в зависимости от кратности его использования (n = 4, Р = = 0.95, введено 50.0 мкг Ag(I))
| № экспери-мента | Десорбция, мкг | sr | Степень извлечения, % |
|---|---|---|---|
| 1 | 47.5 ± 9.0 | 0.12 | 95.0 |
| 2 | 47.0 ± 9.0 | 0.12 | 94.0 |
| 3 | 47.5 ± 8.3 | 0.11 | 95.0 |
| 4 | 46.5 ± 8.1 | 0.11 | 93.0 |
| 5 | 46.0 ± 8.8 | 0.12 | 92.0 |
| 6 | 46.5 ± 8.1 | 0.11 | 93.0 |
| 7 | 45.0 ± 9.3 | 0.13 | 92.0 |
| 8 | 47.0 ± 9.0 | 0.12 | 94.0 |
| 9 | 46.0 ± 9.5 | 0.13 | 92.0 |
| 10 | 44.0 ± 8.3 | 0.12 | 90.0 |
| 11 | 43.0 ± 7.5 | 0.11 | 86.0 |
| 12 | 40.0 ± 7.6 | 0.12 | 80.0 |
* * *
Таким образом, модификация УНТ магнитными наночастицами позволяет не только упростить и облегчить разделение фаз после сорбции элементов, но и решить более принципиальную и важную задачу использования УНТ(Co), УНТ(Fe) и УНТ(Ni) в качестве сорбентов. Здесь уместно напомнить, что ввиду высокой дисперсности и склонности к коагуляции, индивидуальные сорбенты УНТ(Co) и УНТ(Fe) практически непригодны для работы как в статическом, так и в динамическом вариантах ТФЭ из-за сложности разделения фаз после сорбции, а также невозможности заполнения ими хроматографической колонки. Открывшаяся возможность работы с этими сорбентами в динамическом режиме, а также многократного их использования повышает экономическую эффективность разработанного метода извлечения следов благородных металлов из водных сред, пригодного как для пробоподготовки в аналитической практике, так и для технологических целей. Полученные метрологические характеристики разработанного химико-атомно-эмиссионного метода анализа свидетельствуют о надежности и достаточно низких пределах определения ионов Au(III), Ag(I) и Pd(II).
Работа выполнена в рамках Госзадания 075-00355-21-00.
Список литературы
Толмачева В.В., Апяри В.В., Кочук Е.В., Дмитриенко С.Г. Магнитные сорбенты наночастиц оксидов железа для выделения и концентрирования органических соединений // Журн. аналит. химии. 2016. Т. 71. № 4. С. 339. (Tolmacheva V.V., Apyari V.V., Kochuk E.V., Dmitrienko S.G. Magnetic adsorbents based on iron oxide nanoparticles for preconcentration of organic compounds // J. Anal. Chem. 2016. V. 71. № 4. P. 321.)
Safarik I., Horska K., Pospiskova K., Safarikova M. Magnetically responsive activated carbons for bio- and environmental applications // Int. Rev. Chem. Eng. 2012. V. 4. P. 346.
Zhu M., Diao G. Review on the progress in synthesis and application of magnetic carbon nanocomposites // Nanoscale. 2011. V. 3. P. 2748.
Постнов В.Н., Родинков О.В., Москвин Л.Н., Новиков А.Г., Бугайченко А.С., Крохина О.А. От углеродных наноструктур к высокоэффективным сорбентам для хроматографического разделения и концентрирования // Успехи химии. 2016. Т. 85. № 2. С. 115. (Postnov V. N., Rodinkov O.V., Moskvin L.N., Novikov A.G., Bugaichenko A.S., Krokhina O.A. From carbon nanostructures to high-performance sorbents for chromatographic separation and preconcentration // Russ. Chem. Rev. 2016. V. 85. № 2. P. 115.)
Luo M, Liu D., Zhao L., Han J., Liang Y., Wang P., Zhou Z. A novel magnetic ionic liquid modified carbon nanotube for the simultaneous determination of aryloxyphenoxy-propionate herbicides and their metabolites in water // Anal. Chim. Acta. 2014. V. 852. P. 88.
Luo Y.B., Yu Q.W., Yuan B.F., Feng Y.Q. Fast microextraction of phthalate acid esters from beverage, environmental water and perfume samples by magnetic multi-walled carbon nanotubes // Talanta. 2012. V. 90. P. 123.
Chen C., Hu J., Shao D., Li J. Wang X. Adsorption behavior of multiwall carbon nanotube/iron oxide magnetic composites for Ni(II) and Sr(II) // J. Hazard. Mater. 2009. V. 164. P. 923.
Pistone A., Iannazzo D., Fazio M., Celegato F., Barrera G., Tiberto P., Giordano A., Azzerboni B., Galvagno S. Synthesis and magnetic properties of multiwalled carbon nanotubes decorated with magnetite nanoparticles // Phisica B. 2014. V. 435. P. 88.
Редькин А.Н., Кипин В.А., Маляревич Л.В. Синтез углеродных волокнистых наноматериалов из паров этанола на никелевом катализаторе // Неорг. материалы. 2006. Т. 42. № 3. С. 284. (Red’kin A.N., Kipin V.A., Malyarevich L.V. Synthesis of fibrous carbon nanomaterials from ethanol vapor on a nickel catalyst // Inorg. Mater. 2006. V. 42. № 3. P. 242.)
Гражулене С.С., Редькин А.Н., Телегин Г.Ф. Исследование корреляций между физико-химическими свойствами углеродных нанотрубок и типом катализатора для их синтеза // Журн. аналит. химии. 2012. Т. 67. № 5. С. 479. (Grazhulene S.S., Redkin A.N., Telegin G.F. Study of correlations between the physicochemical properties of carbon nanotubes and the nype of catalyst used for tyeir synthesis // J. Anal. Chem. 2012. V. 67. № 5. P. 423.)
Гражулене С.С., Редькин А.Н., Телегин Г.Ф., Баженов А.В., Фурсова Т.Н. Сорбционные свойства углеродных нанотрубок в зависимости от температуры их синтеза и последующей обработки // Журн. аналит. химии. 2010. Т. 65. № 7. С. 699. (Grazhulene S.S., Redkin A.N., Telegin G.F., Bazhenov A.V., Fursova T.N. Adsorption properties of carbon nanotubes depending on the temperature of their synthesis and subsequent treatment // J. Analt. Chem. 2010. V. 65. № 7. P. 682.)
Гражулене С.С., Редькин А.Н. Сорбенты на основе углеродных нанотрубок / Нанообъекты и нанотехнологии в химическом анализе / Под ред. Штыкова С.Н. М.: Наука, 2015. С. 375. (Grazhulene S., Red’kin A. Sorbents based on carbon nanotubes. In: Nanoanalytics: Nanoobjects and Nanotechnologies in Analytical Chemistry / Ed. Shtykov. S. De Gruyter, 2018. P. 343.)
Гражулене С.С., Золотарева Н.И., Редькин А.Н., Шилкина Н.Н., Митина А.А., Колесникова А.М. Магнитный сорбент на основе магнетита и модифицированных углеродных нанотрубок для извлечения некоторых токсичных элементов // Журн. при-кл. химии. 2018. Т. 91. № 11. С. 1642. (Grazhu-lene S.S., Zolotareva N.I., Redkin A.N., Shilkina N.N., Mitina A.A., Kolesnikova A.M. Magnetic sorbent based on magnetite and modified carbon nanotubes for extraction of some toxic elements // J. Appl. Chem. 2018. V. 91. № 11. P. 1847.)
Гражулене С.С., Золотарева Н.И., Редькин А.Н., Шилкина Н.Н., Митина А.А., Колесникова А.М., Ходос И.И. Сорбционные свойства магнитного композита на основе модифицированных углеродных нанотрубок в зависимости от условий синтеза // Журн. прикл. химии. 2020. Т. 93. № 1. С. 66. (Grazhulene S.S., Zolotareva N.I., Redkin A.N., Shilkina N.N., Mitina A.A., Kolesnikova A.M., Khodos I. I. Sorption properties of a magnetic composite based on modified carbon nanotubes: influence of the synthesis conditions // J. Appl. Chem. 2020. V. 93. № 1. P. 57.)
Экспериандова Л.П., Беликов К.Н., Химченко С.В., Бланк Т.А. Еще раз о пределах обнаружения и определения // Журн. аналит. химии. 2010. Т. 65. № 3. С. 229. (Eksperiandova L.P., Belikov K.N., Khimchenko S.V., Blank T.A. Once again about determination and detection limits // J. Anal. Chem. 2010. V. 65. № 3. P. 223.)
Дополнительные материалы отсутствуют.
Инструменты
Журнал аналитической химии