Журнал аналитической химии, 2022, T. 77, № 6, стр. 514-521
Вольтамперометрическое определение тартразина на электроде, модифицированном наночастицами диоксида церия и цетилтрифенилфосфоний бромидом
Г. К. Зиятдинова a, *, Г. К. Будников a
a Химический институт им. А.М. Бутлерова, Казанский федеральный университет
420008 Казань, ул. Кремлевская, 18, Россия
* E-mail: Ziyatdinovag@mail.ru
Поступила в редакцию 11.04.2021
После доработки 08.05.2021
Принята к публикации 08.05.2021
- EDN: JCMFMF
- DOI: 10.31857/S0044450222060202
Аннотация
Созданы стеклоуглеродные электроды (СУЭ), модифицированные наночастицами CeO2 и поверхностно-активными веществами (ПАВ) различной природы, и найдены вольт-амперные характеристики окисления тартразина на них. Электрод, модифицированный катионным ПАВ цетилтрифенилфосфония бромидом (ЦТФФБ), обеспечивает 72.5-кратное увеличение токов окисления тартразина по сравнению с СУЭ. Установлено, что окисление тартразина на CeO2-ЦТФФБ/СУЭ протекает необратимо с участием одного электрона и контролируется поверхностными процессами. Разработан способ вольтамперометрического определения тартразина на CeO2-ЦТФФБ/СУЭ. Диапазон определяемых содержаний составляет 2.50–250 мкМ тартразина с пределом обнаружения 2.4 мкМ. Предложенный способ применен для определения содержания тартразина в напитке “Тархун”.
Для восстановления цвета, утраченного в процессе технологической обработки, или улучшения внешнего вида продуктов питания активно используются красители. Среди большого разнообразия пищевых красителей можно отметить тартразин (5-окси-1-(п-сульфофенил)-4-[(п-сульфофенил)-азо]-пиразол-3-карбоновой кислоты тринатриевая соль). В пищевой промышленности он маркируется как пищевая добавка Е102 [1]. Тартразин входит в состав безалкогольных напитков, соков, желе, конфет, пирожных, хлопьев, супов и других продуктов [2]. Однако тартразин, как и другие синтетические красители, проявляет токсические свойства, зависящие от его концентрации. Высокая концентрация тартразина в сочетании с бензоатом натрия – консервантом, присутствующим в пищевых продуктах, может вызывать гиперактивность у детей, аллергию и астму [1]. В результате распада красителя в организме под действием азоредуктазы образуются токсичные ароматические амины [2]. В связи с этим необходимо строго контролировать содержание тартразина в пищевых продуктах, что требует экспрессных, чувствительных и селективных способов его определения.
Азо- и гидроксильная группы в структуре тартразина электрохимически активны, поэтому для определения тартразина предложен широкий круг электрохимических способов. Так, рассмотрено электровосстановление тартразина на стеклоуглеродном электроде (СУЭ) в кислой среде [3]. Показано, что в условиях адсорбционной инверсионной вольтамперометрии диапазон определяемых содержаний составляет 0.05–0.50 мг/л с пределом обнаружения 0.011 мг/л. Для повышения чувствительности определения тартразина разработан ряд химически модифицированных электродов на основе поверхностно-активных веществ (ПАВ) [4], углеродных наноматериалов [5, 6], наночастиц металлов [7, 8], полимерных покрытий [9] и их сочетаний [10–12]. Для повышения селективности определения тартразина созданы электроды на основе полимеров с молекулярными отпечатками [13–15]. Определение проводят по уменьшению токов восстановления K3Fe(CN)6 в присутствии тартразина [13, 15]. Аналитические характеристики вольтамперометрического определения тартразина на модифицированных электродах представлены в табл. 1.
Таблица 1.
Аналитические характеристики вольтамперометрического определения тартразина на химически модифицированных электродах
| Электрод | Метод | ПрО, мкМ | Диапазон определяемых содержаний, мкМ | Литера-тура |
|---|---|---|---|---|
| УПЭ-додецилсульфат натрия | ЦВА | 5.2 | 20–50, 60–110 | [4] |
| Пиролитический ГЭ/МУНТ | ЦВА | 0.93 | 3.7–130, 130–430 | [5] |
| СУЭ/расслоенный графит | АдАДИВ | 0.0028 | 0.0094–0.37 | [6] |
| СУЭ/нанолисты Bi с хитозаном | ДИВ | 15.12 | 24–980, 980–2780 | [7] |
| УПЭ-наночастицы золота | ДИВ | 0.017 | 0.05–1.5 | [8] |
| УПЭ/полиглицин | ЦВА | 0.283 | 1–27, 35–87 | [9] |
| СУЭ/электровосстановленный оксид графена-TiO2 | ДВА второго порядка | 0.008 | 0.020–20 | [10] |
| ГЭ/поли(L-фенилаланин)/графен | ДИВ | 1.54 | 2.0–100 | [11] |
| УПЭ-наночастицы ZnO/поли(п-аминобензолсульфоновая кислота) | ДИВ | 0.080 | 0.0349–1.246, 1.246–5.44 | [12] |
| СУЭ/ПМО на основе полипиролла | КВВ | 0.001 | 0.001–0.010 | [13] |
| СУЭ/МУНТ-1-пропаргил-3-бутилимидазолий бромид@наночастицы Pt/ПМО на основе 4-винилпиридина | ДИВ | 0.008 | 0.03–5.0, 5.0–20 | [14] |
| СУЭ/ПМО на основе со-электрополимеризованных м-дигидроксибензола и о-фенилендиамина | ДИВ | 0.0035 | 0.005–1.1 | [15] |
Обозначения: ПрО – предел обнаружения, УПЭ – угольно-пастовый электрод, ГЭ – графитовый электрод, МУНТ – многостенные углеродные нанотрубки, ЦВА – циклическая вольтамперометрия, СУЭ – стеклоуглеродный электрод, АдАДИВ – адсорбционная анодная дифференциально-импульсная вольтамперометрия, ДИВ – дифференциально-импульсная вольтамперометрия, ДВА – дифференциальная вольтамперометрия, ПМО – полимер с молекулярными отпечатками, КВВ – квадратно-волновая вольтамперометрия.
Наночастицы CeO2 в сочетании с ПАВ представляют интерес в качестве модификатора электродной поверхности. Такой подход обеспечивает значительное повышение чувствительности и более низкие пределы обнаружения целевых аналитов, что показано на примере природных фенольных антиоксидантов [16–19]. При этом модифицированные электроды не проявляют электрохимическую активность. Это позволяет регистрировать собственный аналитический сигнал определяемого соединения, что повышает его селективность. Применительно к пищевым красителям такое сочетание модификаторов в литературе не описано.
В настоящей работе для определения тартразина предложен СУЭ, модифицированный наночастицами CeO2 и поверхностно-активными веществами.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Реагенты и растворы. Использовали тартразин (85%, Sigma, США), цетилпиридиний бромид (ЦПБ) (98%, Aldrich, Германия), цетилтриметиламмоний бромид (ЦТАБ) (99% Acros Organics, Бельгия), цетилтрифенилфосфоний бромид (ЦТФФБ) (синтезирован на кафедре высокомолекулярных и элементорганических соединений Химического института им. А.М. Бутлерова КФУ), додецилсульфат натрия (ДДС) фармакопейной чистоты (Panreac, Испания), Brij® 35 (Acros Organics, Бельгия) и Triton X-100 (Aldrich, Германия). Остальные реактивы были марки х. ч.
Cтандартный 10 мМ раствор тартразина готовили по точной навеске, которую растворяли в 5.0 мл дистиллированной воды. Более разбавленные растворы готовили непосредственно перед измерениями в мерных колбах емк. 5.0 мл, доводя до метки дистиллированной водой.
Растворы ПАВ (5.0 мМ растворы ЦПБ и ЦТАБ, 3.0 мМ ЦТФФБ, 10 мМ ДДС, Brij® 35 и Triton X-100) готовили, растворяя точные навески в дистиллированной воде. Более разбавленные растворы готовили соответствующим разбавлением стандартных растворов.
Модифицирование электрода. В качестве модификатора поверхности электрода использовали водную дисперсию, содержащую 10 мас. % наночастиц CeO2, с размером частиц <25 нм (Sigma-Aldrich, США). Рабочие дисперсии в растворах ПАВ различной природы и концентрации готовили последовательным разбавлением с последующей ультразвуковой обработкой в течение 10 мин. Концентрацию наночастиц варьировали от 0.5 до 1.5 мг/мл.
На поверхность СУЭ наносили 3 мкл суспензии методом капельного испарения. Перед модификацией рабочую поверхность СУЭ обновляли механически, полируя оксидом алюминия с размером частиц 0.05 мкм. Затем электрод ополаскивали ацетоном и дистиллированной водой.
Вольтамперометрические и хроноамперометрические измерения проводили на потенциостате/гальваностате Autolab PGSTAT 302N (Eco Chemie B.V., Нидерланды) с программным обеспечением NOVA 1.10.1.9 в трехэлектродной электрохимической ячейке объемом 10.0 мл. Использовали рабочий СУЭ (CH Instruments, Inc., США, площадь поверхности 7.07 мм2) и СУЭ, модифицированный наночастицами CeO2, насыщенный хлоридсеребряный электрод сравнения и вспомогательный платиновый электрод. Для расчетов в вольтамперометрии применяли коррекцию базовой линии по программе NOVA 1.10.1.9, что позволило точнее измерять параметры пиков. В электрохимическую ячейку вносили фоновый электролит и аликвоту раствора тартразина (общий объем раствора в ячейке 5.0 мл) и регистрировали дифференциально-импульсные вольтамперограммы при амплитуде импульса 50 мВ и времени импульса 50 мс или циклические вольтамперограммы от 0.4 до 1.5 В при различных скоростях сканирования потенциала. Для количественного определения тартразина использовали вольтамперометрию с линейной разверткой потенциала от 0.4 до 1.6 В со скоростью 250 мВ/с.
Для определения рН фонового электролита использовали рН-метр Эксперт-001 (ООО “Эконикс-Эксперт”, Россия).
Анализ реальных образцов проводили после предварительной дегазации в ультразвуковой ванне в течение 10 мин. В электрохимическую ячейку вносили 500 мкл напитка “Тархун” и регистрировали вольтамперограммы с линейной разверткой потенциала в диапазоне от 0.4 до 1.6 В со скоростью изменения потенциала 250 мВ/с.
Статистическую обработку результатов проводили для 5 измерений при доверительной вероятности 0.95. Результаты представляли как X ± ΔX, где X – среднее значение и ΔX – доверительный интервал. Случайную погрешность определения оценивали по величине относительного стандартного отклонения (sr). Регрессионный анализ выполняли в программе OriginPro 8.0 (OriginLab, США).
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Установлено, что тартразин окисляется на СУЭ при 0.890 В на фоне фосфатного буферного раствора с рН 7.0 (рис. 1). Несмотря на высокую концентрацию тартразина в ячейке (100 мкМ), токи окисления составляют 12 ± 4 нА даже в дифференциально-импульсном режиме, что не позволяет использовать СУЭ для аналитических целей. В связи с этим рассмотрели СУЭ, модифицированные наночастицами CeO2, диспергированными в ПАВ. Следует отметить, что наночастицы CeO2 имеют при рН 7.0 частичный отрицательный поверхностный заряд [20], что обусловливает их электростатическое взаимодействие с положительно заряженными “головами” катионных ПАВ. Для анионного ПАВ ДДС в этих условиях наблюдается электростатическое отталкивание, а в случае неионогенных ПАВ ключевую роль, вероятно, играют гидрофобные взаимодействия. Таким образом, катионные ПАВ более прочно удерживаются на электродной поверхности.
Рис. 1.
Дифференциально-импульсные вольтамперограммы 100 мкМ тартразина на стеклоуглеродном электроде (1) на фоне фосфатного буферного раствора с рН 7.0 (2). Амплитуда импульса 50 мВ, время импульса 50 мс, скорость изменения потенциала 10 мВ/с.

Варьирование природы ПАВ показало, что для всех рассматриваемых ПАВ происходит увеличение токов окисления тартразина по сравнению с СУЭ (табл. 2). Более высокие токи окисления наблюдаются на электродах, модифицированных катионными ПАВ, что объясняется электростатическими взаимодействиями катионного ПАВ с тартразином, присутствующим при рН 7.0 в виде аниона (pKa1 = 2.0, pKa2 = 5.0, pKa3 = 10.89) [21]. Кроме того, сравнение токов окисления для ЦТАБ, ЦПБ и ЦТФФБ иллюстрирует вклад гидрофобных взаимодействий, в частности взаимодействий ароматических колец в структуре ПАВ и тартразина. Максимальные токи наблюдаются в случае ЦТФФБ, обладающего наибольшей гидрофобностью среди изученных катионных ПАВ. Пик окисления тартразина расщепляется на два в случае катионных ЦТАБ и ЦПБ (табл. 2). Аналогичный эффект описан для эвгенола на CeO2-ДДС/СУЭ [16], а также характерен для электроокисления органических соединений в ПАВ-содержащих средах и объясняется изменением скорости переноса электрона [22]. Это также подтверждается смещением потенциалов окисления тартразина.
Таблица 2.
Вольт-амперные характеристики окисления тартразина на электродах, модифицированных CeO2 и ПАВ различной природы (cПАВ = 0.10 мМ, n = 5, P = 0.95)
| Электрод | E, В | I, мкA |
|---|---|---|
| СУЭ | 0.890 | 0.012 ± 0.004 |
| CeO2-ДДС/СУЭ | 0.890 | 0.17 ± 0.04 |
| CeO2-ЦТАБ/СУЭ | 0.750 | 0.078 ± 0.03 |
| 0.910 | 0.18 ± 0.01 | |
| CeO2-ЦПБ/СУЭ | 0.745 | 0.27 ± 0.01 |
| 0.900 | 0.31 ± 0.02 | |
| CeO2-ЦТФФБ/СУЭ | 1.02 | 0.87 ± 0.03 |
| CeO2-Brij® 35/СУЭ | 0.900 | 0.21 ± 0.01 |
| CeO2-Triton X-100/СУЭ | 0.895 | 0.087 ± 0.005 |
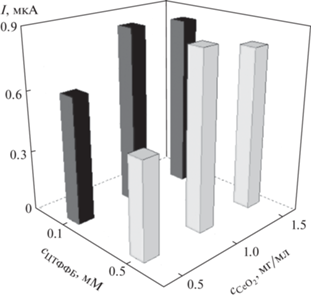
Оценено влияние концентрации наночастиц CeO2 и ЦТФФБ в дисперсии на вольт-амперные характеристики тартразина. Установлено, что потенциалы окисления при этом не изменяются, а токи окисления варьируются статистически значимо (рис. 2). При увеличении концентрации наночастиц СeO2 до 1.0 мг/мл наблюдается увеличение токов окисления независимо от концентрации ЦТФФБ. А при переходе к концентрации наночастиц СeO2 1.5 мг/мл токи уменьшаются, причем для содержания ЦТФФБ 0.10 мМ статистически недостоверно. Таким образом, для дальнейших исследований выбрали электрод, полученный на основе концентрации наночастиц СeO2 1.0 мг/мл в 0.10 мМ растворе ЦТФФБ.
Рис. 2.
Влияние концентраций наночастиц СeO2 и бромида цетилтрифенилфосфония на токи окисления 100 мкМ тартразина на фоне фосфатного буферного раствора с pH 7.0 по данным дифференциально-импульсной вольтамперометрии.
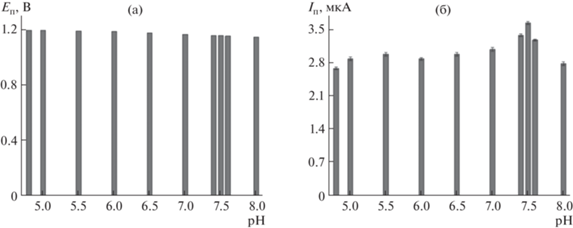
Изучено электроокисление тартразина на CeO2-ЦТФФБ/СУЭ (рис. 3). Варьирование рН фонового электролита от 4.8 до 8.0 показало, что потенциал окисления тартразина смещается в область меньших значений по мере увеличения рН фонового электролита (рис. 3а), что свидетельствует об участии протонов в электродной реакции. Токи окисления тартразина постепенно увеличиваются вплоть до рН 7.5, а затем резко уменьшаются (рис. 3б). Дальнейшие исследования проводили при рН 7.5.
Рис. 3.
Влияние рН фонового электролита на потенциал (а) и токи окисления (б) 250 мкМ тартразина по данным циклической вольтамперометрии. Скорость изменения потенциала 100 мВ/с.
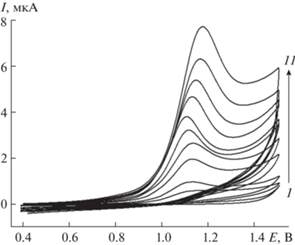
Для установления природы электрохимического процесса оценили влияние скорости изменения потенциала на токи окисления тартразина (рис. 4). Показано, что окисление контролируется адсорбцией аналита, что подтверждается линейной зависимостью токов окисления от v (уравнение (1)) и значением тангенса угла наклона зависимости lnIп от ln v (уравнение (2)):
(1)
$\begin{gathered} {{I}_{{\text{п}}}}\left( {{\text{мкА}}} \right) = \left( {0.06 \pm 0.02} \right) + \\ + \,\,\left( {0.0189 \pm 0.0001} \right)v\,\,({\text{мВ/с}}),~ \\ {{R}^{2}} = 0.9995, \\ \end{gathered} $(2)
$\begin{gathered} {\text{ln}}{{I}_{{\text{п}}}}\,\,({\text{мкA}}) = \left( {2.86 \pm 0.03} \right) + \left( {0.95 \pm 0.01} \right)\ln v{\text{ }}({\text{В/с}}), \\ {{R}^{2}} = 0.9992.~~~ \\ \end{gathered} $Рис. 4.
Циклические вольтамперограммы 100 мкМ тартразина на CeO2-ЦТФФБ/СУЭ на фоне фосфатного буферного раствора с pH 7.5 (1) в зависимости от скорости изменения потенциала: 2 – 10, 3 – 25, 4 – 50, 5 – 75, 6 – 100, 7 – 120, 8 – 150, 9 – 175, 10 – 200, 11 – 250 мВ/с.
Отсутствие катодной ступени на циклических вольтамперограммах и смещение потенциала окисления тартразина в область более положительных значений по мере увеличения υ свидетельствуют о необратимом окислении. Потенциал окисления линейно увеличивается в зависимости от lnv согласно уравнению (3):
(3)
$\begin{gathered} {{Е}_{{\text{п}}}}\left( {\text{В}} \right) = \left( {1.225 \pm 0.002} \right) + \\ + \,\,\left( {0.050 \pm 0.001} \right)\ln v{\text{ }}\left( {{\text{В/с}}} \right),~ \\ {{R}^{2}} = 0.9979. \\ \end{gathered} $Согласно уравнению Лавирона [23] (уравнение (4)) αаn = 0.51.
(4)
${{E}_{{\text{p}}}} = {{E}^{{0'}}} + \frac{{RT}}{{{{\alpha }_{{\text{a}}}}nF}}\ln \frac{{RT{{k}_{s}}}}{{{{\alpha }_{{\text{a}}}}nF}} + \frac{{RT}}{{{{\alpha }_{{\text{a}}}}nF}}\ln v.$Для необратимого процесса αа = 0.5 [24]. Тогда число электронов, участвующих в реакции, равно 1, что хорошо согласуется с данными для других модифицированных электродов [9–12]. Таким образом, с учетом данных [9–12] тартразин окисляется на CeO2-ЦТФФБ/СУЭ с участием одного электрона и одного протона согласно схеме 1 .
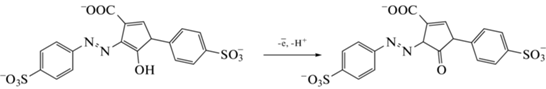
Схема 1 . Окисление тартразина на стеклоуглеродном электроде, модифицированном наночастицами CeO2 и бромидом цетилтрифенилфосфония.
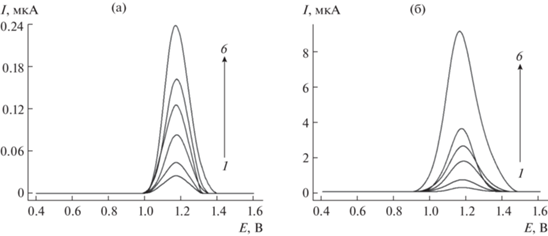
Для количественного определения тартразина использовали вольтамперометрию с линейной разверткой потенциала. При этом на вольтамперограммах наблюдается четко выраженный пик окисления при 1.17 В (рис. 5), высота которого линейно связана с концентрацией тартразина в диапазоне 1.0–15 и 15–250 мкМ (уравнения (5) и (6)).
(5)
$\begin{gathered} {{I}_{{\text{п}}}}\left( {{\text{мкА}}} \right) = \left( {0.008 \pm 0.002} \right) + \left( {14.9 \pm 0.2} \right) \times {{10}^{3}}с({\text{M}}), \\ {{R}^{2}} = 0.9990, \\ \end{gathered} $(6)
$\begin{gathered} {{I}_{{\text{п}}}}\left( {{\text{мкА}}} \right) = \left( {--0.25 \pm 0.04} \right) + \\ + \,\,\left( {37.9 \pm 0.3} \right) \times {{10}^{3}}с\left( {\text{M}} \right),~~~~~~~~~~ \\ {{R}^{2}} = 0.9997. \\ \end{gathered} $Рис. 5.
Вольтамперограммы с линейной разверткой потенциала для тартразина различной концентрации на CeO2-ЦТФФБ/СУЭ на фоне фосфатного буферного раствора с pH 7.5. (a): 1 – 1.0, 2 – 2.5, 3 – 5.0, 4 – 7.5, 5 – 10, 6 – 15 мкМ. (б): 1 – 15, 2 – 25, 3 – 50, 4 – 75, 5 – 100, 6 – 250 мкМ. Скорость изменения потенциала 250 мВ/с.
Предел обнаружения тартразина составляет 0.40 мкМ. Полученные характеристики превосходят описанные для некоторых других химически модифицированных электродов (табл. 1). Кроме того, предложенный электрод характеризуется более простой и экспрессной процедурой изготовления.
Выполнено определение тартразина в модельных растворах. Правильность результатов оценена по методу введено–найдено (табл. 3). Величина относительного стандартного отклонения не превышает 2%. Значения меры правильности свидетельствуют о высокой надежности результатов, получаемых с применением разработанного подхода.
Таблица 3.
Результаты вольтамперометрического определения тартразина в модельных растворах на CeO2-ЦТФФБ/СУЭ на фоне фосфатного буферного раствора с рН 7.5 (n = 5, P = 0.95)
| Введено, мкг | Найдено, мкг | sr | R, % |
|---|---|---|---|
| 2.67 | 2.7 ± 0.1 | 0.049 | 101 ± 4 |
| 13.3 | 13.3 ± 0.2 | 0.015 | 100 ± 2 |
| 26.7 | 26.7 ± 0.3 | 0.0085 | 100 ± 1 |
| 200 | 201 ± 4 | 0.015 | 100 ± 2 |
| 668 | 669 ± 4 | 0.0045 | 100.1 ± 0.6 |
Показана селективность отклика тартразина в присутствии 1000-кратных избытков неорганических ионов (K+, Mg2+, Ca2+, ${\text{NO}}_{3}^{ - },$ Cl– и ${\text{SO}}_{4}^{{2 - }}$), 100-кратных избытков глюкозы, рамнозы и сахарозы, арабиногалактана и аскорбиновой кислоты, а также пищевого красителя желтого “солнечного заката”, который часто используется совместно с тартразином.
Разработанный подход применен для определения тартразина в напитках “Тархун”. На вольтамперограммах регистрируется четко выраженный пик окисления тартразина при 1.17 В (рис. 6), что подтверждается данными метода добавок. Степень открытия составляет 100–101%, что свидетельствует о высокой точности определения и об отсутствии матричных эффектов.
Рис. 6.
Вольтамперограммы с линейной разверткой потенциала напитка “Тархун” (1 – 500 мкл напитка, 2 – 500 мкл напитка + 3.7 мкМ тартразина, 3 – 500 мкл напитка + 5.6 мкМ тартразина) на CeO2-ЦТФФБ/СУЭ на фоне фосфатного буферного раствора с pH 7.5.

Результаты определения тартразина представлены в табл. 4. Полученные содержания согласуются с данными спектрофотометрического определения [25] и не превышают регламентируемый верхний предел содержания тартразина в напитках [26]. Вычисленные значения t- и F-критериев меньше критических при P = 0.95, что свидетельствует об отсутствии систематических погрешностей измерений и равноточности методов вольтамперометрии и спектрофотометрии. Предложенный метод характеризуется достаточной чувствительностью и высокой точностью, а также простотой и доступностью, что позволяет применять его в лабораториях по контролю качества напитков.
Таблица 4.
Результаты определения тартразина в напитках “Тархун” (n = 5, P = 0.95)
| № | Найдено вольтамперометрически, мг/мл | sr | Найдено спектрофотометрически, мг/мл | sr | t* | F** |
|---|---|---|---|---|---|---|
| 1 | 29.9 ± 0.7 | 0.019 | 31 ± 2 | 0.025 | 1.96 | 1.99 |
| 2 | 38.8 ± 0.8 | 0.016 | 38 ± 4 | 0.040 | 1.17 | 6.11 |
| 3 | 26 ± 1 | 0.044 | 27 ± 2 | 0.030 | 1.20 | 2.07 |
Авторы выражают благодарность д.х.н., профессору кафедры высокомолекулярных и элементорганических соединений Химического института им. А.М. Бутлерова Казанского федерального университета И.В. Галкиной за предоставление цетилтрифенилфосфоний бромида.
Список литературы
Aguilar F., Charrondiere U.R., Dusemund B., Galtier P., Gilbert J., Gott D.M., Grilli S., Guertler R., Koenig J., Lambré C., Larsen J-C., Leblanc J-C., Mortensen A., Parent-Massin D., Pratt I., Rietjens I.M.C.M., Stankovic I., Tobback P., Verguieva T., Woutersen R.A. Scientific opinion on the re-evaluation tartrazine (E102) // EFSA J. 2009. V. 7. № 11. Article 1331.
Demirkol O., Zhang X., Ercal N. Oxidative effects of tartrazine (CAS No 1934-21-0) and new coccin (CAS No. 2611-82-7) azo dyes on CHO cells // J. Verbr. Lebensm. 2012. V. 7. № 3. P. 229.
Липских О.И., Николаева А.А., Короткова Е.И. Вольтамперометрическое определение тартразина в пищевых продуктах // Журн. аналит. химии. 2017. Т. 72. № 4. С. 341. (Lipskikh O.I., Nikolaeva A.A., Korotkova E.I. Voltammetric determination of tartrazine in food // J. Anal. Chem. 2017. V. 72. № 4. P. 396.)
Raril C., Manjunatha J.G. Development of sodium dodecyl sulfate based electrochemical sensor for tartrazine determination // Portugal. Electrochim. Acta. 2021. V. 39. № 1. P. 59.
Song Y.Z., Xu J.M., Lv J.S., Zhong H., Ye Y., Xie J.M. Electrochemical reduction of tartrazine at multi-walled carbon nanotube-modified pyrolytic graphite electrode // Russ. J. Phys. Chem. A. 2012. V. 86. № 2. P. 303.
Song X., Shi Z., Tan X., Zhang S., Liu G., Wu K. One-step solvent exfoliation of graphite to produce a highly-sensitive electrochemical sensor for tartrazine // Sens. Actuators B. 2014. V. 197. P. 104.
Asadpour-Zeynali K., Aleshi M. Electrochemical modification of glassy-carbon electrode by bismuth-chitosan nanosheets for electrocatalytic reduction and determination of tartrazine // Portugal. Electrochim. Acta. 2014. V. 32. № 6. P. 369.
Ghoreishi S.M., Behpour M., Golestaneh M. Selective voltammetric determination of tartrazine in the presence of red 10b by nanogold-modified carbon paste electrode // J. Chin. Chem. Soc. 2013. V. 60. № 1. P. 120.
Manjunatha J.G. A novel voltammetric method for the enhanced detection of the food additive tartrazine using an electrochemical sensor // Heliyon. 2018. V. 4. № 11. Article e00986. 14 p.
He Q., Liu J., Liu X., Li G., Deng P., Liang J., Chen D. Sensitive and selective detection of tartrazine based on TiO2-electrochemically reduced graphene oxide composite-modified electrodes // Sensors. 2018. V. 18. № 6. Article 1911.
Tahtaisleyen S., Gorduk O., Sahin Y. Electrochemical determination of tartrazine using a graphene/poly(L-phenylalanine) modified pencil graphite electrode // Anal. Lett. 2020. V. 53. № 11. P. 1683.
Karim-Nezhad G., Khorablou Z., Zamani M., Dorraji P.S., Alamgholiloo M. Voltammetric sensor for tartrazine determinationin soft drinks using poly (p-aminobenzenesulfonic acid)/zinc oxide nanoparticles in carbon paste electrode // J. Food Drug Anal. 2017. V. 25. № 2. P. 293.
Jiang S., Xu J., Xu P., Liu L., Chen Y., Qiao C., Yang S., Sha Z., Zhang J. A novel molecularly imprinted sensor for direct tartrazine detection // Anal. Lett. 2014. V. 47. № 2. P. 323.
Zhao L.J., Zeng B.Z., Zhao F.Q. Electrochemical determination of tartrazine using a molecularly imprinted polymer – multiwalled carbon nanotubes – ionic liquid supported Pt nanoparticles composite film coated electrode // Electrochim. Acta. 2014. V. 146. P. 611.
Zhao X., Liu Y., Zuo J., Zhang J., Zhu L., Zhang J. Rapid and sensitive determination of tartrazine using a molecularly imprinted copolymer modified carbon electrode (MIP-PmDB/PoPD-GCE) // J. Electroanal. Chem. 2017. V. 785. P. 90.
Ziyatdinova G., Ziganshina E., Romashkina S., Budnikov H. Highly sensitive amperometric sensor for eugenol quantification based on CeO2 nanoparticles and surfactants // Electroanalysis. 2017. V. 29. № 4. P. 1197.
Ziyatdinova G., Ziganshina E., Nguyen Cong Ph., Budnikov H. Voltammetric determination of thymol in oregano using CeO2-modified electrode in Brij® 35 micellar medium // Food Anal. Methods. 2017. V. 10. № 1. P. 129.
Ziyatdinova G., Ziganshina E., Shamsevalieva A., Budnikov H. Voltammetric determination of capsaicin using CeO2-surfactant/SWNT-modified electrode // Arab. J. Chem. 2020. V. 13. № 1. P. 1524.
Зиятдинова Г.К., Захарова С.П., Зиганшина Э.Р., Будников Г.К. Вольтамперометрическое определение флавоноидов в лекарственном растительном сырье на электродах, модифицированных наночастицами диоксида церия и поверхностно-активными веществами // Журн. аналит. химии. 2019. Т. 74. № 8. С. 613. (Ziyatdinova G.K., Zakharova S.P., Ziganshina E.R., Budnikov H.C. Voltammetric determination of flavonoids in medicinal plant materials using electrodes modified by cerium dioxide nanoparticles and surfactants // J. Anal. Chem. 2019. V. 74. № 8. P. 816.)
Berg J.M., Romoser A., Banerjee N., Zebda R., Sayes C.M. The relationship between pH and zeta potential of ~30 nm metal oxide nanoparticle suspensions relevant to in vitro toxicological evaluations // Nanotoxicology. 2009. V. 3. № 4. P. 276.
Klett C., Barry A., Balti I., Lelli P., Schoenstein F., Jouini N. Nickel doped Zinc oxide as a potential sorbent for decolorization of specific dyes, methylorange and tartrazine by adsorption process // J. Environ. Chem. Eng. 2014. V. 2. № 2. P. 914.
Зиятдинова Г.К., Зиганшина Э.Р., Будников Г.К. Использование поверхностно-активных веществ в вольтамперометрическом анализе // Журн. аналит. химии. 2012. Т. 67. № 11. С. 968. (Ziyatdinova G.K., Ziganshina E.R., Budnikov H.C. Application of surfactants in voltammetric analysis // J. Anal. Chem. 2012. V. 67. № 11. P. 869.)
Laviron E. Adsorption, autoinhibition and autocatalysis in polarography and in linear potential sweep voltammetry // J. Electroanal. Chem. 1974. V. 52. № 3. P. 355.
Bard A.J., Faulkner L.R. Electrochemical methods, fundamentals and applications. 2nd Ed. New York: John Wiley& Sons Inc., 2001. 850 p.
Güler Z. Determination of synthetic colorants in confectionery and instant drink powders consumed in turkey using UV/VIS spectrophotometry // J. Food Quality. 2005. V. 28. № 1. P. 98.
СанПиН 2.3.2.1293-03. Гигиенические требования по применению пищевых добавок М.: МинздравРоссии, 2003. 416 с.
Дополнительные материалы отсутствуют.
Инструменты
Журнал аналитической химии