Журнал аналитической химии, 2023, T. 78, № 1, стр. 64-73
Газохроматографическая идентификация необычных нестабильных продуктов частичного гидролиза тетраэтоксисилана
И. Г. Зенкевич a, *, Д. А. Баранов a
a Санкт-Петербургский государственный университет, Институт химии
198504 Санкт-Петербург, Университетский просп., 26, Россия
* E-mail: izenkevich@yandex.ru
Поступила в редакцию 10.04.2022
После доработки 07.05.2022
Принята к публикации 07.05.2022
- EDN: KKVZCM
- DOI: 10.31857/S0044450223010152
Аннотация
Газохроматографический анализ долго хранившегося образца тетраэтоксисилана (тетраэтилортосиликат) показал, что в нем отсутствует основной компонент вследствие гидролиза этого соединения следами воды. Вместо него обнаружены этанол и три других компонента с индексами удерживания (RI) на колонке с неподвижной фазой НР-5 537 ± 2 (№ 1), 608 ± 1 (№ 2, основной) и 727 ± 3 (№ 3). Компоненты нестабильны, не могут быть препаративно выделены и в результате ранее не были охарактеризованы. Для их идентификации охарактеризованы химические свойства этого образца, рассмотрена рекуррентная аппроксимация значений RI обнаруженных компонентов и их корреляция с индексами удерживания структурных аналогов. Установлено, что они являются конгенерами исходного тетраэтоксисилана и представляют собой достаточно “экзотические” продукты его частичного гидролиза: триэтоксисиланол (C2H5O)3SiOH, диэтоксисиландиол (C2H5O)2Si(OH)2, и этоксисилантриол (C2H5O)Si(OH)3. В соответствии с литературными данными некоторые силандиолы R2Si(OH)2 и силантриолы RSi(OH)3 достаточно стабильны, в особенности соединения, содержащие заместители, способные к сопряжению с вакантными d-орбиталями атомов кремния. К их числу относятся фенил- (π−d-системы сопряжения) и алкоксизамещенные (p−d-системы) силандиолы и -триолы. Идентифицированные продукты частичного гидролиза тетраэтокисилана относятся ко второму типу.
Нестабильность компонентов анализируемых образцов, в том числе в ходе их хроматографического разделения, существенно осложняет все стадии определения. Несоответствие регистрируемых сигналов числу и химической природе компонентов проб часто приводит к ошибкам и парадоксам в интерпретации результатов [1]. По этой причине примеры нестабильности аналитов как до, так и в процессе анализа заслуживают специального рассмотрения [2]. Одним из подобных соединений является тетраэтоксисилан (C2H5O)4Si (ТЭОС, TEOS, тетраэтилортосиликат, CAS № 78-10-4) – наиболее известный представитель класса тетраалкоксисиланов. В целом этот класс можно считать достаточно подробно охарактеризованным аналитическими параметрами; в базе NIST представлены масс-спектры девяти гомологов тетраалкоксисиланов С4–С16, для восьми из которых известны газохроматографические индексы удерживания (RI) на полидиметилсилоксановых неподвижных фазах, содержащих 5% фенильных групп (так называемые semi-standard фазы [3]).
Тетраэтоксисилан широко применяют в качестве сшивающего (crosslinking) агента для силиконовых полимеров, прекурсора для получения особо чистого диоксида кремния в промышленности полупроводников, при синтезе цеолитов, как компонента гидрофобных покрытий, самоотверждающихся композиций, растворов для поглощения диоксида углерода из промышленных выбросов [4], чернил для струйных принтеров, присадок для повышения стабильности моторных топлив и других целей. Сообщалось о применении тетраэтилортосиликата в составе каталитических композиций для удаления следов галогенсодержащих соединений (на примере трихлорэтилена) из водных сред [5]. Подтверждением значительного интереса к этому соединению служит большое число Российских технических условий его производства, в том числе ТУ 6-09-2687-74, 6-02-708-76, 6-09-3687-79, 6-09-5230-85, 2435-419-05763441-2003, 2637-059-44493-179-04, 2637-187-44493179-2014 и др.
В отсутствие следов воды тетраэтоксисилан достаточно стабилен, но при контакте с водой, как и другие алкоксисиланы [6], легко гидролизуется. Легкость гидролиза объясняет его применение в качестве водоотнимающего средства в некоторых химических процессах [7]. Этой же причиной, скорее всего, обусловлены заметные вариации значений физико-химических свойств тетраэтоксисилана. Например, по данным Merck Index [8] показатель преломления ТЭОС составляет 1.3818, что согласуется с большинством других данных (среднее значение 1.382 ± 0.001). Однако в справочном издании [9] указано значение 1.3928. Столь большие различия свидетельствуют о возможности протекания трудно контролируемых химических трансформаций этого соединения, в том числе, в процессе хранения. Аналогичный разброс значений физико-химических свойств отмечен и для других полиалкоксисиланов. Например, значения плотности триметоксивинилсилана CH2=CH-Si(OCH3)3 варьируют в диапазоне 0.967–0.977, а показателя преломления – 1.3875–1.3975. Величина $n_{{\text{D}}}^{{20}}$ 1.339, приведенная для этого соединения на сайте Sigma-Aldrich, настолько невероятна, что, скорее всего, ошибочна.
Склонность полиалкоксисиланов к гидролизу проявляется при их хранении, а также на стадиях подготовки проб к анализу, тогда как в процессе газохроматографического разделения такие аналиты вполне устойчивы. Подтверждением этого служат индексы удерживания нескольких десятков охарактеризованных тетраалкоксисиланов С4–С22 [10–14].
Газохроматографический анализ хранившегося длительное время образца тетраэтоксисилана, который внешне оставался бесцветной подвижной жидкостью со специфическим эфирным запахом, показал отсутствие в нем целевого соединения и наличие трех неизвестных компонентов с меньшими индексами удерживания. Никаких сведений об их химической природе в литературе найти не удалось, что обусловливает необходимость их идентификации. Решение такой задачи осложнено очевидной нестабильностью таких компонентов и, следовательно, невозможностью их препаративного выделения.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Растворители, реагенты. Препарат тетраэтоксисилана ч.д.а. (Ангарский завод химреактивов, ТУ 6-09-2687-74, CAS № 78-10-4, $n_{{\text{D}}}^{{20}}$ 1.387) хранился длительное время (около 40 лет) в стандартной таре (бутыль емк. 1 л) при комнатной температуре. В начале срока хранения содержание продуктов гидролиза в нем было пренебрежимо малым, а основной регистрируемой примесью был гексаэтокси-1,3-дисилоксан (C2H5O)3Si-O-Si(C2H5O)3 c индексом удерживания 1335 ± 2 на капиллярной колонке со стандартной неполярной фазой OV-101. В работе использовали изопропиловый спирт х.ч. (Криохром, Санкт-Петербург), хлороформ, четыреххлористый углерод, циклогексанон, 2-гексанон, реперные н-алканы С6–С10, все – х.ч. для хроматографии (Реахим, Москва) и ацетофенон (Sigma-Aldrich Rus LLC, Россия).
Тетраэтоксисилан (300 мкл) растворяли в четыреххлористом углероде (1 мл) с добавками (при необходимости) по 100 мкл других реагентов и 100 мкл смеси реперных н-алканов. Выбор CCl4 в качестве растворителя обусловлен меньшим содержанием в нем воды по сравнению, например, с хлороформом (растворимость воды в CCl4 при комнатной температуре по разным данным составляет 0.01–0.03 мас. %, тогда как в CHCl3 – 0.06–0.28 мас. %).
Условия анализа. Газохроматографический анализ проводили на хроматографе Хроматэк-Кристалл 5000.2 с пламенно-ионизационным детектором и WCOT-колонкой длиной 10 м, внутренним диаметром 0.53 мм и толщиной пленки фазы 2.65 мкм с неподвижной фазой НР-5 в режиме программирования температуры от 80 до 200°С (обычно не более 10 мин – до выхода предполагаемого последнего пика на хроматограмме) со скоростью 6 град/мин. Газ-носитель азот, объемная скорость 3.8 мл/мин, линейная скорость 34 см/с, деление потока газа-носителя при вводе проб 1 : 3. Температура испарителя 180°С, детектора 200°С. Пробы дозировали микрошприцем объемом 10 мкл, объем проб 0.5–1.0 мкл. Все пробы отдельно анализировали с добавкой смеси реперных н-алканов С6–С10. Температурную зависимость относительных площадей пиков компонентов образца тетраэтоксисилана от температуры испарителя характеризовали в диапазоне 140–240°С.
Обработка результатов. Статистическую обработку первичных результатов определений проводили с использованием ПО Excel. Компоненты образцов характеризовали линейно-логарифмическими индексами удерживания:
(1)
$\begin{gathered} {\text{R}}{{{\text{I}}}_{х}} = {\text{R}}{{{\text{I}}}_{n}}{\text{ + (R}}{{{\text{I}}}_{n}}_{{{\text{ + }}k}}--{\text{R}}{{{\text{I}}}_{n}}{\text{)}} \times \\ \times \,\,[f({{t}_{{{\text{R}},x}}}) - f({{t}_{{{\text{R,}}n}}})\left] {{\text{ / }}} \right[f({{t}_{{{\text{R,}}n{\text{ + }}k}}})--f({{t}_{{{\text{R,}}n}}})], \\ \end{gathered} $где tR, tR,n и tR,n+k – времена удерживания целевого аналита (х) и ближайших к нему по параметрам удерживания реперных н-алканов с присвоенными им значениями индексов удерживания RIn и RIn+k (RIn = 100nC, где nC – число атомов углерода в молекуле), f(tR) = tR + qlg(tR), где q – переменный коэффициент, вычисляемый по временам удерживания трех реперных компонентов [15].
Для вычисления индексов удерживания использовали программу QBasic.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Тетраэтоксисилан представляет собой бесцветную подвижную жидкость со специфическим запахом, Ткип 167.7 ± 1.4°С, $d_{{\text{4}}}^{{20}}$ 0.932 ± 0.002 и $n_{{\text{D}}}^{{20}}$ 1.382 ± 0.001. Имеющийся в нашем распоряжении образец имел несколько большее значение $n_{{\text{D}}}^{{20}}$ 1.387, что объясняется его гидролизом в процессе хранения. В результате образуется более летучий этанол с меньшим показателем преломления (1.360 ± 0.001), частичное испарение которого приводит к увеличению $n_{{\text{D}}}^{{20}}$ остатка.
Одной из интересных особенностей тетраалкоксисиланов, как и других кремнийсодержащих соединений, представляются аномально большие разности их газохроматографических индексов удерживания RI на стандартных неполярных (полидиметилсилоксаны, RI(np)) и на так называемых semi-standard фазах, к которым относятся углеводородные фазы типа апиезонов (RI(ss)) [3]. Так, для ТЭОС значение RI(np) составляет 978 ± ± 10, а RI(ss) – 853 ± 9 [3]. Такую же аномалию можно проследить и для других полиалкоксисиланов, для которых в табл. 1 сопоставлены экспериментально определенные значения RI(ss) [3] с оценками RI(np) по аддитивной схеме [16]. Столь большие разности индексов удерживания существенно превышают неопределенности их аддитивных оценок.
Таблица 1.
Сравнение экспериментально определенных индексов удерживания [RI(ss)] некоторых тетраалкоксисиланов на углеводородных неподвижных фазах [3] и оценок RI(np) на неполярных полидиметилсилоксановых фазах по аддитивной схеме [14]
| (RO) в Si(OR)4 | RI(np) | RI(ss) | ΔRI |
|---|---|---|---|
| (CH3O)2(C2H5O)2 | 831 | 766 ± 4 | 65 |
| (C2H5O)4 | 1030* | 850 ± 1 | 180 |
| (C3H7O)4 | 1428 | 1163 | 265 |
| (C4H9O)4 | 1825 | 1488 | 337 |
Имеющийся в нашем распоряжении образец характеризовался полным отсутствием отвечающего ТЭОС хроматографического пика в области RI 850–980, что обусловлено гидролизом этого соединения. Конечными продуктами гидролиза ТЭОС всегда считали этанол и диоксид кремния, тогда как природа промежуточных продуктов оставалась неизвестной. В нашем случае на хроматограмме хранившегося образца ТЭОС, фрагмент которой приведен на рис. 1, регистрируются сигналы четырех компонентов (№№ 0–3). Компонент № 0 легко может быть идентифицирован просто по времени удерживания как этиловый спирт, присутствие которого вполне ожидаемо.
Рис. 1.
Фрагмент хроматограммы примесей продуктов частичного гидролиза образца тетраэтоксисилана (без растворителя). Компонент № 0 – этанол, идентификация компонентов №№ 1–3 обсуждается в тексте.
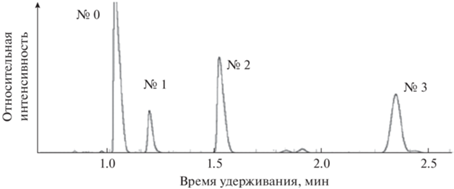
Что же касается компонентов №№ 1–3 с индексами удерживания 537 ± 2 (№ 1), 608 ± 1 (№ 2, наибольший из них) и 727 ± 3 (№ 3), то, как отмечено выше, литературные сведения о них отсутствуют. Следует отметить, что их хромато-масс-спектрометрическая идентификация в данном случае представляется затруднительной, поскольку эти компоненты находятся в области элюирования этанола и других потенциальных растворителей (CHCl3, CCl4) образцов. То, что физико-химические характеристики продуктов частичного гидролиза ТЭОС (включая данные элементного анализа) неизвестны, означает, что препаративное выделение этих компонентов невозможно из-за их очевидной нестабильности. По этой причине их идентификация может быть основана только на совокупности косвенных критериев, каждый из которых недостаточно информативен для получения однозначных ответов. Прежде всего, целесообразно проверить, насколько химические свойства смеси вероятных продуктов частичного гидролиза тетраэтоксисилана соответствуют химическим свойствам самого ТЭОС, однако предварительно целесообразно оценить термическую стабильность компонентов №№ 1–3. Для этого проанализировали раствор ТЭОС в CCl4 при различных температурах испарителя в диапазоне 140–240°С. На рис. 2 зависимости относительных площадей пиков этих компонентов (в % от их суммы) от температуры испарителя представлены в графическом виде. Для всех компонентов зависимости достаточно слабо выражены (для основного пика № 2 вариации Sотн не превышают 2%). Тем не менее для их минимизации выбрано значение Тисп в области экстремумов, т.е. 180°С.
Рис. 2.
Относительные площади пиков компонентов №№ 1–3 (в % от суммы площадей) в зависимости от температуры испарителя в диапазоне 140–240°С; (а) − компонент № 1, (б) − компонент № 2, (в) − компонент № 3.

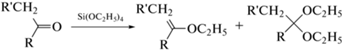
Химические реакции с участием смеси продуктов частичного гидролиза тетраэтоксисилана. Наиболее характерным химическим свойством ТЭОС представляется обмен алкильных групп в молекуле в результате его взаимодействия со спиртами, катализируемого как кислотами, так и основаниями. Такой обмен выявлен для метилового спирта [17], однако принципиальных ограничений этого процесса в случае других спиртов нет (схема 1 ):
Схема 1 . Последовательное замещение этоксигрупп в тетраэтоксисилане на другие алкоксигруппы.
Нельзя не отметить аналогию свойств тетраэтоксисилана и некоторых эфиров других неорганических кислот, например диметилсульфата (CH3O)2SO2 и триметилфосфата (CH3O)3PO, которые используют в качестве алкилирующих реагентов при получении метильных производных соединений с активными атомами водорода (фенолы, амины, енольные формы карбонильных соединений, карбоновые кислоты и др.) для их газохроматографического определения [18, 19]. Аналогичными свойствами обладает этиловый эфир ортомуравьиной кислоты (ортоэтилформиат), СН(ОС2Н5)3 [20]. В случае ТЭОС схему реакции можно записать следующим образом:
Схема 2 . Взаимодействие тетраэтоксисилана с соединениями, содержащими активные атомы водорода.
Схема 3 . Взаимодействие тетраэтоксисилана с карбонильными соединениями.
Этот реагент ранее не применяли для дериватизации, видимо, из-за невысокой степени конверсии аналитов в соответствующие этильные производные. Тем не менее в нашем случае протекание указанных реакций даже в незначительной степени позволяет подтвердить сходство химической природы ТЭОС и регистрируемых продуктов его частичного гидролиза. Индексы удерживания некоторых из таких продуктов приведены в табл. 2.
Таблица 2.
Индексы удерживания и результаты идентификации продуктов взаимодействия некоторых карбонильных соединений с тетраэтоксисиланом
| Субстрат (М) | RI | Справочные значения RI [3] | Продукт реакции (М) | RI | Справочные значения RI |
|---|---|---|---|---|---|
| Циклогексанон (98) | 920 ± 2 | 894 ± 4 | Этиловый эфир енола (126) | 990 ± 1 | (894 ± 4) + (99 ± 20) = = 993 ± 20 [18] |
| Диэтилкеталь (172) | 1140 ± 2 | (894 ± 4) + (266 ± 26) = = 1160 ± 26 [18] | |||
| Ацетофенон (120) | 1081 ± 1 | 1065 ± 4 | Этиловый эфир енола (148) | Следы, ∼1200 |
1155 ± 16 [3]; (1065 ± 4) + (99 ± 20) = = 1164 ± 20 [18] |
| Диэтилкеталь (194) | 1306 | (1065 ± 4) + (266 ± 26) = = 1331 ± 26 [18] | |||
| 2-Гексанон (100) | 790 | 790 ± 3 | Продукты не обнаружены | ||
| Салициловый альдегид (122) | 1063 | 1047 ± 6 | Продукты не обнаружены | ||
При взаимодействии карбонильных соединений R(R'СН2)CO с этилирующими реагентами в кислой среде, кроме диэтилацеталей и кеталей R′СН2C(R)(ОС2Н5)2 (схема 2 ), образуются соответствующие этиловые эфиры енолов (схема 3 ). Они легко могут быть идентифицированы по значениям RI исходных карбонильных соединений и соответствующим инкрементам индексов удерживания, ΔRI. Для трансформации кетонов в этиловые эфиры енолов значение ΔRI составляет 99 ± 20 ед. индекса, а в диэтилкетали – 266 ± 26 [20]. Тогда на основании полученных оценок RI (табл. 2) можно заключить, что циклогексанон и ацетофенон в присутствии ТЭОС образуют некоторые количества как этиловых эфиров енолов, так и диэтилкеталей. Однако оценки по площадям хроматографических пиков показывают, что в обоих случаях степени конверсии не превышают 10%. Добавление каталитических количеств концентрированной серной кислоты не увеличивает содержание продуктов. В случаях же 2-гексанона, салицилового альдегида и некоторых других карбонильных соединений (например, пинаколина) продукты взаимодействия не обнаружены.
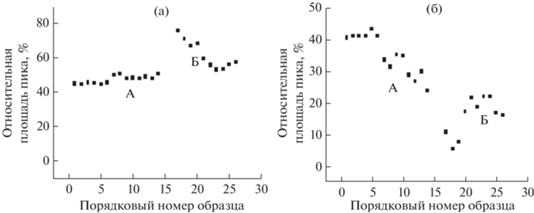
Таким образом, взаимодействие смеси продуктов частичного гидролиза ТЭОС с карбонильными соединениями согласуется с ожидаемыми свойствами самого тетраэтоксисилана, что указывает на их идентичную химическую природу. При этом интересно заметить, что в ходе рассматриваемых процессов с участием трех продуктов гидролиза ТЭОС изменяется их соотношение, что нагляднее всего представить графически (рис. 3а, 3б) для относительных площадей пиков (Sотн) соединений № 2 и № 3. Аналогичная зависимость для пиков компонента № 1 менее наглядна. Участки А на обоих рисунках соответствуют значениям Sотн продуктов № 2 и № 3 в различных образцах, не содержащих соединений, способных вступать с ними во взаимодействие (но которые могут содержать, например, только химически инертные реперные н-алканы). Обращает на себя внимание хорошая воспроизводимость относительных площадей продуктов частичного гидролиза, особенно для № 2. Участки Б соответствуют образцам, проанализированным сразу после добавок различных карбонильных соединений, и демонстрируют существенные вариации значений Sотн. Важно заметить, что через некоторое время соотношение относительных площадей пиков компонентов №№ 2, 3, близкое к значениям для исходного образца, восстанавливается. Из этого можно заключить, что идентифицируемые компоненты №№ 1–3 характеризуются различной реакционной способностью и способны к взаимным превращениям.
Рис. 3.
Относительные площади пиков компонентов № 2 (а) и № 3 (б) (в % от суммы площадей пиков компонентов №№ 1–3) в различных образцах. Область А – индивидуальный тетраэтоксисилан и его растворы, не содержащие других компонентов, кроме реперных н-алканов; область Б – реакционные смеси, содержащие компоненты, способные к взаимодействию с тетраэтоксисиланом или продуктами его частичного гидролиза.
В целом характеристика химических свойств смеси продуктов частичного гидролиза ТЭОС показала, что как реагент для дериватизации (этилирование карбонильных соединений) она недостаточно эффективна. Однако протекание химических реакций (пусть и в незначительной степени) с использованием этой смеси позволяет подтвердить, что ее компоненты действительно нестабильны, скорее всего, находятся в равновесии друг с другом и, по-видимому, все могут участвовать в реакциях. Последнее означает сходство их химической природы, но для подтверждения такого предположения необходимо дополнительно проанализировать значения их газохроматографических индексов удерживания.
Рекуррентная аппроксимация индексов удерживания тетраэтоксисилана и продуктов его частичного гидролиза. Индексы удерживания ТЭОС и регистрируемых продуктов его частичного гидролиза на неподвижной фазе HP-5 образуют нелинейную последовательность: 537 ± 2 (№ 1), 608 ± 1 (№ 2), 727 ± 3 (№ 3) и 978 ± 10 (ТЭОС) (разности равны 71, 115 и 251 ед. индекса соответственно). Известен способ линеаризации нелинейных зависимостей значений различных физико-химических характеристик А(х) органических соединений и, в том числе, хроматографических параметров [21, 22], предполагающий их рекуррентную аппроксимацию:
где Δх = const – постоянный “шаг” вариации значений аргумента, значения коэффициентов a и b вычисляют методом наименьших квадратов.Рекуррентные соотношения применимы к монотонным функциям целочисленных или равноотстоящих значений аргументов, сочетают свойства арифметических и геометрических прогрессий, а их математическими эквивалентами являются полиномы переменных степеней. Точки на графиках рекуррентных зависимостей соответствуют “соседним” значениям функций, тогда как значения аргументов на них никак не представлены. Важно, что соотношения (2) обеспечивают линейную аппроксимацию значений различных свойств с высокими коэффициентами корреляции только в пределах групп структурных аналогов, а именно гомологов или конгенеров.
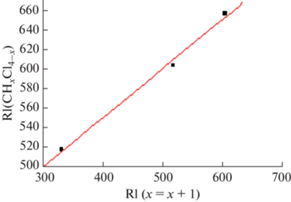
Поскольку применение рекуррентных соотношений для аппроксимации свойств конгенеров на различных примерах охарактеризовано еще недостаточно подробно, его целесообразно проиллюстрировать дополнительно. Простейшую совокупность конгенеров образуют, например, галогенпроизводные метана от метилхлорида до тетрахлор-метана с индексами удерживания на полидиметилсилоксановых неподвижных фазах, содержащих 5% фенильных групп 332 ± 0 (CH3Cl), 518 ± 5 (CH2-Cl2), 605 ± 4 (CHCl3) и 658 ± 5 (CCl4) [3], разности которых равны 53, 87 и 186 ед. индекса соответственно. Рекуррентное представление этих данных соответствует зависимости индексов удерживания хлорметанов CHx-Cl4–x (0 ≤ x ≤ 2) от индексов удерживания хлорметанов, содержащих на один атом хлора меньше (х' = х + 1, т.е. 1 ≤ x' ≤ 3). График этой зависимости представлен на рис. 4; коэффициент корреляции равен 0.998. Этот пример иллюстрирует возможности и особенности рекуррентной линеаризации индексов удерживания конгенеров.
Рис. 4.
Рекуррентная зависимость индексов удерживания хлорметанов CHxCl4–x (0 ≤ x ≤ 2) от индексов удерживания их конгенеров, содержащих на один атом хлора меньше (х' = х + 1, т.е. 1 ≤ x' ≤ 3). Параметры уравнения линейной регрессии: a = 0.51 ± 0.03, b = = 348 ± 17, R = 0.998, S0 = 6.7.
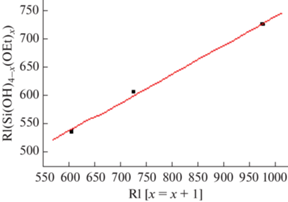
Аналогичная рекуррентная аппроксимация индексов удерживания продуктов частичного гидролиза тетраэтоксисилана (включая сам ТЭОС) может быть представлена в виде зависимости каждого из них от значений RI следующего компонента (с бóльшим временем удерживания) так, как это изображено на рис. 5. Примечательно, что коэффициент корреляции в этом случае также достигает 0.998, а коэффициент а такой же, как и для индексов удерживания хлорметанов (0.51 ± 0.03). На основании линейности рекуррентной зависимости можно сделать вывод, что ТЭОС и продукты его частичного гидролиза также образуют совокупность конгенеров, а именно ряд этоксисиланолов, отличающихся числом этоксильных и гидроксильных групп в молекулах (схема 4 ):
Схема 4 . Последовательный гидролиз тетраэтоксисилана с образованием этоксисиланолов.
Рис. 5.
Рекуррентная зависимость индексов удерживания продуктов частичного гидролиза тетраэтоксисилана от индексов удерживания компонентов с большими индексами удерживания. Параметры уравнения линейной регрессии: a = 0.51 ± 0.03, b = 233 ± ± 23, R = 0.998, S0 = 7.9.
Для двух последних конгенеров можно предположить наличие следующих равновесий (схема 5 ):
Схема 5 . Возможные процессы дегидратации алкоксисиланолов.
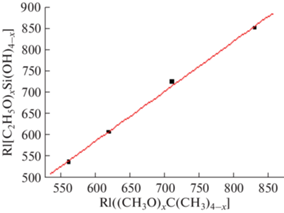
Для еще более наглядного подтверждения природы продуктов частичного гидролиза ТЭОС можно рассмотреть корреляцию непосредственно индексов удерживания серии соединений (C2H5O)xSi(OH)4–x (1 ≤ x ≤ 4) и каких-либо их структурных аналогов, например метоксизамещенных алканов (CH3O)xC(CH3)4–x. На рис. 6 приведен график соответствующей линейной регрессии, коэффициент корреляции которой составляет 0.998, из линейности которого следует сходство хемотаксономических критериев обоих сравниваемых рядов.
Рис. 6.
Зависимость индексов удерживания продуктов частичного гидролиза тетраэтоксисилана (C2H5O)xSi(OH)4–x от индексов удерживания их структурных аналогов (CH3O)xC(CH3)4–x, не содержащих кремний. Параметры уравнения линейной регрессии: a = 1.17 ± 0.04, b = −118 ± 28, R = 0.998, S0 = = 8.4.
Структурные аналоги структурных аналогов продуктов частичного гидролиза ТЭОС с атомами углерода вместо кремния неизвестны из-за их нестабильности. Сведений о выявленных “экзотических” продуктах гидролиза ТЭОС в литературе крайне мало, за исключением упоминания диэтоксисиландиола Si(OH)2(OC2H5)2 как компонента чернил для струйных принтеров [23]. Описан синтез триэтоксисиланола (C2H5O)3SiOH [24], который даже охарактеризован температурой кипения при пониженном давлении (табл. 3). Этот факт позволяет предположить, что родственные по структуре диэтоксисиландиол и этоксисилантриол не только вполне могут существовать, по крайней мере, в растворах, но и стабильны в условиях газохроматографического анализа. Среди кремнийсодержащих соединений с другими фрагментами структуры также известно несколько силандиолов R2Si(OH)2 и силантриолов RSi(OH)3, часть из которых настолько стабильна, что они охарактеризованы физико-химическими параметрами. Поэтому аналогия выявленных продуктов частичного гидролиза ТЭОС с силандиолами и силантриолами других рядов может рассматриваться как еще один довод в пользу возможности образования таких продуктов.
Таблица 3.
Литературные значения свойств некоторых простейших силандиолов R2Si(OH)2, силантриолов RSi(OH)3 и трис-алкоксисиланолов (RO)3SiOH
| Заместители | Мол. масса | CAS № | Свойства (если известны) |
|---|---|---|---|
| Силандиолы R2Si(OH)2 | |||
| Диметил | 92 | 63148-62-9; 1066-42-8; 31692-79-2; 196616-86-1; 31900-57-9 (полимер) | $d_{4}^{{20}}$ 0.97* |
| Винилметил | 104 | 3959-12-4; 157141-20-3 | |
| Диэтил | 120 | 2031-65-4 | $d_{4}^{{20}}$ 1.134; Ткип ∼ 140°С |
| Диаллил | 144 | $d_{4}^{{20}}$ 1.105; Тплавл 81°С | |
| Бутилметокси | 150 | 918547-96-3 | |
| Метилфенил | 154 | 3959-13-5; 31230-04-3 (полимер); 63148-58-3 (полимер) | |
| Фенилэтил | 168 | 18291-94-6 | |
| Диизобутил | 176 | 18230-63-2 | |
| Дициклопентил | 200 | 211495-85-1 | $d_{4}^{{20}}$ 1.06; $n_{4}^{{20}}$ 1.506; logP 2.30 |
| Дифенил | 216 | 947-42-2 | $d_{4}^{{20}}$ 1.255; Тплавл 144−148°С |
| Бис-триметилсилилокси | 240 | 56275-01-5 | |
| Силантриолы RSi(OH)3 | |||
| Метил | 94 | 2445-53-6 | |
| Этил | 108 | 5651-16-1 | |
| Фенил** | 156 | 3047-74-3; 157374-41-9 | $d_{4}^{{20}}$ 1.31; $n_{4}^{{20}}$ 1.593; logP 2.53 |
| Триметилсилилокси | 168 | 56275-01-5 | |
| 3-Глицидилоксипропил | 194 | 51287-18-4 | |
| Трис-алкоксисиланолы (RO)3SiOH | |||
| Трис-этокси | 180 | 27491-84-5 | Tкип 51.5−52°С (1 мм рт. ст.), $d_{4}^{{20}}$ 1.0184; $n_{4}^{{20}}$ 1.3962 |
| Трис-изопропокси | 222 | 27491-86-7 | $d_{4}^{{20}}$ 0.940 |
| Диэтокси-3-глицидилоксипропил | 250 | 110582-73-5 | logP 0.80 |
| Трис-трет-пентилокси | 306 | 17906-35-3 | $d_{4}^{{20}}$ 0.944 |
Литературные данные о силандиолах R2Si(OH)2 и силантриолах RSi(OH)3. В табл. 3 представлены известные литературные данные о некоторых простейших силандиолах R2Si(OH)2, силантриолах RSi(OH)3, а также трис-алкоксисиланолах (RO)3SiOH. Кроме них в Интернете можно найти сведения и о более сложных функциональных производных полигидроксисиланов, например этокси(3-аминопропил)- (CAS № 82178-05-0), метил(3,3,3-трифторпропил- (CAS № 660-78-6), этилгидроперокси- (нет номера CAS) и др. Номера CAS, приведенные для перечисленных в табл. 3 соединений, подтверждают не столько их выделение в индивидуальном виде, сколько проявляемый к таким соединениям интерес. Свидетельством препаративного изолирования тех или иных соединений служат экспериментальные значения физико-химических свойств. В данном случае это диметил-, диэтил-, диаллил-, дициклопентил- и дифенилсиландиолы, фенилсилантриол, а также триэтокси-, трис-изопропокси- и трис-изопентилоксисиланолы. Дифенилсиландиол настолько стабилен, что охарактеризован температурой плавления без разложения (144−148°С). Изучена кристаллическая структура диаллилсиландиола [25]. Для такого “экзотического” соединения, как фенилсилантриол описаны синтез, свойства и реакционная способность [26, 27]. Кроме того, простейший диметилсиландиол идентифицирован в самых разнообразных объектах, в том числе среди летучих компонентов запаха человеческого тела [28], креветок Penaeus monodon [29], сыра [30] и др. Однако во многих случаях техника анализа смесей летучих компонентов предполагает нагревание сорбционных элементов, содержащих уплотнения из силиконовых эластомеров, полидиметилсилоксановых покрытий элементов шприцев для твердофазной микроэкстракции и т.д. По этой причине появление диметилсиландиола в подобных образцах может быть обусловлено термической деструкцией полидиметилсилоксанов. Кроме того, параметры удерживания и положение пиков (CH3)2Si(OH)2 на хроматограммах по данным разных работ часто не совпадают между собой, что свидетельствует об ошибочной идентификации этого соединения (как, например, в работе [29]). Обычно это обусловлено сходством масс-спектров различных полиметилсилоксанов.
* * *
Таким образом, смесь продуктов частичного гидролиза тетраэтоксисилана охарактеризована некоторыми химическими свойствами (этоксилирование карбонильных соединений), результатами рекуррентной аппроксимации их газохроматографических индексов удерживания на неподвижной фазе HP-5 и корреляцией с индексами удерживания структурных аналогов. Это позволило установить, что такие продукты относятся к конгенерам тетраэтоксисилана и представляют собой весьма “экзотические” соединения: триэтоксисиланол (C2H5O)3SiOH, диэтоксисиландиол (C2H5O)2Si(OH)2, и этоксисилантриол (C2H5O)Si(OH)3. Сопоставление свойств различных силандиолов R2Si(OH)2 и силантриолов RSi(OH)3 по литературным данным показывает, что некоторые из них достаточно стабильны. Прежде всего, это относится к соединениям, содержащим заместители, способные к сопряжению с вакантными d-орбиталями атомов кремния: фенильные (π–d-системы сопряжения) и алкоксильные (p–d-системы сопряжения). Идентифицированные в образце тетраэтоксисилана продукты его частичного гидролиза относятся к соединениям именно второго типа. Впервые определенные значения их индексов удерживания могут быть включены в современные базы данных.
Экспериментальные данные настоящей работы получены в Ресурсном центре “Методы анализа состава вещества” Научного парка Санкт-Петербургского государственного университета. Авторы благодарят сотрудников Центра за содействие.
Список литературы
Middleditch B.S. Analytical Artifacts: GC, MS, HPLC, TLC, and PC. Amsterdam: J. Chromatogr. Library. V. 44. 1989. 1033 p.
Zenkevich I.G. Features and new examples of gas chromatographic separation of thermally unstable analytes / Chapter XX in “Recent advances in gas chromatography”. London: IntechOpen Ltd. 2020. P. 1. https://doi.org/10.5772/intechopen.94229
The NIST Mass Spectral Library (NIST/EPA/NIH EI MS Library, 2020 Release). Software/Data Version; NIST Standard Reference Database, Number 69, May 2020. National Institute of Standards and Technology, Gaithersburg, MD 20899: http://webbook.nist.gov (дата обращения: апрель 2022 г.).
Rama S., Zhang Y., Tchuenbou-magala F., Ding Y., Li Y. Encapsulation of 2-amino-2-methyl-1-propanol with tetraethyl orthosilicate for CO2 capture // Frontiers Chem. Sci. Eng. 2019. V. 13. № 4. P. 672. https://doi.org/1007/s11705-019-1856-6
Ramamurthy A.S., Eglal M.M. Degradation of TCE by TEOS coated nZVI in the presence of Cu(II) for groundwater remediation // J. Nanomaterials. 2014. Article 606534. https://doi.org/10.1155/2014/606534
Arkles B., Steinmetz J.R., Zazyczny J., Mehta P. Factors contributing to the stability of alkoxysilanes in aqueous solutions / Silanes and Other Coupling Agents / Ed. Mittal K.L. Utrecht: VSP, 1992. P. 91.
Braddock D.C., Lickiss P.D., Rowley B.C., Pugh B.C.R., Purnomo T., Santhakumar G., Fussell S.J. Tetramethyl orthosilicate (TMOS) as a reagent for direct amidation of carboxylic acids // Org. Lett. 2018. V. 20. P. 950.
The Merck Index – An Encyclopedia of Chemicals, Drugs, and Biological / Ed. O’Neil M.J. Whitehouse Station: Merck and Co. Inc., 2006. 657 p.
Lide R.C. CRC Handbook of Chemistry and Physics. 88th Ed. Boca Raton: CRC Press (Taylor & Francis Group), 2007. P. 3.
Taylor J.H. Gas chromatographic separation and infrared analysis of ethyl propyl silicates // J. Chromatogr. Sci. 1968. V. 6. № 11. P. 557. https://doi.org/10.1093/chromsci/6.11.557
Ellren O., Peetre I.-B., Smith B.E.B. Gas chromatographic investigation of organometallic compounds and their carbon analogues. I. Determination, calculation, and correlation of Kovats retention indices for tetraalkoxysilanes // J. Chromatogr. 1974. V. 88. P. 295. https://doi.org/10.1016/S0021-9673(00)83154-4
Peetre I.-B. Gas chromatographic investigation of organometallic compounds and their carbon analogues. II. Improved method for calculating retention indices of tetraalkoxysilanes // J. Chromatogr. 1974. V. 88. P. 311. https://doi.org/10.1016/S0021-9673(00)83155-6
Крешков А.П., Кириченко Е.А., Марков Б.А. Индексы удерживания алкоксихлорсилано в // Журн. аналит. химии. 1975. Т. 30. № 2. С. 345.
Иванова Н.Т., Франгулян Л.А. Газохроматографический анализ нестабильных и реакционноспособных соединений. М.: Химия, 1979. 232 с.
Kovats’ retention index system / Encyclopedia of Chromatography. 3rd Ed. / Ed. Cazes J. Boca Raton: CRC Press (Taylor & Francis Group), 2010. V. 2. P. 1304.
Stein S.E., Babushok V.I., Brown R.L., Linstrom P.J. Estimation of Kovats retention indices using group contributions // J. Chem. Inf. Model. 2007. V. 47. P. 975. https://doi.org/10.1021/ci600548y
Lim J., Ha S.-W., Lee J.-K. Precise size-control of silica nanoparticles via alkoxy exchange equilibrium of tetraethyl orthosilicate (TEOS) in the mixed alcohol solution // Bull. Korean Chem. Soc. 2021. V. 33. № 3. P. 1067. https://doi.org/10.5012/bkcs.2012.33.3.1067
Derivatization of analytes in chromatography: General aspects / Encyclopedia of Chromatography. 3rd Ed. / Ed. Cazes J. Boca Raton: CRC Press (Taylor & Francis Group), 2010. V. 1. P. 562.
Compounds: Derivatization for GC analysis / Encyclopedia of Chromatography. 3rd Ed. / Ed. Cazes J. Boca Raton, CRC Press (Taylor & Francis Group), 2010. V. 2. P. 1165.
Зенкевич И.Г., Лукина В.М. Хромато-масс-спектрометрическая характеристика диэтилкеталей алифатических карбонильных соединений // Аналитика и контроль. 2019. Т. 23. № 3. С. 410. https://doi.org/10.15826/analitika.2019.23.3.009
Zenkevich I.G. Application of recurrent relationships in chromatography // J. Chemometrics. 2009. V. 23. P. 179. https://doi.org/10.1002/cem.1214
Zenkevich I.G. Recurrent relationships in separation science / Chemometrics in Chromatography / Eds. Komsta L, Heyden Y.V, Sherma J. New York: Taylor & Francis, 2017. Ch. 24. P. 449.
Toyoda T., Matsumoto T., Arakawa T. Jet printing ink composition. Patent USA. 1982. № 4,338,133.
Kazakova V.V., Gorbatsevich O.B., Skvortsova S.A., Demchenko N.V., Muzafarov A.M. Synthesis of triethoxyxilanol // Russ. Chem. Bull. Int. Ed. 2005. V. 54. № 5. P. 1350.
Nobutami K., Masao K. The crystal structure of diallylsilanediol // Bull. Chem. Soc. Jap. 1954. V. 27. № 9. P. 605. https://doi.org/10.1246/bcsj.27.605
Tyler L. Phenylsilanetriol // J. Am. Chem. Soc. 1955. V. 77. № 3. P. 770. https://doi.org/10.1021/ja1608a078
Korkin S.D., Buzin M.I., Matukhina E.V., Zherlitsyna L.N., Auner N., Shchegolikhina O.I. Phenylsilanetriol – Synthesis, stability, and reactivity // J. Organomet. Chem. 2003. V. 686. № 1–2. P. 313. https://doi.org/10.1016/S0022-328X(03)00721-6
Jha S.K., Marina N., Liu C., Hayashi K. Human body odor discrimination by their GC-MS spectra data mining // Anal. Methods. 2015. № 7. P. 9549. https://doi.org/10.1039/C4AY02457A
Pratana R.I., Yuniar I., Hamdani H., Rostini I. Volatile flavor compounds composition of fresh and steamed tiger shrimp (Penaeus monodon) // Int. J. Fish. Aquat. Res. 2019. V. 4. № 1. P. 25.
Stefanikova J., Arvay J., Miskeje M., Kacaniova M. Determination of volatile organic compounds in Slovak bryndza cheese by the electronic nose and the headspace solid-phase microextraction gas chromatography – mass spectrometry // Slovak J. Food Sci. 2020. V. 14. P. 767. https://doi.org/10.5219/1300
Дополнительные материалы отсутствуют.
Инструменты
Журнал аналитической химии