Биология внутренних вод, 2022, № 6, стр. 711-724
Состав, структура и особенности пространственного распределения зоопланктона в Шекснинском водохранилище (Верхняя Волга, Россия)
В. И. Лазарева *
Институт биологии внутренних вод им. И.Д. Папанина Российской академии наук
пос. Борок, Ярославская обл., Некоузский р-н, Россия
* E-mail: lazareva_v57@mail.ru
Поступила в редакцию 03.03.2022
После доработки 21.06.2022
Принята к публикации 27.06.2022
- EDN: XSGYKI
- DOI: 10.31857/S0320965222060122
Аннотация
В июле 2017 г. исследован пелагический зоопланктон Шекснинского водохранилища (бассейн Верхней Волги). В его составе зарегистрировано 60 видов, среди которых пять новых для водоема (копепода Сyclops kikuchii, коловратки Cephalodella gibba, Trichocerca rattus, Euchlanis pyriformis и Notholca labis). На большей части акватории преобладают обычные для водохранилища кладоцеры Limnosida frontosa и Daphnia galeata, копеподы Eudiaptomus gracilis и Mesocyclops leuckarti. Впервые выявлено массовое развитие редкой копеподы Arctodiaptomus laticeps. Средняя биомасса зоопланктона водохранилища достигала 1.22 ± 0.15 г/м3, максимум (2.5–3.4 г/м3) зарегистрирован в западной части оз. Белое – вдвое ниже наблюдаемого в 1970-х и 1990-х годах. Установлено, что индивидуальная плодовитость массовых видов ракообразных заметно ниже по сравнению с другими водохранилищами Волжского каскада.
ВВЕДЕНИЕ
Зоопланктон водохранилищ отличается богатством видов, высокой динамичностью состава и структуры (Лазарева, 2010; Shurganova et al., 2019). Водохранилища каскада р. Волги служат транзитным коридором для расселения северных видов на юг, а южных – на север, в том числе чужеродных форм (Мордухай-Болтовской, Дзюбан, 1976; Lazareva, 2019). Сложная морфометрия водохранилищ, разнообразие биотопов и вариаций гидродинамического режима способствуют неравномерному распределению планктона по акватории и в толще воды по вертикали (Структура…, 2018).
Шекснинское водохранилище – один из самых северных водоемов в каскаде р. Волги, северная граница Ковжинского участка расположена на 60° с.ш. Изучение зоопланктона водоема начато в первые годы после его заполнения (Смирнов, 1966; Луферова, 1966; Пидгайко, 1969) и продолжается до настоящего времени (Антропогенное…, 1981; Современное…, 2002; Думнич, 2005; Ривьер, Литвинов, 2006; Лазарева и др., 2013; Думнич, Лобуничева, 2016, 2018). Формированию сообщества речных участков водохранилища способствовало поступление лимнического планктона из оз. Белое (Луферова, 1966; Пидгайко, 1969). Летом в современном зоопланктоне доминируют ракообразные, в основном Copepoda (Ривьер, 1982; Современное…, 2002; Думнич, 2005; Лазарева и др, 2013). Максимального развития он достигает в июне–августе, биомасса сообщества близка к таковой в неглубоких озерах региона Воже, Лача и Кубенское (Антропогенное…, 1981).
Распределение обилия зоопланктона по акватории водохранилища крайне неравномерно, это определяется гидрофизическим режимом водоема, особенностями его морфометрии, а также уровнем развития фитопланктона (Пидгайко, 1969; Ривьер, 1982; Антропогенное…, 1981; Ривьер, Литвинов, 2006; Лазарева и др., 2013). Анализ многолетней динамики показал, что с середины 1990-х годов увеличился вклад циклопоидных копепод в обилие сообщества, а также кладоцер Bosmina coregoni cf. gibbera (Schoedler, 1863), в середине 2000-х годов на Шекснинском участке – Bosmina c. cf. crassicornis (Современное…, 2002; Лазарева и др., 2013). Также исследовано вертикальное распределение обилия массовых видов в оз. Белое и приплотинном участке водохранилища (Антропогенное…, 1981; Ривьер, Литвинов, 2006). Результаты представленной работы продолжают многолетнее изучение зоопланктона, характеризуют его состав и пространственное распределение в конце 2010-х годов.
Цель работы – оценить богатство фауны, выявить изменения состава и обилия зоопланктона, а также особенности его распределения по акватории Шекснинского водохранилища.
МАТЕРИАЛ И МЕТОДЫ ИССЛЕДОВАНИЯ
Шекснинское водохранилище образовано в 1963 г., водоем вытянут с севера на юг на 262 км от 60°50′ до 59°30′ с.ш. и включает три участка: Ковжинский – пойма рек Ковжа Белозерская и Кема в подпоре водохранилища, Белозерский – оз. Белое, а также речной Шекснинский – затопленные русло и пойма р. Шексна (Современное…, 2002). На Шекснинском участке расположены крупные озеровидные расширения Сизьменское и Приплотинное, отличающиеся значительными глубинами до 11 и 20 м соответственно. Площадь акватории водохранилища 1665 км2, средняя глубина 3.9 м, коэффициент условного водообмена 0.96 год–1 (Современное…, 2002).
По концентрации хлорофилла и биомассе фитопланктона трофический статус экосистемы до начала 2000-х годов определяли как мезо-эвтрофный (Современное…, 2002). Во второй половине 2000-х годов по содержанию хлорофилла а фитопланктона (8.5–12.8 мкг/л) трофический статус водохранилища соответствовал мезотрофному уровню (Лазарева и др., 2013).
В работе использованы данные комплексной экспедиции Института биологии внутренних вод РАН. С 12 по 14 июля 2017 г. обследованы 23 станции преимущественно в пелагиали, расположение точек отбора проб близко к таковому в 2007 г. (Лазарева и др., 2013). Концентрацию растворенного в воде кислорода, электропроводность и температуру воды измеряли портативным прибором YSI–85 (YSI, Inc., USA).
Пробы зоопланктона (Rotifera, Cladocera, Copepoda) отбирали малой сетью Джеди (диаметр входа 12 см, сито с диагональю ячеи 120 мкм) тотально от дна до поверхности воды. Кроме того, исследовали вертикальное распределение зоопланктеров на одной из наиболее глубоких станций (17 м) вблизи плотины Шекснинской ГЭС. Для этого отбирали пробы 10-литровым планктобатометром Дьяченко-Кожевникова с четырех горизонтов 0–5, 6–10, 11–15 и 16–17 м утром в 7 ч. Весь зоопланктон фиксировали 4%-ным формалином. Состав видов определяли по методикам (Кутикова, 1970; Боруцкий и др., 1991; Определитель…, 2010; Степаньянц и др., 2015; Коровчинский и др., 2021; Wilke et al., 2018).
В пробах оценивали численность и биомассу каждого вида, их суммарные значения для трех таксономических групп (Rotifera, Cladocera, Copepoda) и общие для всего зоопланктона. Биомассу рассчитывали по формулам связи индивидуальной массы с длиной тела животных (Ruttner-Kolisko, 1977; Балушкина, Винберг, 1979). Доминантные виды выделяли по их относительной численности (>5% количества Crustacea или Rotifera). Для массовых видов ракообразных учитывали индивидуальную плодовитость самок, которую рассчитывали как среднее количество яиц на одну яйценосную самку. У Cladocera количество яиц в кладке подсчитывали на борту корабля на живых рачках, наркотизированных 5%-ным этанолом.
Для оценки полученных данных использовали пакет статистических программ STATISTICA for Windows v. 12.5 (StatSoft Russia). Индексы сходства состава видов и структуры доминантных комплексов вычисляли по формулам Чекановского–Съеренсена в формах “а” и “b” соответственно (Песенко, 1982). Трофический индекс Е рассчитывали по общему списку зоопланктона согласно формуле и градации значений, приведенной в работах (Андроникова, 1996; Лазарева, 2010).
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ
Гидрофизические характеристики. В 2017 г. глубина в точках отбора проб на русле р. Шексны в Сизьменском разливе и у плотины Шекснинской ГЭС достигала 10–20 м, на других участках – от 4 до 6 м (табл. 1). Вода водохранилища отличалась сравнительно высоким уровнем цветности (>55 град), особенно на Ковжинском участке (180 град). Прозрачность воды определялась цветностью и содержанием взвеси, она была наибольшей на глубоководных станциях Шекснинского участка, у плотины ГЭС достигала 120 см (табл. 1). Воды водохранилища отличаются низкой минерализацией, среднегодовые значения варьируют от 104 до 152 мг/л (Современное…, 2002). В 2017 г. минерализация воды в летнюю межень была крайне низкой – на всех участках <100 мг/л.
Таблица 1.
Гидрофизические и гидрохимические характеристики Шекснинского водохранилища в июле 2017 г.
| Показатель | Участок | ||
|---|---|---|---|
| Ковжинский n = 1 |
Белозерский n = 11 |
Шекснинский n = 11 |
|
| Глубина, м | 6 | 5.3 ± 0.2 | 10 ± 2 |
| Прозрачность, см | 85 | 67 ± 6 | 94 ± 7 |
| Цветность воды, град Pt-Co | 180 | 74 ± 5 | 84 ± 5 |
| Температура воды,°С | $\frac{{17.9}}{{17.9}}$ | $\frac{{16.5 \pm 0.2}}{{16.0 \pm 0.2}}$ | $\frac{{17.6 \pm 0.2}}{{16.2 \pm 0.5}}$ |
| Электропроводность, мкСм/см* | 105.7 | 123 ± 5 | 152 ± 3 |
| Минерализация воды, мг/л** | 69 | 80 ± 3 | 99 ± 2 |
| Концентрация О2 в воде, мг/л | $\frac{{7.5}}{{7.5}}$ | $\frac{{9.9 \pm 0.1}}{{9.4 \pm 0.1}}$ | $\frac{{9.6 \pm 0.1}}{{8.4 \pm 0.4}}$ |
Температура воды была невысокой для июля, варьировала от 15.8 до 18.5°С у поверхности и от 14.8 до 18.4°С у дна водоема. Среднемноголетние значения температуры в июле достигают 19.1°С для оз. Белое и 19.5°С для Шекснинского участка (Современное…, 2002). В 2017 г. по всему водоему прогрев воды был ниже нормы в среднем на 1.9–2.6°С. Это способствовало развитию в планктоне водохранилища северных холодолюбивых видов. У поверхности оз. Белое вода прогревалась слабее на 1°С по сравнению с речным участками, в то же время разница придонных значений температуры воды была несущественной (табл. 1). Различный прогрев воды на озерном и речных участках – характерная особенность водохранилища (Современное…, 2002). По вертикали наибольшая разница поверхностной и придонной температуры отмечена вблизи плотины ГЭС, здесь при глубине 17–20 м она достигала 3.2°С. Содержание растворенного в воде кислорода было высоким по всей акватории (табл. 1). Даже в придонном горизонте глубоководных станций насыщение воды кислородом не опускалось ниже 70%, а у поверхности было близко к 100%.
Состав зоопланктона. Летом 2017 г. в составе зоопланктона (Cladocera, Cyclopoida, Calanoida, Rotifera) зарегистрировано 60 видов (табл. 2), преобладали ракообразные (55% списка). Это почти вдвое меньше, чем выявлено в теплом (температура воды 19–23°С) августе 2005 и 2007 гг. (Лазарева и др., 2013). Наибольшее видовое богатство (54 вида в списке) наблюдали на Шекснинском участке (табл. 3), который характеризуется максимальным разнообразием биотопов и обширными мелководьями. Среднее число видов в пробах было высоким и варьировало от 24 до 26, как и в общем списке 55–70% формировали ракообразные.
Таблица 2.
Список видов летнего зоопланктона Шекснинского водохранилища, выявленных в 2005–2017 гг.
| Таксон | 2005–2007 | 2017 |
|---|---|---|
| Класс Ракообразные – CRUSTACEA | ||
| Сем. Sididae | ||
| Sida crystallina (O.F. Müller, 1776) | + | + |
| Limnosida frontosa Sars, 1862 | +++ | +++ |
| Diaphanosoma brachyurum (Lievin, 1848) | ++ | ++ |
| D.orghidani Negrea, 1982 | ++ | – |
| Latona setifera (O.F. Müller, 1776) | + | – |
| Сем. Daphniidae | ||
| Daphnia longispina (O.F. Müller, 1776) s. str. | + | – |
| D. cristata Sars, 1862 | +++ | +++ |
| D. longiremis Sars, 1862 | + | ++ |
| D. galeata Sars, 1863 | +++ | +++ |
| D. hyalina Leydig, 1860 | – | + |
| D. cucullata Sars, 1862 | ++ | + |
| Simocephalus vetulus (O.F. Müller, 1776) | + | – |
| S. serrulatus (Koch, 1841) | + | – |
| Ceriodaphnia quadrangula (O.F. Müller, 1785) s. l. | + | – |
| C. pulchella Sars, 1862 s. l. | + | ++ |
| C. dubia (Richard, 1894 s. l.) | + | – |
| Scapholeberis mucronata (O.F. Müller, 1776) | + | – |
| Сем. Macrothricidae | ||
| Mасrothrix laticornis (Jurine, 1820) | + | – |
| Сем. Ilyocryptidae | ||
| Ilyocriptus agilis Kurz, 1874 | + | – |
| I. sordidus (Lievin, 1848) | + | – |
| Сем. Eurycercidae | ||
| Eurycercus lamellatus (O.F. Müller, 1776) | + | – |
| Сем. Chydoridae | ||
| Chydorus sphaericus (O.F. Müller, 1776) | ++ | ++ |
| C. gibbus Sars, 1890 | + | + |
| С. ovalis Kurz, 1875 | + | – |
| Pleuroxus uncinatus Baird, 1850 | – | + |
| P. adunctus (Jurine, 1820) | + | – |
| P. truncatus (O.F. Müller, 1785) | + | – |
| P. striatus (Schoedler, 1863) | + | – |
| Rhynchotalona falcata (Sars, 1862) | + | – |
| Disparalona rostrata (Koch, 1841) s. l. | + | – |
| Alona quadrangularis (O.F. Müller, 1785) | + | – |
| Biapertura affinis (Leydig, 1860) | + | + |
| Coronatella rectangula (Sars, 1861) | + | – |
| Flavalona rustica (Scott, 1895) | + | – |
| Acroperus harpae (Baird, 1834) | + | – |
| Leydigia leydigii (Schoedler, 1863) | + | – |
| Graptoleberis testudinaria (Fisсher, 1861) | + | – |
| Monospilus dispar Sars, 1862 | + | – |
| Kurzia latissima (Kurz, 1875) | + | + |
| Oxiurella tenuicaudis (Sars, 1862) | + | – |
| Cем. Вosminidae | ||
| Bosmina longirostris (O.F. Müller, 1776) | + | + |
| B. coregoni Baird, 1857 s. str. | ++ | – |
| В. c. cf. gibbera (Schoedler, 1863) | ++ | +++ |
| B. c. cf. longicornis Schoedler, 1886 | – | + |
| B. c. cf. longispina Leydig, 1860 | ++ | +++ |
| Bosmina c. cf. crassicornis (P.E. Müller), 1887 | ++ | ++ |
| Cем. Рolyphemidae | ||
| Polyphemus pediculus (L., 1758) | + | + |
| Сем. Сercopagidae | ||
| Bythotrephesbrevimanus Lilljeborg, 1901* | – | + |
| Bythotrephes brevimanus × B. cederstroemii (ранее определяли как B. longimanus Leydig) | ++ | ++ |
| Сем. Leptodoridae | ||
| Leptodora kindtii (Focke, 1844) | +++ | +++ |
| Сeм. Cyclopidae | ||
| Macrocyclops albidus (Jurine, 1820) | + | – |
| Eucyclops serrulatus (Fisсher, 1861) | + | – |
| E. macruroides (Lilljeborg, 1901) | + | – |
| E. macrurus (Sars, 1863) | + | – |
| Paracyclops fimbriatus (Fisсher, 1853) | + | + |
| P. affinis (Sars, 1863) | + | – |
| Сyclops vicinus Uljanin, 1875 | ++ | – |
| C. kikuchii Smirnov, 1932* | – | +++ |
| C. kolensis Lilljeborg, 1901 | – | ++ |
| Megacyclops viridis (Jurine, 1820) | ++ | ++ |
| Acanthocyclops vernalis (Fischer, 1853) | + | – |
| A. robustus (Sars, 1863) | + | – |
| Mesocyclops leuckarti (Claus, 1857) | +++ | +++ |
| Thermocyclops oithonoides (Sars, 1863) | +++ | +++ |
| T. crassus (Fisсher, 1853) | + | + |
| Сем. Diaptomidae | ||
| Eudiaptomus gracilis (Sars, 1863) | +++ | +++ |
| E. graciloides (Lilljeborg, 1888) | + | – |
| Arctodiaptomus laticeps (Sars, 1863) | + | ++ |
| Cем. Temoridae | ||
| Heterocope appendiculata Sars, 1863 | ++ | +++ |
| Eurytemora velox (Lilljeborg, 1853) | + | – |
| Класс Rotifera | ||
| Сем. Notommatidae | ||
| Cephalodella gibba (Ehrenberg, 1832)* | – | + |
| C. ventripes (Dixon-Nuttall, 1901) | + | – |
| Сем. Trichocercidae | ||
| Trichocerca (T.) cylindrica (Imhof, 1891) | + | – |
| T.capucina (Wierzejski et Zacharias, 1893) | + | – |
| T.longiseta (Schrank, 1802) | + | – |
| T. rattus (O.F. Müller, 1776)* | – | + |
| T. porcellus (Gosse, 1886) | + | + |
| T. similis (Wierzejski, 1893) | + | – |
| T. rousseleti (Voigt, 1902) | + | – |
| T. intermedia (Stenroos, 1898) | – | + |
| Сем. Synchaetidae | ||
| Synchaeta pectinata Ehrenberg, 1832 | + | + |
| S. oblonga Ehrenberg, 1831 | + | ++ |
| S. kitina Rousselet, 1902 | – | + |
| Polyarthra vulgaris Carlin, 1943 | + | – |
| P. dolichoptera Idelson, 1925 | + | – |
| P. minor Voigt, 1904 | + | + |
| P. longiremis Carlin, 1943 | + | + |
| P. euryptera Wierzejski, 1891 | + | + |
| P. luminosa Kutikova, 1962 | ++ | +++ |
| P. major Bruckhardt, 1900 | ++ | +++ |
| Bipalpus hudsoni (Imhof, 1891) | + | + |
| Ploesoma truncatum (Levander, 1894) | + | – |
| P. lenticulare Herrick, 1885 | + | – |
| Сем. Asplanchnidae | ||
| Asplanchna priodonta Gosse, 1850 | ++ | ++ |
| A. herriсki Guerne, 1888 | + | + |
| Сем. Lecanidae | ||
| Lecaneluna (O.F. Müller, 1776) | + | – |
| Сем. Trichotriidae | ||
| Trichotria truncata (Whitellegge, 1889) | + | – |
| Сем. Euchlanidae | ||
| Euchlanis dilatatalucksiana (Hauer, 1939) | ++ | + |
| E. meneta Myers, 1930 | + | – |
| E. deflexa Gosse, 1851 | + | – |
| E. pyriformis Gosse, 1851* | – | + |
| Сем. Brachionidae | ||
| Brachionus angularis Gosse, 1851 | + | – |
| B. quadridentatus Hermann, 1783 | + | – |
| B. diversicornis (Daday, 1883) | + | – |
| Keratella cochlearis (Gosse, 1851) | ++ | +++ |
| K. quadrata (O.F. Müller, 1786) | ++ | + |
| Kellicottia longispina Kellicott, 1879 | +++ | +++ |
| K. bostoniensis Rousselet, 1908 | + | + |
| Notholca labis Gosse, 1887* | – | + |
| Anureopsis fissa Gosse,1851 | + | – |
| Сем. Conochilidae | ||
| Conochilus hippocrepis (Schrank, 1803) | ++ | +++ |
| C. unicornis Rousselet, 1892 | + | +++ |
| C. coenobasis Skorikov, 1914 | + | – |
| Ceм. Collothecidae | ||
| Collotheca pelagica Rousselet, 1893 | – | + |
| Сем. Testudinellidae | ||
| Pompholyx sulcata Hudson, 1885 | + | + |
| Testudinella patina (Hermann, 1783) | + | – |
| Сем. Filiniidae | ||
| Filinia longiseta (Ehrenberg, 1834) | + | + |
| Сем. Hexarthridae | ||
| Hexarthra intermedia (Wiszniewski, 1929) | + | – |
| Число видов Crustacea | 64 | 33 |
| Число видов Rotifera | 42 | 27 |
| Суммарное число видов зоопланктона | 106 | 60 |
| Трофический индекс Е | 1.31 | 0.59 |
Таблица 3.
Распределение видового богатства зоопланктона по главным участкам Шекснинского водохранилища летом 2017 г.
| Таксон | Участок | Весь водоем (n = 23) |
||||
|---|---|---|---|---|---|---|
| Белозерский (n = 11) |
Шекснинский (n = 11) |
|||||
| S | Sобщ | S | Sобщ | S | Sобщ | |
| Cladocera | 9 ± 0.3 | 14 | 11 ± 1.0 | 21 | 10 ± 0.5 | 23 |
| Copepoda | 7 ± 0.3 | 9 | 7 ± 0.5 | 9 | 7 ± 0.3 | 10 |
| Rotifera | 8 ± 0.5 | 14 | 8 ± 1.0 | 24 | 8 ± 0.5 | 27 |
| Все группы | 24 ± 0.6 | 37 | 26 ± 1.8 | 54 | 24 ± 0.7 | 60 |
В 2017 г. выявлено пять видов, отсутствующих в опубликованных списках зоопланктона исследованного водохранилища (Смирнов, 1966; Луферова, 1966; Пидгайко, 1969; Антропогенное…, 1981; Современное…, 2002; Думнич, 2005; Ривьер, Литвинов, 2006; Лазарева и др., 2013; Думнич, Лобуничева, 2016, 2018). Среди них копепода Сyclops kikuchii Smirnov, 1932, коловратки Cephalodella gibba (Ehrenberg, 1832), Trichocerca rattus (O.F. Müller, 1776), Euchlanis pyriformis Gosse, 1851 и Notholca labis Gosse, 1887.
Копепода Сyclops kikuchii распространена по всей акватории водохранилища (встречаемость 87% проб), численность максимальна (>600 экз./м3) в северной половине оз. Белое. Большинство новых видов коловраток относилось к редким зарослевым формам, найденным единичными экземплярами. Малочисленная коловратка-вселенец Kellicottia bostoniensis Rousselet, 1908 обнаружена единично в оз. Белое вблизи устья р. Ковжа. Впервые она зарегистрирована в водоеме в 2005 г. (Лазарева и др., 2013).
В 2017 г. в Шекснинском участке водохранилища от створа дер. Аристово до плотины Шекснинской ГЭС отмечена сравнительно редкая кладоцера Bythotrephes brevimanus Lilljeborg, 1901, численность вида не превышала 55 экз./м3. На озерном участке водохранилища зарегистрирован лишь обычный для водоемов бассейна р. Волги гибрид Bythotrephes brevimanus × B. cederstroemii, его количество также не велико (<70 экз./м3). По составу зоопланктона трофический статус водохранилища в 2005–2007 гг. соответствовал эвтрофии (индекс Е 1.31), тогда как в 2017 г. – мезотрофии (индекс Е 0.59). Уровень сходства состава Crustacea между этими периодами был высоким (60–80%), однако состав Rotifera заметно различался (сходство 46%).
Доминантные виды. Основу численности зоопланктона (75–85% Crustacea и до 95% Rotifera) определяли 10 видов (табл. 4). Наиболее разнообразным был комплекс доминантов Шекснинского участка, в котором отмечено максимальное число видов ракообразных и коловраток. Напротив, сообщество Ковжинского участка структурно и количественно было крайне бедным (5 доминантов). Это вызвано сильным дождевым паводком в начале второй декады июля, когда приток по рекам Кема и Ковжа увеличился почти втрое. Результатом был вынос в устьевую область этих рек сильно гумифицированной воды с водосбора, в которой почти отсутствовали гидробионты. Уровень сходства структуры группировок доминантов был наименьшим для Ковжинского участка (14–55%), тогда как между Белозерским и Шекснинским участками сходство ядра зоопланктона достигало 45–64%, минимальные значения относились к Rotifera.
Таблица 4.
Встречаемость и обилие доминантных видов (N > 5% Nобщ) зоопланктона Шекснинского водохранилища в июле 2017 г.
| Вид | Участок водохранилища | |||||||
|---|---|---|---|---|---|---|---|---|
| Ковжинский | Белозерский | Шекснинский | ||||||
| N | N% | B% | N | N% | B% | N | N% | |
| Crustacea | ||||||||
| Mesocyclops leuckarti | 0.3 | 34 | 100 | 72.7 ± 8.6 | 58 ± 6 | 100 | 34.3 ± 7.6 | 50 ± 5 |
| Eudiaptomus gracilis | 0.2 | 26 | 100 | 17.8 ± 1.7 | 14 ± 2 | 91 | 17.3 ± 3.4 | 25 ± 7 |
| Thermocyclops oithonoides | 0.3 | 36 | 100 | 4.7 ± 0.9 | – | 91 | 4.5 ± 1.1 | 7 ± 2 |
| Daphnia cristata | 0 | 0 | 100 | 1.1 ± 0.4 | – | 100 | 4.2 ± 0.6 | 7 ± 2 |
| Rotifera | ||||||||
| Conochilus hippocrepis | 0 | 0 | 100 | 48.2 ± 16.4 | 58 ± 6 | 73 | 4.9 ± 1.8 | 7 ± 2 |
| Kellicottia longispina | 0 | 0 | 100 | 15.0 ± 2.7 | 18 ± 3 | 91 | 21.5 ± 6.5 | 31 ± 5 |
| Conochilus unicornis | 0.4 | 22 | 100 | 6.8 ± 2.5 | 8 ± 2 | 91 | 10.5 ± 8.0 | 15 ± 3 |
| Keratella cochlearis | 0 | 0 | 100 | 4.2 ± 0.6 | 5 ± 1 | 91 | 13.6 ± 8.0 | 19 ± 3 |
| Polyarthra luminosa | 0.1 | 6 | 100 | 6.2 ± 1.0 | 7 ± 2 | 64 | 11.2 ± 6.1 | 16 ± 4 |
| P. major | 0 | 0 | 100 | 2.6 ± 0.5 | – | 82 | 5.1 ± 1.6 | 7 ± 2 |
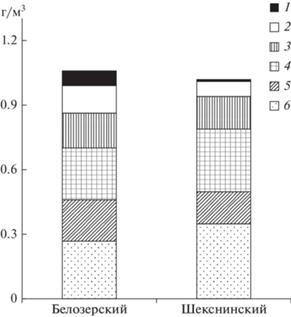
Более 80% биомассы сообщества формировали всего шесть видов ракообразных (рис. 1), среди них преобладали Limnosida frontosa (25–34%), Eudiaptomus gracilis (23–28%), Daphnia galeata (15–18%) и Mesocyclops leuckarti (15%). Их состав и соотношение в Белозерском и Шекснинском участках водоема были очень близки, индекс сходства структуры группировок доминантов превышал 85%.
Рис. 1.
Вклад массовых видов ракообразных в общую биомассу зоопланктона основных участков Шекснинского водохранилища в июле 2017 г. 1 – Arctodiaptomus laticeps, 2 – Heterocope appendiculata, 3 – Mesocyclops leuckarti, 4 – Eudiaptomus gracilis, 5 – Daphnia galeata, 6 – Limnosida frontosa.
В 2017 г. в оз. Белое зарегистрировано массовое развитие сравнительно редкой и крупной (длина тела 1.4–1.8 мм) копеподы Arctodiaptomus laticeps (Sars, 1863), вид встречался на всех станциях. В северной части озера его численность достигала 12 тыс. экз./м3, средний вклад в биомассу сообщества достигал 7%, что сравнимо с таковым Heterocope appendiculata Sars, 1863 (7–12%). В небольшом количестве (<2 тыс. экз./м3) A. laticeps встречался и на Шекснинском участке водоема (55% проб) от дер. Аристово до плотины Шекснинской ГЭС.
Помимо отмеченных в табл. 4 и на рис. 1, часто встречались (>80% проб) еще четыре вида Crustacea, которые в июле не образовывали высокой численности или биомассы (табл. 2). Это кладоцеры Bosmina coregoni cf. gibbera, B. c. cf. longispina Leydig, 1860, Leptodora kindtii (Focke, 1844) и на Шекснинском участке Bosmina c. cf. crassicornis (P.E. Müller, 1887).
Плодовитость массовых видов. В июле 2017 г. на пике размножения размер кладки всех массовых видов копепод был существенно выше (в 2–8 раза), чем таковой кладоцер (табл. 5). Вероятно, это способствовало превышению численности копепод над таковой кладоцер (табл. 4), несмотря на сравнительно низкую скорость популяционного роста копепод (Иванова, 1985; Андроникова, 1996).
Таблица 5.
Плодовитость массовых видов ракообразных (яиц/♀)на разных участках Шекснинского водохранилища в июле 2017 г.
| Вид | n | Участок водохранилища | |||
|---|---|---|---|---|---|
| Белое озеро | Сизьменский разлив | Приплотинный участок | Прочие* | ||
| Mesocyclops leuckarti | 39 | $\frac{{12 \pm 1.0}}{{6 - 22}}$ | $\frac{{12 \pm 2.1}}{{4 - 20}}$ | $\frac{{24 \pm 12.0}}{{10 - 36}}$ | $\frac{{16 \pm 2.2}}{{10 - 24}}$ |
| Eudiaptomus gracilis | 45 | $\frac{{10 \pm 0.3}}{{7 - 13}}$ | $\frac{{13 \pm 0.4}}{{9 - 16}}$ | $\frac{{11 \pm 1.1}}{{9 - 16}}$ | $\frac{{11 \pm 0.9}}{{7 - 15}}$ |
| Arctodiaptomus laticeps | 69 | $\frac{{14 \pm 0.4}}{{8 - 20}}$ | – | $\frac{{11 \pm 1.5}}{{6 - 16}}$ | $\frac{{15 \pm 0.9}}{{14 - 17}}$ |
| Thermocyclops oithonoides | 33 | $\frac{{8 \pm 0.4}}{{4 - 12}}$ | $\frac{{12 \pm 1.0}}{{8 - 16}}$ | $\frac{{10 \pm 1.2}}{{6 - 14}}$ | $\frac{{14 \pm 2.0}}{{12 - 16}}$ |
| Limnosida frontosa | 220 | $\frac{{3 \pm 0.2}}{{1 - 6}}$ | $\frac{{4 \pm 0.5}}{{2 - 7}}$ | $\frac{{2 \pm 0.4}}{{1 - 4}}$ | $\frac{{3 \pm 0.3}}{{1 - 10}}$ |
| Daphnia galeata | 310 | $\frac{{3 \pm 0.2}}{{1 - 8}}$ | $\frac{{6 \pm 0.6}}{{4 - 9}}$ | $\frac{{3 \pm 0.3}}{{1 - 6}}$ | $\frac{{4 \pm 0.6}}{{2 - 10}}$ |
| D. cristata | 275 | $\frac{{2 \pm 0.1}}{{1 - 4}}$ | $\frac{{4 \pm 0.2}}{{1 - 6}}$ | $\frac{{2 \pm 0.1}}{{1 - 3}}$ | $\frac{{3 \pm 0.7}}{{1 - 8}}$ |
| Bosmina coregoni cf. gibbera | 335 | $\frac{{2 \pm 0.2}}{{1 - 7}}$ | $\frac{{3 \pm 0.6}}{{1 - 6}}$ | $\frac{{2 \pm 0.1}}{{2 - 5}}$ | $\frac{{4 \pm 0.3}}{{1 - 6}}$ |
| B. c. cf. longispina | 80 | $\frac{{3 \pm 0.3}}{{2 - 6}}$ | $\frac{{2 \pm 0.6}}{{1 - 4}}$ | $\frac{{2 \pm 0.2}}{{1 - 3}}$ | $\frac{{3 \pm 0.7}}{{1 - 6}}$ |
| B. c. cf. crassicornis | 45 | – | – | $\frac{{2 \pm 0.3}}{{1 - 4}}$ | $\frac{{3 \pm 0.4}}{{1 - 7}}$ |
В оз. Белое наибольшая плодовитость отмечена у Arctodiaptomus laticeps (в среднем 14 яиц/♀) и Mesocyclops leuckarti (12 яиц/♀), на Шекснинском участке лидировали те же виды, но размер кладки был заметно выше (табл. 5). В целом, по акватории водохранилища максимальный размер кладки зарегистрирован у M. leuckarti на приплотинном участке (24 яйца/♀), у Arctodiaptomus laticeps (15 яиц/♀) и Thermocyclops oithonoides (14 яиц/♀) на русле р. Шексна у дер. Аристово, у Eudiaptomus gracilis в Сизьменском разливе (13 яиц/♀). Однако в отдельных биотопах озера и Сизьменского расширения водохранилища зарегистрированы случаи крайне маленьких кладок (2–3 яйца в мешке) у копепод Mesocyclops leuckarti и Thermocyclops oithonoides, на Приплотинном участке – у Arctodiaptomus laticeps (табл. 5). Вероятно, это связано с особенностями условий питания рачков.
Размер кладки всех пяти видов кладоцер в Белом озере был небольшим (в среднем 2–3 яйца/♀), сходную картину наблюдали и в большинстве биотопов Шекснинского участка (табл. 5). Наибольшая плодовитость зарегистрирована у четырех видов в Сизьменском расширении: Daphnia galeata (6 яиц/♀), Limnosida frontosa и Daphnia cristata (по 4 яйца/♀), Bosmina c. cf. gibbera (3 яйца/♀).
Вертикальное распределение. В июле ранним утром массовые виды ракообразных по-разному распределялись по вертикали. Так, кладоцеры Daphnia cristata, Bosmina c. cf. gibbera и копеподы Eudiaptomus gracilis формировали скопления (45–50% численности популяций) в верхнем 5-метровом горизонте вод (рис. 2). У поверхности держалась и основная часть Heterocope appendiculata (60%). В то же время, Daphnia galeata, Bosmina c. cf. longispina и Mesocyclops leuckarti в основном концентрировались (70–90%) в нижнем горизонте на глубине 11–17 м. Большая часть (70%) копеподитов и взрослых особей M. leuckarti и Eudiaptomus gracilis также находилась на глубине от 11 до 17 м (рис. 2б, рис. 2в). Количество их науплиусов до глубины 15 м было почти одинаковым, лишь у дна оно было немного выше (рис. 2в). Минимальное количество всех перечисленных видов и возрастных групп отмечали в слое 6–10 м, но именно здесь находилась половина (50%) популяции фильтратора Arctodiaptomus laticeps.
Рис. 2.
Вертикальное распределение зоопланктона в приплотинном участке Шекснинского водохранилища в июле 2017 г.: а – массовые виды Cladocera (1 – Daphnia cristata, 2 – D. galeata, 3 – Bosmina coregoni cf. gibbera, 4 – B. c. cf. longispina); б – массовые виды Copepoda (5 – Mesocyclops leuckarti, 6 – Eudiaptomus gracilis); в – Соpepoda разновозрастных стадий развития (7 – науплиусы, 8 – копеподиты, 9 – взрослые особи).
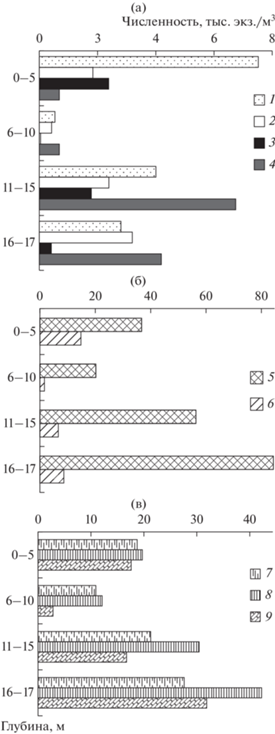
Численность коловраток на приплотинном участке водоема была низкой (<6 тыс. экз./м3). Оба вида рода Conochilus формировали скопления на глубине 16–17 м в 2-метровом слое над дном (60% обилия популяций). Обилие Kellicottia longispina Kellicott, 1879 распределялось по вертикали почти равномерно с минимумом в слое 6–10 м (<5% популяции).
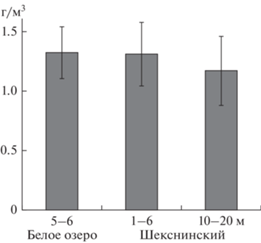
Численность и биомасса. В июле численность сообщества была максимальной (>200 тыс. экз./м3) на Белозерском участке, тогда как биомасса была сравнительно высокой (>1 г/м3) на большей части акватории (табл. 6). Наибольшую биомассу зоопланктона на Белозерском участке регистрировали на разрезе урочище Кустово – р. Водоба (1.4–3.4 г/м3) в западной части озера. Локально высокую биомассу (до 2.5 г/м3) регистрировали также вблизи плотины Шекснинской ГЭС. Однако по среднему уровню биомассы глубоководные участки (10–20 м) в Сизьменском расширении и у плотины ГЭС фактически не отличались от мелководных (1–6 м) биотопов Шекснинского участка водохранилища и оз. Белое (рис. 3). Минимальный уровень обилия отмечали в Ковжинском участке. Основу численности везде формировали копеподы (40–55%) и коловратки (40–50%), тогда как биомассу почти полностью (>95%) и фактически поровну образовывали обе группы ракообразных.
Таблица 6.
Численность (N, тыс. экз./м3) и биомасса (B, г/м3) главных таксонов зоопланктона Шекснинского водохранилища в июле 2017 г.
| Таксон | Участок водохранилища | Весь водоем |
||
|---|---|---|---|---|
| Ковжинский* | Белозерский | Шекснинский | ||
| Nclad | 0.06 | 9.7 ± 2.1 | 13.7 ± 1.7 | 11.2 ± 1.7 |
| Ncop | 0.7 | 116.6 ± 14.1 | 55.4 ± 9.6 | 82.3 ± 10.5 |
| Nrot | 1.8 | 83.5 ± 17.6 | 70.1 ± 32.8 | 73.5 ± 14.8 |
| Nобщ | 2.6 | 209.8 ± 26.3 | 139.2 ± 43.2 | 167.0 ± 21.8 |
| Bclad | 0.001 | 0.66 ± 0.11 | 0.67 ± 0.12 | 0.63 ± 0.09 |
| Bcop | 0.002 | 0.63 ± 0.11 | 0.53 ± 0.12 | 0.55 ± 0.07 |
| Brot | 0.003 | 0.04 ± 0.01 | 0.03 ± 0.02 | 0.04 ± 0.01 |
| Вобщ | 0.006 | 1.33 ± 0.20 | 1.23 ± 0.19 | 1.22 ± 0.15 |
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
По литературным данным зоопланктон Шекснинского водохранилища насчитывает ~155 видов, большинство из которых (~60%) относятся к Crustacea (Смирнов, 1966; Луферова, 1966; Пидгайко, 1969; Антропогенное…, 1981; Современное…, 2002; Думнич, 2005; Ривьер, Литвинов, 2006; Думнич, Лобуничева, 2016, 2018). С учетом данных, представленных в настоящей работе (табл. 2), видовое богатство сообщества возрастает до 180 видов, 54% списка формируют ракообразные. Состав зоопланктона Шекснинского водохранилища (табл. 2) сходен с таковым в Рыбинском водохранилище (по: Лазарева, 2007а), следующем в каскаде водоемов рек Шексны и Волги. Сходство списков Crustacea достигает 60%, Rotifera – 51%. Фауна зоопланктона Шекснинского водохранилища достаточно динамична. Каждое его обследование приносит находки новых видов, отсутствующих в ранее опубликованных списках. Так, в 2005–2007 гг. выявлено 24 новых для водоема видов (Лазарева и др., 2013), в 2017 г. – 5 видов.
Впервые отмеченную в 2017 г. копеподу Сyclops kikuchii ранее считали подвидом С. vicinus Uljanin,1875 (Определитель …, 2010). В 2005–2007 гг. в водохранилище находили только С. vicinus s. str. Lilljeborg, 1901 (Лазарева и др., 2013). Возможно, С. kikuchii и ранее появлялся в водоеме, но в публикациях его указывали в составе С. vicinus s. l. Крупная кладоцера Bythotrephes brevimanus впервые определена в Шекснинском водохранилище Н.М. Коровчинским из сборов Е.В. Лобуничевой 2011–2012 гг. (Korovchinsky, 2018). Не известно, как давно B. brevimanus обитает в водоеме, для фауны оз. Белое он указан в работах (Думнич, Лобуничева, 2016, 2018). На Шекснинском участке водоема вид был обнаружен впервые.
Копепода Arctodiaptomus laticeps в небольшом количестве впервые зарегистрирована в оз. Белое М.Л. Пидгайко (1969). В последующем, ее единично отмечали в 1970-х годах (Антропогенное …, 1981; Ривьер, Литвинов, 2006), также вид обнаружен в сборах 2007 г. В.Н. Столбуновой (устное сообщение). Далее до 2017 г. A. laticeps в Шекснинском водохранилище не регистрировали (Думнич, Лобуничева, 2016, 2018). Его массовое развитие и широкое распространение в водоеме выявлено было впервые.
В целом, состав и структура доминантного комплекса зоопланктона водохранилища в холодном июле 2017 г. (температура воды 16–18°С) близки к отмеченному в сходном по прогреву (18–19°С) июле 1987 г. (Ривьер, Литвинов, 2006). Однако в 2017 г. в планктоне почти отсутствовал Chydorus sphaericus (O.F. Müller, 1776), а из дафний была многочисленна весенняя Daphnia cristata Sars, 1862, а не летняя D. cucullata Sars, 1862. Вероятно, к середине июля сообщество водохранилища еще не трансформировалось в характерное для лета. Причиной такого запаздывания, по-видимому, стала низкая температура воды. Обычно D. cristata и D. longiremis характерны для зоопланктона водохранилища в июне, тогда как D. cucullata – в июле–августе (Антропогенное…, 1981; Лазарева и др., 2013).
Состав доминантных коловраток в 2017 г. (табл. 4) почти совпадал с таковым в 1987 и 2001 гг. (Ривьер, Литвинов, 2006). Однако среди представителей рода Polyarthra многочисленными были P. luminosa Kutikova, 1962 и P. major Bruckhardt, 1900, а не Polyarthra vulgaris Carlin, 1943. Сравнение группировок доминантов в июле 2017 г. (табл. 4) и августе 2005–2007 гг. (по: Лазарева и др., 2013) показало, что их состав и структура существенно различались. Индексы общности структуры не превышали 42% для ракообразных и 34% для коловраток.
Сведения об индивидуальной плодовитости зоопланктеров редко приводят в гидробиологических работах, обычно эти данные анализируют для оценки продуктивности сообщества (Иванова, 1985; Андроникова, 1996; Тимохина, 2000; Лазарева, 2010). Для Шекснинского водохранилища такие исследования ранее не проводили, анализ плодовитости массовых форм ракообразных сделан в данной работе впервые. Уровень индивидуальной плодовитости копепод (размер кладки самок) в Шекснинском водохранилище оказался существенно ниже наблюдаемого в р. Волге. Так, для Mesocyclops leuckarti и Eudiaptomus gracilis в Куйбышевском водохранилище размер кладки в июле достигает в среднем 24 и 18 яиц/♀ соответственно (Тимохина, 2000). В Чебоксарском водохранилище для Mesocyclops leuckarti и Thermocyclops oithonoides плодовитость в августе составляет в среднем 22 и 16 яиц/♀ соответственно (Лазарева и др., 2022). Подобный уровень плодовитости перечисленных видов в Шекснинском водохранилище отмечен только локально (табл. 5).
Размер кладки массовых видов кладоцер в исследованном водоеме в основном невелик (табл. 5). Для Limnosida frontosa он сопоставим с отмеченным в Рыбинском водохранилище (в среднем 2–4 яйца/♀) (Соколова, 2007). Плодовитость Daphnia galeata близка к наблюдаемой в том же водохранилище в июле–августе (в среднем 4 яйца/♀), а для Bosmina c. cf. longispina она ниже отмеченной даже в сентябре (4–5 яиц/♀) (Лазарева, 2010).
В Куйбышевском водохранилище при сходной температуре воды размер кладки B. c. cf. longispina достигает в среднем 12 яиц/♀, а Daphnia galeata – 10 яиц/♀ (Тимохина, 2000), что в 2–3 раза больше по сравнению с Шекснинским водохранилищем. В озерах Карельского перешейка плодовитость Daphnia cristata достигает в среднем 6 яиц/♀ (Иванова, 1985), что вдвое выше таковой на большей части акватории исследованного водоема. Однако для D. cristata из озер Карелии приводят и меньшие значения (2 яйца/♀) (Андроникова, 1996). Сравнительно низкий темп размножения кладоцер в Шекснинском водохранилище, вероятно, определялся низкой температурой воды в летнем сезоне 2017 г. и недостаточной обеспеченностью пищей. Ранее показано, что количество водорослей положительно влияет на обилие зоопланктона (Лазарева и др., 2013). К сожалению, данные о развитии фитопланктона водохранилища в 2017 г. до сих пор не опубликованы.
Общее количество (масса) яиц у ракообразных возрастает с увеличением размера и массы тела самки, а число яиц в кладке сильно варьирует в течение вегетационного периода (Иванова, 1985; Ривьер, 1986; Сущеня и др., 1990; Тимохина, 2000; Лазарева, 2010). Репродуктивная способность самок снижается с возрастом, наибольшее количество яиц обычно наблюдается в двух первых кладках (Филимонов, Соколова, 1973; Гламазда, 1974; Лазарева, 2007б). У пелагических кладоцер наиболее плодовитые самки выходят из покоящихся яиц весной (май–начало июня), они же дают большее число партеногенетических пометов и суммарное количество яиц в течение жизни (Иванова, 1985; Сущеня и др., 1990; Тимохина, 2000; Лазарева, 2007б; Лазарева, 2010). У копепод (Cyclopoida и Calanoida) максимальная индивидуальная плодовитость и наибольшая частота пометов тоже отмечены в начале их размножения в водоеме, что связывают с более крупными размерами самок первых генераций (Тимохина, 2000). Однако некоторые авторы отмечают (Ривьер, 1986), что самые мелкие самки Cyclops kolensis Lilljeborg, 1901 в первых пометах откладывают мало яиц, но их плодовитость возрастает в последующих пометах и в течение жизни они даже могут откладывать больше яиц, чем крупные особи. Кроме того, индивидуальная плодовитость ракообразных сильно зависит от количества и доступности пищи, – в олиготрофных водоемах часто наблюдают меньшую индивидуальную плодовитость рачков, по сравнению с эвтрофными (Иванова, 1985). При низкой плодовитости ракообразных в Шекснинском водохранилище в середине июля их максимальная весенняя плодовитость, теоретически должна быть более высокой.
Вертикальные миграции зоопланктона в водохранилищах определяются в основном совокупностью экологических условий (Маркевич, 1982; Гладышев, 1990). Из этого следует, что характер миграций различается в течение сезона и год от года даже в одном водоеме. Для оз. Белое показано (Антропогенное…, 1981), что летом в дневное время массовые виды коловраток, в том числе род Conochilus, обычно концентрируются у поверхности водоема, крупные дафнии и Heterocope appendiculata – в придонном слое, а остальные копеподы распределяются равномерно во всем столбе воды. Для глубокого участка у плотины Шекснинской ГЭС установлено (Ривьер, Литвинов, 2006), что в первой половине дня массовый вид коловраток Kellicottia longispina держится в верхнем 4-метровом слое, кладоцеры Daphnia galeata и Bosmina c. cf. longispina – глубже 7 и 9 м соответственно, а все массовые виды копепод образуют скопления глубже 5 м.
В июле 2017 г. типичным для глубоководной части водоема было распределение по вертикали B. c. cf. longispina, Daphnia galeata и копепод Mesocyclops leuckarti, концентрировавшихся на глубине. Остальные виды распределялись совершенно иначе (рис. 3), нежели указано в литературе (Антропогенное…, 1981; Маркевич, 1982; Ривьер, Литвинов, 2006). Одной из причин нетипичного распределения части планктонных популяций по вертикали могла быть их перегруппировка между придонным горизонтом и поверхностью воды ранним утром. Это так называемые “сумеречные” миграции, при которых ночью часть планктона поднимается к поверхности, а утром опускается в более глубокие слои воды (Киселев, 1980). Так, в дневное время скопление на глубине коловраток рода Conochilus отмечали в оз. Сиверском, тогда как коловратки рода Kelliсottia ранним утром перемещались с глубины к поверхности водоема (Маркевич, 1982). Типично дневное распределение устанавливается ближе к 12 ч дня (Гладышев, 1990).
В июле 2017 г. средняя биомасса зоопланктона (1.22 ± 0.15 г/м3) в водохранилище была сравнительно высокой. Ее значения близки к зарегистрированным (1.48 ± 0.14 г/м3) 10 лет назад в августе 2007 г., но почти вдвое ниже таковых (2.19 ± ± 0.29 г/м3) в августе 2005 г. (Лазарева и др., 2013). Не выявлено существенного различия в среднем уровне биомассы зоопланктона между Белозерским и Шекснинским участками водохранилища, ранее отмечали ее увеличение в направлении от озера к плотине ГЭС (Ривьер, Литвинов, 2006; Лазарева и др., 2013). Современный уровень биомассы заметно ниже такового (2.5–2.6 г/м3) в конце 1970-х и середине 1990-х годов (Ривьер, 1982; Современное …, 2002). Значительные колебания обилия сообщества год от года обычны для водохранилищ (Лазарева, 2010), в том числе для Шекснинского водохранилища (Современное …, 2002; Думнич, Лобуничева, 2016). Межгодовые вариации биомассы определяются пищевой обеспеченностью зоопланктона и термическим режимом, от которых зависит сезонный ход развития сообщества (Антропогенное …, 1981; Современное …, 2002; Ривьер, Литвинов, 2006; Лазарева и др., 2013). Так, с 1974 по 2015 гг. осенняя биомасса сообщества в оз. Белое варьировала в пределах 0.1–3.4 г/м3 и год от года различалась в 2–34 раза (Думнич, Лобуничева, 2016).
Выводы. Летом 2017 г. в зоопланктоне Шекснинского водохранилища зарегистрировано 60 видов, среди них пять новых для водоема. Анализ литературных данных показал, что видовое богатство сообщества достигает 180 видов, среди которых преобладают Crustacea (54%). Впервые зарегистрировано массовое развитие и широкое распространение в водохранилище редкой копеподы Arctodiaptomus laticeps. На большей части акватории преобладают обычные для водохранилища кладоцеры Limnosida frontosa и Daphnia galeata, копеподы Eudiaptomus gracilis и Mesocyclops leuckarti. Показано, что численность летнего зоопланктона водохранилища (75–85% Crustacea и до 95% Rotifera) определяют 10 видов, а >80% биомассы сообщества формируют только шесть видов Crustacea. Структура зоопланктона в холодном июле 2017 г. сходна с таковой в другие годы с низким летним прогревом вод водохранилища. Впервые проанализирована плодовитость ракообразных, установлено, что в водохранилище размер кладки массовых видов копепод и кладоцер заметно ниже, отмеченного в те же сроки в других водохранилищах Волжского каскада. Средняя биомасса зоопланктона достигает 1.22 ± 0.15 г/м3, локально – 2.5–3.4 г/м3. Крайне низкое обилие сообщества (<0.01 г/м3) отмечено выше оз. Белое на Ковжинском участке. Средний уровень биомассы сообщества летом 2017 г. вдвое ниже такового (2.5–2.6 г/м3) в 1970-х и 1990-х годах.
Список литературы
Андроникова И.Н. 1996. Структурно-функциональная организация зоопланктона озерных экосистем. Санкт-Петербург: Наука.
Антропогенное влияние на крупные озера Северо-Запада СССР. 1981. Ленинград: Наука. Ч. 2.
Балушкина Е.В., Винберг Г.Г. 1979. Зависимость между длиной и массой тела планктонных ракообразных // Экспериментальные и полевые исследования биологических основ продуктивности озер. Ленинград: Зоол. ин-т АН СССР. С. 58.
Боруцкий Е.С., Степанова Л.А., Кос М.С. 1991. Определитель Calanoida пресных вод СССР. Ленинград: Наука.
Гладышев М.И. 1990. Суточная динамика вертикального распределения массовых видов зоопланктона в Сыдинском заливе Красноярского водохранилища // Известия Сибирского отделения АН СССР. Сер. Биологические науки. Вып. 3. С. 78.
Гламазда В.В. 1974. Рост, размножение и продукция массовых видов кладоцер и копепод Цимлянского водохранилища // Тр. Волгоград. отделения Гос. ин-та реч. рыб. хоз-ва. С. 41.
Думнич Н.В. 2005. Особенности формирования структуры зоопланктона крупных озер Вологодской области // Экологическое состояние континентальных водоемов северных территорий. Санкт-Петербург: Наука ВВМ. С. 121.
Думнич Н.В., Лобуничева Е.В. 2016. Динамика зоопланктона озерной части Шекснинского водохранилища (Вологодская область) // Современное состояние биоресурсов внутренних водоемов и пути их рационального использования: Матер. докл. Всерос. конф. с международным участием, посвященной 85-летию Татарского отделения ГосНИОРХ (Казань, 24–29 октября 2016 г.). Казань: ГосНИИ озер. и реч. рыб. хоз-ва. С. 338.
Думнич Н.В., Лобуничева Е.В. 2018. Сезонная динамика зоопланктона озерной части Шекснинского водохранилища (по материалам 2016 г.) // Рыбохозяйственные водоемы России: фундаментальные и прикладные исследования: Матер. 2-ой Всерос. науч. конф. с междунар. участием. Санкт-Петербург: ГосНИИ озер. и реч. рыб. хоз-ва. 2–4 апреля 2018 г. С. 162.
Иванова М.Б. 1985. Продукция планктонных ракообразных в пресных водах. Ленинград: Зоол. ин-т АН СССР.
Киселев И.А. 1980. Планктон морей и континентальных водоемов. Ленинград: Наука. Т. 2.
Коровчинский Н.М., Котов А.А., Синев А.Ю. и др. 2021. Ветвистоусые ракообразные (Crustacea, Cladocera) северной Евразии. Т. 2. Москва: Товарищество науч. изданий КМК.
Кутикова Л.А. 1970. Коловратки фауны СССР. Ленинград: Наука.
Лазарева В.И. 2007а. Состав ракообразных и коловраток Рыбинского водохранилища // Экология водных беспозвоночных. Нижний Новгород: Вектор ТиС. С. 127.
Лазарева В.И. 2007б. Сезонная динамика численности и параметры жизненного цикла Diaphanosoma brachyurum (Lievin) (Crustacea, Sididae) в водоемах разного типа // Экология водных беспозвоночных. Нижний Новгород: Вектор ТиС. С. 144.
Лазарева В.И. 2010. Структура и динамика зоопланктона Рыбинского водохранилища. Москва: Товарищество науч. изданий КМК.
Лазарева В.И., Жданова С.М., Сабитова Р.З. 2022. Расселение восточно-азиатской копеподы Thermocyclops taihokuensis (Harada, 1931) (Crustacea, Cyclopoida) в бассейне реки Волги // Биология внутр. вод. № 2. С. 147.https://doi.org/10.31857/S0320965222010065
Лазарева В.И., Столбунова В.Н., Минеева Н.М., Жданова С.М. 2013. Особенности структуры и пространственного распределения планктона в Шекснинском водохранилище // Биология внутр. вод. № 3. С. 46.https://doi.org/10.7868/S0320965213030091
Луферова Л.А. 1966. Формирование зоопланктона Череповецкого водохранилища // Планктон и бентос внутренних водоемов. Москва: Наука. С. 68.
Маркевич Г.И. 1982. Суточная динамика вертикального распределения массовых форм зоопланктона в оз. Сиверском // Тр. Ин-та биол. внутр. вод. АН СССР. № 45(48). С. 100.
Мордухай-Болтовской Ф.Д., Дзюбан Н.А. 1976. Изменения в составе и распределении фауны Волги в результате антропогенных воздействий // Биологические продукционные процессы в бассейне Волги. Ленинград: Наука. С. 67.
Определитель зоопланктона и зообентоса пресных вод Европейской России. 2010. Т. 1. Зоопланктон. Москва: Товарищество науч. изданий КМК.
Песенко Ю.А. 1982. Принципы и методы количественного анализа в фаунистических исследованиях. Москва: Наука.
Пидгайко М.Л. 1969. Зоопланктон Белого озера в связи с рыбохозяйственным значением водоема // Изв. Гос. ин-та реч. рыб. хоз-ва. Ленинград. Т. 65. С. 111.
Ривьер И.К. 1982. Современное состояние зоопланктона водоемов Волго-Балтийской и Северо-Двинской водных систем // Экологические исследования водоемов Волго-Балтийской и Северо-Двинской водных систем. Ленинград: Наука. С. 90.
Ривьер И.К. 1986. Состав и экология зимних зоопланктонных сообществ. Ленинград: Наука.
Ривьер И.К., Литвинов А.С. 2006. Сравнительный анализ зоопланктона Шекснинского водохранилища в 1987 и 2001 гг. // Вод. ресурсы. Т. 33. № 5. С. 615.
Смирнов Н.Н. 1966. Прибрежные ветвистоусые ракообразные Череповецкого водохранилища // Планктон и бентос внутренних водоемов. Москва; Ленинград: Наука, С. 146.
Современное состояние экосистемы Шекснинского водохранилища. 2002. Ярославль: Изд-во Ярослав. гос. тех. ун-та.
Соколова Е.А. 2007. Многолетние изменения численности и биомассы, структурные характеристики и некоторые черты биологии Limnosida frontosa Sars в Рыбинском водохранилище // Ветвистоусые ракообразные: систематика и биология: Матер. Всерос. шк.-конф. Нижний Новгород: Вектор ТиС. С. 327.
Степаньянц С.Д., Хлебович В.В., Алексеев В.Р. и др. 2015. Определитель рыб и беспозвоночных Каспийского моря. Т. 2: Стрекающие, гребневики, многощетинковые черви, веслоногие ракообразные и мизиды. Санкт-Петербург; Москва: Товарищество науч. изданий КМК.
Структура и функционирование экосистемы Рыбинского водохранилища в начале XXI века. Москва: РАН. 2018.
Сущеня Л.М., Семенченко В.П., Семенюк Г.А., Трубецкова И.Л. 1990. Продукция планктонных ракообразных и факторы среды. Минск: Наука и техника.
Тимохина А.Ф. 2000. Зоопланктон как компонент экосистемы Куйбышевского водохранилища. Тольятти: Ин-т экологии Волжского бассейна РАН.
Филимонов Л.А., Соколова Г.В. 1973. О продукционных возможностях двух массовых видов планктонных циклопов Костромского разлива // Тр. Костромского гос. пед. ин-та. Вып. 31. С. 62.
Korovchinsky N.M. 2018. Further revision of the genus Bythotrephes Leydig (Crustacea: Cladocera: Onychopoda): redescription of B. brevimanus Lilljeborg, reevaluation of B. cederströmii Schödler, and description of a new species of the genus // Zootaxa. V. 4379 (3). P. 347. https://doi.org/10.11646/zootaxa.4379.3.2
Lazareva V.I. 2019. Spreading of Alien Zooplankton Species of Ponto-Caspian Origin in the Reservoirs of the Volga and Kama Rivers // Russian Journal of Biological Invasions. V. 10. № 4. P. 328. https://doi.org/10.1134/S2075111719040040
Ruttner-Kolisko A. 1977. Suggestion for biomass calculation of planktonic rotifers // Arch. Hydrobiol. Ergebn. Limnol. Bd 8. P. 71.
Shurganova G.V., Zhikharev V.S., Gavrilko D.E. et al. 2019. Zooplankton Communities of the Middle River Part of the Cheboksary Reservoir and Factors Influencing Their Species Structure // Povolzhskiy Journal of Ecology. № 3. P. 384. https://doi.org/10.35885/1684-7318-2019-3-384-395
Wilke T., Ahlrichs W.H., Bininda-Emonds O.R.P. 2018. A comprehensive and integrative re-description of Synchaeta oblonga and its relationship to Synchaeta tremula, Synchaeta rufina and Synchaeta littoralis (Rotifera: Monogononta) // Organisms Diversity & Evolution. V. 18. P. 407. https://doi.org/10.1007/s13127-018-0380-8
Дополнительные материалы отсутствуют.
Инструменты
Биология внутренних вод