Физиология человека, 2023, T. 49, № 2, стр. 18-26
Нейрофизиологические показатели у пациентов после коронарного шунтирования в зависимости от успеха реабилитации с применением метода двойных задач
Д. С. Куприянова 1, И. В. Тарасова 1, *, О. А. Трубникова 1, А. С. Соснина 1, И. Н. Кухарева 1, И. Д. Сырова 1, О. Л. Барбараш 1
1 ФГБНУ НИИ комплексных проблем сердечно-сосудистых заболеваний
Кемерово, Россия
* E-mail: iriz78@mail.ru
Поступила в редакцию 06.08.2022
После доработки 26.08.2022
Принята к публикации 09.09.2022
- EDN: MTRCEU
- DOI: 10.31857/S0131164622600641
Аннотация
Проведен анализ влияния когнитивной реабилитации с применением метода двойных задач на нейрофизиологические показатели пациентов с послеоперационной когнитивной дисфункцией (ПОКД) в раннем послеоперационном периоде коронарного шунтирования (КШ) в условиях искусственного кровообращения. В исследовании приняли участие 96 пациентов мужского пола, перенесшие КШ. Всем было проведено детальное нейропсихологическое и электроэнцефалографическое (ЭЭГ) исследование до и после КШ. На 2–3-и сут после операции у всех пациентов была диагностирована ПОКД, и они были произвольно разделены на две группы: с тренингом (n = 54) и без тренинга (n = 42). Начиная с 3–4 сут послеоперационного периода, проводился ежедневный курс тренировок с применением двойной задачи (одновременное выполнение когнитивного и физического компонентов). Повторная диагностика ПОКД была проведена по завершению курса тренинга, на 8–11-е сут. Установлено, что пациенты, успешно прошедшие тренинг (с отсутствием ПОКД на 8–11-е сут) демонстрируют послеоперационное снижение мощности θ1-ритма, тогда как у всех пациентов с наличием ПОКД эти показатели возросли по сравнению с дооперационными данными. Топографические особенности изменений θ1-ритма выявлены в левых теменных областях коры, что может свидетельствовать о нарушении перфузии в этих регионах мозга.
Неоднократно показано, что процесс старения, отягощенный сердечно-сосудистыми заболеваниями, сопровождается выраженным когнитивным дефицитом в результате цереброваскулярных нарушений [1–3]. Коронарное шунтирование (КШ) является необходимым методом для реваскуляризации у пациентов, страдающих тяжелой ишемической болезнью сердца (ИБС). Но кардиохирургические вмешательства в условиях искусственного кровообращения (ИК) и общей анестезии, нацеленные на лечение сердечно-сосудистых заболеваний, могут негативно влиять на когнитивные функции пациентов. К таким состояниям относят послеоперационную когнитивную дисфункцию (ПОКД). Частота развития ПОКД варьирует от 40 до 70% и сохраняется в 30–50% случаев в отдаленном периоде после операции, что влияет на качество жизни и повышает риск смертности в первый год послеоперационного периода [4–6]. Установлено, что активно задействованные в когнитивной деятельности фронто-центральная и париетальная кора находятся в зоне смежного кровоснабжения крупных мозговых артерий и наиболее уязвимы к воздействию периоперационных факторов, таких как гипоперфузия и микроэмболия. В связи с этим для пациентов, перенесших операции с применением ИК, необходима разработка подходов к когнитивной реабилитации, которые учитывают особенности каждого клинического случая [7, 8].
В настоящее время в качестве перспективного реабилитационного подхода предлагается метод двойных задач, включающий в себя одновременное выполнение моторных и когнитивных компонентов. Одновременное выполнение различных задач – ключевой аспект повседневной деятельности и применение для когнитивной реабилитации мультимодального метода, является актуальным, учитывая, что лица с нарушениями мозговых функций справляются с такими задачами хуже. Известно, что основным когнитивным дефицитом, характерным для цереброваскулярных расстройств, является нарушение исполнительного контроля, что вызывает ухудшение управления двумя и более задачами и может оказать негативное влияние на качество жизни пациентов в послеоперационный период [1, 9]. В проведенных ранее работах, использовавших парадигмы двойных задач, были продемонстрированы их положительные эффекты в восстановлении когнитивных и моторных нарушений у пожилых людей [10, 11], при черепно-мозговых травмах [12] и у пациентов с болезнью Паркинсона [13, 14]. Стоит отметить, что использование мультимодального метода для кардиохирургических пациентов, перенесших операцию в условиях ИК, требует включения задач, соответствующих их физическому состоянию в послеоперационный период, а уровень сложности когнитивных заданий может постепенно увеличиваться в ходе тренинга. Метод двойных задач в качестве реабилитационного подхода может иметь обширный восстановительный эффект за счет одновременной стимуляции проблемных зон коры у кардиохирургических пациентов, а изучение изменений нейрофизиологических показателей – информативным способом мониторинга за восстановительной динамикой [15]. Однако влияние когнитивной реабилитации с применением метода двойных задач на нейрофизиологические показатели у кардиохирургических пациентов мало изучено и ее эффективность активно обсуждается.
Принимая во внимание вышесказанное, целью данного исследования явился анализ влияния когнитивной реабилитации с применением метода двойных задач на нейрофизиологические показатели пациентов с ПОКД в раннем послеоперационном периоде КШ в условиях ИК.
МЕТОДИКА
В исследовании принимали участие 96 пациентов (75 мужчин и 21 женщина, медиана возраста – 63.0 г.), поступившие для планового проведения операции КШ в ФГБНУ НИИ “Комплексных проблем сердечно-сосудистых заболеваний” (г. Кемерово). Все пациенты прошли клинико-инструментальное и неврологическое обследования. Критерии исключения из исследования: возраст пациентов старше 70 лет, тяжелые сопутствующие заболевания (хроническая обструктивная болезнь легких, онкопатология), нарушения сердечного ритма, тяжелая форма сердечной недостаточности, алкогольная и наркотическая зависимость, заболевания и/или травмы ЦНС, деменция (сумма баллов по Монреальской шкале оценки когнитивных функций (MoСA) ≤ 20), депрессивное расстройство (сумма баллов по шкале депрессии Бека (BDI-II) ≤ 8), отказ от участия в исследовании.
На 2–3-и сут после операции, после установки диагноза ПОКД, методом конвертов были сформированы две группы: группа послеоперационного когнитивного тренинга (n = 54) и группа сравнения – без тренинга (n = 42). Клинико-анамнестические характеристики исследуемых групп представлены в табл. 1. Операция КШ всем пациентам проведена с применением ИК по стандартной методике. Основные интраоперационные показатели указаны в табл. 2.
Таблица 1.
Клинико-анамнестические характеристики групп пациентов с наличием и отсутствием когнитивного тренинга, Ме [25; 75]
| Показатели | Пациенты, n = 96 | p | |
|---|---|---|---|
| без когнитивного тренинга, n = 42 | с когнитивным тренингом, n = 54 | ||
| Возраст, лет, Me [25; 75] | 62.5 [60; 67] | 64 [60; 68] | n/s |
| Пол (мужчины/женщины), n | 33/9 | 43/12 | n/s |
| Образование, Me [25; 75] | 12 [10; 12] | 11 [10; 15] | |
| Функциональный класс стенокардии, n (%): | n/s | ||
| 0–I | 10 (25) | 4 (7) | |
| II | 22 (50) | 39 (72) | |
| III | 10 (25) | 11 (21) | |
| MoCa, баллы, Ме [25; 75] | 26 [23; 27 ] | 25 [24; 27 ] | n/s |
| BDI-II, баллы, Ме [25; 75] | 1 [0; 2] | 3 [1; 5] | n/s |
| Фракция выброса левого желудочка, Me [25; 75] | 61.5 [48; 66] | 65 [53; 67] | n/s |
| Длительность ИБС, лет, Ме [25; 75] | 3 [1; 11] | 2 [1; 6] | n/s |
| Функциональный класс ХСН по NYHA, n (%): | n/s | ||
| II | 38 (90) | 49 (90) | |
| III | 4 (10) | 5 (10) | |
| Артериальная гипертензия, лет, Ме [25; 75] | 15 [6; 20] | 2 [6; 15] | n/s |
| Стенозы сонных артерий, n (%): | |||
| нет | 33 (79) | 20 (37) | n/s |
| <50% | 9 (21) | 34 (63) | |
Таблица 2.
Интраоперационные параметры групп пациентов с наличием и отсутствием когнитивного тренинга, Ме [25; 75]
Последовательность проведения нейропсихологического, ЭЭГ-исследования и когнитивных тренингов представлена в дизайне исследования на рис. 1.
Расширенное нейропсихологическое тестирование все группы пациентов прошли за 3–5 дней до операции, на 2–3-и и на 8–11-е сут после КШ с использованием программно-аппаратного комплекса “Статус ПФ” (В.И. Иванов, Н.А. Литвинова, М.Г. Березина. Свидетельство об официальной регистрации программы для ЭВМ № 2 001 610 233 от 5.03.2001) [15]. Наличие ПОКД на 2–3 день после операции и по завершению когнитивного тренинга (8–11-е сутки) диагностировали с помощью критерия “20–20” [15]. При этом изменения когнитивных показателей оценивали по формуле: ((исходное значение – послеоперационное значение показателя)/исходное значение) × 100%.
Начиная с 3–4 сут после КШ, пациентам основной группы был проведен ежедневный 5–7-дневный курс тренинга с выполнением двойной задачи. Группа когнитивного тренинга произвольно была разделена на подгруппы по типу используемой моторной задачи: удержание статичной позы с помощью аппаратно-программного стабилографического комплекса “Стабилан-01-2” (Россия) (n = 29) и выполнение простой зрительно-моторной реакции с помощью программного комплекса “Статус ПФ” (n = 28). Когнитивная задача в обеих подгруппах не отличалась и была представлена последовательным вычитанием из числа 100 числа 7, вербальной беглостью и задачей открытого типа “Необычное использование обычного предмета”, где требуется назвать как можно больше вариантов необычного использования обычного предмета (кирпич, линейка, газета). Тренировки проводили в специализированном помещении в первой половине дня с продолжительностью от 5 до 20 мин на одну тренировку, среднее количество составляло 5 тренировок.
Монополярную регистрацию электроэнцефалограммы (ЭЭГ) (62 канала; полоса пропускания 0.1–50.0 Гц, частота дискретизации 1000 Гц) проводили с помощью системы Neuvo SynAmps2 (Compumedics, Charlotte, США) всем пациентам за 3–5 дней до операции и в конце проведения когнитивного тренинга в основной группе и на 8–11-е сут – группе сравнения. Пациент находился в положении сидя с закрытыми глазами в специальном изолированном от света и звука помещении. Фиксацию электродов осуществляли согласно международной системе “10–10%” с использованием 64-канальной шапочки с Ag/AgCl электродами (QuikCap; Neurosoft, США). Электрод-референт был прикреплен к кончику носа, а заземляющий электрод – в центре лба. Электродное сопротивление поддерживали менее <5–10 кОм. Обработку результатов ЭЭГ-записи выполняли автоматически в программе “Scan 4.5” (Compumedics, Charlotte, США) с поиском, удалением артефактов и отбором 30 безартефактных эпох. Полученные показатели усредняли для частотной полосы 4–30 Гц. В настоящем исследовании проанализировали θ1 (4–6 Гц)- и θ2 (6–8 Гц)-диапазоны ЭЭГ с учетом данных предыдущих исследований, в которых была показана диагностическая значимость изменений низкочастотных ритмов для выявления послеоперационного ишемического поражения головного мозга [16].
Результаты исследования были статистически обработаны с помощью программы STATISTICA 10.0 (StatSoft, США). Показатели ЭЭГ нормализовали путем логарифмической трансформации и анализировали с помощью дисперсионного анализа ANOVA с коррекцией статистической значимости методом Гинхауза–Гейссера, анализ взаимодействий проводили с помощью плановых контрастов. Данные на рисунках представлены в виде среднего арифметического и среднеквадратического отклонения. Клинико-анамнестические показатели сравнивали с использованием непараметрического критерия Манна–Уитни, они представлены в табл. 1 и 2 в виде медианы, 25 и 75 квартилей.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ И ИХ ОБСУЖДЕНИЕ
Послеоперационный период коронарного шунтирования не сопровождался неблагоприятными событиями, такими как нарушения мозгового кровообращения, нарушения ритма сердца, инфаркт, повторные вмешательства и летальные исходы. Одновременное выполнение любого из двух вариантов моторной задачи и когнитивных компонентов показало приемлемую субъективную трудность для кардиохирургических пациентов.
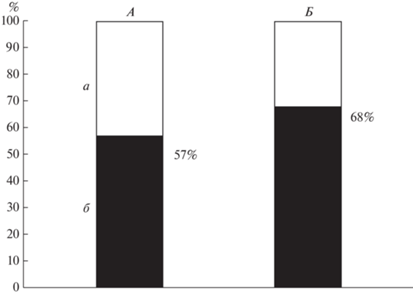
По данным расширенного нейропсихологического тестирования на 2–3-и сут после КШ у всех пациентов была установлена ПОКД (100% случаев). Обнаружено, что на 8–11-е сутки после КШ частота ПОКД под влиянием тренинга снижается до 57%, а у пациентов, не проходивших тренинг, уменьшается до 68%, но достоверных различий по этим данным не получено (рис. 2).
Рис. 2.
Частота развития послеоперационной когнитивной дисфункции (ПОКД) у пациентов с когнитивным тренингом или без него после операции. А – пациенты с когнитивным тренингом, Б – пациенты без когнитивного тренинга, а – пациенты с ПОКД, б – пациенты без ПОКД.
С помощью дисперсионного анализа (ANOVA) проведен анализ суммарных показателей мощности ЭЭГ с выделением следующих меж-субъектных факторов ГРУППА (наличие/отсутствие когнитивного тренинга) × РАННЯЯ ПОКД (наличие, отсутствие) и внутри-субъектных факторов ВРЕМЯ ОБСЛЕДОВАНИЯ (до и после КШ) × × ЛАТЕРАЛЬНОСТЬ (правое, левое полушарие), отдельно для каждого изучаемого диапазона ЭЭГ.
Статистически значимое взаимодействие факторов РАННЯЯ ПОКД × ВРЕМЯ ОБСЛЕДОВАНИЯ было обнаружено в θ1-диапазоне (F (1.92) = = 6.480, p = 0.01). Установлено, что пациенты с ПОКД демонстрировали увеличение суммарной мощности биопотенциалов θ1-ритма по сравнению с исходным уровнем (рис. 3).
Рис. 3.
Показатели мощности биопотенциалов θ1-ритма, в зависимости от наличия послеоперационной когнитивной дисфункции (ПОКД), до и после операции. Сплошная линия – группа пациентов без ПОКД, прерывистая – с ПОКД; * – различия послеоперационных показателей по сравнению с исходными со статистической значимостью p < 0.05.

Патологический “сдвиг” ритмической активности мозга в сторону медленных волн наблюдается при когнитивных дефицитах различной природы и, предположительно, связан с процессами перевозбуждения в миндально-гиппокампальном комплексе и дестабилизации корково-подкорковых нейронных взаимодействий [17].
На рис. 4 представлены спектрограммы ЭЭГ-активности у двух групп пациентов с ПОКД. Можно отметить, что у пациентов группы тренинга перед операцией наблюдается диффузное распределение θ1-активности в париетальных, окципитальных и фронтальных отделах, преимущественно левого полушария. В то время как у пациентов, не проходивших послеоперационный когнитивный тренинг, эти изменения более локальны. В послеоперационном периоде КШ, на 7–10-е сут, у пациентов с тренингом наблюдается уменьшение θ1-активности, тогда как в группе без тренинга – ее увеличение.
Рис. 4.
Спектрограммы θ1-ритма пациентов с послеоперационной когнитивной дисфункцией (ПОКД) с когнитивным тренингом и без него до и после операции. А – пациенты без когнитивного тренинга, Б – пациенты с когнитивным тренингом, а – до операции, б – после операции.

Статистически значимые изменения θ1-ритма обнаружены в левой париетальной области мозга, взаимодействие факторов ГРУППА × РАННЯЯ ПОКД × ВРЕМЯ ОБСЛЕДОВАНИЯ × ЛАТЕРАЛЬНОСТЬ (F (1.92) = 9.554, p = 0.002) (рис. 5). Установлено, что пациенты без ПОКД, прошедшие тренинг, демонстрируют снижение мощности θ1-ритма на 7–10-е сут после операции по сравнению с исходными показателями (p = 0.002), когда у всех пациентов с ПОКД показатели возросли по сравнению с дооперационными данными.
Рис. 5.
Показатели мощности θ1-ритма в левых теменных областях головного мозга у пациентов, прошедших когнитивный тренинг или без него до и после операции. Обозначения см. рис. 4.

Выявленные изменения θ-активности могут свидетельствовать о региональных нарушениях перфузии в послеоперационном периоде у пациентов с ПОКД. Проведенный курс когнитивного тренинга позволил уменьшить проявления ишемического повреждения коры головного мозга, связанного с операцией с применением ИК, однако этот эффект носит ограниченный характер. Выдвинутая ранее гипотеза о возможных ишемических изменениях во фронтальных и париетальных областях головного мозга, связанных с комплексом периоперационных факторов у кардиохирургических пациентов [18–20], подтвердилась лишь частично изменениями в левом париетальном регионе коры. Данные, представленные в метаанализе S. Ghai et al. [21], указывают на усиление церебральной гемодинамики в дорсолатеральной префронтальной и париетальной коре при выполнении когнитивно-моторных задач и связывают этот эффект с их лучшей производительностью. Активность вышеупомянутых областей головного мозга связана с функциями внимания, рабочей памяти и когнитивной гибкости, а также регулирует двигательные акты. В то же время выполнение двух задач не зависит исключительно от одной префронтальной или париетальной области, а скорее включает взаимодействие различных специализированных подсистем головного мозга в процессе обработки информации [22]. Поскольку старение и цереброваскулярные нарушения связаны со снижением скорости обработки получаемой информации, выполнение двойных задач от кардиохирургических пациентов требует бóльшую вовлеченность мозговых ресурсов, следовательно, необходимы такие когнитивные задачи, которые позволяют избежать развития процессов интерференции, когда одна задача ухудшает выполнение другой, но при этом имеют определенную субъективную трудность и могут заинтересовать пациента во время выполнения тренинга [19, 23].
Стоит также отметить, что при проведении курса когнитивного тренинга снижение частоты ПОКД увеличилось только на 11% по сравнению с его отсутствием (57 vs 68%). Возможной причиной ограниченной эффективности выбранного курса когнитивной реабилитации может быть его небольшая продолжительность (в среднем 5–6 тренировок). Также необходимо учитывать, что послеоперационное состояние пациентов (вегетативные нарушения, болевой синдром, послеоперационное лекарственное сопровождение) ограничивали интенсивность тренировок.
ЗАКЛЮЧЕНИЕ
Краткосрочный курс реабилитации с применением метода двойных задач оказал ограниченное положительное влияние на нейрофизиологические показатели пациентов после операции КШ. Положительные эффекты включают уменьшение количества пациентов с ПОКД и менее выраженную корковую дисфункцию. Метод двойных задач может быть использован как эффективный реабилитационный подход для этой категории пациентов при дополнительном рассмотрении продолжительности и интенсивности тренировочного воздействия. Необходимы дальнейшие исследования для определения наилучших параметров когнитивного тренинга для кардиохирургических пациентов.
Этические нормы. Все исследования проведены в соответствии с принципами биомедицинской этики, сформулированными в Хельсинкской декларации 1964 г. и ее последующих обновлениях, и одобрены локальным биоэтическим комитетом НИИ “Комплексных проблем сердечно-сосудистых заболеваний” (Кемерово).
Информированное согласие. Каждый участник исследования представил добровольное письменное информированное согласие, подписанное им после разъяснения ему потенциальных рисков и преимуществ, а также характера предстоящего исследования.
Финансирование работы. Исследование выполнено при финансовой поддержке министерства науки и образования РФ (фундаментальная тема № 122012000364-5 от 20.01.2022). Спонсор не участвовал в разработке дизайна исследования, сборе, анализе, интерпретации данных, написании этой статьи или решении представить ее для публикации.
Конфликт интересов. Авторы декларируют отсутствие явных и потенциальных конфликтов интересов, связанных с публикацией данной статьи.
Вклад авторов в публикацию. Д.С. Куприянова – написание статьи, cбор и обработка материала, статистическая обработка. И.В. Тарасова – концепция и дизайн исследования, статистическая обработка, написание и редактирование статьи. О.А. Трубникова – концепция и дизайн исследования, редактирование текста статьи, утверждение окончательной версии публикации. А.С. Соснина – cбор и обработка материала. И.Н. Кухарева – cбор и обработка материала. И.Д. Сырова – cбор и обработка материала. О.Л. Барбараш – критический анализ интеллектуального содержимого, утверждение окончательной версии публикации.
Список литературы
Talamonti D., Vincent T., Fraser S. et al. The Benefits of Physical Activity in Individuals with Cardiovascular Risk Factors: A Longitudinal Investigation Using fNIRS and Dual-Task Walking // J. Clin. Med. 2021. V. 10. № 4. P. 579.
De Vito A., Bernstein J., Weitzner D. et al. The Effects of Cardiovascular Risk Factors on Repeatable Battery for the Assessment of Neuropsychological Status (RBANS) Performance in Cognitively Healthy Older Adults // Arch. Clin. Neuropsychol. 2021. V. 36. № 2. P. 165.
Zhao E., Lowres N., Woolaston A. et al. Prevalence and patterns of cognitive impairment in acute coronary syndrome patients: A systematic review // Eur. J. Prev. Cardiol. 2020. V. 27. № 3. P. 284.
Трубникова О.А., Тарасова И.В., Барбараш О.Л. Нейрофизиологические механизмы и перспективы использования двойных задач в восстановлении когнитивных функций у кардиохирургических пациентов // Фундаментальная и клиническая медицина. 2020. Т. 5. № 2. С. 101. Trubnikova O.A., Tarasova I.V., Barbarash O.L. [Neurophysiological mechanisms and perspective for the use of dual tasks inrecovering cognitive function after cardiac surgery] // Fundamental and Clinical Medicine. 2020. V. 5. № 2. P. 101.
Tang V.L., Jing B., Boscardin J. et al. Association of Functional, Cognitive, and Psychological Measures With 1-Year Mortality in Patients Undergoing Major Surgery // JAMA Surg. 2020. V. 155. № 5. P. 412.
Relander K., Hietanen M., Rantanen K. et al. Postoperative cognitive change after cardiac surgery predicts long-term cognitive outcome // Brain Behav. 2020. V. 10. № 9. P. e01750.
Ludyga S., Gerber M., Pühse U. et al. Systematic review and meta-analysis investigating moderators of long-term effects of exercise on cognition in healthy individuals // Nat. Hum. Behav. 2020. V. 4. № 6. P. 603.
Greaves D., Psaltis P., Davis D. et al. Risk Factors for Delirium and Cognitive Decline Following Coronary Artery Bypass Grafting Surgery: A Systematic Review and Meta-Analysis // J. Am. Heart Assoc. 2020. V. 9. № 22. P. e017275.
Bech S.R., Kjeldgaard-Man L., Sirbaugh M.C. et al. Attentional Capacity during Dual-task Balance Performance Deteriorates with Age before the Sixties // Exp. Aging Res. 2021. V. 48. № 1. P. 86.
Akin H., Senel A., Taskiran H., Kaya Mutlu E. Do motor-cognitive and motor-motor dual task training effect differently balance performance in older adults? // Eur. Geriatr. Med. 2021. V. 12. № 2. P. 371.
Gallou-Guyot M., Mandigout S., Combourieu-Donnezan L. et al. Cognitive and physical impact of cognitive-motor dual-task training in cognitively impaired older adults: An overview // Neurophysiol. Clin. 2020. V. 50. № 6. P. 441.
Cisneros E., Beauséjour V., de Guise E. et al. The impact of multimodal cognitive rehabilitation on executive functions in older adults with traumatic brain injury // Ann. Phys. Rehabil. Med. 2021. V. 64. № 5. P. 101559.
Sarasso E., Agosta F., Piramide N. et al. Brain activity of the emotional circuit in Parkinson’s disease patients with freezing of gait // Neuroimage Clin. 2021. V. 30. P. 102649.
Johansson H., Ekman U., Rennie L. et al. Dual-Task Effects During a Motor-Cognitive Task in Parkinson’s Disease: Patterns of Prioritization and the Influence of Cognitive Status // Neurorehabil. Neural Repair. 2021. V. 35. № 4. P. 356.
Тарасова И.В., Трубникова О.А., Кухарева И.Н., Барбараш О.Л. Методические подходы к диагностике послеоперационной когнитивной дисфункции в кардиохирургической клинике // Комплексные проблемы сердечно-сосудистых заболеваний. 2015. № 4. С. 73. Tarasova I.V., Trubnikova O.A., Kukhareva I.N., Barbarash O.L. [Methodological approaches to the diagnosis of postoperative cognitive dysfunction in cardiac surgery clinic] // Complex Issues of Cardiovascular Diseases. 2015. № 4. P. 73.
Тарасова И.В., Вольф Н.В., Куприянова Д.С и др. Изменения вызванной синхронизации/десинхронизации электрической активности коры мозга у кардиохирургических пациентов с послеоперационной когнитивной дисфункцией // Сибирский научный медицинский журн. 2021. Т. 41. № 2. С. 12. Tarasova I.V., Volf N.V., Kupriyanova D.S. et al. [Сhanges in event-related synchronization/desynchronization of brain electric activity in cardiosurgical patients with postoperative cognitive dysfunction] // Siberian Scientific Med. J. 2021. Т. 41. № 2. P. 12.
Schumacher J., Taylor J.P., Hamilton C.A. et al. Quantitative EEG as a biomarker in mild cognitive impairment with Lewy bodies // Alzheimers Res. Ther. 2020. V. 12. № 1. P. 82.
Benwell C.S.Y., Davila-Pérez P., Fried P.J. et al. EEG spectral power abnormalities and their relationship with cognitive dysfunction in patients with Alzheimer’s disease and type 2 diabetes // Neurobiol. Aging. 2020. V. 85. P. 83.
Жаворонкова Л.А., Шевцова Т.П., Морареску С.И. и др. Интракортикальные связи при выполнении двойных задач – моторных и счетно-логических или пространственно-образных // Физиология человека. 2019. Т. 45. № 2. С. 16. Zhavoronkova L.A., Shevtsova T.P., Moraresku S.I. et al. Intracortical connections in dual tasks including motor and computing – logical or spatial–visual components // Human Physiology. 2019. V. 45. № 2. P. 126.
Fallahtafti F., Boron J.B., Venema D.M. et al. Task specificity impacts dual-task interference in older adults // Aging Clin. Exp. Res. 2021. V. 33. № 3. P. 581.
Ghai S., Ghai I., Effenberg A.O. Effects of dual tasks and dual-task training on postural stability: a systematic review and meta-analysis // Clin. Interv. Aging. 2017. V. 12. P. 557.
Ljubisavljevic M.R., Oommen J., Filipovic S. et al. Effects of tDCS of Dorsolateral Prefrontal Cortex on Dual-Task Performance Involving Manual Dexterity and Cognitive Task in Healthy Older Adults // Front. Aging Neurosci. 2019. V. 11. P. 144.
Li K.Z.H., Bherer L., Mirelman A. et al. Cognitive Involvement in Balance, Gait and Dual-Tasking in Aging: A Focused Review From a Neuroscience of Aging Perspective // Front. Neurol. 2018. V. 9. P. 913.
Дополнительные материалы отсутствуют.
Инструменты
Физиология человека



