Доклады Российской академии наук. Физика, технические науки, 2020, T. 490, № 1, стр. 24-28
Условия возникновения ударной волны при кавитации в углеродсодержащих растворах
А. Ю. Днестровский 1, *, С. А. Воропаев 1, Н. В. Душенко 1, С. Г. Наймушин 1, академик РАН Э. М. Галимов 1
1 Институт геохимии и аналитической химии
им. В.И. Вернадского Российской академии наук
Москва, Россия
* E-mail: dnestrov0@gmail.com
Поступила в редакцию 25.10.2019
После доработки 25.10.2019
Принята к публикации 28.11.2019
Аннотация
Проведено численное исследование появления ударной волны при схлопывании пузырька в углеродсодержащем водном растворе. Получены условия появления ударной волны в зависимости от растворенного вещества, концентрации раствора и его температуры. Работы проводятся в рамках разработки метода получения алмазов при кавитации в углеродсодержащих жидкостях.
ВВЕДЕНИЕ
Кавитационный способ синтеза, предполагающий использование углеродсодержащих органических жидкостей, открывает новые возможности управления размером и внутренней структурой получаемых наночастиц углерода за счет вариаций молекулярной структуры исходного соединения. Впервые возможность формирования зародышей алмаза во флюиде при возникновении кавитации в природном процессе образования кимберлитовой трубки была показана в пионерской работе Э.М. Галимова [1]. Позже алмазная кристаллическая решетка наночастиц углерода, получаемых при гидродинамической кавитации, была подтверждена в экспериментах с чистым бензолом [2]. В последующих работах было указано на то, что на их электронной дифрактограмме присутствуют запрещенные в алмазной кристаллической структуре линии (200) и (220) [3]. Была принята гипотеза о существовании внешней оболочки с гранецентрированной кристаллической решеткой (ГЦК) с параметром решетки, совпадающим с параметром решетки алмаза a = 3.57 Å. Возник вопрос, является ли наличие такой “шубы” недостатками условий проводимых экспериментов или характерной особенностью внутренних процессов кавитационного синтеза.
В 2016 г. в ГЕОХИ РАН была создана новая экспериментальная установка кавитационного синтеза наноалмазов (УКНА) непрерывного цикла [4, 5], были представлены результаты серии экспериментов с 3%-ным раствором изопропилового спирта (ИПС) в воде [6], которые показали наличие алмазной структуры в некоторых полученных наночастицах при кавитации. В работе [7] были проведены расчеты сжатия пузырька в бензоле и на основе фазовой диаграммы углерода исследованы необходимые условия синтеза наноалмаза. Было обнаружено, что для зарождения наноалмаза при сжатии должна возникать ударная волна. В работах [8–10] были исследованы условия и предложен упрощенный критерий возникновения ударной волны при сжатии пузырька в зависимости от температуры жидкости, внешнего давления и параметров вещества. В данной работе на основе критерия [9] проводится анализ условий появления ударной волны в водном растворе различных углеродсодержащих веществ: этиловый спирт, изопропиловый спирт и ацетонитрил. Показано, что в ацетонитриле условия формирования ударной волны наименее жесткие, причем давление и плотность паров углерода в кавитационном пузырьке могут достигать значений из области формирования алмаза.
ПОСТАНОВКА ЗАДАЧИ
Мы рассматриваем сжатие одиночного пузырька, содержащего смесь водяного пара и пара одного из растворенных веществ: этилового спирта, изопропилового спирта или ацетонитрила. Данные по этим веществам приведены в табл. 1. Начальное состояние определяется радиусом пузырька и составом пара, в котором концентрация растворенного вещества превышает концентрацию в жидкости за счет большей летучести. Для смеси полное давление в начальный момент p0 равно сумме давлений компонентов пара, а с другой стороны, согласно закону Рауля, оно равно сумме давлений насыщенных паров с соответствующими весами:
(1)
$\begin{gathered} {{p}_{0}} = ({{\nu }_{1}} + {{\nu }_{2}})\frac{{{{R}_{u}}{{T}_{0}}}}{{{{V}_{0}}}}, \hfill \\ {{p}_{0}} = \frac{{{{\nu }_{1}}}}{{{{\nu }_{1}} + {{\nu }_{2}}}}{{p}_{{s1}}}({{t}_{0}}) + \frac{{{{\nu }_{2}}}}{{{{\nu }_{1}} + {{\nu }_{2}}}}{{p}_{{s2}}}({{t}_{0}}), \hfill \\ \end{gathered} $Таблица 1
| pcr, бар | Тcr, K | ρcr, кг/м3 | М, г/моль | γ | ρl, кг/м3 | сl, м/с | |
|---|---|---|---|---|---|---|---|
| Вода | 221.2 | 22374.12 | 2317.8 | 18 | 221.325 | 2998.2 | 1497 |
| Этанол | 63 | 241 | 275 | 46 | 221.125 | 789 | 1177 |
| Изопропил | 49 | 235 | 271 | 60 | 221.103 | 785 | 1247 |
| Ацетонитрил | 247.7 | 22272.4 | 240 | 22241.05 | 1.1 | 2787.5 | 1290 |
| Декан | 21 | 618 | 228 | 22142.28 | 1.1 | 730 | 1253 |
| Додекан | 18 | 658 | 226 | 22170.34 | 1.1 | 749 | 1298 |
| Тетрадекан | 16 | 693 | 222 | 22198.38 | 221.026 | 763 | 1331 |
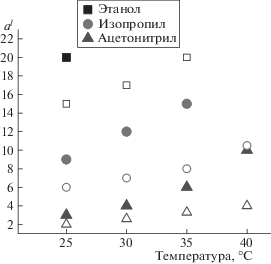
Для определения концентрации пара растворенного вещества, т.е. величины ν2/ν1, проведено экспериментальное исследование растворов с помощью газового хроматографа КристалЛюкс-2000 модуль ПИД-ДТП, колонка HP-PLOTQ 30 м 0.53 мм. Результаты для этилового спирта при различных температурах жидкости в сравнении с табличными данными показаны на рис. 1 в виде зависимостей относительного коэффициента испарения спирта Avap/al от его концентрации в воде al, где Avap – концентрация спирта в паре. Из рис. 1 видно, что полученные зависимости занижают долю спирта по сравнению с табличными значениями [11], что происходит, скорее всего, из-за наличия воздуха в пробах хроматографа. Таким образом, при использовании данных хроматографа доля растворенного вещества в паре оказывается несколько заниженной.
Рис. 1.
Зависимость относительного коэффициента испарения этилового спирта от его концентрации в воде при различных температурах раствора. Измерения хроматографа (сплошные линии) и табличные данные [11] (пунктир).
В расчетах используется математическая модель, в которой жидкость предполагается слабосжимаемой, пар с однородным распределением термодинамических параметров – испытывающий адиабатическое сжатие. Изменение радиуса пузырька R описывается уравнением Рэлея–Плессета
(2)
$\begin{gathered} \left( {1 - \frac{{{{{\dot {R}}}_{i}}}}{{{{c}_{l}}}}} \right)R\ddot {R} + \frac{3}{2}\left( {1 - \frac{{\dot {R}}}{{3{{c}_{l}}}}} \right){{{\dot {R}}}^{2}} = \\ = \left( {1 - \frac{{\dot {R}}}{{{{c}_{l}}}}} \right)\frac{{{{p}_{b}} - \Delta P}}{{{{\rho }_{l}}}} + \frac{R}{{{{c}_{l}}}}\frac{{{{{\dot {p}}}_{b}} - \Delta \dot {P}}}{{{{\rho }_{l}}}}, \\ \end{gathered} $Давление в смеси пара описывается модифицированным уравнением состояния Ван-дер-Ваальса [9] для каждого компонента с использованием данных, приведенных в табл. 1.
Расчеты проводятся согласно методике [9, 10], критерием возникновения ударной волны в пузырьке является выполнение условия
где Rsh – расстояние от межфазной границы до места возникновения в пузырьке ударной волны – точке пересечения характеристик, описывающих распространение возмущения от поверхности пузырька. Если ΔRsh < R, ударная волна успевает возникнуть в пузырьке в ходе его коллапса. В противном случае образования ударной волны не будет.Величина ΔRsh определяется из выражения
(4)
$\Delta {{R}_{{{\text{sh}}}}} \approx - \left( {1 - \frac{{\dot {R}}}{c}} \right)\frac{{{{c}^{2}}}}{{k\ddot {R}}},\quad k = 1 + \frac{{\rho c{\kern 1pt} '(\rho )}}{c},$РЕЗУЛЬТАТЫ
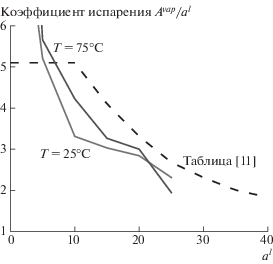
На рис. 2 показаны результаты по решению задачи схлопывания пузырька в чистых жидкостях согласно [10] при температуре 20°С и внешнем давлении 10 бар. Как было показано в [10], условие (3) перестает выполняться при уменьшении внешнего давления или увеличении температуры жидкости. Для веществ с более высоким молекулярным весом легче обеспечить выполнение условия (3), так как параметр $\frac{{\Delta {{R}_{{{\text{sh}}}}}}}{R}$ у них ниже. Необходимо отметить, что так как при пересечении параметром $\frac{{\Delta {{R}_{{{\text{sh}}}}}}}{R}$ единицы формируется ударная волна, то дальнейший расчет по нульмерной модели, не включающей в рассмотрение фактор ударной волны, не имеет смысла.
Рис. 2.
Параметр $\frac{{\Delta {{R}_{{{\text{sh}}}}}}}{R}$ в зависимости от размера пузырька в ходе коллапса в чистых углеводородных жидкостях. Ударная волна возникает при $\frac{{\Delta {{R}_{{{\text{sh}}}}}}}{R}$ < 1.
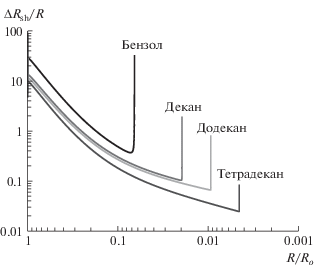
Проведены расчеты для трех растворенных в воде веществ при различной концентрации al, различной температуре жидкости и внешнего давления. На рис. 3 показано изменение параметра $\frac{{\Delta {{R}_{{{\text{sh}}}}}}}{R}$ в ходе сжатия пузырька в зависимости от его радиуса. Видно, что этот параметр принимает наименьшее значение незадолго до остановки сжатия, что происходит в момент максимального ускорения стенки пузырька в сторону сжатия, т.е. величины –$\ddot {R}$. При внешнем давлении ΔP = 10 бар система достигает пограничного режима $\frac{{\Delta {{R}_{{{\text{sh}}}}}}}{R}$ ≈ 1, а при увеличении внешнего давления минимальное значение параметра $\frac{{\Delta {{R}_{{{\text{sh}}}}}}}{R}$ становится меньше единицы, так что при ΔP = 15 бар в 9%-м растворе ИПС в воде формируется ударная волна.
Рис. 3.
Параметр $\frac{{\Delta {{R}_{{{\text{sh}}}}}}}{R}$ в зависимости от размера пузырька в ходе коллапса для случая 9%-го раствора изопропилового спирта (ИПС) в воде при двух различных внешних давлениях.
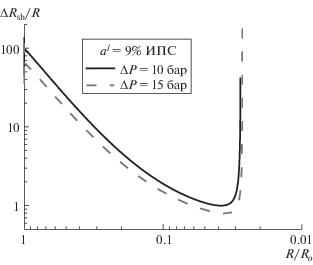
Результаты расчета условия образования ударной волны по критерию (3) представлены на рис. 4 для трех растворенных в воде веществ. Ударная волна возникает при превышении показанной на рис. 4 концентрации вещества. Повышение температуры жидкости вследствие увеличения начального давления пара р0 приводит к необходимости роста концентрации раствора. При повышении внешнего давления ΔP требуемая концентрация падает. Самая слабая концентрация раствора, которая обеспечивает формирование ударной волны, достигается в ацетонитриле.
ВЫВОДЫ
Проведенные исследования физико-химических свойств испарения растворов ряда углеводородных жидкостей (ИПС, этанол и ацетонитрил) позволили определить минимальные концентрации для возникновения ударной волны при схлопывании кавитационных пузырьков. Это важный результат для оптимизации экспериментальных работ по синтезу наночастиц углерода различных кристаллических форм, вплоть до алмаза. Показаны преимущества раствора ацетонитрила в воде перед другими, использовавшимися ранее жидкостями. Отметим также, что при кавитации паровой пузырек не содержит воздуха, поэтому концентрация растворенного вещества в пузырьке должна быть выше, чем показывают измерения хроматографа, которые проводились на воздухе и которые в то же время использовались при моделировании смеси. Поэтому экспериментально определенная относительная концентрация растворенного вещества в пузырьке является заниженной, а результаты по необходимой для образования ударной волны концентрации, приведенные на рис. 3, – завышенными.
Список литературы
Galimov E.M. // Nature. 1973. V. 243. P. 389–391.
Галимов Э.М., Кудин А.М., Скоробогатский В.Н., Плотниченко В.Г., Бондарев О.Л., Зарубин Б.Г., Страздовский В.В., Аронин А.С., Фисенко А.В., Быков И.В., Баринов А.Ю. // ДАН. 2004. Т. 395. № 2. С. 187–191.
Воропаев С.А., Шкинев В.М., Днестровский А.Ю., Пономарева Е.А., Аронин А.С., Бондарев О.Л., Стра-здовский В.В., Скоробогатский В.Н., Елисеев А.А., Спиваков Б.Я., Галимов Э.М. // ДАН. 2012. Т. 446. № 4. С. 388–391.
Душенко Н.В., Воропаев С.А., Пономарева Е.А., Днестровский А.Ю., Шкинев В.М., Аронин А.С., Гали-мов Э.М. // Изв. вузов. Химия и хим. технология. 2016. Т. 59. № 9. С. 80–85.
Днестровский А.Ю., Душенко Н.В., Воропаев С.А. // Инженерно-физ. журн. 2018. Т. 91. № 6. С. 1599–1604.
Душенко Н.В., Днестровский А.Ю., Воропаев С.А. / Всероссийский ежегодный семинар по экспериментальной минералогии, петрологии, геохимии. Труды. 2017. С. 7–10.
Днестровский А.Ю., Воропаев С. А., Забродина Е.А. Моделирование сжатия кавитационного пузырька в бензоле // ДАН. 2016. Т. 469. № 5.
Нигматулин Р.И., Аганин А.А., Топорков Д.Ю., Ильгамов М.А. // ДАН. 2014. Т. 458. № 3. С. 282–286.
Khalitova T.F., Toporkov D.Yu. IOP Conf. Series: Materials Science and Engineering. 2016. V. 158. № 1. Art. 012052. P. 1–5.
Аганин А.А., Топорков Д.Ю. // Учен зап. Казан. ун-та. Сер. Физ.-матем. науки. 2017. Т. 159. Кн. 3. С. 271–281.
Стабников В.Н. Перегонка и ректификация этилового спирта. М.: Пищевая промышленность, 1969. 456 с.
Дополнительные материалы отсутствуют.
Инструменты
Доклады Российской академии наук. Физика, технические науки