Доклады Российской академии наук. Науки о Земле, 2022, T. 503, № 2, стр. 105-112
Растворение перидотита в богатом летучими карбонатном расплаве как механизм образования кимберлитоподобных расплавов (по экспериментальным данным)
А. Г. Сокол 1, *, А. Н. Крук 1, Э. С. Персиков 2
1 Институт геологии и минералогии Сибирского отделения Российской академии наук
Новосибирск, Россия
2 Институт экспериментальной минералогии Российской академии наук
Черноголовка, Россия
* E-mail: sokola@igm.nsc.ru
Поступила в редакцию 25.11.2021
После доработки 16.12.2021
Принята к публикации 20.12.2021
- EDN: MXOTCS
- DOI: 10.31857/S2686739722040181
Аннотация
В экспериментах при 3.0–6.3 ГПа и 1200–1350°С установлено, что при PT-параметрах, близких к условиям в поднимающейся кимберлитовой магме, богатый калием и летучими карбонатный расплав способен эффективно растворять все количество ксеногенного перидотитового материала, которое потенциально может транспортировать. В результате этого процесса расплав обогащается SiO2 (до 30 мас. %) и трансформируется из карбонатного в кимберлитоподобный. В изученном диапазоне условий из-за высокой растворимости CO2 в расплаве и появления магнезита равновесной флюидной фазы в системе не образуется. Реализованное в экспериментах реакционное взаимодействие может выступать наиболее важным фактором начального этапа эволюции магмы. Выполненные в работе расчеты показывают, что даже после растворения 30–50 мас. % лерцолита богатый летучими карбонатно-силикатный расплав имеет высокую степень деполимеризации (отношение числа немостиковых атомов кислорода к числу тетраэдрически координированных ионов (NBO/T) × 100 от 250 до 390), остается маловязким (0.3–32.6 Па с) и способным к быстрому движению к поверхности. Полученные данные свидетельствуют о том, что несмесимость между богатыми калием карбонатно-силикатным и существенно силикатным расплавами возникает лишь при 5.5 ГПа и 1350°С и, по-видимому, оказывает незначительное влияние на эволюцию магмы.
ВВЕДЕНИЕ
Кимберлитовая магма на сегодня рассматривается как непрерывно эволюционирующая гетерофазная среда, состоящая из расплава, флюида и твердых фаз, в том числе алмаза [1–3]. Уникальной особенностью магмы является ее исключительно быстрый подъем с глубин субконтинентальной литосферной мантии к поверхности. Изменение состава магмы вследствие реакционного взаимодействия с транспортируемым ксеногенным материалом традиционно считается одним из наиболее важных факторов ее эволюции [1–5]. Другими значимыми факторами эволюции могли быть процессы кристаллизации в магме силикатных и/или оксидных минералов, а также разложение карбонатов с выделением CO2-флюида [6, 7].
Недавно в работе [8] было показано, что в расплавах модельных систем, содержащих карбонат натрия (80 мас. %) и добавки Opx, Ol или Opx-Cpx, при давлении 2–4 ГПа и температуре 1140–1000°С происходит расслоение на карбонатный и карбонатно-силикатный расплавы – две несмешивающихся жидкости, формирующие в экспериментальных образцах эмульсию. При растворении ортопироксена в расплаве доломита появления эмульсии несмешивающихся расплавов не наблюдалось [9]. Таким образом, расслоение кимберлитовой магмы на два несмешивающихся расплава потенциально может быть еще одним важным фактором ее эволюции. Однако для адекватной оценки этого фактора необходимо определение возможности расслоения в экспериментальных системах, воспроизводящих все потенциальные составы магм.
Начальный этап генерации кимберлитовой магмы связывают с метасоматозом перидотитов источника карбонатными расплавами, генерированными в зонах субдукции [10]. Известно, что плавление карбонатсодержащих пелитов в зонах субдукции при Р < 10 ГПа приводит к образованию богатого калием карбонатного расплава [11] – потенциального прекурсора кимберлитовой магмы. Его участие в генерации кимберлитов подтверждает состав включений в волокнистых алмазах [12]. Первые сведения о возможности расслоения богатого калием и летучими кимберлитоподобного расплава на карбонатно-силикатный и существенно силикатный расплавы при 5.5 ГПа и 1350°С появились в работе [13].
В этой работе экспериментально изучено реакционное взаимодействие богатого летучими и калием карбонатного расплава с гранатовым лерцолитом при 3.0 и 6.3 ГПа и 1200–1350°С. Используя новые и ранее опубликованные данные, полученные нами при 5.5 ГПа и тех же температурах [13], мы впервые для диапазона давлений от 3.0 до 6.3 ГПа экспериментально промоделировали механизм превращения карбонатного расплава в кимберлитоподобный. Для образованных за счет растворения гранатового лерцолита расплавов на основе расчетов в работе оценены количество и формы растворения летучих, вязкость и степень их деполимеризации.
2. МЕТОДИКА
В качестве модели субдукционного агента использовали смесь GS из химически чистых карбонатов и оксидов (SiO2–0.62; TiO2–0.02; Al2O3–0.73; FeO–3.97; MgO–4.77; CaO–15.67; Na2O–0.18; K2O–31.3; CO2–42.74 мас. %). Эта смесь воспроизводила близсолидусный карбонатный расплав, полученный при 8 ГПа и 1100°С при плавлении карбонатизированного пелита [11]. В качестве гранатового лерцолита (Lc) использовали порошок, приготовленный из ксенолита гранатового лерцолита Уд-05-05 из кимберлитовой трубки Удачная-Восточная, Якутия. Ксенолит состоит из Ol–69.3; Opx–8.1; Cpx–13.2; Grt–9.4 мас. %. Использованная система Lc-GS без добавки летучих имела состав: SiO2–29.18; TiO2–0.09; Al2O3–1.75; Cr2O3–0.46; FeO–8.81; MnO–0.07; NiO–0.17; MgO–27.72; CaO–6.99; Na2O–0.21; K2O–10.46; CO2–14.1 (мас. %). H2O и молекулярный CO2 дополнительно вводились в систему в виде безводной щавелевой кислоты (H2C2O4, далее OA). При РТ-параметрах экспериментов она разлагалась по реакции 2H2C2O4 → → 3CO2 + 2H2O + C0. Смесь порошков Lc (49 мас. %), GS (21 мас. %) и OA (30 мас. %) помещали в Pt-ампулы с Re-футеровкой или ампулы из Au. Ампулы герметично заваривали импульсной дуговой сваркой. Количество введенной таким образом в систему воды соответствовало ее оценочным концентрациям в кимберлитовой магме [2], а количество добавленного молекулярного CO2 должно было обеспечить насыщение расплава [13].
Эксперименты были проведены на многопуансонном аппарате типа “БАРС”. Точность контроля давления и температуры составляла ±0.1 ГПа и ±20°С [14, 15]. Длительность экспериментов от 60 до 150 ч, большая концентрация летучих в системе (табл. 1), гомогенность состава новообразованных фаз, значительный размер твердых фаз, а также наличие на некоторых из них огранки (рис. 1) позволяют сделать вывод о том, что практически все образцы достигали равновесия. В связи с тем, что при разложении щавелевой кислоты выделялось незначительное количество C°, в образцах после экспериментов фиксировалось небольшое количество чешуек графита. Наличие графита, карбонатно-силикатного расплава и, в некоторых случаях, магнезита, обеспечивало контроль фугитивности кислорода в системе вблизи к значениям буфера EMOD. Составы полученных фаз исследованы с использованием сканирующего электронного микроскопа “Tescan” MIRA 3 LMU, оснащенного энергодисперсионным микроанализатором INCA Energy 450 (“Oxford Instruments”), а также микрозонда “Jeol” JXA-8100.
Таблица 1.
Условия экспериментов по исследованию реакционного взаимодействия между лерцолитом (Lc) и обогащенным CO2 и H2O карбонатным расплавом (GS). Состав использованной системы: Lc – 49 мас. %, GS – 21 мас. % и щавелевая кислота (OA) – 30 мас. %
| № эксп. | Ампула | СO2 (OA), мас. % | H2O (OA), мас. % | CO2 total, мас. % | P, ГПа | T, °C | t, ч | Фазовый состав |
|---|---|---|---|---|---|---|---|---|
| 2202_2_4 | Au | 20.5 | 5.9 | 30.6 | 3.0 | 1200 | 150 | Cpx + Opx + Mgs + Lcarb-sil |
| 2225_2_4 | Pt + Re | 20.5 | 5.9 | 29.3 | 3.0 | 1350 | 60 | Lcarb-sil |
| 2200_2_4 | Au | 23.2 | 6.7 | 33.1 | 6.3 | 1200 | 150 | Mgs + Lcarb-sil |
| 2208_2_1 | Pt + Re | 20.5 | 5.9 | 30.6 | 6.3 | 1350 | 60 | Opx + Lcarb-sil |
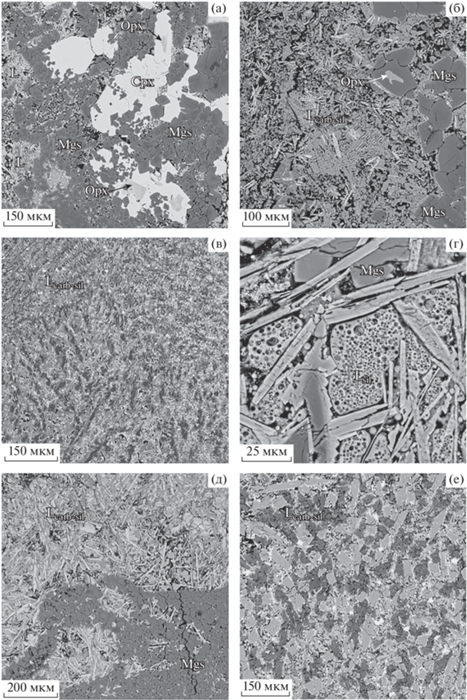
Рис. 1.
РЭМ образцов, полученных в системе Lc–GS–CO2–H2O. а, б – образец № 2202_2_4 (3.0 ГПа и 1200°С) с ксеноморфными кристаллами клинопироксена, содержащими включения ортопироксена, субидиоморфными зернами магнезита и обособлениями закаленного карбонатно-силикатного расплава; в – закаленный карбонатно-силикатный расплав в образце № 2212_2_4 (3.0 ГПа и 1350°С); г – глобули силикатного стекла с пузырьками флюидной фазы в агрегате карбонатных и силикатных закалочных фаз, образец № 707_6_4 (5.5 ГПа и 1350°С) [13]; д – закаленный карбонатно-силикатный расплав и зерна магнезита в образце № 2200_2_4 (6.3 ГПа и 1200°С); е – закаленный карбонатно-силикатный расплав в образце № 2208_2_1 (6.3 ГПа и 1350°С).
В этой работе содержание летучих в расплавах оценено на основании расчета масс-баланса и дефицита суммы химических анализов расплавов. В частности, содержания воды рассчитаны на основе масс-баланса, в предположении ее полного перераспределения в расплавы. Концентрации карбонатного иона CO$_{3}^{{2 - }}$ (табл. 3) оценивали с использованием известной зависимости между SiO2 и CO$_{3}^{{2 - }}$ для карбонатно-силикатных расплавов в системах перидотит–CO2–H2O при мантийных параметрах [16]. Концентрации молекулярного CO2 в расплавах оценены путем вычитания из дефицита суммы химических анализов расплавов содержания в них воды и карбонатного CO$_{3}^{{2 - }}$. Причем эти значения не могли превышать растворимость молекулярного CO2 в карбонатно-силикатных расплавах [13]. Вязкость расплавов рассчитывалась по улучшенной модели прогноза и расчетов вязкости магматических расплавов [17] как функция основных параметров экспериментов. Для оценки степени деполимеризации и особенностей структуры расплавов использовался структурно-химический критерий (степень деполимеризации – 100NBO/T) [18].
Таблица 2.
Условия экспериментов, весовая фракция расплавов в образцах, их состав и расчетное содержание летучих (мас. %)
| 2202_2_4 Lcarb-sil | 2225_2_4 Lcarb-sil | 674_8_3* Lcarb-sil | 707_6_4* Lcarb-sil | 707_6_4* Lsil | 2181_2_1* Lcarb-sil | 2181_2_1* Lsil | 2200_2_4 Lcarb-sil | 2108_2_1 Lcarb-sil | |
|---|---|---|---|---|---|---|---|---|---|
| Р, ГПа | 3.0 | 3.0 | 5.5 | 5.5 | 5.5 | 5.5 | 5.5 | 6.3 | 6.3 |
| T, °C | 1200 | 1350 | 1200 | 1350 | 1350 | 1350 | 1350 | 1200 | 1350 |
| SiO2 | 30.5 | 18.6 | 27.4 | 28.9 | 61.4 | 27.6 | 55.6 | 32.8 | 23.7 |
| TiO2 | 0.2 | 0.2 | 0.1 | 0.1 | 0.0 | 0.0 | 0.0 | 0.1 | 0.0 |
| Al2O3 | 2.5 | 2.6 | 1.9 | 2.1 | 1.1 | 2.4 | 0.8 | 2.9 | 2.1 |
| Cr2O3 | 0.2 | 0.2 | 0.2 | 0.2 | 0.0 | 0.3 | 0.0 | 0.2 | 0.2 |
| FeO | 4.0 | 2.9 | 4.4 | 4.8 | 0.4 | 4.3 | 0.3 | 4.4 | 4.1 |
| MnO | 0.0 | 0.0 | 0.1 | 0.1 | 0.0 | 0.0 | 0.0 | 0.1 | 0.2 |
| MgO | 4.4 | 19.6 | 7.5 | 15.5 | 0.5 | 12.0 | 0.0 | 7.0 | 24.3 |
| CaO | 6.8 | 5.3 | 6.7 | 6.5 | 0.8 | 6.0 | 0.0 | 11.2 | 7.3 |
| Na2O | 0.4 | 0.8 | 0.2 | 0.1 | 0.7 | 0.3 | 0.9 | 0.1 | 0.0 |
| K2O | 10.0 | 9.5 | 9.4 | 6.2 | 15.3 | 6.7 | 23.8 | 8.9 | 8.0 |
| Сумма | 58.9 | 60.0 | 57.9 | 64.5 | 80.2 | 59.5 | 81.5 | 67.9 | 64.4 |
| VL | 0.70 | 0.91 | 0.64 | 0.70 | 0.03 | 0.70 | 0.01 | 0.57 | 0.98 |
| H2Ototal | 5.9 | 5.9 | 6.2 | 5.9 | 5.9 | 5.9 | 5.9 | 6.7 | 5.9 |
| H2OL | 8.4 | 6.5 | 9.8 | 8.4 | 8.4 | 8.4 | 8.4 | 11.8 | 6.0 |
| CO2L | 32.7 | 33.5 | 32.4 | 27.1 | 11.4 | 32.0 | 10.1 | 20.4 | 29.6 |
Примечание: * – по данным работы [13]; VL – весовая фракция расплава в образце.
Таблица 3.
Физико-химические параметры карбонатно-силикатных и силикатных расплавов в системе Lc–GS–CO2–H2O, расчетные значения их вязкости (η), энергии активации вязкого течения (Е) и степени деполимеризации (100NBO/T)
| 2202_2_4 Lcarb-sil | 2225_2_4 Lcarb-sil | 674_8_3 Lcarb-sil | 707_6_4 Lcarb-sil | 707_6_4 Lsil | 2181_2_1 Lcarb-sil | 2181_2_1 Lsil | 2200_2_4 Lcarb-sil | 2108_2_1 Lcarb-sil | |
|---|---|---|---|---|---|---|---|---|---|
| Т, °С | 1200 | 1350 | 1200 | 1350 | 1350 | 1350 | 1350 | 1200 | 1350 |
| Рлит, ГПа | 3.0 | 3.0 | 5.5 | 5.5 | 5.5 | 5.5 | 5.5 | 6.3 | 6.3 |
| Р(Н2О), ГПа | 1.16 | 0.94 | 2.3 | 3.6 | 3.57 | 3.7 | 3.72 | 3.65 | 2.15 |
| Р(СО2), ГПа | 1.84 | 2.06 | 3.2 | 1.9 | 1.93 | 1.8 | 1.78 | 2.65 | 4.15 |
| OH–, wt. % | 3 | 4 | 4 | 3 | 4 | 3 | 3 | 3 | 4 |
| H2O, wt. % | 5.4 | 2.5 | 5.8 | 5.4 | 4.4 | 5.4 | 5.4 | 8.8 | 2 |
| CO2 wt. % | 10 | 19.2 | 10 | 10.6 | 11.4 | 14.3 | 10.1 | 7.4 | 8.3 |
| CO$_{3}^{{2 - }}$ wt. % | 15.1 | 14.3 | 17.9 | 16.5 | 0 | 17.8 | 0 | 13 | 21.3 |
| Vcr | 0.3 | 0.09 | 0.36 | 0.3 | – | 0.3 | – | 0.43 | 0.02 |
| 100NBO/T | 360 | 391 | 365 | 361 | 82.5 | 380 | 93.5 | 251 | 388 |
| Е, кДж/моль | 130.4 | 121.4 | 141.2 | 142 | 141 | 137 | 139 | 146.2 | 142.7 |
| η, Па с | 4.5 | 0.32 | 14.6 | 3.65 | 1.22 | 2.74 | 1 | 32.6 | 1.33 |
3. РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
После экспериментов (табл. 1) в полученных образцах преобладает агрегат карбонатных и силикатных дендритных фаз, возникших при закалке карбонатно-силикатного расплава. Согласно расчету масс-баланса, концентрация расплава варьирует от 57 до 70 мас. % при 1200°С и от 71 до 100 мас. % при 1350°С (табл. 2, рис. 1). Со снижением давления с 6.3 до 3.0 ГПа степень плавления увеличивается. Поскольку в качестве исходного использовался тонкоистертый порошок ксенолита, то в полученных после эксперимента образцах все твердые фазы являются новообразованными. При 1200°С размер кристаллов силикатов и карбонатов достигает 100–500 мкм. В опыте при 3.0 ГПа и 1200°С кристаллические фазы сформировали сложную мозаичную текстуру (рис. 1a). В ней ксеноморфные зерна клинопироксена размером до 300–500 мкм содержат включения ортопироксена. Причем ортопироксен иногда имеет частично сохранившиеся грани, а чаще ксеноморфен и несет следы растворения. Такие же включения неправильной формы встречаются в субидиоморфных зернах магнезита. Расплав располагается как в небольших обособлениях среди кристаллических фаз, так и концентрируется в горячей зоне. В большей части продуктов опытов присутствуют линзообразные выделения ликвидусного магнезита (рис. 1д).
В магнезитах, полученных в опытах при 3.0 и 6.3 ГПа и 1200°С, содержание FeO и CaO изменяется в диапазоне 7–9 мас. % и 1.65–1.75 мас. % соответственно. Клинопироксены из эксперимента № 2202_2_4 содержат 5.3 мас. % FeO, до 1 мас. % Na2O и имеют Ca# = 42. Образовавшиеся ортопироксены содержат 7.1–7.5 мас. % FeO, а концентрация CaO в них увеличивается со снижением давления с 0.17 до 0.8 мас. %.
Несмотря на то что исходные составы содержали значительное количество CO2 и H2O, в агрегатах дендритных кристаллов, образованных после закалки карбонатно-силикатного расплава, не фиксировалось появления пузырей флюидной фазы. В изученной нами ранее системе Lc–GS–CO2–H2O при 5.5 ГПа и 1350°С среди закалочных фаз обнаружены глобулы вспененного силикатного стекла, размером от первых микрон до 100 мкм, содержащие большое количество пузырьков флюидной фазы (рис. 1 г) [13]. Глобулы вспененного стекла концентрируются в агрегате закалочных фаз карбонатов и силикатов. Сами глобулы не сдержат закалочных кристаллов карбонатов. Если бы они были продуктами закалки карбонатно-силикатного расплава, то они должны были бы равномерно распределены по объему закалочного агрегата, а любая порция расплава между ликвидусными кристаллами или во включениях, должна была в равных пропорциях содержать как глобулы, так и закалочные кристаллы карбонатов. Однако этого не наблюдается. Глобулы концентрируются лишь вблизи кристаллов магнезита, а в нем самом обнаружены включения, объем которых на 75% заполнен одной глобулой [13].
В полученных в этой работе образцах с аналогичным содержанием CO2 и H2O глобулы силикатного стекла не фиксировалось. В опыте при 3.0 ГПа и 1200°С наблюдаются выделения похожего вспененного стекла, но без четких границ с агрегатом закалочных кристаллов. Более того, закалочные кристаллы карбонатов в значительном количестве появляются непосредственно в стекле. Наличие закалочных карбонатов в стекле может свидетельствовать о том, что разница в составах силикатного и карбонатно-силикатного расплавов при 3.0 ГПа и 1200°С исчезает. Вопрос о том, существовали ли пузыри флюидной фазы в глобулах силикатного расплава при 5.5 ГПа и 1350°С, а также при 3.0 ГПа и 1200°С, на наш взгляд, остается открытым. Ряд косвенных признаков указывает на их закалочную природу.
В целом составы расплавов, полученных в результате реакционного взаимодействия, в силу высоких степеней плавления, более или менее близки к валовому составу использованной системы Lc–GS–CO2–H2O (табл. 2). Таким образом, их составы близки к составу магмы, которая могла бы в диапазоне давлений 3.0–6.3 ГПа и температур 1200–1350°С образоваться в результате растворения перидотитового материала богатым летучими карбонатным расплавом. В опытах этой работы (табл. 1 и 2) расслоение на силикатный и силикатно-карбонатный расплавы не наблюдалось. В полученных карбонатно-силикатных расплавах содержание SiO2 варьирует от 19 до 33 мас. %, отношение MgO/CaO изменяется от 0.6 до 3.3 (рис. 2), а содержание K2O близко к 8–10 мас. %. Как показано ранее в работе [13], при образовании эмульсии состав его карбонатно-силикатной части меняется незначительно (за исключением K2O, содержание которого падало до 6.2–6.7 мас. %) (табл. 2), а силикатная часть состоит из 51–66 мас. % SiO2, 12–28 мас. % K2O и незначительного количества других компонентов (около 1 мас. % Al2O3; 0.5–1 мас. % Na2O; до 0.5 мас. % FeO).
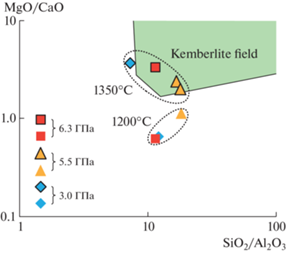
Рис. 2.
Диаграмма SiO2/Al2O3–MgO/CaO (мас. %) с составами полученных экспериментально расплавов и полем первичных кимберлитовых расплавов по данным [5].
Полученные нами с использованием улучшенной модели прогноза и расчетов вязкости магматических расплавов [17] данные (табл. 3) свидетельствуют о том, что вязкость карбонатно-силикатных и существенно силикатных расплавов значительно уменьшается с ростом следующих параметров: температуры, содержания в них ОН–, CO$_{3}^{{2 - }}$. В меньшей степени она снижается с ростом общего содержания Н2О и СО2. Напротив, вязкость значительно увеличивается с ростом концентрации кристаллов в карбонатно-силикатном расплаве. Влияние литостатического и парциальных давлений Н2О и СО2 зависит от степени деполимеризации расплавов: при 100NBO/T ≤ 200 вязкость расплавов значительно снижается, а при 200 ≤ 100NBO/T ≤ 400, напротив, значительно увеличивается с ростом Рлит, P(H2O) и P(CO2). Полученные данные свидетельствуют, что вязкость карбонатно-силикатных расплавов (с кристаллами) и силикатных расплавов при PT-параметрах экспериментов соизмерима и они чрезвычайно маловязкие. Такие расплавы должны обладать высокой подвижностью при PT-параметрах выноса кимберлитовой магмы из мантии.
Анализ полученных в системе Lc–GS–CO2–H2O данных позволяет сделать вывод, что богатый калием карбонатный расплав с большим количеством летучих способен при 3.0–6.3 ГПа и 1200–1350°С – условиях, близких к оценочным для поднимающейся кимберлитовой магмы [19], эффективно растворять до 50 мас. % захваченного в виде ксенолитов перидотитового материала. Согласно модели [17], присутствие в расплаве более 40 мас. % твердой фазы должно приводить к резкому росту его вязкости и остановке подъема. То есть расплав способен растворять все то количество перидотитового материала, которое на момент отделения от протолита потенциально может транспортировать. Причем в результате реакционного взаимодействия расплав обогащается SiO2 (до 30 мас. %) и другими компонентами, характерными для кимберлитовой магмы. На рис. 2 можно видеть, что в интервале давлений 3.0–6.3 ГПа и температур 1350°С полученные экспериментально составы расплавов близки к реконструированному в работе [5] составу кимберлитовой магмы. Характерно, что в той же системе Lc–GS без добавления летучих растворимость перидотитового материала при близких PT-параметрах незначительна и расплав при взаимодействии с ним остается существенно карбонатным [20]. Согласно данным [13], реакционное взаимодействие богатого летучими расплава начинается с карбонатизации оливина, которая обеспечивает образование магнезита и ортопироксена, а также обогащение расплава SiO2. Более глубокая стадия может включать также и карбонатизацию ортопироксена. При 5.5–6.3 ГПа и 1200–1350°С в системе Lc–GS–CO2–H2O кристаллизации клинопироксена не наблюдается. Однако при 3.0 ГПа и 1200°С растворение перидотита сопровождается кристаллизацией магнезита и клинопироксена. Причем реликты ортопироксена в виде включений указывают на то, что после полной карбонатизации оливина взаимодействие в системе идет согласно реакции:
В целом полученные экспериментальные данные доказывают, что наиболее важным фактором начального этапа эволюции магмы может быть реакционное взаимодействие богатого летучими карбонатного расплава с ксенолитами. Причем, несмотря на растворение около 50 мас. % перидотитового материала, богатый летучими расплав остается маловязким и способным к быстрому движению к поверхности. Однако вследствие высокой растворимости CO2 и частичной карбонатизации перидотита он, по-видимому, не вскипает с образованием флюида.
Ранее в работе [8] сделан вывод о том, что богатый натрием карбонатный расплав за счет растворения ортопироксена разделяется на две несмешивающиеся карбонатную и существенно силикатную жидкости. Причем последняя достигает насыщения молекулярным CO2 и вскипает с отделением пузырьков. При декомпрессии эмульсии силикатный расплав обеспечивает непрерывную подачу пузырьков CO2. В богатой калием системе Lc–GS–CO2–H2O мы также наблюдали появление глобул силикатного расплава, содержащего большое количество пузырьков. Однако, по нашему мнению, пузырьки флюидной фазы образовывались при закалке образцов. На основании данных [13] и этой работы можно заключить, что образование двух богатых калием несмешивающихся расплавов: карбонатно-силикатного и существенно силикатного, вследствие их сопоставимо низкой вязкости и относительно узкого PT-диапазона стабильности эмульсии (табл. 2, 3), по-видимому, не играет существенной роли в эволюции магмы. Однако этот вопрос требует дальнейшей детальной проработки.
Список литературы
Kamenetsky V.S., Golovin A.V., Maas R., Giuliani A., Kamenetsky M.B., Weiss, Y. Towards a New Model for Kimberlite Petrogenesis: Evidence from Unaltered Kimberlites and Mantle Minerals // Earth-Science Rev. 2014. V. 139. P. 145–167.
Mitchell R.H., Giuliani A., O’Brien H. What is a Kimberlite? Petrology and Mineralogy of Hypabyssal Kimberlites // Elements: An International Magazine of Mineralogy, Geochemistry, and Petrology. 2019. V. 15 (6). P. 381–386.
Kamenetsky V.S., Kamenetsky M.B., Weiss Y., Navon O., Nielsen T.F.D., Mernagh T.P. How Unique is the Udachnaya-East kimberlite? Comparison with Kimberlites from the Slave Craton (Canada) and SW Greenland // Lithos. 2009. V. 112. P. 334–346.
Russell J.K., Porritt L.A., Lavallée Y., Dingwell D.B. Kimberlite Ascent by Assimilation-fuelled Buoyancy // Nature. 2012. V. 481. P. 352–356.
Rock N.M.S., Bowes D.R., Wright A.E. Lamprophyres. Blackie and Sons Ltd. New York, 1991. 285 p.
Mitchell R.H. Kimberlites: Mineralogy, Geochemistry and Petrology. New York, Plenum Press, 1986. 442 p.
Eggler D.H. Kimberlites: How Do They Form? In Kimberlites and Related Rocks: Their Composition, Occurrence, Origin and Emplacement (ed. J. Ross ). Sydney, Blackwell Scientific Publications, 1989. P. 489–504.
Kamenetsky V.S., Yaxley G.M. Carbonate–silicate Liquid Immiscibility in the Mantle Propels Kimberlite Magma Ascent // Geochim. Cosmochim. Acta. 2015. V. 158. P. 48–56.
Sharygin I.S., Litasov K.D., Shatskiy A., Safonov O.G., Golovin A.V., Ohtani E., Pokhilenko N.P. Experimental Constraints on Orthopyroxene Dissolution in Alkali-carbonate Melts in the Lithospheric Mantle: Implications for Kimberlite Melt Composition and Magma Ascent // Chem. Geol. 2017. V. 455. P. 44–56.
Becker M., Le Roex A. P. Geochemistry of South African On- and Off-craton, Group I and Group II Kimberlites: Petrogenesis and Source Region Evolution // J. Petrol. 2006. V. 47. P. 673–703.
Grassi D., Schmidt M.W. Melting of Carbonated Pelites at 8–13 GPa: Generating K-rich Carbonatites for Mantle Metasomatism // Contrib. Mineral. Petrol. 2011. V. 162. P. 169–191.
Navon O. Diamond Formation in the Earth’s Mantle // Proceedings of the 7th International Kimberlite Conference. Cape Town, Red Roof Design, 1999. V. 2. P. 584–604.
Sokol A.G., Kruk A.N. Role of CO2 in the Evolution of Kimberlite Magma: Experimental Constraints at 5.5 GPa and 1200–1450°C // Lithos. 2021. V. 386. 106042.
Palyanov Y.N., Borzdov Y.M., Khokhryakov A.F., Kupriyanov I.N., Sokol A.G. Effect of Nitrogen Impurity on Diamond Crystal Growth Processes. Crystal Growth Design // 2010. V. 10. P. 3169–3175.
Sokol A.G., Borzdov Y.M., Palyanov Y.N., Khokhryakov A.F. High-temperature Calibration of a Multi-anvil High Pressure Apparatus // High Pressure Research. 2015. V. 35 (2). P. 139–147.
Sun C., Dasgupta R. Slab–mantle Interaction, Carbon Transport, and Kimberlite Generation in the Deep Upper Mantle // Earth Planet. Sci. Lett. 2019. V. 506. P. 38–52.
Persikov E.S., Bukhtiyarov P.G. Viscosity of Magmatic Melts: Improved Structural-chemical Model // Chemical Geol. 2020. V. 556. P. 5.
Persikov E.S., Bukhtiyarov P.G. Experimental and Theoretical Studies of the Viscosity of the Fluid Magmatic Systems in Conjunction with the Structure of Melts at the Thermodynamic Parameters of the Earth’s Crust and Upper Mantle. Advances in Experimental and Genetic Mineralogy // Special Publication to 50th Anniversary of D.S. Korzhinsky Institute of Experimental Mineralogy of the Russian Academy of Sciences. Yuriy Litvin, Oleg Safonov (Eds), Chapter 4. 2020. P. 69–95.
Kavanagh J.L., Sparks R.S.J. Temperature Changes in Ascending Kimberlite Magma // Earth Planet. Sci. Lett. 2009. V. 286. P. 404–413.
Sokol A.G., Kruk A.N., Chebotarev D.A., Palyanov Y.N. Carbonatite Melt–peridotite Interaction at 5.5–7.0 GPa: Implications for Metasomatism in Lithospheric Mantle // Lithos. 2016. V. 248. P. 66–79.
Дополнительные материалы отсутствуют.
Инструменты
Доклады Российской академии наук. Науки о Земле


