Доклады Российской академии наук. Науки о жизни, 2020, T. 491, № 1, стр. 159-163
МЕХАНИЗМ ДЕЙСТВИЯ СТИМФОРТЕ НА АКТИВАЦИЮ ЗАЩИТЫ КЛЕТОК – МИШЕНЕЙ ВИРУСНОЙ ИНФЕКЦИИ
Д. Г. Мальдов 1, *, П. Г. Дерябин 2, С. С. Григорян 2, Д. В. Мишин 2, В. Л. Андронова 2, Е. И. Исаева 2, Г. А. Галегов 2, А. В. Ильичев 1
1 ЗАО “СКАЙ ЛТД”
129301 Москва, Россия
2 ФГБУ “Национальный исследовательский центр эпидемиологии и микробиологии им. Н.Ф. Гамалеи” Минздрава РФ
123098 Москва, Россия
* E-mail: maldov-dg@yandex.ru
Поступила в редакцию 06.02.2020
После доработки 06.02.2020
Принята к публикации 06.02.2020
Аннотация
Стимфорте в широком диапазоне концентраций (15–225 мкг/мл) полностью подавляет цитопатогенную активность вируса гепатита С (ВГС) в клеточной культуре Vero-V. При введении препарата в культуру до заражения наиболее важную роль в подавлении инфекции играют интерфероны (ИФН). При введении Стимфорте после заражения механизм, по-видимому, иной. Активаторами продукции ИФН являются в основном (или исключительно) лиганды рецепторных комплексов TLR-4 и NOD-2 в составе препарата. Действие этих веществ, вероятно, синергично, как синергично в клетках Vero-V действие липополисахарида (ЛПС) и мурамилдипептида (MDP).
ВВЕДЕНИЕ
При изучении влияния иммуностимулирующего препарата “Стимфорте” на хроническую инфекцию у мышей, вызванную вирусом гепатита С (ВГС), было показано, что одним из основных факторов, обусловливающих его противовирусное действие, является защитная реакция клеток-мишеней, в частности, синтез интерферона-β (ИФН-β) [1]. Эффективное подавление репликации вируса в культуре клеток Vero-V в присутствии Стимфорте также связано главным образом с выработкой ИФН [2]. Однако, факторы, активирующие продукцию самих ИФН при использовании Стимфорте, до настоящего времени не были установлены.
В составе Стимфорте обнаружены лиганды TLR-4 [2] и, возможно, NOD-2, являющихся одними из основных стимуляторов продукции ИФН, действующих аддитивно [3, 4]. Однако, активация продукции ИФН и других цитокинов Стимфорте была показана только в клетках иммунной системы [5–7].
Целью данной работы было изучение действия Стимфорте на инфекцию ВГС в клетках Vero-V, не являющихся элементом иммунной системы, роль в этом процессе ИФН, и рецепторного аппарата, через который стимулируется усиление активности ИФН.
МАТЕРИАЛЫ И МЕТОДЫ
Эффекторы. Для позитивного воздействия на рецепторный аппарат клеток Vero-V использовали стандартные лиганды NOD-2 (мурамилдипептид [MDP, InvivoGen, США]) и TLR-4 (липополисахарид [ЛПС, МЕДГАМАЛ, Россия]), а также препарат Стимфорте (ЗАО “СКАЙ ЛТД”). Для ингибирования TLR-4 использовали антитела (Santa Cruz Biotechnology, США), специфические к патогенсвязывающему участку этого рецептора. Для подавления NOD-2 пути использовали ингибитор его молекулярного адаптера – GSK717 (Sigma-Aldrich, США).
Клетки и вирусы. Культура клеток почки зеленой мартышки Vero-V (вакцинный клон) получена из лаборатории культур тканей ФГБУ “Национальный исследовательский центр эпидемиологии и микробиологии им. Н.Ф. Гамалеи”. Для изучения инфекционной активности ВГС и постановки реакции биологической нейтрализации использовали одно- или двухдневные культуры клеток.
Высокопродуктивный вариант вируса гепатита С (ВГС) получен нами, как описано ранее [8].
Оценка противовирусной активности препарата “Стимфорте”. Культуральную среду с препаратом в известной концентрации вносили в лунки планшета со сформировавшимся клеточным монослоем в момент заражения клеток, за 12 ч до или через 12 ч после заражения ВГС (множественность инфицирования (МИ) 0.1 и 0.01 ТЦИД50/мл). Учет результатов проводили, когда в контрольных не обработанных препаратом культурах происходила тотальная гибель клеток вследствие вирусной инфекции.
Биологическую активность интерферона (ИФН) в пробах, полученных после активации клеток Vero-V препаратом Стимфорте определяли в соответствии с ранее описанной методикой по подавлению репликации вируса везикулярного стоматита в клетках Vero-V [1].
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
При использовании для заражения клеток Vero-V ВГС в дозе, обеспечивающей МИ 0.1 ТЦИД50/кл, были получены следующие результаты (табл. 1). Стимфорте в концентрациях от 14 мкг/мл до 223 мкг/мл полностью защищал клетки от гибели не зависимо от времени внесения (за 12 ч до заражения, одновременно с заражением вирусом или через 12 ч после заражения). При концентрации 446 мкг/мл наблюдалась 50% гибель клеток в условиях, когда Стимфорте вводили одновременно с заражением или при заражении через 12 ч после введения препарата, но, если препарат вносили через 12 ч после заражения, все клетки выживали. В лунках без препарата (контроль) все клетки погибли в результате цитопатического действия вируса. При заражении клеток до введения препарата гибели клеток не наблюдалось при всех исследованных концентрациях Стимфорте.
Таблица 1.
Противовирусное действие препарата “Стимфорте” в отношении инфекции, вызванной ВГС в культурах клеток Vero-V
| Множественность инфицирования | Время внесения препарата | Концентрация препарата (мкг/мл)/ количество погибших клеток (%) | |||||||
|---|---|---|---|---|---|---|---|---|---|
| 893 | 446 | 223 | 111 | 55 | 28 | 14 | 0 | ||
| 0.1 ТЦИД50 | за 12 ч до заражения | 100 | 50 | 0 | 0 | 0 | 0 | 0 | 100 |
| в момент заражения | 100 | 50 | 0 | 0 | 0 | 0 | 0 | 100 | |
| через 12 ч после заражения | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 100 | |
| 0.01 ТЦИД50 | за 12 ч до заражения | 100 | 50 | 0 | 0 | 0 | 0 | 0 | 100 |
| в момент заражения | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 100 | |
| через 12 ч после заражения | 100 | 50 | 0 | 0 | 0 | 0 | 100 | 100 | |
При десятикратном снижении заражающей дозы ВГС (0.01 ТЦИД50/кл), если клетки заражали через 12 ч после добавления препарата, результат не отличался от результата, полученного при МИ 0.1 ТЦИД50/кл. Такие же результаты наблюдали при заражении клеток за 12 ч до введения Стимфорте. При одновременном с заражением введении Стимфорте в интервале концентраций от 14 до 893 мкг/лунку все клетки выжили.
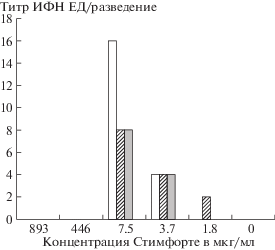
Одним из наиболее вероятных механизмов ингибирующего действия Стимфорте на репродукцию ВГС является стимуляция продукции ИФН. В соответствии с результатами, представленными на рис. 1, внесение Стимфорте в культуральную среду в дозах 27–55 мкг/мл за 12 ч или одновременно с заражением ВГС (МИ 0.1 или 0.01 ТЦИД50/кл) индуцирует синтез ИФН дозозависимым образом и обеспечивает 100% защиту клеток, т.е. полностью предотвращает репродукцию ВГС. В высоких концентрациях 446–893 мкг/мл Стимфорте не активирует продукцию ИФН, что может быть обусловлено особенностью его действия, описываемого колоколообразной кривой зависимости активности препарата от концентрации, или его токсичностью в высоких концентрациях. Вместе с тем, обращает на себя внимание тот факт, что препарат в низкой концентрации 14 мкг/мл не стимулирует синтез ИФН в детектируемых количествах, но оказывает 100% защитное действие, как и в дозах, вызывающих синтез ИФН. Подобный эффект выявляется также при внесении Стимфорте в дозах до 55 мкг/мл через 12 ч после заражения, т.е. продукция ИФН не индуцируется, но обеспечивается 100% защита инфицированных клеток от гибели. Следовательно, индукция ИФН не может быть единственным путем воздействия на репродукцию ВГС in vitro.
Рис. 1.
Активность интерферонов, индуцированных различными дозами Стимфорте при разных введениях. Время заражения и дозы вируса:
□ – 12 ч до заражения ТЦИД50 = 0.1;
 – одновременно с заражением ТЦИД50 = 0.1;
– одновременно с заражением ТЦИД50 = 0.1;
 – одновременно с заражением ТЦИД50 = 0.01;
– одновременно с заражением ТЦИД50 = 0.01;
 – 12 ч после заражения ТЦИД50 = 0.01;
– 12 ч после заражения ТЦИД50 = 0.01;
Ранее нами было показано, что иммуностимулирующая активность Стимфорте обусловлена взаимодействием препарата с ТLR4 рецепторами [2]. Для их выявления в клетках Vero-V мы использовали в качестве лиганда ТLR4-рецепторов ЛПС и в качестве их блокатора антиТLR4–антитела. Для доказательства существования NOD-2 рецепторов в этих клетках использовали MDP и ингибитор молекулярного адаптера пути NOD-2 рецептора – GSK-717. Действие этих эффекторов оценивали через 24 и 72 ч после введения по активности ИФН. Использование данного метода обусловлено природой клеток Vero-V – иммортализированных фибробластов почек зеленой мартышки, в которых невозможно провести измерение продукции ИФН с помощью иммуноферментного анализа из-за видоспецифичности этих цитокинов.
Из данных, приведенных в табл. 2, видно, что активирующее действие ЛПС в концентрации 100 нг/мл на продукции ИФН было на грани достоверности (в разведении 1/2 через 24 ч) и в 4 раза слабее, чем эффект MDP (100 нг/мл). Однако, при сочетанном использовании ЛПС в той же концентрации с MDP в неактивной концентрации 30 нг/мл наблюдается достоверное действие на продукцию активных ИФН через 72 ч (разведение 1/8), хотя через 24 ч влияние на продукцию ИФН еще не обнаруживалось. При снижении концентрации ЛПС до 30 нг/мл комбинация потеряла активность. Таким образом, очевидно, что клетки Vero-V сенситивны как к MDP, так и к ЛПС, а ответ на одновременное введение этих веществ аддитивен или даже синергичен.
Таблица 2.
Действие эффекторов, взаимодействующих с ТLR-4 и NOD-2 на продукцию активных интерферонов клетками Vero-V
| Препараты, действующие на клетки Vero-V | Титр интерферона в клетках, ед/мл* | |
|---|---|---|
| 24 ч | 72 ч | |
| Контроль клеток | <2 | <2 |
| MDP (100 нг/мл) | 8** | <2 |
| Стимфорте (30 мкг/мл) | <2 | <2 |
| Стимфорте (50 мкг/мл) | 16** | 8** |
| Стимфорте (100 мкг/мл) | 16** | 4** |
| АнтиТLR4-антитела (10мкг/мл) + Стимфорте (50 мкг/мл) | <2 | <2 |
| Стимфорте (50 мкг/мл) + GSK-717 (50 нM/мл) | <2 | <2 |
| Стимфорте (50 мкг/мл) + GSK-717 (1 мкМ/мл) | <2 | <2 |
| MDP (100 нг/мл) + GSK-717 (200 нМ/мл) | <2 | 2 |
| ЛПС 100 нг/мл | 2 | <2 |
| ЛПС 30 нг/мл | <2 | <2 |
| ЛПС 30 нг/мл + 30 мкг/мл Стимфорте | 4** | <2 |
| ЛПС 30 нм/мл + MDP 30 нг/мл | <2 | <2 |
| Стимфорте 30 мкг/мл + MDP 30 нг/мл | 16** | 2 |
| ЛПС 100 нг/мл + MDP 30 нг/мл | <2 | 8** |
В концентрациях 50 и 100 мкг/мл Стимфорте максимально эффективно усиливал продукцию ИФН через 24 ч, но через 72 ч активность препарата в концентрации 100 мкг/мл снижалась более значительно, что согласуется с полученными нами ранее результатами – стимулирующая активность Стимфорте описывается колоколообразной концентрационной кривой [9, 10].
В концентрации 30 мкг/мл Стимфорте не активен. Но при добавлении ЛПС или MDP (по 30 нг/мл) активность комбинации через 24 ч возрастает до титра 1/4 и 1/16, соответственно, что доказывает аддитивный характер взаимодействия Стимфорте с этими веществами.
Как видно из табл. 2, продукция ИФН полностью блокируется и антителами к ТLR-4 и ингибитором GSK-717, и стимулируется MDP и Стимфорте. Таким образом, активация продукции ИФН под действием Стимфорте является результатом его воздействия на рецепторы ТLR-4 и NOD-2.
К сожалению, низкий титр ИФН и отсутствие его продукции при использовании Стимфорте в дозе 30 мкг/мл (крутая концентрационная кривая) не позволяют в должной мере оценить эффекты воздействия на каждый из рецепторов Vero-V количественно. Тем не менее полученные результаты позволяют предположить пути воздействия Стимфорте на продукцию ИФН. Так как ЛПС усиливает продукцию ИФН, а антитела к TLR-4 ее блокируют, то, следовательно, в клетках Vero-V есть TLR4-рецепторы. MDP также вызывает усиленную продукцию ИФН, а GSK-717 ее ингибирует, что достоверно указывает на наличие NOD2- рецепторов в этих клетках.
В литературе имеются экспериментально подтвержденные доказательства синергизма между опосредованной TLR-2, TLR-4 и NOD2 продукцией цитокинов [11–13]. Кроме того, NOD2 и TLR4 аддитивно воздействуют на продукцию ИЛ-6, TNF-α, CXCL1 и CCL2 в нейтрофилах после стимуляции пептидогликаном, MDP и агонистами TLR (Pam3, CSK4 и ЛПС) [14]. Как TLR-4, так и NOD2 являются активаторами NF-κB и MAPK пути и каждый из этих рецепторов имеет свой путь для эпигенетических реакций защиты клеток от патогенов, которые в одних случаях конкурируют, а в других их действие аддитивно [15].
Таким образом, инфекция ВГС в клетках Vero-V подавляется Стимфорте при его предварительном введении посредством стимуляции продукции ИФН, которая осуществляется через рецепторы ТLR-4 и NOD-2. Этот же механизм, по-видимому, может быть основным при подавлении хронической инфекции ВГС у мышей [1].
ВЫВОДЫ
1. Клетки Vero-V содержат как ТLR-4 так и NOD-2 рецепторы подобно клеткам иммунной системы.
2. Стимфорте действует на репликацию ВГС в культуре клеток Vero-V, подавляя продукцию вируса и способствуя выживанию клеток.
3. Действие препарата частично обусловлено стимулированием продукции ИФН.
4. Стимулирование продукции ИФН при взаимодействии Стимфорте с клетками Vero-V происходит в основном или исключительно через рецепторы NOD-2 и TLR-4.
Список литературы
Мальдов Д.Г., Андронова В.Л., Григорян С.С. и др. // ДАН. 2017. Т. 477. № 2. С. 257–260.
Мальдов Д.Г., Чирвон Е.А., Ильичев А.В., и др. // Иммунология. 2011. № 4. С. 195–200.
Colonna M. // Eur. J. Immunol. 2007. V. 37. № 2. P. 306–309.
Tötemeyer S., Sheppard M., Lloyd A. et al. // J. Immunol. 2006. V. 176. № 8. P. 4804–4810.
Cui J., Chen Y., Wang H.Y. et al. // Hum. Vaccin. Immunother. 2014. V. 10. № 11. P. 3270–3285.
Cui J., Zhu L., Xia X. et al. // Cell. 2010. V. 141. № 3. P. 483–496.
Benko S., Magalhaes J.G., Philpott D.J., et al. // J. Immunol. 2010. V. 185. № 3. P. 1681–1691.
Дерябин П.Г., Львов Д.К. // ДАН. 1998. Т. 358. № 5. С. 685–687.
Мальдов Д.Г., Бельков А.П., Ильичев А.В и др. // Иммунология. 2009. Т. 30. № 2. С. 96–97.
Мальдов Д.Г., Григорян С.С., Галегов Г.А. и др. // Иммунология. 2011. Т. 32. № 5. С. 250–256.
Farzi A., Reichmann F., Meinitzer A. et al. // Brain Behav. Immun. 2015. V. 44. P. 106–120.
Fritz J.H., Girardin S.E., Fitting C., et al. // Eur. J. Immunol. 2005. V. 35. № 8. P. 2459–2470.
Tada H., Aiba S., Shibata K., et al. // Infect. Immun. 2005. V. 73. № 12. P. 7967–7976.
Netea M.G., Ferwerda G., de Jong D.J., et al. // J. Immunol. 2005. V. 174. № 10. P. 6518–6523.
Jeong Y.J., Kang M.J., Lee S.J., et al. // Immunology. 2014. V. 143. № 2. P. 269–276.
Дополнительные материалы отсутствуют.
Инструменты
Доклады Российской академии наук. Науки о жизни


