Доклады Российской академии наук. Науки о жизни, 2021, T. 497, № 1, стр. 131-134
ОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ ОЛОВА В БУРОЙ ВОДОРОСЛИ SACCHARINA LATISSIMA БАРЕНЦЕВА МОРЯ
Л. О. Метелькова 1, З. А. Жаковская 1, Г. И. Кухарева 1, Г. М. Воскобойников 2, *, академик РАН Г. Г. Матишов 2
1 Санкт-Петербургский научно-исследовательский центр экологической безопасности Российской академии наук – обособленное структурное подразделение Федерального государственного бюджетного учреждения науки «Санкт-Петербургский Федеральный исследовательский центр Российской академии наук» (НИЦЭБ РАН – СПб ФИЦ РАН)
Санкт-Петербург, Россия
2 ФГБУН Мурманский морской биологический институт РАН (ММБИ РАН)
Мурманск, Россия
* E-mail: grvosk@mail.ru
Поступила в редакцию 03.10.2020
После доработки 21.10.2020
Принята к публикации 23.10.2020
Аннотация
Проведена оценка степени загрязнения оловоорганическими соединениями – монобутилоловом, дибутилоловом, трибутилоловом, тетрабутилоловом, трифенилоловом и трициклогексилоловом Saccharina latissimа, доминирующей среди водорослей-макрофитов, из сублиторали Кольского залива и Восточного Мурмана Баренцева моря. Полученные результаты показали умеренное загрязнение исследованных образцов оловоорганическими соединениями. Суммарное содержание шести соединений олова находилось в диапазоне 17–74 нг/г (сухого веса) в пробах водорослей. Анализ индексов деградации бутил-производных олова указал на активно протекающие процессы трансформации трибутилолова и тетрабутилолова в водорослях.
ВВЕДЕНИЕ
Оловоорганические соединения (ООС) являются востребованными в современной промышленности продуктами и находят широкое применение во всем мире в качестве стабилизаторов поливинилхлорида, в производстве полиуретанов, силикона, красок и пестицидов [1–3]. Особое распространение получили соединения трибутилолова (ТБО) как биоцидные компоненты противообрастательных (antifouling) красок в судостроении [4]. Использование таких красок приводит к поступлению значительного количества биоцидов в гидробионты. Воздействуя на живые морские организмы, ООС разрушают, в основном, эндокринную и иммунную системы. Все известные ООС обладают как острой, так и хронической токсичностью, однако наибольший вред гидробионтам оказывают соединения трибутилолова (ТБО) и трифенилолова (ТФО) [5–7]. В литературе отсутствуют сведения о степени загрязнения ООС водорослей-макрофитов, являющимися средообразующими организмами литорали и сублиторали большинства морей. Цель настоящей работы состояла в определении присутствия и оценке степени загрязнения ООС Saccharina latissimа, вида водорослей, доминирующих в сублиторали северных морей. Полученные данные будут способствовать пониманию механизмов накопления, преобразования ООС в тканях сахарины. Необходимо отметить, что помимо академического данные сведения имеют и чисто практический интерес: заросли S. latissimа являются местом обитания и размножения многих гидробионтов, исследуемый вид широко используется в пищевой, медицинской промышленности.
МАТЕРИАЛЫ И МЕТОДЫ
Образцы бурой водоросли Saccharina latissimа (Phaeophyceae) отбирались осенью 2019 г. на побережье Кольского залива и Восточного Мурмана (Баренцево море) с глубины 9 м (табл. 1), высушивались при комнатной температуре, гомогенизировались и направлялись на анализ. Аналитическая процедура определения массовой доли ООС в водорослях была разработана на основе методики ISO количественного определения производных (дериватов) ООС в воде методом ГХ/МС [8]. В качестве внутреннего стандарта и дериватизирующего агента использовались трипропилолово и тетраэтилборат натрия соответственно. ГХ/МС анализ экстрактов в целевом режиме SIM (Selection Ion Monitoring) проводился на хроматомасс-спектрометре единичного разрешения QP 2010 (Shimadzu). При анализе использовали капиллярную колонку средней полярности TR-5MS (60 м × 0.25 мм × 0.25 мкм). Идентификацию аналитов проводили по двум характеристическим ионам с учетом точных времен удерживания. Расчет массовой доли для каждого соединения производился методом внутреннего стандарта с использованием коэффициентов пересчета на катион органического олова, указанных в методике ISO [8]. Предел количественного измерения при указанных ГХ/МС параметрах и расчете на сухой вес составил 0.1 нг/г. Контроль растворителей и сорбента осуществлялся с теми же условиями концентрирования и хроматографии, что и для исследуемых образцов. Определяли шесть видов ООС – трициклогексилолово (ТЦГО), ТФО, тетрабутилолово (ТТБО), ТБО и его метаболиты – монобутилолово (МБО) и дибутилолово (ДБО).
Таблица 1.
Станции отбора проб водорослей Saccharina latissima и концентрации ООС в исследованных образцах
| № Ст | Место отбора проб | Содержание ООС, нг/г сухого веса S. latissimi | ||||||
|---|---|---|---|---|---|---|---|---|
| Баренцево море, глубина 9 м | МБО | ДБО | ТБО | ТТБО | ТФО | ТЦО | Общее содержание | |
| 1. | Кольский залив, губа Ретинская 69°11'20"с.ш. 36°36'87"в.д. | 7.8 | 2.0 | 1.4 | 13.0 | 6.6 | 15.0 | 45.8 |
| 2. | Кольский залив, губа Грязная 69°04′07″ с. ш. 33°17′36″ в. д. | 6.0 | 1.2 | 1.8 | 8.4 | <0.1 | <0.1 | 17.4 |
| 3. | Восточный Мурман, губа Зеленецкая 69°07′09″ с.ш., 36°05′35″ в.д. | 19.0 | 3.6 | 1.0 | 11 | <0.1 | <0.1 | 34.6 |
| 4. | Восточный Мурман, губа Ярнышная 69°6’27.2″ с.ш. 36°3’29.1″в.д. | 43.0 | 14.0 | 7.8 | 8.8 | <0.1 | <0.1 | 73.6 |
| 5. | Восточный Мурман, губа Порчниха 69°4'30" с.ш. 36°16'44" в.д. | 12.0 | 2.8 | 4.8 | 10.0 | <0.1 | <0.1 | 29.6 |
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Результаты анализов продемонстрировали присутствие в пробах S. latissima всех видов изучаемых ООС (табл. 1).
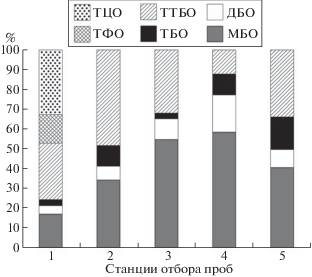
Очевидно, что в тканях водорослей происходит накопление и, возможно, трансформация ООС, сорбированных из воды. Источником алкилированных производных олова (ТТБО, ТБО, ДБО и МБО) является, преимущественно, водный транспорт. Среднее суммарное содержание четырех алкилированных ООС в образцах водорослей сублиторали Кольского залива (станции 1, 2) и Восточного Мурмана (станции 3–5) составили соответственно 21 и 46 нг/г. Во всех образцах доминировали МБО и ТТБО. Их вклад в общее содержание ООС составил в среднем 79%. Исключение составляет образец, отобранный в губе Ретинской (станция 1, Кольский залив), в котором помимо алкилированных соединений олова обнаружены ТФО и ТЦО. Этот факт свидетельствует о локальном загрязнении губы Ретинской пестицидами, содержащими соединения ТФО и ТЦО. На рис. 1 показано относительное содержание каждого ООС в образцах водорослей. Среди бутил-производных олова МБО является наиболее стабильным [2] и должно естественным образом накапливаться в донных осадках и водорослях при невысокой транспортной нагрузке на акваторию. Его доминирование говорит об активно проходящих процессах деструкции начальных соединений – ТБО и ТТБО, поступивших в водную среду. Преобладание в образцах водорослей ТТБО указывает на широкую распространенность этого соединения в качестве загрязнителя водной среды изучаемого региона, в частности Баренцева моря.
Полученные данные о концентрациях индивидуальных соединений (МБО, ДБО, ТБО, ТТБО, ТФО и ТЦО), а также сумма ООС в исследованных образцах (табл. 1) демонстрируют присутствие детектируемых количеств ООС в водорослях.
ЗАКЛЮЧЕНИЕ
Результаты исследования показали присутствие ООС во всех образцах водорослей-макрофитов. При этом наблюдаемые концентрации оказались невысокими. Зарегистрированное присутствие в каждом изученном образце ТТБО указывает на широкую распространенность этого загрязнителя в экосистеме Баренцева моря.
Анализ профилей бутил-производных олова выявил высокое долевое содержание МБО в тканях Saccharina latissima. Доминирование указанного метаболита свидетельствует об активно проходящих в водорослях процессах деструкции начальных соединений – ТБО и ТТБО, поступивших в водную среду. Полученные данные указывают также на дополнительное загрязнение губы Ретинской пестицидами, содержащими соединения ТФО и ТЦО.
Несмотря на умеренные выявленные концентрации ООС, эти соединения должны в дальнейшем контролироваться в воде, биоте, а также донных отложениях из-за потенциального риска для гидробионтов и экосистемы Баренцева моря в целом, учитывая возрастающий антропогенный прессинг на Мурманское побережье Баренцева моря: строительство на побережье комплексов по перегрузке, переработке углеводородного сырья.
Список литературы
Майстренко В.Н., Клюев Н.А. Эколого-аналитический мониторинг стойких органических загрязнителей. М.: БИНОМ, 2004, 323 с.
De Carvalho Oliviera R., Santelli R.E. Occurrence and chemical speciation analysis of organotin compounds in the environment: A review. // Talanta. 2010. V. 82. P. 9–24. https://doi.org/10.1016/j.talanta.2010.04.046
Ghazi D., Rasheed Z., Yousif E. Review of organotin compounds: chemistry and applications. // International journal of research in engineering and innovation. 2018. V. 2(4). P. 340–348. https://doi.org/10.32474/AOICS.2018.03.000161
Richter J., Fettig I., Philipp R., Jakubowski N. Tributyltin—critical pollutant in whole water samples—development of traceable measurement methods for monitoring under the European Water Framework Directive (WFD) 2000/60/EC. // Environ. Sci. Pollut. Res. 2015. V. 22. P. 9589–9594. https://doi.org/10.1007/s11356-015-4614-4
Environmental health criteria for tributyltin compounds/ International Programme on Chemical Safety // World Heals Organization. Geneva. 1990.
De Castro T.F., Junior A.S.V., Padilha F.F., Droppa-Almeida D., Saalfeld G.Q., Pires D.M., Pereira J.R., Corcini C.D., Colares E.P. Effects of exposure to triphenyltin (TPT) contaminant on sperm activity in adulthood of Calomys laucha exposed through breastfeeding. // Environ. Sci. Pollut. Res. 2019. V. 26. P. 8280–8288. https://doi.org/10.1007/s11356-019-04365-1
Su G., Zhang X., Raine J.C., Xing L., Higley E., Hecker M., Giesy J.P., Yu H. Mechanisms of toxicity of triphenyltin chloride (TPTC) determined by a live cell reporter array // Environ. Sci. Pollut. Res. 2013. V. 20. P. 803–811. https://doi.org/10.1007/s11356-012-1280-7
International Organization for Standardization. Water quality – Determination of selected organotin compounds – Gas chromatographic method. ISO 17353:2004 (E).
Дополнительные материалы отсутствуют.
Инструменты
Доклады Российской академии наук. Науки о жизни