Доклады Российской академии наук. Науки о жизни, 2022, T. 507, № 1, стр. 536-541
НОРТРИПТИЛИН МОДУЛИРУЕТ МИГРАЦИЮ ЛИМФОЦИТОВ И МОНОЦИТОВ ПЕРИФЕРИЧЕСКОЙ КРОВИ ПАЦИЕНТОВ С ХРОНИЧЕСКОЙ ОБСТРУКТИВНОЙ БОЛЕЗНЬЮ ЛЕГКИХ
А. Г. Кадушкин 1, *, А. Д. Таганович 1, Л. В. Мовчан 2, Т. С. Колесникова 1, Е. В. Ходосовская 1, Т. В. Шман 2
1 Учреждение образования “Белорусский государственный медицинский университет”
Минск, Беларусь
2 Государственное учреждение “Республиканский научно-практический центр детской онкологии, гематологии и иммунологии”
Минский район, Беларусь
* E-mail: kadushkyn@gmail.com
Поступила в редакцию 13.05.2022
После доработки 28.06.2022
Принята к публикации 02.07.2022
- EDN: ERNRAH
- DOI: 10.31857/S2686738922050122
Аннотация
В настоящем исследовании с помощью метода проточной цитометрии изучено влияние нортриптилина (1 и 10 мкМ), будесонида (10 нМ) и их комбинации на миграцию лимфоцитов и моноцитов периферической крови пациентов с хронической обструктивной болезнью легких (ХОБЛ) к хемокинам CCL5 и CXCL10. Нортриптилин (10 мкМ), самостоятельно и в сочетании с будесонидом, подавлял миграцию к CCL5 и CXCL10 Т-хелперов, цитотоксических Т-лимфоцитов, NK-клеток и B-лимфоцитов, а также ускорял перемещение к этим хемокинам моноцитов. Сочетание нортриптилина (1 мкМ) и будесонида превосходило способность одного будесонида подавлять хемотаксис субпопуляций лимфоцитов к CXCL10, но не к CCL5. Комбинация нортриптилина (10 мкМ) и будесонида супрессировала миграцию к CCL5 и CXCL10 субпопуляций лимфоцитов и активировала хемотаксис к обоим хемокинам моноцитов более значительно, чем один будесонид. Результаты исследования демонстрируют способность нортриптилина самостоятельно модулировать миграцию лимфоцитов и моноцитов периферической крови пациентов с ХОБЛ и потенцировать эффекты будесонида.
ВВЕДЕНИЕ
В настоящее время от 300 до 400 млн человек во всем мире страдают от хронической обструктивной болезни легких (ХОБЛ). Это заболевание ежегодно уносит жизни до 3 млн пациентов [1]. По оценкам экспертов, в глобальном масштабе ХОБЛ приводит к экономическим издержкам в размере 2.1 трлн. долларов США. Ожидается, что к 2030 г. эти цифры могут увеличиться более чем вдвое [1].
Несмотря на риск развития серьезных побочных эффектов, ингаляционные глюкокортикостероиды (ИГКС), лекарственные средства (ЛС) с противовоспалительным механизмом действия широко используются для лечения ХОБЛ. Добавление ИГКС к бронходилататору (длительно действующему β2-агонисту (ДДБА) или комбинации ДДБА и длительно действующего антихолинергического препарата) снижает риск будущих обострений у пациентов с предшествующими обострениями ХОБЛ [2]. Однако глюкокортикостероиды (ГКС) имеют ограниченную эффективность в снижении риска смерти и уровня провоспалительных медиаторов, улучшении функции легких и качества жизни пациентов с ХОБЛ [3, 4].
Исследования, направленные на поиск ЛС, способных потенцировать действие ГКС, привели к выявлению нортриптилина как ЛС, обладающего такими свойствами [5, 6]. Нортриптилин относится к группе трициклических антидепрессантов (ТЦА) и одновременно является активным метаболитом амитриптилина, который также принадлежит к группе ТЦА. Нортриптилин используется для лечения депрессии, тревоги и никотиновой зависимости у пациентов с ХОБЛ [7, 8]. Проведенные нами ранее исследования позволили установить синергичное супрессирующее действие нортриптилина и ГКС в отношении секреции цитокинов мононуклеарными клетками периферической крови (МКПК) больных ХОБЛ [9, 10].
Привлечение лимфоцитов и моноцитов в легкие, где они продуцируют провоспалительные медиаторы, происходит под воздействием хемокинов – лигандов для хемокиновых рецепторов, локализованных на поверхности клеток. Полагают, что основное значение в перемещении клеток крови пациентов с ХОБЛ в легкие играют лиганд-рецепторные пары CCR5-CCL5 и СXCR3-CXCL9/CXCL10/CXCL11 [11, 12]. На это в том числе указывают данные об увеличенной миграции МКПК пациентов с ХОБЛ в направлении CCL5, CXCL9, CXCL10 и CXCL11 по сравнению со здоровыми курящими и некурящими людьми [13]. Сообщается о подавлении хемотаксиса полиморфноядерных клеток в места воспаления под влиянием нортриптилина [14]. Однако сведения о способности этого ЛС потенцировать эффекты ГКС, связанные с угнетением миграции МКПК, отсутствуют.
Целью исследования явилось оценить способность комбинации нортриптилина и ГКС влиять на перемещение лимфоцитов и моноцитов крови пациентов с ХОБЛ в направлении хемокинов CCL5 и CXCL10.
МАТЕРИАЛЫ И МЕТОДЫ
Характеристика пациентов. Донорами крови для проведения исследования явились 8 больных ХОБЛ (6 мужчин и 2 женщины), в возрасте 61.5 (59.0–68.3) лет [медиана (25-й – 75-й процентили)], имеющих индекс курящего человека 39.0 (16.3–43.8) пачка/лет и 2–3 степень тяжести заболевания (в соответствии с критериями Глобальной инициативы по хронической обструктивной болезни легких). Критериями исключения из исследования явились наличие у пациентов бронхиальной астмы, заболеваний соединительной ткани с изменениями функции дыхательной системы, онкологических и аутоиммунных заболеваний, нарушений свертывающей системы крови, а также прием системных ГКС или обострение ХОБЛ в течение 6 нед до начала исследования.
Выделение МКПК. Венозную кровь у пациентов забирали утром натощак в объеме 15 мл в пробирку, содержащую гепарин натрия (Белмедпрепараты, Беларусь) в концентрации 10 ЕД/мл в качестве антикоагулянта. МКПК выделяли из периферической крови путем центрифугирования на градиенте плотности 1.077 с использованием раствора Lymphopure (Biolegend, США). Клетки ресуспендировали в концентрации 1 × 106/мл в культуральной среде RPMI 1640 (Gibco, США), обогащенной 1% фетальной телячьей сывороткой (ФТС, Capricorn Scientific, Германия).
Инкубация МКПК с лекарственными средствами. В стерильные пробирки помещали 1 мл клеточной суспензии и инкубировали с ГКС будесонидом (10 нM, Glentham Life Sciences Ltd, Великобритания), нортриптилином (1 и 10 мкМ, Sigma-Aldrich, США) или их комбинацией в увлажненной 5% CO2/95% воздушной среде при 37°C. Спустя 1 ч 100 мкл клеточной суспензии (100 000 клеток) переносили в верхние камеры (съемные вставки) 24-луночного миграционного планшета, имеющие поры диаметром 5 мкм (Costar Corning, США). В нижние камеры миграционного планшета помещали 600 мкл миграционного буфера, состоящего из культуральной среды RPMI 1640, обогащенной 1% ФТС и хемокинами CCL5 (10 нМ, R&D systems, США) или CXCL10 (10 нМ, Gibco, США). В качестве нестимулированного контроля использовали миграционный буфер, не содержащий хемокины. Далее планшеты инкубировали при 37°C, 5% CO2/95% атмосферного воздуха. По окончании 2 ч клетки, мигрировавшие в нижнюю камеру, собирали, отмывали при помощи фосфатного солевого буфера (ФСБ, Cell Wash, BD Biosciences, Польша) (условия центрифугирования: 500 g, 5 мин, комнатная температура) и ресуспендировали в ФСБ. Добавляли коктейль моноклональных антител, состоящий из CD3-FITC/СD14-PE/CD19-ECD/ CD4-PerCP-Cy5.5/CD56-PC7/CD8-APC/CD45-APC Alexa Fluor 750 (Beckman Coulter, Франция; Exbio, Чехия; BD Biosciences, США), после чего клетки инкубировали в темноте в течение 20 мин при температуре 4°С. Далее клетки отмывали при помощи 3 мл ФСБ, содержащего 0.2% бычий сывороточный альбумин (BD Biosciences, США), и фиксировали путем внесения в пробирки 300 мкл 1% раствора параформальдегида. Используя проточный цитометр Navios (Beckman Coulter, США), настроенный на среднюю скорость потока клеток, подсчитывали их количество в течение 100 с.
Образцы анализировали с использованием программного обеспечения Kaluza (Beckman Coulter). T-хелперы идентифицировали как CD45+CD3+CD4+, цитотоксические Т-лимфоциты (ЦТЛ) – CD45+CD3+CD8+, B-лимфоциты – CD45+CD19+, NK-клетки – CD45+CD3-CD56+, моноциты – CD14+ клетки.
Статистическая обработка данных. Статистическая обработка данных осуществлялась с использованием программы GraphPad Prism версия 7.00 (GraphPad Software, США). Оценка результатов исследования проводилась методом однофакторного дисперсионного анализа (ANOVA) с последующим апостериорным попарным сравнением показателей с помощью критерия Тьюки. При всех видах статистического анализа критическое значение уровня значимости принимали как равное 5%.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
В настоящем исследовании будесонид подавлял миграцию ЦТЛ, NK-клеток, B-лимфоцитов и ускорял перемещение моноцитов к хемокину CCL5 (рис. 1). Схожим образом ГКС влияли на хемотаксис NK-клеток, B-лимфоцитов и моноцитов в направлении CXCL10, но не были способны изменить миграцию к этому хемокину T-хелперов и ЦТЛ (рис. 2).
Рис. 1.
Влияние нортриптилина и будесонида на хемотаксис мононуклеарных клеток периферической крови в направлении CCL5. Представлены графики, демонстрирующие влияние нортриптилина (Нортр, 1 и 10 мкМ), будесонида (Буд, 10 нМ) и их сочетания на миграцию Т-хелперов (а), цитотоксических Т-лимфоцитов (ЦТЛ) (б), NK-клеток (в), В-лимфоцитов (г) и моноцитов (д), индуцированную 10 нМ CCL5. Здесь и на рис. 2: результаты представлены в виде среднего ± стандартная ошибка среднего; n = 8. * p < 0.05 по сравнению с контролем (клетками крови, находившимися в присутствии хемокина, но в отсутствии лекарственных средств); ♦p < 0.05 по сравнению с Буд 10 нМ; #p < 0.05 по сравнению с Нортр 10 мкМ; §p < 0.05 по сравнению с Нортр 1 мкМ.
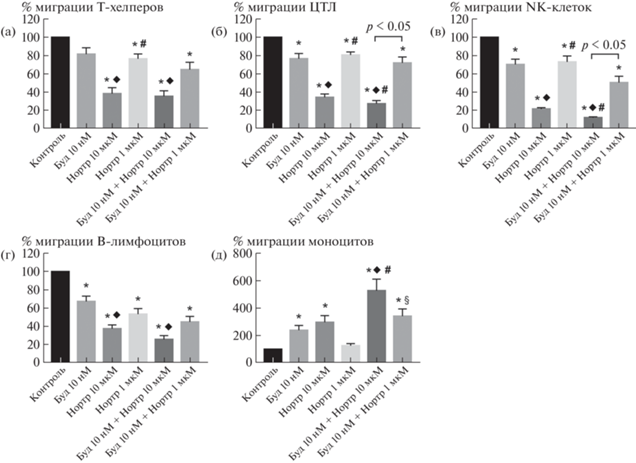
Рис. 2.
Влияние нортриптилина и будесонида на хемотаксис мононуклеарных клеток периферической крови в направлении CXCL10. Представлены графики, демонстрирующие влияние нортриптилина (Нортр, 1 и 10 мкМ), будесонида (Буд, 10 нМ) и их сочетания на миграцию Т-хелперов (а), цитотоксических Т-лимфоцитов (ЦТЛ) (б), NK-клеток (в), В-лимфоцитов (г) и моноцитов (д), индуцированную 10 нМ CXCL10.

Добавление к клеточной суспензии нортриптилина в обеих концентрациях (1 и 10 мкМ) приводило к снижению миграции T-хелперов, ЦТЛ, NK-клеток и B-лимфоцитов в направлении CCL5. В минимальной концентрации (1 мкМ) нортриптилин не влиял на перемещение ЦТЛ и моноцитов к CXCL10, зато подавлял хемотаксис к этому лиганду рецепторов CXCR3 Т-хелперов, NK-клеток и B-лимфоцитов. Вместе с тем применение ТЦА в более высокой концентрации (10 мкМ) продемонстрировало его выраженное ингибирующее действие на миграцию к CXCL10 субпопуляций лимфоцитов и активирующее влияние на перемещение к нему моноцитов.
Комбинация будесонида и нортриптилина (1 мкМ) не имела преимуществ по сравнению с одним будесонидом в отношении миграции МКПК к CCL5, но превосходила способность ГКС подавлять хемотаксис лимфоцитов к CXCL10. Сочетанное использование будесонида и нортриптилина в концентрации 10 мкМ сопровождалось более существенным (ингибирующим – на лимфоциты, активирующим – на моноциты) влиянием на хемотаксис клеток крови к CCL5 и CXCL10 по сравнению с эффектом одного будесонида. Способность изменять миграцию лимфоцитов крови к обоим хемокинам оказалась лишь незначительно лучше у комбинации нортриптилина (10 мкМ) с будесонидом, чем у одного ТЦА в той же концентрации, тогда как сочетанное действие этих же лекарственных средств на хемотаксис моноцитов крови было более выраженным по сравнению с одним нортриптилином (10 мкМ).
Как известно, у пациентов с ХОБЛ наблюдается скопление лимфоцитов в легочной ткани, где они синтезируют провоспалительные цитокины, металлопротеиназы, цитотоксические гранулы (перфорины, гранзим В). Эти белки способствуют привлечению в дыхательные пути нейтрофилов и разрушают протеины внеклеточного матрикса легких с последующим развитием эмфиземы [15, 16]. Приведенные в настоящем исследовании данные в совокупности со значением лимфоцитов в патогенезе ХОБЛ дают основание полагать, что нортриптилин как самостоятельно, так и в совокупности с будесонидом, может замедлить прогрессирование ХОБЛ за счет снижения количества мигрировавших в легкие лимфоцитов.
Сообщается, что под влиянием ГКС наступает активация популяции противовоспалительных моноцитов, которые проявляют повышенную способность к миграции в очаг воспаления, продуцируют противовоспалительные медиаторы, обладают высокой фагоцитарной активностью и ограничивают активацию Т-лимфоцитов, что в конечном счете приводит к разрешению воспалительного процесса [17]. Учитывая такие сведения, мы предполагаем, что повышение хемотаксиса моноцитов к хемокинам CCL5 и CXCL10 под влиянием ГКС будесонида и нортриптилина (10 мкМ), выявленное в нашем исследовании, может быть связано с мобилизующим действием ЛС на противовоспалительные моноциты, что в последующем может способствовать подавлению воспаления. Для подтверждения данной гипотезы требуется проведение дополнительных исследований, в которых будет определен фенотип мигрировавших моноцитов.
Обобщая полученные данные, можно сделать заключение, что нортриптилин (10 мкМ), самостоятельно и в сочетании с будесонидом (10 нМ), подавляет миграцию к CCL5 и CXCL10 Т-хелперов, ЦТЛ, NK-клеток и B-лимфоцитов крови пациентов с ХОБЛ, а также ускоряет перемещение к этим хемокинам моноцитов крови. Комбинация нортриптилина (10 мкМ) и будесонида обладает более выраженным действием на миграцию клеток крови больных ХОБЛ (ингибирующим – на субпопуляции лимфоцитов и активирующим – на моноциты), чем один будесонид.
Список литературы
Adeloye D., Agarwal D., Barnes P.J., et al. Research priorities to address the global burden of chronic obstructive pulmonary disease (COPD) in the next decade // J. Glob. Health. 2021. V. 11. Art. 15003.
Agusti A., Fabbri L.M., Singh D., et al. Inhaled corticosteroids in COPD: friend or foe? // Eur. Respir. J. 2018. V. 52. Art. 1801219.
Babu K.S., Kastelik J.A., Morjaria J.B. Inhaled corticosteroids in chronic obstructive pulmonary disease: a pro-con perspective // Br. J. Clin. Pharmacol. 2014. V. 78. P. 282–300.
Yang I.A., Clarke M.S., Sim E.H., et al. Inhaled corticosteroids for stable chronic obstructive pulmonary disease // Cochrane Database Syst. Rev. 2012. V. 7. Article CD002991.
Lehár J., Krueger A.S., Avery W., et al. Synergistic drug combinations tend to improve therapeutically relevant selectivity // Nat. Biotechnol. 2009. V. 27. № 7. P. 659–666.
Mercado N., To Y., Ito K., et al. Nortriptyline reverses corticosteroid insensitivity by inhibition of phosphoinositide-3-kinase-δ // J. Pharmacol. Exp. Ther. 2011. V. 337. № 2. P. 465–470.
Howes S., Hartmann-Boyce J., Livingstone-Banks J., et al. Antidepressants for smoking cessation // Cochrane Database Syst. Rev. 2020. V. 4. № 4. Article CD000031.
Tselebis A., Pachi A., Ilias I., et al. Strategies to improve anxiety and depression in patients with COPD: a mental health perspective // Neuropsychiatr. Dis. Treat. 2016. V. 12. P. 297–328.
Kadushkin A., Tahanovich A., Movchan L., et al. Nortriptyline enhances corticosteroid sensitivity of blood T cells from patients with chronic obstructive pulmonary disease // J. Physiol. Pharmacol. 2021. V. 72. № 5. P. 793–805.
Kadushkin A.G., Tahanovich A.D., Movchan L.V., et al. Nortriptyline overcomes corticosteroid resistance in NK and NKT-like cells from peripheral blood of patients with chronic obstructive pulmonary disease // Research Results in Pharmacology. 2022. V. 8. № 1. P. 59–70.
Кадушкин А.Г., Таганович А.Д., Мовчан Л.В., и др. Субпопуляционный состав B-лимфоцитов крови, коэкспрессирующих CD5 и хемокиновые рецепторы, у пациентов с хронической обструктивной болезнью легких // Иммунология. 2022. Т. 43. № 2. С. 197–207.
Кадушкин А.Г., Таганович А.Д., Мовчан Л.В., и др. Популяционная перестройка B-лимфоцитов, экспрессирующих хемокиновые рецепторы, у пациентов с хронической обструктивной болезнью легких // Биомедицинская химия. 2022. Т. 68. № 2. С. 134–143.
Costa C., Traves S.L., Tudhope S.J., et al. Enhanced monocyte migration to CXCR3 and CCR5 chemokines in COPD // Eur. Respir. J. 2016. V. 47. № 4. P. 1093–1102.
Sacerdote P., Bianchi M., Panerai A.E. Chlorimipramine and nortriptyline but not fluoxetine and fluvoxamine inhibit human polymorphonuclear cell chemotaxis in vitro // Gen. Pharmacol. 1994. V. 25. P. 409–412.
Rovina N., Koutsoukou A., Koulouris N.G. Inflammation and immune response in COPD: where do we stand? // Mediators Inflamm. 2013. V. 2013. Art. 413735.
Polverino F., Seys L.J., Bracke K.R., et al. B cells in chronic obstructive pulmonary disease: moving to center stage // Am. J. Physiol. Lung Cell Mol. Physiol. 2016. V. 311. № 4. P. L687–L695.
Ehrchen J.M., Roth J., Barczyk-Kahlert K. More Than Suppression: Glucocorticoid Action on Monocytes and Macrophages // Front. Immunol. 2019. V. 10. Art. 2028.
Дополнительные материалы отсутствуют.
Инструменты
Доклады Российской академии наук. Науки о жизни


