Экология, 2019, № 1, стр. 22-29
Внутривидовая дифференциация глухой кукушки (Cuculus optatus) в пределах ареала: связь с обилием видов-хозяев
С. Г. Мещерягина a, М. Г. Головатин a, *, Г. Н. Бачурин b
a Институт экологии растений и животных УрО РАН
620144 Екатеринбург, ул. 8 Марта, 202, Россия,
b Научно-практический центр биоразнообразия
623850 Свердловская обл, Ирбит, ул. Мира, 56, Россия,
* E-mail: golovatin@ipae.uran.ru
Поступила в редакцию 15.06.2018
После доработки 18.06.2018
Аннотация
Показано распространение рас глухой кукушки в пределах репродуктивного ареала. Выявлено их географическое разобщение. Области распространения рас приурочены к районам повышенной плотности населения соответствующего расообразующего вида-хозяина. Отмечена зависимость обилия гнездового паразита от плотности расообразующих видов и пеночек с чисто-белыми яйцами как дополнительных хозяев. Роль группы дополнительных хозяев оказывается важной в местах, где доля расообразующего вида в общей численности пеночек невелика.
Глухая кукушка Cuculus optatus Gould, 1845 (ранее C. saturatus horsfieldi Moore, 1857) – облигатный гнездовой паразит, распространенный в Северной Палеарктике [1, 2] и специализирующийся на эксплуатации родительской заботы пеночек рода Phylloscopus [3, 4]. Среди представителей этого рода отсутствуют виды, репродуктивный ареал [5] которых охватывал бы целиком современную территорию размножения глухой кукушки. Поэтому в отдельных частях своего широкого ареала гнездовой паразит сталкивается с различными по составу и обилию фаунистическими комплексами пеночек и, следовательно, вынужден использовать разных видов-хозяев.
Исследования на обыкновенной кукушке Cuculus canorus показывают, что специализация на эксплуатации определенного хозяина выражается в соответствии окраски [6] и морфометрических признаков [7, 8] яиц гнездового паразита яйцам хозяина. Такая специализация приводит к формированию внутривидовых рас (gentes), между которыми обнаружены различия в унаследованной по материнской линии митохондриальной ДНК при отсутствии различий по ядерной ДНК [9–11].
У глухой кукушки на основе анализа оологического материала с территории России выявлены 4 варианта окраски скорлупы яиц, соответствующих яйцам пеночек: таловки Phylloscopus borealis, сибирской теньковки Ph. collybita tristis, корольковой пеночки Ph. proregulus и зарнички Ph. inornatus + + Ph. humei [12–15]. Зарнички Ph. inornatus и Ph. humei имеют сходную морфологию яиц и сравнительно недавно разделены на отдельные виды [16–18]. По аналогии с обыкновенной кукушкой специализированные варианты окраски яиц глухой кукушки также рассматриваются как расы.
Эволюцию рас обыкновенной кукушки связывают с плотностью населения и однородностью географического распределения подходящих хозяев [19]. Цель настоящей работы – проанализировать географическое распространение рас глухой кукушки, обращая внимание на связь между плотностью населения гнездового паразита и видов-хозяев.
МАТЕРИАЛ И МЕТОДЫ
Рассмотрено 425 случаев гнездового паразитизма глухой кукушки на территории России и Восточного Казахстана, включающих находки яиц (n = 294) и птенцов в период выкармливания видом-хозяином (n = 131). Данные были получены в результате полевых исследований (n = 127), осмотра оологических коллекций (n = 46) и анализа опубликованных сведений (n = 252) (подробнее см. [15]).
При наличии ооморфологических данных (n = 229) расовую принадлежность определяли по комплексу морфометрических признаков яйца (табл. 1). Длину (L) и диаметр (B) яиц измеряли цифровым штангенциркулем с разрешением 10 µm. На основе этих данных и цифровых фотографий вычисляли объем каждого яйца, используя программу Egg Scanner Beta [20] или формулу V = (1/6πB2L) – в случае отсутствия фотографий яиц [21]. Индекс удлиненности яиц определяли по формуле v = = (L – B)/B × 100% [22].
Таблица 1.
Морфометрические характеристики яиц, используемые при определении рас Cuculus optatus
| Морфометрические показатели | Раса Cuculus optatus | |||
|---|---|---|---|---|
| borealis (n = 16) |
collybita (n = 62) |
inornatus (n = 14) |
proregulus (n = 32) |
|
| Длина яиц L, мм min–max |
<20.5 (19.08, 19.73) 18.55–20.70 |
<20.5 (18.86, 19.26) 17.10–20.80 |
<20.5 (18.00, 18.88) 16.20–20.0 |
>20.5 20.59, 21.12 19.70–22.45 |
| Диаметр яиц B, мм min–max |
>13.7 (14.02, 14.67) 13.38–15.35 |
>13.7 (13.82, 14.06) 13.20–14.80 |
<13.2 (12.74, 13.11) 12.50–13.60 |
13.2 < B < 13.7 (13.27, 13.65) 12.20–14.50 |
| Индекс удлиненности яиц v, % min–max |
<38.5 (33.0, 38.0) 26.0–45.0 |
<38.5 (35.0, 38.0) 22.0–51.0 |
38.5 < v < 50.0 (39.0, 46.0) 26.0–55.0 |
>50.0 (53.0, 58.0) 37.0–66.0 |
| Объем яиц V, мл min–max |
>1.8 (1.98, 2.22) 1.81–2.54 |
>1.8 (1.91, 2.01) 1.67–2.45 |
<1.8 (1.58, 1.71) 1.39–1.87 |
>1.8 (1.94, 2.08) 1.59–2.38 |
| Цветовые оттенки в окраске рисуночных элементов скорлупы | Оранжевый, красный, бледно-фиолетовый, бежево-коричневый | Черно-коричневый | Красный, красно-коричневый, бледно-фиолетовый, бежево-коричневый | Бледно-фиолетовый, бежево-коричневый, красно-коричневый |
При работе с коллекционными материалами дополнительно сравнивали особенности окраски каждого яйца глухой кукушки с окраской яиц в вариационных рядах видов-хозяев, а при работе с данными других авторов ориентировались на описания окраски скорлупы, метрические характеристики и имеющиеся фотоматериалы. В нескольких случаях определение производили только по размеру яиц кукушки.
Обнаруженных кукушат относили к соответствующей расе только в тех районах, где присутствовали либо единственная раса глухой кукушки (по находкам яиц), либо единственный расообразующий вид-хозяин (n = 58). В местах, где было два расообразующих вида, расу определяли предположительно как наиболее вероятную по виду-хозяину гнезда (n = 7) или распространенной расе в ближайших районах (n = 2). В местах симпатричного размножения нескольких рас глухой кукушки при отсутствии необходимой информации для идентификации расы (n = 129) данные использовали только для расчета частоты эксплуатирования отдельных видов-хозяев.
Виды хозяев разделяли на 3 группы: 1) расообразующий хозяин – вид, с которым у гнездового паразита существует выраженное миметическое сходство яиц (см. табл. 1) и который успешно выращивает кукушат; 2) дополнительный хозяин – близкородственный к расообразующему вид, симпатрично гнездящийся в тех же местообитаниях, способный успешно вырастить кукушонка, но с которым у паразита отсутствует миметическое сходство яиц; 3) случайный хозяин – вид, не родственный расообразующему хозяину, паразитирование на котором, как правило, не приводит к благополучному результату. При отсутствии сведений о виде-хозяине, когда яйца были отложены вне гнезда на землю в природных условиях (n = 1), либо получены при содержании глухой кукушки в неволе (n = 7), либо изъяты из яйцевода погибших самок (n = 4), либо находились в оологической коллекции без яиц хозяина и необходимых указаний на этикетке (n = 1), данные использовали только для указания мест встречаемости рас кукушки.
Для получения представления об обилии видов-хозяев – пеночек – в пределах ареала глухой кукушки использовали опубликованные данные региональных учетов птиц из 340 географических точек с территории восточнее Предуралья (около 200 источников, например [23–27]). Область западнее Предуралья не рассматривали из-за отсутствия достоверных регистраций размножения глухой кукушки. Для каждой точки рассчитывали средний показатель плотности пеночек в местообитаниях, пригодных для заселения глухой кукушкой (хвойные и смешанные леса, приречные кустарниковые заросли, залесенные болота, гари и выруба на поздних стадиях зарастания). К областям повышенного обилия вида-хозяина относили территории, где средняя плотность пеночек была выше 10 пар/км2. Кроме того, отдельно выделяли области со средней плотностью 5–9.9 и более 15 пар/км2. Границы ареалов птиц приведены по картам-схемам, составленным В.Г. Виноградовым [28], с корректировкой по другим источникам [5, 16, 29]. При рассмотрении распространения рас глухой кукушки отдельная географическая точка включала данные с площади приблизительно 50 × 50 км (около 2.5 тыс. км2).
Связь численности гнездового паразита с обилием хозяев оценивали методами корреляционного и регрессионного анализа. При этом данные по местообитаниям, заселяемым глухой кукушкой, группировали в зависимости от доли расообразующего хозяина в общей численности пеночек: 90.0–100, 70.0–89.9, 30.0–69.9 и 1.0–29.9%. Для каждой группы рассчитывали уравнение множественной линейной регрессии для данных по обилию глухой кукушки (Co) в зависимости от трех факторов: обилия расообразующих видов пеночек (Rh), общего обилия дополнительных видов пеночек с чисто-белыми яйцами (Ah-w) и пятнистыми яйцами (Ah-p). Значимость полученного уравнения проверяли по критерию Фишера, а значимость коэффициентов регрессии с помощью t-критерия Стьюдента. Оценивали линейную корреляцию (r Пирсона) обилия кукушки с общей численностью всех пеночек и отдельно с каждой указанной группой пеночек. Связь обилия гнездового паразита с численностью случайных хозяев в данной работе не рассматривали.
Названия птиц приведены в соответствии со списком орнитофауны стран Северной Евразии в границах бывшего СССР [30].
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Распределение по видам-хозяевам. На территории России глухая кукушка использует в качестве хозяев 28 видов [15, 31], из пеночек эксплуатирует 12 видов (табл. 2). Ее яиц и птенцов не найдено в гнездах сахалинской Phylloscopus borealoides и индийской Ph. griseolus пеночек. Большинство случаев гнездового паразитизма приходится на долю расообразующих видов: Ph. collybita tristis, Ph. inornatus + Ph. humei, Ph. proregulus, Ph. borealis (рис. 1). Среди дополнительных хозяев глухой кукушкой чаще эксплуатировались пеночки, имеющие чисто белую скорлупу яиц: зеленая Ph. trochiloides, бурая Ph. fuscatus, светлоголовая Ph. coronatus и бледноногая Ph. tenellipes. Другие виды дополнительных хозяев, имеющие пятнистую с неокрашенным фоном скорлупу яиц – толстоклювая пеночка Ph. schwarzi, весничка Ph. trochilus и трещотка Ph. sibilatrix, – крайне редко подвергались гнездовому паразитизму. Расообразующие виды также могут выступать в качестве дополнительных хозяев, когда в их гнезда откладывают яйца кукушки несоответствующей расы. Такое иногда происходит в местах симпатричного распространения расообразующих видов.
Таблица 2.
Распределение случаев гнездового паразитизма рас Cuculus optatus в гнездах пеночек Phylloscopus (знаком “?” отмечены случаи, где раса была определена предположительно)
| Виды-хозяева | Раса Cuculus optatus | Итого | |||
|---|---|---|---|---|---|
| borealis | collybita | inornatus | proregulus | ||
| Расообразующие | |||||
| Ph. borealis | 10 + 4? | 3 | 2 | 2 | 21 |
| Ph. collybita tristis | – | 117 + 2? | – | – | 119 |
| Ph. inornatus + Ph. humei | 2 | 1 | 33 + 1? | 8 | 45 |
| Ph. proregulus | – | 3 | 2 | 10 | 15 |
| Дополнительные с чисто белыми яйцами | |||||
| Ph. trochiloides | – | 9 | – | 1? | 10 |
| Ph. fuscatus | 9 | 1 | 3 | 6 | 19 |
| Ph. coronatus | – | – | – | 16 | 16 |
| Ph. tenellipes | – | – | – | 10 | 10 |
| Дополнительные с пятнистыми яйцами | |||||
| Ph. schwarzi | – | 1 | – | 4 | 5 |
| Ph. trochilus | 1 | 1 | – | – | 2 |
| Ph. sibilatrix | – | 1 | – | – | 1 |
| Итого | 26 | 139 | 41 | 57 | 263 |
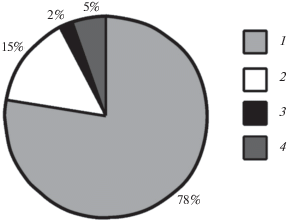
Рис. 1.
Частота эксплуатирования Cuculus optatus гнезд видов-хозяев (n = 412): 1 – расообразующие, 2 – дополнительные с чисто-белыми яйцами, 3 – дополнительные с пятнистыми яйцами, 4 – случайные.
Анализ видового состава пеночек, с которыми у глухой кукушки образовались устойчивые связи при гнездовом паразитизме (расообразующие виды и дополнительные хозяева с чисто белыми яйцами), показывает, что все они являются дальними мигрантами Восточно-Азиатско-Австралийского и Центрально-Азиатского пролетного путей [5]. К ним же относится толстоклювая пеночка Ph. schwarzi, имеющая пятнисто-окрашенные яйца. Однако этот вид редко эксплуатируется глухой кукушкой (1.3%), что, видимо, обусловлено различиями их местообитаний в период размножения: толстоклювая пеночка предпочитает открытые ландшафты. Другие два вида, также с пятнистыми яйцами – Ph. trochilus и Ph. sibilatrix, являются мигрантами Афро-Евразийского пролетного пути и крайне редко подвергаются гнездовому паразитизму глухой кукушкой (0.7%), хотя гнездятся совместно с расообразующими хозяевами в тех же местообитаниях и часто в достаточном количестве.
В качестве случайных хозяев глухой кукушки зарегистрировано 16 видов: по три случая у синей мухоловки Cyanoptila cyanomelana и чечевицы Carpodacus erythrinus, по два – у славки-мельничек Sylvia curruca, сибирского жулана Lanius cristatus и маскированной овсянки Ocyris personatus, по одному – у черногорлой завирушки Prunella atrogularis, пятнистого сверчка Locustella lanceolata, чернобровой Acrocephalus bistrigiceps и садовой A. dumetorum камышевок, белогорлого дрозда Monticola gularis, синехвостки Tarsiger cyanurus, сибирской чечевицы Carpodacus roseus, желтогорлой овсянки Cristemberiza elegans, рыжей Ocyris rutilus, седоголовой O. spodocephalus и таежной O. tristrami овсянок.
Географическое распространение рас глухой кукушки по ареалу. Расы глухой кукушки территориально разобщены в пределах репродуктивного ареала вида (рис. 2). Из 45 географических точек, где была точно установлена расовая принадлежность глухой кукушки, лишь в 4 местах зафиксированы зоны контакта нескольких рас. В 6 точках раса была определена лишь предположительно из-за необходимости дополнительного уточнения ооморфологии (на картах-схемах обозначено знаком “?”).
Рис. 2.
Пространственное распределение мест встречаемости рас Cuculus optatus: а – borealis (черные ромбы), б – collybita (черные квадраты), в – inornatus (черные круги), г – proregulus (черные треугольники) на фоне территорий с разной плотностью соответствующего вида-хозяина; 1 – репродуктивный ареал C. optatus; 2 – ареал гнездования вида-хозяина; 3, 4 и 5 – территории с плотностью вида-хозяина соответственно более 5.0–9.9, 10.0–14.9 и более 15.0 пар/км2. Знаком “?” показаны места, где требуются уточнения по ооморфологии для достоверности определения расы гнездового паразита.
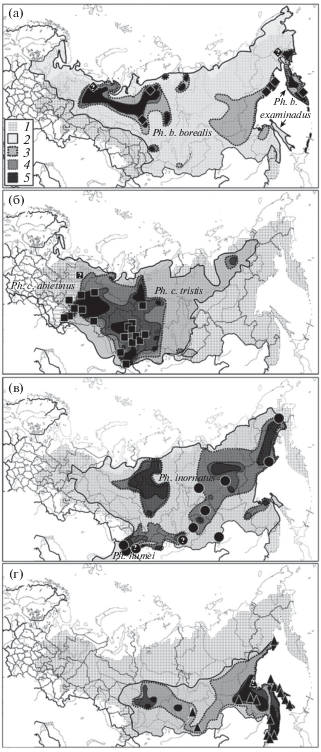
Раса borealis распространена вдоль северной границы ареала от Предуралья до Камчатки; раса collybita – на Среднем и Южном Урале, в центральной и южной частях Западной Сибири; раса inornatus – от Алтая на северо-восток через Забайкалье до Чукотки; раса proregulus – в юго-восточной части ареала от Забайкалья до Приморья и Сахалина, на север до Магаданской области. Пространственно расы приурочены к областям, где средняя плотность расообразующего вида-хозяина более 10 пар/км2 (см. рис. 2). В местах, где отсутствует расообразующий хозяин, глухая кукушка не зарегистрирована.
Совместное распространение рас выявлено на территории юго-восточной части Магаданской области для borealis – inornatus – proregulus, в северо-восточном Забайкалье – для inornatus – proregulus, на северо-западном Алтае – для inornatus – collybita, и в Центральной Сибири на территории Туруханского р-на Красноярского края – для borealis – collybita.
Следует отметить, что у каждого расообразующего вида в пределах ареала имеются области, где вид обилен – средняя плотность более 10–15 пар/км2, но соответствующая раса глухой кукушки отсутствует (см. рис. 2). Особенность этих областей состоит в их изолированности от других мест высокой плотности вида. Так, в Центральной Сибири, где плотность зарнички высокая, вместо расы inornatus встречаются расы collybita и borealis, хозяева которых на этой территории имеют также достаточно высокую плотность населения. Аналогичная ситуация наблюдается в среднем течении р. Енисей, где в местах высокой плотности корольковой пеночки и сибирской теньковки распространена только раса collybita. Также в северо-восточной Якутии в местах высокой плотности сибирской теньковки и зарнички распространена только раса inornatus. Можно предположить, что изолированные области высокой плотности видов-хозяев возникли относительно недавно, уже после того, как на этих территориях сформировались другие расы кукушки. Возможно и иное объяснение – для формирования расы обязательным условием является наличие непрерывной и обширной области высокой плотности расообразующего вида-хозяина. Исследования на обыкновенной кукушке в европейских регионах показали, что плотность и пространственная однородность населения возможных хозяев могут служить предикторами появления специализированных рас гнездового паразита [19].
Характер зависимости обилия глухой кукушки от обилия видов-хозяев. Связь обилия глухой кукушки с суммарной плотностью пеночек была положительной (рис. 3). Вместе с тем при моновидовом населении пеночек, состоящем практически исключительно из расообразующего вида (≥90% в населении пеночек), плотность гнездового паразита по мере увеличения обилия хозяина возрастала более интенсивно, чем при многовидовом населении пеночек. Когда население хозяев состояло из нескольких видов, обилие кукушки менялось сходным образом независимо от доли расообразующего вида в населении.
Рис. 3.
Зависимость обилия глухой кукушки Cuculus optatus от суммарного обилия пеночек Phylloscopus на территориях, различающихся долей расообразующего вида (Rh). r – коэффициенты корреляции Пирсона (p < 0.0001).
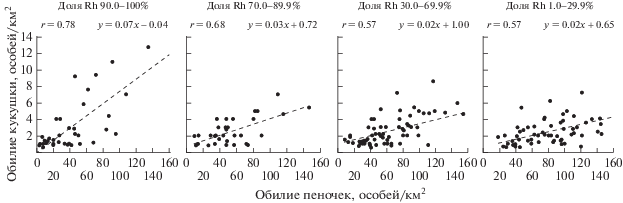
Множественный регрессионный анализ показал увеличение зависимости обилия глухой кукушки от обилия дополнительных хозяев – пеночек с чисто белыми яйцами – по мере снижения доли расообразующего вида в населении (табл. 3). Связь с численностью дополнительных хозяев, имеющих пятнистые яйца, не обнаружена (r = = 0.01–0.20, p = 0.2–0.9). Таким образом, для существования глухой кукушки значимым моментом является наличие пеночек с чисто белыми яйцами в качестве резервного вида-хозяина, что позволяет в случае снижения численности расообразующего хозяина переключиться на их эксплуатацию. Однако при полном отсутствии расообразующего хозяина кукушка не встречается.
Таблица 3.
Значимость влияния обилия видов-хозяев (Rh – расообразующий, Ah-w – дополнительный с чисто-белыми яйцами и Ah-p – дополнительный с пятнистыми яйцами) на обилие глухой кукушки в линейной множественной регрессионной модели
| Доля Rh, % | F-критерий | p-level | b-коэффициенты регрессии | r Пирсона | |||||
|---|---|---|---|---|---|---|---|---|---|
| Rh | Ah-w | Ah-p | b0 | Rh | Ah-w | Ah-p | |||
| 90–100 | F(3.36) = 36.3 | <0.00001 | 0.09 | –0.60 | –1.40 | 0.07 | 0.80 | 0.10 | 0.15 |
| 70–89 | F(3.35) = 12.2 | <0.00001 | 0.06 | –0.06 | –0.06 | 0.84 | 0.70 | 0.37 | 0.20 |
| 30–69 | F(3.62) = 19.2 | <0.00001 | 0.04 | 0.03 | –0.01 | 0.71 | 0.60 | 0.59 | 0.02 |
| 1–29 | F(3.62) = 14.4 | <0.00001 | 0.01 | 0.03 | 0.01 | 0.59 | 0.46 | 0.60 | 0.01 |
ЗАКЛЮЧЕНИЕ
Анализ случаев гнездового паразитизма глухой кукушки на территории России и Восточного Казахстана показал, что устойчивые связи вида существуют с 4 расообразующими хозяевами, а в качестве дополнительных хозяев – с пеночками, имеющими чисто белые яйца. Все они являются дальними мигрантами Восточно-Азиатско-Австралийского и Центрально-Азиатского пролетных путей. Впервые рассмотрены особенности географического распределения рас в пределах ареала глухой кукушки. Оказалось, что они географически разобщены: на севере от Предуралья до Камчатки распространена раса таловки borealis; западную часть ареала, до р. Енисей включительно, занимает раса теньковки collybita; восточнее, от Алтая через Забайкалье до Чукотки, встречается раса зарнички inornatus; от Забайкалья до Приморья и Сахалина и на север до Магаданской области – корольковой пеночки proregulus. Расы приурочены к областям, где средняя плотность расообразующего вида-хозяина достаточно высока – более 10 пар/км2. Роль дополнительных хозяев оказывается важной в местах, где доля расообразующего вида в населении пеночек невелика.
Авторы выражают искреннюю признательность за помощь в полевых работах и сборе материалов по гнездовому паразитизму кукушек И.Ф. Вурдовой, О.В. Бурскому, А.А. Ананину, О.П. Вальчук и Л.В. Капитоновой; за организацию работ в музейных фондах – Н.Н. Балацкому, П.С. Томковичу, Я.А. Редькину, И.В. Фадееву и О.С. Загайновой; за бесценный труд по оценке численности птиц – региональным орнитологам, авторам научных работ, не упомянутых в библиографическом списке из-за редакционных ограничений.
Работа выполнена в рамках государственного задания Института экологии растений и животных УрО РАН и поддержана Комплексной программой УрО РАН (проект № 18-9-4-22).
Список литературы
Payne R.B. The Cuckoos. Oxford, U.K.: Oxford University Press, 2005. 644 p.
Xia C., Liang W., Carey G.J., Zhang Y. Song characteristics of oriental cuckoo Cuculus optatus and himalayan cuckoo Cuculus saturatus and implications for distribution and taxonomy // Zool. Stud. 2016. V. 55. № 38. P. 1–9. doi 10.6620/zs.2016.55-38
Нумеров А.Д. Межвидовой и внутривидовой гнездовой паразитизм у птиц. Воронеж: ФГУП ИПФ Воронеж, 2003. 517 с.
Erritzøe J., Mann C.F., Brammer F., Fuller R.A. Oriental cuckoo Cuculus saturatus // Cuckoos of the World (Helm Identification Guide). London, 2012. P. 468–472.
Дементьев Г.П., Гладков Н.А., Благосклонов К.Н. и др. Птицы Советского Союза. Т. 6. М.: Сов. наука, 1954. 792 с.
Moksnes A., Røskaft E. Egg-morphs and host preference in the common cuckoo (Cuculus canorus): an analysis of cuckoo and host eggs from European museum collections // J. Zool. 1995. V. 236. № 4. P. 625–648. doi 10.1111/j.1469-7998.1995.tb02736.x
Latter O.H. The Egg of Cuculus canorus. An enquiry into the dimensions of the cuckoo’s egg and the relation of the variations to the size of the eggs of the foster-parent, with notes on coloration // Biometrika. 1902. V. 1. № 2. P. 164–176. doi 10.2307/2331486
Antonov A., Stokke B.G., Vikan J.R. et al. Egg phenotype differentiation in sympatric cuckoo Cuculus canorus gentes // J. Evol. Biol. 2010. V. 23. № 6. P. 1170–1182. doi 10.1111/j.1420-9101.2010.01982.x
Gibbs H.L., Sorenson M.D., Marchetti K. et al. Genetic evidence for female host-specific races of the common cuckoo // Nature. 2000. V. 407. № 6801. P. 183–186. doi 10.1038/35025058
Fossøy F., Antonov A., Moksnes A. et al. Genetic differentiation among sympatric cuckoo host races: males matter // Proc. R. Soc. Lond. B Biol. Sci. 2011. V. 278. № 1712. P. 1639–1645. doi 10.1098/rspb.2010.2090
Fossøy F., Sorenson M.D., Liang W. et al. Ancient origin and maternal inheritance of blue cuckoo eggs // Nat. Commun. 2016. V. 7. e10272. doi 10.1038/ncomms10272
Кисленко Г.С., Наумов P.Л. Паразитизм и экологические расы обыкновенной и глухой кукушек в азиатской части СССР // Орнитология. 1967. Т. 8. С. 79–97.
Балацкий Н.Н. Ооморфологические характеристики глухой кукушки Cuculus saturatus в Северной Азии // Актуальные проблемы оологии. Липецк, 1998. С. 21–22.
Балацкий Н.Н., Бачурин Г.Н. Кукушки Западной Сибири и сопредельных территорий // Беркут. 1999. Т. 8. № 2. С. 172–182.
Мещерягина С.Г., Бачурин Г.Н., Бурский О.В. Распространение рас глухой кукушки на территории России: обзор регистраций гнездового паразитизма по видам-хозяевам // Фауна Урала и Сибири. 2017. Вып. 2. С. 139–163.
Red’kin Ya.A., Konovalova M.V. On the taxonomy of Yellow-browed Warbler, Phylloscopus inornatus sensu lato, based on the analysis of collection specimens (Aves: Sylviidae) // Zoosystematica Rossica. 2004. V. 13. P. 137–150.
Irwin D.E., Alström P., Olsson U. et al. Cryptic species in the genus Phylloscopus (Old World leaf warblers) // Ibis. 2001. V. 143. № 2. P. 233–247. doi 10.1111/j.1474-919X.2001.tb04479.x
Martens J. Systematic notes on Asian birds: 72. A preliminary review of the leaf warbler genera Phylloscopus and Seicercus // Br. Ornithol. Club Occ. Publ. 2010. V. 5. P. 41–116.
Soler J.J., Vivaldi M.M., Møller A.P. Geographic distribution of suitable hosts explains the evolution of specialized gentes in the European cuckoo Cuculus canorus // BMC Evol. Biol. 2009. V. 9. № 1. e 88. doi 10.1186/ 1471-2148-9-88
Митяй И.С. Современные подходы к описанию объема и площади поверхности птичьих яиц // Бранта: Cб. научн. тр. Азово-Черноморской орнитологической станции. 2009. № 12. С. 148–156.
Муравьев И.В., Сухова О.В., Юдин К.И. Принцип “золотого сечения” при расчете геометрических показателей в оологических исследованиях // Изв. Пензенского гос. педагогич. ун-та им. В.Г. Белинского. 2008. Т. 6. № 10. С. 194–199.
Костин Ю.В. О методике ооморфологических исследований и унификации описаний оологических материалов // Методики исследования продуктивности и структуры видов птиц в пределах их ареалов: Сб. статей. Ч. 1. Вильнюс, 1977. С. 14–22.
Ананин А.А. Птицы Северного Прибайкалья: динамика и особенности формирования населения. Улан-Удэ: Изд-во Бурятского госуниверситета, 2010. 296 с.
Бабенко В.Г. Птицы Нижнего Приамурья. М.: Прометей, 2000. 725 с.
Рогачева Э.В. Птицы Средней Сибири: распространение, численность, зоогеография. М.: Наука, 1988. 310 с.
Романов А.А. Птицы плато Путорана. М.: Тип. Россельхозакадемии, 1996. 297 с.
Торопов К.В., Шор Е.Л. Птицы южной тайги Западной Сибири: 25 лет спустя. Новосибирск: Наука-Центр, 2012. 636 с.
Виноградов В.Г. Ареалы: Виды птиц [Электронный ресурс] // BioDat: Живая природа и биоразнообразие: Ареалы животных и растений. URL: http://biodat.ru/ db/areal/index.htm (дата обращения: 25.01.2016).
Кузиков И.В. Обзор распространения и случаев залетов глухой кукушки Cuculus optatus в европейской части России // Русский орнитолог. журн. 2015. Т. 24. Экспресс-выпуск 1107. С. 523–549.
Коблик Е.А., Архипов В.Ю. Фауна птиц стран Северной Евразии в границах бывшего СССР: Списки видов // Зоологические исследования. 2014. № 14. 171 с.
Мещерягина С.Г. Расы Cuculus optatus Gould на территории России: особенности связей с видами-хозяевами // Экология: факты, гипотезы, модели: Мат-лы конф. молодых ученых. / Екатеринбург: ИЭРиЖ УрО РАН, 2017. С. 72–86.
Дополнительные материалы отсутствуют.


