Экология, 2020, № 2, стр. 134-140
Динамика структуры и разнообразия рыбных сообществ горных рек Крыма на примере реки Альма
Е. П. Карпова *
Институт биологии южных морей им. А.О. Ковалевского РАН
299011 Севастополь, просп. Нахимова, 2, Россия
* E-mail: karpova_jey@mail.ru
Поступила в редакцию 11.02.2019
После доработки 03.07.2019
Принята к публикации 07.08.2019
Аннотация
Прослежены пространственные и временные изменения видового состава и структуры рыбного населения одной из типичных малых рек Крыма. Отмечено, что под влиянием хозяйственной деятельности и изменения водного режима, связанного преимущественно с антропогенными факторами, наблюдаются более чем пятикратное увеличение количества видов рыб, смена доминирующих комплексов, снижение видового сходства с нативными сообществами и рост показателей видового разнообразия, наиболее выраженный на тех участках, где благодаря различным формам хозяйственной деятельности произошли разрушение биотопов и замена зоны перекатов зоной плесов.
Состояние рыбного населения малых рек зависит от многих факторов, среди которых, начиная со второй половины XX в., основную роль играют последствия различных форм хозяйственной деятельности, за короткий срок вызывающие кардинальные структурные перестройки рыбных сообществ. Трансформация биотических параметров малых рек и последующие сукцессионные изменения являются следствием малого самовосстановительного потенциала и высокой чувствительности к действию различных факторов антропогенного и природного характера [1–5]. Экологическая емкость по отношению к основным факторам антропогенного воздействия для рек горного типа еще более незначительна – она существенно меняется в зависимости от сезонного расхода воды. В меженный период уязвимость водных сообществ резко увеличивается, но и во время сильных паводков комплекс абиотических воздействий, результатом которых является необратимый дрифт гидробионтов и кардинальные изменения морфологии донных отложений, определенные типы которых служат для рыб субстратом для нереста и местом нагула, приводят к значительным сдвигам структурно-функциональных характеристик рыбных сообществ. При усилении воздействия антропогенных факторов экосистемы горных рек могут выйти из состояния импульсной стабильности [6].
Характер антропогенных преобразований идентичен для всех горных рек Крыма: в ходе освоения речных долин для массового развития садоводства и земледелия их русла были спрямлены и зарегулированы, на реках построены гидроузлы, русловые водохранилища, многочисленные несанкционированные водозаборы, при этом значительная часть природных биотопов была уничтожена. Аборигенное рыбное население горных рек представлено незначительным количеством видов, однако в ходе масштабного зарыбления вновь созданных водохранилищ в водоемы бассейнов крымских водотоков (водохранилища и пруды) вселялись хозяйственно ценные виды-интродуценты. В частности, в водохранилища основных рек Крыма было целенаправленно вселено не менее 18 видов, а аборигенные рыбы в реках были признаны сорными и подлежащими истреблению. Затем на протяжении нескольких десятилетий зарыбление водоемов проводилось без ихтиологического контроля, исследования пресноводной ихтиофауны практически отсутствовали и не отслеживались процессы случайной интродукции видов.
Одним из модельных горных водотоков Крыма является р. Альма, одна из основных рек юго-западного макросклона Крымских гор. Процессы изменений, происходящие в малых горных реках, выражены в ней наиболее ярко в связи с тем, что ее хозяйственное использование весьма интенсивно и длится несколько дольше, чем прочих рек Крыма. Кроме того, р. Альма отличается маловодностью и вследствие этого более высокой чувствительностью к воздействию различных по характеру экологических факторов. По тем изменениям, которые уже произошли в этом водотоке, можно судить о вероятных векторах трансформации ихтиофауны других рек при усилении комплексного антропогенного воздействия на их биоценозы.
Помимо кардинальных перемен, произошедших в видовом составе рыбного населения реки за время хозяйственных преобразований Альминской долины, нами были отмечены изменения в пространственном распределении некоторых видов после прекращения поступления в Крым днепровских вод, вызвавшего резкое усиление антропогенной нагрузки на все природные водотоки ввиду того, что значительно увеличилась интенсивность водозабора.
В связи с вышесказанным большой интерес представляют исследования динамики видового состава и обилия рыб в р. Альма, отражающие общие для крымских рек тенденции. Цель работы – анализ трансформации ихтиоценозов горных рек Крыма под воздействием антропогенных факторов.
МАТЕРИАЛ И МЕТОДИКА
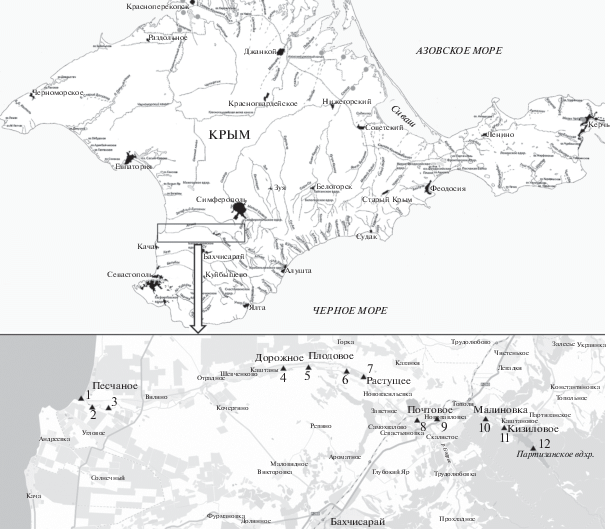
Исследования состава и структуры рыбного населения в р. Альма носят мониторинговый характер и проходили в периоды 2007–2013 гг. и 2016–2018 гг. на 11 станциях на трех участках русла реки, значительно отличающихся по экологическим характеристикам (рис. 1). Первый из участков расположен в нижнем течении реки (ст. 1–3), два других находятся в предгорной части: один из них слабо затронут хозяйственной деятельностью и по своим гидрологическим и биотопическим условиям сохранил характерные для крымских рек морфологию русла, строение дна, течение и т.п. (с преобладанием зон перекатов) (ст. 4–9), а другой расположен в зарегулированной зоне ниже плотины руслового водохранилища, где преобладают сильно заиленные зоны плесов (ст. 10, 11). Эпизодические исследования проводили на акватории водохранилища (ст. 12).
Сбор проб в русле реки осуществляли методом гона в меженный период – с июня по сентябрь включительно, на каждой из обозначенных на схеме станций. При помощи волокуши с ячеей 6 мм или сачка из хамсароса с размером ячеи 6.5 мм, имеющего входное отверстие полукруглой формы размером 1.6 × 0.8 м и площадью 1 м2, и заграждения из мелкоячейного хамсароса отгораживали участок русла реки протяженностью от 100 до 150 м. Рыб с этого участка сгоняли в орудие лова в 5-кратной повторности, при этом максимально изымали все рыбное население – от сеголеток до старших возрастных групп. Станции в пределах каждого из трех районов были идентичны по своим характеристикам: на них обязательно присутствовали основные типы биотопов – зона переката и зона плеса. Уловистость орудий лова не определяли, поскольку для учетов в разное время применяли одни и те же орудия лова в одних и тех же биотопах, за исключением водохранилища.
Временны́е ряды были сформированы из ежегодных оценок относительной численности 19 видов по результатам 15 обловов в каждый из описанных временны́х периодов (2007–2013 гг. и 2016–2018 гг.) на трех различных по биотопическим и гидрологическим свойствам участках – нижнем течении, среднем течении в незарегулированной части и среднем течении в зарегулированной части. Общий вылов составил 3918 особей в первый период исследований и 3193 особи – во второй. Объем собранного материала в разные годы в нижнем течении реки составил 3858 рыб, в незарегулированной части среднего течения – 1793, в зарегулированной – 1460.
Для уточнения видового состава также проводили обловы в русле реки при помощи ручных сачков, вентерей, крючковых снастей и жаберных сетей с ячеей от 12 до 25 мм. На акватории Партизанского водохранилища качественные исследования рыбного населения осуществляли с использованием жаберных сетей с ячеей 20–50 мм. Видовую принадлежность рыб определяли с помощью определителей [7–9]. Названия рыб приведены согласно каталогу [10].
Сравнительный анализ видового состава рыбного населения проводился для различных временны́х периодов. Первый из них охватывает период до 2007 г. и основан на литературных данных о видовом составе рыб бассейна реки. Еще два периода включают собственные данные как о видовом, так и количественном составе: один период продолжался с 2007 г. по 2013 г. и характеризовался довольно стабильными гидрологическими и экологическими условиями, другой начался с прекращением функционирования Северо-Крымского канала в 2014 г., после чего резко увеличился водозабор из всех крымских рек, в том числе несанкционированный, осуществляемый местными жителями для полива садов и огородов.
Для выявления уровня видового сходства ихтиофаун был применен коэффициент Серенсена-Чекановского. При сравнении различных временны́х периодов использовали как собственные, так и литературные данные. Показатели видового богатства и разнообразия (индекс видового разнообразия Шеннона, индекс видового богатства Маргалефа, индекс выровненности Пиелоу и индекс доминирования Симпсона) были определены на основании собственных данных по результатам проведенных обловов, в ходе которых устанавливали усредненную долю особей каждого вида в уловах за периоды 2007–2013 гг. и 2016–2018 гг. Оценка доминирования выполнена согласно работе [11]: редкий вид – менее 0.1%; малочисленный – 0.1–1.0%; обычный – 1.1–5.0%; субдоминантный – 5.1–10.0%; доминантный – более 10%; супердоминантный – более 50% от общей численности улова. Для оценки степени статистической значимости изменений, произошедших в доминировании (относительной численности) отдельных видов в разные временны́е периоды, использован t-критерий Стьюдента (M и m – среднее значение и его ошибка, df – число степеней свободы), при этом анализ данных включал проверку на нормальность распределения с использованием критерия Колмогорова-Смирнова и однородность дисперсий с применением F-критерия, которую проводили с помощью программы Statistica 10. При этом подтвердилась нормальность распределения для трех редких и малочисленных чужеродных видов рыб (уклеи, амурского чебачка и обыкновенной щиповки) в нижнем течении реки. Для анализа статистической значимости различий в структуре сообществ рыб в те же временны́е периоды применяли непараметрический критерий Манна-Уитни (U). Ввиду того, что основные изменения наблюдались не в видовом составе, а в количественных характеристиках таксонов в сравниваемых сообществах, для типизации рыбного населения выполнен кластерный анализ на основе индекса Брэя-Кертиса, при вычислении которого использовалась доля видов по численности в пробах.
РЕЗУЛЬТАТЫ
В результате наших исследований в бассейне р. Альма было отмечено 30 видов, а общий состав ихтиофауны за весь период ее изучения с учетом литературных данных составил 34 вида из 7 семейств, принадлежащих 5 отрядам (табл. 1).
Таблица 1.
Видовой состав рыб бассейна р. Альма
| № | Вид | Статус вида |
Наличие вида | |||||
|---|---|---|---|---|---|---|---|---|
| 1 | 2 | 3 | 4 | 5 | 6 | |||
| 1 | Горчак Rhodeus amarus | И | + | + | + | |||
| 2 | Карась серебряный Carassius gibelio | И | + | + | + | |||
| 3 | Карась обыкновенный Carassius carassius | И | + | |||||
| 4 | Карп, сазан Cyprinus carpio | И | + | + | + | |||
| 5 | Усач крымский Barbus tauricus | А | + | + | + | + | + | |
| 6 | Белый амур Ctenopharyngodon idella | И | + | |||||
| 7 | Толстолобик белый Hypophthalmichthys molitrix | И | + | |||||
| 8 | Толстолобик пестрый Hypophthalmichthys nobilis | И | + | |||||
| 9 | Крымский пескарь Gobio krymensis | А | + | + | + | + | ||
| 10 | Чебачок амурский Pseudorasbora parva | И | + | + | ||||
| 11 | Голавль Squalius cephalus | А | + | + | + | + | ||
| 12 | Лещ Abramis brama | И | + | + | ||||
| 13 | Густера Blicca bjoerkna | И | + | |||||
| 14 | Быстрянка южная Alburnoides fasciatus | А | + | + | + | + | + | |
| 15 | Уклея Alburnus alburnus | И | + | + | ||||
| 16 | Шемая крымская Alburnus mentoides | А | + | + | + | + | ||
| 17 | Верховка Leucaspius delineatus | И | + | + | ||||
| 18 | Плотва Rutilus rutilus | И | + | + | + | + | ||
| 19 | Щиповка обыкновенная Cobitis taenia | И | + | + | + | |||
| 20 | Сиг обыкновенный Coregonus lavaretus | И | + | |||||
| 21 | Форель радужная Oncorhynchus mykiss | И | + | |||||
| 22 | Ручьевая форель Salmo labrax | А | + | + | ||||
| 23 | Щука Esox lucius | И | + | + | ||||
| 24 | Кефаль сингиль Liza aurata | А | + | |||||
| 25 | Кефаль пиленгас Liza haematocheila | А | + | |||||
| 26 | Кефаль лобан Mugil cephalus | А | + | |||||
| 27 | Колюшка трехиглая Gasterosteus aculeatus | А | + | |||||
| 28 | Окунь обыкновенный Perca fluviatilis | И | + | + | + | |||
| 29 | Ерш обыкновенный Gymnocephalus cernua | И | + | |||||
| 30 | Судак Sander lucioperca | И | + | + | ||||
| 31 | Бычок гонец Babka gymnotrachelus | И | + | + | ||||
| 32 | Бычок головач Ponticola kessleri | И | + | + | + | |||
| 33 | Бычок песочник Neogobius fluviatilis | И | + | + | + | |||
| 34 | Трубконосый бычок Proterorhinus semilunaris | И | + | + | ||||
| ВСЕГО | 7 | 13 | 13 | 13 | 19 | 8 | ||
Примечание. И – интродуцент, А – аборигенный; 1–2 – литературные данные: 1 – период до 1950 г. [12, 13]; 2 – период 1955–2007 гг. [9, 14–16]; период 2007–2018 гг. [17, 18]; 3–6 – наши данные: 3 – устьевая часть реки; 4 – нижнее и среднее течение в период 2007–2013 гг.; 5 – нижнее и среднее течение в период 2016–2018 гг.; 6 – акватория водохранилища.
В устьевой части реки впервые был отмечен регулярный заход из морской прибрежной зоны трех видов кефалей, только на этом участке была выловлена трехиглая колюшка.
В нижнем течении (ст. 1–3 в районе с. Песчаное) река имеет равнинный характер. На данном участке происходит выгул водоплавающих домашних птиц, для полива садов и огородов местными жителями сооружаются запруды, в которых скапливается ил, присутствует сильная эвтрофикация, в результате чего наблюдается бурное развитие нитчатых водорослей и водной растительности. Степень загрязнения иногда так велика, что местами возникают заморные явления. На этом участке русла в 2007–2013 гг. нами было отмечено 10 видов. При этом наблюдалось супердоминирование (73.5%) одного чужеродного вида – горчака, доминантом являлась шемая крымская (13.4%), субдоминантом – бычок песочник (7.7%). К обычным видам относились крымский усач и голавль (по 2.7% каждый), прочие были малочисленными и редкими, составляя в сумме 1.2% по численности. В 2016–2018 гг. в составе сообщества данного участка было также зарегистрировано 10 видов, однако в этот период горчак принадлежал к доминирующему комплексу (40.5%) наряду с крымской шемаей (15.2%) и серебряным карасем (13.3%), к субдоминантам относились голавль (8.2%), бычок песочник (7.0%), уклея (5.7%) и чебачок амурский (5.1%), обыкновенным видом являлась щиповка (3.8%), а малочисленными – густера и бычок головач (по 0.6% каждый).
В среднем течении реки на участке, слабо преобразованном в результате хозяйственной деятельности (ст. 4–9 между селами Дорожное и Новопавловка), в 2007–2013 гг. супердоминантом была быстрянка южная (в среднем 52.6% по численности), к доминирующему комплексу принадлежали голавль (22.7%) и шемая крымская (17.5%), а 5 видов (пескарь крымский, усач крымский, чебачок амурский, бычки гонец и трубконосый) относились к обычным, составляя суммарно 7.2%. В 2016–2018 гг. количество видов в этом районе увеличилось до 11, при этом по-прежнему супердоминантом была южная быстрянка (68.1%), однако теперь к доминирующему комплексу принадлежал также аллохтонный вид – трубконосый бычок (10.7%), к субдоминирующему – голавль и крымский усач (8.2 и 7.6% соответственно). Обыкновенными видами на этом участке являлись крымский пескарь (1.5%) и обыкновенная щиповка (1.7%), к малочисленным и редким относились крымская шемая, уклея, верховка, густера и бычок гонец, составлявшие в сумме 2.2% уловов.
На зарегулированном участке среднего течения (ст. 10, 11 в районе сел Малиновка и Кизиловое) наблюдаются значительные колебания гидрологических параметров. Наименьший расход воды, вплоть до полного пересыхания, обычно отмечается здесь летом в связи с тем, что часть вод отводится в Альминское водохранилище, используется для орошения, и на отдельных участках с галечными отложениями в меженный период почти полностью прекращается поверхностный сток. Преобладающим видом – супердоминантом – на этом участке в 2007–2013 гг. была обыкновенная щиповка (в среднем 71.1% в уловах по численности), доминантом – пескарь крымский (11.6%), субдоминантами – голавль (9.9%) и быстрянка (5.8%), к малочисленным относились трубконосый бычок и крымский усач, составляя в сумме 1.6% по численности. В 2016–2018 гг., после выпадения значительного количества осадков и нескольких экстремальных сбросов воды из водохранилища, вызвавших паводковые наводнения, илистые наносы и растительность на зарегулированном участке были полностью смыты и обнажилось каменистое ложе реки. В этот период супердоминантом стала южная быстрянка (72.3%), к доминирующему комплексу принадлежал крымский пескарь (16.5%), обыкновенными видами являлись голавль (4.7%), обыкновенная щиповка (2.7%), крымский усач и плотва (по 1.2%), к малочисленным и редким относились шемая (0.6%), трубконосый бычок, речной окунь и форель (по 0.3% каждый).
При сравнении показателей доминирования в разные периоды наблюдений (2007–2013 гг. и 2016–2018 гг.) на трех выделенных участках было отмечено, что в нижнем течении реки (ст. 1–3), согласно t-критерию Стьюдента, статистически значимо (p < 0.05) увеличилась доля в сообществах лимнофильных интродуцентов – чебачка амурского (df = 14, M1 = 1.1 × 10–3, m1 = 1.8 × 10–3, M2 = = 5.9 × 10–2, m2 = 2.3 × 10–2), уклеи (df = 14, M1 = = 0.4 × 10–3, m1 = 0.1 × 10–4, M2 = 5.5 × 10–2, m2 = = 6.6 × 10–3), обыкновенной щиповки (df =14, M1 = 1.01 × 10–2, m1 = 0.15 × 10–2, M2 = 3.37 × 10–2, m2 = 1.23 × 10–2).
В отношении прочих видов статистически значимых отличий в показателях доминирования не зафиксировано, хотя наблюдалась тенденция снижения относительной численности горчака (с 82.5% в 2016 г. до 26.3% в 2018 г.), которая может быть связана с резким уменьшением количества крупных двустворчатых моллюсков в результате вымывания илистых наносов при экстремальных паводках 2015 г., в результате которого произошло снижение пополнения популяции этого остракофильного вида.
Парный сравнительный анализ сообществ по ранговому критерию Манна-Уитни в различные временные периоды (2007–2013 гг. и 2016–2018 гг.) выявил статистически значимые на уровне p < 0.05 различия в структуре для рыбного населения незарегулированной части среднего течения (объем выборок: N1 = 11; N2 = 8; Uэмп=21).
ОБСУЖДЕНИЕ
Впервые сведения о составе фауны рыб р. Альма приводятся в работах К.Ф. Кесслера [12] и Я.Я. Цееба [13] и относятся к периоду до 1930-го года – в них отмечается всего шесть аборигенных и один интродуцированный вид (карп) (см. табл. 1). Аналогичные невысокие показатели характерны для нативной ихтиофауны большинства крымских рек [13] и в целом типичны для рек горного типа [2, 19–21]. Видовой состав рыб в нижнем и среднем течении в тот период отличался незначительно [13], а видовое сходство было весьма высоким (табл. 2). До начала 1950-х годов в водотоках Крыма не проводились ихтиологические исследования и отсутствуют сведения о наличии изменений в ихтиофауне. В середине XX в. 8 промысловых видов были интродуцированы для зарыбления недавно созданных водохранилищ [9, 14], а позднее фауна пополнилась еще 4 видами (см. табл. 1), проникшими, вероятно, в результате случайной интродукции [15, 16]. С учетом полученных нами данных к настоящему моменту состав ихтиофауны реки увеличился по сравнению с аборигенным более чем в 5 раз. За время наших наблюдений, начиная с 2007 г., также отмечен рост числа видов в среднем и нижнем течении как за счет появления нового для водотока вида – густеры, так и регулярной регистрации лимнофильных рыб, ранее отмеченных только в лентических водах водохранилища (плотва, серебряный карась, верховка) [17, 18]. Очевидно, источником их распространения служат два русловых водохранилища (Альминское и Партизанское). Процессы биоинвазий в малых реках начались давно и активно изучаются, однако столь высокие их темпы обычно отмечаются в лентических экосистемах [5, 22] и не характерны для водотоков горного типа [19–21]. Вероятно, одной из основных причин этого является чрезмерное по сравнению с масштабами самих рек Крыма изменение гидрологических характеристик при их зарегулировании.
Таблица 2.
Коэффициент видового сходства Серенсена-Чекановского для сообществ различных участков течения реки в разные временны́е периоды
| Период исследований | Участок | До 1950 г. | 2007–2013 гг. | 2016–2018 гг. | |||||
|---|---|---|---|---|---|---|---|---|---|
| СТ | НТ | СТt | СТn | НТ | СТt | СТn | НТ | ||
| До 1950 г. | СТ | – | 0.8 | 0.5 | 0.62 | 0.43 | 0.53 | 0.5 | 0.13 |
| НТ | – | – | 0.67 | 0.67 | 0.43 | 0.57 | 0.53 | 0.14 | |
| 2007–2013 гг. | СТt | – | – | – | 0.77 | 0.38 | 1 | 0.71 | 0.25 |
| СТn | – | – | – | – | 0.47 | 0.67 | 0.74 | 0.33 | |
| НТ | – | – | – | – | – | 0.6 | 0.38 | 0.6 | |
| 2016–2018 гг. | СТt | – | – | – | – | – | – | 0.67 | 0.3 |
| СТn | – | – | – | – | – | – | – | 0.42 | |
В результате анализа пространственно-временных вариаций видового состава (см. табл. 2) выявлены кардинальные отличия современной ихтиофауны нижнего течения реки как от нативной для этого участка, регистрировавшейся в водотоке до середины прошлого века, так и современной фауны разных по антропогенной нагрузке районов среднего течения, а мера этих отличий, выраженная индексом Серенсена-Чекановского, продолжает увеличиваться на протяжении последнего десятилетия. В среднем течении реки фаунистическое сходство ихтиоценов достаточно велико как в пространственном, так и во временно́м аспекте, однако также имеет тенденцию к снижению, что происходит в основном за счет постепенного увеличения количества аллохтонных видов.
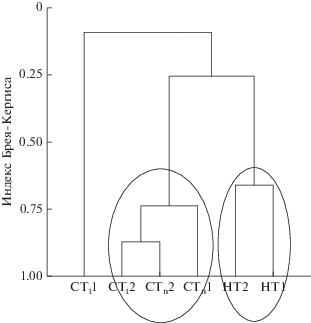
Однако наиболее значительные пространственные и временны́е вариации наблюдаются в количественных характеристиках видов. По этим показателям сильно выделяется сообщество зарегулированной части среднего течения в период 2007–2013 гг. – его уровень сходства соответствует значению индекса Брея-Кертиса 0.1 (рис. 2). Прочие сообщества среднего течения оказались достаточно близки между собой (уровень сходства более 0.75) и объединены в общий кластер, который на уровне сходства около 0.3 отличается от сообществ нижнего течения (2-й кластер).
Рис. 2.
Дендрограмма сходства рыбного населения: СТt1 – среднего течения в зарегулированной части в период 2007–2013 гг.; СТt 2 – то же в период 2016– 2018 гг.; СТn 1 – среднего течения в незарегулированной части в период 2007–2013 гг.; СТn 2 – то же в период 2016–2018 гг.; НТ1 – нижнего течения в период 2007–2013 гг.; НТ2 – то же в период 2016–2018 гг.
Вероятно, изменения в сообществах среднего течения были связаны с резкими колебаниями водного режима, в результате которых увеличились показатели относительной численности лимнофильных интродуцентов и доля южной быстрянки. Резкий рост количественных характеристик этого вида, а в зарегулированной части среднего течения также крымского пескаря позволяет рассматривать их как экстремобионтные в отличие от прочих аборигенных (крымский усач, голавль, крымская шемая), обилие которых по сравнению с сообществами первой половины XX в. [13] в целом весьма невелико.
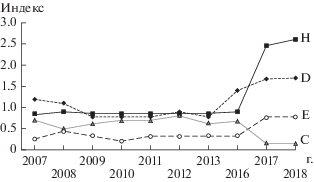
За последнее десятилетие произошло значительное увеличение показателей видового богатства и видового разнообразия на всем протяжении русел рек Крыма, особенно сильно выраженное на зарегулированных участках как в нижнем, так и среднем течении. Временна́я динамика средних значений индексов видового разнообразия (рис. 3) отражает резкое увеличение видового богатства, снижение выровненности сообществ и некоторый рост показателей доминирования. На зарегулированном участке среднего течения р. Альмы отмечали рост выровненности и снижение доминирования в сообществах, что, вероятно, является временной реакцией на воздействие сильных паводков. Так как для рыбного населения горных рек характерна видовая бедность при выраженном доминировании отдельных представителей ихтиофауны [19–21], то формальное улучшение показателей разнообразия, скорее, свидетельствует о заметных нарушениях в структуре нативных сообществ.
ЗАКЛЮЧЕНИЕ
В горных реках Крыма наблюдаются значительные сдвиги в видовой и количественной структуре рыбных сообществ в сторону преобладания аллохтонных видов. В незарегулированной части среднего течения рек рыбное население находится в относительно стабильном состоянии, в нижнем течении наблюдаются снижение выровненности и увеличение меры доминирования, что свидетельствует о негативных тенденциях в состоянии и структуре ихтиоценов, связанных с тем, что благодаря равнинному характеру этих участков они весьма благоприятны для лимнофильных вселенцев. В целом состояние биотопов и характер водного режима горных рек Крыма, который определяется преимущественно искусственным регулированием уровня водохранилищ, являются факторами, определяющими структурные характеристики рыбных сообществ на всем протяжении среднего и нижнего течения.
Исследования выполнены в рамках программ Института биологии южных морей им. А.О. Ковалевского РАН по теме “Закономерности формирования и антропогенная трансформация биоразнообразия и биоресурсов Азово-Черноморского бассейна и других районов Мирового океана” (№ АААА-А18-118020890074-2).
Список литературы
Дгебуадзе Ю.Ю., Слынько Ю.В., Кияшко В.И. Рыбное население // Экосистема малой реки в изменяющихся условиях среды. М.: Тов-во научн. изд. КМК, 2007. С. 267–279.
Giller P.S., Malmquist B. The Biology of Streams and Rivers. New York: Oxford University Press, 1998. P. 235–283.
Growns I. The influence of changes to river hydrology on freshwater fish in regulated rivers of the Murray-Darling basin // Hydrobiologia. 2008. V. 596. P. 203–211.
Robinson C.T., Tockner K., Ward J.V. The fauna of dynamic riverine landscapes // Freshwater Biology. 2002. V. 47. № 4. P. 661–677.
Beatty S.J., Morgan D.L. Introduced freshwater fishes in a global endemic hotspot and implications of habitat and climatic change // BioInvasions Records. 2013. V 2. № 1. P. 1–9.
Yildirim A., Arslan M., Pegg M. Patterns of fish communities along A Mountain River: The Upper Coruh River (Turkey) // Polish J. of Ecology. 2008. V. 56. № 4. P. 731–736.
Берг Л.С. Рыбы пресных вод СССР и сопредельных стран. М.; Л.: Изд-во АН СССР, 1948. Ч. 1. С. 3–464; 1949. Ч. 2. С. 465–934; 1949. Ч. 3. С. 935–1381.
Веселов Е.А. Определитель пресноводных рыб фауны СССР. М.: Просвещение, 1977. 238 с.
Делямуре С.Л. Рыбы пресных водоемов. Симферополь: Крым, 1964. 70 с.
Fricke R., Eschmeyer W.N., Van der Laan R. (eds.). Eschmeyer’s Catalog of Fishes: Genera, Species, References. 2019. (http://researcharchive.calacademy.org/ research/ichthyology/catalog/fishcatmain.asp).
Терещенко В.Г., Надиров С.Н. Формирование структуры рыбного населения предгорного водохранилища // Вопросы ихтиологии. 1996. Т. 36. № 2. С. 169–178.
Кесслер К.Ф. Путешествие с зоологической целью к северному берегу Черного моря и в Крым в 1858 году. Киев: Универс. тип., 1860. 248 с.
Цееб Я.Я. Предварительные итоги изучения ихтиофауны крымских речек // Тр. Крымск. НИИ. 1929. Т. 2. Вып. 2. С. 112–123.
Делямуре С.Л. Рыбы пресных водоемов. Симферополь: Крым, 1966. 66 с.
Мирошниченко А.И. Рыбы внутренних водоемов Крыма. Устойчивый Крым. Водные ресурсы. Симферополь: Таврида, 2003. С. 142–145.
Culling M.A., Janko K., Boroń A. et al. European colonization of the spined loach Cobitis taenia from Ponto-Caspian refugia based on mitochondrial DNA variation // Molecular Ecology. 2006. № 15. P. 173–190.
Карпова Е.П., Болтачев А.Р. Особенности формирования и современное состояние ихтиофауны внутренних водоемов Крыма // Збірник праць Зоологічного музею. 2011. № 42. С. 75–91.
Карпова Е.П. Чужеродные виды рыб в пресноводной ихтиофауне Крыма // Российский журн. биологич. инвазий. 2016. № 3. С. 47–60.
Решетников С.И., Пашков А.Н. Экосистемы малых рек Черноморского побережья Северо-Западного Кавказа. Краснодар: Биотех-Юг, 2009. 152 с.
Uğurlu S., Polat N. Fish Fauna of the Karaabdal Stream (Samsun-Turkey) // Turkish Journal of Fisheries and Aquatic Sciences. 2008. № 8. P. 121–124.
Küçük F., Gümüş E., Gülle I., Güçlü S. S. The Fish Fauna of the Goksu River (Türkiye). Taxonomic and Zoogeographic Features // Turkish Journal of Fisheries and Aquatic Sciences. 2007. № 7. P. 53–63.
İnnal D. Alien fish species in reservoir systems in Turkey: a review // Management of Biological Invasions. 2012. V. 3. № 2. P. 115–119.
Дополнительные материалы отсутствуют.